文档内容
专题61 盐类水解及应用
1.【2023年北京卷】下列过程与水解反应无关的是
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸
D.向沸水中滴入饱和 溶液制备 胶体
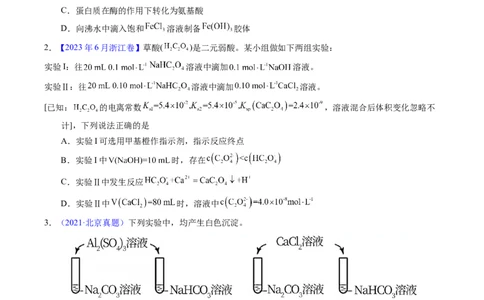
2.【2023年6月浙江卷】草酸( )是二元弱酸。某小组做如下两组实验:
实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中
3.(2021·北京真题)下列实验中,均产生白色沉淀。
下列分析不正确的是
A.NaCO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B.CaCl 能促进NaCO、NaHCO 水解
2 2 3 3
C.Al (SO ) 能促进NaCO、NaHCO 水解
2 4 3 2 3 3
D.4个实验中,溶液滴入后,试管中溶液pH均降低
4.【2021年江苏卷】室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol·L-1NaHCO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产生白色沉淀
3 2实验3:向0.1mol·L-1NaCO 溶液中通入CO,溶液pH从12下降到约为9
2 3 2
实验4:向0.1mol·L-1NaCO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
下列说法正确的是
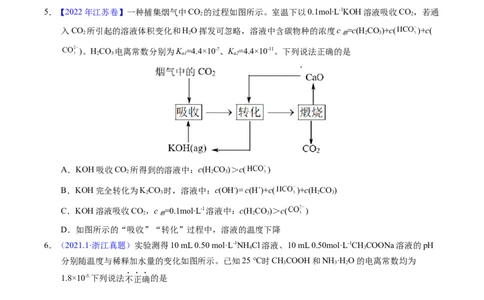
A.由实验1可得出:K (H CO)>
a2 2 3
B.实验2中两溶液混合时有:c(Ca2+)·c(CO )[CH COO-]>[H+]>[OH-]
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则(Na+)>(CH COO-)>(H+)
3
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
9.(2019·浙江高考真题)聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和
4 n 4 2
KClO 在水溶液中反应得到。下列说法不正确的是
3A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗6/n mol KClO
3 4 n 3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
10.(2019·浙江高考真题)下列溶液呈碱性的是
A.NH NO B.(NH )SO C.KCl D.KCO
4 3 4 2 4 2 3
11.(2018·浙江高考真题)下列物质因发生水解而使溶液呈酸性的是
A.HNO B.CuCl C.KCO D.NaCl
3 2 2 3
12.(2017·浙江高考真题)下列物质的水溶液因水解而呈酸性的是( )
A.NaOH B.(NH )SO C.NaCO D.NaCl
4 2 4 2 3
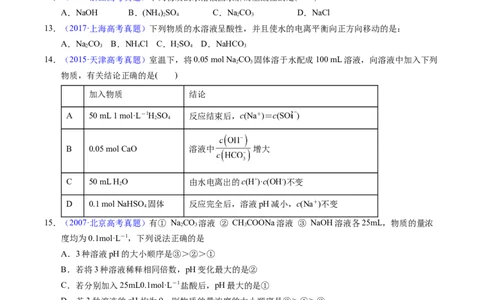
13.(2017·上海高考真题)下列物质的水溶液呈酸性,并且使水的电离平衡向正方向移动的是:
A.NaCO B.NH Cl C.HSO D.NaHCO
2 3 4 2 4 3
14.(2015·天津高考真题)室温下,将0.05 mol Na CO 固体溶于水配成100 mL溶液,向溶液中加入下列
2 3
物质,有关结论正确的是( )
加入物质 结论
A 50 mL 1 mol·L-1HSO 反应结束后,c(Na+)=c(SO )
2 4
B 0.05 mol CaO 溶液中 增大
C 50 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D 0.1 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
15.(2007·北京高考真题)有① NaCO 溶液 ② CHCOONa溶液 ③ NaOH溶液各25mL,物质的量浓
2 3 3
度均为0.1mol·L-1,下列说法正确的是
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25mL0.1mol·L-1盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
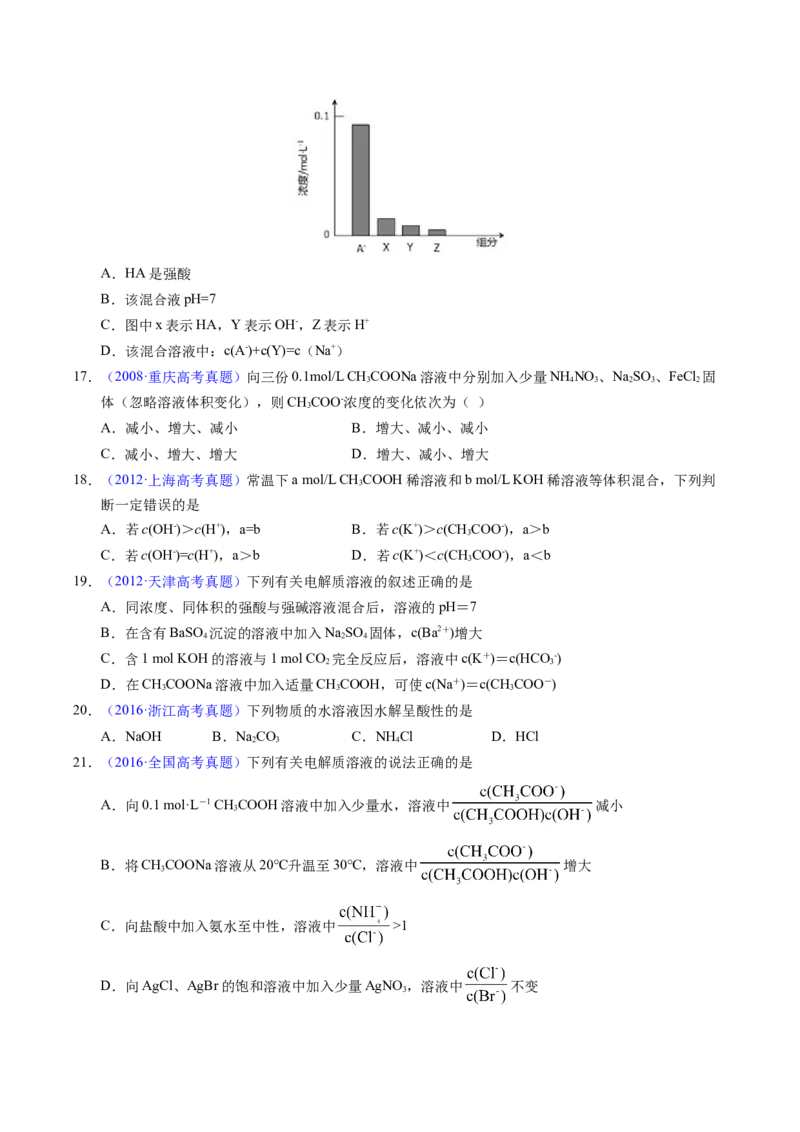
16.(2014·广东高考真题)常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液
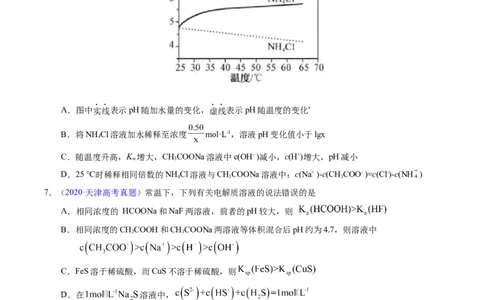
中部分微粒组分及浓度如图所示,下列说法正确的是A.HA是强酸
B.该混合液pH=7
C.图中x表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
17.(2008·重庆高考真题)向三份0.1mol/L CH COONa溶液中分别加入少量NH NO 、NaSO 、FeCl 固
3 4 3 2 3 2
体(忽略溶液体积变化),则CHCOO-浓度的变化依次为( )
3
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
18.(2012·上海高考真题)常温下a mol/L CH COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判
3
断一定错误的是
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CHCOO-),a>b
3
C.若c(OH-)=c(H+),a>b D.若c(K+)<c(CHCOO-),a<b
3
19.(2012·天津高考真题)下列有关电解质溶液的叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO 沉淀的溶液中加入NaSO 固体,c(Ba2+)增大
4 2 4
C.含1 mol KOH的溶液与1 mol CO 完全反应后,溶液中c(K+)=c(HCO -)
2 3
D.在CHCOONa溶液中加入适量CHCOOH,可使c(Na+)=c(CHCOO-)
3 3 3
20.(2016·浙江高考真题)下列物质的水溶液因水解呈酸性的是
A.NaOH B.NaCO C.NH Cl D.HCl
2 3 4
21.(2016·全国高考真题)下列有关电解质溶液的说法正确的是
A.向0.1 mol·L-1 CH COOH溶液中加入少量水,溶液中 减小
3
B.将CHCOONa溶液从20℃升温至30℃,溶液中 增大
3
C.向盐酸中加入氨水至中性,溶液中 >1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO,溶液中 不变
322.(2012·上海高考真题)将l00ml 1mol/L 的NaHCO 溶液等分为两份,其中一份加入少许冰醋酸,另外
3
一份加入少许Ba(OH) 固体,忽略溶液体积变化。两份溶液中c(CO2-)的变化分别是
2 3
A.减小、减小 B.减小、增大 C.增大、增大 D.增大、减小
23.(2015·海南高考真题)化学与生活密切相关。下列应用中利用了物质氧化性的是( )
A.明矾净化水 B.纯碱去油污
C.食醋除水垢 D.漂白粉漂白织物
24.(2009·全国高考真题)现有等浓度的下列溶液:①醋酸,②苯酚,③苯酚钠,④碳酸,⑤碳酸钠,⑥
碳酸氢钠。按溶液pH由小到大排列正确的是
A.④①②⑤⑥③B.④①②⑥⑤③ C.①④②⑥③⑤ D.①④②③⑥⑤
25.(2013·天津高考真题)下列有关电解质溶液的说法正确的是( )
A.在蒸馏水中滴加浓HSO ,K 不变
2 4 W
B.CaCO 难溶于稀硫酸,也难溶于醋酸
3
C.在NaS稀溶液中,c(H+)=c(OH-)-2c(H S)-c(HS-)
2 2
D.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同
3 4
26.(2009·北京高考真题)有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合面成:①CHCOONa
3
与HCl ②CHCOONa与NaOH ③CHCOONa与NaCl ④CHCOONa与NaHCO 下列各项排序正确的
3 3 3 3
是( )
A.pH:②>③>④>① B.c(CHCOO-):②>④>③>①
3
C.溶液中c(H+):①>③>②>④ D.c(CHCOOH):①>④>③>②
3
27.(2014·山东高考真题)已知某温度下CHCOOH和NH ·H O的电离常数相等,现向10mL浓度为
3 3 2
0.1mol·L-1的CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B. 先增大再减小
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10mL时,c(NH +)=c(CHCOO-)
4 3
28.(2013·广东高考真题)下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=4的醋酸中:c(H+)= 0.4mol·L-1
B.饱和碳酸氢钠溶液中(已知碳酸氢钠溶液呈碱性):c(Na+)= c(HCO -)
3
C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)
D.pH=12的纯碱溶液中:c(OH-)=1.0×10-12mol·L-1
29.(2009·天津高考真题)25 ℃时,浓度均为0.2 mol/L的NaHCO 和NaCO 溶液中,下列判断不正确的
3 2 3
是
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.c(OH-)前者大于后者D.分别加入NaOH固体,恢复到原温度,c(CO2-)均增大
3
30.(2008·海南高考真题)下列离子方程式中,属于水解反应的是( )
A.HCOOH+H O HCOO-+ H O+
2 3
B.CO+H O HCO -+ H+
2 2 3
C.CO2-+ H O HCO -+ OH-
3 2 3
D.HS-+ H O S2-+ H O+
2 3