文档内容
2023 年高考考前押题密卷(福建卷)
化学·全解全析
注意事项:
1.本试卷分选择题和非选择题两部分。答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 S-32 Cl-35.5 K-39
一、选择题:本题共10小题,每小题4分,共40分。每小题只有一项符合题目要求。
1.化学与生活密切相关。下列说法正确的是
A.使用医用酒精对物体表面消毒时,医用酒精的浓度是95%
B.北京冬奥会采用银离子抗菌技术制作的速滑服,可有效防护细菌侵入
C.最大单体面积“发电玻璃”使用的碲化镉属于金属材料
D.《清明上河图》原作是在绢上作画,绢的主要成分是纤维素
【答案】B
【详解】A.医用消毒酒精中乙醇的体积分数为75%,故A错误;
B.北京冬奥会采用银离子抗菌技术制作的速滑服,可有效防护细菌侵入,故B正确;
C.碲化镉属于新型无机非金属材料,C错误;
D.《清明上河图》是在生丝织成的绢上作画,绢的主要成分是蛋白质,故D错误;
故选B。
2.从樟科植物枝叶提取的精油中含有甲、乙两种成分:
下列有关说法错误的是
A.甲、乙均属于芳香烃
B.甲、乙分子均具有极性
C.甲、乙均能使酸性KMnO 及溴的四氯化碳溶液褪色
4
D.甲可以通过氧化反应制备乙
【答案】A
【详解】A.甲、乙两分子中均含有氧原子,不属于烃类,都是芳香族化合物,A错误;
B.甲、乙两分子均不对称,具有极性,B正确;
C.甲、乙两分子中均含碳碳双键,故二者均可以使酸性KMnO 及溴的四氯化碳溶液褪色,C正确;
4
1
学科网(北京)股份有限公司D.甲中醇羟基可以在Cu作催化剂条件下被氧气氧化为醛基,D正确;
故答案为A。
3.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.104 g苯乙烯( )含有σ键数目为11N
A
B.在氢氧碱性燃料电池中,当正极上消耗22.4 L气体时,转移的电子数为2N
A
C.在精炼铜的过释中,当阴极析出铜32 g时,阴阳极转移电子数均为N
A
D.等物质的量的N 和C H 所含有的电子数均为14N
2 2 2 A
【答案】C
【详解】A.104 g苯乙烯为1mol,单键均为σ键,双键中含有1个σ键1个π键,苯环碳原子之间存在6
个σ键,则1mol苯乙烯含有16mol σ键,数目为16N ,A错误;
A
B.没有说明是否为标况,不能计算气体物质的量,不能计算转移电子数,B错误;
C.阴极铜离子得到电子生成铜单质,当阴极析出铜32 g时,为0.5mol,根据电子守恒可知,阴阳极转移
电子数均为N ,C正确;
A
D.等物质的量的N 和C H,但是没有说明是否均为1mol,故不能减少所含有的电子数,D错误;
2 2 2
故选C。
4.过氧化钙是一种用途广泛的优良供氧剂,性质与过氧化钠相似。选用下列部分装置(部分固定装置略)合
理组装可制备过氧化钙,其中不适合或不必要选取的装置是
A. B. C. D.
【答案】D
【详解】制备过氧化钙时,用双氧水制备氧气,钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,
而制备的氧气中会混有水蒸气,所以在与钙化合之前需要干燥,选用试剂是浓硫酸,同时为防止空气中水
蒸气进入,最后还需要连接浓硫酸的洗气瓶,制备过程中不需要装有NaOH溶液的洗气瓶,故选D。
5.下列物质性质实验对应的离子方程式书写正确的是
A.漂白粉溶液吸收CO 后产生白色沉淀:
2
B.Fe(OH) 溶于氢碘酸:
3
C.用碳酸钠溶液处理锅炉水垢:
D.同浓度同体积NHHSO 溶液与NaOH溶液混合:
4 4
【答案】C
【详解】A. 漂白粉溶液吸收CO 后产生碳酸钙沉淀和次氯酸,反应的离子方程式是
2
2
学科网(北京)股份有限公司,故A错误;
B. 溶于氢碘酸生成碘化亚铁、碘单质、水,反应的离子方程式是
,故B错误;
D. 用碳酸钠溶液处理锅炉水垢,沉淀硫酸钙转化为碳酸钙沉淀,反应的离子方程式是
,故C正确;
C. 同浓度同体积NHHSO 溶液与NaOH溶液混合,NHHSO 与NaOH等物质的量反应生成硫酸铵、硫酸
4 4 4 4
钠、水,反应的离子方程式是 ,故D错误;
故选C。
6.明代《徐光启手迹》记载了制备王水的方法,其主要流程如图所示(水蒸气等部分产物已省略),下列说
法中正确的是
A.X不能使酸性 溶液褪色
B.操作1的名称为蒸馏
C.流程中涉及的均为非氧化还原反应
D.步骤ⅱ能在铁容器中进行
【答案】B
【详解】A.由题意,Fe元素化合价升高,故部分硫元素化合价降低,X的化学式应为SO ,SO 具有还原
2 2
性能使酸性KMnO 溶液褪色,故A错误;微信搜索“高中试卷君”公众号 领取押题卷联考卷
4
B.操作1后得到硝酸,该过程中制取硝酸是利用了硝酸易挥发的性质,则操作1的名称为蒸馏,故B正
确;
C.步骤i中煅烧绿矾生成SO 过程中,S、Fe的化合价发生变化,属于氧化还原反应,故C错误;
2
D.王水是浓硝酸和浓盐酸按体积比=1:3的混合物,会腐蚀铁容器,步骤ⅱ不能在铁容器中进行,故D错
误;
故选B。
7.W、X、Y、Z为原子序数递增的短周期主族元素,四种元素可组成一种新型化合物 ,其中W
的原子半径在短周期主族元素中最大,X的质子数是Z核外最外层电子数的2倍。下列叙述正确的是
A.四种元素对应的最高价氧化物的水化物中,只有一种是强酸
B.W与另外三种元素形成的二元化合物均含离子键,水溶液呈碱性
C.简单离子半径:Z>Y>W
D.简单气态氢化物的稳定性:X>Z
【答案】A
3
学科网(北京)股份有限公司【分析】W的原子半径在短周期主族元素中最大,W为Na;X的质子数是Z核外最外层电子数的2倍,
分情况讨论:若Z核外最外层电子数为7,则Z为Cl、X为Si,由化合物中元素化合价代数和为0可知,Y
元素化合价为-3,Y为P;若Z核外最外层电子数为6,则Z为S、X为Mg,Y元素化合价为+7,不合理;
若Z核外最外层电子数为5,则X的质子数为10,不合理;可知Z为Cl、X为Si、Y为P。
【详解】A.氢氧化钠为强碱,硅酸为弱酸,磷酸为中强酸,高氯酸为强酸,A项正确;
B.氯化钠水溶液呈中性,B项错误;
C.核外电子排布相同的离子,原子序数大的半径小,磷离子的半径大于氯离子的,C项错误;
D.同周期主族元素从左到右,非金属性依次增强,则简单气态氢化物的稳定性Cl>Si,D项错误;
故答案为:A。
8.反应物(S)转化为产物P或 )的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A.进程I是吸热反应
B.平衡时P产率:
C.生成P的速率:
D.进程IV中,Z不是催化剂
【答案】D
【详解】A.进程I反应物的总能量大于生成物的总能量,该反应是放热反应,故A错误;
B. 中加了催化剂,降低反应所需活化能,但平衡不移动,因此平衡时P产率: ,故B错误;
C. 的第二阶段的活化能大于 的任意阶段的活化能,活化能越大,反应速率越慢,因此生成P的速率:
,故C错误;微信搜索“高中试卷君”公众号 领取押题卷联考卷
D.根据进程IV中参与反应的物质和生成的物质,则说明Z不是催化剂,故D正确。
综上所述,答案为D。
9.盐酸羟胺 主要用作还原剂和定影剂。以外排烟气中的 以及 、盐酸为原料通过电化
学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
4
学科网(北京)股份有限公司A.制备总反应方程式为
B.该电化学装置中的离子交换膜最好选择质子交换膜
C.制备过程中,Pt电极所在极室溶液的pH基本保持不变
D.每生成1mol盐酸羟胺,电路中转移电子的物质的量:
【答案】D
【详解】A.根据 以及 、盐酸为原料制备盐酸羟胺, 制备总反应方程式为
,故A正确;
B.根据电极反应,左边氢气失去电子变为氢离子,右边 变为 需要不断消耗氢离子,因此该电
化学装置中的离子交换膜最好选择质子交换膜,氢离子从左边不断移动到右边,故B正确;
C.制备过程中,Pt电极为负极,氢气失去电子变为氢离子,氢离子穿过交换膜进入到右室,转移多少电
子,生成多少氢离子,就会向右移动多少氢离子,因此Pt电极所在极室溶液的pH几乎不变,故C正确;
D.根据总反应方程式 ,生成2mol,转移(4x+2)mol
电子,则每生成1mol盐酸羟胺,电路中转移电子的物质的量: ,故D错误。
综上所述,答案为D。微信搜索“高中试卷君”公众号 领取押题卷联考卷
10.砷酸( )为三元弱酸,室温下向0.1mol/L的 溶液中滴加NaOH溶液,溶液中各微粒的物
质的量分数 随pH的变化如图所示。
已知 ,下列叙述正确的是
A.反应 的平衡常数值为
B.室温下, 离子的电离程度强于水解程度
C.向VL 0.1mol/L 溶液中滴加0.05mol/L NaOH溶液至 时,消耗NaOH溶液体积大于VL
D.图中pH为4.7和9.8时均有
【答案】C
【详解】A.由图像可得 ,pH=11.3时 ,此时
5
学科网(北京)股份有限公司,反应 的平衡常数 ,A错误;
B.当 时,溶液pH=9.8呈碱性,所以 离子的水解程度强于电离程度,B错误;
C.根据图像,当溶液pH=6.8时,溶液中 ,向VL 0.1mol/L的 溶液中滴
加等体积0.05mol/L的NaOH溶液的时刻,生成的 与剩余的 物质的量相等,由于前者水解
程度小于后者的电离程度( ),此时溶液显酸性,若要使pH=7,需继续滴加NaOH溶液,所以
消耗NaOH溶液体积大于VL,C正确;
D.在pH为4.7和9.8时均有电荷守恒关系式:
,但两点的物料守恒(也叫元素守恒)式不同,pH为4.7时有
,电荷守恒式和物料守恒式作差可得:
,pH为9.8时有物料守恒式
,电荷守恒式和物料守恒式作差可得:
,D错误;
故选C。
二、非选择题:本题共5小题,共60分。
11.(14分)
钴是生产电池材料、高温合金、磁性材料及催化剂的重要原料。一种以湿法炼锌净化渣(含有Co、
Zn、Fe、Cu、Pb等金属及其氧化物)为原料提取钴的工艺流程如图所示:
已知:①常温下,K (CuS)=8.9×10-36,K (CoS)=1.8×10-22。
sp sp
②溶液的氧化还原电位为正表示该溶液显示出一定的氧化性。氧化还原电位越高,氧化性越强;电位
越低,氧化性越弱。
回答下列问题:
(1)“浸出渣”的主要成分为_________(填化学式)。工业上,在“浸出”过程中,常选用硫酸浸取,而
不用盐酸,原因是______________________________。
(3)Na S常用作沉淀剂,在“铜渣”中检测不到Co2+,“除铜液”中Co2+浓度为0.18mol•L-1,则此时溶
2
液的pH<______[已知常温下,饱和HS水溶液中存在关系式:c2(H+)·c(S2-)=1.0×10-22(mol•L-1)3]。
2
(4)“氧化”过程中,NaSO 与Fe2+发生反应的离子方程式为_____________________________。
2 2 8
(5)“沉铁”过程中,NaCO 的作用是_______________________。
2 3
6
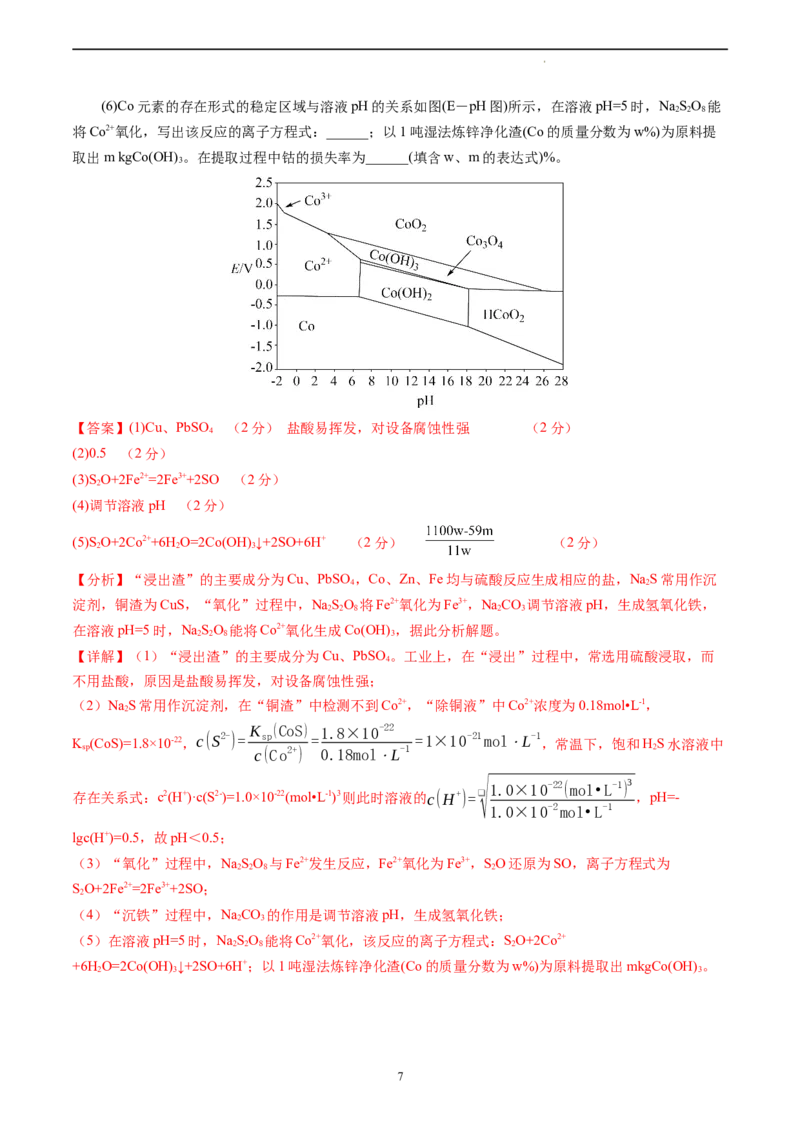
学科网(北京)股份有限公司(6)Co元素的存在形式的稳定区域与溶液pH的关系如图(E-pH图)所示,在溶液pH=5时,NaSO 能
2 2 8
将Co2+氧化,写出该反应的离子方程式:______;以1吨湿法炼锌净化渣(Co的质量分数为w%)为原料提
取出m kgCo(OH) 。在提取过程中钴的损失率为______(填含w、m的表达式)%。
3
【答案】(1)Cu、PbSO (2分) 盐酸易挥发,对设备腐蚀性强 (2分)
4
(2)0.5 (2分)
(3)S O+2Fe2+=2Fe3++2SO (2分)
2
(4)调节溶液pH (2分)
(5)S O+2Co2++6H O=2Co(OH) ↓+2SO+6H+ (2分) (2分)
2 2 3
【分析】“浸出渣”的主要成分为Cu、PbSO ,Co、Zn、Fe均与硫酸反应生成相应的盐,NaS常用作沉
4 2
淀剂,铜渣为CuS,“氧化”过程中,NaSO 将Fe2+氧化为Fe3+,NaCO 调节溶液pH,生成氢氧化铁,
2 2 8 2 3
在溶液pH=5时,NaSO 能将Co2+氧化生成Co(OH) ,据此分析解题。
2 2 8 3
【详解】(1)“浸出渣”的主要成分为Cu、PbSO 。工业上,在“浸出”过程中,常选用硫酸浸取,而
4
不用盐酸,原因是盐酸易挥发,对设备腐蚀性强;
(2)NaS常用作沉淀剂,在“铜渣”中检测不到Co2+,“除铜液”中Co2+浓度为0.18mol•L-1,
2
K (CoS) 1.8×10-22
K (CoS)=1.8×10-22,c(S2-)= sp = =1×10-21mol⋅L-1 ,常温下,饱和HS水溶液中
sp c(Co2+) 0.18mol⋅L-1 2
√1.0×10-22(mol•L-1) 3
存在关系式:c2(H+)·c(S2-)=1.0×10-22(mol•L-1)3则此时溶液的c(H+)=❑ ,pH=-
1.0×10-2mol•L-1
lgc(H+)=0.5,故pH<0.5;
(3)“氧化”过程中,NaSO 与Fe2+发生反应,Fe2+氧化为Fe3+,SO还原为SO,离子方程式为
2 2 8 2
SO+2Fe2+=2Fe3++2SO;
2
(4)“沉铁”过程中,NaCO 的作用是调节溶液pH,生成氢氧化铁;
2 3
(5)在溶液pH=5时,NaSO 能将Co2+氧化,该反应的离子方程式:SO+2Co2+
2 2 8 2
+6H O=2Co(OH) ↓+2SO+6H+;以1吨湿法炼锌净化渣(Co的质量分数为w%)为原料提取出mkgCo(OH) 。
2 3 3
7
学科网(北京)股份有限公司理论生成Co为1000kg×w%=10wkg,实际生成的Co的质量为: ,在提取过程中钴的损
失率为 。
12.(13分)
(三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原
料制备 。
已知:① 在 时恰好完全沉淀为 ;
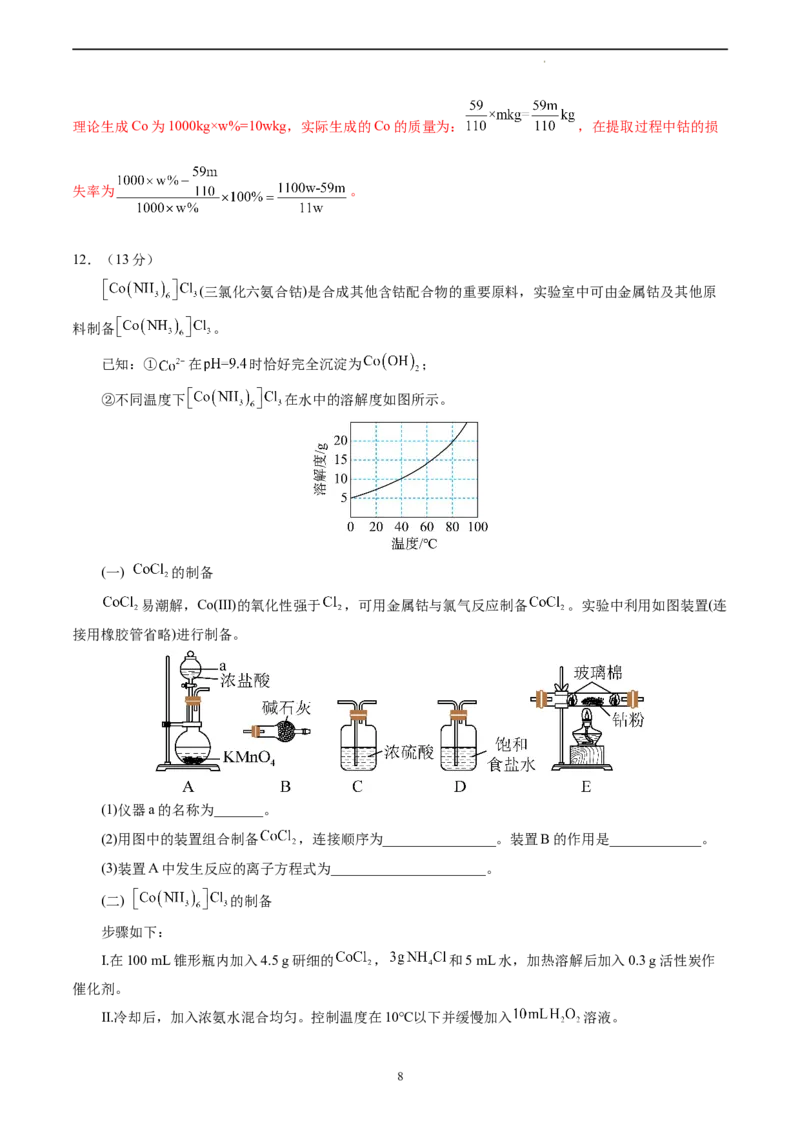
②不同温度下 在水中的溶解度如图所示。
(一) 的制备
易潮解,Co(Ⅲ)的氧化性强于 ,可用金属钴与氯气反应制备 。实验中利用如图装置(连
接用橡胶管省略)进行制备。
(1)仪器a的名称为_______。
(2)用图中的装置组合制备 ,连接顺序为________________。装置B的作用是_____________。
(3)装置A中发生反应的离子方程式为______________________。
(二) 的制备
步骤如下:
Ⅰ.在100 mL锥形瓶内加入4.5 g研细的 , 和5 mL水,加热溶解后加入0.3 g活性炭作
催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入 溶液。
8
学科网(北京)股份有限公司Ⅲ.在60℃下反应一段时间后,经过_______、过滤、洗涤、干燥等操作,得到 晶体。
(4)在加入浓氨水前,需在步骤Ⅰ中加入 ,请结合平衡移动原理解释原因________________。
(5)步骤Ⅱ中在加入 溶液时,控制温度在10℃以下并缓慢加入的目的是___________、
___________。
(6)制备 的总反应的化学方程式为________________________。
(7)步骤Ⅲ中的操作名称为_______。
【答案】(1)分液漏斗 (1分)
(2) A→D→C→E→B (2分)
防止多余的 污染空气,同时防止空气中的水蒸气进入装置E,使 潮解 (2分)
(3) (2分)
(4) 溶于水电离出 ,使 的电离平衡逆向移动,防止加入氨水时溶液中 过大,生
成 沉淀 (2分)
(5)控制反应速率 (1分) 防止温度过高使 和 分解 (1分)
(6) (2分)
【分析】利用浓盐酸与高锰酸钾反应制氯气,通过饱和食盐水除去氯气中的氯化氢,再通过浓硫酸干燥,
得到的干燥纯净的氯气通入装置E与钴加热条件下反应生成氯化钴;再利用氯化钴与氨化铵在活性炭催化
下反应制 ;
【详解】(1)仪器a的名称为分液漏斗;
(2)装置A用于制备Cl,装置D用于除去Cl 中的HCl,装置C用于干燥Cl,装置E用于制备CoCl ,
2 2 2 2
装置B的作用是防止多余的氯气污染空气,同时防止空气中的水蒸气进入装置E,使CoCl 潮解,故连接
2
顺序为A→D→C→E→B;
(3)装置A中KMnO 和浓盐酸反应制备Cl;
4 2
(4) 溶于水电离出 ,能使 的电离平衡逆向移动,进而可以抑制 的电离,
防止加入氨水时溶液中 过大,生成 沉淀,有利于 的配位;
(5) 和 受热易分解,步骤Ⅱ中控制温度在10℃以下并缓慢加入 溶液是为了控制反应
速率,防止温度过高使 和 分解;微信搜索“高中试卷君”公众号 领取押题卷联考卷
(6)在题给制备反应中, 是氧化剂,根据得失电子守恒、原子守恒可得总反应的化学方程式为
;
9
学科网(北京)股份有限公司13.(13分)
2020年中国向世界宣布2030年前实现碳达峰,2060年前实现碳中和。转化和吸收CO 的研究成为更
2
加迫切的任务。
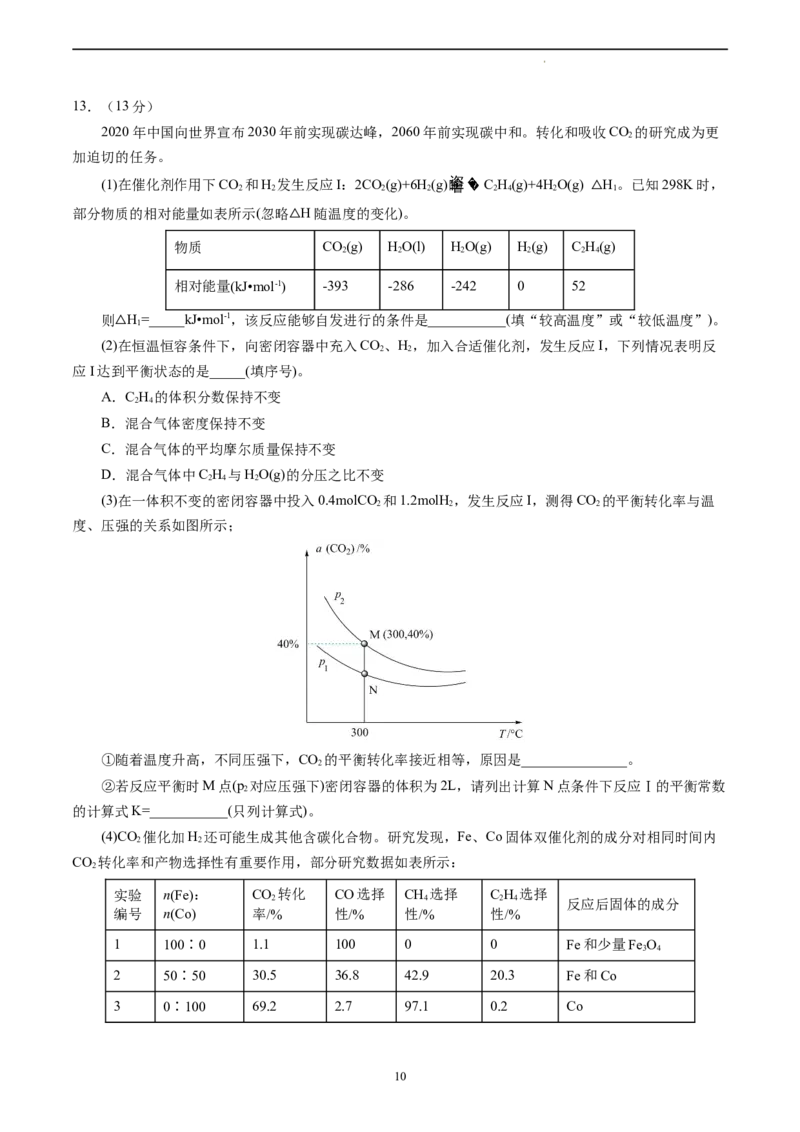
(1)在催化剂作用下CO 和H 发生反应I:2CO(g)+6H(g) C H(g)+4HO(g) H。已知298K时,
2 2 2 2 2 4 2 1
部分物质的相对能量如表所示(忽略 H随温度的变化)。 △
物质 △ CO(g) HO(l) HO(g) H(g) C H(g)
2 2 2 2 2 4
相对能量(kJ•mol-1) -393 -286 -242 0 52
则 H=_____kJ•mol-1,该反应能够自发进行的条件是___________(填“较高温度”或“较低温度”)。
1
(2)在恒温恒容条件下,向密闭容器中充入CO、H,加入合适催化剂,发生反应I,下列情况表明反
△ 2 2
应I达到平衡状态的是_____(填序号)。
A.C H 的体积分数保持不变
2 4
B.混合气体密度保持不变
C.混合气体的平均摩尔质量保持不变
D.混合气体中C H 与HO(g)的分压之比不变
2 4 2
(3)在一体积不变的密闭容器中投入0.4molCO 和1.2molH,发生反应I,测得CO 的平衡转化率与温
2 2 2
度、压强的关系如图所示;
①随着温度升高,不同压强下,CO 的平衡转化率接近相等,原因是_______________。
2
②若反应平衡时M点(p 对应压强下)密闭容器的体积为2L,请列出计算N点条件下反应Ⅰ的平衡常数
2
的计算式K=___________(只列计算式)。
(4)CO 催化加H 还可能生成其他含碳化合物。研究发现,Fe、Co固体双催化剂的成分对相同时间内
2 2
CO 转化率和产物选择性有重要作用,部分研究数据如表所示:
2
实验 n(Fe): CO 转化 CO选择 CH 选择 C H 选择
2 4 2 4 反应后固体的成分
编号 n(Co) 率/% 性/% 性/% 性/%
1 100∶0 1.1 100 0 0 Fe和少量Fe O
3 4
2 50∶50 30.5 36.8 42.9 20.3 Fe和Co
3 0∶100 69.2 2.7 97.1 0.2 Co
10
学科网(北京)股份有限公司下列说法错误的是______(填序号)。
A.实验1中生成Fe O 的化学方程式为3Fe+4CO =Fe O+4CO
3 4 2 3 4
B.用该方法制备CH 时,最好选用金属Co作催化剂
4
C.n(Fe):n(Co)对该制备过程影响很大
D.若生成等物质的量的CH 和C H,转移的电子数比值为2∶1
4 2 4
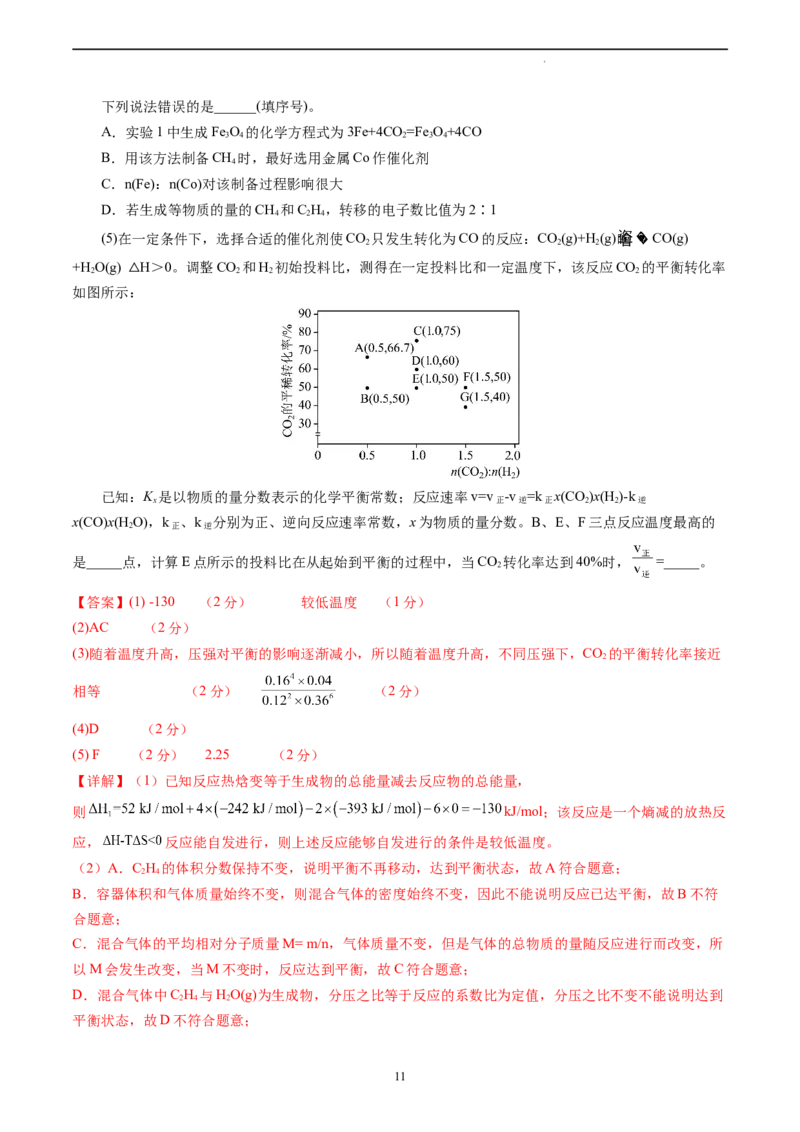
(5)在一定条件下,选择合适的催化剂使CO 只发生转化为CO的反应:CO(g)+H(g) CO(g)
2 2 2
+H O(g) H>0。调整CO 和H 初始投料比,测得在一定投料比和一定温度下,该反应CO 的平衡转化率
2 2 2 2
如图所示:
△
已知:K 是以物质的量分数表示的化学平衡常数;反应速率v=v -v =k x(CO)x(H )-k
x 正 逆 正 2 2 逆
x(CO)x(H O),k 、k 分别为正、逆向反应速率常数,x为物质的量分数。B、E、F三点反应温度最高的
2 正 逆
是_____点,计算E点所示的投料比在从起始到平衡的过程中,当CO 转化率达到40%时, =_____。
2
【答案】(1) -130 (2分) 较低温度 (1分)
(2)AC (2分)
(3)随着温度升高,压强对平衡的影响逐渐减小,所以随着温度升高,不同压强下,CO 的平衡转化率接近
2
相等 (2分) (2分)
(4)D (2分)
(5) F (2分) 2.25 (2分)
【详解】(1)已知反应热焓变等于生成物的总能量减去反应物的总能量,
则 kJ/mol;该反应是一个熵减的放热反
应, 反应能自发进行,则上述反应能够自发进行的条件是较低温度。
(2)A.C H 的体积分数保持不变,说明平衡不再移动,达到平衡状态,故A符合题意;
2 4
B.容器体积和气体质量始终不变,则混合气体的密度始终不变,因此不能说明反应已达平衡,故B不符
合题意;
C.混合气体的平均相对分子质量M= m/n,气体质量不变,但是气体的总物质的量随反应进行而改变,所
以M会发生改变,当M不变时,反应达到平衡,故C符合题意;
D.混合气体中C H 与HO(g)为生成物,分压之比等于反应的系数比为定值,分压之比不变不能说明达到
2 4 2
平衡状态,故D不符合题意;
11
学科网(北京)股份有限公司故选AC。
(3)①随着温度升高,压强对平衡的影响逐渐减小,所以随着温度升高,不同压强下,CO 的平衡转化率
2
接近相等;
②在一体积不变的密闭容器中投入0.4molCO 和1.2molH,发生反应I,CO 的平衡转化率为40%,则反应
2 2 2
二氧化碳0.16mol;
若反应平衡时M点(p 对应压强下)密闭容器的体积为2L,平常常数只受温度影响,则MN两点的平衡常数
2
相同,故N点条件下反应Ⅰ的平衡常数的计算式K= ;
(4)A.由题干表中数据可知,实验1中CO的选择性100%,则该反应的化学方程式为
,A正确;
B.由题干表中数据可知,实验1和实验3比较可知,当用Co作催化剂时 的转化率最高, 的选择
性也很高,则制备 时最好选用金属CO作催化剂,B正确;
C.由题干表中数据可知, 的不同对 的转化率、CO、 、 的选择性均影响很大,
即 对该制备过程影响很大,C正确;
D.本反应中是由 中的+4价的C降低为 中的-2价和CH₄中的-4价,生成等物质的量的 和
,转移的电子数比值为2∶3,D错误;
故选D;
(5)反应为吸热反应,升高温度平衡正向移动,二氧化碳转化率增大;B、E、F投料比不同但转化率相
同,且F点 和 初始投料比最大,说明F点的温度最高;达到平衡状态E点, 转化率刚好达到
50%,设初始投料 和 均为1mol,列三段式:
此时 ;
当 转化率达到40%时,
12
学科网(北京)股份有限公司。
14.(10分)
空气中含大量的氮元素,日常生活中铁的应用非常广泛,可见生产、生活等离不开化学。
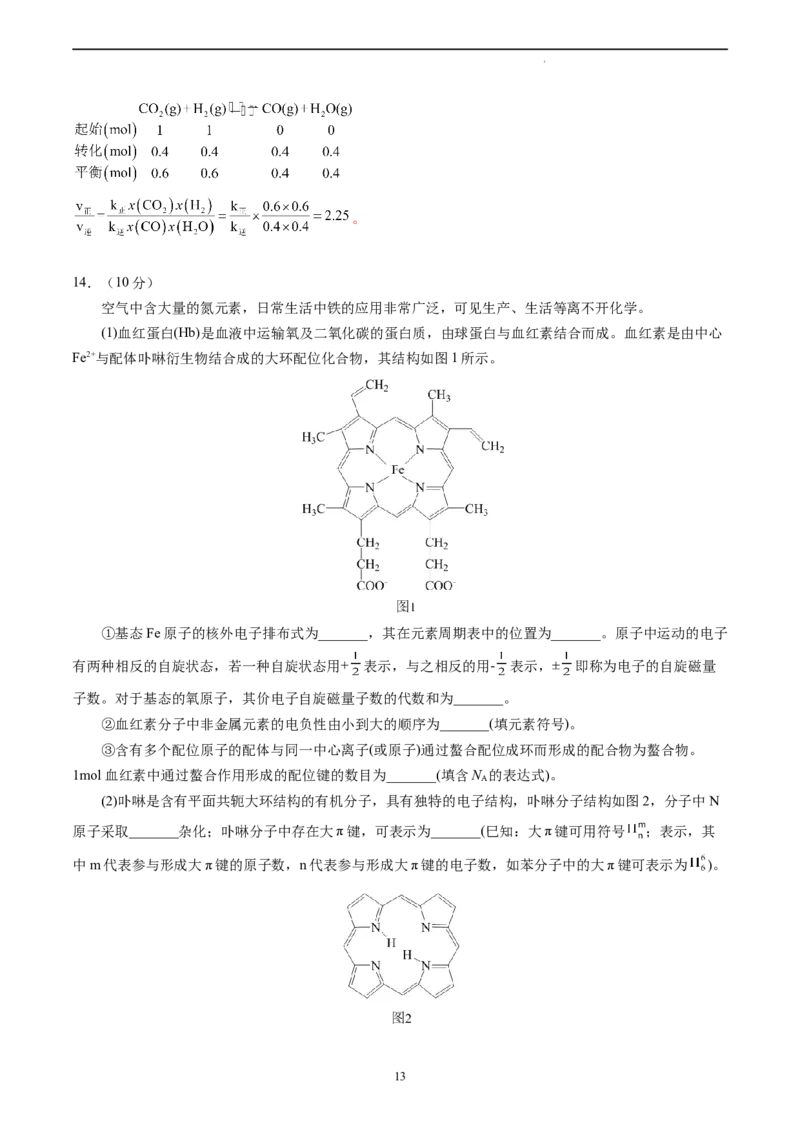
(1)血红蛋白(Hb)是血液中运输氧及二氧化碳的蛋白质,由球蛋白与血红素结合而成。血红素是由中心
Fe2+与配体卟啉衍生物结合成的大环配位化合物,其结构如图1所示。
①基态Fe原子的核外电子排布式为_______,其在元素周期表中的位置为_______。原子中运动的电子
有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用- 表示,± 即称为电子的自旋磁量
子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为_______。
②血红素分子中非金属元素的电负性由小到大的顺序为_______(填元素符号)。
③含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。
1mol血红素中通过螯合作用形成的配位键的数目为_______(填含N 的表达式)。
A
(2)卟啉是含有平面共轭大环结构的有机分子,具有独特的电子结构,卟啉分子结构如图2,分子中N
原子采取_______杂化;卟啉分子中存在大π键,可表示为_______(巳知:大π键可用符号 ;表示,其
中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 )。
13
学科网(北京)股份有限公司(3)Fe O 晶胞(图3)可以划分成8个小的立方单位(图4),分别由4个I型和4个II型小单位拼在一起构
3 4
成。Fe O 晶胞中有_______个O2-, 代表_______。
3 4
【答案】(1)[Ar]3d64s2 (1分) 第四周期Ⅷ族 (1分) +1或-1 (1分)
H< C< N