文档内容
2023 年高考考前押题密卷(重庆卷)
化学·全解全析
1 2 3 4 5 6 7 8 9 10 11 12 13 14
B A C B D C C D A C D C B A
1. 【解析】B
A.用泡沫灭火器灭火时铝离子与碳酸氢根离子在溶液中发生相互促进的水解反应,生成氢氧化铝和二氧化碳
气体,选项A错误;
B.原子是化学变化中的最小微粒,化学变化中原子核不会变,该过程属于核聚变,选项B正确;
C.制备黑火药的原料为S、KNO、C,三者比例为1:2:3,故C错误。
3
D.添加料酒和食醋,使菜变得味香可口的原因是乙醇与乙酸发生酯化反应产生具有特殊香味的乙酸乙酯,选
项D错误。
2. 【解析】A
A. 中心原子价层电子对数为2+ =4,VSEPR模型为四面体构型,故A正确;
B. 的水解方程式为 ,B项错误
C. 苯的实验式为CH,故C错误;
D. 同素异形体是同种元素不同结构的单质, 、 、 、 都是化合物,D项错误;
3. 【解析】C
A.用铁做电极电解饱和食盐水发生的是铁的吸氧腐蚀,阳极反应为Fe-2e-=Fe2+,阴极反应为2HO+O+4e-
2 2
=4OH-,则总反应为:2Fe+2H O+O=2Fe(OH) ,Fe(OH) 进一步被氧气氧化为Fe(OH) ,故A错误;
2 2 2 2 3
B. 因为苯酚的酸性弱于 强于 ,所以苯酚钠溶液中通入 ,生成苯酚和 ,常温下,
苯酚难溶于水,溶液中出现白色浑浊,B错误;
C. 溶液中通入 ,生成黄绿色的 离子,反应的离子方程式为:
,C正确;
D. 与 , 在酸性条件下的氧化性比 强,所以反应为:
,D错误;
4. 【解析】B
A. 氨气极易溶于水,不能用装水的量气管确定其体积,A错误
B. Cu与稀硝酸在常温下发生氧化还原反应产生Cu(NO )、NO、HO,因此可以用装置甲制NO气体,B
3 2 2
1
学学科科网网((北北京京))股股份份有有限限公公司司项正确
C. 该反应为放热反应,导致大试管中温度升高压强增大,红墨水左低右高,C项不能达到实验目的;
D. Cu(NO ) 溶液加热时会促进铜离子水解,且生成硝酸易挥发,应根据其溶解度受温度的影响变化较大,采
3 2
用冷却结晶法制备Cu(NO )·6H O. D错误。
3 2 2
5. 【解析】D
A. 缺标准状况,无法计算22.4L二氧化硫的物质的量,且二氧化硫与水反应为可逆反应,可逆反应不可能完
全进行,所以无法计算使溶液中亚硫酸、亚硫酸氢根、亚硫酸根的数目总和,故A错误;
B. 中含1mol钙离子和2mol氢负离子,离子数目为3 ,故B错误
C. 根据热化学方程式可知,生成 时反应放热 ,则生成 的分子数为 ,故C错误;
D. 乙醇和水分子中均含有氧原子,50 g质量分数为46%的乙醇水溶液中含有的氧原子总数为
,故D正确;
6. 【答案】C 微信搜索“高中试卷君”公众号 领取押题卷联考卷
【分析】Z是元素周期表中电负性最大的元素,则Z为F。基态X原子中有3个未成对电子且其原子序数小于
9,则X为N。根据原子序数大小关系,可判断Y为O。Y和W同主族,则W为S。常温下 的最
高价氧化物对应的水化物溶液的pH=12,说明R的最高价氧化物对应的水化物为强碱,R为K。
A.简单离子半径r(S2-)>r(K+),A项不符合题意;
B.一般来说主族元素最高正价就是原子序数,N的最高正价为+5价,但是F,O比较特殊,O的最高正价为
+2(OF),F没有正价, B项不符合题意
2
C.N为半充满电子排布,其第一电离能大于O,则第一电离能: ,C项符合题意。
D.O的电负性大于S,HO中的成键电子对相比HS更靠近中心原子,成键电子对间的斥力更大,则键角也
2 2
更大。简单氢化物的键角:HO>HS,D项不符合题意。
2 2
7. 【解析】C
A. 与 形成络合物,颜色变化不是因为 将其氧化,加入 , 的存在影响配合物的
种类,颜色发生了变化不是因为 还原,A错误;
B. 水的电离平衡 ,加入CHCOONH 中的CHCOO-与H+结合而 与OH-结合促使HO的
3 4 3 2
电离平衡正向移动,加入的CHCOONH 越多平衡正移的趋势越大,但CHCOO-和 结合的能力相同,导
3 4 3
致溶液中H+和OH-的浓度相等溶液呈中性,B项错误;
C. 取5mL 0.1mol·L-1 KI溶液,滴加5~6滴0.1mol·L-1 FeCl 溶液,两者可以发生反应:2Fe3++2I-=2Fe2++I ,碘
3 2
遇淀粉变蓝。由于Fe3+量少,如果不是可逆反应,则反应后溶液中应该不含Fe3+,但是充分反应后,再滴加少
量的KSCN溶液,溶液变红,说明KI与FeCl 的反应是可逆反应,C正确;
3
2
学学科科网网((北北京京))股股份份有有限限公公司司D. 向AgNO 溶液中滴加过量氨水,得到澄清溶液不是因为Ag+与NH ·H O能大量共存,而是发生反应
3 3 2
AgNO+NH·H O=AgOH↓+NH NO ,生成的AgOH和过量的氨水反应生成溶于水的[Ag(NH)]OH:
3 3 2 4 3 3 2
AgOH+2NH·H O=[Ag(NH)]OH+2H O,D错误;
3 2 3 2 2
8. 【答案】D
【详解】A.布洛芬中含有羧基和饱和烷烃基,是苯甲酸的同系物,A正确;
B.该修饰过程发生取代反应,所以原子利用率小于100%,B正确;
C.X分子中本换上的碳原子有 杂化,饱和碳原子为 杂化,C正确;
D.根据X分子结构,含有12种化学环境不同的氢原子,D错误;
故选D。
9. 【答案】A
【详解】A.a的坐标为(0,0,0),b的坐标 ,则a原子位于坐标原点,b原子在体对角线的顶点,可知
c原子到x轴、y轴、z轴的距离分别是 , , ,即c的坐标为 ,A正确;
B.该晶胞中Zn原子的配位数是4,则ZnSe晶胞中Se原子的配位数也是4,B错误;
C.Se的简化电子排布式:[Ar]3d104s24p4,C错误;
D. 和 半径不同,则晶胞棱长将改变,D错误;
10. 【答案】C
A. CO用于处理大气污染物 的反应为 ,A不符合题意
B. 由图2可知,总反应为反应物总能量大于生成物总能量的放热反应,反应ΔH=-361.22kJ/mol,B不符合题
意
C. 反应①的活化能为149.6 kJ/mol,反应②的活化能为108.22 kJ/mol,反应活化能越大,反应速率越慢,总反
应的决速步是慢反应,所以总反应的决速步是反应①,
D. 从图2可知,开始加入的是Zn+。
11. 【答案】D
【分析】由图可知,A极发生还原反应生成羧酸,反应为 ,A为
阴极;B极发生氧化反应生成 ,反应为 -2e-+Br- +H+,B为阳极;
【详解】A.电解池中阳离子向阴极迁移,H+向A极移动,A错误;
B.由分析可知,A极发生还原反应生成羧酸,反应为
3
学学科科网网((北北京京))股股份份有有限限公公司司,B错误;
C.铅蓄电池放电总反应为: ;若使用铅蓄电池作电源,则每生成0.5mol苯乙酸,
根据电子守恒可知, ,消耗1molH SO ,质量为98g,C错误;
2 4
D.该反应的总反应为 , 故原子利用
率为100%,有利于实现碳中和,D正确;微信搜索“高中试卷君”公众号 领取押题卷联考卷
故选D。
12. 【答案】C
【分析】 , (含少量的 和 )溶液加入氢氧化
钡,可以促使 转化为 ,进而和钡离子生成 沉淀;过滤滤液电解阳极上发生氧化反应五价氯
转化为七价氯得到 ,阴极生成氢气和氢氧根离子,浓缩加入饱和氯化铵将 转化为溶解度较小
结晶析出;
【详解】A.由分析可知,加入 可以增加溶液的碱性,促使 转化为 ,A错误;
B.电解时阴极附近生成氢氧根离子,溶液pH增大,B错误;
C.电解生成氢氧化钠,加入饱和 溶液,铵根离子和氢氧根离子反应会生成氨气,C正确;
D. 、 、 三种物质中, 首先结晶析出,故其溶解度最小,D错误;
故选C。
13. 【答案】B
【分析】10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质的量为(0.2+0.
2+0.1)mol×(1-20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡时
n(ClNO)=7.5×10-3mol·L-1·min-1×10min×2L=0.15mol,设①中反应的NO 为xmol,②中反应的Cl 为ymol,则:
2 2
4
学学科科网网((北北京京))股股份份有有限限公公司司则0.5x+2y=0.15,(0.2-x+0.2-2y+0.1-y)+0.5x+2y=0.4,解得x=0.1、y=0.05,
【详解】A.据分析,平衡后c(NO)= =0.05mol·L-1,A错误;
B.由分析,平衡时 的转化率为 %=50%,B正确;
C.平衡常数只受温度影响,反应在绝热条件下进行,反应②放热,使温度升高,平衡逆向移动,平衡常数K
2
减小, C错误;
D.①2NO (g)+NaCl(s) NaNO (s)+ClNO(g) ΔH<0平衡常数K ;②2NO(g)+Cl (g) 2ClNO(g) ΔH<0平
2 3 1 1 2 2
衡常数K ;由盖斯定律可知,由①×2-②可得反应4NO (g)+2NaC1(s) 2NaNO (s)+2NO(g)+Cl (g),则4NO (g)
2 2 3 2 2
+2NaC1(s) 2NaNO (s)+2NO(g)+Cl (g)的平衡常数K= , D错误;
3 2
答案选B。
14. 【答案】A
【详解】A.在 溶液呈中主要存在电离平衡: , ,水解平衡:
, ,因为 ,电离程度大于水解程度,溶液显酸性,
= , > ,即a+ a < 14,A错误;
1 2
B.根据电荷守恒,在磷酸溶液中: ,B正确;
C.pH=7时pKa=pH,可知 =H PO ,因为该废水pH约为6,c( )>c( ), 少部分电离
2
生成 ,所以c( )>c( ),故溶液中存在:c( )>c( )>c( ),C正确;
D.该废水中主要的离子为 ,加入 溶液生成 的主要反应为
,D正确;
故选A。
15. 【答案】
(1) (1分) 价电子排布为 ,失去一个电子形成更稳定的 半满结构(2分)
5
学学科科网网((北北京京))股股份份有有限限公公司司(2) (2分)
(3) (2分)
(4) (2分) 草酸钪沉淀转化为可溶性络合物(1分)
(5) (2分) (2分)
【详解】(1)Fe为26号元素,其价电子排布式为: , 价电子排布为 ,失去一个电子后形成
, 价电子排布为 ,半满结构更稳定,因此 易被氧化成 ,故答案为: ; 价电子
排布为 ,失去一个电子形成更稳定的 半满结构;
(2)“浸取”时铁屑被 氧化为 , 被还原为 ,根据得失电子守恒和原子守恒可得反应的
离子方程式是 ;
(3)常温下, ,当 时, ,
;微信搜索“高中试卷君”公众号 领取押题卷联考卷
(4) 的平衡常数
。由已知信息③可知,草酸可与多种金属离子形成可
溶性络合物,故草酸用量过多时,草酸钪沉淀可能会转化为可溶性络合物,导致钪的沉淀率下降;
(5)设起始时 的物质的量为1 mol,质量为462 g,由图可知,250℃时,减少的质量为
, ,即晶体失去5个结晶水,故250℃时晶体的主要成分是
。250~550℃减少的质量为 ,可知550℃时晶体的主要成分是 。
850℃时剩余固体的质量为 ,除去钪元素质量后剩余质量为
,应为氧元素的质量, ,则850℃时晶体的化学式为 ,
故550~850℃发生反应的化学方程式为 。
16. 【答案】
6
学学科科网网((北北京京))股股份份有有限限公公司司(1) (2分)
(2) I (1分) 主反应 催化加氢制甲醇放热,竞争反应吸热,150~250℃时升温使主反应平衡逆向移
动的程度大于竞争反应平衡正向移动的程度 (2分) 50 (2分) (2分)
(3) (2分) b(1分)
(4) 阳离子(1分) (2分)
【详解】(1)由题图可看出反应物和生成物的总能量差值,故热化学方程式为
;
(2)①升高温度, 催化加氢制甲醇[提示:该反应放热]的平衡逆向移动,甲醇的物质的量分数减小,故
曲线Ⅰ代表 的物质的量分数随温度的变化;
② 催化加氢制甲醇为放热反应,升高温度,平衡逆向移动, 转化率降低,竞争反应
为吸热反应,升高温度,平衡正向移动, 转化率升高,150~250℃时
升高温度使 催化加氢制甲醇平衡逆向移动的程度大于竞争反应平衡正向移动的程度,使 转化率下降;
③ 平衡转化率为20%,则 转化的物质的量为0.2 mol,生成CO的物质的量为0.1 mol,列出三段式:
平衡时气体总物质的量为3.8 mol, 。 的平衡分压为 , 的平衡
分压为 ,CHOH的平衡分压为 , 的平衡分压为 ,则
3
在题给一定温度下的压强平衡常数 ;
7
学学科科网网((北北京京))股股份份有有限限公公司司(3)将坐标(7.2,56.2)和(7.5,27.4)代入 ,得 ,
,解得 ;题图中对应的直线斜率越大,对应反应的
越小,催化效率越高,故比催化剂a更高效的催化剂为b。
(4)从图分析,c电极产生氮气,为阳极反应,d上产生氢气,为阴极反应,则a为负极,锌失去电子,结合
氢氧根离子,故该交换膜为阴离子交换膜,b为正极,与b极室相连的交换膜为阳离子交换膜,装置Ⅱ阳极上
的反应式为 。
17. 【答案】
(1)分液漏斗(1分)
(2) A→D→C→E→B (2分) 防止多余的 污染空气,同时防止空气中的水蒸气进入装置E,使
潮解(2分)
(3) (2分)
(4) 溶于水电离出 ,使 的电离平衡逆向移动,防止加入氨水时溶液中 过大,生成
沉淀 (2分)
(5)控制反应速率 (1分) 防止温度过高使 和 分解(1分)
(6) (2分)
(7)趁热过滤、冷却结晶(1分)
【分析】利用浓盐酸与高锰酸钾反应制氯气,通过饱和食盐水除去氯气中的氯化氢,再通过浓硫酸干燥,得到
的干燥纯净的氯气通入装置E与钴加热条件下反应生成氯化钴;再利用氯化钴与氨化铵在活性炭催化下反应
制 ;微信搜索“高中试卷君”公众号 领取押题卷联考卷
【详解】(1)仪器a的名称为分液漏斗;
(2)装置A用于制备Cl,装置D用于除去Cl 中的HCl,装置C用于干燥Cl,装置E用于制备CoCl ,装置
2 2 2 2
B的作用是防止多余的氯气污染空气,同时防止空气中的水蒸气进入装置E,使CoCl 潮解,故连接顺序为
2
A→D→C→E→B;
(3)装置A中KMnO 和浓盐酸反应制备Cl;
4 2
(4) 溶于水电离出 ,能使 的电离平衡逆向移动,进而可以抑制 的电离,防止
加入氨水时溶液中 过大,生成 沉淀,有利于 的配位;
(5) 和 受热易分解,步骤Ⅱ中控制温度在10℃以下并缓慢加入 溶液是为了控制反应速
8
学学科科网网((北北京京))股股份份有有限限公公司司率,防止温度过高使 和 分解;
(6)在题给制备反应中, 是氧化剂,根据得失电子守恒、原子守恒可得总反应的化学方程式为
;
(7)根据已知信息②可知, 在水中的溶解度随着温度的升高而增大,应先趁热过滤除去活性
炭等杂质,再经冷却结晶、过滤、洗涤、干燥等操作得到 晶体。
18. 【答案】
(1)C H O(2分)
9 10
(2)取代反应(1分)
(3)FeCl 溶液或浓溴水(1分) 醚键、羧基(2分)
3
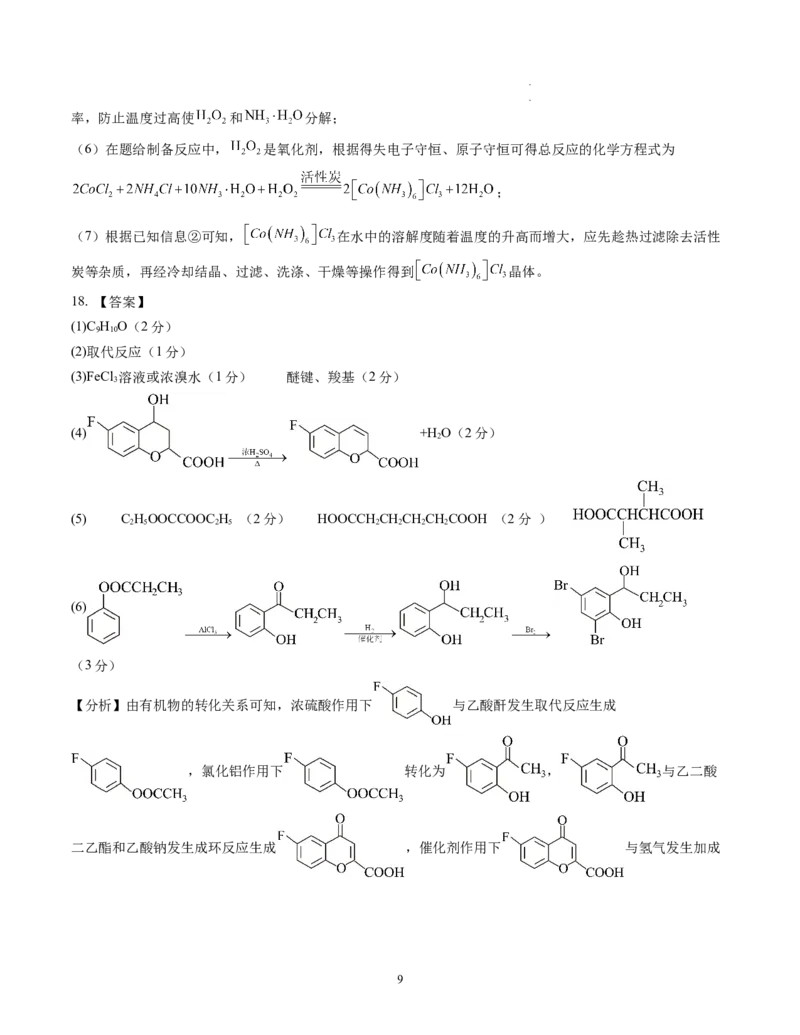
(4) +H O(2分)
2
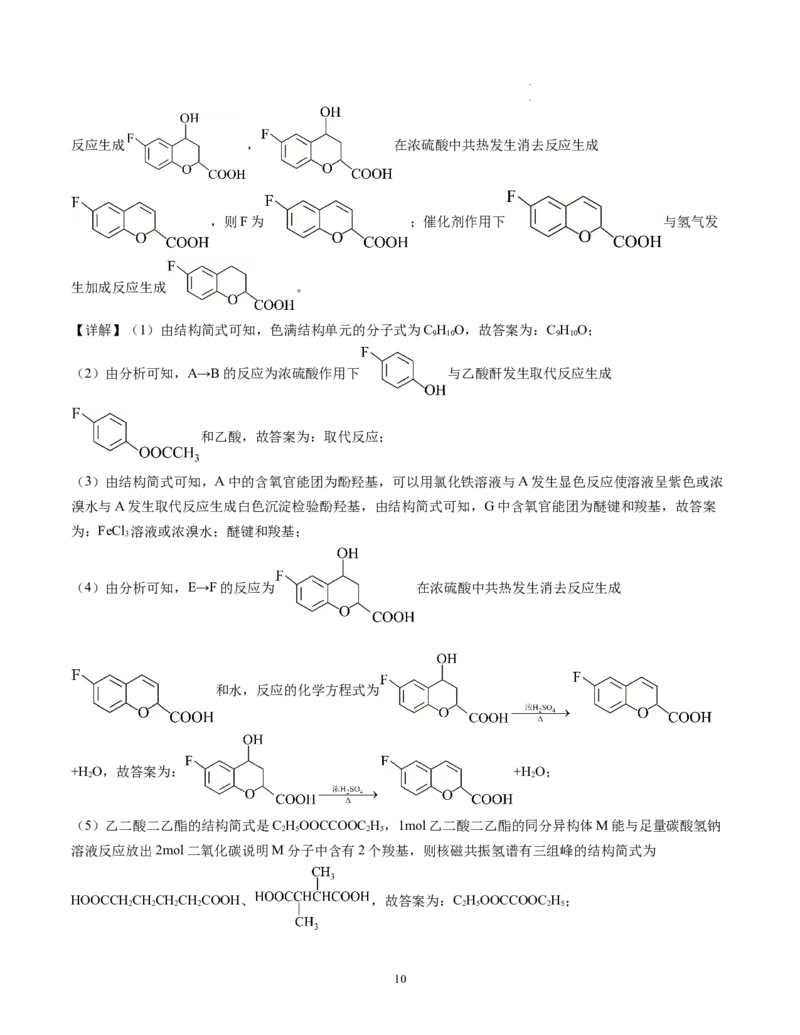
(5) C HOOCCOOC H (2分) HOOCCH CHCHCHCOOH (2分 )
2 5 2 5 2 2 2 2
(6)
(3分)
【分析】由有机物的转化关系可知,浓硫酸作用下 与乙酸酐发生取代反应生成
,氯化铝作用下 转化为 , 与乙二酸
二乙酯和乙酸钠发生成环反应生成 ,催化剂作用下 与氢气发生加成
9
学学科科网网((北北京京))股股份份有有限限公公司司反应生成 , 在浓硫酸中共热发生消去反应生成
,则F为 ;催化剂作用下 与氢气发
生加成反应生成 。
【详解】(1)由结构简式可知,色满结构单元的分子式为C H O,故答案为:C H O;
9 10 9 10
(2)由分析可知,A→B的反应为浓硫酸作用下 与乙酸酐发生取代反应生成
和乙酸,故答案为:取代反应;
(3)由结构简式可知,A中的含氧官能团为酚羟基,可以用氯化铁溶液与A发生显色反应使溶液呈紫色或浓
溴水与A发生取代反应生成白色沉淀检验酚羟基,由结构简式可知,G中含氧官能团为醚键和羧基,故答案
为:FeCl 溶液或浓溴水;醚键和羧基;
3
(4)由分析可知,E→F的反应为 在浓硫酸中共热发生消去反应生成
和水,反应的化学方程式为
+H O,故答案为: +H O;
2 2
(5)乙二酸二乙酯的结构简式是C HOOCCOOC H,1mol乙二酸二乙酯的同分异构体M能与足量碳酸氢钠
2 5 2 5
溶液反应放出2mol二氧化碳说明M分子中含有2个羧基,则核磁共振氢谱有三组峰的结构简式为
HOOCCH CHCHCHCOOH、 ,故答案为:C HOOCCOOC H;
2 2 2 2 2 5 2 5
10
学学科科网网((北北京京))股股份份有有限限公公司司HOOCCH CHCHCHCOOH; ;
2 2 2 2
(6)由有机物的转化关系可知,以 为原料制备 的合成步骤为氯化铝作用
下 转化为 ,催化剂作用下 与氢气发生加成反应生成
, 与溴水发生取代反应生成 ,合成路线为
,故答
案为:
。
11
学学科科网网((北北京京))股股份份有有限限公公司司12
学学科科网网((北北京京))股股份份有有限限公公司司