文档内容
长沙市一中2026届高三月考试卷(一)
化 学
时量:75分钟 满分:100分
得分:
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Cl—35.5
Cr—52 Mn—55
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一项符合题目要求)
1.化学与生活密切相关。下列说法正确的是
A. FeCl₃溶液可用于腐蚀印刷铜质线路板是因为 Fe比 Cu的金属性强
B.“天和核心舱”推进系统中的腔体采用的氮化硼陶瓷属于新型无机非金属材料
C.红色油漆中含有的三氧化二铁属于金属材料
D.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
2.下列化学用语表述正确的是
A. HClO的空间填充模型:
B.羟基的电子式:O:H
C. NaCl溶液中的水合离子:(
D. Fe²⁺ ·········································
3.设NA为阿伏加德罗常数的值,下列说法错误的是
A.25℃、101 kPa条件下,12.25 L SO₂ 中所含原子数为1.5NA
B.1 L-0.1m ol/L K₂Cr₂O₇溶液中 Cr₂O²⁻离子数为0.1NA
C.23g有机物C₂H₆O中含有极性共价键的数目可能为4NA
D.0.5m ol C₂H₅OH 中采用sp³杂化的原子数为1.5NA
4.下列选项所示物质间的转化在指定条件下可以实现的是
A.海水中提取镁:浓缩海水-石灰乳 Mg(OH)₂(s)盐酸-MgCl₂(aq)电解 Mg
B.漂白粉CO₃HClO光照Cl₂
C. SiO₂ C₆溶CO₂Na₂SlO₃→H₂SiO₃
D.制备配合物:CuSO₄溶液过量氨水,[Cu(NH₃)₄]SO₄乙醇[Cu(NH₃)₄]SO₄·H₂O
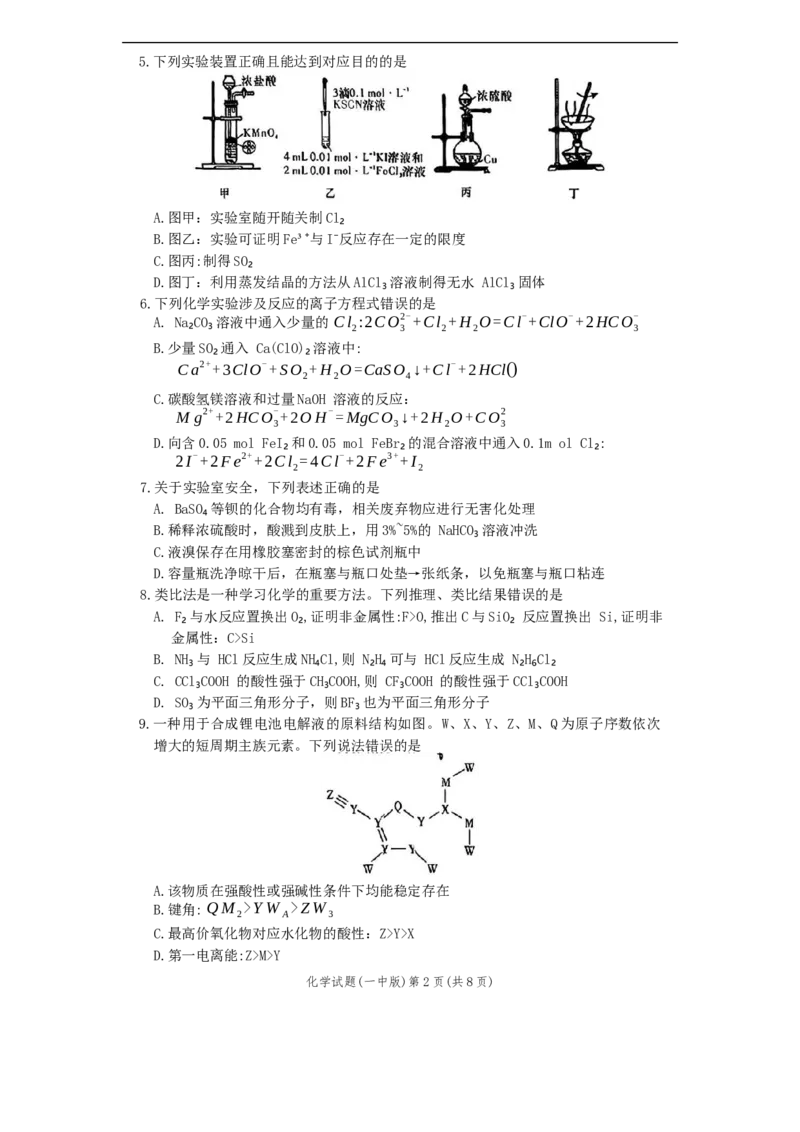
化学试题(一中版)第1页(共8页)5.下列实验装置正确且能达到对应目的的是
A.图甲:实验室随开随关制Cl₂
B.图乙:实验可证明Fe³⁺与I⁻反应存在一定的限度
C.图丙:制得SO₂
D.图丁:利用蒸发结晶的方法从AlCl₃溶液制得无水 AlCl₃固体
6.下列化学实验涉及反应的离子方程式错误的是
A. Na₂CO₃溶液中通入少量的 Cl :2CO2-+Cl +H O=Cl-+ClO-+2HCO-
2 3 2 2 3
B.少量SO₂通入 Ca(ClO)₂溶液中:
Ca2++3ClO-+SO +H O=CaSO ↓+Cl-+2HCl O
2 2 4
C.碳酸氢镁溶液和过量NaOH 溶液的反应:
M g2++2HCO-+2OH-=MgCO ↓+2H O+CO2
3 3 2 3
D.向含0.05 mol FeI₂和0.05 mol FeBr₂的混合溶液中通入0.1m ol Cl₂:
2I-+2Fe2++2Cl =4Cl-+2Fe3++I
2 2
7.关于实验室安全,下列表述正确的是
A. BaSO₄等钡的化合物均有毒,相关废弃物应进行无害化处理
B.稀释浓硫酸时,酸溅到皮肤上,用3%~5%的 NaHCO₃溶液冲洗
C.液溴保存在用橡胶塞密封的棕色试剂瓶中
D.容量瓶洗净晾干后,在瓶塞与瓶口处垫→张纸条,以免瓶塞与瓶口粘连
8.类比法是一种学习化学的重要方法。下列推理、类比结果错误的是
A. F₂与水反应置换出O₂,证明非金属性:F>O,推出C与SiO₂ 反应置换出 Si,证明非
金属性:C>Si
B. NH₃与 HCl反应生成NH₄Cl,则 N₂H₄可与 HCl反应生成 N₂H₆Cl₂
C. CCl₃COOH 的酸性强于CH₃COOH,则 CF₃COOH 的酸性强于CCl₃COOH
D. SO₃为平面三角形分子,则BF₃也为平面三角形分子
9.一种用于合成锂电池电解液的原料结构如图。W、X、Y、Z、M、Q为原子序数依次
增大的短周期主族元素。下列说法错误的是
A.该物质在强酸性或强碱性条件下均能稳定存在
B.键角: QM >YW >ZW
2 A 3
C.最高价氧化物对应水化物的酸性:Z>Y>X
D.第一电离能:Z>M>Y
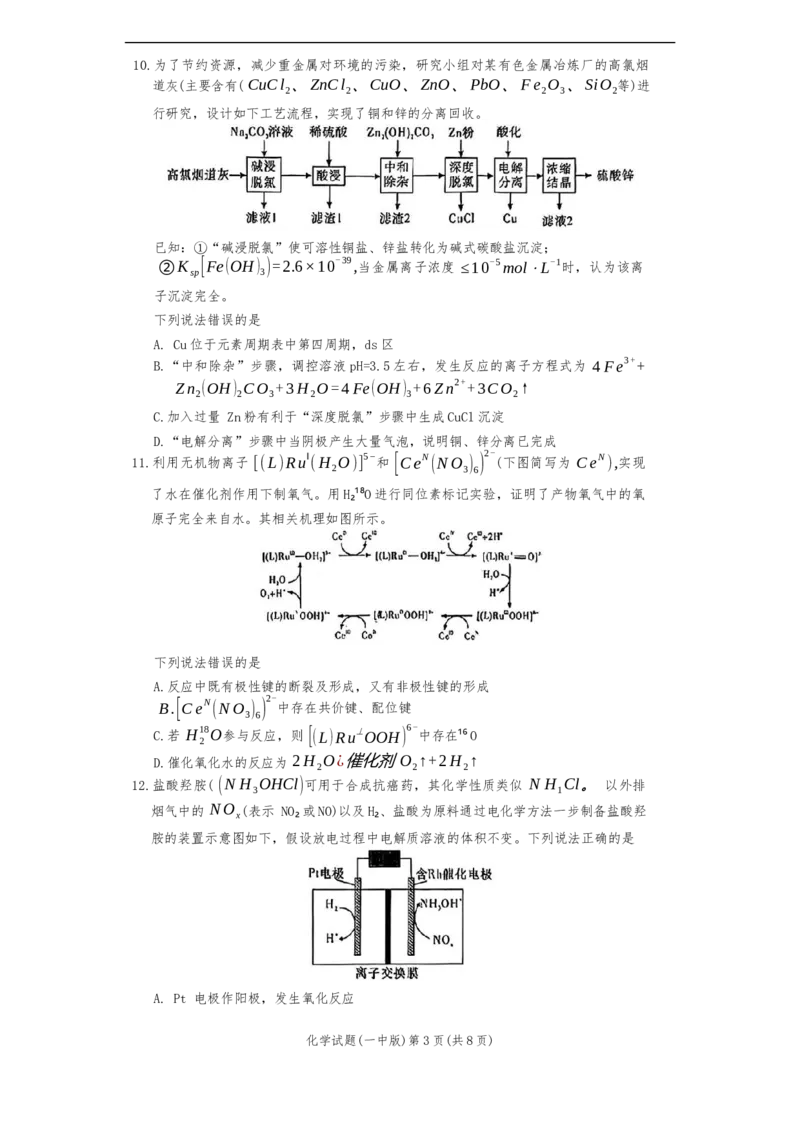
化学试题(一中版)第2页(共8页)10.为了节约资源,减少重金属对环境的污染,研究小组对某有色金属冶炼厂的高氯烟
道灰(主要含有( CuCl 、ZnCl 、CuO、ZnO、PbO、Fe O 、SiO 等)进
2 2 2 3 2
行研究,设计如下工艺流程,实现了铜和锌的分离回收。
已知:①“碱浸脱氯”使可溶性铜盐、锌盐转化为碱式碳酸盐沉淀;
②K [Fe(OH) )=2.6×10-39,当金属离子浓度 ≤10-5mol⋅L-1时,认为该离
sp 3
子沉淀完全。
下列说法错误的是
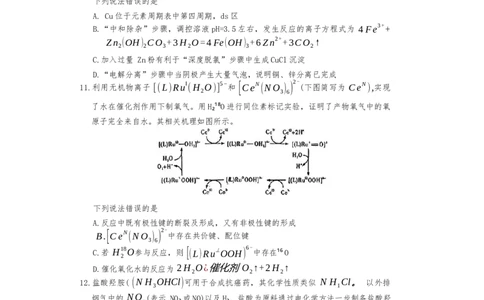
A. Cu位于元素周期表中第四周期,ds区
B.“中和除杂”步骤,调控溶液pH=3.5左右,发生反应的离子方程式为 4Fe3++
Zn (OH) CO +3H O=4Fe(OH) +6Zn2++3CO ↑
2 2 3 2 3 2
C.加入过量 Zn粉有利于“深度脱氯”步骤中生成CuCl沉淀
D.“电解分离”步骤中当阴极产生大量气泡,说明铜、锌分离已完成
11.利用无机物离子 [(L)Ru‖ (H O)] 5−和 [CeN (NO ) ) 2- (下图简写为 CeN ),实现
2 3 6
了水在催化剂作用下制氧气。用H₂¹⁸O进行同位素标记实验,证明了产物氧气中的氧
原子完全来自水。其相关机理如图所示。
下列说法错误的是
A.反应中既有极性键的断裂及形成,又有非极性键的形成
B.[CeN (NO ) )
2-
中存在共价键、配位键
3 6
C.若 H18O参与反应,则 [(L)Ru⟂OOH) 6- 中存在¹⁶O
2
D.催化氧化水的反应为 2H O¿催化剂O ↑+2H ↑
2 2 2
12.盐酸羟胺( (N H OHCl)可用于合成抗癌药,其化学性质类似 N H Cl。 以外排
3 1
烟气中的 NO (表示 NO₂或NO)以及H₂、盐酸为原料通过电化学方法一步制备盐酸羟
x
胺的装置示意图如下,假设放电过程中电解质溶液的体积不变。下列说法正确的是
A. Pt 电极作阳极,发生氧化反应
化学试题(一中版)第3页(共8页)B 含 Rh 催化电极的电极反应式为 NO +(2x+1)e-+(2x+2)H+=
x
N H OH++xH O
3 2
C.若NO₂表示 NO₂,当右室溶液质量增加5.1g 时,消耗 NO₂的物质的量为0.1m
ol
D.若NOr表示 NO,反应一段时间后,左室溶液 pH减小
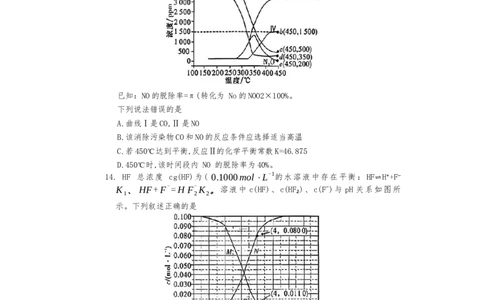
13.脱除尾气中的CO、NO包括以下两个反应: 1.2NO(g)+CO(g)=N O(g)+
2
CO (g´)△H <0;I.[.N O(g)+CO(g)=N (g)+CO (g)△H <0。将
2 1 2 2 2 2
恒定组成的混合气体通入恒容不同温度的反应器,相同时间内检测反应中涉及的
各物质的浓度,结果如图。
已知:NO的脱除率=π(转化为 No的NOO2×100%。
下列说法错误的是
A.曲线Ⅰ是CO,Ⅱ是NO
B.该消除污染物CO和NO的反应条件应选择适当高温
C.若450℃达到平衡,反应Ⅱ的化学平衡常数K=46.875
D.450℃时,该时间段内 NO 的脱除率为40%。
14. HF 总浓度 cg(HF)为( 0.1000mol⋅L-1的水溶液中存在平衡:HF⇌H⁺+F⁻
K 、HF+F-=H F-K 。溶液中 c(HF)、c(HF₂)、c(F⁻)与 pH 关系如图所
1 2 2
示。下列叙述正确的是
A. M、N分别为c(HF)~pH、c(HF₂)~pH关系曲线
c(H+)⋅c(F-) c(H F-)
B.K = ≈7×10-4,K = 2 ≈5
1 c(HF) 2 c(HF)⋅c(F-)
C.溶液中( c (HF)=c(F-)+c(HF)+c(H F-)
a 2
D. pH=1|的溶液中(
c(H+)=c(F-)+c(H F-)+c(OH-)
2
化学试题(一中版)第4 页(共8页)答题卡
题号 1 2 3 4 5 6 7 8 9 10 11 I2 13 14 得分
答案
二、非选择题(本题共4 小题,共58分)
15.(14分)三氯化铬是常用的媒染剂和催化剂,易潮解、易升华,高温下易
被氧气氧化。实验室用 Cr₂O₃和CCl₄(沸点76.8℃)在高温下制备无水(
CrCl ,同时生成COCl₂气体(能与水反应生成两种酸性气体)。可利用下面
3
装置模拟制取三氯化铬(K₁、K₂为气流控制开关)。
(1)下列实验图标中与本实验无关的是 (填标号)。
A B C D
(2)装置乙和装置丁的水槽中盛装的液体分别为 、 (填“冷
水”或“热水”)
(3)从安全的角度考虑,整套装置的不足是 。
(4)装置己中 NaOH溶液能够吸收COCl₂,发生反应的离子方程式为
(5)Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图所示。
请补充完整由 CrCl 溶液制备纯净的( Cr(OH) 的实验方案:取适量(
3 3
CrCl 溶液,加入 NaOH 溶液, ;充分反
3
应 后 过 滤 , 用 蒸 馏 水 洗 涤 沉 淀 ,
,则证明沉淀已洗涤干净;低温烘干沉淀,得到( Cr(OH) 晶体。
3
(6)取三氯化铬样品 mg,配制成250mL溶液。移取25.00mL于碘量瓶中,
加热至沸腾后,加适量 2mol⋅L-1NaOH溶液,生成绿色沉淀
Cr(OH) 。冷却后,加足量 30%H₂O₂,小火加热至绿色沉淀完全溶
3
解。冷却后,加入2
化学试题(一中版)第5 页(共8页)mol⋅L-1H SO 酸化,再加入足量KI溶液,加塞摇匀充分反应后,
2 4
铬元素只以 Cr³⁺存在,暗处静置 5m in 后,加入指示剂,用(
0.1mol⋅L-1标准 Na₃S₂O₃溶液滴定至终点,消耗标准 Na₂S₂O₃溶液V
mL(杂质不参加反应)。
已 知 :
Cr(OH) +3H O +4OH-=2CrO2-+8H O:2Na S O +I =-
3 2 2 3 2 2 2 3 2
Na S O +2NaI。样 品 中 无 水 三 氯 化 铬 的 质 量 分 数 为
2 1 6
(用含m、V的代数式表示)。
16.(14分)以大洋锰结核(主要由 MnO₂ 和铁的氧化物组成,还含有 Al₂O₃、
MgO、ZnO、CaO、SiO₂ 等)为原料,制备 Mn₂O,及 Mn(H PO ) ⋅2H O的
2 4 2 2
工艺流程如下
已 知 :25℃ 时
,K (MnS)=2.5×10-13;K (ZnS)=2.9×10-25;K (MnF )=5.3×10⁻
,p sp w 2
³;Kₛₚ(MgF₂) = 7.4×10⁻¹¹; Kₛₚ[Mn(OH)₂]= 1.9 ×10⁻¹³;
K (MnCO )=2.2×10-11;K (N H ⋅H O)=1.0×10-47
xp 3 b 3 2
(1)基态 Zn的价电子排布式为 。
(2)滤渣1的主要成分是 。
(3)“净化”步骤中,加入的Na₂S浓度不宜过大,原因是 。
(4)“ 沉 锰 ” 时 , 生 成 MnCO₃ 的 离 子 方 程 式 为
。“沉锰”时需缓慢向含 MnSO₄ 的溶液中滴加 NH₄HCO₃,否则会发生反
应 MnCO (s)+2QH- (aq)=Mn(OH) (s)+CO2- (aq)而 生 成
3 2 3
Mn(OH)₂,该反应的平衡常数 K= (保留一位小数)。
(5)“操作qK”的过程为 、洗涤、干燥。
(6)Mn的某种氧化物的晶胞(立方体结构)如图
所示。已知该晶胞参数为a nm,该晶体的密
度为. g·cm⁻³((设NA 为阿伏加
德罗常数,用含a和NA的代数式表示)。
17.(15分)利用工业废气中的 H₂S制备焦亚硫酸
钠 (Na S O )的一种流程示意图如下。
2 2 5
已知: ①Na S O 在空气中易被氧化,受热易分解;
2 2 5
②室温下,H₂CO₃和 H₂SO₃的电离常数如下。
物质 H₂CO₃ H₂SO₃
K (25❑∘C) K₀₁=4.5×10⁻⁷、K ₀₁=1.4×10⁻²、
A
K =4.7×10-11 Kₐ₂=6.0×10⁻⁸
A2化学试题(一中版)第6页(共8页)Ⅰ.在多级串联反应釜中,Na₂CO₃悬浊液与持续通入的SO₂进行如下反应。
第一步: 2Na CO +SO +H O=Na SO +2NaHCO ;
2 3 2 2 2 3 3
第 二 步 : NaHCO +SO =NaHSO +CO Na SO +SO +H O=
3 2 3 2 2 3 2 2
,2NaHSO₃。
Ⅱ.当反应釜中溶液pH达到3.8~4.1时,形成的 NaHSO₃过饱和溶液
静置后会结品析出焦亚硫酸钠晶体。
(1)焦亚硫酸(H₂S₂O₅)的结构式为 其中·S的杂化方
式为 。常温下焦亚硫酸钠溶于水形成的溶液显
(填“酸”“中”或“碱”)性。
(2)配碱槽中,母液和过量Na₂CO₃配制反应液,发生反应的化学方程
式是 。
(3)下列试剂、仪器组合也可用于处理尾气的是 (填标号)。
(4)若反应条件或用量等因素控制不当,则所得的 Na₂S₂O₅产品中往往
含有杂质。①若检验产品中含有杂质Na₂CO₃,下列试剂的使用顺序
依次为 (填标号)。
a.稀硫酸 b.澄清石灰水 c.品红溶液 d.酸性KMnO₄溶液
②久置的 Na₂S₂O₅固体中若含有 Na₂SO₄ 杂质,其可能的原因是
(用化学方程式解释)。
(5)Na₂S₂O₅ 生产过程中会产生 SO₂,SO₂ 在空气中的含量超过 0.02
mg·L⁻¹ 就会危害人类健康。可用如下装置测定空气中 SO₂ 的含
量。
①取 5.mL,5×10-4mol⋅L-1的碘溶液加入试管中,再加入2~3滴
淀粉溶液,在测定地点慢慢抽气,每次抽气100 mL,直到试管中
的溶液 (填写现象)。
②记录抽气次数n。n≥ ,说明气体符合安全标准(假设气
体均处于标准状况)。
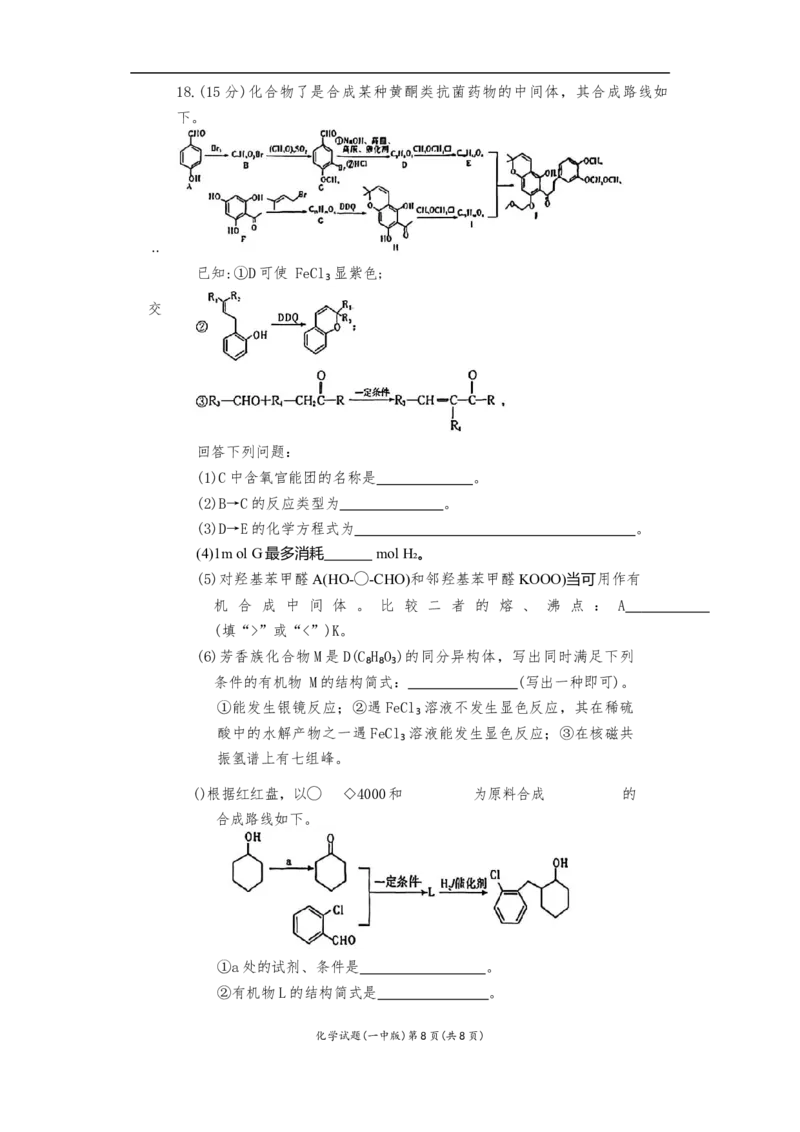
化学试题(一中版)第7 页(共8页)18.(15分)化合物了是合成某种黄酮类抗菌药物的中间体,其合成路线如
下。
已知:①D可使 FeCl₃显紫色;
交
回答下列问题:
(1)C中含氧官能团的名称是 。
(2)B→C的反应类型为 。
(3)D→E的化学方程式为 。
(4)1m ol G最多消耗 mol H₂。
(5)对羟基苯甲醛A(HO-◯-CHO)和邻羟基苯甲醛KOOO)当可用作有
机 合 成 中 间 体 。 比 较 二 者 的 熔 、 沸 点 : A
(填“>”或“<”)K。
(6)芳香族化合物M是D(C₈H₈O₃)的同分异构体,写出同时满足下列
条件的有机物 M的结构简式: (写出一种即可)。
①能发生银镜反应;②遇FeCl₃溶液不发生显色反应,其在稀硫
酸中的水解产物之一遇FeCl₃溶液能发生显色反应;③在核磁共
振氢谱上有七组峰。
()根据红红盘,以◯ ◇4000和 为原料合成 的
合成路线如下。
①a处的试剂、条件是 。
②有机物L的结构简式是 。
化学试题(一中版)第8页(共8页)
: