文档内容
湘豫名校联考
2023 年 9 月高三一轮复习诊断考试(一)
化 学
注意事项:
1.本试卷共10页。时间90分钟,满分100分。答题前,考生先将自己的姓名、准考证号填写
在试卷指定位置,并将姓名、考场号、座位号、准考证号填写在答题卡上,然后认真核对条形
码上的信息,并将条形码粘贴在答题卡上的指定位置。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。作答非选择题时,将答案写在答题卡上对应的
答题区域内。写在本试卷上无效。
3.考试结束后,将试卷和答题卡一并收回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 K 39 Mn 55
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.古代文化典籍蕴含着丰富的化学知识。下列古代文献涉及氧化还原反应的是( )
A.《本草经集注》中关于硝石( )和朴消( )的鉴别方法:“以火烧之,紫青烟起,乃真
硝石也”
B.《荀子·劝学》中“冰水为之,而寒于水”
C.《梦溪笔谈》中“石穴中水,所滴皆为钟乳”
D.《天工开物》中“凡火药,硫为纯阳,硝为纯阴,两精逼合,成声成变,此乾坤幻出神物也”
2.下列化学用语的应用或概念描述正确的是( )
A.醋酸的电离方程式:
B.乙酸乙酯的结构简式:
C.P原子的结构示意图:
D. 分子的球棍模型:
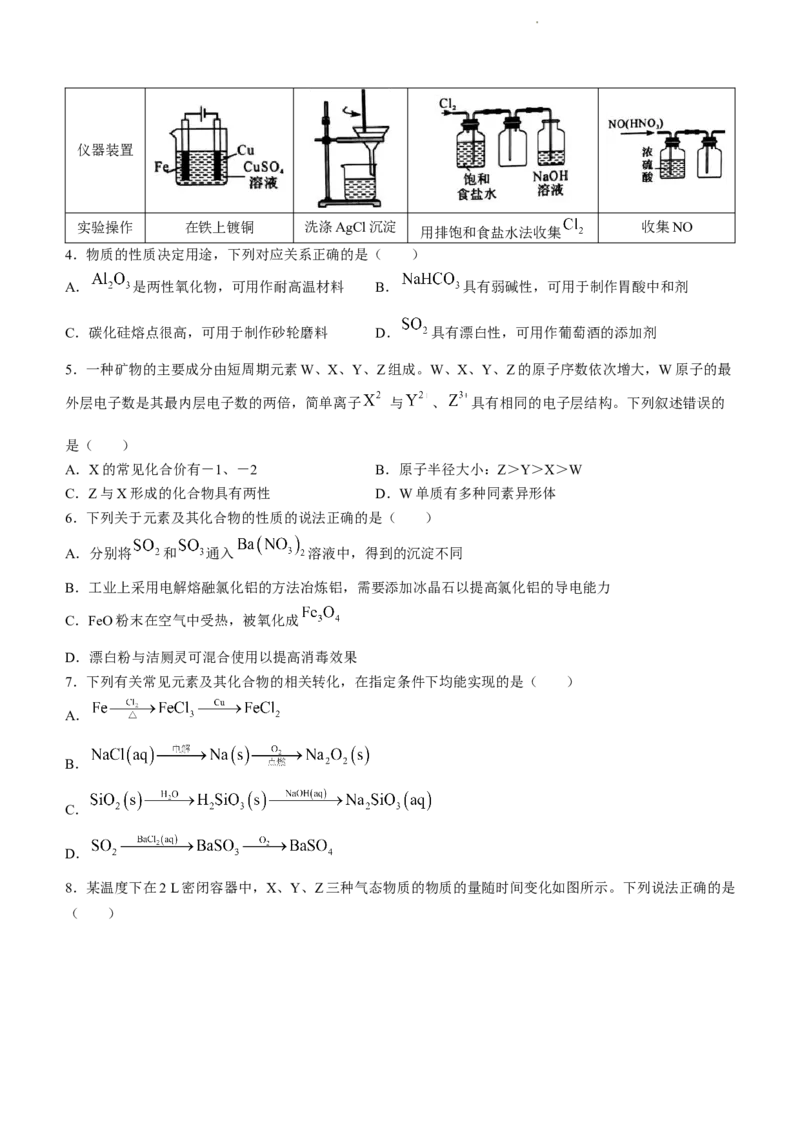
3.下列装置可以用于相应实验的是( )
选项 A B C D
学科网(北京)股份有限公司仪器装置
实验操作 在铁上镀铜 洗涤AgCl沉淀 收集NO
用排饱和食盐水法收集
4.物质的性质决定用途,下列对应关系正确的是( )
A. 是两性氧化物,可用作耐高温材料 B. 具有弱碱性,可用于制作胃酸中和剂
C.碳化硅熔点很高,可用于制作砂轮磨料 D. 具有漂白性,可用作葡萄酒的添加剂
5.一种矿物的主要成分由短周期元素W、X、Y、Z组成。W、X、Y、Z的原子序数依次增大,W原子的最
外层电子数是其最内层电子数的两倍,简单离子 与 、 具有相同的电子层结构。下列叙述错误的
是( )
A.X的常见化合价有-1、-2 B.原子半径大小:Z>Y>X>W
C.Z与X形成的化合物具有两性 D.W单质有多种同素异形体
6.下列关于元素及其化合物的性质的说法正确的是( )
A.分别将 和 通入 溶液中,得到的沉淀不同
B.工业上采用电解熔融氯化铝的方法冶炼铝,需要添加冰晶石以提高氯化铝的导电能力
C.FeO粉末在空气中受热,被氧化成
D.漂白粉与洁厕灵可混合使用以提高消毒效果
7.下列有关常见元素及其化合物的相关转化,在指定条件下均能实现的是( )
A.
B.
C.
D.
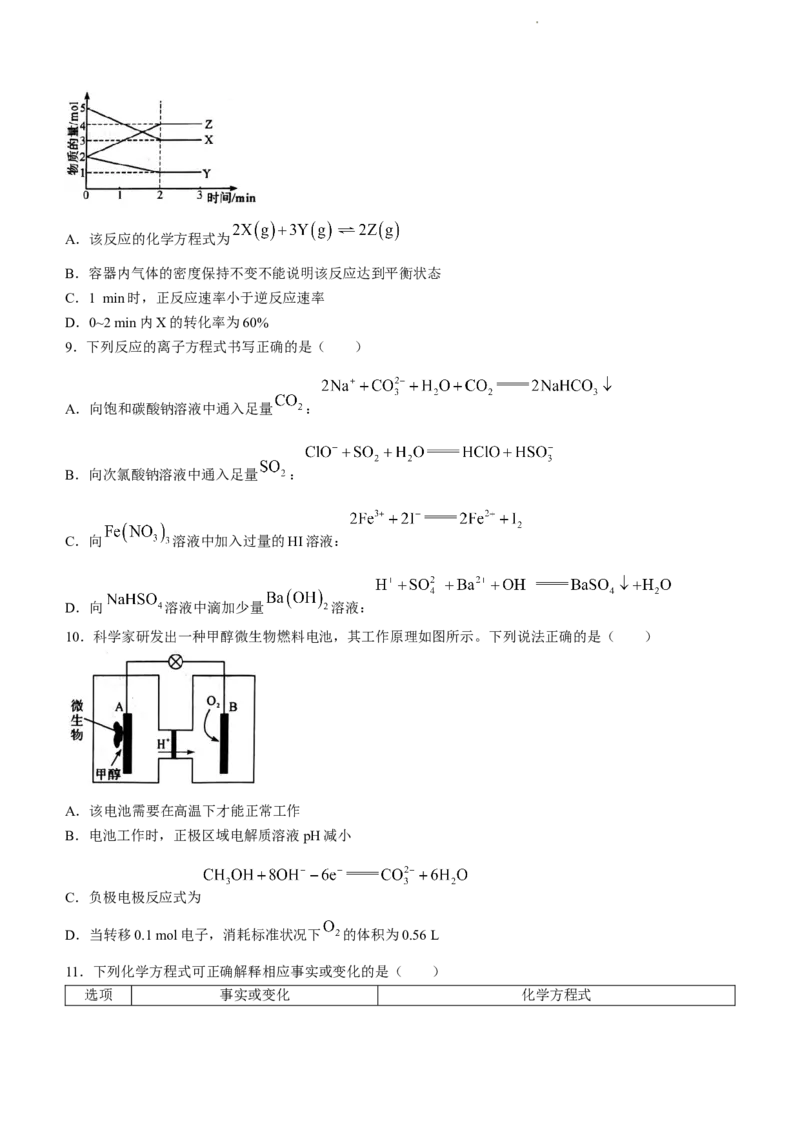
8.某温度下在2 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化如图所示。下列说法正确的是
( )
学科网(北京)股份有限公司A.该反应的化学方程式为
B.容器内气体的密度保持不变不能说明该反应达到平衡状态
C.1 min时,正反应速率小于逆反应速率
D.0~2 min内X的转化率为60%
9.下列反应的离子方程式书写正确的是( )
A.向饱和碳酸钠溶液中通入足量 :
B.向次氯酸钠溶液中通入足量 :
C.向 溶液中加入过量的HI溶液:
D.向 溶液中滴加少量 溶液:
10.科学家研发出一种甲醇微生物燃料电池,其工作原理如图所示。下列说法正确的是( )
A.该电池需要在高温下才能正常工作
B.电池工作时,正极区域电解质溶液pH减小
C.负极电极反应式为
D.当转移0.1 mol电子,消耗标准状况下 的体积为0.56 L
11.下列化学方程式可正确解释相应事实或变化的是( )
选项 事实或变化 化学方程式
学科网(北京)股份有限公司A 将稀硫酸滴入 溶液中产生淡
黄色沉淀
B 浓硝酸保存于棕色试剂瓶中
C 雷雨天气空气中的氮气和氧气反应
D
工业上用足量氨水吸收
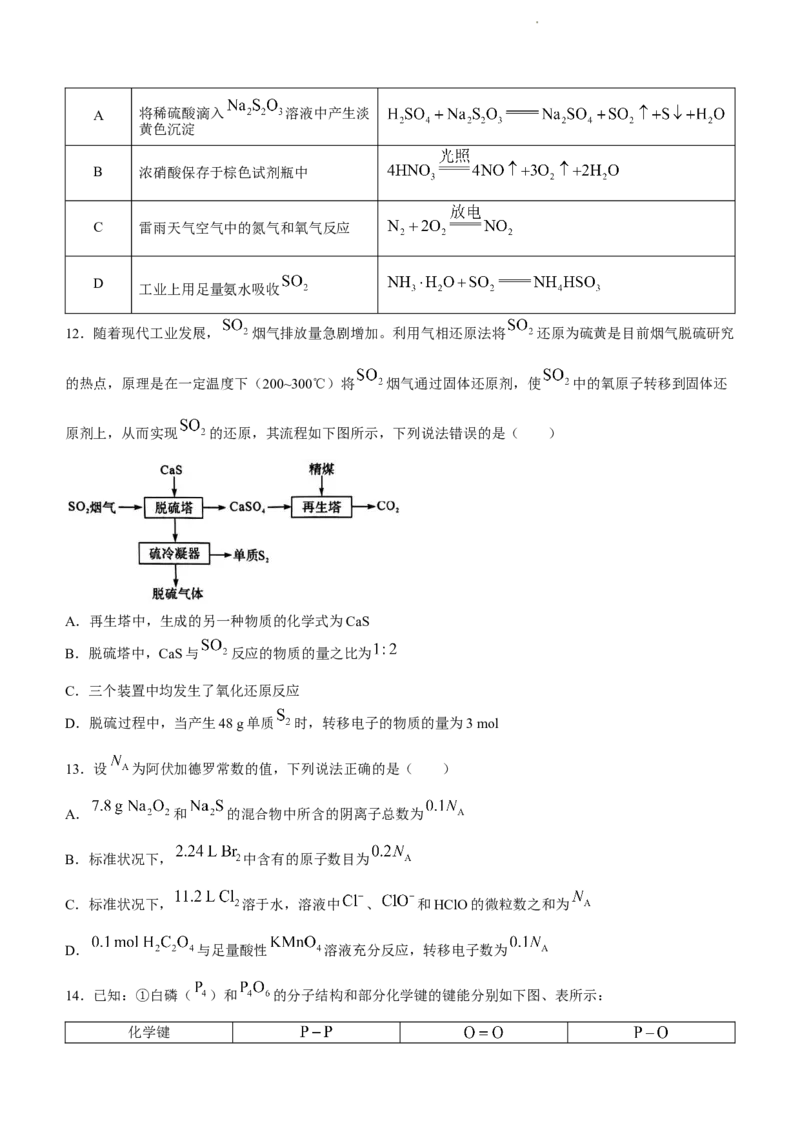
12.随着现代工业发展, 烟气排放量急剧增加。利用气相还原法将 还原为硫黄是目前烟气脱硫研究
的热点,原理是在一定温度下(200~300℃)将 烟气通过固体还原剂,使 中的氧原子转移到固体还
原剂上,从而实现 的还原,其流程如下图所示,下列说法错误的是( )
A.再生塔中,生成的另一种物质的化学式为CaS
B.脱硫塔中,CaS与 反应的物质的量之比为
C.三个装置中均发生了氧化还原反应
D.脱硫过程中,当产生48 g单质 时,转移电子的物质的量为3 mol
13.设 为阿伏加德罗常数的值,下列说法正确的是( )
A. 和 的混合物中所含的阴离子总数为
B.标准状况下, 中含有的原子数目为
C.标准状况下, 溶于水,溶液中 、 和HClO的微粒数之和为
D. 与足量酸性 溶液充分反应,转移电子数为
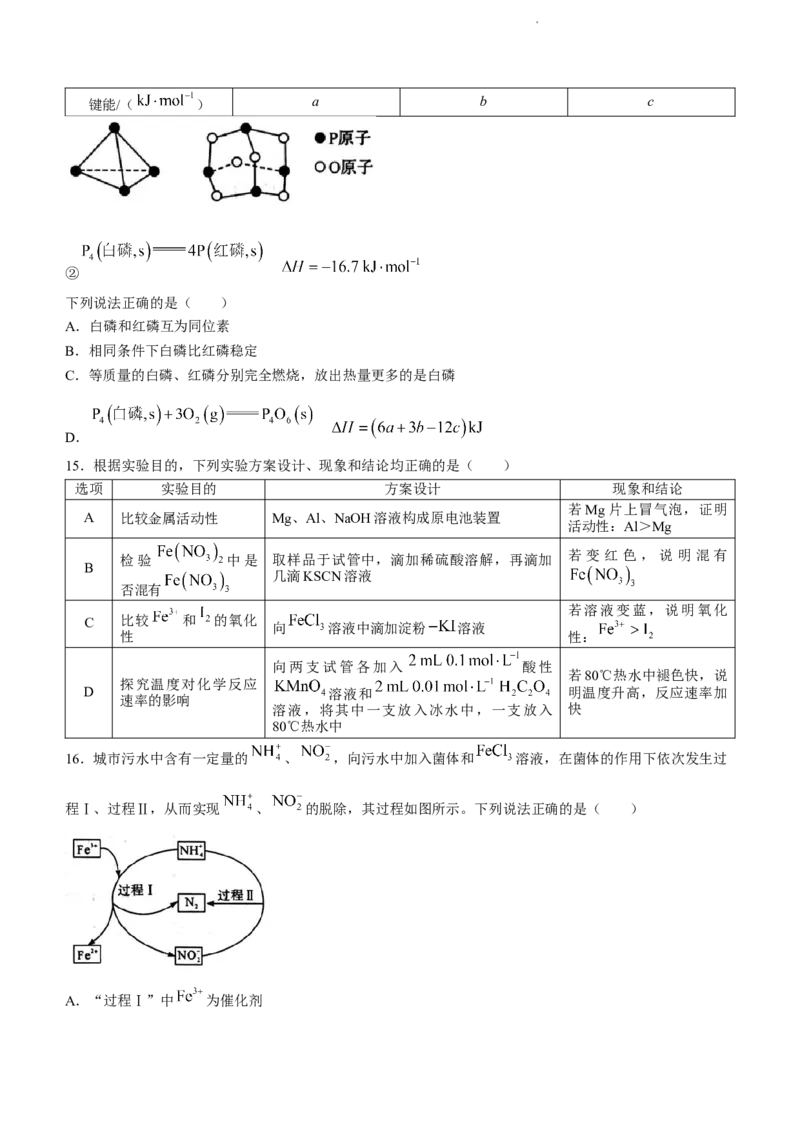
14.已知:①白磷( )和 的分子结构和部分化学键的键能分别如下图、表所示:
化学键
学科网(北京)股份有限公司键能/( ) a b c
②
下列说法正确的是( )
A.白磷和红磷互为同位素
B.相同条件下白磷比红磷稳定
C.等质量的白磷、红磷分别完全燃烧,放出热量更多的是白磷
D.
15.根据实验目的,下列实验方案设计、现象和结论均正确的是( )
选项 实验目的 方案设计 现象和结论
若Mg片上冒气泡,证明
A 比较金属活动性 Mg、Al、NaOH溶液构成原电池装置
活动性:Al>Mg
若 变 红 色 , 说 明 混 有
检验 中是 取样品于试管中,滴加稀硫酸溶解,再滴加
B
几滴KSCN溶液
否混有
若溶液变蓝,说明氧化
C 比较 和 的氧化
向 溶液中滴加淀粉 溶液
性 性:
向两支试管各加入 酸性
若80℃热水中褪色快,说
探究温度对化学反应
D 溶液和 明温度升高,反应速率加
速率的影响
溶液,将其中一支放入冰水中,一支放入 快
80℃热水中
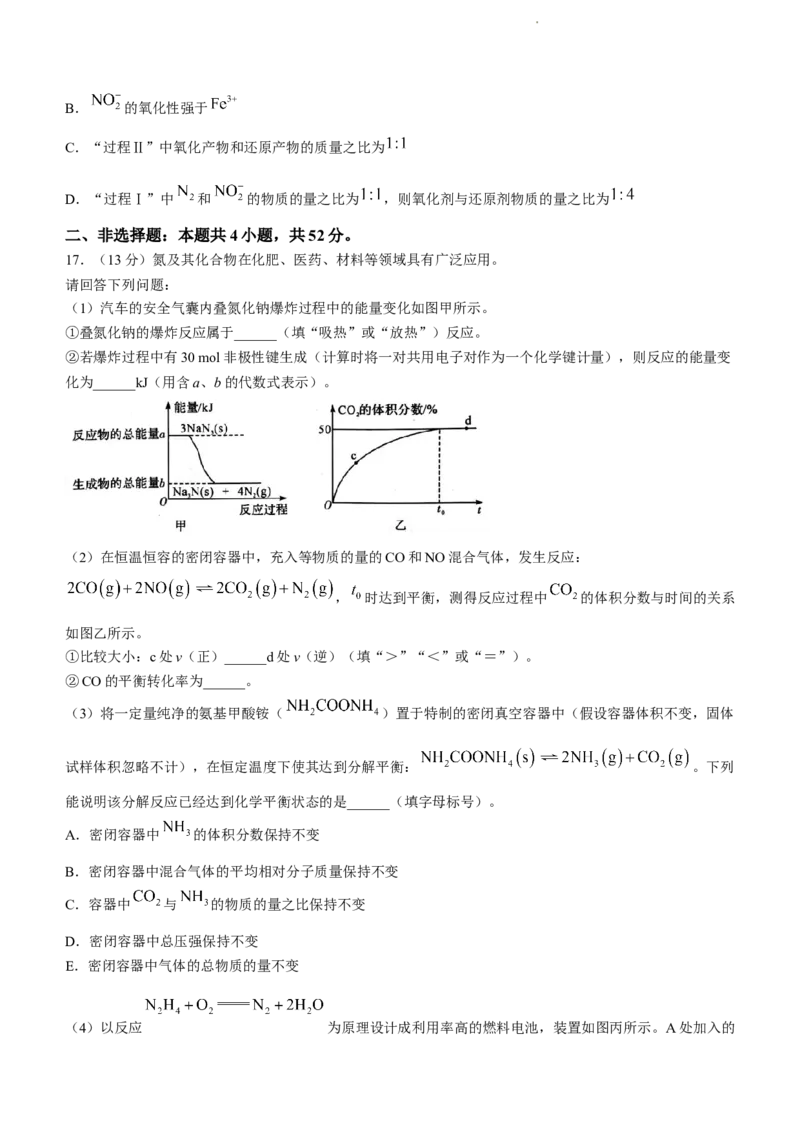
16.城市污水中含有一定量的 、 ,向污水中加入菌体和 溶液,在菌体的作用下依次发生过
程Ⅰ、过程Ⅱ,从而实现 、 的脱除,其过程如图所示。下列说法正确的是( )
A.“过程Ⅰ”中 为催化剂
学科网(北京)股份有限公司B. 的氧化性强于
C.“过程Ⅱ”中氧化产物和还原产物的质量之比为
D.“过程Ⅰ”中 和 的物质的量之比为 ,则氧化剂与还原剂物质的量之比为
二、非选择题:本题共4小题,共52分。
17.(13分)氮及其化合物在化肥、医药、材料等领域具有广泛应用。
请回答下列问题:
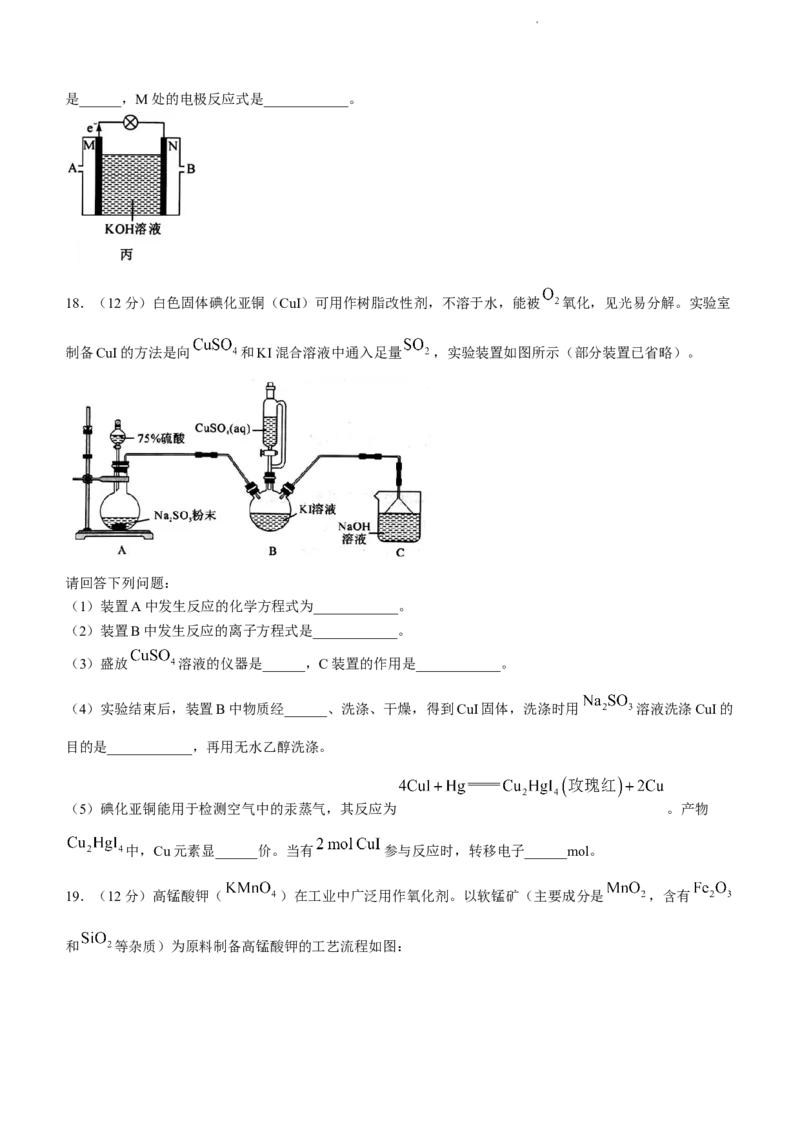
(1)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示。
①叠氮化钠的爆炸反应属于______(填“吸热”或“放热”)反应。
②若爆炸过程中有30 mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应的能量变
化为______kJ(用含a、b的代数式表示)。
(2)在恒温恒容的密闭容器中,充入等物质的量的CO和NO混合气体,发生反应:
, 时达到平衡,测得反应过程中 的体积分数与时间的关系
如图乙所示。
①比较大小:c处v(正)______d处v(逆)(填“>”“<”或“=”)。
②CO的平衡转化率为______。
(3)将一定量纯净的氨基甲酸铵( )置于特制的密闭真空容器中(假设容器体积不变,固体
试样体积忽略不计),在恒定温度下使其达到分解平衡: 。下列
能说明该分解反应已经达到化学平衡状态的是______(填字母标号)。
A.密闭容器中 的体积分数保持不变
B.密闭容器中混合气体的平均相对分子质量保持不变
C.容器中 与 的物质的量之比保持不变
D.密闭容器中总压强保持不变
E.密闭容器中气体的总物质的量不变
(4)以反应 为原理设计成利用率高的燃料电池,装置如图丙所示。A处加入的
学科网(北京)股份有限公司是______,M处的电极反应式是____________。
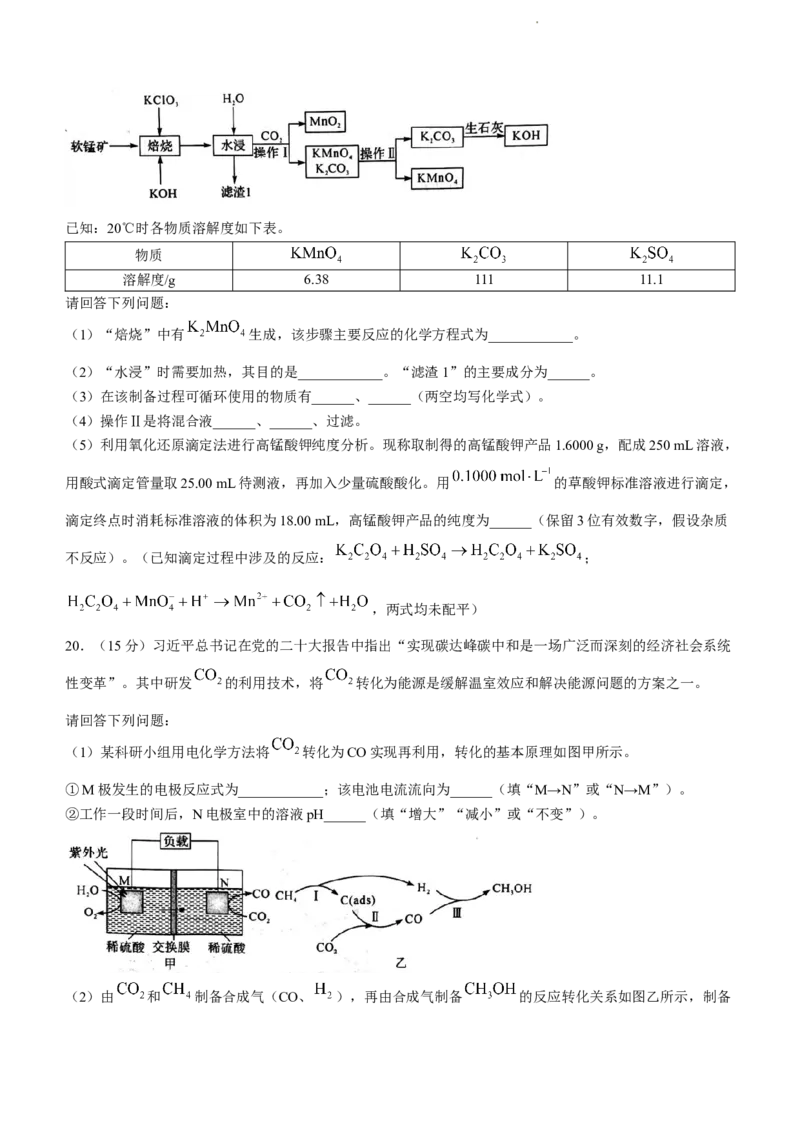
18.(12分)白色固体碘化亚铜(CuI)可用作树脂改性剂,不溶于水,能被 氧化,见光易分解。实验室
制备CuI的方法是向 和KI混合溶液中通入足量 ,实验装置如图所示(部分装置已省略)。
请回答下列问题:
(1)装置A中发生反应的化学方程式为____________。
(2)装置B中发生反应的离子方程式是____________。
(3)盛放 溶液的仪器是______,C装置的作用是____________。
(4)实验结束后,装置B中物质经______、洗涤、干燥,得到CuI固体,洗涤时用 溶液洗涤CuI的
目的是____________,再用无水乙醇洗涤。
(5)碘化亚铜能用于检测空气中的汞蒸气,其反应为 。产物
中,Cu元素显______价。当有 参与反应时,转移电子______mol。
19.(12分)高锰酸钾( )在工业中广泛用作氧化剂。以软锰矿(主要成分是 ,含有
和 等杂质)为原料制备高锰酸钾的工艺流程如图:
学科网(北京)股份有限公司已知:20℃时各物质溶解度如下表。
物质
溶解度/g 6.38 111 11.1
请回答下列问题:
(1)“焙烧”中有 生成,该步骤主要反应的化学方程式为____________。
(2)“水浸”时需要加热,其目的是____________。“滤渣1”的主要成分为______。
(3)在该制备过程可循环使用的物质有______、______(两空均写化学式)。
(4)操作Ⅱ是将混合液______、______、过滤。
(5)利用氧化还原滴定法进行高锰酸钾纯度分析。现称取制得的高锰酸钾产品1.6000 g,配成250 mL溶液,
用酸式滴定管量取25.00 mL待测液,再加入少量硫酸酸化。用 的草酸钾标准溶液进行滴定,
滴定终点时消耗标准溶液的体积为18.00 mL,高锰酸钾产品的纯度为______(保留3位有效数字,假设杂质
不反应)。(已知滴定过程中涉及的反应: ;
,两式均未配平)
20.(15分)习近平总书记在党的二十大报告中指出“实现碳达峰碳中和是一场广泛而深刻的经济社会系统
性变革”。其中研发 的利用技术,将 转化为能源是缓解温室效应和解决能源问题的方案之一。
请回答下列问题:
(1)某科研小组用电化学方法将 转化为CO实现再利用,转化的基本原理如图甲所示。
①M极发生的电极反应式为____________;该电池电流流向为______(填“M→N”或“N→M”)。
②工作一段时间后,N电极室中的溶液pH______(填“增大”“减小”或“不变”)。
(2)由 和 制备合成气(CO、 ),再由合成气制备 的反应转化关系如图乙所示,制备
学科网(北京)股份有限公司合成气的反应中,若生成 ,反应Ⅰ和Ⅱ中共转移电子的物质的量为______。
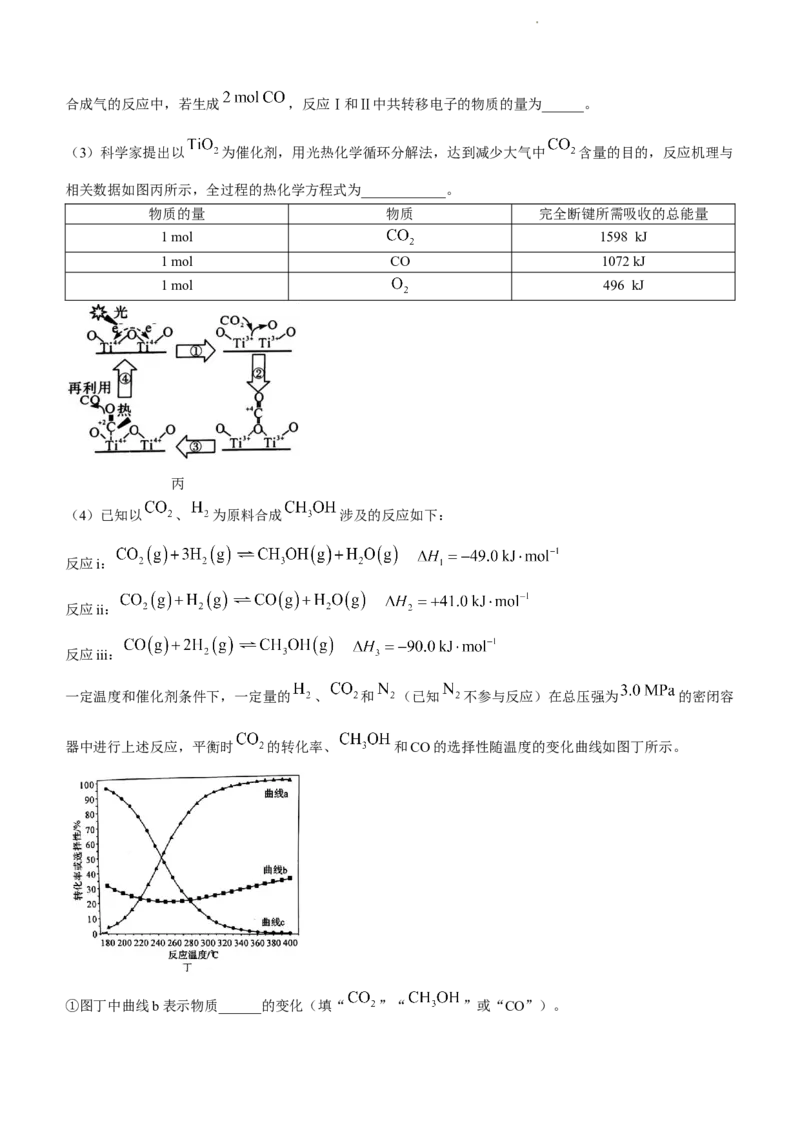
(3)科学家提出以 为催化剂,用光热化学循环分解法,达到减少大气中 含量的目的,反应机理与
相关数据如图丙所示,全过程的热化学方程式为____________。
物质的量 物质 完全断键所需吸收的总能量
1 mol 1598 kJ
1 mol CO 1072 kJ
1 mol 496 kJ
丙
(4)已知以 、 为原料合成 涉及的反应如下:
反应i:
反应ii:
反应iii:
一定温度和催化剂条件下,一定量的 、 和 (已知 不参与反应)在总压强为 的密闭容
器中进行上述反应,平衡时 的转化率、 和CO的选择性随温度的变化曲线如图丁所示。
①图丁中曲线b表示物质______的变化(填“ ”“ ”或“CO”)。
学科网(北京)股份有限公司②某温度下, 反应到达平衡,测得容器中 的体积分数为12.5%。此时用 的分压表示
内的反应速率 ______ 。
湘豫名校联考
2023 年 9 月高三一轮复习诊断考试(一)
化学参考答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
答案 D C C B B C A B A D A C A C C C
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.D 【命题意图】本题考查了中国古代文化以及氧化还原反应。命题意图是增强爱国主义情怀以及对双基
的掌握。
【解析】依据实验现象可判断该方法应用了焰色试验,属于物理变化,A错误;结冰过程只有状态变化,属
于物理变化,B错误;石穴中水,所滴皆为钟乳,涉及的反应为碳酸钙分解生成碳酸钙,没有元素化合价的
变化,不是氧化还原反应,C错误;火药爆炸发生反应 ,存在
元素化合价的变化,属于氧化还原反应,D正确。
2.C 【命题意图】本题考查了化学用语。命题意图是考查宏观辨识与微观探析的核心素养。
【解析】醋酸属于弱酸,其电离方程式为 ,A错误; 为
丙酸甲酯的结构简式,乙酸和乙醇发生酯化反应生成乙酸乙酯,其结构简式为 ,B错误;
P为15号元素,核外电子层上电子数分别为2、8、5,C正确;臭氧为V形结构,该球棍模型与其结构不符,
D错误。
3.C 【命题意图】本题考查了实验装置和基本实验操作。命题意图是考查实验操作能力以及图象的识别能
力。
【解析】图示装置中Fe为阳极,阳极电极反应为 ,Cu为阴极,阴极电极反应为
,不能在铁上镀铜,铁上镀铜应用Cu作阳极、Fe为阴极,A错误;洗涤沉淀时,不能
学科网(北京)股份有限公司搅拌,易捣破滤纸,应使水自然流下,重复2~3次,B错误; 在饱和食盐水中的溶解度很低,可以用排
饱和食盐水法收集 ,C正确;NO易被空气氧化成 ,不能用排空气法收集NO,D错误。
4.B 【命题意图】本题考查了物质的性质与用途。命题意图是考查分析问题和解决问题的能力。
【解析】 用作耐高温材料,是因为它的熔点高,与其两性无关,A错误;胃酸的主要成分是HCl,
具有弱碱性,能中和酸,B正确;碳化硅是共价晶体,用于制作砂轮磨料利用了其硬度大、耐磨的
性质,与熔点高不存在对应关系,C错误; 用作葡萄酒的食品添加剂是因为 的还原性,能起到杀菌
消毒,延缓葡萄酒氧化变质的作用,D错误。
5.B 【命题意图】本题考查了元素推断及元素周期律。命题意图是考查推理能力。
【解析】短周期简单离子 与 、 具有相同的电子层结构,则它们均为10电子微粒,X为O,Y为
Mg,Z为Al,W原子最外层电子数是其最内层电子数的两倍,则W为C。X为O,氧的常见价态有-1价和
-2价,如 和 ,A正确;W为C,X为O,Y为Mg,同主族元素电子层数越多,原子半径越大,
电子层数相同时,原子序数越小,原子半径越大,所以原子半径大小:Y>Z>W>X,B错误;Z为Al,X
为O,它们可形成 ,为两性氧化物,C正确;W为C,碳的同素异形体有:金刚石、石墨、石墨烯、
富勒烯、碳纳米管等,D正确。
6.C 【命题意图】本题考查了元素化合物的知识,命题意图是考查分析问题和解决问题的能力。
【解析】分别将 和 通入 溶液中,溶液呈酸性,硝酸根离子在酸性条件下具有强氧化性,
则生成的沉淀均为 ,A错误;氯化铝为共价化合物,熔融状态下不导电,工业上常电解熔融的氧化铝,
需要添加冰晶石作助熔剂,B错误;FeO不稳定,其粉末在空气中受热,易被氧化生成稳定的 ,C正
确;漂白粉的有效成分 和洁厕灵的主要成分盐酸反应生成有毒的氯气,可能会造成意外事故,所
以漂白粉与洁厕灵不能混合使用,D错误。
7.A 【命题意图】本题考查了元素及其化合物的相互转化。命题意图是考查模型认知和变化观念的核心素
养。
【解析】铁与氯气加热可生成氯化铁,氯化铁溶液和铜会发生氧化还原反应生成氯化亚铁和氯化铜,均能实
现相关转化,A正确;电解 生成氢氧化钠、氢气和氯气,钠在氧气中燃烧生成过氧化钠,B错误;
不溶于水,不能生成 ,硅酸与 生成 ,C错误;亚硫酸的酸性
学科网(北京)股份有限公司弱于盐酸,二氧化硫和氯化钡溶液不反应,D错误。
8.B 【命题意图】本题考查了化学平衡相关计算。命题意图是考查变化观念与平衡思想的核心素养。
【解析】从图中可以看出,随着反应的不断进行,X、Y的物质的量不断减小,Z的物质的量不断增大,则
X、Y为反应物,Z为生成物,最终反应物都有剩余,则反应可逆;依据2 min内的物质的量变化,可确定
X、Y、Z的化学计量数之比为 ,所以该反应的化学方程式是 ,A错误;因
为该反应是反应前后为纯气体的反应,所以容器内气体的总质量保持不变,容器容积不变,则密度不变,所
以密度不变不能说明反应达平衡状态,B正确;1 min时,反应向生成Z的方向进行,则正反应速率大于逆
反应速率,C错误;0~2 min内X的转化率为 ,D错误。
9.A 【命题意图】本题考查了离子方程式的书写。命题意图是考查模型认知的核心素养。
【解析】碳酸钠易溶于水,碳酸氢钠微溶于水,向饱和碳酸钠溶液中通入足量 气体会有碳酸氢钠晶体析
出,离子方程式为 ,A正确;次氯酸钠具有强氧化性,二氧
化硫具有还原性,两者会发生氧化还原反应: ,B错误;由于还
原剂 过量,则 、 完全和 反应生成 、NO和 :
,C错误;向 溶液中滴加少量
溶液,离子方程式为 ,D错误。
10.D 【命题意图】本题考查了化学电源。命题意图是考查证据推理与模型认知的核心素养。
【解析】微生物高温下会失去生理活性,电池不能正常工作,A错误;A为负极,B为正极,正极电极反应
式为 ,生成 ,酸性减弱,pH增大,B错误;电解质溶液显酸性,则负极电
极反应式为 ,C错误;当转移0.1 mol电子,消耗 的物质的量为
0.025 mol,标准状况下体积为0.56 L,D正确。
11.A 【命题意图】本题考查了化学方程式的书写。命题意图是考查变化观念的核心素养。
学科网(北京)股份有限公司【解析】 与硫酸反应生成 和S单质,A正确;浓硝酸保存于棕色试剂瓶中是因为浓硝酸遇光分
解生成二氧化氮、氧气和水,反应的化学方程式为 ,B错误;雷
雨天气空气中的氮气和氧气反应生成NO: ,C错误;氨水足量生成正盐,反应式为
,D错误。
12.C 【命题意图】本题考查了硫及其化合物的转化。命题意图是考查模型认知的核心素养。
【解析】在再生塔中精煤与 反应生成 ,C被氧化成 ,根据元素价态变化规律可知 被
还原成CaS,A正确;在脱硫塔中CaS与 反应生成 和 ,根据原子守恒,脱硫塔中发生反应的
化学方程式为 ,B正确;“硫冷凝器”中为气态硫单质被冷凝为固态硫
单质,为物理变化,C错误;CaS中S元素的化合价由-2价升高至0价, 中S元素的化合价部分由+4
价升高至+6价、部分由+4价降低至0价,生成 转移4 mol电子,当产生48 g单质 时转移电子的
物质的量为 ,D正确。
13.A 【命题意图】本题考查了阿伏加德罗常数的计算。命题意图是考查宏观识与微观探析的核心素养。
【解析】1个过氧化钠分子是由2个钠离子和1个过氧根离子构成的、1个硫化钠分子是由2个钠离子和1个
硫离子构成的,1分子中均含有1个阴离子,且两者的相对分子质量均为78,则 和 混合物
可看作 ,且物质的量为0.1 mol,其所含的阴离子总数为 ,A正确;标准状况下, 不是气态,
不能用标准状况下气体摩尔体积计算,B错误;标准状况下 的物质的量为 ,
氯气与水反应是可逆反应,不能完全反应,所以溶液中 、 和HClO的微粒数之和小于 ,C错误;
学科网(北京)股份有限公司与足量酸性 溶液充分反应后变为 气体, 中C元素的化合价由+3价变为+4
价,即 充分反应转移2 mol电子,则 与足量酸性 溶液充分反应,转
移电子数为 ,D错误。
14.C 【命题意图】本题考查了反应热的计算。命题意图是考查宏观辨识与微观探析的核心素养。
【解析】白磷和红磷互为同素异形体,A错误; ,属
于放热反应,生成物比反应物稳定,则比较稳定的是红磷,B错误;等质量的白磷、红磷分别完全燃烧,因
为白磷的能量比红磷高,而产物及状态均相同,则白磷燃烧放出的热量更高,所以放出热量更多的是白磷,
C正确; ,单位错误,D错误。
15.C 【命题意图】本题考查实验探究与设计。命题意图是考查实验设计能力和动手能力。
【解析】判断金属的活动性是与酸或水反应的剧烈程度来判断,不是与碱反应,A错误;检验 中
是否混有 ,若滴加稀硫酸溶解,则 和 构成强氧化性溶液会将 氧化为 ,再滴加
几滴KSCN溶液肯定变红,B错误;向 溶液中滴加淀粉 溶液,发生反应
,淀粉遇 变蓝,说明氧化性: ,C正确;高锰酸钾过量,两支试管
均不会褪色,D错误。
16.C 【命题意图】本题考查了氧化还原反应的相关知识。命题意图是考查图象分析能力和化学计算能力。
【解析】 为氧化剂,被还原为 ,A错误;“过程Ⅰ”中, 为氧化剂, 为氧化产物,则
的氧化性强于 ,B错误;“过程Ⅱ”中的反应为 ,氧化产物和还
原产物均为 ,质量之比为 ,C正确;当 和 的物质的量之比为 时,“过程Ⅰ”的反应为
,氧化剂与还原剂的物质的量之比为 ,D错
误。
二、非选择题:本题共4小题,共52分。
学科网(北京)股份有限公司17.(13分)【答案】(1)①放热(1分) ② 或 (2分)
(2)①>(2分) ②80%(2分) (3)DE(2分,少答得1分,答错得0分)
(4) (2分) (2分)
【命题意图】本题考查了化学反应速率与化学平衡、反应能量变化的计算、燃料电池等知识。命题意图是培
养证据推理与模型认知的核心素养。
【解析】(1)①根据图甲,叠氮化钠爆炸,生成物的总能量降低,反应属于放热反应;②根据图甲,
反应生成 和 ,放出 能量,氮分子中有3个非极性共价键,若爆
炸过程中有30 mol非极性键生成(一对共用电子对作为一个化学键),说明生成10 mol氮气,则反应的能量
变化为 。
(2)①由题图乙可知,随反应进行,反应物浓度降低,正反应速率减慢,c处v(正)>d处v(正);d处
反应达到平衡,d处v(正)=d处v(逆),所以c处v(正)>d处v(逆)。
②设充入CO和NO的物质的量均为 ,平衡时生成 的物质的量为 ,则有
初始量(mol) n n 0 0
转化量(mol) 2x 2x 2x x
平衡量(mol) 2x x
, ,CO的平衡转化率为 。
(3)反应物是固体且体积忽略不计,则容器中氨气和二氧化碳物质的量之比为 ,密闭容器中氨气体积分
数不变,A不符合题意;混合气体为 和 ,无论反应如何进行,气体物质的量之比始终为 ,则混
合气体的平均相对分子质量为定值,当平均相对分子质量不变时,不能判断反应已经达到平衡状态,B不符
合题意;容器中二氧化碳与氨气的物质的量按照系数比生成,比例始终不变,不能判断反应已经达到平衡状
态,C不符合题意;反应为气体体积增大的反应,容器内总压强不变,反应达到平衡,D符合题意;反应前
后物质的量不等,故当容器内气体的总物质的量不变,达到平衡,E符合题意。
(4)由题图丙电子的流向可知,M电极为负极,在燃料电池中通入燃料的一极为负极,即A处加入的是
,M电极为负极,发生氧化反应,故M处的电极反应式为 。
学科网(北京)股份有限公司18.(12分)【答案】(1) (2分)
(2) (2分)
(3)恒压分(滴)液漏斗(1分) 吸收尾气(1分)
(4)过滤(1分) 防止CuI被 氧化同时可以除去吸附的 (2分)
(5)+1(1分) 1(2分)
【命题意图】本题考查了物质的制备实验以及氧化还原反应的计算。命题意图是培养科学探究与创新意识的
学科核心素养。
【解析】(1)装置A中发生反应的化学方程式为 。
(2)在装置B中 、 、KI发生氧化还原反应制取CuI,根据得失电子守恒、电荷守恒、原子守恒,
结合物质的拆分原则,可知该反应的离子方程式为 。
(3)盛放 溶液的仪器是恒压分液漏斗,C装置的作用是吸收尾气。
(4)产物CuI为难溶物,经过滤、洗涤除杂即可。选择 溶液洗涤防止CuI被氧化同时可以除去吸附
的 。
(5)根据化合物中各元素正负化合价代数和为零的原则可知,在 中,设铜元素的化合价为x,则
,得 ;反应 中,Cu元素化合价
部分由+1价降低到0价,被还原,CuI为氧化剂,Hg元素化合价由0价升高到+2价,Hg为还原剂,当有
参与反应时,只有 元素的化合价发生变化,转移1 mol电子。
19.(12分)【答案】(1) (2分)
(2)加快水浸的速率(2分) (1分)
(3) (1分) KOH(1分)(两空顺序可以颠倒)
学科网(北京)股份有限公司(4)蒸发浓缩(1分) 冷却结晶(1分) (5)71.1%或0.711(3分)
【命题意图】本题考查了工艺流程以及化学实验。考查证据推理与模型认知的核心素养。
【解析】软锰矿(主要成分是 ,含有 和 等杂质),加入 和KOH,焙烧将
氧化为 ,反应的化学方程式为 ,
不反应, 生成 ,水浸后得到 、 溶液,滤渣为 ,向滤液中通入适量的
, 发生歧化反应: , 生成
沉淀,过滤,滤渣为 和 ,将滤液结晶即可得到 。
(1)软锰矿(主要成分是 ,含有 和 等杂质),加入 和KOH,焙烧将 氧化
为 ,反应的化学方程式为 。
(2)“水浸”时需要加热,可以加快水浸的速率;滤渣为不与碱反应的 。
(3)分析题述工艺流程,在该制备过程可以循环使用的物质有 和KOH。
(4)从题表中数据可知,20℃时 和 的溶解度差别较大,可用重结晶方法分离它们,所以操
作Ⅱ是将混合液蒸发浓缩、冷却结晶。
(5)根据滴定发生反应的关系式 可得
,则高锰酸钾产品的纯
度为 。
20.(15分)【答案】(1)① (2分) N→M(1分)
②增大(2分) (2)6 mol(2分,不带单位扣1分)
学科网(北京)股份有限公司(3) (3分,或写
)
(4)① (2分) ② (3分)
【命题意图】本题考查了化学反应原理及其化合物知识。命题意图是培养证据推理、科学态度与社会责任的
核心素养。
【解析】(1)①由题图甲可知,M极发生氧化反应生成氧气,为负极;N极发生还原反应生成CO,为正极,
电流从正极流向负极,M极发生氧化反应生成氧气: 。②N极二氧化碳得到
电子发生还原反应生成CO,电极反应式为 ,生成 ,酸性减弱,pH
增大。
(2)反应Ⅱ: ,生成 需消耗 ,反应中转移电子数2 mol;反应Ⅰ:
,生成 转移4 mol电子,若生成 ,两反应总共转移电子数6 mol。
(3) 分解为CO和 ,化学方程式为 ,根据分子化学键完全断裂时的能量变化
图可知, 完全断裂吸收1598 kJ能量, 完全断裂吸收1072 kJ能量, 完全断裂
应该吸收496 kJ能量;所以 分解产生 和 ,需吸收
能量,则全过程的热化学方程式为
。
(4)反应ii为吸热反应,升温CO的选择性升高,该反应中 的转化率升高,CO的曲线为a。而反应i为
学科网(北京)股份有限公司放热反应,升高温度平衡逆向,反应中 的转化率降低, 的选择性降低, 的曲线为c。
两反应综合效应, 的转化率曲线为b。②某温度下,在总压强为 的密闭容器中进行上述反应,
反应到达平衡,测得容器中 的体积分数为12.5%,
,
。
学科网(北京)股份有限公司