文档内容
沈丘县长安高中 2024 届高三年级第一次月考化学试题
一、单选题(每题3分,共 48分)
1.2015 年8月12 日天津港国际物流中心内某公司的危险品仓库发生严重火灾,
涉及的危险品包括压缩液化气体、电石和过氧化物等。以下灭火方法正确的是
A.使用大量水 B.使用泡沫式灭火器
C.使用黄沙 D.使用干粉(NaHCO )
3
2.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=1 的无色溶液中:Na+、Cu2+、Cl-、CO 2-
3
B.使酚酞呈红色的溶液中:K+、Na+、NO -、Cl-
3
C.0.1mol·L-1的FeCl 溶液中:H+、Al3+、SO 2-、ClO-
2 4
D.由水电离出的c(H+)=1×10-10mol·L-1的溶液中:Mg2+、NH +、SO 2-、
4 4
HCO -
3
3.下列方程式正确的是
A.Fe (SO ) 溶液和足量Zn充分反应:2Fe3++Zn═2Fe2++Zn2+
2 4 3
B.NaClO溶液与FeCl 溶液混合:Fe2++2ClO-+2H O═Fe(OH) ↓+2HClO
2 2 2
C.氢氧化铁与 HI溶液反应的离子方程式为Fe(OH) +3H+═Fe3++3H O
3 2
D.氧化铁溶于稀硝酸的离子方程式为Fe O +6H+═2Fe3++3H O
2 3 2
4.虎年春晚,一段舞蹈诗剧《只此青绿》惊艳了观众。舞者生动的还原了北宋
名画《千里江山图》,《千里江山图》历经千年,依旧色彩艳丽,璀璨夺目。下列
有关《千里江山图》所用的颜料说法正确的是
A.石绿(孔雀石),主要成份为碱式碳酸铜
B.赭石是氧化物类刚玉族赤铁矿,也是“车中幸有司南柄,试与迷途指大方”
中“司南柄”的主要成分
C.《千里江山图》历经千年依然色彩艳丽,璀璨夺目,是由于所用颜料化学
性质稳定,耐酸耐碱
D.颜料中所用的朱砂是碱性氧化物
5.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.分子数为N 的CO和C H 混合气体的体积约为22.4L
A 2 4
B.标准状况下,4.48L 重水(D O)中含有的中子数为2N
2 A
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}C.用 MnO 与浓盐酸制取Cl 时,每生成0.5molCl 则转移电子数为N
2 2 2 A
D.0.1L3.0mol·L-1的NH NO 溶液中含有NH +的数目为0.3N
4 3 4 A
6.利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的 S2,制取石膏
(CaSO 2H O)的过程如下:
4 2
下列说法正确的是
A.SO2的空间结构名称为正四面体 B.过程Ⅰ后溶液pH增大
4
C.过程Ⅱ中反应的离子方程式为2S24MnO210H 4MnOH S O2H O
3 2 2 3 2
D.CaSO 2H O属于混合物
4 2
7.下列有关物质的性质与用途,不具有对应关系的是
A.Na O 为淡黄色固体,可用作潜水艇中的供氧剂
2 2
B.Fe O 为红棕色,可用做红色颜料
2 3
C.Al O 的熔点高,常用作耐火、耐高温材料
2 3
D.NaClO具有强氧化性,常作为杀菌、消毒剂
8.下列物质的转化在给定条件下能实现的是( )
①CO2CO C COFe 2 O 3CO
点燃 2 高温 高温 2
②Fe
点
O
燃
2Fe
2
O
3
H2SO4Fe
2
(SO
4
)
3
③SO
2
氨水NH
4
HSO
3
H2S
O4(aq) (NH
4
)
2
SO
4
④AlCl 电解AlNaOHNaAlO
3 2
⑤CuSO (aq)过量NaOH(aq)Cu(OH) 葡萄糖Cu O
4 2 Δ 2
A.①②③ B.①③⑤ C.②③⑤ D.③④⑤
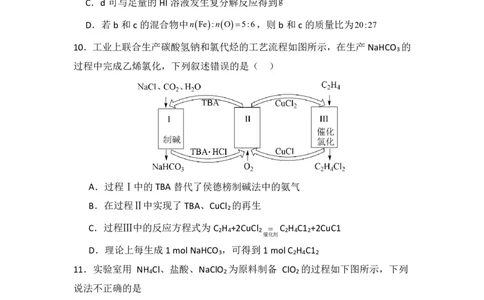
9.价一类二维图和实验是学习元素及其化合物的重要方法。铁及其化合物的价
一类二维图如图所示。下列说法正确的是
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}A.高温时,a 与水蒸气反应转化为c
B.若f、g 都是盐酸盐,则这两种物质均可通过化合反应获得
C.d 可与足量的HI溶液发生复分解反应得到g
D.若b 和c的混合物中nFe:nO5:6,则b 和c的质量比为20:27
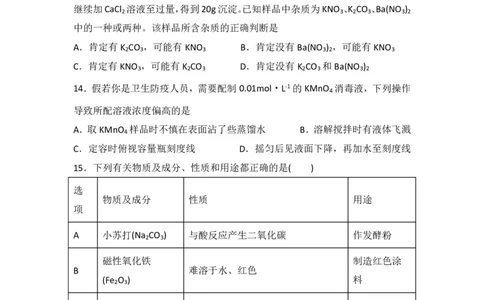
10.工业上联合生产碳酸氢钠和氯代烃的工艺流程如图所示,在生产NaHCO 的
3
过程中完成乙烯氯化,下列叙述错误的是( )
A.过程Ⅰ中的TBA 替代了侯德榜制碱法中的氨气
B.在过程Ⅱ中实现了TBA、CuCl 的再生
2
C.过程Ⅲ中的反应方程式为C H +2CuCl C H C1 +2CuC1
2 4 2 2 4 2
催化剂
D.理论上每生成1molNaHCO ,可得到1molC H C1
3 2 4 2
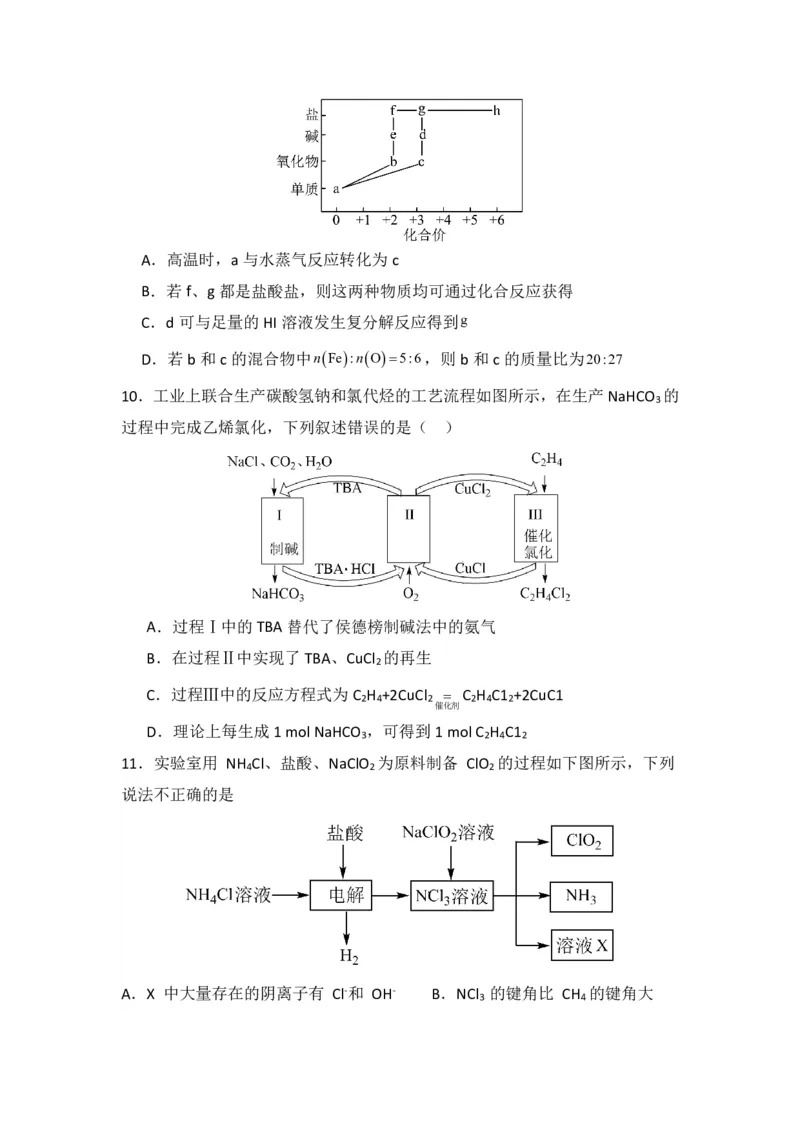
11.实验室用 NH Cl、盐酸、NaClO 为原料制备 ClO 的过程如下图所示,下列
4 2 2
说法不正确的是
A.X 中大量存在的阴离子有 Cl-和 OH- B.NCl 的键角比 CH 的键角大
3 4
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}C.NaClO 变成 ClO 发生了氧化反应 D.制取 3molClO 至少需要 0.5molNH Cl
2 2 2 4
12.下列有关Na CO 和NaHCO 的性质,叙述错误的是
2 3 3
A.鉴别Na CO 和NaHCO 可以用BaCl 溶液,不可用Ba(OH) 溶液
2 3 3 2 2
B.向饱和Na CO 溶液中通入过量CO ,有晶体析出
2 3 2
C.小苏打可以用于泡沫灭火器的反应物质
D.除去NaHCO 溶液并混有的少量Na CO ,用加热法
3 2 3
13.将某Na CO 固体样品21.6g 放入足量水中,固体完全溶解得无色澄清溶液,
2 3
继续加CaCl 溶液至过量,得到20g沉淀。已知样品中杂质为KNO 、K CO 、Ba(NO )
2 3 2 3 3 2
中的一种或两种。该样品所含杂质的正确判断是
A.肯定有K CO ,可能有KNO B.肯定没有Ba(NO ) ,可能有KNO
2 3 3 3 2 3
C.肯定有 KNO ,可能有K CO D.肯定没有K CO 和Ba(NO )
3 2 3 2 3 3 2
14.假若你是卫生防疫人员,需要配制0.01mol‧L-1的KMnO 消毒液,下列操作
4
导致所配溶液浓度偏高的是
A.取KMnO 样品时不慎在表面沾了些蒸馏水 B.溶解搅拌时有液体飞溅
4
C.定容时俯视容量瓶刻度线 D.摇匀后见液面下降,再加水至刻度线
15.下列有关物质及成分、性质和用途都正确的是( )
选
物质及成分 性质 用途
项
A 小苏打(Na CO ) 与酸反应产生二氧化碳 作发酵粉
2 3
磁性氧化铁 制造红色涂
B 难溶于水、红色
(Fe O ) 料
2 3
C 蓝矾(CuSO ·5H O) 蓝色 检验水蒸气
4 2
能和某些有色物质反应生成无色物
D 二氧化硫(SO ) 漂白草织品
2
质
A.A B.B C.C D.D
16.某小组在实验室中用下图所示装置(夹持装置已略去)制取碳酸镧[La (CO ) ],
2 3 3
制备原理为2LaCl +6NH +3CO +3H O=La (CO ) ↓+6NH Cl。下列说法正确的是
3 3 2 2 2 3 3 4
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}A.干燥管的作用是增大反应物间的接触面积
B.试剂X 为饱和Na CO 溶液,试剂Y 为饱和NH Cl 溶液
2 3 4
C.若用稀硫酸代替装置I 中的稀盐酸,则实验时可以不用盛试剂X 的装置
D.实验时一般先通入装置II产生的气体,再通入装置I产生的气体
二、填空题
17.以黄铜矿(CuFeS )为主要原料的炼铜方法有火法炼铜、氧化浸出、生物浸出、
2
配位浸出、电化学浸出法等。
高温
Ⅰ.火法炼铜:8CuFeS +21O 8Cu+4FeO+2Fe O +16SO ΔH<0
2 2 2 3 2
(1)反应中被氧化的元素是 (填元素符号)。
(2)实际生产是在沸腾炉中进行,反应温度为 600~620℃。控制反应温度的方法
是 。
(3)冶炼过程中产生大量SO ,下列处理方案中合理的是 (填字母)。
2
A.高空排放 B.制备硫酸
C.用纯碱溶液吸收制 Na SO D.用浓硫酸吸收
2 3
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有SO2-生成。
4
(4)配平该反应方程式:
CuFeS + H O + H+ Cu2++ Fe3++ SO2-+ H O。
2 2 2 4 2
(5)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,
除温度较高双氧水分解之外,还可能的原因是 。
Ⅲ.生物浸出:
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,
反应釜中各物质的转化关系如图所示。
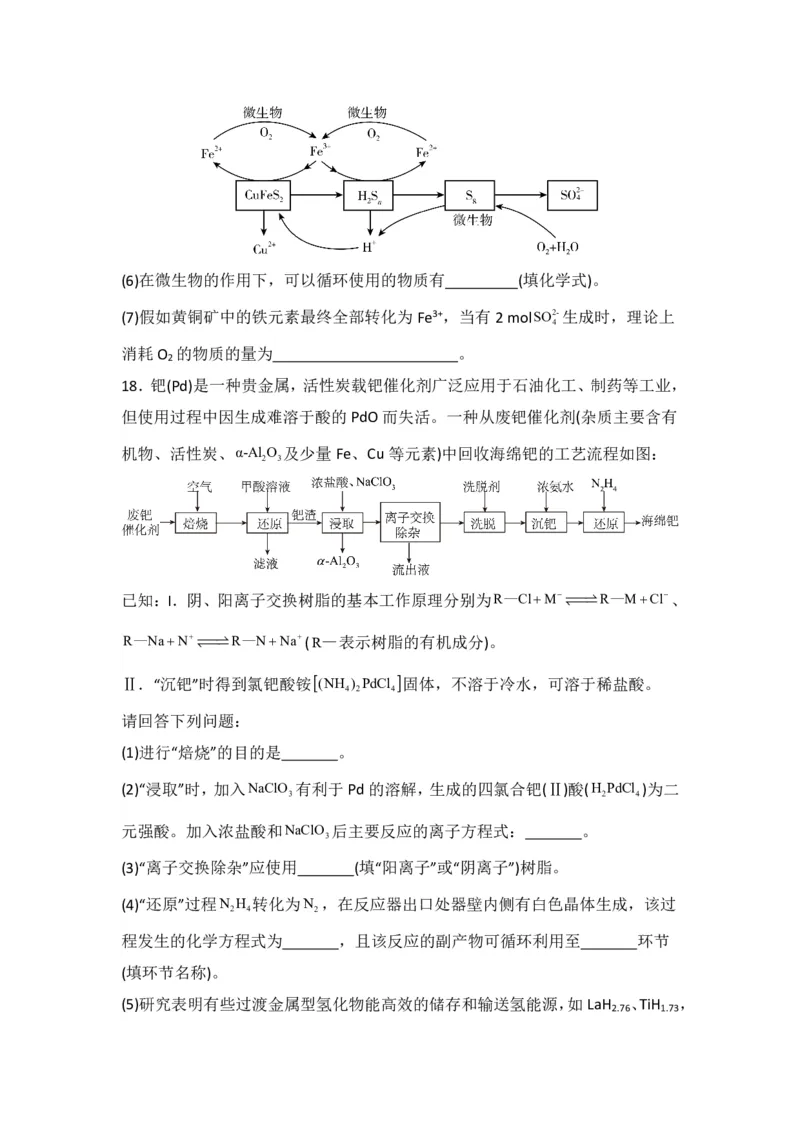
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}(6)在微生物的作用下,可以循环使用的物质有 (填化学式)。
(7)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2molSO2-生成时,理论上
4
消耗O 的物质的量为 。
2
18.钯(Pd)是一种贵金属,活性炭载钯催化剂广泛应用于石油化工、制药等工业,
但使用过程中因生成难溶于酸的PdO而失活。一种从废钯催化剂(杂质主要含有
机物、活性炭、α-Al O 及少量Fe、Cu等元素)中回收海绵钯的工艺流程如图:
2 3
已知:I.阴、阳离子交换树脂的基本工作原理分别为R—ClM R—MCl、
R—NaN R—NNa (R—表示树脂的有机成分)。
Ⅱ.“沉钯”时得到氯钯酸铵
(NH ) PdCl
固体,不溶于冷水,可溶于稀盐酸。
4 2 4
请回答下列问题:
(1)进行“焙烧”的目的是 。
(2)“浸取”时,加入NaClO 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸(H PdCl )为二
3 2 4
元强酸。加入浓盐酸和NaClO 后主要反应的离子方程式: 。
3
(3)“离子交换除杂”应使用 (填“阳离子”或“阴离子”)树脂。
(4)“还原”过程N H 转化为N ,在反应器出口处器壁内侧有白色晶体生成,该过
2 4 2
程发生的化学方程式为 ,且该反应的副产物可循环利用至 环节
(填环节名称)。
(5)研究表明有些过渡金属型氢化物能高效的储存和输送氢能源,如LaH 、TiH ,
2.76 1.73
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为
10.64g·cm-3,相对原子质量为106.4),试写出钯(Pd)的氢化物的化学式 。
在第二步还原过程中,也可用H 代替N H 进行热还原,但消耗的H 质量比理论
2 2 4 2
值略高,其原因是 。
19.物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、
提高学习效率、解决问题都有着重要的意义。
请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁
直观。
①图中所示所属的分类方法为 。
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无
法将其中两种物质归为一类的是 。
A.具有还原性 B.属于氧化物 C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已
经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放
在 。
药品柜 甲柜 乙柜 丙柜 丁柜
药品 乙醇、乙酸 活性炭、红磷 锌粒、铜片 氯化钠、氯化钾
A.甲柜 B.乙柜 C.丙柜 D.丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将
一定量的稀硫酸逐滴滴入到氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直
至有少量气泡产生,此过程中共发生的离子反应有 个。
(2)含铁元素的物质有很多,在生产、生活中应用广泛。取少量某油漆的原料
Fe O (红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶
2 3
液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}为 ,另在小烧杯中加入20mL蒸馏水,加热
至沸腾后,向沸水中滴入2mL 上述棕黄色溶液,继续加热至液体呈 色,
停止加热,证明所得分散系类型的实验方法的名称是 。
20.FeCl 、FeCl 在工业生产中有很多用途,其中FeCl 是一种常用的还原剂、媒
3 2 2
染剂,某实验小组用如下两种方法来制备无水FeCl 。有关物质的性质如下:
2
C H Cl(氯 C H Cl (二氯
6 5 6 4 2
FeCl FeCl
3 2
苯) 苯)
溶解 不溶于C H Cl、C H Cl 、苯,易溶于乙醇,
6 5 6 2 2
不溶于水,易溶于苯、乙醇
性 易吸水
熔点
-45 53 易升华
/℃
沸点
132 173
/℃
(1)用H 还原无水FeCl 制取FeCl 。有关装置如图1所示:
2 3 2
①A 装置中装锌粒的仪器名称是 ;检查A 装置的气密性的方法是 。
②H 还原无水FeCl 制取FeCl 的化学方程式为 。
2 3 2
③按气流由左到右的方向,上述仪器的连接顺序为 (填字母,装置可多次使
用)。
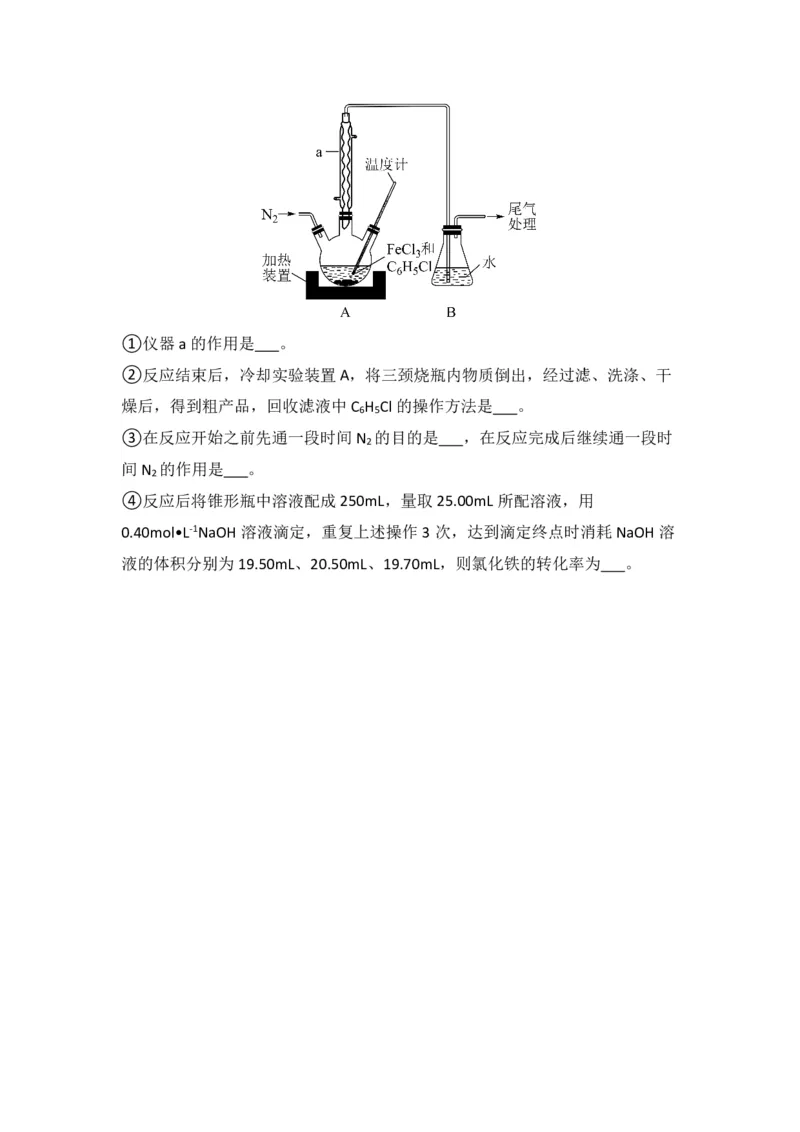
(2)利用反应2FeCl +C H Cl→2FeCl +C H Cl +HCl↑,制取无水FeCl 并测定FeCl 的
3 6 5 2 6 4 2 2 3
转化率。按图2 装置,在三颈烧瓶中放入 32.5g无水氯化铁和过量的氯苯,控制
反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}①仪器a 的作用是 。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干
燥后,得到粗产品,回收滤液中C H Cl 的操作方法是 。
6 5
③在反应开始之前先通一段时间N 的目的是 ,在反应完成后继续通一段时
2
间N 的作用是 。
2
④反应后将锥形瓶中溶液配成250mL,量取25.00mL 所配溶液,用
0.40mol•L-1NaOH溶液滴定,重复上述操作3 次,达到滴定终点时消耗NaOH溶
液的体积分别为19.50mL、20.50mL、19.70mL,则氯化铁的转化率为 。
{#{QQABRQIEggiAQABAAQgCEwVwCAMQkACCACoOxAAAoAAAQANABAA=}#}