文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第1课时 分子结构的测定和多样性 价层电子对互斥模型
培优第一阶——基础过关练
1.(2022·云南省石屏县第一中学高二阶段练习)下列分子或离子中,中心原子含有孤电子对的是
A.PCl B.NO C.SiCl D.PbCl
5 4 2
2.(2022·海南·儋州川绵中学高二阶段练习)下列分子的中心原子的价层电子对数是3的是
A. B. C. D.
3.(2022·北京石景山·高二期末)下列化学用语或图示表达正确的是
A.NaCl的电子式 B.SO 的VSEPR模型
2
C.p-p σ键电子云轮廓图 D.NO 的空间结构模型
4.(2022·湖南·邵东创新实验学校高二期中)下列轮廓图或模型中错误的是
A.p—p σ键电子云轮廓图
B.p—p π键电子云轮廓图
y y
C.CH 分子的球模模型
4
D.NH 分子的VSEPR模型
3
5.(2022·浙江·高二期末)下列有关分子空间结构的说法正确的是
A.HClO、BF、NCl 分子中所有原子的最外层电子都满足了8电子稳定结构
3 3
B.P 和CCl 都是正四面体形分子且键角都为109°28′
4 4
C.分子中键角的大小:BeCl >SO>NH>CCl
2 3 3 4
D.BeF 分子中,中心原子Be的价层电子对数等于2,其空间结构为直线形,成键电子对数等于2,没有
2
孤电子对
6.(2022·北京市第十二中学高二阶段练习)下列各组微粒的空间结构相似的是
A. 与 B. 与 C. 与 D. 与7.(2022·陕西西安·高二期末)下列微粒的空间结构与其 模型不一致的是
A.SO B.BF C.CH D.NH
2 3 4
8.(2022·山西运城·高二期末)经过X射线衍射实验等发现, 中存在 离子,下列粒子的VSEPR
模型与空间结构都与 相同的是
A. B. C. D.
9.(2022·新疆·乌苏市第一中学高二阶段练习)下列分子构型为正四面体且键角为109°28′的是
①P ②NH ③CCl ④CH ⑤HS ⑥CO
4 3 4 4 2 2
A.③④ B.⑤⑥ C.①③④ D.②③④
10.(2022·河南开封·高二阶段练习)关于价层电子对互斥理论说法错误的是
A.价层电子对包括σ键电子对和中心原子上的孤电子对
B.分子中键角越大,价层电子对相互排斥力越小,分子越稳定
C.用该理论预测HS和BF 的空间结构为V形和平面三角形
2 3
D.该理论一定能预测出多中心原子的分子、离子或原子团的空间构型
11.(2021·湖北·华中师范大学潜江附属中学高二阶段练习)下列各组粒子的空间结构相同的是
①NH 和HO;②NH 和HO+;③NH 和HO+;④O 和SO ;⑤CO 和BeCl 。
3 2 3 3 3 3 2 2 2
A.全部 B.①②③⑤ C.③④⑤ D.②⑤
培优第二阶——拓展培优练
12.(2022·重庆市江津第五中学校高二期中)下列说法中正确的是
A.NO 、SO 、BF、NCl 分子中每原子的最外层电子都满足了8电子稳定结构
2 2 3 3
B.P 和CH 都是正四面体形分子且键角都为109°28′
4 4
C.NH 的电子式为 ,离子呈平面正方形结构
D.NH 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
3
13.(2022·新疆石河子一中高二阶段练习)下列粒子的VSEPR模型为四面体、且其空间结构为V形的是
A. B. C. D.SF
2
14.(2022·宁夏·贺兰县景博中学高二阶段练习)下列离子的VSEPR模型与其空间结构一致的是
A. B. C. D.
15.(2022·云南省石屏县第一中学高二阶段练习)用VSEPR模型预测下列分子或离子的立体结构,其中
正确的是
A.CH 与CHCl 均为正四面体 B.BeCl 与SO 为直线形
4 2 2 2 2
C.BF 与PCl 为三角锥形 D.NO 与CO 为平面三角形
3 3
16.(2022·山东枣庄·高二期末)下列分子或离子中,键角由大到小排列正确的是① ②NH ③HO④BF ⑤CO
3 2 3 2
A.⑤④①②③ B.⑤①④②③
C.④①②⑤③ D.③②④①⑤
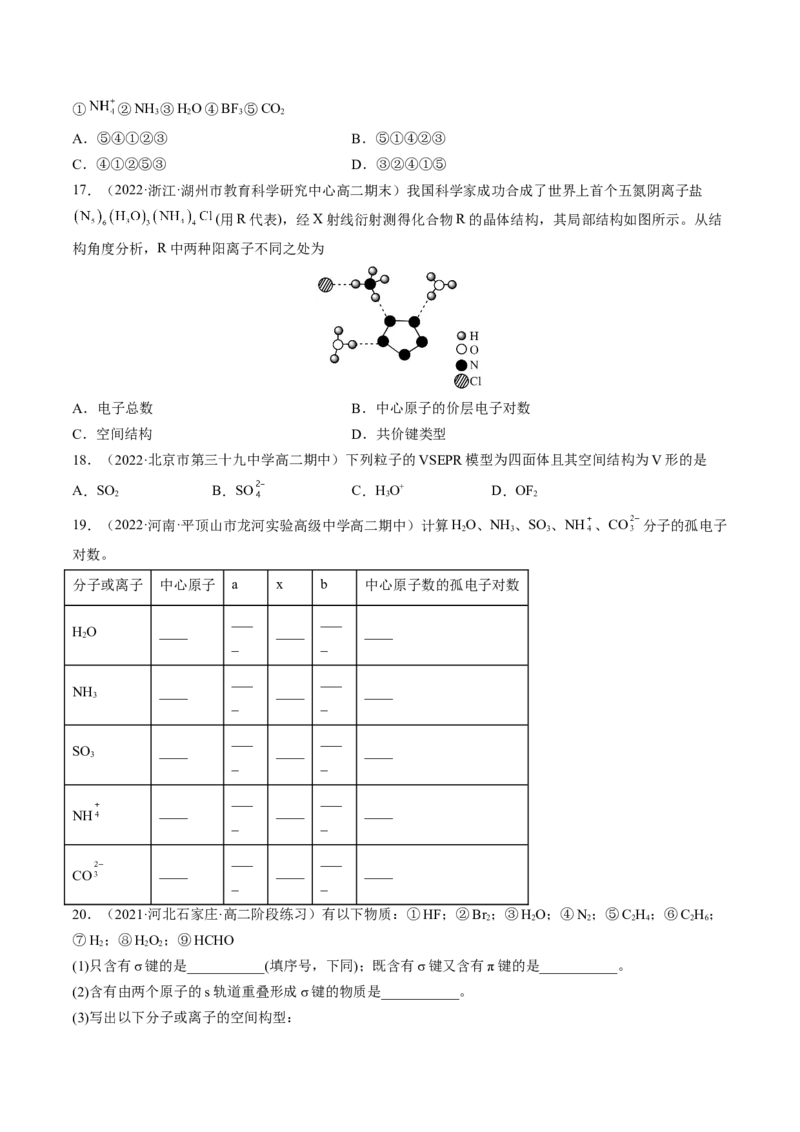
17.(2022·浙江·湖州市教育科学研究中心高二期末)我国科学家成功合成了世界上首个五氮阴离子盐
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。从结
构角度分析,R中两种阳离子不同之处为
A.电子总数 B.中心原子的价层电子对数
C.空间结构 D.共价键类型
18.(2022·北京市第三十九中学高二期中)下列粒子的VSEPR模型为四面体且其空间结构为V形的是
A.SO B.SO C.HO+ D.OF
2 3 2
19.(2022·河南·平顶山市龙河实验高级中学高二期中)计算HO、NH 、SO 、NH 、CO 分子的孤电子
2 3 3
对数。
分子或离子 中心原子 a x b 中心原子数的孤电子对数
___ ___
HO ____ ____ ____
2
_ _
___ ___
NH ____ ____ ____
3
_ _
___ ___
SO ____ ____ ____
3
_ _
___ ___
____ ____ ____
NH
_ _
___ ___
____ ____ ____
CO
_ _
20.(2021·河北石家庄·高二阶段练习)有以下物质:①HF;②Br ;③HO;④N;⑤C H;⑥C H;
2 2 2 2 4 2 6
⑦H;⑧HO;⑨HCHO
2 2 2
(1)只含有σ键的是___________(填序号,下同);既含有σ键又含有π键的是___________。
(2)含有由两个原子的s轨道重叠形成σ键的物质是___________。
(3)写出以下分子或离子的空间构型:NH :___________,HO:___________,SiH:___________,BeCl :___________,CO:
3 2 4 2 2
___________。
21.(2021·宁夏·贺兰县景博中学高二期中)用价层电子对互斥模型推测下列分子或离子的空间构型。
(1)BeCl ___________;
2
(2)SO ___________;
(3)SCl ___________;
2
(4)BF ___________;
3
(5)PF ___________;
3
(6)NH ___________;
22.(2022·吉林·抚松县第一中学高二开学考试)在 分子中
(1) 的价层电子对的空间构型为___________
(2)以极性键相结合,具有正四面体结构的分子是___________
(3)以极性键相结合,具有三角锥型结构的分子是___________
(4)以极性键相结合,具有V型结构的分子是___________
(5)以极性键相结合,而且共价键的极性最大的是___________
23.(2021·河北·邢台一中高二阶段练习)短周期元素A、B、C、D原子序数依次增大,且C元素最高价
氧化物对应的水化物在水溶液中能电离出电子数相等的阴、阳离子。A、C位于同一主族,A为非金属元
素,B的最外层电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。E单
质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏。请回答下列问题:
(1)基态D原子的价电子轨道表示式___________________________。
(2)由上述A、B、D三种元素形成的ADB分子中存在的 键分别称为_________。
(3)B、D两种元素可形成多种阴离子,如 、 、 等,这三种阴离子的空间结构分别为
______________________。比较 和 的键角大小并说明理由:_______________________。
(4)E元素原子基态时电子所占据的轨道个数为:_________;试分析 具有较强还原性的原因
___________________________。