文档内容
课时作业
A篇·知识对点训练
1.下列变化不属于化学变化的是( )
A.煤的干馏 B.石油分馏
C.由乙烯制聚乙烯 D.重油裂化
答案 B
解析 石油的分馏是利用原油中各组分沸点的不同,将复杂的混合物分离成
较简单和更有用的混合物的过程,属于物理变化。
2.下列关于煤、石油、天然气等资源的说法正确的是( )
A.石油裂化得到的汽油是纯净物
B.石油产品都可用于聚合反应
C.天然气是一种清洁的化石燃料
D.水煤气是通过煤的液化得到的气体燃料
答案 C
解析 裂化汽油是由含碳原子数为5~11的烷烃和烯烃等组成的混合物,A
错误;石油产品中有些不含双键的烃类物质不能用于聚合反应,B错误;以甲烷
为主要成分的天然气是一种很好的清洁燃料,C正确;水煤气是通过煤的气化得
到的气体燃烧,D错误。
3.有关煤的说法正确的是( )
A.煤中含有碳的单质、苯、二甲苯、焦炉气
B.煤的干馏是物理变化
C.煤由复杂的有机物和无机物组成,煤的干馏是化学变化
D.煤主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素
答案 C
解析 煤主要含有碳元素,同时还含有少量的氢、硫、氧、氮等元素;煤是
由复杂的有机物和无机物组成的。煤的干馏可获得焦炭、苯、二甲苯、焦炉气等,
属于化学变化。
4.石油裂化的主要目的是为了( )
A.提高轻质液体燃料的产量
B.便于分馏
C.获得短链不饱和气态烃
D.提高汽油的质量
答案 A
解析 石油裂化的目的是为了提高轻质液体燃料的产量和质量,其中以提高
产量为主要目的。5.煤在干馏时得到的气态产物是( )
A.天然气 B.水煤气
C.焦炉气 D.高炉煤气
答案 C
解析 煤干馏时得到的气体是焦炉气,主要成分为氢气、甲烷、乙烯和一氧
化碳。
6.我国冀东渤海湾有储量达10亿吨的大型油田。下列关于石油的说法正确
的是( )
A.石油属于可再生矿物能源
B.石油的裂化是物理变化
C.石油主要含有碳、氢两种元素
D.石油分馏的各馏分均是纯净物
答案 C
解析 石油属于不可再生资源,A错误;石油的裂化有新物质生成,属于化
学变化,B错误;石油分馏的各馏分为混合物,D错误。
7.化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
A.地球上最基本的能源是化学能
B.太阳能热水器、沼气的使用、玉米制乙醇都涉及生物质能的利用
C.利用二氧化碳制造全降解塑料能有效减少“白色污染”
D.人们可以把放热反应释放的能量转化为其他可利用的能量,而吸热反应
没有利用价值
答案 C
解析 地球上最基本的能源是太阳能,A错误;生物质能是绿色植物通过叶
绿素将太阳能转化为化学能并存储在生物质内部的能量,所以使用太阳能热水器
不涉及生物质能的利用,B错误;降解塑料在自然环境中能分解为无害物质,从
而减少“白色污染”,C正确;吸热反应也有利用价值,如有时需要通过吸热反
应吸收热量来降低环境温度,D错误。
8.下列有关石油和煤的利用叙述不正确的是( )
A.煤的干馏就是将煤隔绝空气在高温条件下使之分解,得到焦炭、煤焦油
等物质的过程
B.煤的液化就是将煤转化成甲醇、乙醇等液态物质的过程
C.煤的气化就是将煤在高温条件下由固态转化为气态的物理变化过程
D.石油通过催化裂化,可以获得碳原子数较少的轻质油
答案 C
解析 A项,煤的干馏是将煤隔绝空气加强热使之分解的过程,煤的干馏产
品主要有焦炭、煤焦油、焦炉气等;B项,煤的液化是将煤转化为液体燃料(如甲醇等)的过程;C项,煤的气化是将煤转化为气体燃料(如CO、H )的过程,为
2
化学变化;D项,石油的催化裂化是将相对分子质量大、沸点高的烃断裂为相对
分子质量小、沸点低的烃的过程,从而获得轻质油。
9.如何实现化石燃料的综合利用,减少化石燃料燃烧所造成的环境污染,
是人类面临的重大挑战。下列关于化石燃料及其使用的一些说法中不正确的是(
)
A.煤的气化是指将固态煤粉碎成气态煤,以使煤燃烧时能与氧气充分接触
而完全燃烧
B.天然气除可用作清洁能源外,也可用于合成氨和生产甲醇等
C.石油分馏得到的汽油和石油催化裂化得到的汽油其成分不相同
D.化石燃料也是重要的化工原料,乙烯和苯就是分别来自于石油和煤的基
本化工原料
答案 A
解析 A中,煤的气化是将固态煤转化为可燃性气体的过程,主要反应的化
学方程式为C+H O(g)=====CO+H 。
2 2
10.由石油裂化和裂解得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:
根据以上材料和你所学的化学知识回答下列问题:
(1)由CH CH 制得有机物A的化学方程式是_________________,反应类型
2 2
是________。
(2)由A与B合成丙烯酸乙酯的化学方程式是_________________,反应类型
是________。
(3)由石油裂解产物乙烯合成聚乙烯塑料的化学方程式是______________。
答案 (1)CH CH +H O――→CH CH OH 加成反应
2 2 2 3 2
(2)CH CHCOOH+CH CH OH((((
2 3 2
CH CHCOOCH CH +H O 取代反应(或酯化反应)
2 2 3 2
(3)nCH CH ――→CH —CH
2 2 2 2
解析 类比制取乙酸乙酯的反应可知有机物 A 为 CH CH OH,B 为
3 2
CH CHCOOH,故A为乙烯与H O发生加成反应的产物。聚乙烯是以乙烯为单
2 2
体,通过加聚反应制得的。
B篇·综合提升训练
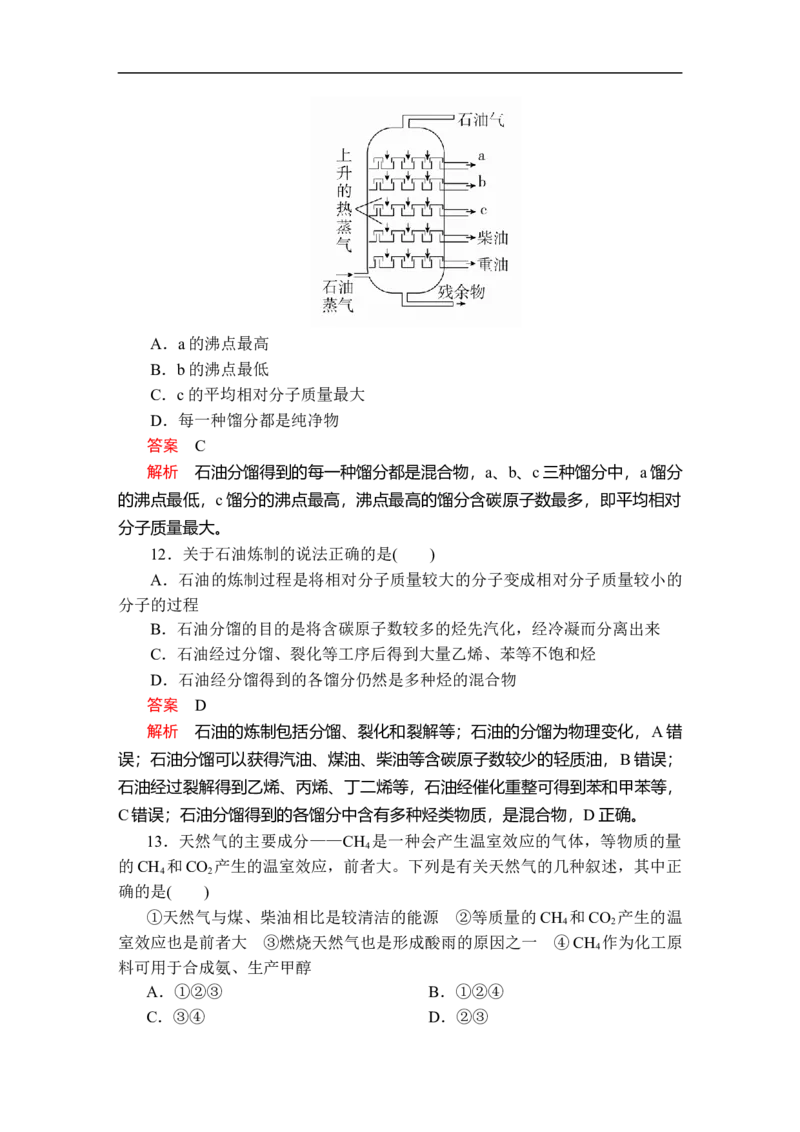
11.如图所示是石油分馏塔的示意图,a、b、c三种馏分中( )A.a的沸点最高
B.b的沸点最低
C.c的平均相对分子质量最大
D.每一种馏分都是纯净物
答案 C
解析 石油分馏得到的每一种馏分都是混合物,a、b、c三种馏分中,a馏分
的沸点最低,c馏分的沸点最高,沸点最高的馏分含碳原子数最多,即平均相对
分子质量最大。
12.关于石油炼制的说法正确的是( )
A.石油的炼制过程是将相对分子质量较大的分子变成相对分子质量较小的
分子的过程
B.石油分馏的目的是将含碳原子数较多的烃先汽化,经冷凝而分离出来
C.石油经过分馏、裂化等工序后得到大量乙烯、苯等不饱和烃
D.石油经分馏得到的各馏分仍然是多种烃的混合物
答案 D
解析 石油的炼制包括分馏、裂化和裂解等;石油的分馏为物理变化,A错
误;石油分馏可以获得汽油、煤油、柴油等含碳原子数较少的轻质油,B错误;
石油经过裂解得到乙烯、丙烯、丁二烯等,石油经催化重整可得到苯和甲苯等,
C错误;石油分馏得到的各馏分中含有多种烃类物质,是混合物,D正确。
13.天然气的主要成分——CH 是一种会产生温室效应的气体,等物质的量
4
的CH 和CO 产生的温室效应,前者大。下列是有关天然气的几种叙述,其中正
4 2
确的是( )
①天然气与煤、柴油相比是较清洁的能源 ②等质量的CH 和CO 产生的温
4 2
室效应也是前者大 ③燃烧天然气也是形成酸雨的原因之一 ④CH 作为化工原
4
料可用于合成氨、生产甲醇
A.①②③ B.①②④
C.③④ D.②③答案 B
解析 ①天然气与煤、柴油相比,是相对清洁的能源;②CH 的摩尔质量为
4
16 g·mol-1,CO 的摩尔质量为44 g·mol-1,则等质量时,CH 产生的温室效应大
2 4
于CO ;③天然气燃烧不产生硫、氮的氧化物,不会形成酸雨;由CH 的用途知
2 4
④正确。
14.煤是重要的能源和化工原料,直接燃烧既浪费资源又污染环境。最近,
某企业利用“煤粉加压气化制备合成气新技术”将煤变成合成气(一氧化碳及氢
气总含量≥90%),把煤“吃干榨尽”。下列有关说法正确的是( )
①煤粉加压气化制备合成气的过程涉及化学变化和物理变化 ②煤粉加压气
化制备合成气的过程仅涉及化学变化 ③该技术实现了煤的清洁利用 ④该技术
实现了煤的高效利用
A.①②③ B.①②④
C.①③④ D.②③④
答案 C
解析 煤粉加压气化制备合成气的过程将煤变成了以CO和H 为主要成分的
2
合成气,此过程涉及化学变化和物理变化,减少了煤直接燃烧造成的污染,提高
了煤的利用率。
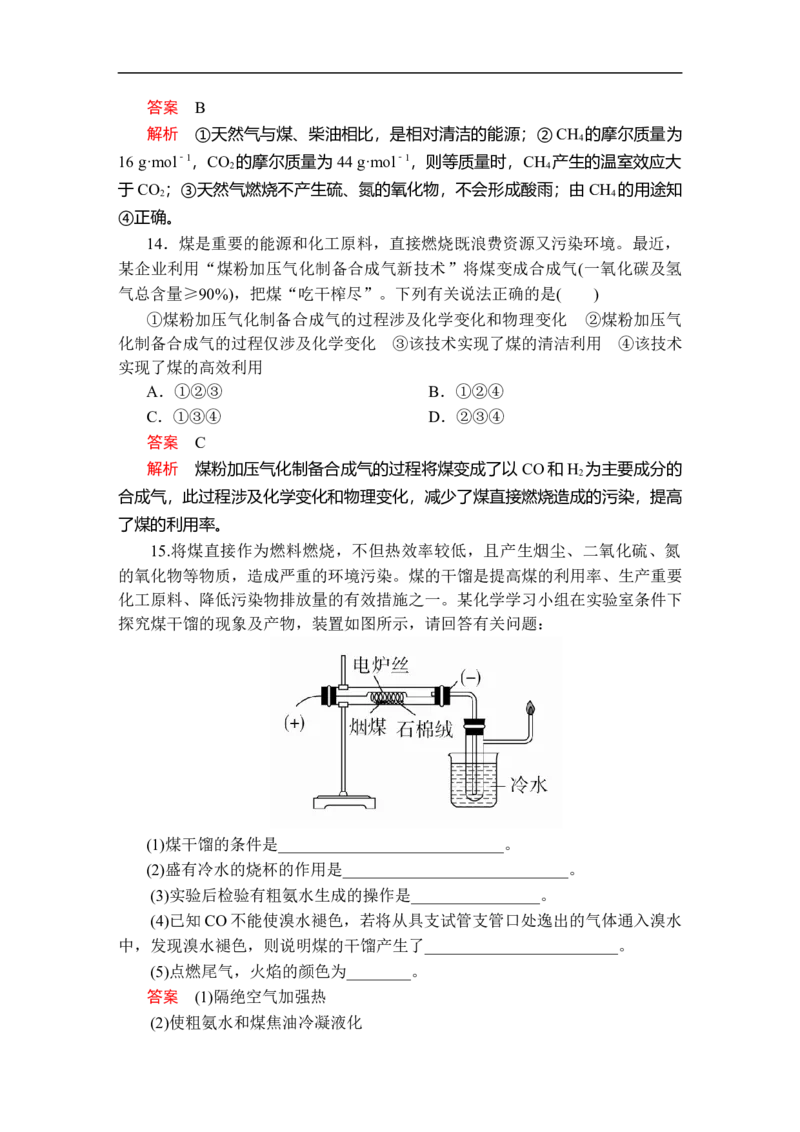
15.将煤直接作为燃料燃烧,不但热效率较低,且产生烟尘、二氧化硫、氮
的氧化物等物质,造成严重的环境污染。煤的干馏是提高煤的利用率、生产重要
化工原料、降低污染物排放量的有效措施之一。某化学学习小组在实验室条件下
探究煤干馏的现象及产物,装置如图所示,请回答有关问题:
(1)煤干馏的条件是____________________________。
(2)盛有冷水的烧杯的作用是____________________________。
(3)实验后检验有粗氨水生成的操作是________________。
(4)已知CO不能使溴水褪色,若将从具支试管支管口处逸出的气体通入溴水
中,发现溴水褪色,则说明煤的干馏产生了________________________。
(5)点燃尾气,火焰的颜色为________。
答案 (1)隔绝空气加强热
(2)使粗氨水和煤焦油冷凝液化(3)将具支试管取出,塞上试管塞并加热,将湿润的红色石蕊试纸放在支管
口处,若试纸变蓝,则说明有粗氨水生成
(4)乙烯等不饱和烃类物质
(5)淡蓝色
解析 (1)根据煤干馏的定义可知其条件为隔绝空气加强热。
(2)冷水浴的作用是冷凝,使粗氨水和煤焦油冷凝液化。
(3)可用湿润的红色石蕊试纸检验是否有NH 逸出。
3
(4)溴水褪色,证明煤干馏过程产生了乙烯等不饱和烃类物质。
(5)CO、CH 、H 等气体燃烧时火焰呈淡蓝色。
4 2
16.煤气化是有效利用化石能源的手段之一,有关反应为 ① C+
H O(g)=====CO+H 、②CO+H O(g)((((CO +H ,获得的气体称为水煤气。某
2 2 2 2 2
研究性学习小组为探究气体的成分,进行了如下实验。
【实验】 使水蒸气通过灼热的焦炭,收集反应后流出的气体。
【提出假设】 对气体的成分提出了三种假设。
假设1:该气体是CO、H 、H O。
2 2
假设2:该气体是CO 、H 、H O。
2 2 2
(1)假设3:____________________________。
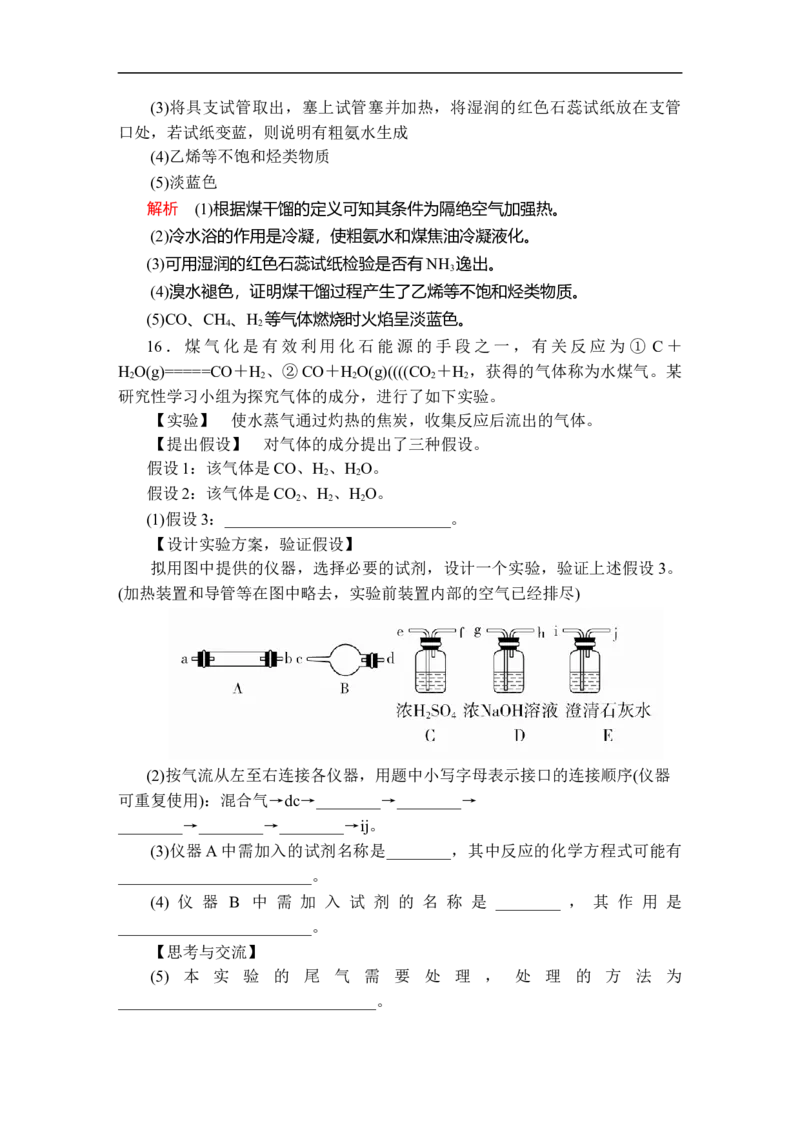
【设计实验方案,验证假设】
拟用图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设3。
(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)
(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器
可重复使用):混合气→dc→________→________→
________→________→________→ij。
(3)仪器A中需加入的试剂名称是________,其中反应的化学方程式可能有
________________________。
(4) 仪 器 B 中 需 加 入 试 剂 的 名 称 是 ________ , 其 作 用 是
________________________。
【思考与交流】
(5) 本 实 验 的 尾 气 需 要 处 理 , 处 理 的 方 法 为
________________________________。答案 (1)该气体是CO、H 、H O、CO
2 2 2
(2)ij gh ef ab dc
(3)氧化铜(或其他合理答案) CuO+H =====Cu+H O、CuO+CO=====Cu
2 2
+CO
2
(4)无水硫酸铜 检验混合气体中是否有水
(5)可在装置最后的导气管口放一燃着的酒精灯将气体燃烧(或其他合理答案)
解析 (1)根据反应原理,混合气体组成存在三种情况,第三种情况的气体组
成的CO、H 、H O、CO 。
2 2 2
(2)为了验证混合气中含CO、H 、H O、CO ,实验仪器的先后连接顺序为检
2 2 2
验水分→检验二氧化碳→除掉二氧化碳→除掉水分→还原装置→检验水分→检验
二氧化碳,仪器连接顺序为混合气体→dc→ij→gh→ef→ab→dc→ij。
(3)仪器A用于检验氢气和一氧化碳,可以选用氧化铜,利用氢气、一氧化
碳加热还原氧化铜完成检验,反应的化学方程式为 CuO+H =====Cu+H O,
2 2
CuO+CO=====Cu+CO 。
2
(4)白色的无水硫酸铜遇水后变成蓝色,所以可在装置 B中加入无水硫酸铜
(CuSO ),通过观察颜色是否改变来确定混合气体中是否有水蒸气。
4
(5)一氧化碳有毒,直接排放到空气中会污染环境,可在装置最后的导管口
处放一个点燃的酒精灯,利用燃烧的方法消除CO的污染等。