文档内容
下列说法正确的是
育才高级中学12月月考化学试题 A.上述反应在任何温度下均可自发进行
B.上述反应反应物的总能量大于生成物的总能量
注意事项: c(CH OCH )
3 3
C.上述反应平衡常数K=
填写答题卡的内容用2B铅笔填写 c2 (CO )⋅c6 (H )
2 2
第Ⅰ卷 客观题
D.上述反应达到平衡后,加入催化剂,平衡正向移动
第Ⅰ卷的注释
5.(3分)下列有关说法正确的是
阅卷人
一、选择题(共15题;共45分)
A.将Al (SO ) 、Na SO 、FeCl 溶液蒸干均得不到原溶质
得分 2 4 3 2 3 3
1.(3分)中华传统文化蕴含着丰富的化学知识,下列诗句蕴含的化学知识分析不正确的是
c(N H+)
( )
B.往100mL的0.1mol⋅L−1氨水中加蒸馏水至1L, 4 的比值增大
c(N H ⋅H O)
3 2
A.“沧海月明珠有泪,蓝田日暖玉生烟”,句中珠字对应的化学物质是碳酸钙,属于强
C.将AB型强电解质溶于水,该过程的ΔH可能大于零,也可能小于零,但ΔS一定大于
电解质
零
B.“欲渡黄河冰塞川,将登太行雪满山”,这个过程能自发进行
D.为减小或消除中和反应反应热的测定实验的偶然误差,需要多次测定,取平均值,每
C.“煮豆燃豆萁,豆在釜中泣”,这里的能量变化主要是化学能转化为热能
次测定需要使用温度计2次
D.“粉身碎骨浑不怕,要留清白在人间”,大理石变为生石灰的过程是吸热反应
6.(3分)在密闭容器中发生如下反应:mA(g)+nB(g)⇌pC(g),达到平衡后,保持温度不
2.(3分)基本概念和理论是化学思维的基石,下列说法错误的是
变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中
A.盖斯定律表明反应热只与反应体系的始态和终态有关,而与反应的途径无关
错误的是
B.氮的固定是将大气中游离态的氮转化为氮的化合物的过程
A.m+n>p B.平衡向逆反应方向移动
C.加入催化剂,不仅可以降低活化能,还能减小该化学反应的ΔH
C.A的转化率降低 D.活化分子百分数不变
D.活化能是活化分子具有的平均能量与反应物分子具有的平均能量之差
7.(3分)已知25 ℃下,醋酸溶液中存在下述关系:K=c(H+)·c(CH COO-)/c(CHCOOH)=
3.(3分)发展绿色甲醇产业有助于减少温室气体排放和空气污染。“零碳甲醇燃料”燃烧 3 3
1.75×10-5,其中K是该温度下醋酸的电离平衡常数。有关K的下列说法正确的是( )
[2CH OH(g)+3O (g)=2CO (g)+4H O(g)]的过程中焓变和熵变均正确的是
3 2 2 2
A.当向该溶液中加入一定量的硫酸时,K值增大
A.ΔH>0,ΔS<0 B.ΔH<0,ΔS<0
B.升高温度,K值增大
C.ΔH>0,ΔS>0 D.ΔH<0,ΔS>0
C.向醋酸溶液中加水,K值增大
催化剂
4.(3分)反应2CO (g)+6H(g) CH OCH (g)+3HO(g);△H<0可实现CO 的资源化,
2 2 ⇌ 3 3 2 2 D.向醋酸溶液中加氢氧化钠,恢复到25 ℃时,K值增大
8.(3分)我国科学家在一颗距离地球100光年的行星上发现了不可思议的“水世界”,引起了全球科学界的轰动。下列有关说法错误的是 C.常温下,pH=3的醋酸溶液和pH=11的氢氧化钡溶液等体积混合后溶液的pH<7
D.常温下,pH为5的醋酸和pH为9的NaOH两种溶液中,由水电离的c(H+)之比为1:1
A.温度升高,水的电离平衡正向移动,c(H+)增大,但溶液仍然保持中性
13.(3分)常温下,0.1mol⋅L−1氨水pH=11,0.1mol⋅L−1醋酸pH=3,下列说法正确的
B.室温下,pH=4的盐酸溶液中,c (H+)=5×10−9mol⋅L−1 是
水
A.常温时,CH COOH的电离平衡常数与NH ⋅H O的相等
3 3 2
C.由水电离出的c (H+)=c (OH−)时,溶液不一定呈中性
水 水 B.将0.1mol⋅L−1氨水稀释10倍,pH<10
D.向水中加入NaHSO 固体后(溶液温度不变),水的电离程度减小
4 C.0.1mol⋅L−1醋酸溶液中:c(CH COOH)>c(CH COO−)>c(H+)>c(OH−)
3 3
9.(3分)下列说法正确的是
D.CH COONH 溶液因水解呈酸性
A.NaHCO 、NaHSO 都能促进水的电离 3 4
3 4
14.(3分)已知:25℃时有关弱酸的电离平衡常数,下列有关说法正确的是
B.某盐溶液呈酸性,该盐一定发生了水解反应
弱酸化学式 H SO HClO H CO
2 3 2 3
c(CH COO−)
3
C.加水稀释稀醋酸溶液的过程中,溶液中 逐渐增大 K =4.3×10−7
c(CH 3 COOH) 电离平衡常数 K =1.3×10−2;K =6.3×10−8 2.95×10−8 a1
a1 a2 K =5.6×10−11
D.常温下,pH=10的CH COONa溶液与pH=10的氨水,水的电离程度相同 a2
3
10.(3分)在25 ℃时,某稀溶液中由水电离产生的H+浓度为1.0×10-13 mol/L,下列有关该 A.等物质的量浓度的酸溶液pH关系为:pH(HClO)ClO−>HSO−
A.该溶液可能呈酸性 B.该溶液一定呈碱性 3 3
C.该溶液的pH一定是1 D.该溶液的pH不可能为13
C.少量的CO 通入NaClO溶液中发生反应:2ClO−+CO +H O=CO2−+2HClO
2 2 2 3
11.(3分)常温下的某一元酸HA,下列事实不能证明HA为弱酸的是
A.相同条件下,浓度均为0.1mol⋅L−1的HA溶液和盐酸,HA溶液的导电能力弱 D.足量的SO 与NaClO溶液发生的反应只有:ClO−+SO +H O=HSO−+HClO
2 2 2 3
B.0.1mol⋅L−1NaA溶液能使酚酞试液变红
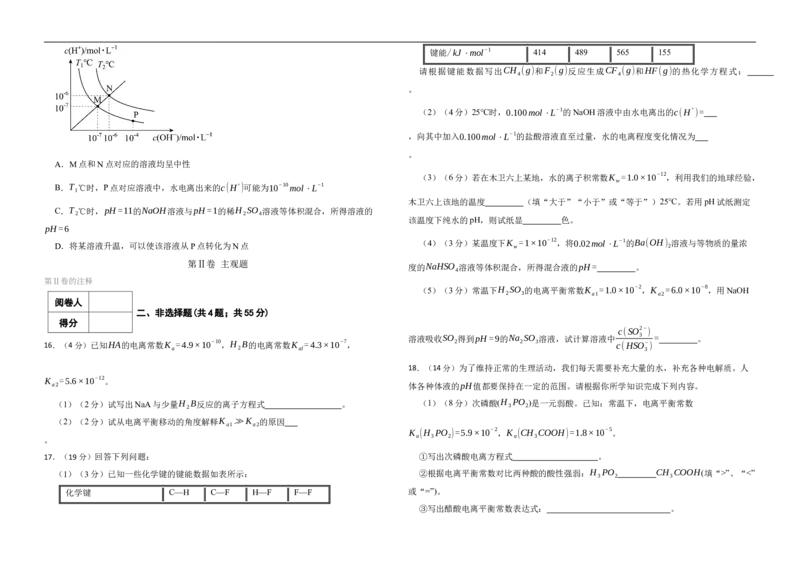
15.(3分)不同温度下,水溶液中c(H+)和c(OH−)的物质的量浓度的关系如图所示。下列说
C.往HA溶液中滴加同浓度的NaOH溶液,呈中性时,酸和碱溶液的体积关系:
V ”、“<”
3 2 3
化学键 C—H C—F H—F F—F 或“=”)。
③写出醋酸电离平衡常数表达式: 。④取等体积、物质的量浓度相等的H PO 、CH COOH两溶液,分别用等浓度的KOH稀
3 2 3 c.HCOO−+CH COOH=CH COO−+HCOOH
3 3
溶液中和,则消耗的KOH溶液的体积大小关系为:H PO CH COOH(填“>、<”
3 2 3
(4)(3分)0.1mol/L的NaCl溶液与0.1mol/L的CH COONH 溶液对比,水的电离程
3 4
或“=”)。
度:前者 后者(填“>”“<”或“=”)
(2)(2分)常温下,0.1mol/LCH COOH的溶液在加水稀释过程中,下列表达式的数
3
(5)(3分)pH相同的NaClO和CH COOK的两溶液中:c(Na+)-c(ClO-) c(K+)-
3
据一定变大的是___________。
c(CH COO-)(填“>”“<”或“=”)
3
c(OH−)
A.c(CH COO−) B. (6)(3分)已知N H ·H O的电离与NH ·H O相似。硫酸肼(N H SO )是一种重要
3 c(H+) 2 4 2 3 2 2 5 4
的化工原料,属于碱式盐,根据表格中提供的平衡常数分析N H SO 溶液显 性(填
2 5 4
c(CH COOH) c(H+)⋅c(CH COO−) “酸”、“碱”或“中”)。
3 3
C. D.
c(H+) c(CH COOH)
3
(3)(2分)常温下,将pH=1的盐酸与pH=12的NaOH溶液混合后,所得溶液的
pH=3,则盐酸与NaOH溶液的体积比为___________。
A.1:11 B.11:1 C.1:9 D.9:1
(4)(2分)将0.23g金属钠溶于水恢复至常温并配制成1000mL的溶液的pH= 。
19.(18分)下表是25℃时某些弱酸的电离平衡常数。
化
学 CH COOH NH ·H O HClO HCO HCOOH NH·H O
3 3 2 2 3 2 4 2
式
Ka1=4.1×10-7 Kb1=10-5.75
K Ka=1.8×10-5 Kb=1.8×10-5 Ka=3.0×10-8 Ka=1.77×10-4
Ka2=5.6×10-11 Kb2=10-8.9
(1)(3分)0.1mol/LCH COOH溶液与0.1mol/L的氨水等体积混合后,溶液呈
3
性(填“酸”、“碱”或“中”)。
(2)(3分)常温下,pH=5的CH COOH溶液与pH=9的NaOH溶液混合后,溶液呈中
3
性,则CH COOH溶液的体积 NaOH溶液的体积(填“>”“<”或“=”)
3
(3)(3分)由表格中的数据判断下列离子方程式正确的是 (填字母)。
a.2ClO−+H O+CO =2HClO+CO2−
2 2 3
b.HCOOH+HCO−=HCOO−+CO ↑+H O
3 2 2(2)B
答案解析部分
(3)C
1.【答案】B
(4)12
2.【答案】C
19.【答案】(1)中
3.【答案】D
(2)<
4.【答案】B
(3)b
5.【答案】B
(4)<
6.【答案】A
(5)=
7.【答案】B
(6)酸
8.【答案】B
9.【答案】C
10.【答案】A
11.【答案】D
12.【答案】B
13.【答案】A
14.【答案】B
15.【答案】D
16.【答案】(1)A−+H B=HA+HB−
2
(2)H B分步电离,第一步电离产生的H+抑制了第二步电离
2
17.【答案】(1)CH (g)+4F (g)=CF (g)+4HF(g)ΔΗ=−1940kJ⋅mol−1
4 2 4
(2)1×10−13mol⋅L−1;先增大,后减小
(3)大于;淡黄色
(4)10
(5)60
c(CH COO−)·c(H+)
18.【答案】(1)H PO ⇌H++H PO−;>;K = 3 ;=
3 2 2 2 a c(CH COOH)
3