文档内容
湘 豫 名 校 联 考
#$#%&#$#’学年新高考适应性调研考试
化学参考答案
题号 ! # ( % ’ " ) * + !$ !! !# !( !%
答案 , - - - . / / , , / . , . /
一!选择题"本题共!%小题#每小题(分#共%#分$在每小题给出的四个选项中#
只有一项是符合题目要求的$
!0,!%试题立意&本题以!化学与生命"生活"生产和生态#为学科情境$考查对!糖类"蛋白质的性质"硫酸的工
业制备和绿色化学理念#的认知与理解%该题涉及的知识均来源于教材%
%解析&利用静脉注射葡萄糖溶液的方式来迅速补充营养!.项错误"盐卤等物质能使蛋白质聚沉!-项错误"
硫黄或其他含硫矿物先被氧化为12 !再进一步转化为硫酸!,项正确"绿色化学的核心思想是改变#先污染
#
后治理$现状!实现从源头消除环境污染!/项错误%故选,%
#0-!%试题立意&本题以!硼及其化合物#为学科情境$考查对!轨道表示式"31456模型"电子式"电离方程式#
的认知与理解%
%解析&三氟化硼&-7’中!中心原子硼的价层电子对数为(!孤电子对为$!31456模型为 !-项错误%
(
故选-%
(0-!%试题立意&本题以!化学实验基本知识与技能#为学科情境$考查对!化学物质标识"浓硫酸稀释"物质萃
取分离"物质检验#的认知与理解%该题涉及的知识部分来源于教材%
%解析&!中标识表示腐蚀类物质!.项正确"容量瓶不能用于溶液稀释!-项错误"使用分液漏斗!加入,,8
%
萃取分离碘水中的9!,项正确"溴乙烷消去反应生成的乙烯中可能含有乙醇!乙醇也能使酸性高锰酸钾溶
#
液褪色!应先用水吸收乙醇!排除干扰!/项正确%故选-%
%0-!%试题立意&本题以!学科探索#为学科情境$考查对!物质结构与性质"腈的水解"高聚物"金属的腐蚀与防
护#的认知与理解%该题涉及的知识部分来源于教材%
%解析&过氧化钠含有过氧键!发生反应时氧元素化合价从&!降低为&#!表现强氧化性!.项正确"乙腈
&,:,;’在酸性条件下水解!最终生成乙酸!-项错误"羧基具有亲水性!含碳碳双键的单体!能发生加聚反
(
应!,项正确"阴极发生还原反应!金属被保护!/项正确%故选-%
’0.!%试题立意&本题以!天然活性物质柿单宁#为学科情境$考查对!有机物的结构"性质与用途的定性"定量
关系"氢键"<射线衍射#的认知与理解%
%解析&该物质含酚羟基!容易被氧化!可用作抗氧化抑菌剂!.项正确"苯环邻位的羟基之间可以形成分子内
氢键!-项错误"相对分子质量可通过质谱仪测定!,项错误"酯基不与: 发生加成反应!!=>8该物质能与
#
+=>8: 发生加成反应!/项错误%故选.%
#
"0/!%试题立意&本题以!学科探索#为学科情境$考查对!复杂离子方程式"化学方程式"沉淀溶解#的认知与理
解%该题涉及的知识全部来源于教材%
化学参考答案!第!!!!!页!共"页"
书书书%解析&向一定体积的氢氧化钡溶液中逐滴加入稀硫酸的反应为-?#@@12#
%
&@#:@@#2:&"""-?12 %#@
#:2!/项错误%故选/%
#
)0/!%试题立意&本题以!三氧化硫分子结构的多样性#为学科情境$考查对!物质的量相关计算"手性异构体"
分子极性"杂化轨道理论#的认知与理解%
%解析&标准状况下!12 为固态!.项错误"气态12 是非极性分子!-项错误"三聚体&12 ’结构对称!不
( ( ( (
存在手性异构体!,项错误"链状&12
(
’
!
中硫原子价层电子对数为%!没有孤电子对!因此是AB(杂化!/项正
确%故选/%
*0,!%试题立意&本题以!工业生产#为学科情境$考查对!海水提溴"高分子分离膜"盐类水解"制碱原理#的认
知与理解%该题涉及的知识部分来源于教材%
%解析&#吹出提溴$中溴离子被氧化成溴单质属于氧化还原反应!.项正确"分离膜根据膜孔大小分为微滤
膜(超滤膜(纳滤膜和反渗透膜等!可用于分离不同的物质!-项正确"富二价盐浓水中的 CD,8
#
蒸干时水解
生成CD&2:’
#
!,项错误"氯化铵水解使溶液呈酸性!能与铁锈反应!/项正确%故选,%
+0,!%试题立意&本题以!合金材料#为学科情境$考查对!晶胞化学式"配位数"晶体的性质"材料组成与性能的
关系#的认知与理解%
%解析&运用均摊法!该铝锂合金的化学式为.8
(
EF!摩尔质量为**D)=>8&!!.项正确"观察晶胞结构图!可
知同层与EF紧邻的.8为%个!上层(下层各为%个!与EF紧邻的.8为!#个!-项正确"晶体在强度方面会
表现出各向异性!,项错误"EF的相对原子质量小!密度小!有利于航空结构件轻量化!/项正确%故选,%
!$0/!%试题立意&本题以!新型的电化学合成氨#为学科情境$考查对!电化学基本原理"电极判断"电极反应
式#的认知与理解%
%解析&电极C生成;: !发生还原反应!作阴极!与电源负极相连!.项错误"电极;发生反应*%2:&&
(
%G&"""#:
#
2@2 #$!-项错误"电极C发生反应*;2
(
&@*G&@":
#
2""";: ($@+2:&!电解一段时间后!
H;2
(
储罐中B:增大!,项错误"硝酸盐电化学合成氨与传统合成氨相比具有条件温和(环境友好的优势!/
项正确%故选/%
!!0.!%试题立意&本题以!实验探究#为学科情境$考查对!对照实验"焰色试验"酸式盐的酸碱性"浓硫酸的特
性#的认知与理解%
%解析&!=>82 和%=>8;2 与空气形成对照!带有火星的木条复燃!说明;2 支持燃烧!.项正确"无色
# # #
溶液中可能含有氢氧化钠!-项错误"若;?:.为;?:12
%
!;?:.溶液的B:%)!若;?:.为;?:12
(
!
;?:.溶液的B:%)!无法确定:
#
.是强酸还是弱酸!,项错误"浓硫酸与蔗糖反应生成的二氧化硫能使
溴水褪色!验证浓硫酸具有强氧化性!/项错误%故选.%
!#0,!%试题立意&本题以!,5I针脚中金的绿色回收#为学科情境$考查对!金属的性质"配位化合物"超分子"
氧化还原反应计算#的认知与理解%
%解析&通过稀硝酸氧化的方法可以除去,J(;F和,>等杂质金属实现金的富集!.项错误"H.J-K 中不含
%
非极性键!-项错误"自组装是超分子的重要特征!,项正确"%+.J-K
%
,&@(1
#
2#
’
&@!*2:&"""%.J@
"12#
%
&@!"-K&@+:
#
2!(=>8;?
#
1
#
2
’
还原一维复合物")-K!最多生成.J的质量为%=>8L!+)D)=>8&!M
)**D!/项错误%故选,%
!(0.!%试题立意&本题以!酸碱中和滴定实验#为学科情境$考查对!水的电离"电离平衡"水解平衡"溶液中离
子浓度大小比较"溶液中离子平衡计算#的认知与理解%
化学参考答案!第!!!!#页!共"页"#&:@’)#&.&’
%解 析&由 题 目 可 知 发 生 反 应 ;?2:@ :. &’;?.@ :
#
2!可 得 "
:.
M
#&:.’
M
#&:@’)#&;?2:’)$&;?2:’L!$&( #&:@’)$&;?2:’
M 可得*#&:@’)$&;?2:’M&" )$&;?2:’@
#&;?2:’+’$&$&;?2:’,L!$&( +’$&$&;?2:’, :.
$0$$$($L!$&(=>8
’$" %因此" M!L!$&’%C点时酸过量有剩余!溶液中的氢离子浓度为 !水电离出
:. :. #$L!$&(E
"
的#&:@’M N ("0)L!$&!$=>8)E&!!.项错误";点时!:.已中和’$O!:.的电离常数大于
!0’L!$&’
;?.的水解常数!:.的电离程度大于;?.的水解程度!-项正确"5)P的变化过程中*#&;?@’@#&:@’
M#&2:&’@#&.&’!且#&.&’*#&:.’!推导出#&;?@’@#&:@’*#&2:&’@#&:.’!,项正确"B:M)
时!#&:@’M!$&)=>8)E&!!代入线性公式中可得*$&;?2:’(%+0’$=E!/项正确%故选.%
!%0/!%试题立意&本题以!二氧化碳资源化#为学科情境$考查对!化学反应的方向"限度和调控$化学平衡常数
计算#的认知与理解%
%解析&题中可逆反应的正反应方向为气体分子数减小的反应!增大压强!平衡正向移动!%&,:2:’增大!曲
(
线C代表等温过程+%&,:
(
2:’#&,的变化关系!.项错误"曲线;代表等压过程+%&,:
(
2:’#’,的变化关
系!温度升高!%&,:2:’减小!该反应为放热反应!在低温条件下自发进行!-项错误"%&,:2:’M$0$%!反
( (
应条件可能为%L!$’5?!#’$Q&等温曲线’或’L!$’5?!#"’Q左右&等压曲线’!,项错误"#!$Q时!
$0!$L$0!$
%&,:2:’M$0!$!经计算可得*%&:2’M$0!$!%&,2’M$0#$!%&: ’M$0"$!" M L&’L
( # # # B $0#$L$0"$(
!$’5?’&#M+0(L!$&!(5?&#!/项正确%故选/%
’因题目图中纵坐标O应删去#故此题所有考生都得分(
二!非选择题"本题共%小题#共’*分$
!’0!!%分"!!"’A#!#分"
!#"CD,2
(
@#:@"""CD#@@,2 #$@:
#
2!#分"
!(""0!%!#分"
!%"抑制-?12 转化为-?,2!#分"
% (
!’"增大反应物间的接触面积#加快除钡速率!#分"
!"";:;2!或硝酸铵"!#分"
% (
高温
!)"(1K2@#.8"""(1K@.8
#
2
(
!#分"
%试题立意&本题以!天青石制备高纯1K,2#为学科情境$考查对!价层电子排布式"离子反应"化学反应速
(
率"沉淀转化的定性分析与定量计算"金属冶炼#的认知与理解%
%解析&&!’
(*
1K元素位于第五周期第$.族!基态1K原子的价层电子排布式为’A#%
&#’酸浸时!CD,2
(
与:,8反应的离子方程式为CD,2
(
@#:@"""CD#@@,2 #$@:
#
2%
" &1K12’ (0%%L!$&) #&12#&’
&(’1K12
%
@,2#
(
& &’1K,2
(
@12#
%
& 的"M
"
AB
&1K,2
%
’
M
’0"$L!$&!$
("!%!当(M
#&,2
%
#&’
%"时!沉淀
AB ( (
转化平衡正向移动!有利于1K12
%
转化为1K,2
(
!即#&12#
%
&’%")#&,2#
(
&’M"!%L$0$!=>8)E&!M
"0!%=>8)E&!%
&%’添加一定量的&;: ’12 !增大12#& 的浓度!抑制-?12 转化为-?,2 %
% # % % % (
&’’喷雾方式增大硫酸小液滴与-?#@接触的表面积!加快除钡速率%
化学参考答案!第!!!!(页!共"页"&"’硝化时!发生反应*1K,2
(
@#;:
%
;2
(
"""1K&;2
(
’
#
@#;: ($@,2 #$@:
#
2"碳化时!发生反应*
1K&;2
(
’
#
@#;:
(
@,2
#
@:
#
2"""1K,2 (#@#;:
%
;2
(
!能循环利用的物质是;:
%
;2
(
%
高温
&)’高纯1K,2
(
高温分解生成1K2!1K2与.8发生置换反应*(1K2@#.8"""(1K@.8
#
2
(
%
!"0!!’分"!!";!或氮"!#分"
!#"反应体系的碱性增大#可能生成7G!2:"!#分"
#
!("#7G,2
(
@#:
#
2@:
#
2 #"""#7G!2:"
(
@#,2 #$!#分"!-?,8
#
!#分"
!%"B:太高#反应体系中7G(@浓度小$B:太低#反应体系中配体与:@结合#%,
!$
:
!#
;
#
2
*
&%&浓度小!#分"
!’"酸式滴定管!!分"!磷酸与7G(@配位形成无色配离子7G%!:52
%
"
#
&&#使反应更完全#也消除7G(@的黄
#’$
’#’$L!$&(L L’"
#’
色对判断滴定终点的影响!#分"! L!$$O!#分"
)
%试题立意&本题以!乙二胺四乙酸铁钠制备#为学科情境$考查对!第一电离能"配合物的基本概念"氧化还
原反应方程式书写"氧化还原反应滴定"实验条件的控制#的认知与理解%
%解析&&!’乙二胺四乙酸铁钠中的配位原子有;(2!其中基态;原子#B轨道半充满!难失电子!第一电离
能大%
&#’;?,2 溶液呈碱性!添加过快!会导致反应体系的碱性增大!可能生成7G&2:’%
# ( #
&(’:
#
2
#
将7G,2
(
氧化为7G&2:’
(
!反应的化学方程式为#7G,2
(
@#:
#
2@:
#
2 #"""#7G&2:’
(
@#,2 #$"
洗涤液中没有12#&!证明7G&2:’洗涤干净!选用-?,8 检验12#&%
% ( # %
&%’B:太高!反应体系中7G(@转化生成7G&2:’
(
!7G(@浓度小"B:太低!反应体系中配体中的;会优先与
:@配位!+, : ;2,%&浓度小!均不利于生成乙二胺四乙酸铁钠%
!$ !# # *
&’’高锰酸钾能氧化乳胶管!应使用酸式滴定管盛装"磷酸与7G(@配位形成无色配离子7G+&:52 ’,&!使
% #
反应更完全!也消除7G(@的黄色对判断滴定终点的影响"锌把铁离子还原为亚铁离子!酸性高锰酸钾溶液
再将亚铁离子氧化为铁离子%CR2
%
&#’7G#@反应中!消耗的高锰酸钾的物质的量为#)$L!$&(=>8!根据
电子得失守恒可知!该反应中铁离子的物质的量是’#)$L!$&(=>8!则该晶体中铁元素的质量分数的表达
#’$
’#)$L!$&(L L’"
#’
式为 L!$$O%
)
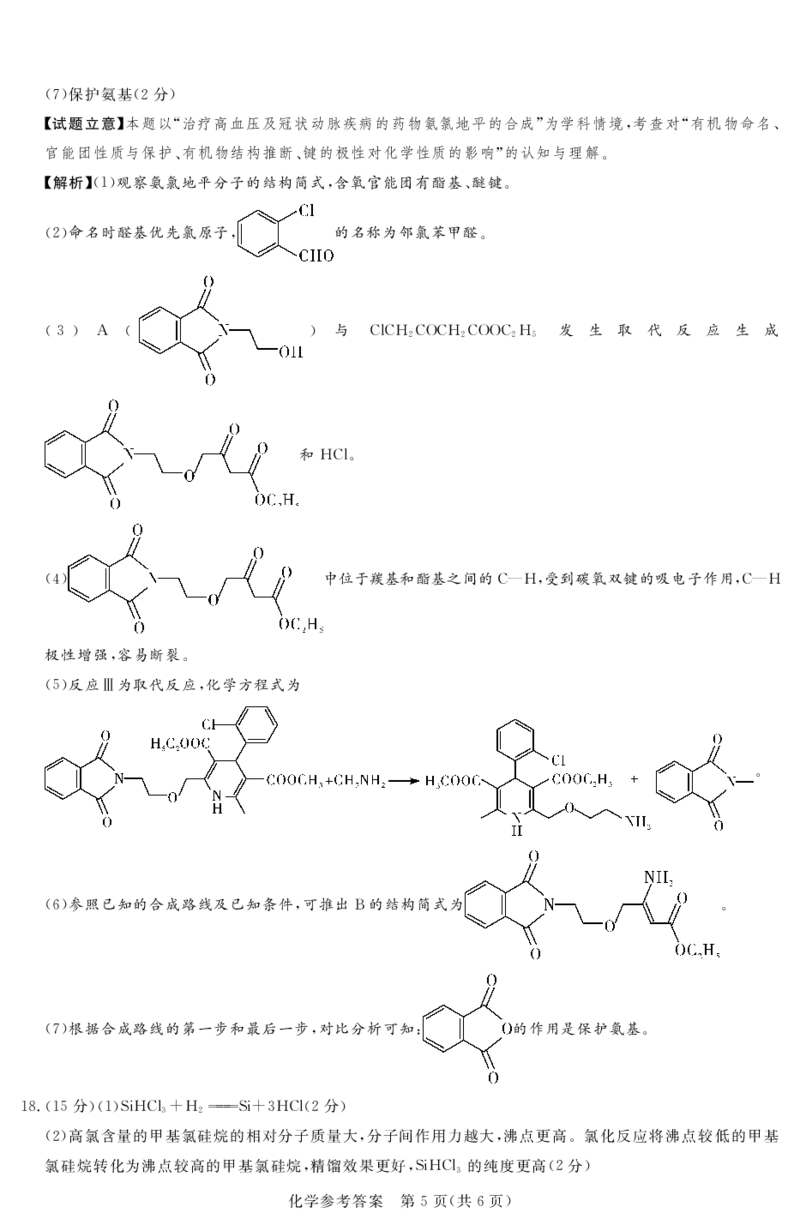
!)0!!%分"!!"酯基(醚键!#分"
!#"邻氯苯甲醛!或# 氯苯甲醛"!#分"
!("取代反应!#分"
!%"位于羰基和酯基之间的,):#受到碳氧双键的吸电子作用#,):极性增强#容易断裂!#分"
!’" !#分"
!"" !#分"
化学参考答案!第!!!!%页!共"页"!)"保护氨基!#分"
%试题立意&本题以!治疗高血压及冠状动脉疾病的药物氨氯地平的合成#为学科情境$考查对!有机物命名"
官能团性质与保护"有机物结构推断"键的极性对化学性质的影响#的认知与理解%
%解析&&!’观察氨氯地平分子的结构简式!含氧官能团有酯基(醚键%
&#’命名时醛基优先氯原子! 的名称为邻氯苯甲醛%
&(’ . & ’ 与 ,8,:,2,:,22,: 发 生 取 代 反 应 生 成
# # # ’
和:,8%
&%’ 中位于羰基和酯基之间的,-:!受到碳氧双键的吸电子作用!,-:
极性增强!容易断裂%
&’’反应%为取代反应!化学方程式为
%
&"’参照已知的合成路线及已知条件!可推出-的结构简式为 %
&)’根据合成路线的第一步和最后一步!对比分析可知* 的作用是保护氨基%
!*0!!’分"!!"1F:,8
(
@: #"""1F@(:,8!#分"
!#"高氯含量的甲基氯硅烷的相对分子质量大#分子间作用力越大#沸点更高*氯化反应将沸点较低的甲基
氯硅烷转化为沸点较高的甲基氯硅烷#精馏效果更好#1F:,8 的纯度更高!#分"
(
化学参考答案!第!!!!’页!共"页"!("避免1F:,8 与空气(水反应!合理即可"!#分"
(
!%"!增大,8
#
浓度!或适当降温或及时分离出生成物#任答一点即可"!#分"
&S!!分"!T1
#
的活化能比T1
!
的活化能小#按反应机理S反应的速率大!#分"
,8
,,
’&#""0*!#分"!(:
(
,++1F++,:
#
,8!#分"
,,
:
%试题立意&本题以!三氯硅烷生产多晶硅#为学科情境$考查对!物质制备原理"分子结构与性质"化学反应
机理"化学平衡移动"化学反应热效应定量计算#的认知与理解%
%解析&&!’:
#
还原1F:,8
(
的反应为1F:,8
(
@: #"""1F@(:,8%
&#’高氯含量的甲基氯硅烷的相对分子质量大!分子间作用力越大!沸点更高%氯化反应将沸点较低的甲基
氯硅烷转化为沸点较高的甲基氯硅烷!精馏效果更好!1F:,8 的纯度更高%
(
&(’三氯硅烷在空气中极易燃烧!与水剧烈反应!氯化反应中通入氮气的作用是避免1F:,8与空气(水反应%
(
&%’!1F:,8
(
和,8
#
按反应机理?进行反应*1F:,8
(
@,8 #"""1F,8
%
@:,8!该反应是气体分子数不变的放
热反应!通过增大,8 浓度(适当降温(及时分离出生成物等均促进平衡正向移动!提高1F:,8 的转化率"
# (
&T1
#
的活化能比T1
!
的活化能小!按反应机理S反应的速率大"’由图可知*,8
#
&D’@:)&D’""",8)&D’@
:,8&D’!)*
!
M&#$(0(UV)=>8&!!1F:,8
(
&D’@,8)&D’"""1F,8
(
)&D’@:,8&D’!)*
#
M&"(0’UV)=>8&!!
两式相加可得*1F:,8
(
&D’@,8
#
&D’@:)&D’"""1F,8
(
)&D’@#:,8&D’)*M&#""0*UV)=>8&!"
,8
,,
(&,:
(
’
#
1F:,8和,8
#
发生氯化反应!取代1F-:得到&,:
(
’
#
1F,8
#
!取代,-:得到 :
(
,++1F++,:
#
,8%
,,
:
化学参考答案!第!!!!"页!共"页"