文档内容
2024—2025 学年度上学期 2022 级
10 月月考化学试卷
命题人:张昊玥 审题人:王新姣
考试时间:2024年10月24日
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 K 39 Mn 55 Zn 65
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1.“尚义四台遗址”是中国北方地区考古发现的最早定居村落,时间最久的距今已有10000~10400
年,入围“2023年度全国十大考古新发现”终评项目名单。下列关于该发现的说法错误的是
A.可通过对动物骨骼中14C的测定确定遗址时间
B.遗址中出土的陶器属于硅酸盐产品
C.遗址中出土的动物骨骼和贝类遗物能保存至今是因为浸泡过福尔马林
D.遗址中出土的打制石器、细石器、磨制石器等的制造过程属于物理变化
2.化学创造美好生活。下列生产活动没有运用相应化学原理的是
选项 生产活动 化学原理
A 办公场所喷洒“84”消毒液消毒 NaClO有强氧化性,能使蛋白质变性
B 利用红薯制葡萄糖 淀粉在催化剂作用下发生水解反应
长途运输菠萝时,将其放置在盛装浸有酸
C 酸性高锰酸钾溶液吸收乙烯
性高锰酸钾溶液的硅藻土的容器中
D 用Na O 作呼吸面具的氧气来源 Na O 能分解生成O
2 2 2 2 2
3.“嫦娥六号”的返回展现了我国强大的实力。下列说法正确的是
A.运载火箭采用液氧和煤油作为推进剂,液氧与臭氧互为同素异形体
B.氢氧燃料电池生成H O,H O的空间填充模型为
2 2
C.太阳能电池板使用的晶体硅为分子晶体
D.月壤样本中含有3He的质子数为3
4.酪氨酸在人体内的一种非正常代谢过程如图所示。下列说法不正确的是
A.尿黑酸能形成分子内氢键
B.1mol尿黑酸最多可与含3molBr 的溴水反应
2
C.酪氨酸能发生加成、取代、消去和加聚反应
D.对羟基苯丙酮酸分子中所有碳原子可能在同一平面5.下列方案设计、现象和结论均正确的是
选项 实验目的 方案设计 现象和结论
探究碳酸钠溶液 取2.0mL0.lmol/LNa CO 溶液,滴入酚酞溶液变红,再滴入
2 3
A 碱性是CO 2-水解 滴入3滴酚酞,观察现象,再 BaCl 后出现白色沉淀,溶液颜色
3 2
导致 滴入3滴lmol/LBaCl 溶液 变浅
2
将淀粉和稀硫酸混合加热一
产生红色沉淀,淀粉水解为葡萄
B 探究淀粉的水解 段时间后,再加入新制的
糖
Cu(OH) 加热
2
探究电解质的强 用pH计测量醋酸溶液、盐酸 盐酸的pH小,CH COOH是弱电
3
C
弱 的pH, 解质
探究酸性氧化物 有白色沉淀生成,生成了BaSO
D 将SO 通入BaCl 溶液 3
和盐的反应 2 2 沉淀
SiHCl
6.三氯甲硅烷( 3)是制取高纯硅的重要原料,常温下为
无色液体,沸点为31.8℃,熔点为-126.5℃,易水解。实
Δ
Si3HCl SiHCl H
3 2
验室根据反应 ,利用下图装置制备
SiHCl
3粗品(加热及夹持装置略)。下列说法正确的是
SiHCl
A.制备 3的第一步操作是通入HCl气体
B.将球形冷凝管改为直形冷凝管冷凝效果更佳
C.C和D之间需要加一个干燥装置
SiHCl 3NaOHSiHCl 3NaClSiO H OH
D.用NaOH溶液吸收 3的化学方程式为 3 2 2 2
7.三甲基镓[(CH ) Ga]是应用最广泛的一种金属有机化合物,可通过如下反应制备:
3 3
GaCl CH Al CH GaAlCl
3 3 3 3 3 3。下列说法错误的是
A.Al原子的核外电子有13种空间运动状态
B.(CH ) Ga中Ga原子的杂化方式为sp2
3 3
C.AlCl 常以二聚体(Al Cl )形式存在,二聚体中各原子均满足8电子结构
3 2 6
D.Al的第一电离能比同周期相邻元素小
8.部分含N及Cl物质的分类与相应化合价关系如
图所示,下列推断不合理的是
A.对应含氧酸的酸性强弱为e´>e
B.工业上通过a→b→c→d→e来制备HNO
3
C.c´能使有色鲜花褪色
D.利用a还原c或者d可消除氮氧化物的污染9.含有某化合物(结构如图所示)的复方制剂具有清热解毒、消肿止
痛的功效。四种短周期元素X、Y、Z、W的原子序数依次增
大,并且它们的价电子数之和为11,下列说法错误的是
A.Y原子和Z原子的杂化方式不完全相同
B.电负性:Z>X>Y>W
C.与Z同周期的元素中,第一电离能比Z小的有5种
D.X、Y、W可形成含离子键和配位键的化合物
10.不能正确表示下列反应的离子方程式的是
A.将NO 通入NaOH溶液中:2NO +2OH-=NO -+NO -+H O
2 2 3 2 2
B.硫化钠溶液加入过量亚硫酸:2S2-+5H SO =3S↓+3H O+4HSO -
2 3 2 3
C.将浓氨水滴入AgCl沉淀中:2NH •H O+AgCl=[Ag(NH ) ]++2H O+Cl-
3 2 3 2 2
D.NaOH溶液溶解Al O :Al O +2OH-+2H O=2[Al(OH) ]-
2 3 2 3 2 4
11.含NO烟气需要处理后才能排放。现有两种方法处理NO烟气:
方法Ⅰ.酸性条件下,用NaClO 作氧化剂将NO氧化为NO -。若加入Fe3+,则NO的氧化率
2 3
更高。
方法Ⅱ.在钒基催化剂作用下发生脱硝反应,机理如图所示:
下列说法错误的是
A.方法Ⅰ中氧化剂与还原剂的物质的量之比为4:3
B.方法Ⅰ中加入Fe3,氧化率更高的原因可能是产生氧化性更强
的ClO
2
催化剂
C.方法Ⅱ总反应的化学方程式为4NH 4NOO 4N 6H O
3 2 2 2
D.反应过程中V5 O被还原
12.某兴趣小组在实验室模拟侯氏制碱法制备NaHCO ,部分实验装置如图,下列说法正确的是
3
A.实验过程中向启普发生器中添加液体时,可以取下Ⅰ处胶塞加入
B.所用试剂有稀硫酸、浓硫酸、CaCO 、饱和食盐水、NH Cl、Ca(OH) 、蒸馏水
3 4 2
C.开始实验时,应先打开活塞Ⅱ,再打开活塞Ⅲ
D.试剂d为冰水,以降低NaHCO 的溶解度,促进晶体的析出
313.某固体混合物可能含有Al、(NH ) SO 、MgCl 、AlCl 、FeCl 、NaCl中的一种或几种,现对
4 2 4 2 3 2
该混合物做如图实验,所得现象和有关数据如图(气体体积均已换算成标准状况下的体积)。下
列说法错误的是
A.“步骤①”中发生了反应2Al+2NaOH+6H O=2Na[Al(OH) ]+3H ↑
2 4 2
B.“步骤②”和“步骤③”中反应消耗的H+的物质的量之比大于1:3
C.混合物中一定含有Al、(NH ) SO 、MgCl 、NaCl,不含AlCl
4 2 4 2 3
D.混合物中一定不含有FeCl ,可能含有NaCl和AlCl
2 3
14.铋酸钠(NaBiO )是一种强氧化剂,微溶于水。以泡铋矿[主要成分是(BiO) CO ,含SiO 等杂质]
3 2 3 2
为原料制备铋酸钠的流程如图所示。下列叙述错误的是
A.将滤液1和滤液2合并后加入适量盐酸,可得到NaCl溶液
B.“酸浸”时发生反应(BiO) CO +6HCl=2BiCl +CO ↑+3H O
2 3 3 2 2
C.分离得到NaBiO 的操作是蒸发浓缩、降温结晶、过滤、洗涤、干燥
3
D.“氧化”时发生反应的离子方程式:Bi(OH) +Cl +3OH-+Na+=NaBiO +2Cl-+3H O
3 2 3 2
15.硫酸亚铁铵晶体,又称摩尔盐,是分析化学中重要的基准物质,其化学式可表示为
(NH ) Fe(SO ) •xH O 。为测定其结晶水含量并进一步探究其在惰性气体氛围中的热分解反应
4 2 4 2 2
过程,现取一定质量的摩尔盐晶体做热重分析,绘制出如下的热重曲线。
剩余固体质量
已知:①TG 100%
原样品质量
②摩尔盐在580℃下完全分解,得到红棕色固体
则下列说法正确的是
A.用KSCN溶液检验摩尔盐中的金属阳离子
B.x=6
C.用湿润的红色石蕊试纸检验205~420℃间分解
产生的气体,试纸变蓝
D.0~580℃发生的化学方程式为:
580℃
4NH FeSO xH OO 8NH 2Fe O 8SO +x+4H O
4 2 4 2 2 2 3 2 3 3 2
二、非选择题(本题包括4个小题,共55分)16(13分).以湿法炼锌厂所产的钴锰渣(主要成分为Co O 、CoO、NiO、MnO ,含少量Fe O 、
2 3 2 2 3
ZnO、CuO、CaO等)为原料回收制备CoC O 的工艺如下:
2 4
K CuS=1.310-36 K CuOH =2.210-20 K ZnS=1.310-24
已知:常温下, sp , sp 2 , sp 。
回答下列问题:
(1)“酸浸”时可能产生有毒气体 ,说出该气体的一种用途 。
(2)若K
2
S溶液的pH=13,试分析Cu2 主要以 [填“CuS”或“
CuOH
2”]形式除去,通过计
算说明你的理由 。
MnO MnO
(3)“滤渣3”中含有S、 2,写出得到 2的化学方程式 。
(4)P204、P507对金属离子的萃取率与pH的关系如图所示。
①直接用于分离钴镍的萃取剂是 。
②“萃余液2”中的主要成分为 (填化学式),指出分离钴镍的合适pH范围为 (填标
号)。
A.3~4 B.4~5 C.5~6 D.6~7
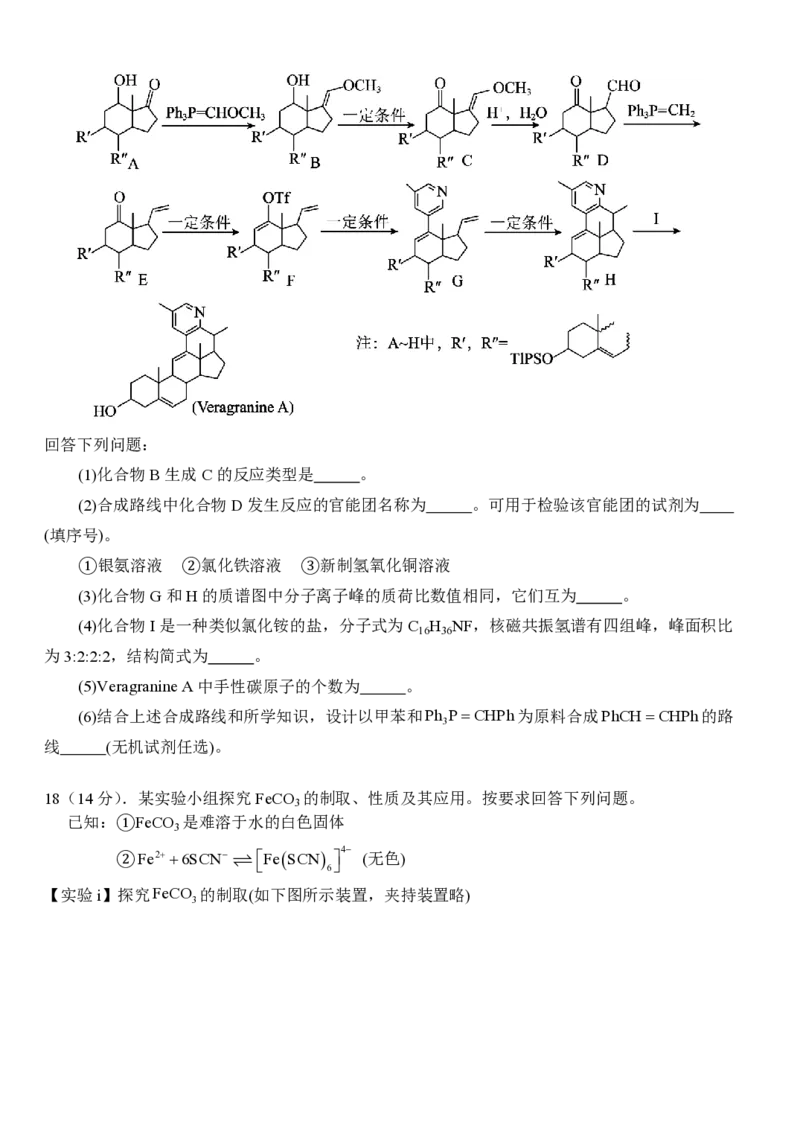
17(14分).Veragranine A是治疗骨关节疼痛的药物,一种合成路线如图(Ph为苯基,略去部分试
剂和条件,忽略立体化学)。回答下列问题:
(1)化合物B生成C的反应类型是 。
(2)合成路线中化合物D发生反应的官能团名称为 。可用于检验该官能团的试剂为
(填序号)。
①银氨溶液 ②氯化铁溶液 ③新制氢氧化铜溶液
(3)化合物G和H的质谱图中分子离子峰的质荷比数值相同,它们互为 。
(4)化合物I是一种类似氯化铵的盐,分子式为C H NF,核磁共振氢谱有四组峰,峰面积比
16 36
为3:2:2:2,结构简式为 。
(5)Veragranine A中手性碳原子的个数为 。
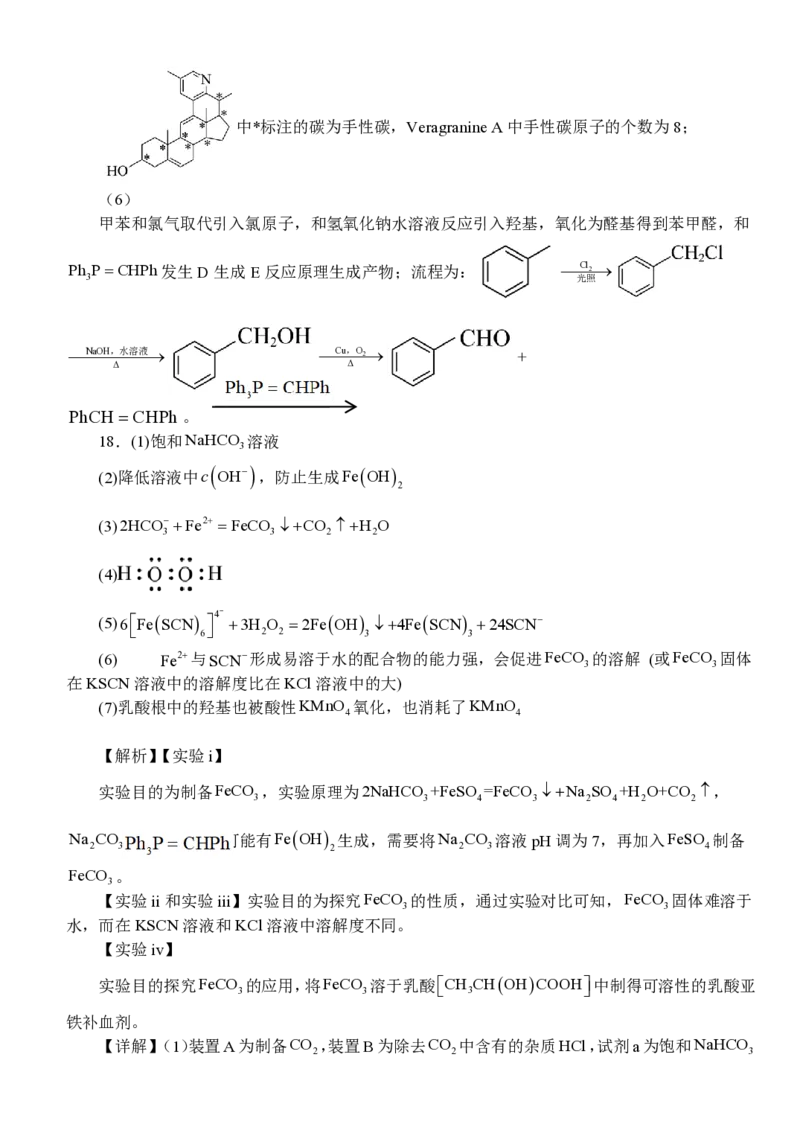
(6)结合上述合成路线和所学知识,设计以甲苯和Ph PCHPh为原料合成PhCHCHPh的路
3
线 (无机试剂任选)。
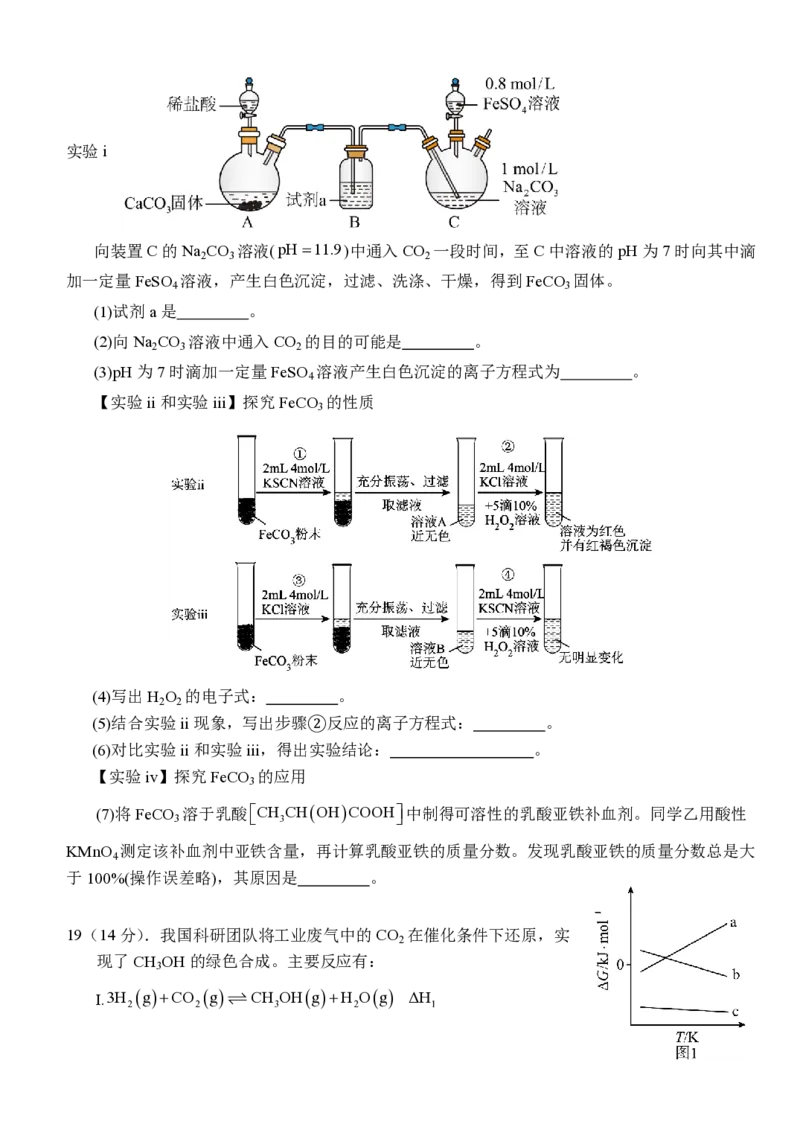
18(14分).某实验小组探究FeCO 的制取、性质及其应用。按要求回答下列问题。
3
已知:①FeCO 是难溶于水的白色固体
3
②Fe2 6SCN FeSCN 4 (无色)
6
【实验i】探究FeCO 的制取(如下图所示装置,夹持装置略)
3实验i
向装置C的Na CO 溶液(pH11.9)中通入CO 一段时间,至C中溶液的pH为7时向其中滴
2 3 2
加一定量FeSO 溶液,产生白色沉淀,过滤、洗涤、干燥,得到FeCO 固体。
4 3
(1)试剂a是 。
(2)向Na CO 溶液中通入CO 的目的可能是 。
2 3 2
(3)pH为7时滴加一定量FeSO 溶液产生白色沉淀的离子方程式为 。
4
【实验ii和实验iii】探究FeCO 的性质
3
(4)写出H O 的电子式: 。
2 2
(5)结合实验ii现象,写出步骤②反应的离子方程式: 。
(6)对比实验ii和实验iii,得出实验结论: 。
【实验iv】探究FeCO 的应用
3
(7)将FeCO
3
溶于乳酸
CH
3
CHOHCOOH
中制得可溶性的乳酸亚铁补血剂。同学乙用酸性
KMnO 测定该补血剂中亚铁含量,再计算乳酸亚铁的质量分数。发现乳酸亚铁的质量分数总是大
4
于100%(操作误差略),其原因是 。
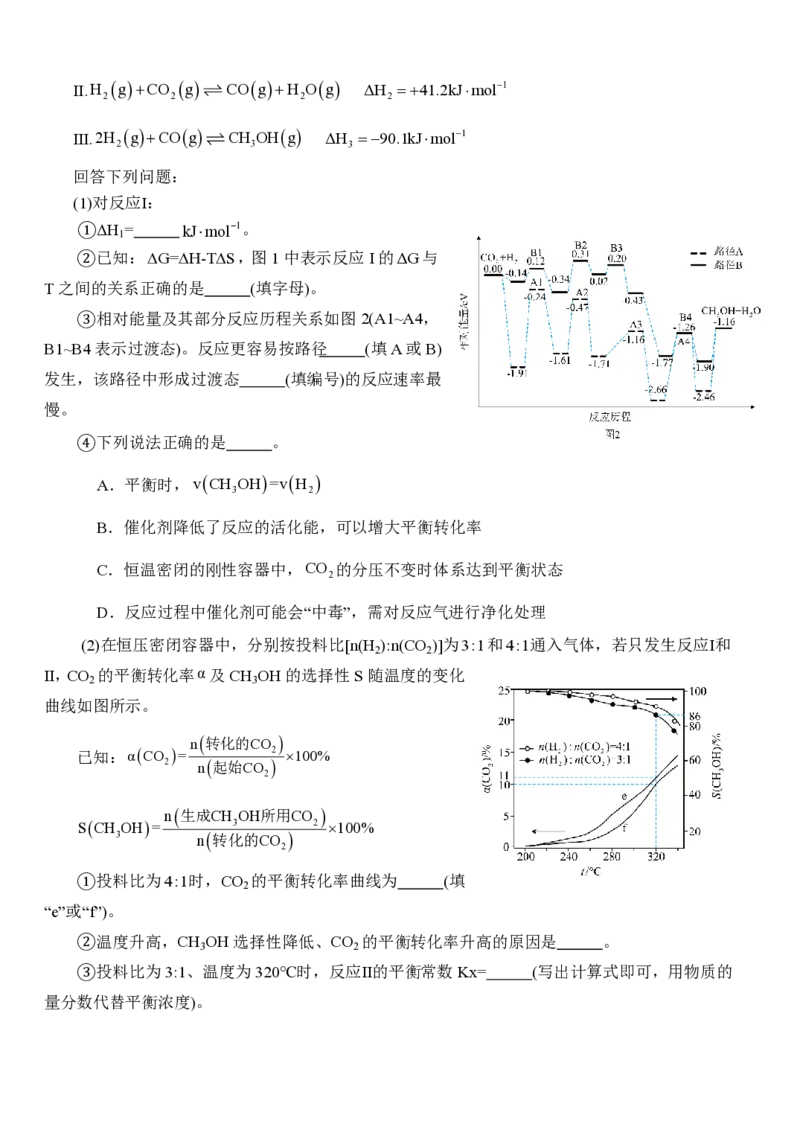
19(14分).我国科研团队将工业废气中的CO 在催化条件下还原,实
2
现了CH OH的绿色合成。主要反应有:
3
Ⅰ.3H
2
gCO
2
g
CH
3
OHgH
2
Og ΔH
1Ⅱ.H
2
gCO
2
g
COgH
2
Og ΔH
2
41.2kJmol1
Ⅲ.2H
2
gCOg
CH
3
OHg ΔH
3
90.1kJmol1
回答下列问题:
(1)对反应Ⅰ:
①ΔH = kJmol1。
1
②已知:G=H-TS,图1中表示反应I的ΔG与
T之间的关系正确的是 (填字母)。
③相对能量及其部分反应历程关系如图2(A1~A4,
B1~B4表示过渡态)。反应更容易按路径 (填A或B)
发生,该路径中形成过渡态 (填编号)的反应速率最
慢。
④下列说法正确的是 。
A.平衡时,vCH OH=vH
3 2
B.催化剂降低了反应的活化能,可以增大平衡转化率
C.恒温密闭的刚性容器中,CO 的分压不变时体系达到平衡状态
2
D.反应过程中催化剂可能会“中毒”,需对反应气进行净化处理
(2)在恒压密闭容器中,分别按投料比[n(H ):n(CO )]为3:1和4:1通入气体,若只发生反应Ⅰ和
2 2
Ⅱ,CO 的平衡转化率α及CH OH的选择性S随温度的变化
2 3
曲线如图所示。
n转化的CO
已知:αCO = 2 100%
2 n起始CO
2
n生成CH OH所用CO
SCH OH= 3 2 100%
3 n转化的CO
2
①投料比为4:1时,CO 的平衡转化率曲线为 (填
2
“e”或“f”)。
②温度升高,CH OH选择性降低、CO 的平衡转化率升高的原因是 。
3 2
③投料比为3:1、温度为320℃时,反应Ⅱ的平衡常数Kx= (写出计算式即可,用物质的
量分数代替平衡浓度)。高三年级第二次周练化学答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C D A C A C A B C D
题号 11 12 13 14 15
答案 A D D C B
1.【详解】A.可通过对动物骨骼中14C的测定确定遗址时间,A正确;
B.遗址中出土的陶器属于硅酸盐产品,B正确;
C.10000~10400年之前,没有福尔马林,C错误;
D.遗址中出土的打制石器、细石器、磨制石器等的制造过程属于物理变化,D正确;
故选C。
2.【详解】A.NaClO有强氧化性,能使蛋白质氧化变性从而杀灭病毒,故A正确;
B.红薯的主要成分是淀粉,淀粉在催化剂作用下发生水解反应生成葡萄糖,故B正确;
C.菠萝成熟时会释放催熟剂乙烯,用酸性高锰酸钾溶液吸收乙烯可以起到保鲜的作用,故C
正确;
D.Na O 可与CO 反应生成Na CO 和O2,故用Na O 作呼吸面具的氧气来源,故D错误;
2 2 2 2 3 2 2
答案选D。
3.【详解】A.液氧和O 都是由同种元素形成的不同单质,二者属于同素异形体,A正确;
3
B.H O空间构型是V形 ,B错误;
2
C.晶体硅属于共价晶体,C错误;
D.3He的质量数为3,质子数为2,D错误;答案选A。
4.【详解】A.尿黑酸分子中,有1个酚羟基与羧基位于苯环的邻位,二者间能形成分子内氢
键,A正确;
B.尿黑酸分子中,苯环上存在3个邻位H原子,可被Br 取代,则1mol尿黑酸最多可与含
2
3molBr 的溴水反应,B正确;
2
C.酪氨酸分子中的苯基能发生加成反应和取代反应,但酪氨酸分子不能发生消去和加聚反应,
C不正确;
D.对羟基苯丙酮酸分子中,所有碳原子连接的碳原子都不超过2个,则所有碳原子可能在同
一平面上,D正确;故选C。
5.【详解】A.CO2和Ba2+反应生成BaCO3沉淀,溶液中CO2浓度减小,CO2水解平衡逆
3 3 3
向移动,溶液中OH-度减小,碱性减弱,溶液颜色变浅,可验证碳酸钠溶液碱性是CO2水解导致,
3
A项正确;
B.应在碱性条件下加入新制的Cu(OH) ,检验水解产物,淀粉和稀硫酸混合加热一段时间后,
2
溶液显酸性,加入新制的Cu(OH) 加热不会生成砖红色沉淀,B项错误;
2
C.醋酸溶液、盐酸的浓度未知,不能通过测定pH比较电解质的强弱,C项错误;D.SO 和BaCl 溶液不反应,D项错误;答案选A。
2 2
6.【详解】A.制备SiHCl 的第一步操作是检查装置的气密性,A错误;
3
B.球形冷凝管冷凝回流比直形冷凝管效果好,B错误;
C.SiHCl 易水解,所以要在C、D之间加一个干燥装置,防止D中的水蒸气进入蒸馏烧瓶中,
3
使SiHCl 水解,C正确;
3
D.用NaOH溶液吸收SiHCl 的化学方程式为
3
5NaOHSiHCl 3NaClNa SiO 2H OH ,D错误;
3 2 3 2 2
故答案选C。
7.【详解】A.Al原子的核外电子有13个电子,占据7个轨道,有7种空间运动状态,A错
误;B.(CH ) Ga中Ga原子的价层电子对是3,杂化方式为sp2 ,B正确;
3 3
C.AlCl 常以二聚体Al Cl 形式存在 ,二聚体中各原子均满足8电
3 2 6
子结构,C正确;D.Al的第一电离能比镁小,因为镁3S能级处于全满,比铝要大,所以Al的
第一电离能比同周期相邻元素小,D正确; 故选A。
8. 【详解】A.硝酸和高氯酸都是相应元素的最高价酸,最高价酸的酸性和非金属性相关,
非金属性越强,最高价酸的酸性越强,非金属性Cl>N,所以酸性:HClO >HNO ,故A合理;
4 3
B.工业上制备硝酸,首先发生的是氨的催化氧化,即氨被氧气氧化为NO,然后NO再被氧化为
NO ,最后NO 和水反应生成HNO 和NO,NO可以循环使用,即工业上是通过制备硝酸,不经
2 2 3
过氮气这一步,故B不合理;C.d'为NO ,与水反应产生的硝酸具有强氧化性,能使有色鲜花褪
2
色,故C合理;D.NH 中N为-3价,NO和NO 中N的化合价为正价,NH 和NO或NO 反应
3 2 3 2
时,都可以发生归中反应生成氮气和水,可以用氨还原NO或NO 消除氮氧化物的污染,故D合
2
理;答案选B。
9. 【详解】A.化合物中,B原子形成3个或4个σ键,杂化方式分别为sp2、sp3,O的杂
化方式为sp3,A正确;B.同周期,从左到右,电负性增大;同族,从上到下,主族电负性减小;
元素的电负性:O>H>B>Na,B正确;C.第三周期,第一电离能比O小的有Li、Be、B、C,
4种元素,C错误;D.X、Y、W可以形成NaBH ,NaBH 为离子化合物,含有离子键、极性共
4 4
价键和配位键,故D正确;答案选C。
10.【详解】A.将NO 通入NaOH溶液中,生成可溶的亚硝酸钠和硝酸钠,选项所给离子方
2
程式正确,A正确;B.硫化钠中的硫元素为-2价,亚硫酸中的硫元素为+4价,两者反应生成硫
单质,由于亚硫酸过量,生成亚硫酸氢根,选项所给离子方程式正确,B正确;C.银离子和氨可
以形成[Ag(NH ) ]+离子,配合物离子较稳定,可以通过平衡移动将氯化银沉淀溶解,选项所给离
3 2
子方程式正确,C正确;D.氧化铝是两性氧化物,可以溶于强碱,选项所给离子方程式配平不正
确,正确的离子方程式为Al O +2OH−+3H O=2[Al(OH) ]−,D错误;
2 3 2 4
本题选D。
11.【详解】A.方法Ⅰ中,NaClO 中Cl元素化合价由+3降低至-1,作氧化剂,NO中N元素
2
化合价由+2升高至NO中的+5价,作还原剂,根据化合价升降守恒可知氧化剂与还原剂的物质的
3
量之比为3:4,故A项错误;B.方法Ⅰ中加入Fe3,可将NaClO 氧化为ClO ,氯元素化合价更
2 2
高,氧化性更强,故B项正确;C.由图可知,方法Ⅱ中加入反应物为NH 、O 、NO,产出的生
3 2成物为H O、N ,由于不确定各物质的比例,根据化合价升降守恒可知反应方程式为
2 2
催化剂 催化剂
4NH 4NOO 4N 6H O或4NH 2NO2O 3N 6H O等,故C项正确;D.反
3 2 2 2 3 2 2 2
应过程中V5 O转化为NONH V4 OH,V元素化合价降低被还原,故D项正确;综上所述,
2
错误的是A项。
12. 【详解】A.实验过程中向启普发生器中添加液体时,应从球形漏斗加入,A项错误;
B.制备CO 应使用稀盐酸不应使用稀硫酸,生成的CO 无需干燥,NH Cl和Ca(OH) 用于制取
2 2 4 2
NH ,尾气中含有NH ,可用稀硫酸吸收,B项错误;C.因NH 溶解度大,开始实验时应先打开
3 3 3
活塞Ⅲ,再打开活塞Ⅱ,C项错误;D.反应结束后将锥形瓶放入冰水浴中可以降低NaHCO 的溶
3
解度,促进NaHCO 晶体的析出,D项正确;故选:D。
3
13. 【详解】A.“步骤①”中涉及铝与氢氧化铝反应,发生了反应
2Al2NaOH2H O=2NaAlO 3H ,选项A正确;
2 2 2
B.“步骤②”为H++OH-=H O和AlO-+H++H O=Al(OH) ,“步骤③”为
2 2 2 3
Al(OH) 3H+=Al3++3H O,二者反应消耗的H的物质的量之比因过量氢氧根离子过量而大于1:3,
3 2
选项B正确;
C.根据分析可知,混合物中一定含有Al、NH SO 、MgCl 、NaCl,不含有AlCl ,选项
4 2 4 2 3
C正确;
D.混合物中一定不含有FeCl 和AlCl ,含有NaCl ,选项D错误;
2 3
14. 【详解】A.滤液1的溶质是NaCl和NaOH,滤液2的溶质是NaCl和NaOH,两滤液
合并后加入适量盐酸可得到NaCl溶液,故A项正确;B.“酸浸”时(BiO) CO 与盐酸反应生成氯
2 3
化铋、二氧化碳和水,选项中的化学方程式正确,故B项正确;C.NaBiO 微溶于水,过滤即可
3
得到产品NaBiO ,故C项错误;D.“氧化”时发生氧化还原反应,生成NaBiO 、NaCl和H O,
3 3 2
选项中离子方程式正确,故D项正确;故本题选C。
15.【详解】A.摩尔盐中含有的是亚铁离子,不能使用KSCN溶液检验,A错误;B.摩尔
盐在580℃下完全分解,得到红棕色固体为氧化铁,设NH FeSO xH O为1mol,则根据铁
4 2 4 2 2
元素守恒可知,氧化铁为0.5mol,质量为80g,由图可知,最终
TG1-9.2%-9.2%-9.2%-52.0%=20.4%,则最初摩尔盐为 80g÷20.4%=392g,相对分子质量为 392,
则通过相对分子质量可知:x=6,B正确;C.加热首先失去结晶水,失去六个结晶水,则失重
618
100%27.6%,则205~420℃间分解产生的气体为水,不能使湿润的红色石蕊试纸变蓝,C
392
错误;D.实验探究其在惰性气体氛围中的热分解反应过程,无氧气参与,D错误;答案选B。
16.(1) SO 食品添加剂(如用于葡萄酒)、作漂白剂、制硫酸
2
(2) CuS CuOH s+S2-aq=CuSs+2OH-aq
2K=
K
sp
CuOH
2
=
2.210-20
=1.71016>105反应进行彻底,故Cu2主要以CuS形式除去
K CuS 1.310-36
sp
(3)H SO +MnSO +2CoOH =MnO +2CoSO +4H O
2 4 4 3 2 4 2
(4) P507 NiSO B
4
【详解】(1)“酸浸”时,稀硫酸、K SO 发生反应,可能产生有毒气体SO ,该气体的一种用
2 3 2
途为:制硫酸、食品添加剂(如葡萄酒)、漂白剂(任写一种)。
(2)K CuSc Cu2 c S2 1.31036,
sp
K CuOH c Cu2 c2 OH 2.21020,对于平衡:
sp
2
CuOH sS2aq CuSs2OHaq,平衡常数:
2
c2 OH c2 OH c Cu2 K CuOH
K
sp
2
1.71016>105,反应进行彻底,所以Cu2主要
c S2 c S2 c Cu2 K CuS
sp
以CuS形式除去;
(3)“滤渣 3”中,Mn2+转化为MnO ,Co(OH) 转化为Co2+,依据得失电子守恒,化学方程
2 3
式:H SO +MnSO +2CoOH MnO +2CoSO +4H O;
2 4 4 3 2 4 2
(4)①从图中可以看出,在P204中,相同pH时,Co2+和Ni2+的萃取率非常接近,而在P507
中,二者相同萃取率时的pH相差较大,所以直接用于分离钴、镍的萃取剂是P507;
②根据分析可知,“萃余液2”中的主要成分为NiSO ;分析图中曲线,分离钴、镍的合适pH
4
范围为4~5,故选B。
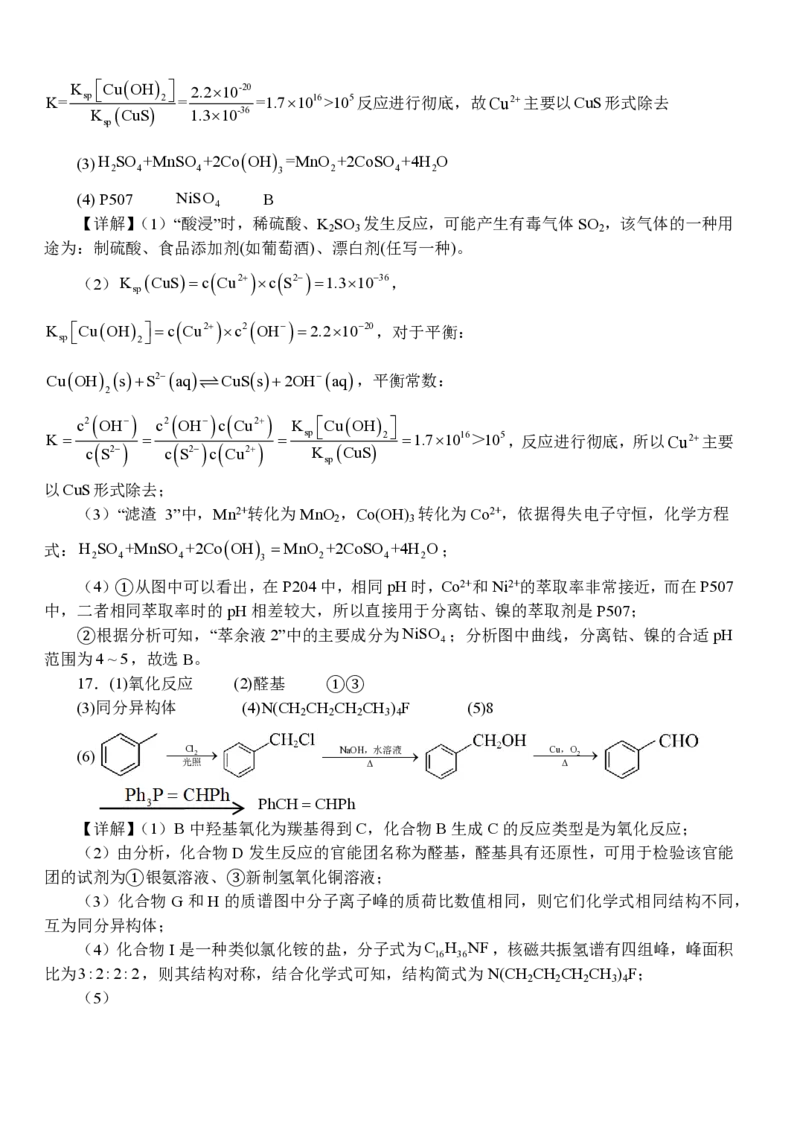
17.(1)氧化反应 (2)醛基 ①③
(3)同分异构体 (4)N(CH CH CH CH ) F (5)8
2 2 2 3 4
(6) Cl2 NaOH,水溶液 Cu,O2
光照 Δ Δ
PhCHCHPh
【详解】(1)B中羟基氧化为羰基得到C,化合物B生成C的反应类型是为氧化反应;
(2)由分析,化合物D发生反应的官能团名称为醛基,醛基具有还原性,可用于检验该官能
团的试剂为①银氨溶液、③新制氢氧化铜溶液;
(3)化合物G和H的质谱图中分子离子峰的质荷比数值相同,则它们化学式相同结构不同,
互为同分异构体;
(4)化合物I是一种类似氯化铵的盐,分子式为C H NF,核磁共振氢谱有四组峰,峰面积
16 36
比为3:2:2:2,则其结构对称,结合化学式可知,结构简式为N(CH CH CH CH ) F;
2 2 2 3 4
(5)中*标注的碳为手性碳,Veragranine A中手性碳原子的个数为8;
(6)
甲苯和氯气取代引入氯原子,和氢氧化钠水溶液反应引入羟基,氧化为醛基得到苯甲醛,和
Ph PCHPh发生D生成E反应原理生成产物;流程为: Cl2
3 光照
NaOH,水溶液 Cu,O2 +
Δ Δ
PhCH CHPh 。
18.(1)饱和NaHCO 溶液
3
(2)降低溶液中c OH ,防止生成FeOH
2
(3)2HCOFe2 FeCO CO H O
3 3 2 2
(4)
(5)6FeSCN
4
3H O 2FeOH 4FeSCN 24SCN
6 2 2 3 3
(6) Fe2与SCN形成易溶于水的配合物的能力强,会促进FeCO 的溶解 (或FeCO 固体
3 3
在KSCN溶液中的溶解度比在KCl溶液中的大)
(7)乳酸根中的羟基也被酸性KMnO 氧化,也消耗了KMnO
4 4
【解析】【实验i】
实验目的为制备FeCO ,实验原理为2NaHCO +FeSO =FeCO Na SO +H O+CO ,
3 3 4 3 2 4 2 2
Na CO 溶液显碱性,可能有FeOH 生成,需要将Na CO 溶液pH调为7,再加入FeSO 制备
2 3 2 2 3 4
FeCO 。
3
【实验ii和实验iii】实验目的为探究FeCO 的性质,通过实验对比可知,FeCO 固体难溶于
3 3
水,而在KSCN溶液和KCl溶液中溶解度不同。
【实验iv】
实验目的探究FeCO 的应用,将FeCO 溶于乳酸CH CHOHCOOH中制得可溶性的乳酸亚
3 3 3
铁补血剂。
【详解】(1)装置A为制备CO ,装置B为除去CO 中含有的杂质HCl,试剂a为饱和NaHCO
2 2 3溶液,CO 在饱和NaHCO 溶液中不溶解,HCl与NaHCO 能反应而被除去;
2 3 3
故答案为:饱和NaHCO 溶液;
3
(2)Na CO 溶液显碱性,与FeSO 反应会有FeOH 生成,向Na CO 溶液中通入CO 的目
2 3 4 2 2 3 2
的为降低溶液中c OH ,防止生成FeOH ;
2
故答案为:降低溶液中c OH ,防止生成FeOH ;
2
(3)通入CO 一段时间,Na CO +CO +H O=2NaHCO ,溶液的pH为7时,溶液主要成分
2 2 3 2 2 3
为NaHCO ,故加入FeSO 发生反应为2NaHCO +FeSO =FeCO Na SO +H O+CO ,离子方
3 4 3 4 3 2 4 2 2
程式为2HCOFe2 FeCO CO H O;
3 3 2 2
故答案为:2HCOFe2 FeCO CO H O;
3 3 2 2
(4)H O 结构中含有HO、OO共价键,电子式为 ;
2 2
故答案为: ;
(5)由已知②Fe2 6SCN FeSCN 4 可知,实验ii中FeCO 粉末中加入4mol/LKSCN
6 3
溶液后,过滤得到的溶液A中含有FeSCN 4 ,滴入H O 溶液后溶液变红色,说明生成Fe3
6 2 2
与SCN结合,有红褐色沉淀,说明有FeOH 生成,故离子反应方程式为
3
6FeSCN
4
3H O 2FeOH 4FeSCN 24SCN;
6 2 2 3 3
故答案为:6FeSCN
4
3H O 2FeOH 4FeSCN 24SCN;
6 2 2 3 3
(6)对比实验ii和实验iii,实验iiFeCO 粉末中加入4mol/LKSCN溶液后,过滤得到的溶液
3
A,滴入H O 溶液后溶液变红色并有红褐色沉淀,说明溶液A中含有FeSCN 4 ,FeCO 粉末
2 2 6 3
在KSCN溶液中溶解度较大,实验iiiFeCO 粉末中加入4mol/LKCl溶液后,过滤得到的溶液B,
3
滴入KSCN溶液及H O 溶液后溶液无现象,说明溶液B中不含有Fe2+,FeCO 粉末在KCl溶液中
2 2 3
难溶,故得出实验结论:Fe2与SCN形成易溶于水的配合物的能力强,会促进FeCO 的溶解;
3
FeCO 固体在KSCN溶液中的溶解度比在KCl溶液中的大;
3
故答案为:Fe2与SCN形成易溶于水的配合物的能力强,会促进FeCO 的溶解;FeCO 固体
3 3
在KSCN溶液中的溶解度比在KCl溶液中的大;
(7)同学乙用酸性KMnO 测定该补血剂中亚铁含量,原理为
4
MnO5Fe2 8H=Mn2+5Fe3 4H O,根据消耗的KMnO 的物质的量计算Fe2的物质的量,
4 2 4再计算乳酸亚铁的质量分数,但忽略了CH CHOHCOO结构中含有羟基,羟基也能被KMnO
3 4
氧化而消耗KMnO ,消耗的KMnO 的物质的量增大,使计算乳酸亚铁的质量分数大于100%;
4 4
故答案为:乳酸根中的羟基也被酸性KMnO 氧化,也消耗了KMnO 。
4 4
19.(1) 48.9 a B B2 CD
(2) e 反应Ⅰ是放热反应,反应Ⅱ是吸热反应,当温度升高,反应Ⅰ逆向移动,反应Ⅱ正
0.10.014
向移动,反应Ⅱ正向移动的程度大于反应Ⅰ逆向移动的程度
0.92.728
【详解】(1)①根据盖斯定律,对反应Ⅰ=反应Ⅱ+反应Ⅲ,
ΔH =ΔH +ΔH =41.2-90.1=-48.9kJ/mol。
1 2 3
②G=H-TS,反应ⅠS<0,H<0,随温度升高,G增大,故正确的是a;
③A1~A4,B1~B4,路径B活动化能小,反应更容易按路径B发生;B1到B2的能量壁垒最
大,反应速率最慢;
④A.未标注正逆反应,平衡时,正逆反应速率相等,且不同物质表示化学反应速率与化学计量数
成正比,A错误
B.催化剂降低了反应的活化能,不能影响化学平衡移动,B错误;
C.恒温密闭的刚性容器中,CO 的分压是变量,当平衡时,分压不不变,C正确;
2
D.反应过程中催化剂可能会“中毒”而失效,需对反应气进行净化处理,D正确;
故选CD;
(2)①相同条件下,投料比为4:1时比3:1正向移动,CO 转化率增加,CO 的平衡转化率
2 2
曲线为e;
②反应Ⅰ是放热反应,反应Ⅱ是吸热反应,当温度升高,反应Ⅰ逆向移动,反应Ⅱ正向移动,反
应Ⅱ正向移动的程度大于反应Ⅰ逆向移动的程度,从而导致CH OH选择性降低、CO 的平衡转化率
3 2
升高;
③投料比为3:1、温度为320℃时,反应ⅡH
2
gCO
2
g
COgH
2
Og,设反应nH
2
=3mol,nCO =1mol,设转化了nCO =1mol×10%=0.1mol,SCH OH =86%,则
2 2 3
nCH OH=0.086mol,列三段式:
3
3H g + CO g CH OHg + H Og
2 2 3 2
起始(mol) 3 1 0 0
,
转化(mol) 0.258 0.086 0.086 0.086
平衡(mol) 2.728 0.9 0.086 0.1H g CO g COg H Og nH O nCO
2 2 2 2
起始(mol) 3 1 0 0 n n 0.10.014
,K = 总 总 = ;
转化(mol) 0.014 0.014 0.014 0.014 x nCO nH 0.92.728
2 2
平衡(mol) 2.728 0.9 0.014 0.1 n n
总 总