文档内容
张家口市 2025-2026 学年度第一学期高二年级期末教学质量监测
化学
本试卷共 6 页,18 小题,满分 100 分。考试时长 75 分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在试卷和答题卡上。
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Cl:35.5 Cu:64 Sn:119
一、单项选择题:本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的 4 个选项中,只
有一项符合题目要求。
1. 文物是重要的历史文化遗产,是历史的见证。文物也会随着时间的推移受到不同程度的损害。下列文物
的损害与电化学腐蚀有关的是
A.裂开的“红山文化 B.生锈的“明代铸铁
陶塑站姿男俑” 莲花熏香炉”
C.泛黄的“康熙真迹 D.磨损的“郑家沟玉
——台省箴” 龙”
第 1页/共 19页A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.陶塑站姿男俑的裂开为无机材料的干裂,与电化学腐蚀无关,故 A 不符合题意;
B.生锈的“明代铸铁莲花熏香炉”是金属铁的锈蚀,和电化学腐蚀有关,故 B 符合题意;
C.泛黄的“康熙真迹——台省箴”是纸张的氧化过程,与电化学腐蚀无关,故 C 不符合题意;
D.磨损的“郑家沟玉龙”是磨损过程,物理变化,与电化学腐蚀无关,故 D 不符合题意;
故选 B。
2. 下列能正确表示元素的原子处于能量最低状态的是
A. C: B. N:
C. O: D. F:
【答案】A
【解析】
【详解】A.原子处于基态时能量最低,处于激发态时能量较高。基态碳原子的电子排布式为 ,
根据洪特规则,其 2p 轨道的 2 个电子分占不同轨道且自旋平行,A 符合题意;
B.基态氮原子的电子排布式为 ,图中电子排布为 ,2s 轨道的 1 个电子跃迁到能量较
高的 2p 轨道,是激发态,图中原子并非处于能量最低状态 ,B 不符合题意;
C.基态氧原子的电子排布式为 ,图中电子排布为 ,是激发态,图中原子并非处
于能量最低状态 ,C 不符合题意;
D.基态氟原子的电子排布式为 ,图中电子排布为 ,是激发态,图中原子并非处
于能量最低状态 ,D 不符合题意;
故选 A。
3. 量取一定量乙酸溶液,并用 NaOH 标准液测定该乙酸溶液浓度的滴定实验中,下列玻璃仪器一定不需要
的是
A. 玻璃棒 B. 酸式滴定管 C. 锥形瓶 D. 碱式滴定管
第 2页/共 19页【答案】A
【解析】
【详解】A.玻璃棒在滴定过程中无作用,因溶液混合可通过摇晃锥形瓶实现,故一定不需要,A 符合题意;
B.酸式滴定管用于量取一定体积乙酸溶液至锥形瓶,也可用移液管等,故可能用到,B 不符合题意;
C.锥形瓶为滴定过程中乙酸与 NaOH 溶液的反应容器,一定需要,C 不符合题意;
D.碱式滴定管用于盛放 NaOH 溶液进行滴定实验,一定需要,D 不符合题意;
故答案选 A。
4. 食醋是厨房中不可或缺的调味剂,约含 的醋酸( )。下列对醋酸溶液认识错误的是
A. 能使石蕊溶液变红 B. 能溶解大理石
C. 溶液中存在 分子 D. 溶液中存在
【答案】D
【解析】
【详解】A.醋酸是酸,能使石蕊溶液变红,A 正确;
B.醋酸能与大理石(主要成分碳酸钙)反应生成可溶性醋酸钙、水和二氧化碳,因此能溶解大理石,B 正
确;
C.醋酸是弱酸,在溶液中部分电离,存在未电离的 CHCOOH 分子,C 正确;
3
D.在醋酸溶液中,根据电荷守恒,c(H+) = c(CH
3
COO-) + c(OH-),由于 c(OH-) > 0,因此 c(H+)严格大于 c
(CHCOO-),D 错误;
3
5. 勒夏特列原理在生产和生活中具有重要意义。下列事实不能用勒夏特列原理解释的是
A. 热的纯碱溶液去油效果更好 B. 可乐瓶打开后有气泡冒出
C. 制备 时使用高效催化剂 D. 通过排饱和 溶液的方法收集
【答案】C
【解析】
【详解】A.碳酸根离子水解( )是吸热反应,热的纯碱溶液中,升高温度
使平衡向正反应方向移动,碱性增强,去油效果更好,符合勒夏特列原理,A 不符合题意;
B.CO 溶解平衡[ ]受压强影响,可乐瓶内高压,打开瓶盖后压强减小,平衡向气体
2
逸出方向移动,产生气泡,符合勒夏特列原理,B 不符合题意;
C.制备 SO 的反应( )中,催化剂仅加快反应速率,不影响化学平衡,不能
3
第 3页/共 19页用平衡移动原理解释,不符合勒夏特列原理,C 符合题意;
D.CO 溶解平衡为 ,饱和 NaHCO 溶液中存在高浓度的 ,使平衡逆向
2 3
移动,抑制 CO 溶解,利于气体收集,符合勒夏特列原理,D 不符合题意;
2
故答案选 C。
6. 一定条件下,反应 在密闭容器中进行,下列措施对该反应的速率无影
响的是
A. 缩小容器体积 B. 恒容条件下,升高体系温度
C. 恒压条件下,加入一定量 C D. 总压强恒定条件下,充入一定量 He
【答案】C
【解析】
【详解】A.缩小容器体积会增加气体物质的浓度,从而加快反应速率,因此该措施对反应速率有影响,A
不符合题意。
B.恒容条件下升高体系温度会加快分子运动,增加有效碰撞频率,从而加快反应速率,因此该措施对反应
速率有影响,B 不符合题意。
C.恒压条件下加入固体 C,固体 C 的浓度被视为常数且不影响气体浓度,因此反应速率不变,该措施对反
应速率无影响,C 符合题意。
D.总压强恒定条件下充入 He(惰性气体),为保持总压恒定,容器体积增大,导致气体反应物浓度降低,
反应速率减慢,因此该措施对反应速率有影响,D 不符合题意;
故选 C。
7. 室温下,含有下列离子组的溶液中,水的电离程度不受影响的是
A. B.
C. D.
【答案】D
【解析】
【详解】A.该离子组含有 (弱碱阳离子,水解呈酸性)和 CHCOO-(弱酸阴离子,水解呈碱性),
3
两者均能水解,影响水的电离平衡,A 不符合题意;
B.该离子组含有 Cu2+(弱碱阳离子,能水解产生 H+ ),影响水的电离平衡,B 不符合题意;
C.该离子组含有 OH-(氢氧根离子),溶液呈碱性,抑制水的电离,C 不符合题意;
第 4页/共 19页D.该离子组中所有离子(K+ 、Na+ 为强碱阳离子, 、 为强酸阴离子)均不水解,溶液呈中性,
水的电离程度不受影响,D 符合题意;
故选 D。
8. 化学与生产、生活息息相关。下列劳动项目与所述的化学知识关联正确的是
选项 劳动项目 化学知识
A 利用“84”消毒液消毒杀菌 NaClO 水解使溶液显碱性
B 生石灰发热包加水用于蒸煮米饭
C 工业合成氨气时采用高温高压条件 高温高压条件下有利于提高氨的平衡产率
D 草木灰和铵态氮肥不能混合使用 含有铵根离子的盐类热稳定性差
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.“84”消毒液消毒杀菌主要依靠次氯酸(HClO)的强氧化性,NaClO 水解显碱性是其性质之一,
但并非消毒的直接原因,关联不准确,A 错误;
B.生石灰(CaO)与水反应生成氢氧化钙是放热反应(ΔH < 0),释放的热量可用于加热,如蒸煮米饭,
关联正确,B 正确;
C.工业合成氨采用高温是为了提高反应速率,高温会降低氨的平衡产率(因反应放热);高压有利于提高
平衡产率。选项中“高温高压有利于提高氨的平衡产率”的说法错误,C 错误;
D.草木灰的主要成分是碳酸钾(KCO),其水溶液呈碱性,铵态氮肥中含有铵根离子,该离子在水溶液
2 3
中会发生水解,生成弱碱一水合氨和氢离子,二者会发生相互促进的水解反应,导致氨气挥发,造成氮素
流失,降低肥料效力,与铵盐热稳定性差无关,关联错误,D 错误;
故选 B。
9. 下列关于金属腐蚀与防护的描述正确的是
A. 铁器上连接锌片可减缓铁器腐蚀速率
B. 干燥的空气中铁器更易被腐蚀
第 5页/共 19页C. 与纯金属相比,合金的腐蚀速率一定快
D. 将铁器与直流电源的正极相连可对铁器形成牺牲阳极的阴极保护
【答案】A
【解析】
【详解】A.铁器上连接锌片属于牺牲阳极保护法,锌作为阳极被腐蚀,铁作为阴极被保护,从而减缓铁器
腐蚀速率,故 A 正确;
B.干燥的空气中缺乏电解质(如水),铁器腐蚀速率较慢,潮湿环境更易腐蚀,故 B 错误;
C.合金的腐蚀速率不一定比纯金属快,例如不锈钢(合金)比纯铁更耐腐蚀,故 C 错误;
D.将铁器与直流电源正极相连会使铁器成为阳极,会加速腐蚀,这与牺牲阳极的阴极保护法原理相反,正
确做法是将铁器与更活泼的金属相连或与直流电源的负极相连,故 D 错误;
故答案选 A。
10. 设 为阿伏加德罗常数的值,下列说法正确的是
A. 室温下, 的 溶液中所含 数目为
B. 与 混合后充分反应,生成的 分子数目为
C. 溶液中所含 数目为
D. 电解精炼铜时,阳极质量减少 ,导线上转移的电子数目为
【答案】A
【解析】
【详解】A. 的 溶液中 ,故 数目为 ,A 正确;
B. 与 的反应是可逆反应,不能完全进行到底,生成的 分子数目小于 ,B 错误;
C. 溶液中 会水解和电离,故所含 数目小于 ,C 错误;
D.电解精炼铜时,阳极材料含有锌、铁等杂质也会放电,质量减少 64 g 时转移电子数不确定,D 错误;
故答案选 A。
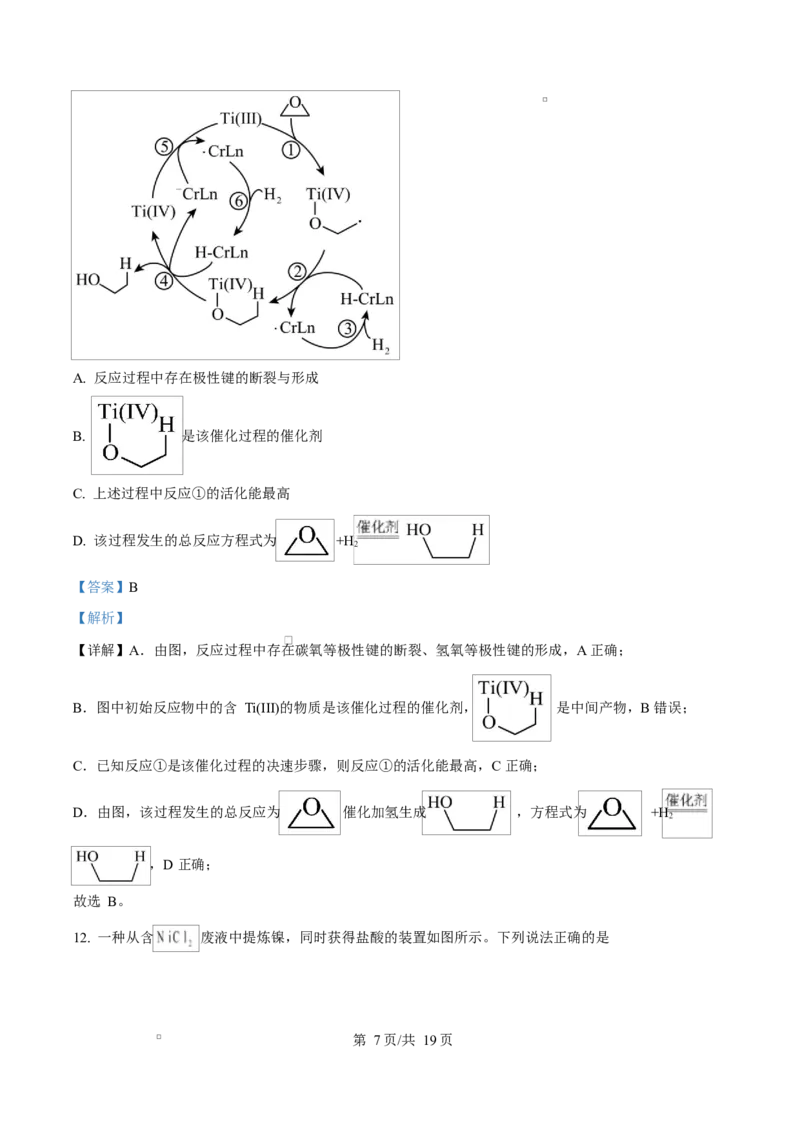
11. 某大学科研小组在温和条件下对环氧乙烷( )催化加氢的研究有了重大突破,反应的机理如图所
示。已知反应①是该催化过程的决速步骤。下列说法错误的是
第 6页/共 19页A. 反应过程中存在极性键的断裂与形成
B. 是该催化过程的催化剂
C. 上述过程中反应①的活化能最高
D. 该过程发生的总反应方程式为 +H
2
【答案】B
【解析】
【详解】A.由图,反应过程中存在碳氧等极性键的断裂、氢氧等极性键的形成,A 正确;
B.图中初始反应物中的含 Ti(III)的物质是该催化过程的催化剂, 是中间产物,B 错误;
C.已知反应①是该催化过程的决速步骤,则反应①的活化能最高,C 正确;
D.由图,该过程发生的总反应为 催化加氢生成 ,方程式为 +H
2
,D 正确;
故选 B。
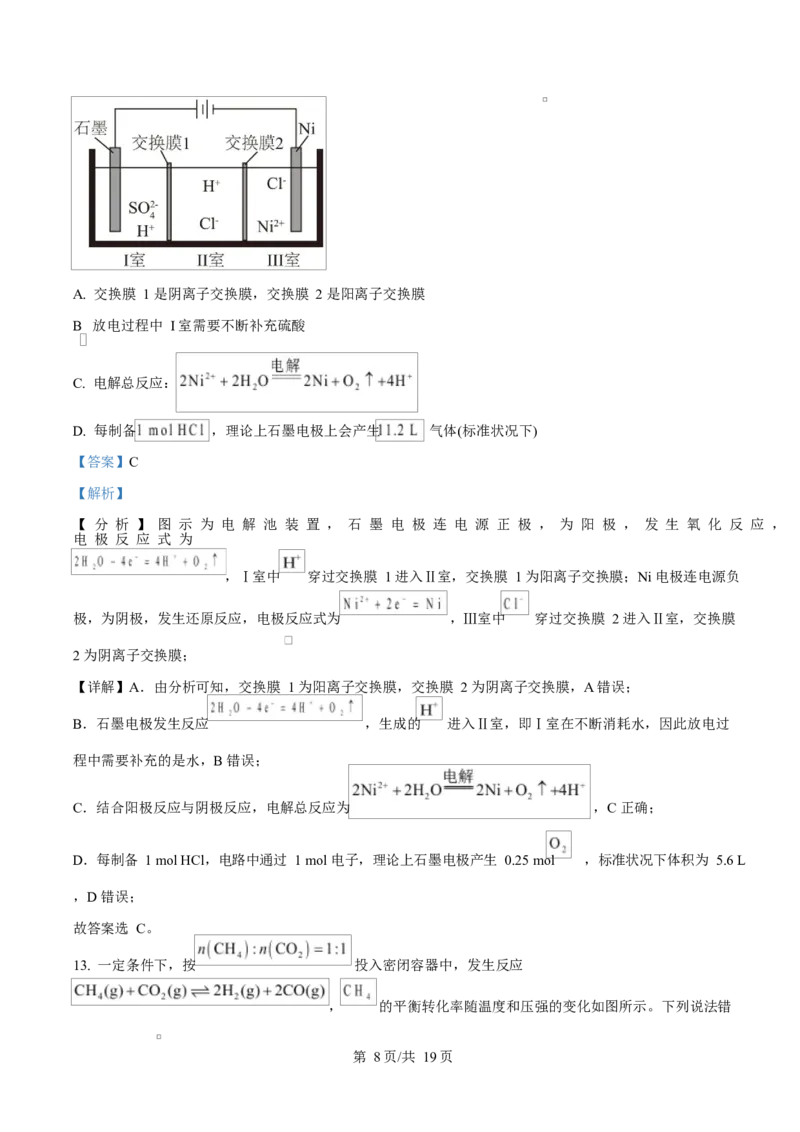
12. 一种从含 废液中提炼镍,同时获得盐酸的装置如图所示。下列说法正确的是
第 7页/共 19页A. 交换膜 1 是阴离子交换膜,交换膜 2 是阳离子交换膜
B 放电过程中 I 室需要不断补充硫酸
C. 电解总反应:
D. 每制备 ,理论上石墨电极上会产生 气体(标准状况下)
【答案】C
【解析】
【 分 析 】 图 示 为 电 解 池 装 置 , 石 墨 电 极 连 电 源 正 极 , 为 阳 极 , 发 生 氧 化 反 应 ,
电 极 反 应 式 为
,Ⅰ室中 穿过交换膜 1 进入Ⅱ室,交换膜 1 为阳离子交换膜;Ni 电极连电源负
极,为阴极,发生还原反应,电极反应式为 ,Ⅲ室中 穿过交换膜 2 进入Ⅱ室,交换膜
2 为阴离子交换膜;
【详解】A.由分析可知,交换膜 1 为阳离子交换膜,交换膜 2 为阴离子交换膜,A 错误;
B.石墨电极发生反应 ,生成的 进入Ⅱ室,即Ⅰ室在不断消耗水,因此放电过
程中需要补充的是水,B 错误;
C.结合阳极反应与阴极反应,电解总反应为 ,C 正确;
D.每制备 1 mol HCl,电路中通过 1 mol 电子,理论上石墨电极产生 0.25 mol ,标准状况下体积为 5.6 L
,D 错误;
故答案选 C。
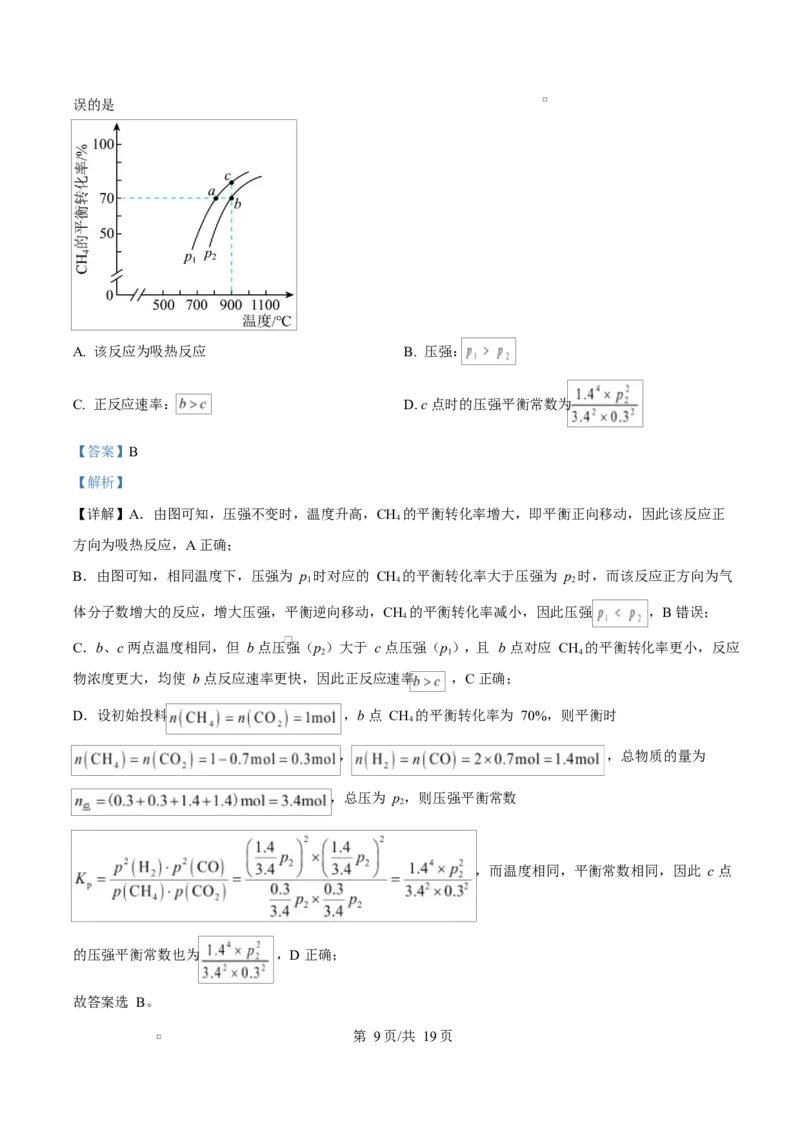
13. 一定条件下,按 投入密闭容器中,发生反应
, 的平衡转化率随温度和压强的变化如图所示。下列说法错
第 8页/共 19页误的是
A. 该反应为吸热反应 B. 压强:
C. 正反应速率: D. c 点时的压强平衡常数为
【答案】B
【解析】
【详解】A.由图可知,压强不变时,温度升高,CH 的平衡转化率增大,即平衡正向移动,因此该反应正
4
方向为吸热反应,A 正确;
B.由图可知,相同温度下,压强为 p 时对应的 CH 的平衡转化率大于压强为 p 时,而该反应正方向为气
1 4 2
体分子数增大的反应,增大压强,平衡逆向移动,CH 的平衡转化率减小,因此压强 ,B 错误;
4
C.b、c 两点温度相同,但 b 点压强(p)大于 c 点压强(p),且 b 点对应 CH 的平衡转化率更小,反应
2 1 4
物浓度更大,均使 b 点反应速率更快,因此正反应速率 ,C 正确;
D.设初始投料 ,b 点 CH 的平衡转化率为 70%,则平衡时
4
, ,总物质的量为
,总压为 p,则压强平衡常数
2
,而温度相同,平衡常数相同,因此 c 点
的压强平衡常数也为 ,D 正确;
故答案选 B。
第 9页/共 19页14. 氟化镁悬浊液中,用 或 调节 , 的关系如图所示 ,
时开始出现 沉淀。已知: , 。下列叙述错误的是
A.
B. 若向 的悬浊液中通入 HF 会提高 溶解度
C. 时溶液中存在:
D. 时溶液中
【答案】B
【解析】
详解】A.温度不变, 不变,pH=9~10 时,pMg=3.7,即
不变,则 浓度也不变;根据物料守恒
,碱性条件下, ,则 ,故
,A 正确;
B. 的沉淀溶解平衡为 ,向 的悬浊液中通入 HF,发生反
应 ,则 增大,平衡逆向移动, 溶解度降低,B 错误;
C.pH=4 时, ,根据 ,得到
,即 ,又因为物料守恒 ,
因此 ,C 正确;
D.pH≥10 时开始出现 沉淀,即
第 10页/共 19页;pH=11 时, ,则
,
,因此
,D 正确;
故答案选 B。
二、非选择题:本题共 4 小题,共 58 分。
15. 能源是人类生存和发展不可或缺的因素, 是三种重要的气体燃料,其燃烧热( )分别为
,回答下列问题:
(1)基态 O 原子核外电子占据最高能层的符号是___________,其核外电子的空间运动状态有___________
种。
(2)C 位于元素周期表中___________区,电负性:C___________O(填“>”“=”或“<”)。
(3)CO 燃烧热的热化学方程式表示为___________。
(4) ,a___________(填“>”“=”或“<”
)891。
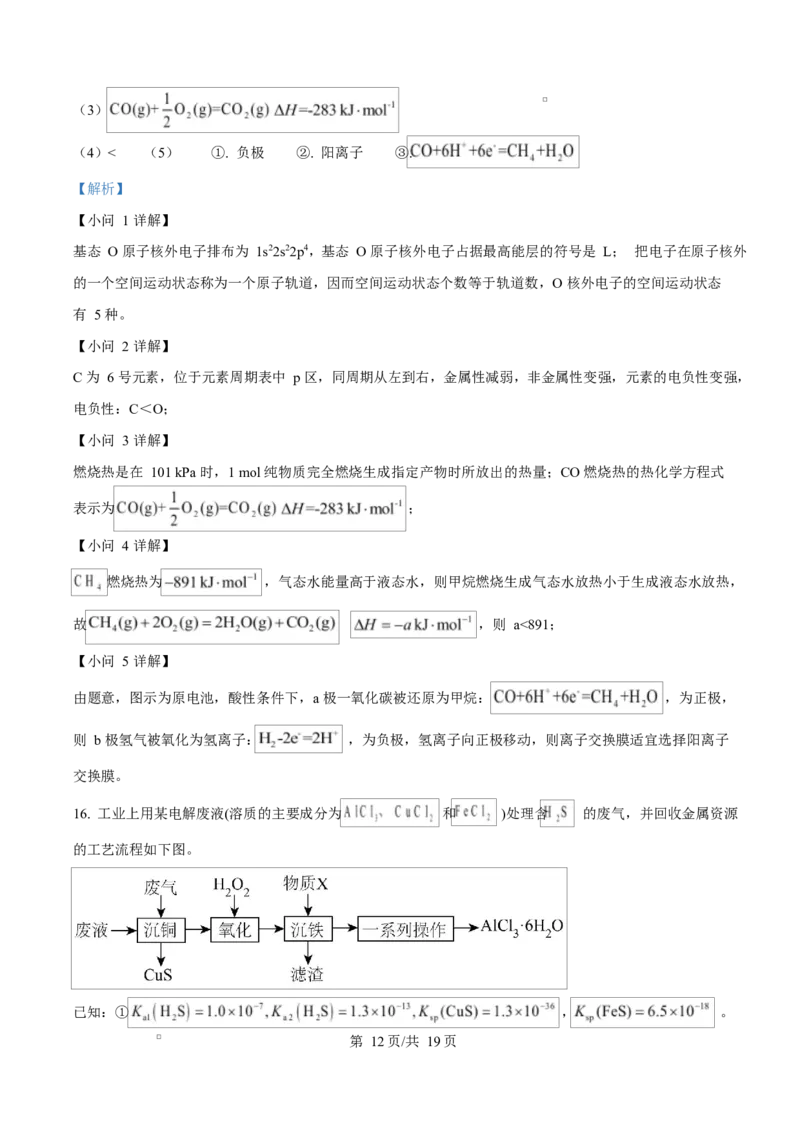
(5)垃圾发电厂用 处理焚烧后的 CO,在产生直流电的同时产生清洁能源甲烷,装置如图所示。
①电极 b 为___________(填“正极”或“负极”),离子交换膜适宜选择___________(填“阴离子”或“阳
离子”)交换膜。
②电极 a 上发生反应的电极反应式为___________。
【答案】(1) ①. L ②. 5
(2) ①. p ②. <
第 11页/共 19页(3)
(4)< (5) ①. 负极 ②. 阳离子 ③.
【解析】
【小问 1 详解】
基态 O 原子核外电子排布为 1s22s22p4,基态 O 原子核外电子占据最高能层的符号是 L; 把电子在原子核外
的一个空间运动状态称为一个原子轨道,因而空间运动状态个数等于轨道数,O 核外电子的空间运动状态
有 5 种。
【小问 2 详解】
C 为 6 号元素,位于元素周期表中 p 区,同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强,
电负性:C<O;
【小问 3 详解】
燃烧热是在 101 kPa 时,1 mol 纯物质完全燃烧生成指定产物时所放出的热量;CO 燃烧热的热化学方程式
表示为 ;
【小问 4 详解】
燃烧热为 ,气态水能量高于液态水,则甲烷燃烧生成气态水放热小于生成液态水放热,
故 ,则 a<891;
【小问 5 详解】
由题意,图示为原电池,酸性条件下,a 极一氧化碳被还原为甲烷: ,为正极,
则 b 极氢气被氧化为氢离子: ,为负极,氢离子向正极移动,则离子交换膜适宜选择阳离子
交换膜。
16. 工业上用某电解废液(溶质的主要成分为 和 )处理含 的废气,并回收金属资源
的工艺流程如下图。
已知:① , 。
第 12页/共 19页②相关金属离子形成氢氧化物沉淀的 pH 范围如下表:
金属离子
开始沉淀的 pH 3.8 6.3 1.5
沉淀完全的 pH 5.0 8.3 2.8
回答下列问题:
(1)基态铜原子 价电子排布式为___________;基态硫原子最高能级电子云轮廓图为___________。
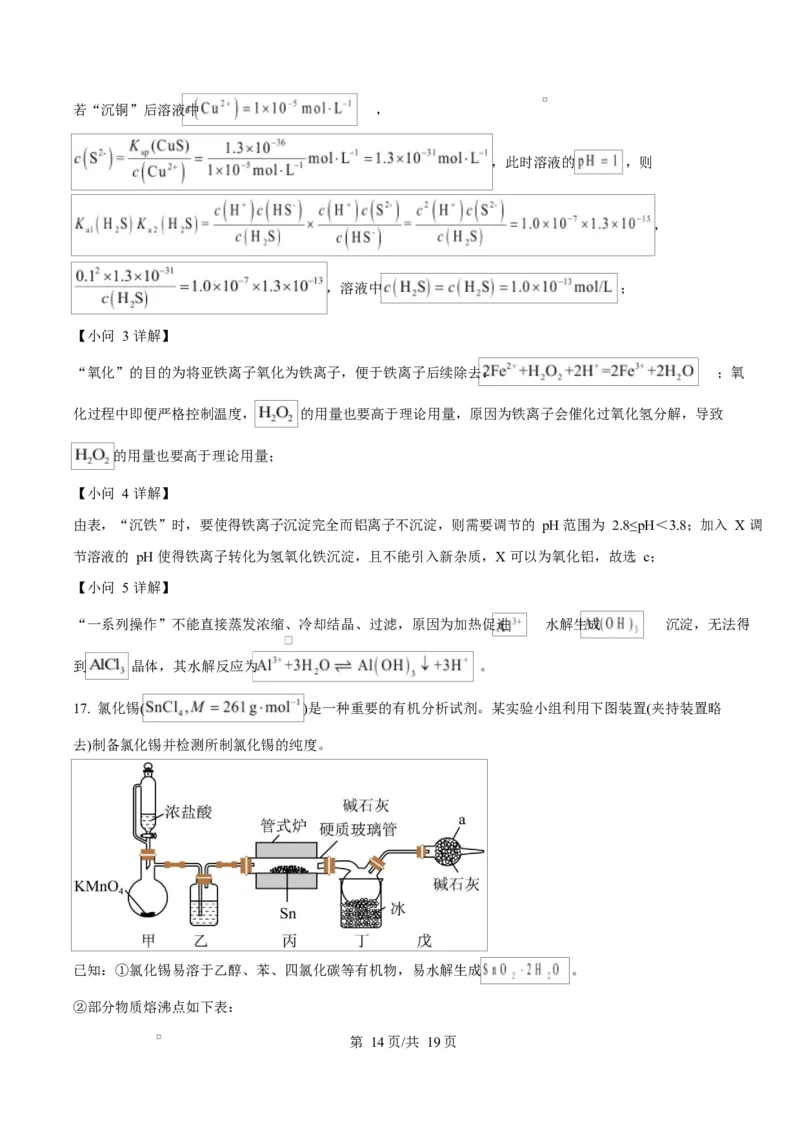
(2)若“沉铜”后溶液中 ,且此时溶液的 ,则溶液中
___________。
(3)“氧化”的目的为___________(用离子方程式表示);氧化过程中即便严格控制温度, 的用量也
要高于理论用量,原因为___________。
(4)“沉铁”时需要调节的 pH 范围为___________;物质 X 可选用___________(填选项字母)。
a. b.CuO c. d.
(5)“一系列操作”不能直接蒸发浓缩、冷却结晶、过滤,原因为___________(结合离子方程式解释)。
【答案】(1) ①. 3d104s1 ②. 哑铃形
(2)
(3) ①. ②. 铁离子会催化过氧化氢分解
(4) ①. 2.8≤pH<3.8 ②. c
(5)
【解析】
【分析】电解废液通入含硫化氢的废气,铜离子生成硫化铜沉淀,过滤滤液加入过氧化氢氧化亚铁离子为
铁离子,加入 X 调节溶液的 pH 使得铁离子转化为氢氧化铁沉淀,且不能引入新杂质,X 可以为氧化铝,
得到氯化铝溶液,处理后的氯化铝晶体;
【小问 1 详解】
铜为 29 号元素,基态铜原子的价电子排布式为 3d104s1;基态 S 原子核外电子排布为 1s22s22p63s23p4,则基
态硫原子最高能级电子云轮廓图为哑铃形;
【小问 2 详解】
第 13页/共 19页若“沉铜”后溶液中 ,
,此时溶液的 ,则
,
,溶液中 ;
【小问 3 详解】
“氧化”的目的为将亚铁离子氧化为铁离子,便于铁离子后续除去: ;氧
化过程中即便严格控制温度, 的用量也要高于理论用量,原因为铁离子会催化过氧化氢分解,导致
的用量也要高于理论用量;
【小问 4 详解】
由表,“沉铁”时,要使得铁离子沉淀完全而铝离子不沉淀,则需要调节的 pH 范围为 2.8≤pH<3.8;加入 X 调
节溶液的 pH 使得铁离子转化为氢氧化铁沉淀,且不能引入新杂质,X 可以为氧化铝,故选 c;
【小问 5 详解】
“一系列操作”不能直接蒸发浓缩、冷却结晶、过滤,原因为加热促进 水解生成 沉淀,无法得
到 晶体,其水解反应为 。
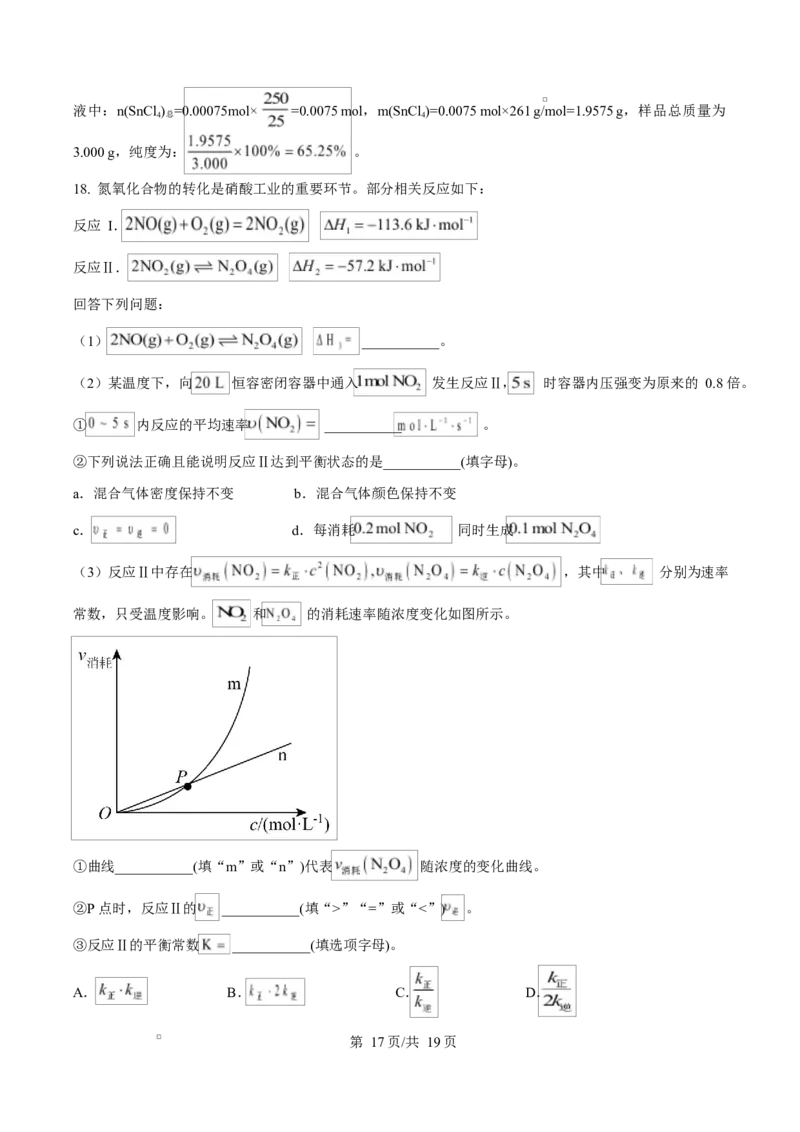
17. 氯化锡( )是一种重要的有机分析试剂。某实验小组利用下图装置(夹持装置略
去)制备氯化锡并检测所制氯化锡的纯度。
已知:①氯化锡易溶于乙醇、苯、四氯化碳等有机物,易水解生成 。
②部分物质熔沸点如下表:
第 14页/共 19页Sn
熔点 217
沸点 685 114
回答下列问题:
(1)装置乙中盛放的试剂名称为___________。
(2)装置戊所用仪器 a 的名称为___________,其盛装碱石灰的作用是___________。
(3)氯化锡易水解从而影响其纯度,某实验小组通过下列实验测氯化锡纯度(杂质中不含其他含氯物质)。
实验操作:用分析天平称取 氯化锡样品,配成 溶液,移取 溶液于锥形瓶中,
滴加指示剂 溶液。在不断摇动下,用 标准溶液滴定至有砖红色沉淀
( )生成,30 秒内不褪色。平行测试 5 次,消耗 标准溶液如下表所示。
滴定次数 1 2 3 4
起始读数 1.10 2.00 0.20 0.50
终点读数 31.20 31.80 28.20 30.40
①氯化锡水解时发生反应的化学方程式为___________。
②滴定时 标准溶液应选用___________(填“酸式”或“碱式”)滴定管,在使用滴定管前,首先要
___________,洁净的滴定管在盛装溶液前应润洗,其操作为___________(填选项字母),重复润洗操作
次。
A.从滴定管上口加入 蒸馏水 B.从滴定管上口加入 标准溶液
C.倾斜转动滴定管,使液体润湿全部滴定管内壁 D.上下晃动滴定管,使液体润湿全部滴定管内壁
E.将液体从滴定管上口倒入预置的烧杯中 F.将液体从滴定管下部放入预置的烧杯中
③平均消耗 标准溶液的体积为___________mL。若滴定前滴定管中有气泡,滴定后气泡消失,用该
数据计算最终所测纯度___________(填“偏大”“偏小”或“无影响”)。
④计算氯化锡的纯度为___________(保留 4 位有效数字)。
【答案】(1)浓硫酸 (2) ①. 球形干燥管 ②. 吸收未反应的 Cl,防止污染空气;同时防止外
2
第 15页/共 19页界水蒸气进入装置丁,避免 SnCl 水解
4
(3) ①. SnCl
4
+4H
2
O=SnO 2⋅2H
O↓+4HCl ②. 酸式 ③. 检漏 ④. B→C→F ⑤. 30.00
2
⑥. 偏大 ⑦.
【解析】
【分析】装置甲中高锰酸钾与浓盐酸反应生成 Cl,氯化锡易水解,装置乙用于除去 Cl 中的 HO,装置丙
2 2 2
中 Sn 与 Cl 反应生成 SnCl ,装置丁用于冷凝收集 SnCl ,装置戊中的碱石灰可防止外界水蒸气进入丁装置,
2 4 4
同时吸收未反应的 Cl。
2
【小问 1 详解】
根据题目,装置甲中高锰酸钾与浓盐酸反应生成 Cl,氯化锡易水解,装置乙用于除去 Cl 中的 HO,因此,
2 2 2
装置乙中应盛放浓硫酸。
【小问 2 详解】
观察装置图,仪器 a 为球形干燥管。SnCl 易水解,需防止外界水蒸气进入装置丁。此外,未反应的 Cl 需
4 2
被吸收,避免污染环境。因此,碱石灰的作用是:吸收未反应的 Cl,防止污染空气;同时防止外界水蒸气
2
进入装置丁,避免 SnCl 水解。
4
【小问 3 详解】
①根据题目,SnCl
4
易水解生成 SnO
2
·2H
2
O。根据元素守恒,反应方程式为:SnCl
4
+4H
2
O=SnO 2⋅2H
O↓+
2
4HCl;
②AgNO 溶液具有氧化性,会腐蚀橡胶,因此应使用酸式滴定管。使用前需检查滴定管 否漏水(检漏)。
3
润洗时,应从滴定管上口加入 3~5mL AgNO 标准溶液(B),倾斜转动滴定管,使溶液润湿全部内壁(C),
3
再将液体从下部放出(F)。即操作为:B→C→F。
③滴定消耗的体积:第 1 次:31.20mL - 1.10 mL = 30.10 mL,第 2 次:31.80 mL - 2.00 mL = 29.80 mL,第 3
次:28.20 mL - 0.20 mL = 28.00 mL(明显异常,舍去),第 4 次:30.40 mL - 0.50 mL = 29.90 mL,第 5 次:
31.40 mL - 1.20 mL = 30.20 mL,取其余 4 次的平均值:
V= mL=30.00ꢀmL,若滴定前滴定管中有气泡,滴定后气泡消失,会导致读数
偏大,即消耗的 AgNO 体积偏大。根据反应方程式:SnCl +4AgNO =4AgCl↓+Sn(NO ) 可得:n(SnCl )=
3 4 3 3 4 4
n(AgNO),若 V(AgNO )偏大,则 n(SnCl )偏大,最终纯度偏大。
3 3 4
④ 已知:c(AgNO )=0.1000ꢀmol/L,V(AgNO )=30.00ꢀmL=0.03ꢀL, n(AgNO)=0.1000mol/L×0.03L=0.003ꢀmol,
3 3 3
n(SnCl )= n(AgNO)= ×0.003mol=0.00075ꢀmol 这是 25.00 mL 溶液中 SnCl 的物质的量,原 250.00 mL 溶
4 3 4
第 16页/共 19页液中:n(SnCl ) =0.00075mol× =0.0075ꢀmol,m(SnCl )=0.0075ꢀmol×261ꢀg/mol=1.9575ꢀg,样品总质量为
4 总 4
3.000 g,纯度为: 。
18. 氮氧化合物的转化是硝酸工业的重要环节。部分相关反应如下:
反应 I.
反应Ⅱ.
回答下列问题:
(1) ___________。
(2)某温度下,向 恒容密闭容器中通入 发生反应Ⅱ, 时容器内压强变为原来的 0.8 倍。
① 内反应的平均速率 ___________ 。
②下列说法正确且能说明反应Ⅱ达到平衡状态的是___________(填字母)。
a.混合气体密度保持不变 b.混合气体颜色保持不变
c. d.每消耗 同时生成
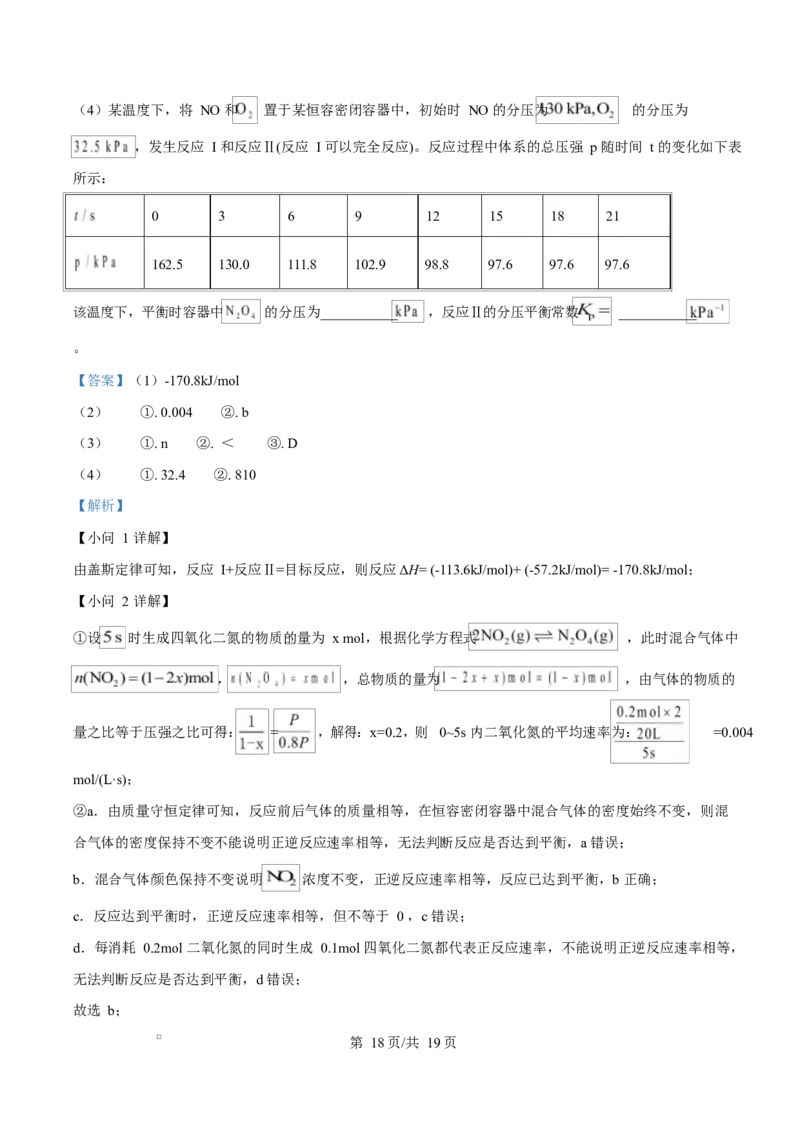
(3)反应Ⅱ中存在 ,其中 分别为速率
常数,只受温度影响。 和 的消耗速率随浓度变化如图所示。
①曲线___________(填“m”或“n”)代表 随浓度的变化曲线。
②P 点时,反应Ⅱ的 ___________(填“>”“=”或“<”) 。
③反应Ⅱ的平衡常数 ___________(填选项字母)。
A. B. C. D.
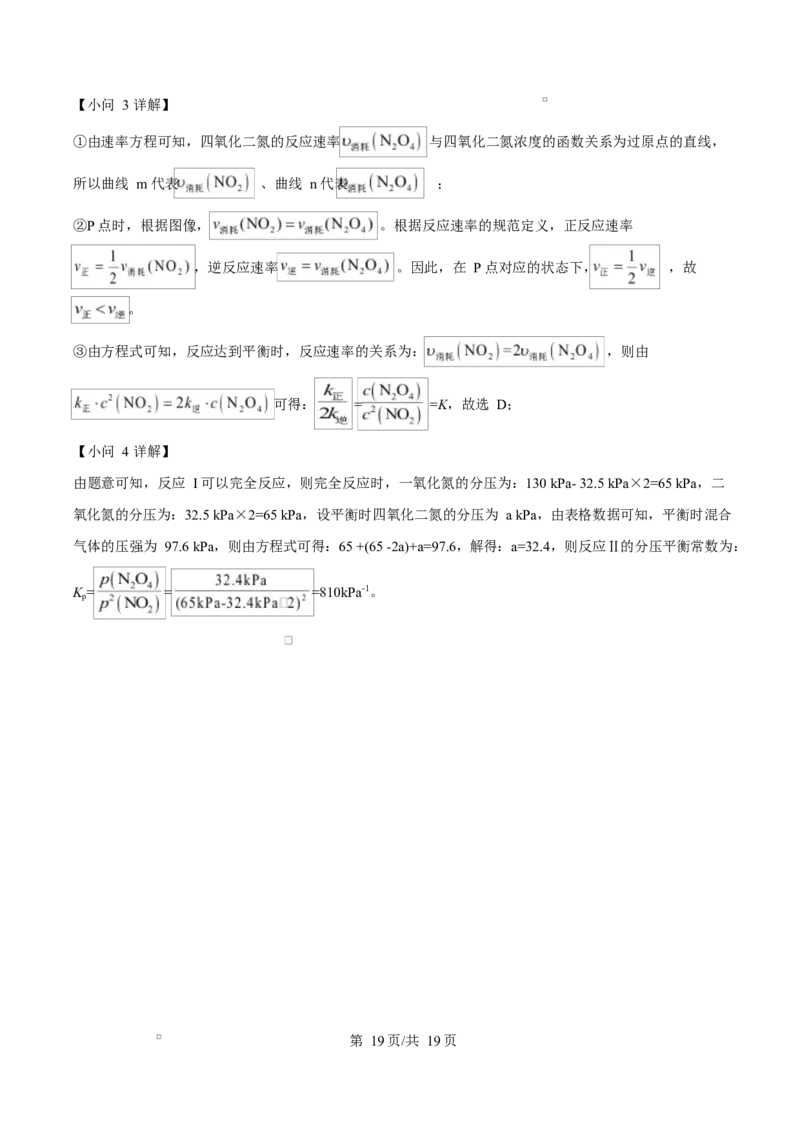
第 17页/共 19页(4)某温度下,将 NO 和 置于某恒容密闭容器中,初始时 NO 的分压为 的分压为
,发生反应 I 和反应Ⅱ(反应 I 可以完全反应)。反应过程中体系的总压强 p 随时间 t 的变化如下表
所示:
0 3 6 9 12 15 18 21
162.5 130.0 111.8 102.9 98.8 97.6 97.6 97.6
该温度下,平衡时容器中 的分压为___________ ,反应Ⅱ的分压平衡常数 ___________
。
【答案】(1)-170.8kJ/mol
(2) ①. 0.004 ②. b
(3) ①. n ②. < ③. D
(4) ①. 32.4 ②. 810
【解析】
【小问 1 详解】
由盖斯定律可知,反应 I+反应Ⅱ=目标反应,则反应ΔH= (-113.6kJ/mol)+ (-57.2kJ/mol)= -170.8kJ/mol;
【小问 2 详解】
①设 时生成四氧化二氮的物质的量为 x mol,根据化学方程式 ,此时混合气体中
, ,总物质的量为 ,由气体的物质的
量之比等于压强之比可得: = ,解得:x=0.2,则 0~5s 内二氧化氮的平均速率为: =0.004
mol/(L·s);
②a.由质量守恒定律可知,反应前后气体的质量相等,在恒容密闭容器中混合气体的密度始终不变,则混
合气体的密度保持不变不能说明正逆反应速率相等,无法判断反应是否达到平衡,a 错误;
b.混合气体颜色保持不变说明 浓度不变,正逆反应速率相等,反应已达到平衡,b 正确;
c.反应达到平衡时,正逆反应速率相等,但不等于 0 ,c 错误;
d.每消耗 0.2mol 二氧化氮的同时生成 0.1mol 四氧化二氮都代表正反应速率,不能说明正逆反应速率相等,
无法判断反应是否达到平衡,d 错误;
故选 b;
第 18页/共 19页【小问 3 详解】
①由速率方程可知,四氧化二氮的反应速率 与四氧化二氮浓度的函数关系为过原点的直线,
所以曲线 m 代表 、曲线 n 代表 ;
②P 点时,根据图像, 。根据反应速率的规范定义,正反应速率
,逆反应速率 。因此,在 P 点对应的状态下, ,故
。
③由方程式可知,反应达到平衡时,反应速率的关系为: ,则由
可得: = =K,故选 D;
【小问 4 详解】
由题意可知,反应 I 可以完全反应,则完全反应时,一氧化氮的分压为:130 kPa- 32.5 kPa×2=65 kPa,二
氧化氮的分压为:32.5 kPa×2=65 kPa,设平衡时四氧化二氮的分压为 a kPa,由表格数据可知,平衡时混合
气体的压强为 97.6 kPa,则由方程式可得:65 +(65 -2a)+a=97.6,解得:a=32.4,则反应Ⅱ的分压平衡常数为:
K = = =810kPa-1。
p
第 19页/共 19页