文档内容
2009年全国普通高等学校招生统一考试
上海化学试卷
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对后的
条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
第Ⅰ卷 (共66分)
考生注意:
1.答第Ⅰ卷前,考生务必在答题卡上用钢笔或圆珠笔清楚填写姓名、准考证号、校验码,
并用2B铅笔正确涂写准考证号和校验码。
2.第Ⅰ卷(1—
22小题),由机器阅卷,答案必须全部涂写在答题卡上。考生应将代表正确答案的小方格
用2B铅笔涂黑。注意试题题号和答题纸编号一一对应,不能错位。答案需要更改时,必须
将原选项用橡皮擦去,重新选择。答案不能涂写在试卷上,涂写在试卷上一律不给分。
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 V-51 Cr-52
Mn-55 Fe-56 Cu-64
一、选择题(本题共10分,每小题2分,只有一正确选项,答案涂写在答题卡上。)
1.下列措施不能达到节能减排目的的是
A.利用太阳能制氢燃料 B.用家用汽车代替公交车
C.利用潮汐能发电 D.用节能灯代替白炽灯
2.以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是
A.:He B. C.1s2 D.
3.有机物的种类繁多,但其命中是有规则的。下列有机物命名正确的是
4.用浓氯化铵溶液处理过的舞台幕布不易着火。其原因是
①幕布的着火点升高 ②幕布的质量增加
③氯化铵分解吸收热量,降低了温度 ④氯化铵分解产生的气体隔绝了空气
A.①② B.③④ C.③④ D.②④
5.下列对化学反应的认识错误的是w.w.w.k.s.5.u.c.o.m
第- 1 -页 | 共9页A.会引起化学键的变化 B.会产生新的物质
C.必然引起物质状态的变化 D.必然伴随着能量的变化
二、选择题(本题共36分,每小题3分,只有一个正确选项,答案涂写在答题卡上。)
6.下列实验装置不适用于物质分离的是
7.在下列变化①大气固氮②硝酸银分解③实验室制取氨气中,按氮元素被氧化、被还原、
既不被氧化又不被还原的顺序排列,正确的是
A.①②③ B.②①③ C.③②① D.③①②
8.在通常条件下,下列各组物质的性质排列正确的是w.w.w.k.s.5.u.c.o.m
A.熔点:CO >KCl>SiO B.水溶性:HCl>H S>SO
2 2 2 2
C.沸点:乙烷>戊烷>丁烷 D.热稳定性:HF>H O> NH
2 3
9.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构
如右图。下列叙述正确的是
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和9mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
10.9.2g金属钠投入到足量的重水中,则产生的气体中含有
A.0.2mol中子 B.0.4mol电子
C.0.2mol质子 D.0.4mol分子
11.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度
为115~125℃,反应装置如右图。下列对该实验的描述错误的是
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
12.N 代表阿伏加德罗常数。下列有关叙述正确的是
A
A.标准状况下,2.24LH O含有的分子数等于0.1N
2 A
第- 2 -页 | 共9页B.常温下,100mL1mol/L Na CO 溶液中阴离子总数大于0.1N
2 3 A
C.分子数为N 的CO、C H 混合气体体积约为22.4L,质量为28g
A 2 4
D.3.4gNH 中含N—H键数目为0.2N
3 A
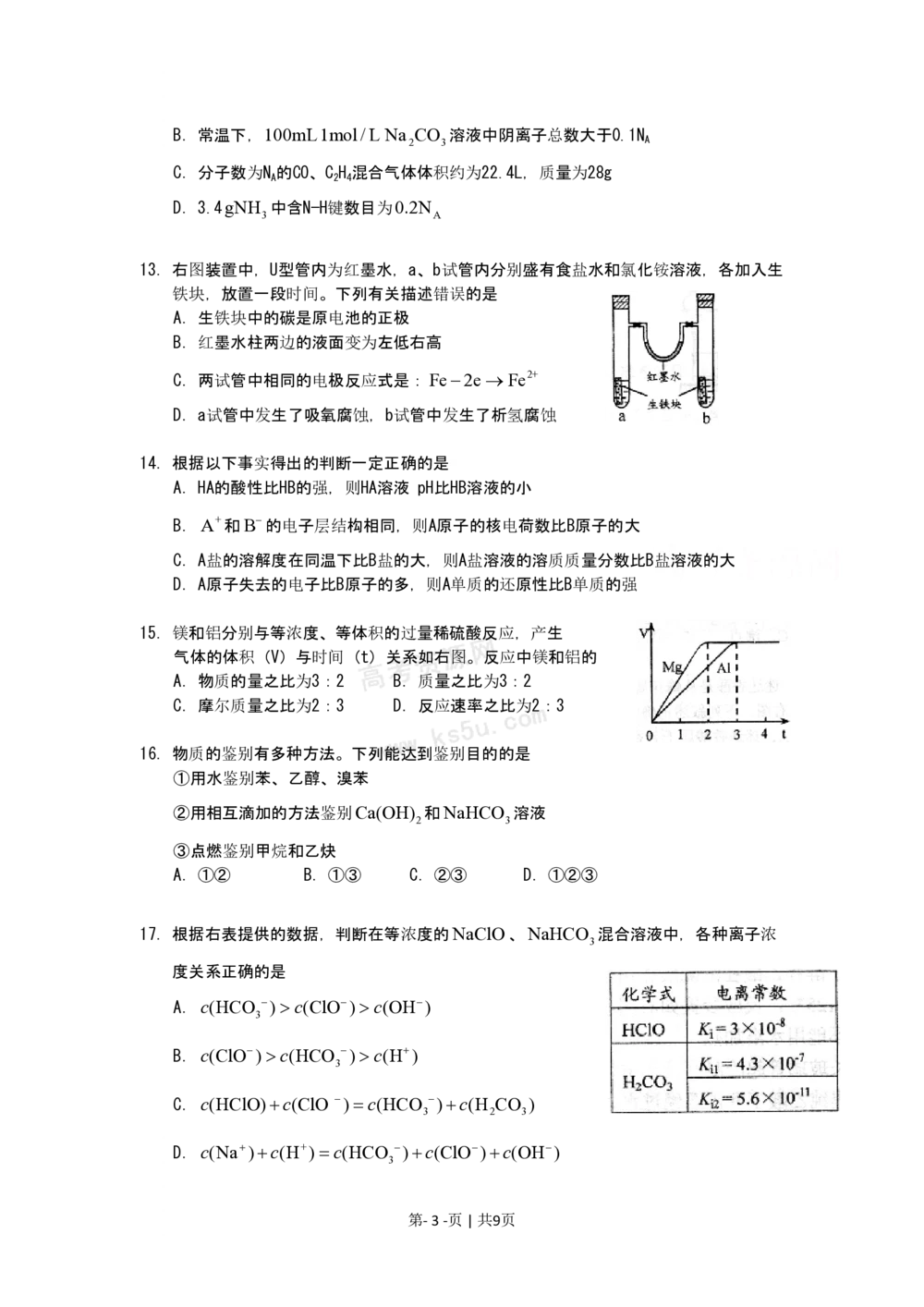
13.右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生
铁块,放置一段时间。下列有关描述错误的是
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe-2e®Fe2+
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
14.根据以下事实得出的判断一定正确的是w.w.w.k.s.5.u.c.o.m
A.HA的酸性比HB的强,则HA溶液 pH比HB溶液的小
B.A+和B-的电子层结构相同,则A原子的核电荷数比B原子的大
C.A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
15.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生
气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
A.物质的量之比为3:2 B.质量之比为3:2
C.摩尔质量之比为2:3 D.反应速率之比为2:3
16.物质的鉴别有多种方法。下列能达到鉴别目的的是
①用水鉴别苯、乙醇、溴苯
②用相互滴加的方法鉴别Ca(OH) 和NaHCO 溶液
2 3
③点燃鉴别甲烷和乙炔
A.①② B.①③ C.②③ D.①②③
17.根据右表提供的数据,判断在等浓度的NaClO、NaHCO 混合溶液中,各种离子浓
3
度关系正确的是
A.c(HCO -)>c(ClO-)>c(OH-)
3
B.c(ClO-)>c(HCO -)>c(H+)
3
C.c(HClO)+c(ClO -)=c(HCO -)+c(H CO )
3 2 3
D.c(Na+)+c(H+)=c(HCO -)+c(ClO-)+c(OH-)
3
第- 3 -页 | 共9页三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确选项
的,多选不给分;有两个正确选项的,选对一个给2分,选错一个,该小题不给分,答案
涂写在答题卡上。)
18.下列离子方程式正确的是
A.H SO 与Ba(OH) 溶液反应: Ba2++OH-+H++SO2- ®BaSO ¯+H O
2 4 2 4 4 2
B.CuSO 溶液吸收H S气体: Cu2++H S®CuS¯+2H+
4 2 2
C.AlCl 溶液中加入过量的浓氨水: Al3++4NH ·H O®A1O-+4NH++2H O
3 3 2 2 4 2
D.等体积、等浓度的Ba(OH) 稀溶液与NH HCO 稀溶液混合:
2 4 3
Ba2++2OH- +NH++HCO- ®BaCO ¯+NH ·H O+H O
4 3 3 3 2 2
19.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q 、Q 均为正值):
l 2
H (g)+Cl (g)®2HCl(g)+Q H (g)+Br (g)®2HBr(g)+Q
2 2 1 2 2 2
有关上述反应的叙述正确的是w.w.w.k.s.5.u.c.o.m
A.Q >Q
1 2
B.生成物总能量均高于反应物总能量
C.生成1molHCl气体时放出Q 热量
l
D.1mol HBr(g)具有的能量大于1mol HBr(l)具有的能量
20.对于常温下pH为1的硝酸溶液,下列叙述正确的是
A.该溶液lmL稀释至100mL后,pH等于3
B.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12。
D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍
21.下列坐标图所表示的量的关系错误的是
A. 烷烃分子中碳原子数x与碳的质量分数y的关系
B. NO 溶于水完全转化为硝酸,x与消耗氧气的量y的关系
x
C. 氯化钠溶液中加水的量x与溶质的质y的关系
D. 酒精水溶液中海清的质量分数x与酒精水溶液密度y的关系
第- 4 -页 | 共9页22.实验室将9g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所
得固体中含金属单质为18g,则该氧化物粉末可能是
A.Fe O 和MnO B.MnO 和VO C.Cr O 和VO D Fe O 和FeO
2 3 2 2 2 5 2 3 2 5 3 4
上海化学试卷
本试卷分为第Ⅰ卷(第1—4页)和第Ⅱ卷(第5—10页)
两部分。全卷共10页。满分150分,考试时间120分钟。
第Ⅱ卷(共84分)
考生注意:
1.答第Ⅱ卷前,考生务必将姓名、准考证号、校验码等填写清楚。
2.第Ⅱ卷从第23题到第31题,考生应用钢笔或圆珠笔将答案直接写在试卷上。
四、(本题共24分)w.w.w.k.s.5.u.c.o.m
23.海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl ®C1+Cl ②Cl+H ®HCl+H ③H+C1 ®HCl+Cl ……
2 2 2
反应②中形成的化合物的电子式为 ;反应③中被破坏的化学键属
于 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期
族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F 、Cl 、Br 、I 的顺序由难变易
2 2 2 2
(4)卤素单质的键能大小如右图。由图推断:
①非金属性强的卤素,其单质分子的化学键
断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:
24.某反应中反应物与生成物有:AsH 、H SO 、KBrO 、K SO 、H AsO 、
3 2 4 3 2 4 3 4
H O和一种未知物质X。
2
(1)已知KBrO 在反应中得到电子,则该反应的还原剂是 。
3
(2)已知0.2mol KBrO 在反应中得到1mol电子生成X,则X的化学式为 。
3
(3)根据上述反应可推知 。
第- 5 -页 | 共9页a.氧化性:KBrO >H AsO b.氧化性:H AsO >KBrO
3 3 4 3 4 3
c.还原性:AsH >X d.还原性:X>AsH
3 3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方
向和数目:
25.
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。w.w.w.k.s.5.u.c.o.m
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe O (s)+3CO(g)ˆˆ† 2Fe(s)+3CO (g)
2 3 ‡ˆˆ 2
①该反应的平衡常数表达式为:K=
②该温度下,在2L盛有Fe O 粉末的密闭容器中通入CO气体,10min后,生成了单
2 3
质铁11.2g。则10min内CO的平均反应速率为
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
① ②
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
和温度(T)的关系示意图中与铝热反应最接近的是 。
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:
欲使上述体系中Al3+浓度增加,可加入的物质是 。
五、(本题共24分)
26.根据硫化氢气体的实验室制法和性质完成下列填空。
(1)若用启普发生器制取硫化氢气体,则制取气体的原料可选用________。
a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁
c.稀硫酸与硫化钠 d.稀盐酸与硫化亚铁
(2)现要组装一套可以控制硫化氢气体产生速率的装置,请在下图中选择合适的仪器;
______________(填编
号)。
第- 6 -页 | 共9页(3)如右图,在一个充满氧气的集气瓶中加入少量品红稀硫溶液,
点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到
的现象是___________________________________________________。
(4)在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为:
______________________________________________________________
反应过程中,溶液的pH______(填“变大”、“变小”或“不变”)。
(5)点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图
的装置能起到此作用的是___________。
(6)已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在
空气中的体积分数为30%时,其爆炸产物是______________________。
27.实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁
,以下是提纯大理石的实验步骤:
(1)溶解大理石时,用硝酸而不同硫酸的原因是_______________________________。
(2)操作Ⅱ的目的是______________,溶液A(溶质是共价化合物)是___________。
(3)写出检验滤液中是否含铁离子方程式:_____________________________________
______________________________________________________________________。
(4)写出加入碳酸铵所发生反应的离子方程式:________________________________
写出滤液B的一种用途:_________________________
(5)CaO 中一般含CaO。试按下列提示完成CaO 含量分析的实验设计。
2 2
试剂:氢氧化钠标准溶液、盐酸标准溶液、酚酞 仪器:电子天平、锥形瓶、滴定管
实验步骤:
①_______;②加入_________________;③加入酚酞,用氢氧化钠标准溶液滴定。
(6)若理论上滴定时耗用标准溶液20.00mL恰好完全反应,实际操作中过量半滴(1mL溶液
为25滴),则相对误差为______________
六、(本题共20分)
28.环氧氯丙烷是制备树脂的主要原料,工业上有不同的合成路线,以下是其中的两条(
有些反应未注明条件)。
第- 7 -页 | 共9页完成下列填空:
(1)写出反应类型:反应①_________________ 反应③___________________
(2)写出结构简式:X_____________________ Y________________________
(3)写出反应②的化学方程式:______________________________________________
(4)与环氧氯丙烷互为同分异构体,且属于醇类的物质(不含 及 结构
)
有__________种。
29.尼龙-
66广泛用于制造机械、汽车、化学与电气装置的零件,亦可制成薄膜用作包装材料,其合
成路线如下图所示(中间产物E给出两条合成路线)。
完成下列填空:
(1)写出反应类型:反应②__________________反应③___________________________
(2)写出化合物D的结构简式:_______________________________________________
(3)写出一种与C互为同分异构体,且能发生银镜反应的化合物的结构简式:
____________________________________________________________________________
(4)写出反应①的化学方程式:
____________________________________________________________________________
(5)下列化合物中能与E发生化学反应的是_________。
a.NaOH b.Na CO c.NaCl d.HCl
2 3
(6)用化学方程式表示化合物B的另一种制备方法(原料任选):
____________________________________________________________________________
七、(本题共16分)w.w.w.k.s.5.u.c.o.m
30.臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高
压放电管来制取臭氧:3O ¾放¾电¾®2O
2 3
第- 8 -页 | 共9页(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为______g/mol
(保留一位小数)。
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为_____________L
。
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中
,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为________________
__。
31.烟气中NO 是NO和NO 的混合物(不含N O )。
x 2 2 4
(1)根据废气排放标准,1m3烟气最高允许含400mgNO 。若NO 中NO质量分数为0.85
x x
,则1m3烟气中最高允许含NO__________L(标准状况,保留2位小数)。
(2)工业上通常用溶质质量分数为0.150的Na CO 水溶液(密度1.16g/mL)作为NO
2 3 x
吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L(保留2位小数)。
(3)已知: NO+NO +Na CO ®2NaNO +CO ①
2 2 3 2 2
2NO +Na CO ®NaNO +NaNO +CO ②
2 2 3 2 3 2
1m3含2000mgNO 的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,
x
吸收后的烟气_______排放标准(填“符合”或“不符合”),理由:__________________
__。
(4)加入硝酸可改变烟气中NO和NO 的比,反应为:
2
NO+2HNO →3NO +H O
3 2 2
当烟气中n(NO):n(NO )=2:3时,吸收率最高。
2
1m3烟气含2000mgNO ,其中n(NO):n(NO )=9:1。
x 2
计算:(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)。
(ii)lm3烟气达到最高吸收率90%时,吸收后生成NaNO 的质量(假设上述吸收反应中,
2
反应①比反应②迅速。计算结果保留1位小数)。
第- 9 -页 | 共9页