文档内容
2025 年秋期长寿中学高二年级半期考试
化学试题
可能用到的相对原子质量:H-1 C-12 O-16 Sn-119 Cl-35.5
第Ⅰ卷(选择题 共42分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1. 下列过程中,化学反应速率的增大对人类有益的是( )
A. 金属的腐蚀 B. 食物的腐败
C. 塑料的老化 D. 氨的合成
2. 下列溶液肯定显酸性的是( )
A. pH<7 的溶液 B. 含H⁺的溶液
C. c(H⁺)>c(OH⁻)的溶液 D. 加酚酞显无色的溶液
3. 化学与生产、生活密切相关,下列说法错误的是( )
A. 施化肥时,将草木灰和硝酸铵混合使用效果更好
B. 明矾能用作净水剂,是因为其含有的Al³⁺水解生成具有吸附性的胶体
C. 用NaCO 溶液清洗油污时,加热可以增强去污效果
2 3
D. Na CO、NaS溶液水解显碱性,应用带橡胶塞的试剂瓶保存
2 3 2
4. 下列不能说明HClO是弱电解质的是( )
A. 用等浓度的盐酸和HClO溶液做导电能力实验,后者灯泡比前者暗
B. 次氯酸的稀溶液中HClO分子和ClO⁻离子共存
C. 向次氯酸钙溶液中通入适量二氧化硫,产生白色沉淀
D. 常温下,0.1mol•L⁻¹ HClO溶液的pH=4.2
5.医学研究证实:痛风病与关节滑液中形成的尿酸钠(NaUr)有关(NaUr增多,病情加重),其化学原理
为: △H<0,下列说法不正确的是( )
A.大量饮水会增大痛风病发作的可能性
B.秋冬季节更易诱发关节疼痛
C.饮食中摄入过多咸菜,会加重痛风病病情
D.患痛风病的人应少吃能代谢产生更多尿酸的食物
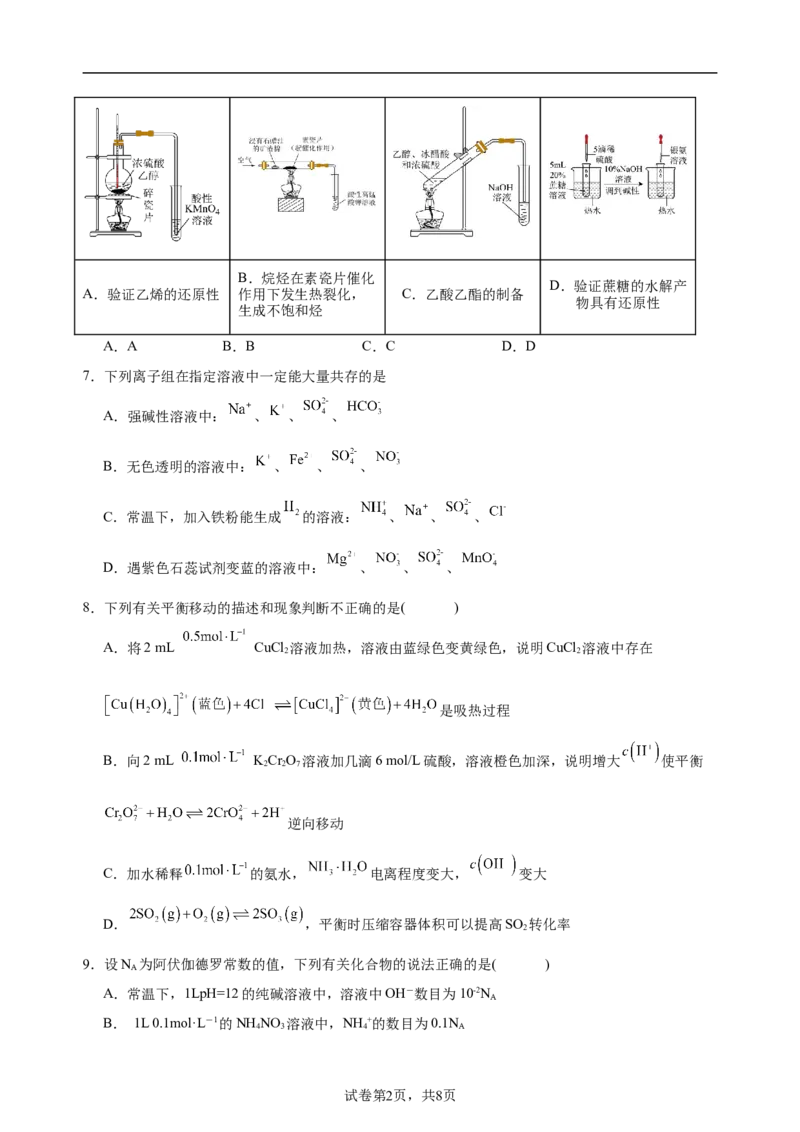
6.下列实验操作能达到目的的是( )B.烷烃在素瓷片催化
D.验证蔗糖的水解产
A.验证乙烯的还原性 作用下发生热裂化, C.乙酸乙酯的制备
物具有还原性
生成不饱和烃
A.A B.B C.C D.D
7.下列离子组在指定溶液中一定能大量共存的是
A.强碱性溶液中: 、 、 、
B.无色透明的溶液中: 、 、 、
C.常温下,加入铁粉能生成 的溶液: 、 、 、
D.遇紫色石蕊试剂变蓝的溶液中: 、 、 、
8.下列有关平衡移动的描述和现象判断不正确的是( )
A.将2 mL CuCl 溶液加热,溶液由蓝绿色变黄绿色,说明CuCl 溶液中存在
2 2
是吸热过程
B.向2 mL KCr O 溶液加几滴6 mol/L硫酸,溶液橙色加深,说明增大 使平衡
2 2 7
逆向移动
C.加水稀释 的氨水, 电离程度变大, 变大
D. ,平衡时压缩容器体积可以提高SO 转化率
2
9.设N 为阿伏伽德罗常数的值,下列有关化合物的说法正确的是( )
A
A.常温下,1LpH=12的纯碱溶液中,溶液中OH-数目为10-2N
A
B. 1L 0.1mol·L-1的NH NO 溶液中,NH +的数目为0.1N
4 3 4 A
试卷第2页,共8页C.1 mol N 与 3mol H 充分反应生成 NH 的分子数为 2N
2 3 3 A
D.25°C,1L 0.1 mol•L⁻¹HNO
3
溶液由水电离出的 c(H⁺) 为 0.1mol•L⁻¹
10.25°C时,0.1mol•L⁻¹ 的 NaOH 溶液和 0.1mol•L⁻¹ 的醋酸溶液等体积混合后,所得溶液中
c(Na⁺)、c(CH₃COO⁻) 的正确关系是( )
A. c(Na⁺) = c(CH
3
COO⁻) B. c(Na⁺) < c(CH
3
COO⁻)
C. c(Na⁺) > c(CH
3
COO⁻) D. 不能确定
11.已知: 遇铁氰化钾( 会产生特征的蓝色沉淀; 是难溶于水的黄色固体。将
的 溶液和 溶液等体积混合后,取混合液分别完成下列实验,均能说
明溶液中存在化学平衡“ ”的是( )
实验编号 实验操作 实验现象
① 滴入 溶液 溶液变红色
② 滴入 溶液 有黄色沉淀生成
③ 滴入 溶液 有蓝色沉淀生成
④ 滴入淀粉溶液 溶液变蓝色
A.①和② B.②和④ C.③和④ D.①和③
12.已知反应: , 时该反应的化学平衡常数 。一定条件下,
分别在甲、乙、丙3个恒容密闭容器中加入X和Y,反应体系中各物质的物质的量浓度的相关数据如表:
起始时物质的浓度/( ) 10分钟时物质的浓度/( )
容器 温度/
甲 400 1 1 0.5
乙 1 1 0.4
丙 400 1 2 a
下列说法中,正确的是( )
A.甲中,10分钟内X的化学反应速率:B.甲中,10分钟时反应已达到化学平衡状态
C.乙中,可能
D.丙中,
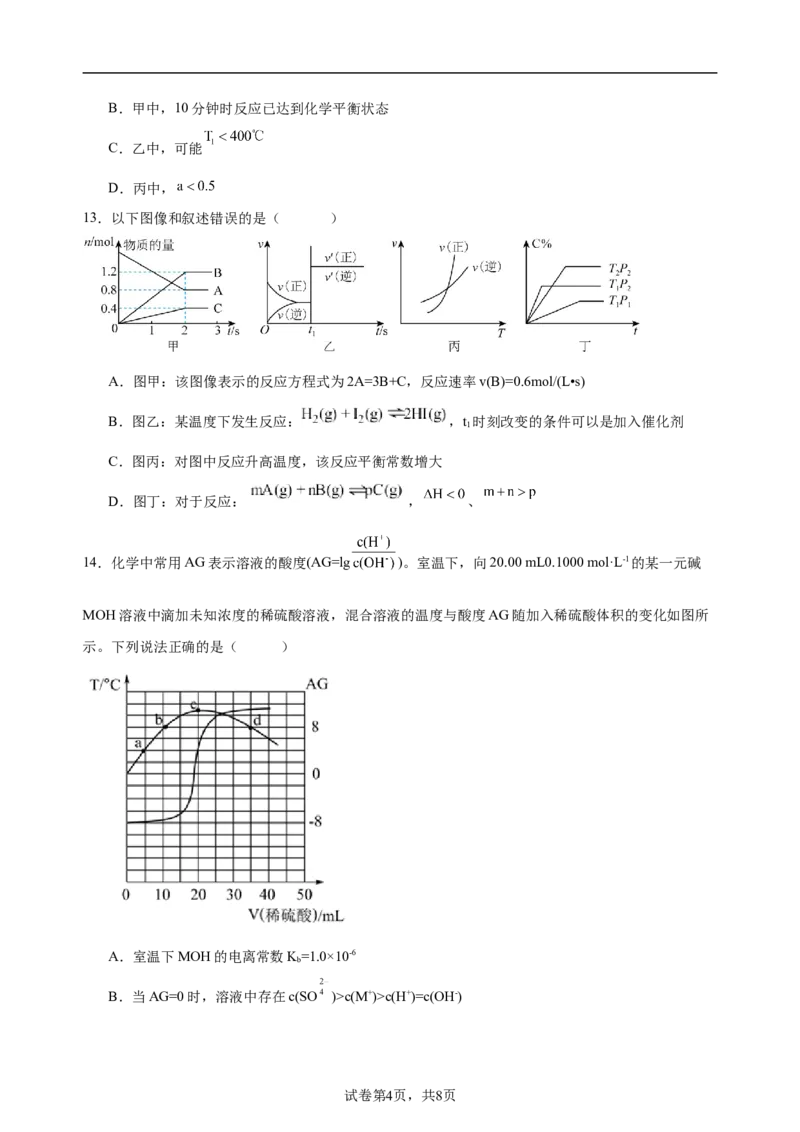
13.以下图像和叙述错误的是( )
A.图甲:该图像表示的反应方程式为2A=3B+C,反应速率v(B)=0.6mol/(L•s)
B.图乙:某温度下发生反应: ,t 时刻改变的条件可以是加入催化剂
1
C.图丙:对图中反应升高温度,该反应平衡常数增大
D.图丁:对于反应: , 、
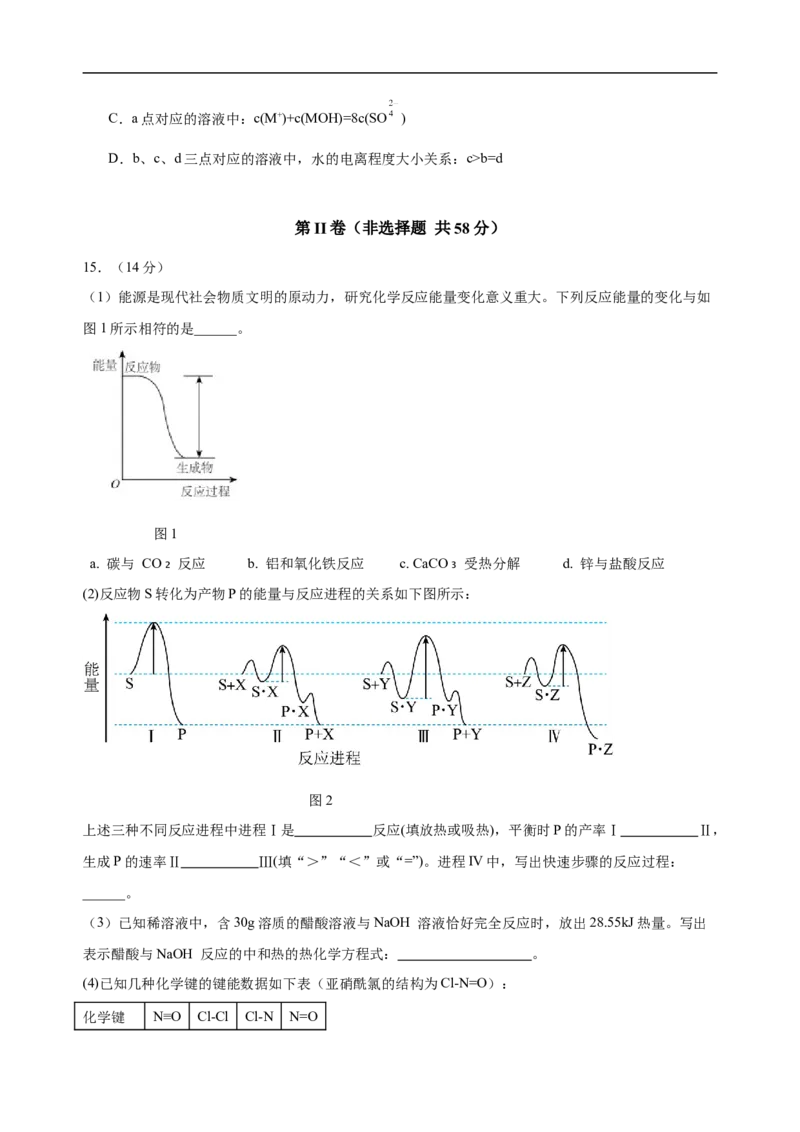
14.化学中常用AG表示溶液的酸度(AG=lg )。室温下,向20.00 mL0.1000 mol·L-1的某一元碱
MOH溶液中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所
示。下列说法正确的是( )
A.室温下MOH的电离常数K=1.0×10-6
b
B.当AG=0时,溶液中存在c(SO )>c(M+)>c(H+)=c(OH-)
试卷第4页,共8页C.a点对应的溶液中:c(M+)+c(MOH)=8c(SO )
D.b、c、d三点对应的溶液中,水的电离程度大小关系:c>b=d
第II卷(非选择题 共58分)
15.(14分)
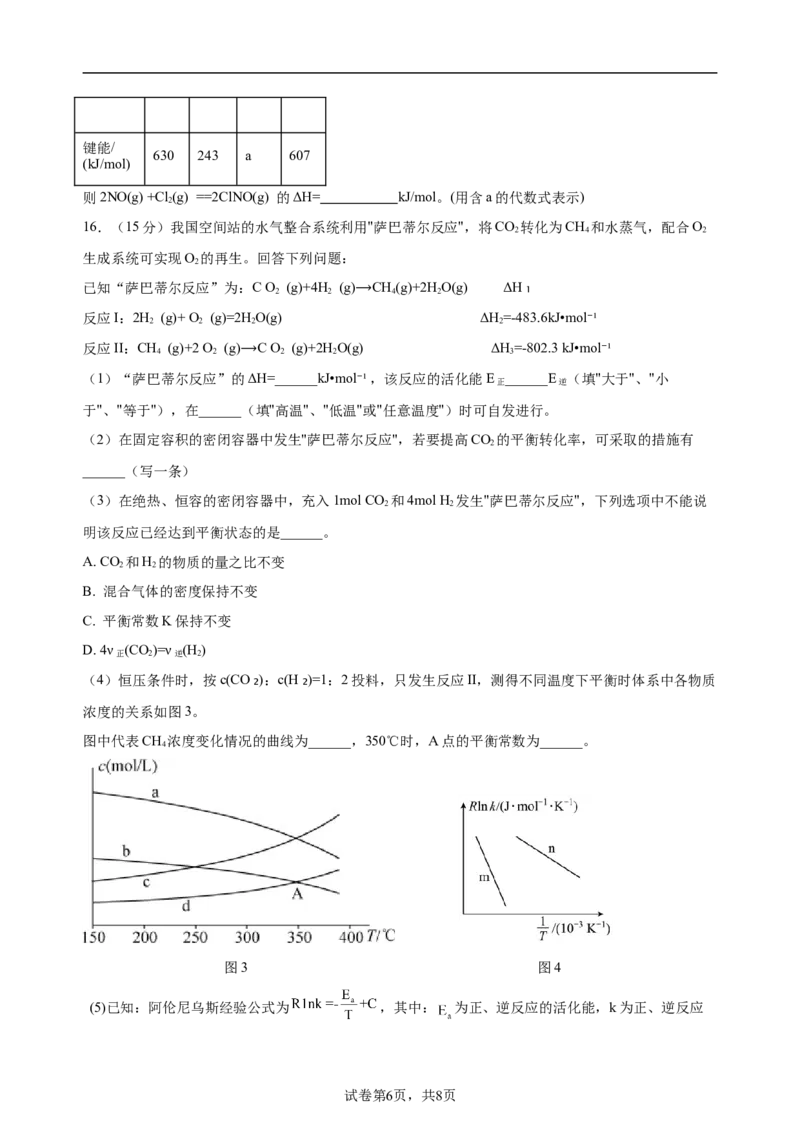
(1)能源是现代社会物质文明的原动力,研究化学反应能量变化意义重大。下列反应能量的变化与如
图1所示相符的是______。
图1
a. 碳与 CO₂ 反应 b. 铝和氧化铁反应 c. CaCO₃ 受热分解 d. 锌与盐酸反应
(2)反应物S转化为产物P的能量与反应进程的关系如下图所示:
图2
上述三种不同反应进程中进程Ⅰ是 反应(填放热或吸热),平衡时P的产率Ⅰ Ⅱ,
生成P的速率Ⅱ Ⅲ(填“>”“<”或“=”)。进程IV中,写出快速步骤的反应过程:
______。
(3)已知稀溶液中,含30g溶质的醋酸溶液与NaOH 溶液恰好完全反应时,放出28.55kJ热量。写出
表示醋酸与NaOH 反应的中和热的热化学方程式: 。
(4)已知几种化学键的键能数据如下表(亚硝酰氯的结构为Cl-N=O):
化学键 N≡O Cl-Cl Cl-N N=O键能/
630 243 a 607
(kJ/mol)
则2NO(g) +Cl (g) ==2ClNO(g) 的ΔH= kJ/mol。(用含a的代数式表示)
2
16.(15分)我国空间站的水气整合系统利用"萨巴蒂尔反应",将CO 转化为CH 和水蒸气,配合O
2 4 2
生成系统可实现O 的再生。回答下列问题:
2
已知“萨巴蒂尔反应”为:C O
2
(g)+4H
2
(g)⟶CH
4
(g)+2H
2
O(g) ΔH₁
反应I:2H
2
(g)+ O
2
(g)=2H
2
O(g) ΔH
2
=-483.6kJ•mol⁻¹
反应II:CH
4
(g)+2 O
2
(g)⟶C O
2
(g)+2H
2
O(g) ΔH
3
=-802.3 kJ•mol⁻¹
(1)“萨巴蒂尔反应”的ΔH=______kJ•mol⁻¹,该反应的活化能E
正
______E
逆
(填"大于"、"小
于"、"等于"),在______(填"高温"、"低温"或"任意温度")时可自发进行。
(2)在固定容积的密闭容器中发生"萨巴蒂尔反应",若要提高CO 的平衡转化率,可采取的措施有
2
______(写一条)
(3)在绝热、恒容的密闭容器中,充入1mol CO 和4mol H 发生"萨巴蒂尔反应",下列选项中不能说
2 2
明该反应已经达到平衡状态的是______。
A. CO 和H 的物质的量之比不变
2 2
B. 混合气体的密度保持不变
C. 平衡常数K保持不变
D. 4ν (CO)=ν (H )
正 2 逆 2
(4)恒压条件时,按c(CO₂):c(H₂)=1:2投料,只发生反应II,测得不同温度下平衡时体系中各物质
浓度的关系如图3。
图中代表CH 浓度变化情况的曲线为______,350℃时,A点的平衡常数为______。
4
图3 图4
(5)已知:阿伦尼乌斯经验公式为 ,其中: 为正、逆反应的活化能,k为正、逆反应
试卷第6页,共8页速率常数,R和C为常数。某实验小组针对反应I进行实验,依据实验数据获得如图4曲线。曲线中表
示正反应速率的是 (填“m”或“n”)。
17. (15分)滴定法是一种常见的定量实验分析法,常见的滴定除了有酸碱中和滴定,还有氧化还原滴
定。
I. 某同学用0.1000mol•L⁻¹的盐酸标准溶液滴定未知浓度的NaOH溶液。请回答下列问题:
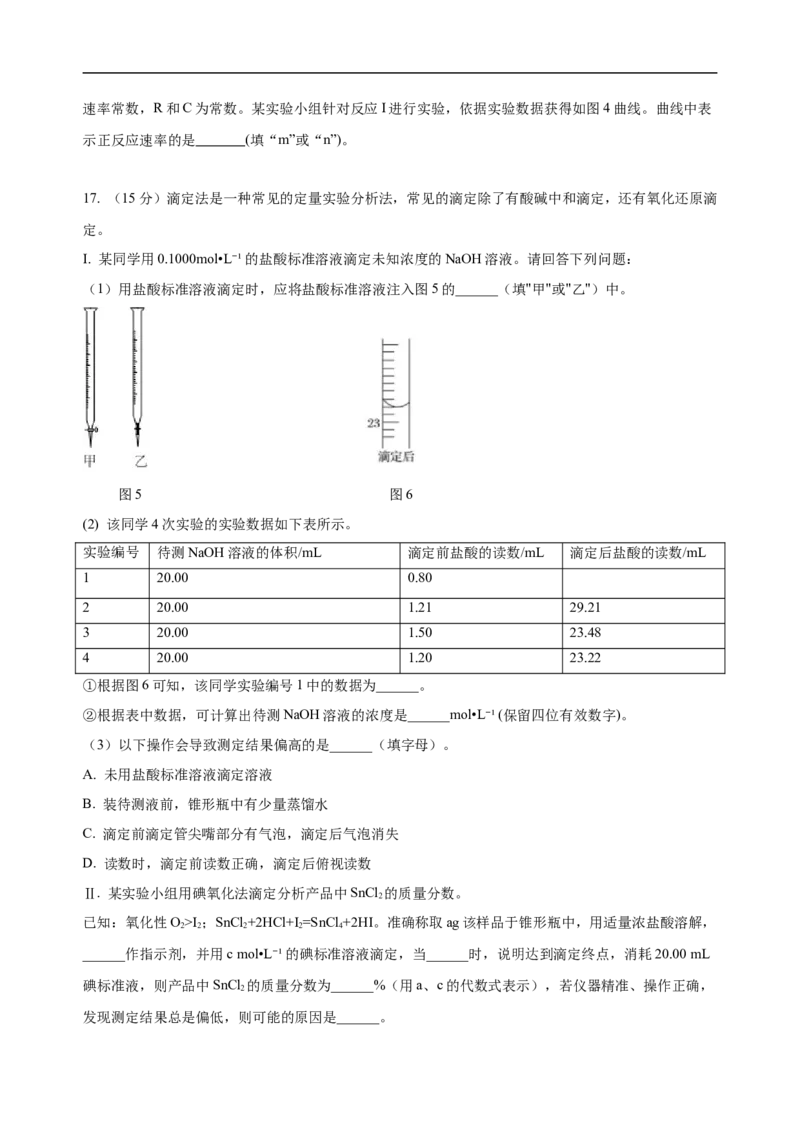
(1)用盐酸标准溶液滴定时,应将盐酸标准溶液注入图5的______(填"甲"或"乙")中。
图5 图6
(2) 该同学4次实验的实验数据如下表所示。
实验编号 待测NaOH溶液的体积/mL 滴定前盐酸的读数/mL 滴定后盐酸的读数/mL
1 20.00 0.80
2 20.00 1.21 29.21
3 20.00 1.50 23.48
4 20.00 1.20 23.22
①根据图6可知,该同学实验编号1中的数据为______。
②根据表中数据,可计算出待测NaOH溶液的浓度是______mol•L⁻¹(保留四位有效数字)。
(3)以下操作会导致测定结果偏高的是______(填字母)。
A. 未用盐酸标准溶液滴定溶液
B. 装待测液前,锥形瓶中有少量蒸馏水
C. 滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D. 读数时,滴定前读数正确,滴定后俯视读数
Ⅱ. 某实验小组用碘氧化法滴定分析产品中SnCl 的质量分数。
2
已知:氧化性O>I ;SnCl +2HCl+I =SnCl +2HI。准确称取ag该样品于锥形瓶中,用适量浓盐酸溶解,
2 2 2 2 4
______作指示剂,并用c mol•L⁻¹的碘标准溶液滴定,当______时,说明达到滴定终点,消耗20.00 mL
碘标准液,则产品中SnCl 的质量分数为______%(用a、c的代数式表示),若仪器精准、操作正确,
2
发现测定结果总是偏低,则可能的原因是______。18. (14分)水溶液广泛存在于生命体及赖以生存的环境中,许多化学反应都是在水溶液中进行的,请回
答下列问题:
(1)写出CHCOONa溶液水解的离子方程式是______。
3
(2)将0.1mol•L⁻¹CH
3
COOH加水稀释,有关稀释后的溶液,下列说法正确的是______。
A. 电离程度增大
B. 增大
C. 溶液导电性增强
D. 溶液中CHCOOH分子数目增多
3
(3)某温度下,纯水的c(H⁺)=2×10⁻⁷mol•L⁻¹,若温度不变,某稀盐酸中c(H⁺)=2×10⁻²mol•L⁻¹,则此
溶液中由水电离产生的c(H⁺)=______mol•L⁻¹。
(4)25℃时,等浓度的下列4种溶液:
① NH Cl ② CHCOONH ③ NH HSO ④ NH •H O
4 3 4 4 4 3 2
这4种溶液中c(NH 4⁺)由大到小的顺序是______(用序号表示)。
(5)25℃时,将pH=11的Ba(OH) 溶液VₐL与pH=2的盐酸VL混合,若所得溶液pH=4,则Vₐ:
2 b
V=______。
b
(6)常温下,浓度均为0.1mol•L⁻¹的下列5种溶液的pH如表所示:
溶质 CHCOONa NaHCO NaCO NaClO NaCN
3 3 2 3
pH 8.8 9.7 11.6 10.3 11.1
①在相同条件下,①CHCOOH、②HCO、③HClO、④HCN溶液的酸性由强到弱的顺序为______
3 2 3
(用序号表示)。
②将少量二氧化碳通入NaClO溶液中的离子方程式为______。
试卷第8页,共8页参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 D C A C A D C C A B
题号 11 12 13 14
答案 A C A C
15.(1)b
(2) 放热 ; = ; > ;S+X → S-X (或 S+X → P-X)
(3) CHCOOH(aq) +NaOH(aq)=CH COONa(aq)+H O H= -57.1kJ·mol-1
3 3 2
(4)289-2a △
16.(1)-164.9, 大于, 低温
(2)增大H 的浓度(或压强) (或“降低温度”)
2
(3)A, B, D
(4)d ;1
(5)n
17.Ⅰ(1)甲
(2)22.80;0.1100
(3)C
Ⅱ淀粉溶液;溶液恰好由无色变为蓝色且半分钟内不褪色; ; Sn2+被空气中
O 氧化而部分变质
2
18. (1)CH
3
COO⁻ + H
2
O ⇌ CH
3
COOH + OH⁻
(2)A B
(3)2 × 10⁻¹² (或 5 × 10⁻¹³)
(4)③ > ① > ② > ④
(5)9 : 1
(6) ① ① > ② > ③ > ④ ② CO 2 + ClO⁻ + H 2 O = HClO + HCO 3⁻