文档内容
2024/2025学年度春学期高三第一次联考
化学试题
命题人:刘春来 审题人:汤其来 做题人:陈锦阳
注意事项:
1.请将答案填写在答题卡上,写在试题卷或其他区域均无效。
2.本试卷总分100分,考试时间75分钟。
3.可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 K-39
I-127 Pb-207
选 择 题 (共39分)
一、单项选择题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项符合
题意。
1.化学与人类生活、能源开发、资源利用等密切相关。下列说法正确的是
A.塑料奶瓶比玻璃奶瓶更有利于健康,且更加经久耐用
B.研发使用高效催化剂,可提高反应中原料的转化率
C.硅燃烧放出的热量多,且燃烧产物对环境污染程度低,可做“未来石油”
D.用KFeO 取代Cl 处理饮用水,可杀菌消毒,但不能沉降水中的悬浮物
2 4 2
2.下列有关化学用语表示正确的是
A.HClO的结构式:H-O-Cl B.对硝基甲苯的结构简式:
C.CHF 的电子式: D.CO 的比例模型:
2 2 2
3.实验室制取SO 并回收CuSO 的实验原理及装置不能达到实验目的是
2 4
CuSO 溶液
气体 4
浓硫酸 气体
铜片 NaOH溶液
浓硫酸
C.吸收尾气 D.将硫酸铜溶
A.制取SO B.干燥SO
2 2 中 的 S O 液蒸发浓缩
2
4.下列表示对应化学反应的离子方程式正确的是A.醋酸溶液与Mg(OH) 反应:Mg(OH) +2H+===Mg2++2HO
2 2 2
B.明矾溶液中滴加过量氨水:Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
C.小苏打溶液中加足量澄清石灰水:2HCO+Ca2++2OH-===CaCO ↓+2HO+CO
3 2
D.SO 通入FeCl 溶液中:SO +Fe3++2HO===SO+Fe2++4H+
2 3 2 2
阅读下列资料,完成5~7题:
卤族元素单质及其化合物应用广泛。(CN) 具有与卤素单质相似的化学性质。F 在常
2 2
温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的NaSO 反应生成硫酰氟(SO F)。
2 4 2 2
CaF 与浓硫酸反应可制得 HF,常温下,测得氟化氢的相对分子质量约为 37。SO 通入
2 2
KClO 酸性溶液中可制得黄绿色气体ClO ,该气体常用作自来水消毒剂。工业用Cl 制备
3 2 2
TiCl 的热化学方程式为TiO(s)+2Cl(g)+2C(s) TiCl (g)+2CO(g) ΔH = -
4 2 2 4
49kJ·mol-1。
5.下列说法不正确的是
A.(CN) 分子中含有非极性键
2
B.ClO 、SO 中心原子的杂化方式均为sp3
C.常温下,氟化氢不可能以(HF) 分子的形式存在
2
D.F 与熔融NaSO 反应时一定有氧元素化合价升高
2 2 4
6.下列物质性质与用途具有对应关系的是
A.铜单质化学性质不活泼,可用于制作储存F 的容器
2
B.ClO 呈黄绿色,可用于自来水消毒
2
C.SO 具有氧化性,可用于与KClO 反应制ClO
2 3 2
D.浓硫酸沸点很高,可用于与CaF 反应制HF
2
7.下列关于反应TiO(s)+2Cl(g)+2C(s) TiCl (g)+2CO(g)的说法不正确的是
2 2 4
A.保持其他条件不变,平衡时加入TiO,平衡不移动
2
B.反应生成1 mol TiCl ,转移电子数目为4×6.02×1023
4
C.及时分离出CO,有利于TiCl 生成
4
D.保持其他条件不变,平衡时通入Cl,达到新平衡时 变小
2
8.分枝酸在微生物、植物的芳香族氨基酸的生物合成系统中作为中间体,其结构简式如图。下列关于分枝酸的叙述不正确的是
A.分枝酸的分子式为C HO
10 8 6
B.1mol分枝酸最多消耗2molNaOH
C.分枝酸分子中含2个手性碳原子
D.一定条件下,分枝酸可发生取代、加成、氧化和聚合反应
9.下列物质的制备与工业生产不相符的是
⃗ O /催化剂,△ ⃗ O 和H O
①NH 2 NO 2 2 HNO
3 3
⃗MnO 加热 ⃗澄清石灰水
②浓HCl 2 Cl 漂白粉
2
⃗加热 ⃗ 电解
③MgCl (aq) 无水MgCl Mg
2 2
⃗NH 和CO ⃗ 加热
④饱和NaCl(aq) 3 2 NaHCO Na CO
3 2 3
⑤铝土矿
⃗NaOH溶液
NaAlO 溶液
⃗足量CO
2Al(OH)
⃗灼烧
Al O
⃗电解
Al
2 3 2 3
A.①④ B.①⑤ C.②③ D.③⑤
10.钠离子电池是利用Na+在电极之间“嵌脱”实现充放电(原理如图所示),工作时总反应
放电
为NaMO +nC Na MO +Na C (M为一种过渡元
x 2 ⇌ x-y 2 y n
充电
素)。下列说法正确的是
A.放电时,Na+由Y极通过交换膜移向X极
B.放电时,正极反应式为NaMO +ye-=Na
x 2 x-
MO +yNa+
y 2
C.充电时,过渡元素M发生氧化反应
D.用铅蓄电池对该钠离子电池充电,铅蓄电池中每消耗20.7g铅,钠离子电池正极区
域质量减少4.6g
11.对下列实验现象或操作解释错误的是
现象或操作 解 释
KI淀粉溶液中滴入氯水变蓝,再通入SO ,蓝色
A 2 SO 具有漂白性
2
褪去
配制SnCl 溶液时,先将SnCl 溶于适量稀盐酸,
2 2 抑制Sn2+水解,并防止Sn2+
B 再用蒸馏水稀释,最后在试剂瓶中加入少量的锡
被氧化为Sn4+
粒
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉 不能说明该溶液中一定含有
C
淀生成 SO 2-
4向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中
D K (AgCl)>K (AgI)
sp sp
滴加少量AgNO 溶液,出现黄色沉淀
3
12. 硫代硫酸钠( )的制备和应用相关流程如图所示。
已知:25℃时, 的 , ; 的
,
下列说法正确的是
A. 步骤1所得的溶液中:
.
B 步骤1过程中pH=8时,
C. 步骤3所得 清的液中:
D. 步骤3的离子方程式为:
13.由CO 催化加氢制CHOH的反应体系中,发生的主要反应如下。
2 3
反应I:CO(g)+H(g)=CO(g)+HO(g);ΔH=+41.1kJ•mol-1。
2 2 2
反应II:CO(g)+3H(g)=CH OH(g)+H O(g);ΔH=-49.0kJ•mol-1。
2 2 3 2
在其他条件相同的情况下,按n(CO)∶n(H )=1∶3(总量一定)投料于恒容密闭容器中进行反
2 2
应,CO 的平衡转化率和甲醇的选择性[甲醇的选择性:n (CH OH) ]随温度
2 生成 3
n (CH OH)+n (CO)
生成 3 生成
的变化趋势如图所示。下列说法不正确的是
A.若反应2CHOH(g)=CH OCH (g)+HO(g);ΔH=-24.5kJ•mol-1,则由H 和CO制备二
3 3 3 2 2
甲醚的热化学方程式:2CO(g)+4H(g)=CH OCH (g)+HO(g);ΔH=-204.7kJ•mol-1
2 3 3 2
B.根据图中数据,温度选择553K,达到平衡时,反应体系内甲醇的产量最高
c(CH OH)
C.473~513K范围内,温度升高,平衡时的 3 逐渐增大
c(H O)
2
D.随着温度的升高,CO 的平衡转化率增加但甲醇的选择性降低,其原因可能是反应
2
II平衡逆向移动幅度弱于反应I正向移动幅度
二、非选择题:共4题,共61分
14.(16分)钴是重要的金属材料,以镍电解钴渣[主要成分为Co(OH) 、Fe(OH) 、
3 3
Ni(OH) 等氢氧化物]为原料制备氢氧化高钴Co(OH) 的流程如下:
3 3
已知:①氧化性:
② 一般在 时,能被氧化水解生成Ni(OH) 沉淀.
3
(1)基态Fe3+的电子排布式为____________.
(2)“溶解”得到的溶液中含有的主要阳离子有H+、Co2+、____________.
(3)“除铁”过程加入NaCO 的作用是____________.
2 3
(4)“一次沉钴”时主要反应的离子方程式为____________;此过程会夹带生成少量的
Ni(OH) 沉淀,利用含Co2+母液淘洗沉淀的目的是____________.
3
(5)“二次沉钴”过程生成Co(OH) 的总化学反应方程式为____________.
3(6)钴氧化物和Al O 按照适量的比例高温煅烧可得到钴蓝,钴蓝可用于青花瓷的颜料.
2 3
钴蓝晶体是由图甲所示的结构构成.图甲包含Ⅰ型和Ⅱ型两种小立方体.图乙是钴蓝的晶
胞,已知该晶胞的顶点和面心为钴原子.
①图乙所示字母中,Ⅰ型小立方体分别是a、____________(填字母序号).
②一个钴蓝晶胞中包含Con+、Al3+、O2-的个数依次为____________.
15.(16分)有机物F是一种治疗关节炎止痛药,合成F的一种传统法路线如下:
R
RCl
AlCl
已 知 : ① ; ② 3 ; ③
OH COOH
CO、Pd R、R'表示烃基
R R' R R'
。
(1)B中含氧官能团的名称为 。
(2) 已知D经过反应可生成E,E的分子式C H N ,写出E的结构简式
13 17
。
(3) A→B的反应类型为 、A→B的反应方程式为 。
(4) 写出同时满足下列条件的F的一种同分异构体的结构简式: (写一
种)。
①能发生银镜反应;②能发生水解反应,其水解产物之一能与 FeCl 溶液发生显色反
3
应;③分子中只有4种不同化学环境的氢。
(5)合成F( )的一种改良法是以2-甲基-1-丙醇( )、苯、
乙酸酐[(CH CO) O]为原料来合成,写出有关F的合成路线流程图(无机试剂任选)。合成
3 2
路线流程图示例如下:
NaOH溶液
HBr
H
2
C=CH
2
CH
3
CH
2
Br
△
CH
3
CH
2
OH
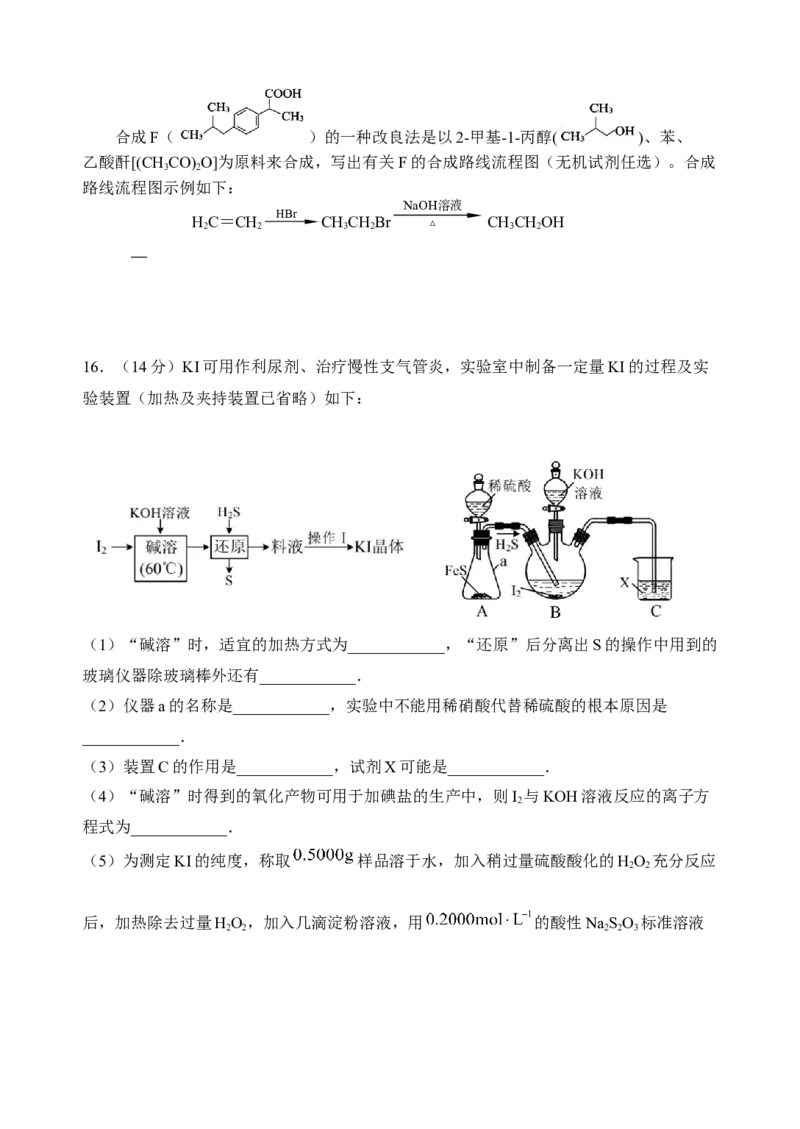
16.(14分)KI可用作利尿剂、治疗慢性支气管炎,实验室中制备一定量KI的过程及实
验装置(加热及夹持装置已省略)如下:
(1)“碱溶”时,适宜的加热方式为____________,“还原”后分离出S的操作中用到的
玻璃仪器除玻璃棒外还有____________.
(2)仪器a的名称是____________,实验中不能用稀硝酸代替稀硫酸的根本原因是
____________.
(3)装置C的作用是____________,试剂X可能是____________.
(4)“碱溶”时得到的氧化产物可用于加碘盐的生产中,则I 与KOH溶液反应的离子方
2
程式为____________.
(5)为测定KI的纯度,称取 样品溶于水,加入稍过量硫酸酸化的HO 充分反应
2 2
后,加热除去过量HO,加入几滴淀粉溶液,用 的酸性NaSO 标准溶液
2 2 2 2 3滴定 ,终点时消耗14.50ml标准溶液,则样品的纯度
为____________(写出计算过程,计算结果保留两位有效数字).
17(15分).消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。
(1)已知:N(g)+O(g)=2NO(g) ΔH=a kJ·mol-1
2 2
2NO(g)+O(g)=2NO (g) ΔH=b kJ·mol-1
2 2
4NH (g)+5O(g)=4NO(g)+6HO(1) ΔH=c kJ·mol-1
3 2 2
则反应8NH (g)+6NO (g)=7N(g)+12HO(1) △H= kJ·mol-1
3 2 2 2
(2)氮肥厂的废水中氮元素以NH ·HO、NH 和NH 的形式存在,对氨氮废水无害化处理
3 2 3
已成为全球科学研究热点,下面是两种电化学除氨氮的方法。
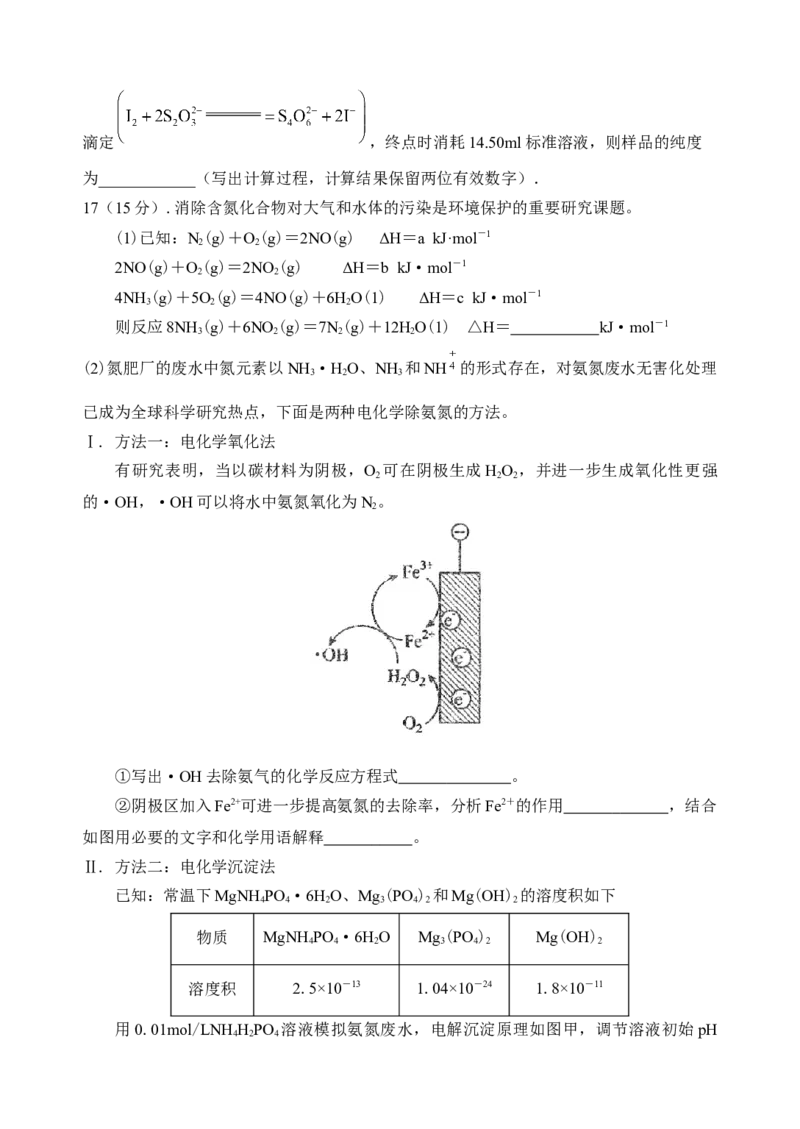
Ⅰ. 方法一:电化学氧化法
有研究表明,当以碳材料为阴极,O 可在阴极生成HO ,并进一步生成氧化性更强
2 2 2
的·OH,·OH可以将水中氨氮氧化为N。
2
①写出·OH去除氨气的化学反应方程式 。
②阴极区加入Fe2+可进一步提高氨氮的去除率,分析Fe2+的作用 ,结合
如图用必要的文字和化学用语解释 。
Ⅱ. 方法二:电化学沉淀法
已知:常温下MgNH PO ·6HO、Mg(PO ) 和Mg(OH) 的溶度积如下
4 4 2 3 4 2 2
物质 MgNH PO ·6HO Mg(PO ) Mg(OH)
4 4 2 3 4 2 2
溶度积 2.5×10-13 1.04×10-24 1.8×10-11
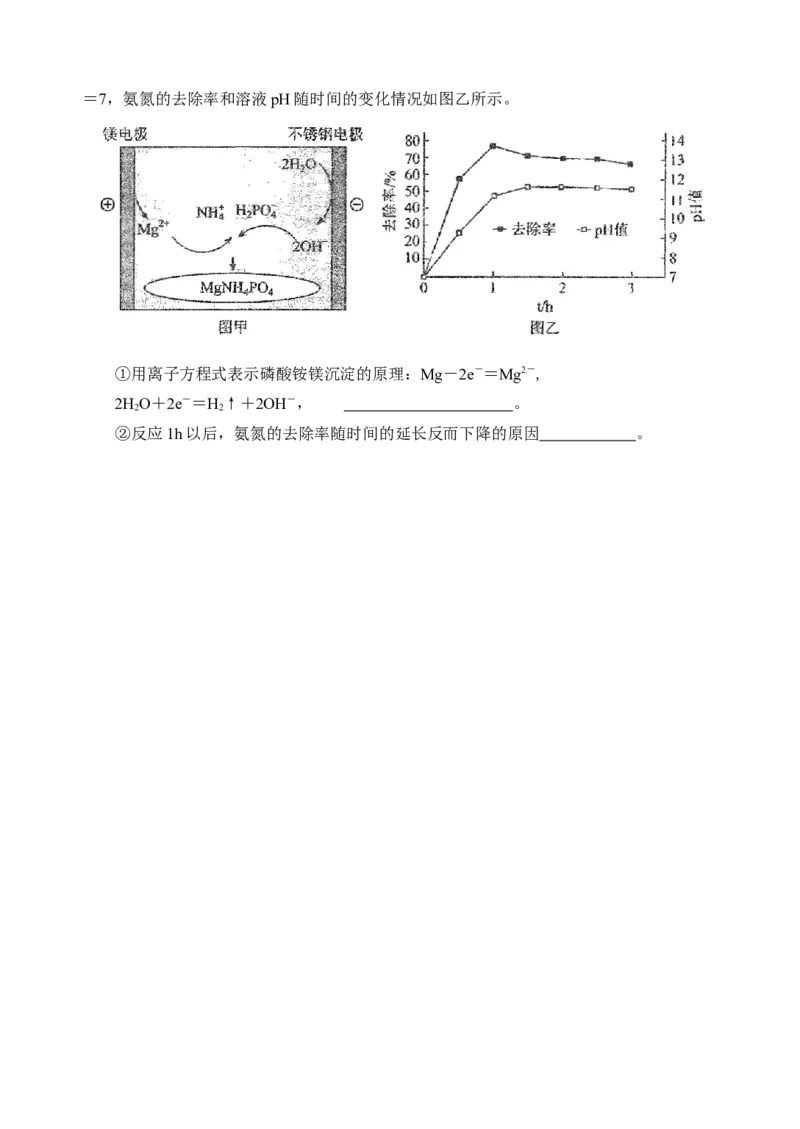
用0.01mol/LNH HPO 溶液模拟氨氮废水,电解沉淀原理如图甲,调节溶液初始pH
4 2 4=7,氨氮的去除率和溶液pH随时间的变化情况如图乙所示。
①用离子方程式表示磷酸铵镁沉淀的原理:Mg-2e-=Mg2-,
2HO+2e-=H↑+2OH-, 。
2 2
②反应1h以后,氨氮的去除率随时间的延长反而下降的原因 。