文档内容
南宁二中 2024 届 5 月月考试题
化 学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H 1 N14 O 16 Mg 24 Fe 56 Zn 65 Ga 70
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意。
1. 陆川青砖青瓦烧制技艺、横州铜器制作技艺、桂平乳泉井酒酿造技艺、东兰壮族服饰制作技艺等入选了广西第
九批区级非遗代表性项目。下列描述错误的是
A.陆川青砖青瓦呈现青色的原因是含有二价铁
B.横州出土的“鸟纹变形羽人纹铜鼓”表面的铜绿主要成分是碱式碳酸铜
C.桂平乳泉井酒的酿造过程涉及蒸馏操作
D.东兰壮族服饰原材料的主要成分为棉、麻,点燃时有烧焦羽毛的气味
2.化学语言是表达化学思想不可缺少的重要工具。下列说法正确的是
A B C D
激发态硼原子的电子排布
HCl中共价键的电子云图 HS的电子式 的 模型
图 2
A.A B.B C.C D.D
3. 下列实验装置或操作不能达到实验目的的是
甲 乙 丙 丁
A.图甲的操作为将定容后的溶液摇匀
B.图乙操作可用于氢氧化钠标准溶液滴定未知浓度的盐酸
C.用丙装置观察钠在空气中燃烧的现象
D.用丁装置检验浓硫酸与铜反应后的产物中是否含有
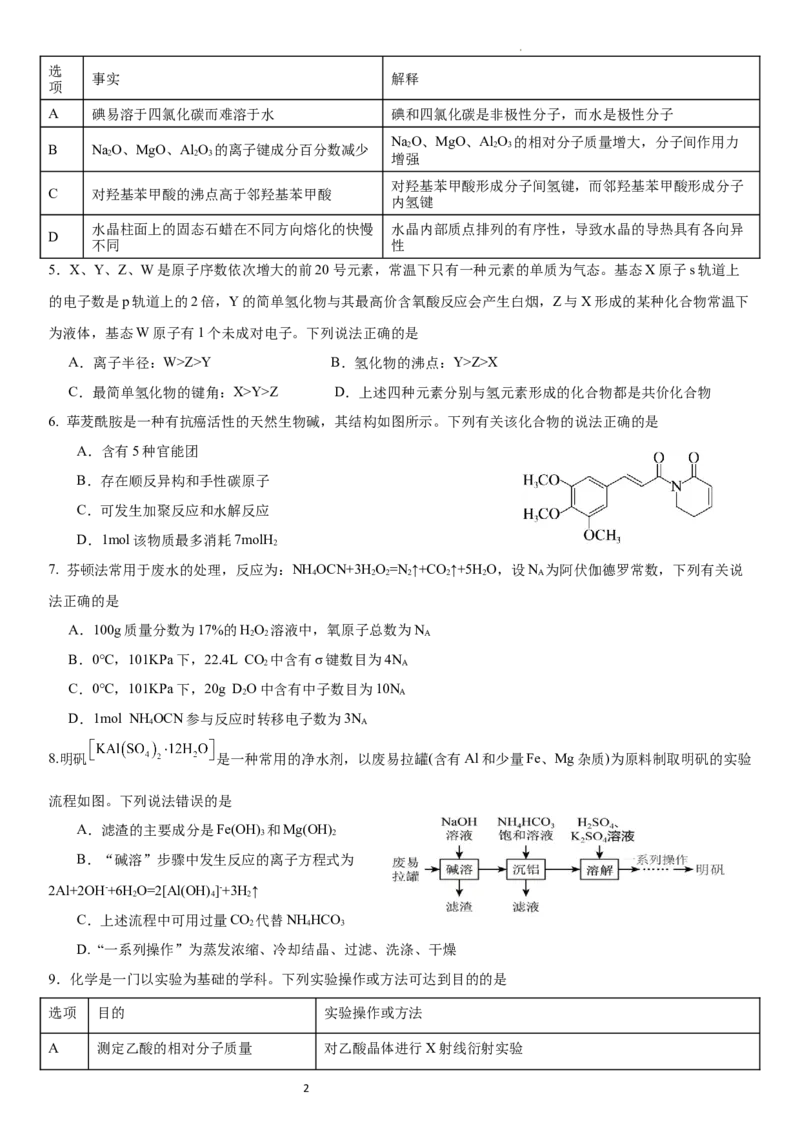
4.下列关于事实的解释错误的是
1
学科网(北京)股份有限公司选
事实 解释
项
A 碘易溶于四氯化碳而难溶于水 碘和四氯化碳是非极性分子,而水是极性分子
NaO、MgO、Al O 的相对分子质量增大,分子间作用力
B NaO、MgO、Al O 的离子键成分百分数减少 2 2 3
2 2 3 增强
对羟基苯甲酸形成分子间氢键,而邻羟基苯甲酸形成分子
C 对羟基苯甲酸的沸点高于邻羟基苯甲酸
内氢键
水晶柱面上的固态石蜡在不同方向熔化的快慢 水晶内部质点排列的有序性,导致水晶的导热具有各向异
D
不同 性
5.X、Y、Z、W是原子序数依次增大的前20号元素,常温下只有一种元素的单质为气态。基态X原子s轨道上
的电子数是p轨道上的2倍,Y的简单氢化物与其最高价含氧酸反应会产生白烟,Z与X形成的某种化合物常温下
为液体,基态W原子有1个未成对电子。下列说法正确的是
A.离子半径:W>Z>Y B.氢化物的沸点:Y>Z>X
C.最简单氢化物的键角:X>Y>Z D.上述四种元素分别与氢元素形成的化合物都是共价化合物
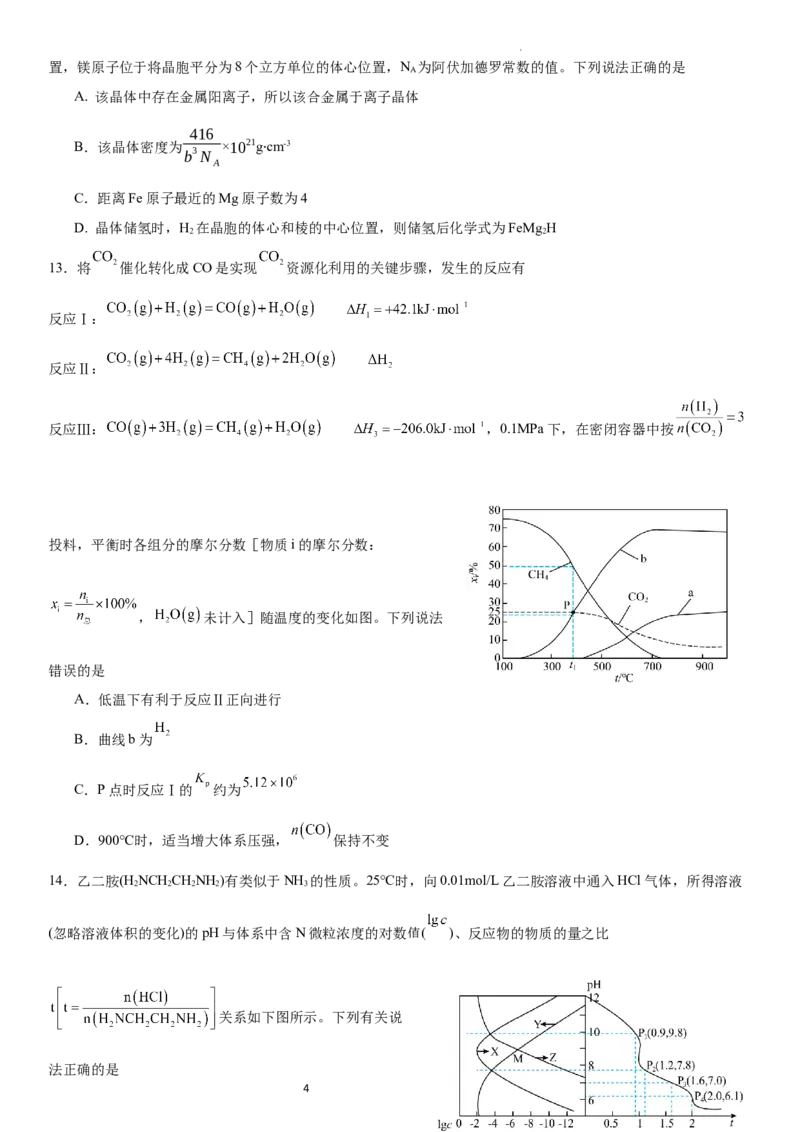
6. 荜茇酰胺是一种有抗癌活性的天然生物碱,其结构如图所示。下列有关该化合物的说法正确的是
A.含有5种官能团
B.存在顺反异构和手性碳原子
C.可发生加聚反应和水解反应
D.1mol该物质最多消耗7molH
2
7. 芬顿法常用于废水的处理,反应为:NH OCN+3H O=N ↑+CO ↑+5H O,设N 为阿伏伽德罗常数,下列有关说
4 2 2 2 2 2 A
法正确的是
A.100g质量分数为17%的HO 溶液中,氧原子总数为N
2 2 A
B.0℃,101KPa下,22.4L CO 中含有σ键数目为4N
2 A
C.0℃,101KPa下,20g DO中含有中子数目为10N
2 A
D.1mol NH OCN参与反应时转移电子数为3N
4 A
8.明矾 是一种常用的净水剂,以废易拉罐(含有Al和少量Fe、Mg杂质)为原料制取明矾的实验
流程如图。下列说法错误的是
A.滤渣的主要成分是Fe(OH) 和Mg(OH)
3 2
B.“碱溶”步骤中发生反应的离子方程式为
2Al+2OH-+6H O=2[Al(OH) ]-+3H ↑
2 4 2
C.上述流程中可用过量CO 代替NH HCO
2 4 3
D. “一系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
9.化学是一门以实验为基础的学科。下列实验操作或方法可达到目的的是
选项 目的 实验操作或方法
A 测定乙酸的相对分子质量 对乙酸晶体进行X射线衍射实验
2
学科网(北京)股份有限公司B 比较Mg和Al的金属性强弱 向浓度均为 和 溶液中滴加浓氨水至过量
C 证明压强影响平衡移动 对 反应容器压缩容积,混合气体的颜色变深
比较室温下 、 溶液中滴加少量 溶液,振荡充分后,再滴
D
溶度积的大小 加几滴
10.一种能捕获和释放 的电化学装置如下图所示。其中a、b均为惰性电极,电解质溶液均为KCl溶液。当K连
接 时,b极区溶液能捕获通入的 。下列说法错误的是
A.K连接 时,a连接电源正极
B.K连接 时,b极发生反应:
C.K连接 时,a极区 的值增大
D.该装置通过“充电”和“放电”调控b极区溶液pH,捕获和释放
11. 氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。
下列离子方程式书写错误的是
A.过程I将 转化为NH : +OH- NH ↑+H O
3 3 2
B.过程II将残留的NH ∙H O转化N:3ClO-+2NH∙H O=3Cl-+N ↑+5H O
3 2 2 3 2 2 2
C.过程III将残留的NaClO转化NaCl:ClO-+SO 2-=Cl-+SO 2-
3 4
D.NaSO 溶液呈碱性的原因:SO 2-+2H O=HSO +2OH-
2 3 3 2 2 3
12.铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶点和面心 的位
3
学科网(北京)股份有限公司置,镁原子位于将晶胞平分为8个立方单位的体心位置,N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 该晶体中存在金属阳离子,所以该合金属于离子晶体
416
B.该晶体密度为 ×1021g·cm-3
b3N
A
C.距离Fe原子最近的Mg原子数为4
D. 晶体储氢时,H 在晶胞的体心和棱的中心位置,则储氢后化学式为FeMg H
2 2
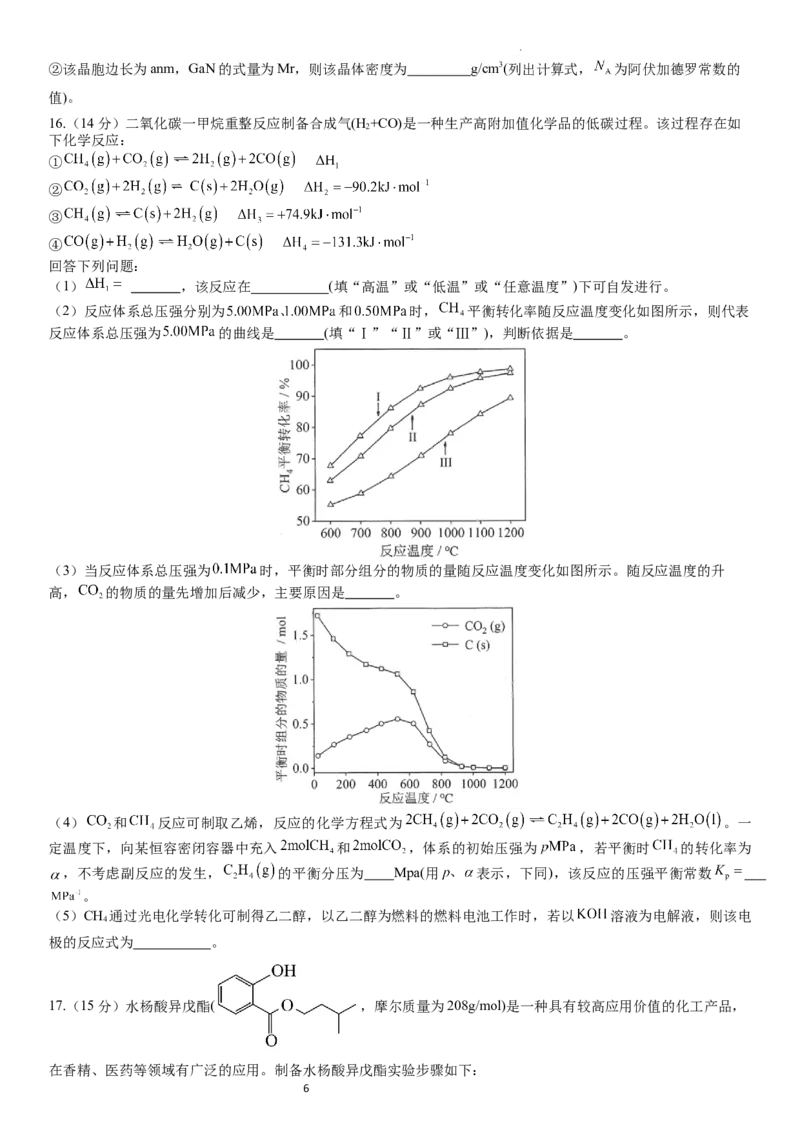
13.将 催化转化成CO是实现 资源化利用的关键步骤,发生的反应有
反应Ⅰ:
反应Ⅱ:
反应Ⅲ: ,0.1MPa下,在密闭容器中按
投料,平衡时各组分的摩尔分数[物质i的摩尔分数:
, 未计入]随温度的变化如图。下列说法
错误的是
A.低温下有利于反应Ⅱ正向进行
B.曲线b为
C.P点时反应Ⅰ的 约为
D.900℃时,适当增大体系压强, 保持不变
14.乙二胺(H NCH CHNH )有类似于NH 的性质。25℃时,向0.01mol/L乙二胺溶液中通入HCl气体,所得溶液
2 2 2 2 3
(忽略溶液体积的变化)的pH与体系中含N微粒浓度的对数值( )、反应物的物质的量之比
关系如下图所示。下列有关说
法正确的是
4
学科网(北京)股份有限公司A.图中曲线Y表示
B.P 所示溶液:
3
C.P 所示溶液:
4
D.图中M点对应的
二、非选择题:本题共4小题,共58分。
15.(14分)氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓Ga(Fe O)、铁酸锌ZnFe O、
2 2 4 3 2 4
SiO]制备GaN的工艺流程如下:
2
已知:
①Ga与Al同主族,化学性质相似。
②常温下,K [Zn(OH) ]=10-16.6,K [Ga(OH)]=10-35.1,K [Fe(OH) ]=10-38.5。
sp 2 sp 3 sp 3
③Ga3+、Fe3+在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
反萃取率/%
盐酸浓度/mol/L
Ga3+ Fe3+
2 86.9 9.4
4 69.1 52.1
6 17.5 71.3
回答下列问题:
(1)“酸浸”时能提高反应速率的措施有 (答1条即可)
(2)“酸浸”所得浸出液中Ga3+、Zn2+浓度分别为0.21g/L、65g/L。常温下,为尽可能多地提取Ga3+并确保不混
入Zn(OH) ,用CaO“调pH”时须不能大于 (假设调pH时溶液体积不变)
2
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a= mol/L,b= mol/L(选填上表中盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致Ga3+的沉淀率降低,原因是 (用离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的GaO 与NH 在高温下反应可制得GaN,同时生成另一种
2 3 3
产物,该反应化学方程式为 。
(6)GaN晶体的一种立方晶胞如图下所示。
①Ga原子价电子有 种空间运动状态。
5
学科网(北京)股份有限公司②该晶胞边长为anm,GaN的式量为Mr,则该晶体密度为 g/cm3(列出计算式, 为阿伏加德罗常数的
值)。
16.(14分)二氧化碳一甲烷重整反应制备合成气(H +CO)是一种生产高附加值化学品的低碳过程。该过程存在如
2
下化学反应:
①
②
③
④
回答下列问题:
(1) ,该反应在 (填“高温”或“低温”或“任意温度”)下可自发进行。
(2)反应体系总压强分别为 和 时, 平衡转化率随反应温度变化如图所示,则代表
反应体系总压强为 的曲线是 (填“Ⅰ”“Ⅱ”或“Ⅲ”),判断依据是 。
(3)当反应体系总压强为 时,平衡时部分组分的物质的量随反应温度变化如图所示。随反应温度的升
高, 的物质的量先增加后减少,主要原因是 。
(4) 和 反应可制取乙烯,反应的化学方程式为 。一
定温度下,向某恒容密闭容器中充入 和 ,体系的初始压强为 ,若平衡时 的转化率为
,不考虑副反应的发生, 的平衡分压为 Mpa(用 表示,下同),该反应的压强平衡常数
。
(5)CH 通过光电化学转化可制得乙二醇,以乙二醇为燃料的燃料电池工作时,若以 溶液为电解液,则该电
4
极的反应式为 。
17.(15分)水杨酸异戊酯( ,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,
在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
6
学科网(北京)股份有限公司①取27.6g(0.20mol)水杨酸、43.2mL(0.40mol)异戊醇、8mL环己烯和2mL浓硫酸依次加到圆底烧瓶中。
②按照下图搭建反应装置,在145~155℃油浴下加热回流至不再有水生成。
③待反应液冷却后依次用水、NaHCO 溶液、饱和NaCl溶液洗涤至中性后分出有机层。
3
④干燥、减压蒸馏有机层,收集到31.2g产物。
⑤用红外光谱仪和核磁共振仪对产物进行表征。
已知:
①环己烯(沸点83℃)可与水形成沸点为70℃的共沸物。
②沸点:水杨酸211℃、异戊醇131℃、环己烯83℃、水杨酸异戊酯282℃。
回答以下问题:
(1)反应中浓硫酸的作用是吸水剂和 ,加入环己烯的目的是 。
(2)写出制备水杨酸异戊酯的化学方程式 。
(3)步骤②中表明反应中不再有水生成的现象是 。
(4)洗涤反应液时需要使用的主要仪器是 。
(5)步骤③中NaHCO 溶液的作用是 。
3
(6)本次实验的产率为 %。
(7)红外光谱图中可获得产物信息包括 。
a.产物中碳氧双键键长 b.产物相对分子质量
c.产物中含有酯基结构 d.产物中氧元素质量分数
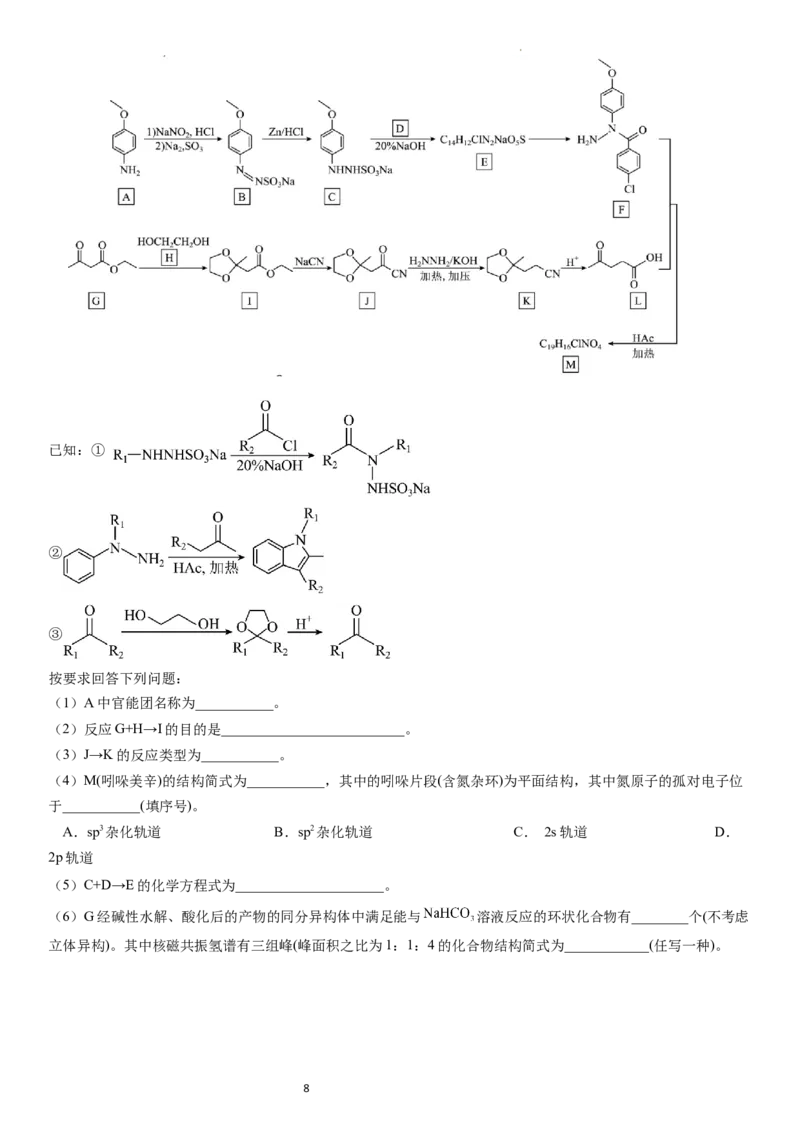
18.(15分)吲哚美辛M是一种可减少发热、疼痛的非留体类抗炎药,其合成路线(部分试剂及反应条件略)如下图
所示。
7
学科网(北京)股份有限公司已知:①
②
③
按要求回答下列问题:
(1)A中官能团名称为___________。
(2)反应G+H→I的目的是__________________________。
(3)J→K的反应类型为___________。
(4)M(吲哚美辛)的结构简式为___________,其中的吲哚片段(含氮杂环)为平面结构,其中氮原子的孤对电子位
于___________(填序号)。
A.sp3杂化轨道 B.sp2杂化轨道 C. 2s轨道 D.
2p轨道
(5)C+D→E的化学方程式为_____________________。
(6)G经碱性水解、酸化后的产物的同分异构体中满足能与 溶液反应的环状化合物有________个(不考虑
立体异构)。其中核磁共振氢谱有三组峰(峰面积之比为1:1:4的化合物结构简式为____________(任写一种)。
8
学科网(北京)股份有限公司