文档内容
镇江市2015年初中毕业升学考试化学试卷
说明:1.本试卷共6页,满分100分,考试时间100分钟。请将答案填写在答题卷上。
2.可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5
Na-23 K-39 Ca-40 Fe-56 Cu-64 Ba-137
一、单项选择题(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.下列属于纯净物的是
A.液态氮 B.加碘盐 C.食用醋 D.高钙奶
2.下列属于化学变化的是
A.矿石粉碎 B.冰雪消融 C.石油分馏 D.葡萄酿酒
3.下列物质俗称与化学式相对应的是
A.水银—Ag B.干冰—HO C.苛性钠—NaOH D.生石灰—Ca(OH)
2 2
4.下列说法错误的是
A.煤气泄漏,应关阀开窗 B.明矾净水,能杀菌消毒
C.煤炭脱硫,可防止酸雨 D.金属回收,使资源再生
5.下列对物质的归类正确的是
选 项 归 类 物 质
A 氧化物 水、双氧水、氢氧化钾
B 可燃气体 氢气、氧气、天然气
C 营养物质 淀粉、油脂、蛋白质
D 大气污染物 粉尘、氮氧化物、二氧化碳
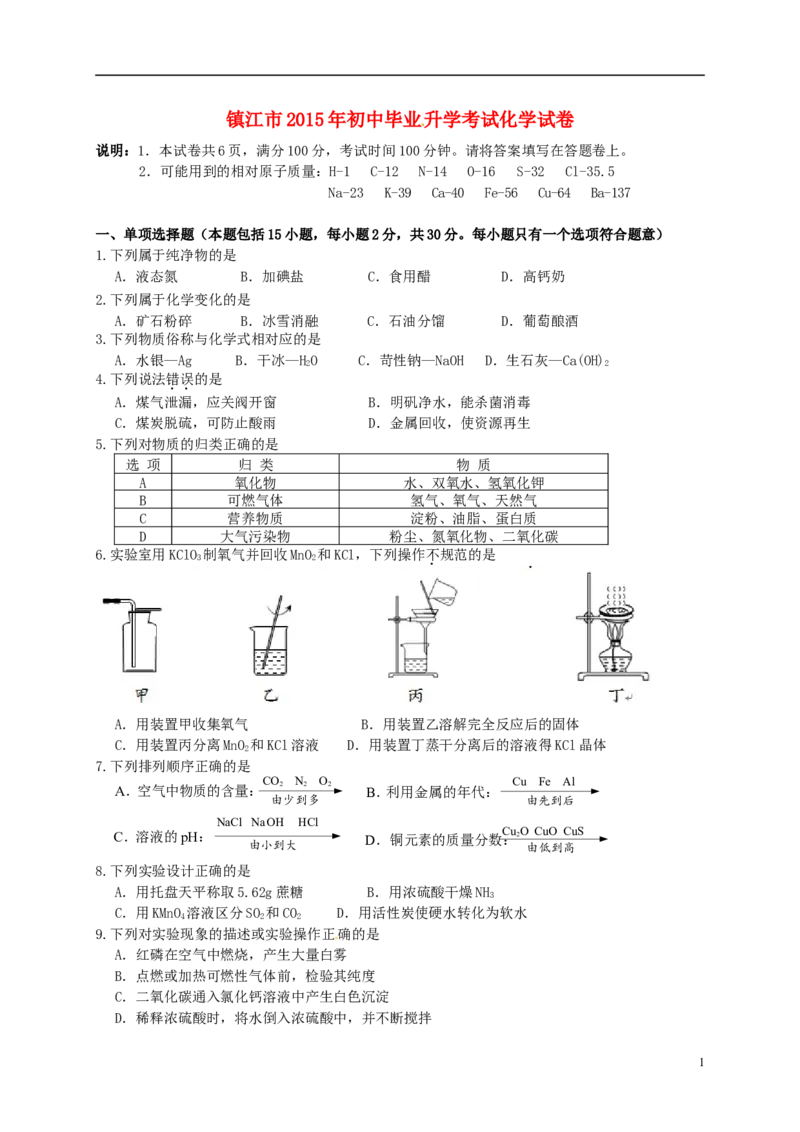
6.实验室用KClO 制氧气并回收MnO 和KCl,下列操作不规范的是
3 2
A.用装置甲收集氧气 B.用装置乙溶解完全反应后的固体
C.用装置丙分离MnO 和KCl溶液 D.用装置丁蒸干分离后的溶液得KCl晶体
2
7.下列排列顺序正确的是
CO N O Cu Fe Al
A.空气中物质的含量: 2 2 2 B.利用金属的年代:
由少到多 由先到后
NaCl NaOH HCl
C.溶液的pH: D.铜元素的质量分数 C : u 2 O CuO CuS
由小到大 由低到高
8.下列实验设计正确的是
A.用托盘天平称取5.62g蔗糖 B.用浓硫酸干燥NH
3
C.用KMnO 溶液区分SO 和CO D.用活性炭使硬水转化为软水
4 2 2
9.下列对实验现象的描述或实验操作正确的是
A.红磷在空气中燃烧,产生大量白雾
B.点燃或加热可燃性气体前,检验其纯度
C.二氧化碳通入氯化钙溶液中产生白色沉淀
D.稀释浓硫酸时,将水倒入浓硫酸中,并不断搅拌
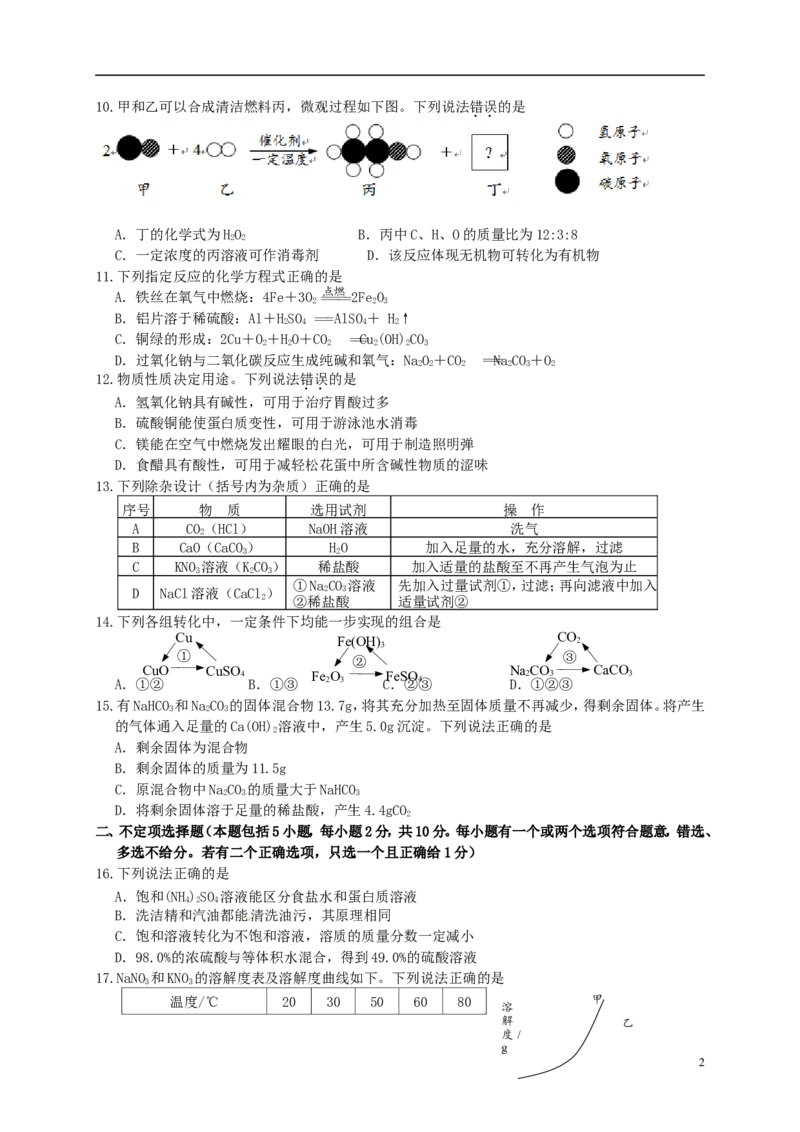
110.甲和乙可以合成清洁燃料丙,微观过程如下图。下列说法错误的是
A.丁的化学式为HO B.丙中C、H、O的质量比为12:3:8
2 2
C.一定浓度的丙溶液可作消毒剂 D.该反应体现无机物可转化为有机物
11.下列指定反应的化学方程式正确的是
点燃
A.铁丝在氧气中燃烧:4Fe+3O 2FeO
2 2 3
B.铝片溶于稀硫酸:Al+HSO AlSO+ H↑
2 4 4 2
C.铜绿的形成:2Cu+O+HO+CO Cu(OH)CO
2 2 2 2 2 3
D.过氧化钠与二氧化碳反应生成纯碱和氧气:NaO+CO NaCO+O
2 2 2 2 3 2
12.物质性质决定用途。下列说法错误的是
A.氢氧化钠具有碱性,可用于治疗胃酸过多
B.硫酸铜能使蛋白质变性,可用于游泳池水消毒
C.镁能在空气中燃烧发出耀眼的白光,可用于制造照明弹
D.食醋具有酸性,可用于减轻松花蛋中所含碱性物质的涩味
13.下列除杂设计(括号内为杂质)正确的是
序号 物 质 选用试剂 操 作
A CO(HCl) NaOH溶液 洗气
2
B CaO(CaCO) HO 加入足量的水,充分溶解,过滤
3 2
C KNO 溶液(KCO) 稀盐酸 加入适量的盐酸至不再产生气泡为止
3 2 3
①NaCO 溶液 先加入过量试剂①,过滤;再向滤液中加入
D NaCl溶液(CaCl) 2 3
2 ②稀盐酸 适量试剂②
14.下列各组转化中,一定条件下均能一步实现的组合是
Cu Fe(OH) CO 2
3
① ③
②
CuO CuSO Na CO CaCO
4 Fe O FeSO 2 3 3
A.①② B.①③ 2 3 C.②③4 D.①②③
15.有NaHCO 和NaCO 的固体混合物13.7g,将其充分加热至固体质量不再减少,得剩余固体。将产生
3 2 3
的气体通入足量的Ca(OH) 溶液中,产生5.0g沉淀。下列说法正确的是
2
A.剩余固体为混合物
B.剩余固体的质量为11.5g
C.原混合物中NaCO 的质量大于NaHCO
2 3 3
D.将剩余固体溶于足量的稀盐酸,产生4.4gCO
2
二、不定项选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意,错选、
多选不给分。若有二个正确选项,只选一个且正确给1分)
16.下列说法正确的是
A.饱和(NH)SO 溶液能区分食盐水和蛋白质溶液
4 2 4
B.洗洁精和汽油都能清洗油污,其原理相同
C.饱和溶液转化为不饱和溶液,溶质的质量分数一定减小
D.98.0%的浓硫酸与等体积水混合,得到49.0%的硫酸溶液
17.NaNO 和KNO 的溶解度表及溶解度曲线如下。下列说法正确的是
3 3
温度/℃ 20 30 50 60 80 甲
溶
解 乙
度/
g
2NaNO 3 87.6 94.9 110 122 148 •
溶解度S/g
KNO 31.6 45.3 85.5 110 167
3
A.甲表示NaNO 溶解度曲线
3
B.40℃时,饱和溶液的溶质质量分数:KNO>NaNO
3 3 0 t 温度/℃
1
C.t应介于60℃~80℃
1
D.80℃时KNO 饱和溶液中含有少量NaNO,要得到较纯净的KNO 晶体,可采用降温结晶、过滤等操
3 3 3
作
18.烧杯中盛有BaCl 和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的NaCO 溶液,烧
2 2 3
杯中溶液的质量与滴加溶液的质量关系
烧 杯 d•
如右图所示。下列说法正确的是
中 c
b •
A.ab段产生白色沉淀 溶 液 •
的
B.bc段溶液质量增加86.3g
质 a•
C.c点对应溶液的溶质质量分数为7.5%
量/g
106.0 212.0 NaCO
D.向d点溶液中滴加酚酞试液,溶液显红色 0 2 3
溶液的质量/g
19.下列各组溶液,不用其他试剂就不能鉴别出来的是
A.CuSO、NaOH、MgCl、NaCl B.KOH、稀HCl、FeCl、NaNO
4 2 3 3
C.KCl、AgNO、稀HCl、稀HNO D.稀HCl、NaCO、BaCl、NaSO
3 3 2 3 2 2 4
20.右下图为利用燃煤烟气生产NaSO 和化工原料乙烯(CH)的原理。下列说法正确的是
2 4 2 4
A.副产物M的化学式为HCl 海水 太阳能电池组
- +
B.装置中存在化学能转化为电能的过程 燃煤烟气
(SO 、CO )
C.生产过程中,乙烯制备装置中溶液的 2 2 石墨
CO CH
pH会增大 O 2 2 2 4 O
2
D.乙烯制备装置中的反应可表示为:
HSO
CO 2
2CO+2HO H S O CH+3O 2
2 2 2 4 2 4 2 NaSO 和M的溶液 4
通电 2 4 溶液
Na SO 制备装置 乙烯制备装置
2 4
三、填空题(本题包括5小题,共18分)
21.(4分)用化学符号表示:
(1)锌元素 ▲ ; (2)2个亚铁离子 ▲ ;
(3)五氧化二磷 ▲ ; (4)人体缺少 ▲ 元素会骨质疏松
22.(6分)选择下列适当的物质填空(填字母序号):
A.氢气 B.焦炭 C.金刚石 D.硝酸钾
E.维生素 F.硫酸 G.蛋白质 H.武德合金
(1)理想绿色能源 ▲ ; (2)可用作保险丝 ▲ ;
(3)自然界硬度最大的是 ▲ ; (4)铅蓄电池中的酸 ▲ ;
(5)蔬菜、水果中富含 ▲ ; (6)复合肥料 ▲ 。
23.(2分)用石英砂(主要成分SiO)制造的分离膜可以让CO 透过,而其它气体不能透过。CO 通过分
2 2 2
离膜后被氨水吸收转化为氮肥,如右下图所示。 氨水
分离膜
(1)SiO 的化学名称为 ▲ 。
2
高浓度的
(2)此氮肥的化学式为 ▲ 。
CO 气体
2
氮肥
24.(4分)用工业碳酸钙(含有少量AlO、FeO)生产医药CaCl ·2H O的主要流程如下:
2 3 2 3 2 2
盐酸 试剂A (NH 4 ) 2 CO 3 盐酸
操作1 操作2 操作3
工业 溶液 溶液 CaCO
3
溶 液 CaCl 2·2H
2
O
CaCO 1 2 3
3
阶段一 阶段二
3(1)加入试剂A的目的是除去溶液1中少量AlCl、FeCl。试剂A可以选择 ▲ (选填序号)。
3 3
a.NaCO b.Ba(OH) c.Ca(OH)
2 3 2 2
(2)阶段一的目的是 ▲ 。
(3)操作1、2中,所用玻璃仪器有 ▲ 、玻璃棒、烧杯、胶头滴管。
操作3包括:蒸发浓缩、 ▲ 、过滤、洗涤等。
25.(2分)金属加工工业排放的废水中含有NaNO、NaOH,可加入铝粉加热除去。
2
(1)NaNO 中氮元素的化合价为 ▲ 。
2
(2)除去时,生成NaAlO 和能使湿润红色石蕊试纸变蓝的气体,反应的化学方程式为
2
▲ 。
四、实验题(本题包括2小题,共17分)
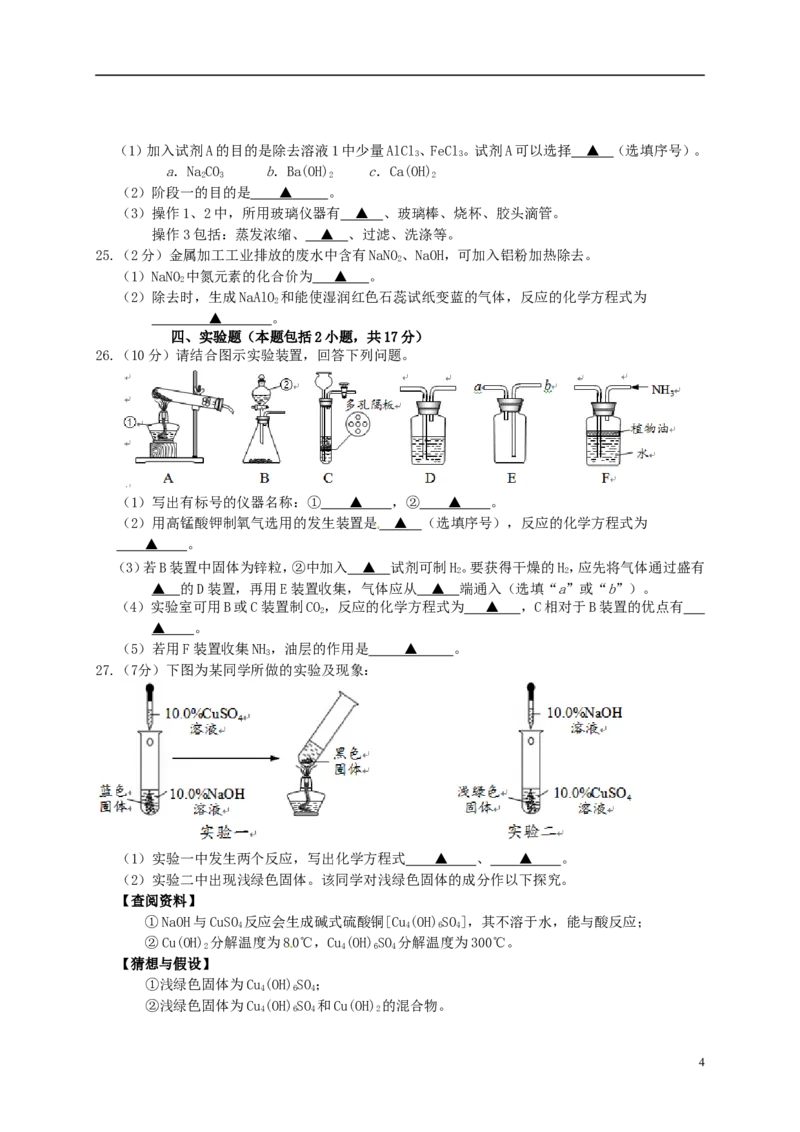
26.(10分)请结合图示实验装置,回答下列问题。
(1)写出有标号的仪器名称:① ▲ ,② ▲ 。
(2)用高锰酸钾制氧气选用的发生装置是 ▲ (选填序号),反应的化学方程式为
▲ 。
(3)若B装置中固体为锌粒,②中加入 ▲ 试剂可制H。要获得干燥的H,应先将气体通过盛有
2 2
▲ 的D装置,再用E装置收集,气体应从 ▲ 端通入(选填“a”或“b”)。
(4)实验室可用B或C装置制CO,反应的化学方程式为 ▲ ,C相对于B装置的优点有
2
▲ 。
(5)若用F装置收集NH,油层的作用是 ▲ 。
3
27.(7分)下图为某同学所做的实验及现象:
(1)实验一中发生两个反应,写出化学方程式 ▲ 、 ▲ 。
(2)实验二中出现浅绿色固体。该同学对浅绿色固体的成分作以下探究。
【查阅资料】
①NaOH与CuSO 反应会生成碱式硫酸铜[Cu(OH)SO],其不溶于水,能与酸反应;
4 4 6 4
②Cu(OH) 分解温度为80℃,Cu(OH)SO 分解温度为300℃。
2 4 6 4
【猜想与假设】
①浅绿色固体为Cu(OH)SO;
4 6 4
②浅绿色固体为Cu(OH)SO 和Cu(OH) 的混合物。
4 6 4 2
4【实验验证】
①将实验二的试管加热至100℃,出现黑色固体,则证明浅绿色固体中含有 ▲ 。
②从实验二加热后的试管中分离出固体的操作有 ▲ 、洗涤等。证明固体已洗涤干净的方
法是 ▲ 。
③将②中所得固体溶于足量 ▲ (选填序号),再滴加Ba(NO) 溶液,出现白色沉淀。
3 2
A.盐酸 B.稀硝酸 C.稀硫酸
【结论】猜想②正确。
【拓展与思考】
若将实验二中的浅绿色固体浸泡在过量的NaOH溶液中,密封放置一天后,固体全部变为蓝色。写出此
反应的化学方程式 ▲ 。
五、推断题(本题包括2小题,共11分)
28.(5分)有一包不纯的KCO 粉末,可能含有NaCO、BaSO、CuCl、KCl、KNO、Ca(NO) 中的一种或几
2 3 2 3 4 2 3 3 2
种,为分析含有的杂质,现进行如下实验。
(1)取样溶于水,无固体残留,得无色溶液。则粉末中一定不含有 ▲ 、 ▲ 、 ▲ 。
(2)取上述溶液适量,滴加AgNO 溶液,有白色沉淀,再加入足量稀HNO,沉淀部分溶解,则此粉末中
3 3
一定含有的杂质是 ▲ 。
(3)为确定NaCO 是否存在,某同学称取13.8g粉末溶于水,加入足量BaCl 溶液,充分反应生成
2 3 2
19.7g沉淀质量,则原粉末中一定含有NaCO。你认为此结论 ▲ (选填“是”或“否”)正
2 3
确。
29.(6分)右下图表示某些物质间转化关系。A、B为组成元素相同的无色液体,D是大理石的主要成
分,C、F、H为气体,且H有刺激性气味。
(1)E的化学式为 ▲ 。
C
MnO
(2)反应①的化学方程式为 ▲ 。 A 2
① B
(3)反应②的化学方程式为 ▲ 。
G NH 4 Cl H
由此反应可知,在农业生产中施用 E 加热 ②
高温
铵态氮肥时应注意 ▲ 。 D
一定条件
F
(4)自然界中普遍存在着F转化为C的
反应,名称为 ▲ ;工业生产中 尿素[CO(NH 2 ) 2 ]
用F和H合成尿素,反应中F和H的质量比为 ▲ 。
六、综合题(本题包括1小题,共14分)
30.(14分)目前,我国钢铁产量居世界第一,为国民经济的发展奠定了坚实的基础。
(一)铁的广泛应用
1.我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理 ▲ 。
2.铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为
原料可制作耐酸防护服材料。以上叙述中不涉及到 ▲ (选填序号)。
A.合金 B.无机非金属材料 C.合成材料 D.复合材料
3.某品牌的麦片中含微量铁粉,食用后可在胃酸的作用下转化为人体可吸收的铁元素,反应的
化学方程式为 ▲ 。
(二)铁锈成分的探究
植物油
1.右图为某兴趣小组探究铁生锈的三个实验, 铁钉 铁钉
铁钉
最先观察到铁锈的是 ▲ (选填序号)。 NaCl
水 水
溶液
A B C
2.铁生锈的主要过程为:Fe O 2 、 H 2 O Fe(OH) 2 O 2 、 H 2 O Fe(OH) 3 风 吹 日 晒 Fe 2 O 3 ·xH 2 O
O 、CO 、HO
2 2 2
5次要过程为:Fe FeCO
3
写出Fe Fe(OH) 反应的化学方程式 ▲ 。
2
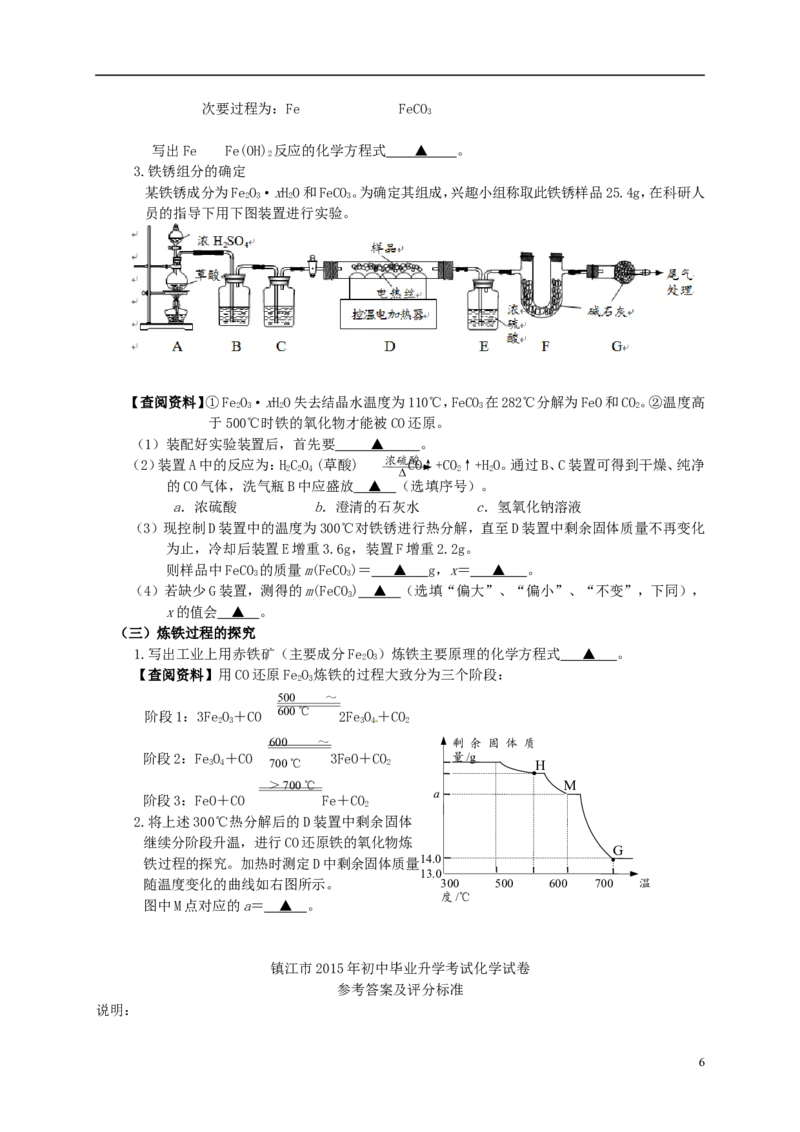
3.铁锈组分的确定
某铁锈成分为FeO·xHO和FeCO。为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人
2 3 2 3
员的指导下用下图装置进行实验。
【查阅资料】①FeO·xHO失去结晶水温度为110℃,FeCO 在282℃分解为FeO和CO。②温度高
2 3 2 3 2
于500℃时铁的氧化物才能被CO还原。
(1)装配好实验装置后,首先要 ▲ 。
(2)装置A中的反应为:HCO (草酸) 浓硫C酸O↑+CO↑+HO。通过B、C装置可得到干燥、纯净
2 2 4 ∆ 2 2
的CO气体,洗气瓶B中应盛放 ▲ (选填序号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(3)现控制D装置中的温度为300℃对铁锈进行热分解,直至D装置中剩余固体质量不再变化
为止,冷却后装置E增重3.6g,装置F增重2.2g。
则样品中FeCO 的质量m(FeCO)= ▲ g,x= ▲ 。
3 3
(4)若缺少G装置,测得的m(FeCO) ▲ (选填“偏大”、“偏小”、“不变”,下同),
3
x的值会 ▲ 。
(三)炼铁过程的探究
1.写出工业上用赤铁矿(主要成分FeO)炼铁主要原理的化学方程式 ▲ 。
2 3
【查阅资料】用CO还原FeO 炼铁的过程大致分为三个阶段:
2 3
500 ~
600℃
阶段1:3FeO+CO 2FeO +CO
2 3 3 4 2
600 ~ 剩 余 固 体 质
阶段2:FeO+CO 3FeO+CO 量/g
3 4 700℃ 2 H
•
>700℃ M
a
阶段3:FeO+CO Fe+CO
2
2.将上述300℃热分解后的D装置中剩余固体
继续分阶段升温,进行CO还原铁的氧化物炼
G
铁过程的探究。加热时测定D中剩余固体质量14.0 •
13.0
随温度变化的曲线如右图所示。 300 500 600 700 温
度/℃
图中M点对应的a= ▲ 。
镇江市2015年初中毕业升学考试化学试卷
参考答案及评分标准
说明:
61.化学专用名词或仪器名称写错不给分。
2.化学方程式中化学式写错不给分;若化学方程式不配平或配错,每错一个扣0.5分,
未注明反应条件、未标出“↑”或“↓”及出现差错,不扣分。
3.与参考答案不同的合理答案均给分。
一、单项选择题(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题意)
1. A 2. D 3.C 4.B 5.C 6.D 7.B 8.C 9.B 10.A
11. C 12.A 13.D 14.B 15.D
二、不定项选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意,错选、
多选不给分。若有二个正确选项,只选一个且正确给1分)
16.A 17. CD 18.BD 19.C 20.AD
三、填空题(本题包括5小题,共18分)
21.(共4分,每空1分)
(1)Zn (2)2Fe2+ (3)PO (4)Ca
2 5
22.(共6分,每空1分)
(1)A (2)H (3)C (4)F (5)E (6)D
23.(共2分,每空1分)
(1)二氧化硅 (2)NHHCO 或(NH)CO
4 3 4 2 3
24.(共4分,每空1分)
(1)c
(2)提纯碳酸钙(或除去工业碳酸钙中的杂质)
(3)漏斗 降温结晶(或冷却结晶或结晶)
25.(共2分,每空1分)
(1)+3
(2)2Al+NaNO+NaOH+HO 2NaAlO+NH↑
2 2 △ 2 3
四、实验题(本题包括2小题,共17分)
26.(共10分,每空1分)
(1)①酒精灯 ②分液漏斗(滴液漏斗)
(2)A 2KMnO △ KMnO + MnO + O↑
4 2 4 2 2
(3)盐酸(或稀硫酸) 浓硫酸 a
(4)CaCO+2HCl CaCl+ HO + CO↑
3 2 2 2
控制反应的发生和停止(或随开随用,随关随停)
(5)防止NH 溶于水
3
27.(共7分,每空1分)
(1)CuSO+2NaOH Cu(OH)↓+NaSO
4 2 2 4
△
Cu(OH) CuO+HO
2 2
(2)【实验验证】
①Cu(OH)
2
②过滤
取最后一次洗涤液,滴加BaCl[或Ba(NO )、Ba(OH)]溶液,无沉淀生成,则固体已洗
2 3 2 2
净。
③A或B或AB
7【拓展与思考】
Cu(OH)SO+2NaOH 4Cu(OH)+NaSO
4 6 4 2 2 4
五、推断题(本题包括2小题,共11分)
28.(共5分,每空1分)
(1)BaSO CuCl Ca(NO)(全对给3分,对2错1给1分,对1错2不给分;只填一空且正确
4 2 3 2
给1分,只填二空且正确给2分,只填二空,有错,不给分。)
(2)KCl
(3)是
29.(共6分,每空1分)
(1)CaO
MnO
2
(2)2HO 2HO+O↑
2 2 2 2
△
(3)Ca(OH)+2NHCl CaCl+2NH↑+2HO
2 4 2 3 2
铵态氮肥不能与碱性物质混合使用
(4)光合作用 22:17(或44:34、1.3、1.29)
六、综合题(本题1小题,共14分)
30.(共14分,除最后一空2分外,其余每空1分)
(一)1.Fe+CuSO FeSO+Cu(或其它可溶性铜盐与铁反应)
4 4
2.B
3.Fe+2HCl FeCl+H↑
2 2
(二)1.C
2.2Fe+O+2HO 2Fe(OH)
2 2 2
3.(1)检查装置的气密性
(2)c
(3)5.8 2
(4)偏大 偏大
高温
(三)1.FeO+3CO 2Fe+3CO
2 3 2
2.18.0(或18)
8