文档内容
浙江省湖州市2018年中考化学真题试题
3.通常情况下,不列能实现“1+1=2”这一结果的是
A.1毫升酒精加1毫升水得到2毫升酒精的水溶液
B.1克酒精加1克水得到2克酒精的水溶液
C.1克食盐加1克水得到2克食盐的水溶液
D.1克食盐溶液加1克硝酸银溶液得到2克混合溶液
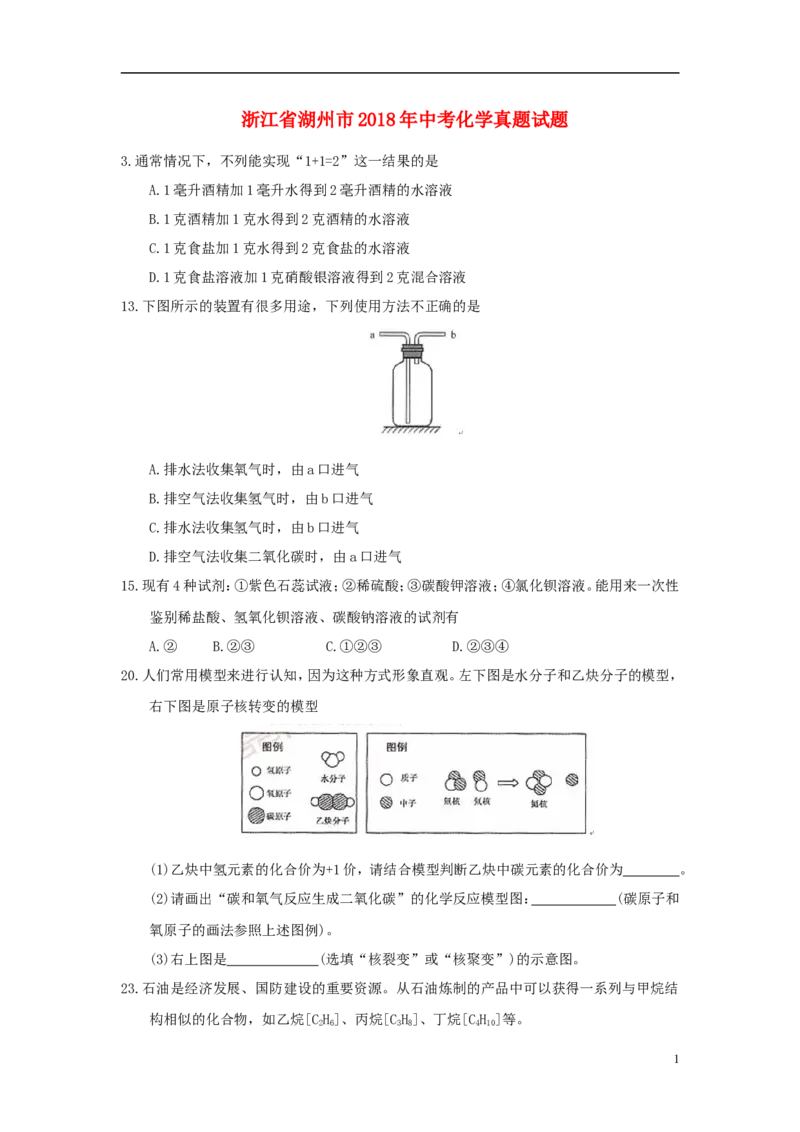
13.下图所示的装置有很多用途,下列使用方法不正确的是
A.排水法收集氧气时,由a口进气
B.排空气法收集氢气时,由b口进气
C.排水法收集氢气时,由b口进气
D.排空气法收集二氧化碳时,由a口进气
15.现有4种试剂:①紫色石蕊试液;②稀硫酸;③碳酸钾溶液;④氯化钡溶液。能用来一次性
鉴别稀盐酸、氢氧化钡溶液、碳酸钠溶液的试剂有
A.② B.②③ C.①②③ D.②③④
20.人们常用模型来进行认知,因为这种方式形象直观。左下图是水分子和乙炔分子的模型,
右下图是原子核转变的模型
(1)乙炔中氢元素的化合价为+1价,请结合模型判断乙炔中碳元素的化合价为 。
(2)请画出“碳和氧气反应生成二氧化碳”的化学反应模型图: (碳原子和
氧原子的画法参照上述图例)。
(3)右上图是 (选填“核裂变”或“核聚变”)的示意图。
23.石油是经济发展、国防建设的重要资源。从石油炼制的产品中可以获得一系列与甲烷结
构相似的化合物,如乙烷[CH]、丙烷[CH]、丁烷[CH ]等。
2 6 3 8 4 10
1(1)甲烷是一种①无色、无味的气体,②难溶于水,③在1500℃以上的高温下能分解为碳
和氢气,④充分燃烧后生成二氧化碳和水。以上叙述中属于甲烷物理性质的是
(选填序号)。
(2)请模仿甲烷在氧气中充分燃烧的化学方程式,写出丙烷在氧气中充分燃烧的化学方
程式: 。
25.高锰酸钾是初中常用的一种试剂,它可以和很多物质反应,发生颜色变化。小明和小丽把
经硫酸酸化的高锰酸钾溶液和草酸[HCO]溶液混合,发现刚开始反应时溶液褪色不
2 2 4
明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查
到了如下资料:
资料1:2KMnO+5HCO+3HSO= KSO+2MnSO+8HO+10CO↑
4 2 2 4 2 4 2 4 4 2 2
资料2:通常情况下,反应物浓度变大。反应加快;温度开高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。小明经过分析,否定了假
设一,理由是 。
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入
等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO,发现
4
A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是
。这一实验基于的假设
是 。
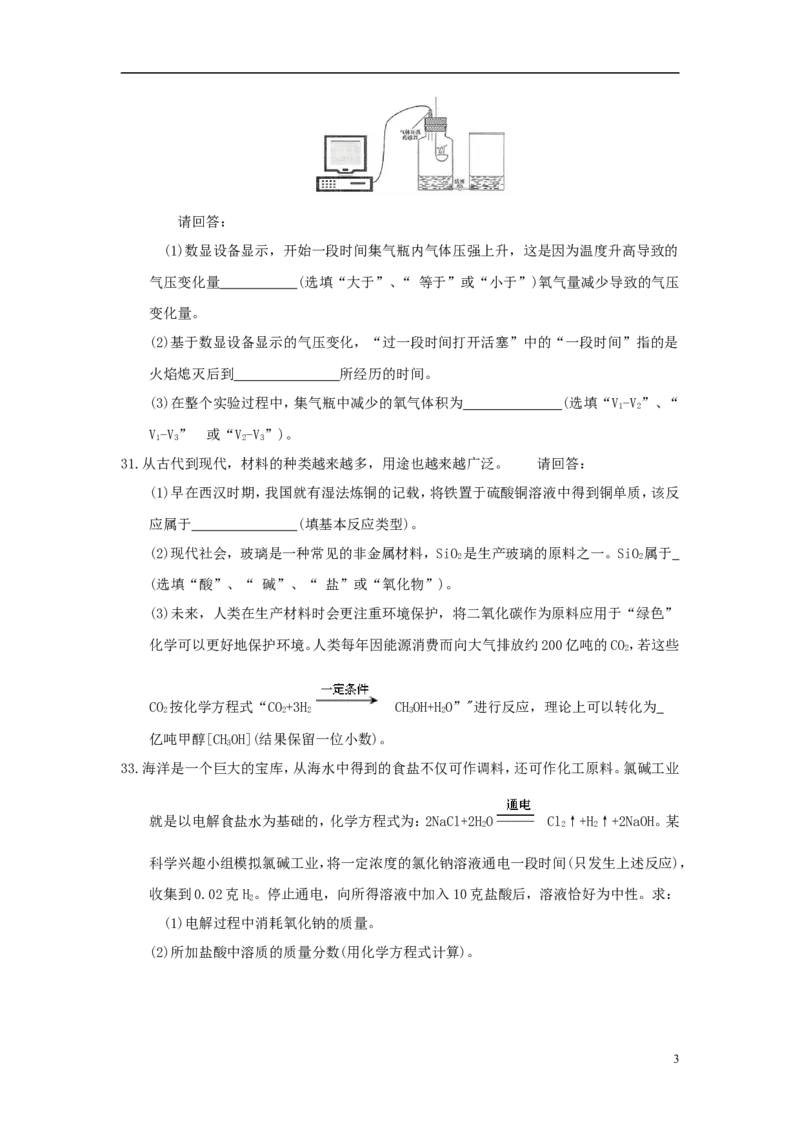
28.某科学兴趣小组对“测定空气中氧气含量”的实验进行了改进:将数显设备、气体压强
传感器和空气中氧气含量测量装置按下图连接。装置气密性良好,调节右边敞口容器和
集气瓶里的水面相平,此时集气瓶内气体的体积为V。关闭活塞,点燃燃烧匙内的红磷,
1
立即塞紧瓶塞,待火焰熄灭后,过一段时间打开活塞,观察到集气瓶中的水位上升。待集
气瓶内的水面不再上升时,集气瓶内的气体体积为V。 然后向右边容器内加入一定
2
量的水至两边水面再次相平,此时集气瓶内的气体体积为V。在点燃红磷至打开活塞这
3
一过程中,观察到数显设备显示集气瓶内的气体压强先上升后下降,再趋于稳定。
2请回答:
(1)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的
气压变化量 (选填“大于”、“ 等于”或“小于”)氧气量减少导致的气压
变化量。
(2)基于数显设备显示的气压变化,“过一段时间打开活塞”中的“一段时间”指的是
火焰熄灭后到 所经历的时间。
(3)在整个实验过程中,集气瓶中减少的氧气体积为 (选填“V-V”、“
1 2
V-V” 或“V-V”)。
1 3 2 3
31.从古代到现代,材料的种类越来越多,用途也越来越广泛。 请回答:
(1)早在西汉时期,我国就有湿法炼铜的记载,将铁置于硫酸铜溶液中得到铜单质,该反
应属于 (填基本反应类型)。
(2)现代社会,玻璃是一种常见的非金属材料,SiO 是生产玻璃的原料之一。SiO 属于
2 2
(选填“酸”、“ 碱”、“ 盐”或“氧化物”)。
(3)未来,人类在生产材料时会更注重环境保护,将二氧化碳作为原料应用于“绿色”
化学可以更好地保护环境。人类每年因能源消费而向大气排放约200亿吨的CO,若这些
2
CO 按化学方程式“CO+3H CHOH+HO”"进行反应,理论上可以转化为
2 2 2 3 2
亿吨甲醇[CHOH](结果保留一位小数)。
3
33.海洋是一个巨大的宝库,从海水中得到的食盐不仅可作调料,还可作化工原料。氯碱工业
就是以电解食盐水为基础的,化学方程式为:2NaCl+2HO Cl↑+H↑+2NaOH。某
2 2 2
科学兴趣小组模拟氯碱工业,将一定浓度的氯化钠溶液通电一段时间(只发生上述反应),
收集到0.02克H。停止通电,向所得溶液中加入10克盐酸后,溶液恰好为中性。求:
2
(1)电解过程中消耗氧化钠的质量。
(2)所加盐酸中溶质的质量分数(用化学方程式计算)。
3参考答案
3B 13A 15B
20.(1)-1 (2) (3)核聚变
23.(1)①② (2)CH+5O 3CO +4HO
3 8 2 2 2
25.(1)随着反应进行,反应物浓度变小(2分)
(2)减小反应过程中温度变化对实验结果的影响(2分)
反应过程中生成的硫酸锰对该反应有催化作用(2分)
28. (1)大于(2分)
(2)集气瓶内的温度恢复到室温(或“数显设备的示数已不变”或“集气瓶内的气压
保持稳定”)(2分)
(3)V- V(2分)
1 3
31.(1)置换反应 (2)氧化物 (3)145.5
33.(1)1.17 (2)7.3% 解题过程略
4