文档内容
五年(2021-2025)高考化学真题分类汇编
专题23 工艺流程综合题——原材料转化制备类
考向 五年考情(2021-2025) 命题趋势
2025·广东卷、2025·河北卷、
2025·江苏卷、2024·黑吉辽
工艺流程综合题选取的情境紧密联系与人类
卷、2024·贵州卷、2024·山东
密切相关的生产生活实际,试题的命制从情
卷、2024·湖北卷、2024·浙江
境素材开始,以学科素养为目标导向,选取
6月卷、2023·海南卷、2023·
某个学科素养的一个方面或几个方面,深入
原材料转化制备类工艺流 重庆卷、2023·全国甲卷、
考查学生学科素养的表现层次。利用科研前
程综合题 2023·全国乙卷、2023·湖南
沿和生产实际的真实情境,展现研究过程或
卷、2023·北京卷、2023·山东
者生成过程的具体实际问题,考查学生的探
卷、2022·全国甲卷、2022·广
究与创新能力。主要分为两大考查方向:一
东卷、2022·北京卷、2022·福
是分离、提纯类;二是原材料转化制备类。
建卷、2022·辽宁卷、2022·山
东卷、2021·山东卷
1.(2025·广东卷)我国是金属材料生产大国,绿色生产是必由之路。一种从多金属精矿中提取Fe、Cu、
Ni等并探究新型绿色冶铁方法的工艺如下。
已知:多金属精矿中主要含有Fe、Al、Cu、Ni、O等元素。
氢氧化物
(1)“酸浸”中,提高浸取速率的措施有 (写一条)。
(2)“高压加热”时,生成 的离子方程式为: 。
(3)“沉铝”时,pH最高可调至 (溶液体积变化可忽略)。已知:“滤液1”中
, 。
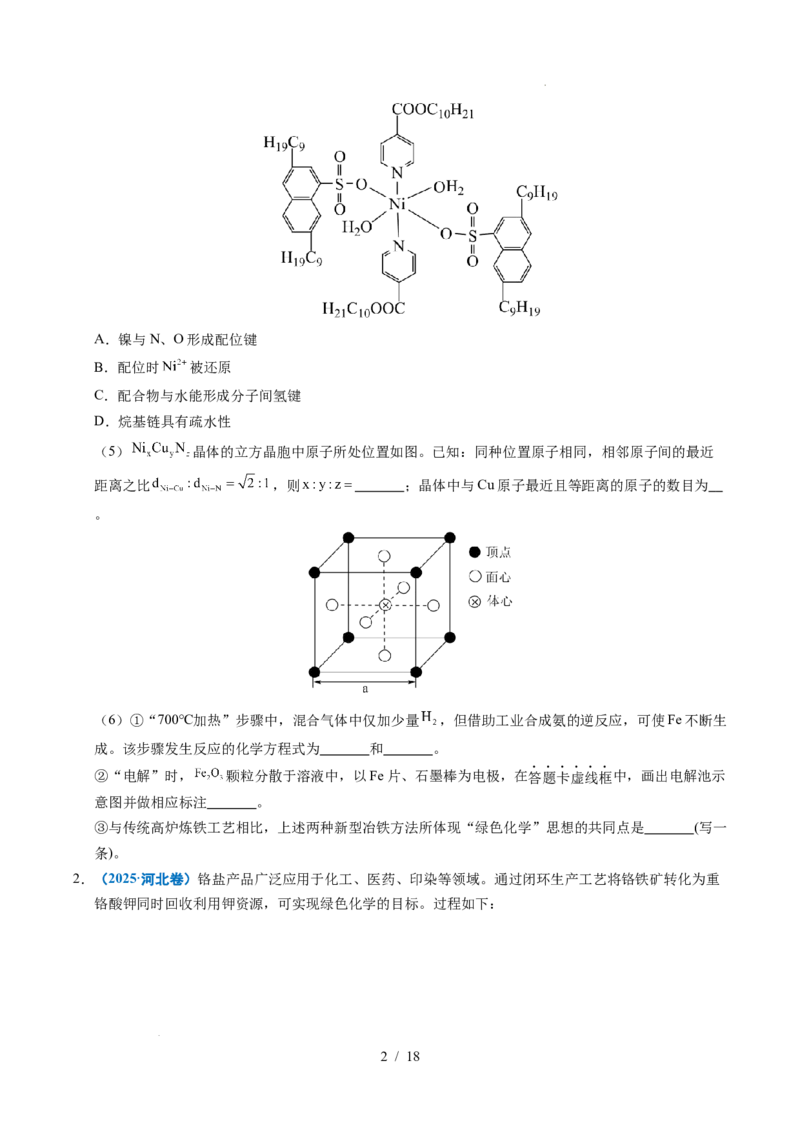
(4)“选择萃取”中,镍形成如图的配合物。镍易进入有机相的原因有_______。
1 / 18
学科网(北京)股份有限公司A.镍与N、O形成配位键
B.配位时 被还原
C.配合物与水能形成分子间氢键
D.烷基链具有疏水性
(5) 晶体的立方晶胞中原子所处位置如图。已知:同种位置原子相同,相邻原子间的最近
距离之比 ,则 ;晶体中与Cu原子最近且等距离的原子的数目为
。
(6)①“700℃加热”步骤中,混合气体中仅加少量 ,但借助工业合成氨的逆反应,可使Fe不断生
成。该步骤发生反应的化学方程式为 和 。
②“电解”时, 颗粒分散于溶液中,以Fe片、石墨棒为电极,在答题卡虚线框中,画出电解池示
意图并做相应标注 。
③与传统高炉炼铁工艺相比,上述两种新型冶铁方法所体现“绿色化学”思想的共同点是 (写一
条)。
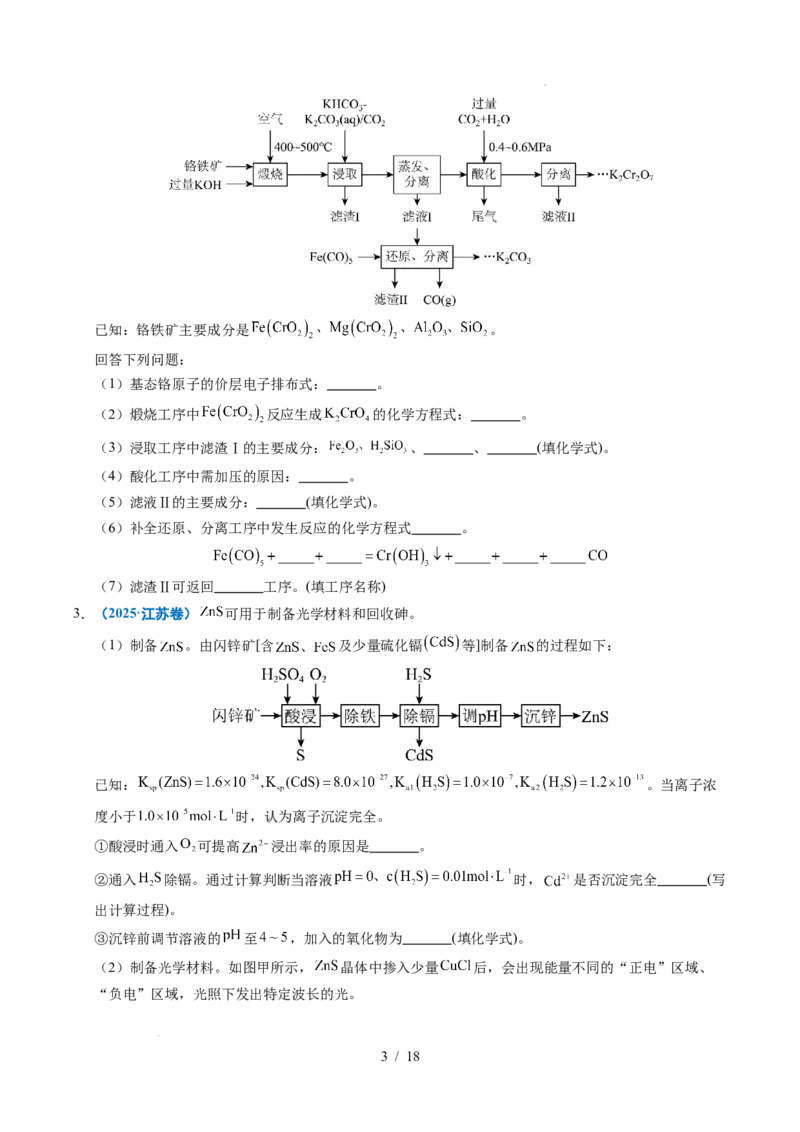
2.(2025·河北卷)铬盐产品广泛应用于化工、医药、印染等领域。通过闭环生产工艺将铬铁矿转化为重
铬酸钾同时回收利用钾资源,可实现绿色化学的目标。过程如下:
2 / 18
学科网(北京)股份有限公司已知:铬铁矿主要成分是 。
回答下列问题:
(1)基态铬原子的价层电子排布式: 。
(2)煅烧工序中 反应生成 的化学方程式: 。
(3)浸取工序中滤渣Ⅰ的主要成分: 、 、 (填化学式)。
(4)酸化工序中需加压的原因: 。
(5)滤液Ⅱ的主要成分: (填化学式)。
(6)补全还原、分离工序中发生反应的化学方程式 。
(7)滤渣Ⅱ可返回 工序。(填工序名称)
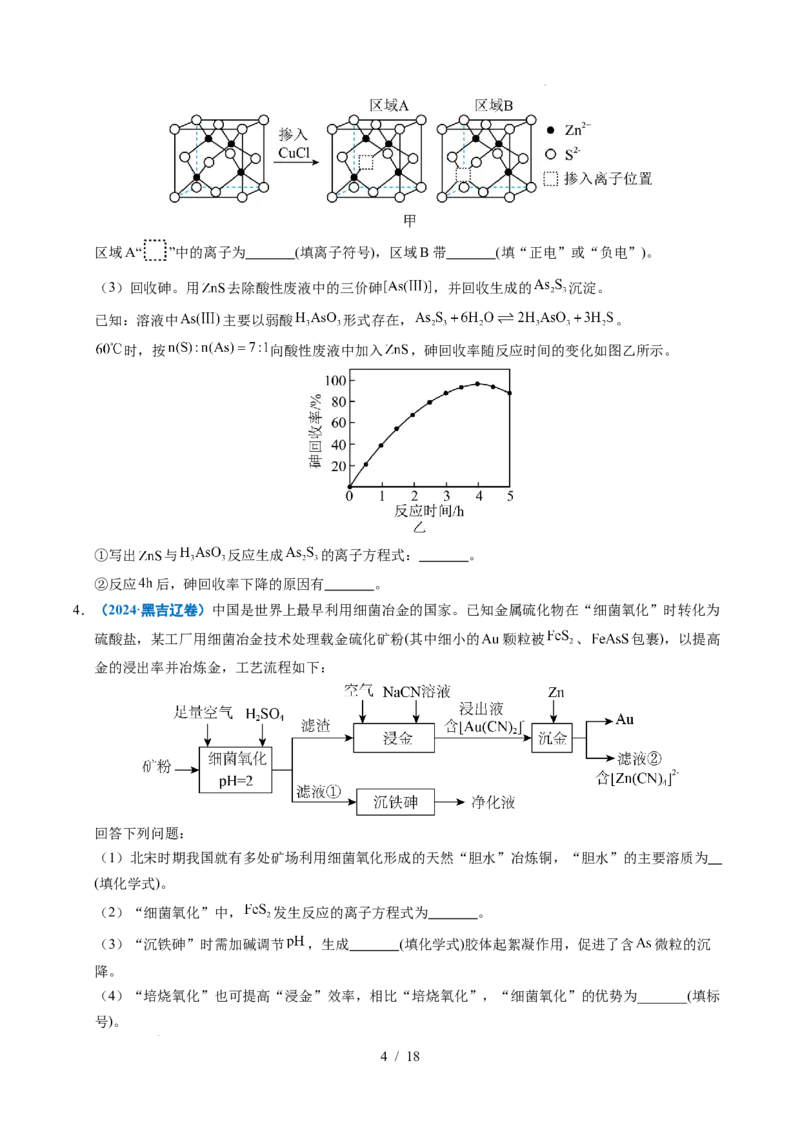
3.(2025·江苏卷) 可用于制备光学材料和回收砷。
(1)制备 。由闪锌矿[含 及少量硫化镉 等]制备 的过程如下:
已知: 。当离子浓
度小于 时,认为离子沉淀完全。
①酸浸时通入 可提高 浸出率的原因是 。
②通入 除镉。通过计算判断当溶液 时, 是否沉淀完全 (写
出计算过程)。
③沉锌前调节溶液的 至 ,加入的氧化物为 (填化学式)。
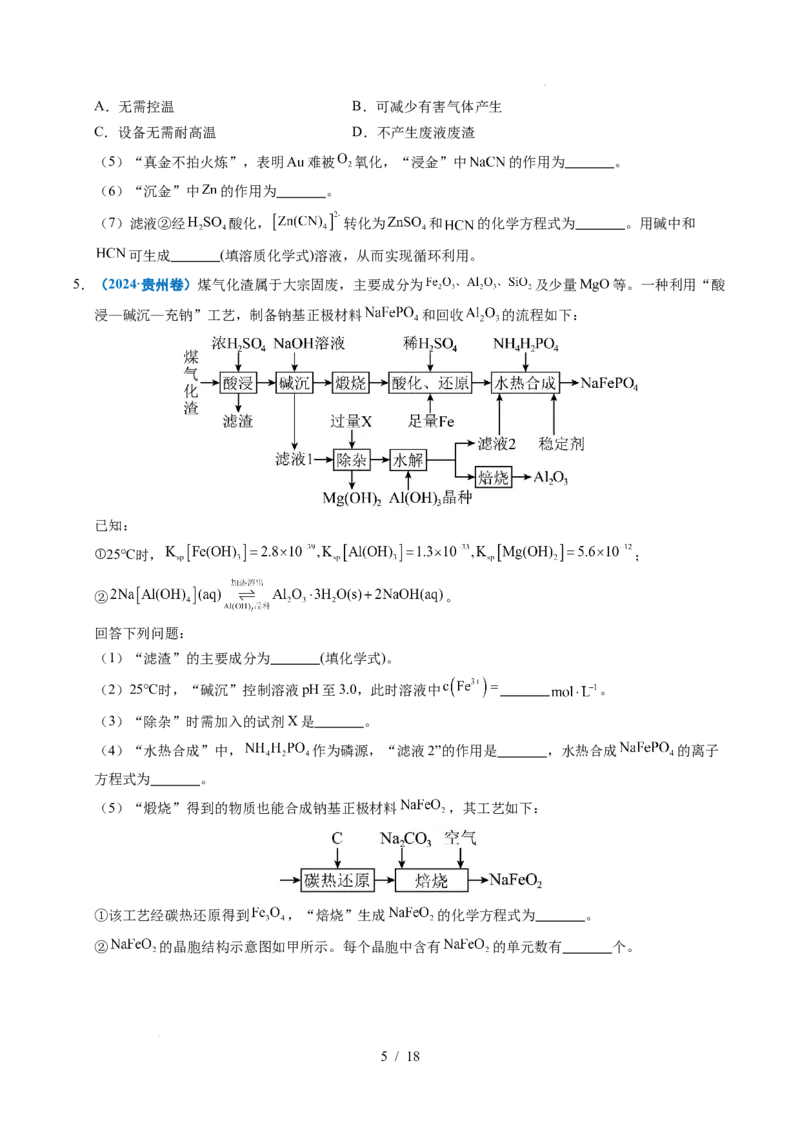
(2)制备光学材料。如图甲所示, 晶体中掺入少量 后,会出现能量不同的“正电”区域、
“负电”区域,光照下发出特定波长的光。
3 / 18
学科网(北京)股份有限公司区域A“ ”中的离子为 (填离子符号),区域B带 (填“正电”或“负电”)。
(3)回收砷。用 去除酸性废液中的三价砷 ,并回收生成的 沉淀。
已知:溶液中 主要以弱酸 形式存在, 。
时,按 向酸性废液中加入 ,砷回收率随反应时间的变化如图乙所示。
①写出 与 反应生成 的离子方程式: 。
②反应 后,砷回收率下降的原因有 。
4.(2024·黑吉辽卷)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧化”时转化为
硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的 颗粒被 、 包裹),以提高
金的浸出率并冶炼金,工艺流程如下:
回答下列问题:
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”的主要溶质为
(填化学式)。
(2)“细菌氧化”中, 发生反应的离子方程式为 。
(3)“沉铁砷”时需加碱调节 ,生成 (填化学式)胶体起絮凝作用,促进了含 微粒的沉
降。
(4)“培烧氧化”也可提高“浸金”效率,相比“培烧氧化”,“细菌氧化”的优势为_______(填标
号)。
4 / 18
学科网(北京)股份有限公司A.无需控温 B.可减少有害气体产生
C.设备无需耐高温 D.不产生废液废渣
(5)“真金不拍火炼”,表明 难被 氧化,“浸金”中 的作用为 。
(6)“沉金”中 的作用为 。
(7)滤液②经 酸化, 转化为 和 的化学方程式为 。用碱中和
可生成 (填溶质化学式)溶液,从而实现循环利用。
5.(2024·贵州卷)煤气化渣属于大宗固废,主要成分为 及少量MgO等。一种利用“酸
浸—碱沉—充钠”工艺,制备钠基正极材料 和回收 的流程如下:
已知:
①25℃时, ;
② 。
回答下列问题:
(1)“滤渣”的主要成分为 (填化学式)。
(2)25℃时,“碱沉”控制溶液pH至3.0,此时溶液中 。
(3)“除杂”时需加入的试剂X是 。
(4)“水热合成”中, 作为磷源,“滤液2”的作用是 ,水热合成 的离子
方程式为 。
(5)“煅烧”得到的物质也能合成钠基正极材料 ,其工艺如下:
①该工艺经碳热还原得到 ,“焙烧”生成 的化学方程式为 。
② 的晶胞结构示意图如甲所示。每个晶胞中含有 的单元数有 个。
5 / 18
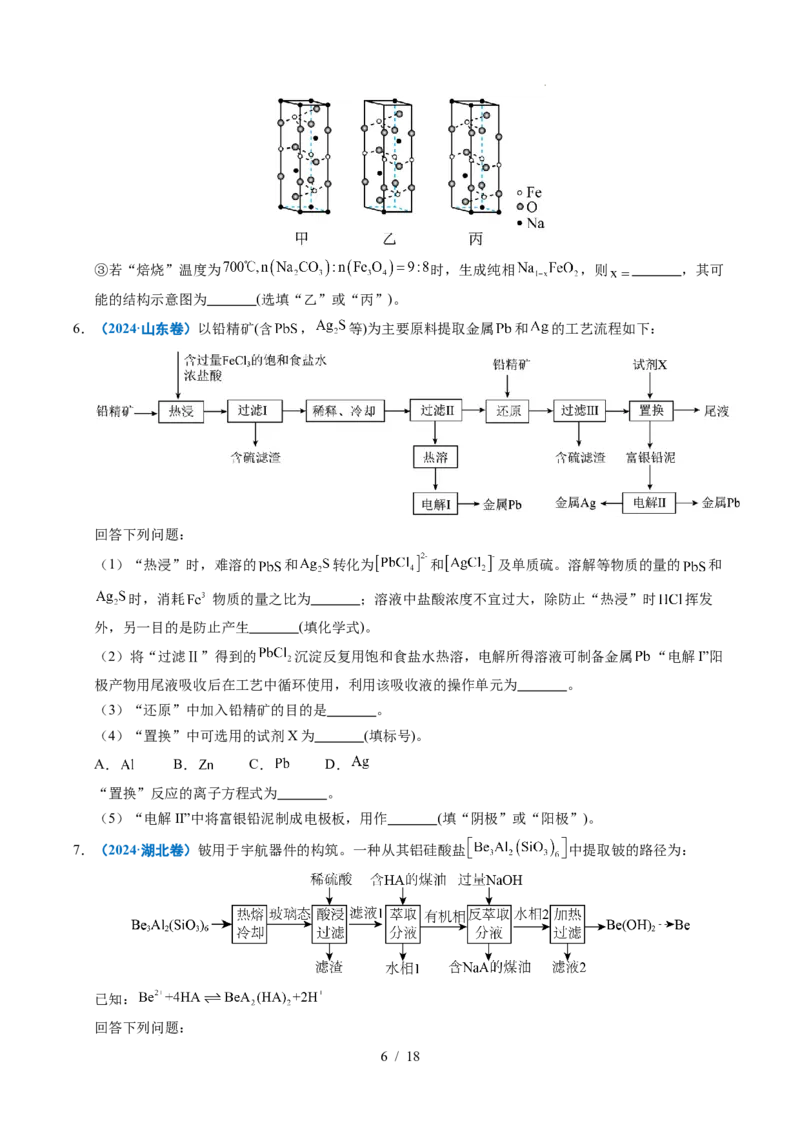
学科网(北京)股份有限公司③若“焙烧”温度为 时,生成纯相 ,则 ,其可
能的结构示意图为 (选填“乙”或“丙”)。
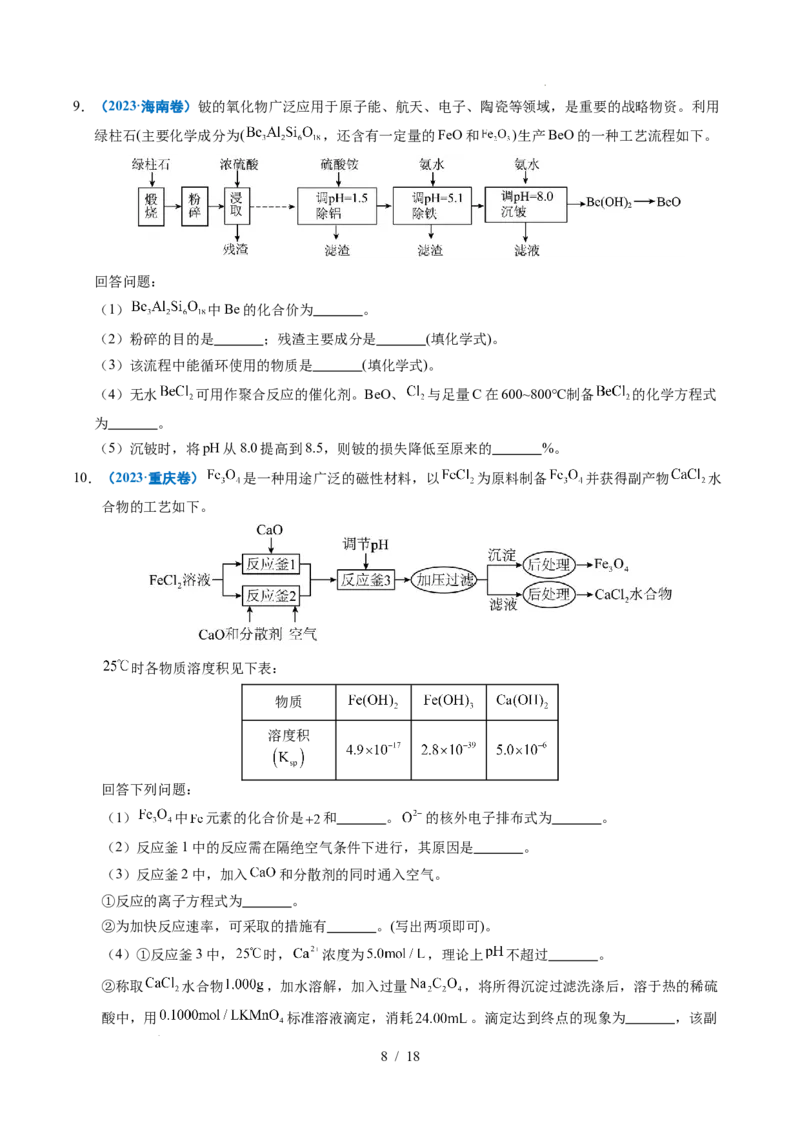
6.(2024·山东卷)以铅精矿(含 , 等)为主要原料提取金属 和 的工艺流程如下:
回答下列问题:
(1)“热浸”时,难溶的 和 转化为 和 及单质硫。溶解等物质的量的 和
时,消耗 物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发
外,另一目的是防止产生 (填化学式)。
(2)将“过滤Ⅱ”得到的 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳
极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填标号)。
A. B. C. D.
“置换”反应的离子方程式为 。
(5)“电解II”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。
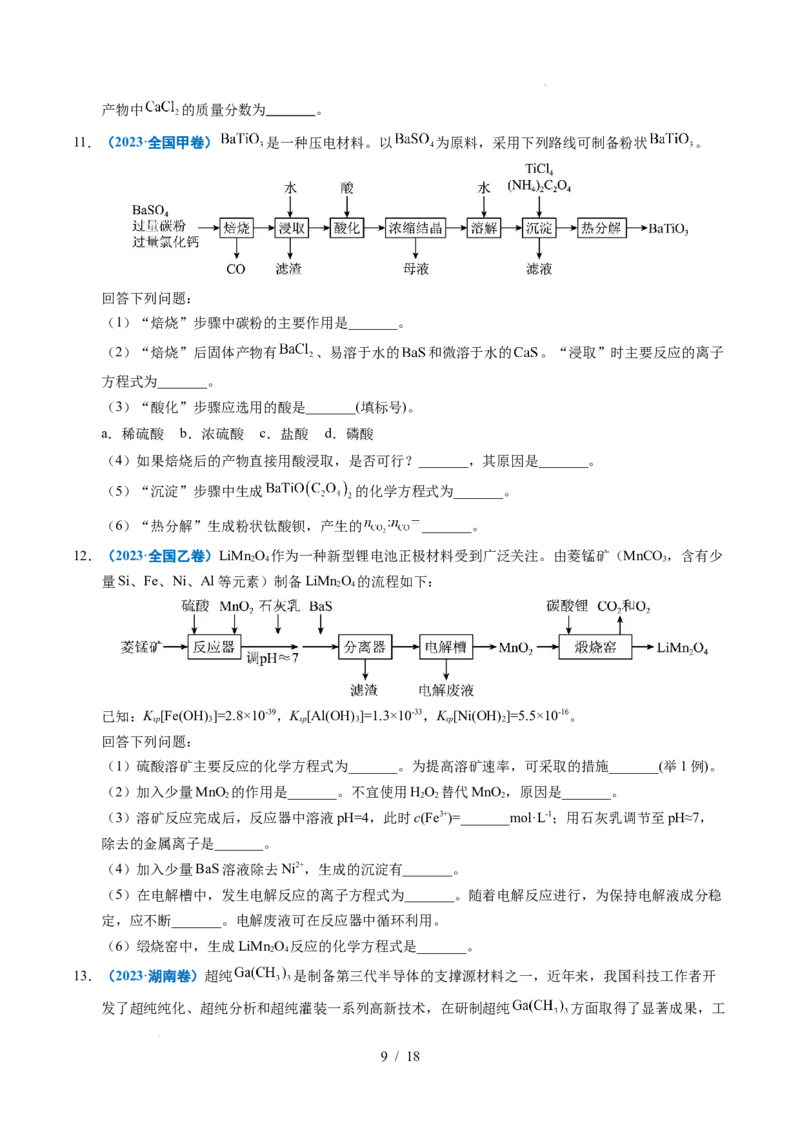
7.(2024·湖北卷)铍用于宇航器件的构筑。一种从其铝硅酸盐 中提取铍的路径为:
已知:
回答下列问题:
6 / 18
学科网(北京)股份有限公司(1)基态 的轨道表示式为 。
(2)为了从“热熔、冷却”步骤得到玻璃态,冷却过程的特点是 。
(3)“萃取分液”的目的是分离 和 ,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察
到的现象是 。
(4)写出反萃取生成 的化学方程式 。“滤液2”可以进入 步骤再利用。
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是 。
(6) 与醋酸反应得到某含4个 的配合物,4个 位于以1个O原子为中心的四面体的4个
顶点,且每个 的配位环境相同, 与 间通过 相连,其化学式为 。
8.(2024·浙江6月卷)矿物资源的综合利用有多种方法,如铅锌矿(主要成分为 )的利用有火法
和电解法等。
已知:① ;
②电解前后 总量不变;③ 易溶于水。
请回答:
(1)根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果, 中硫元素体现的性质是 (选
填“氧化性”、“还原性”、“酸性”、“热稳定性”之一)。产物B中有少量 ,该物质可溶于
浓盐酸, 元素转化为 ,写出该反应的化学方程式 ;从该反应液中提取 的步骤
如下:加热条件下,加入 (填一种反应试剂),充分反应,趁热过滤,冷却结晶,得到产品。
(2)下列说法正确的是_______。
A.电解池中发生的总反应是 (条件省略)
B.产物B主要是铅氧化物与锌氧化物
C. 化合物C在水溶液中最多可中和
D. 的氧化性弱于
(3)D的结构为 ( 或 ),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶
液探究X为何种元素。
①实验方案:取D的溶液,加入足量 溶液,加热充分反应,然后 ;
②写出D(用 表示)的溶液与足量 溶液反应的离子方程式 。
7 / 18
学科网(北京)股份有限公司9.(2023·海南卷)铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用
绿柱石(主要化学成分为( ,还含有一定量的FeO和 )生产BeO的一种工艺流程如下。
回答问题:
(1) 中Be的化合价为 。
(2)粉碎的目的是 ;残渣主要成分是 (填化学式)。
(3)该流程中能循环使用的物质是 (填化学式)。
(4)无水 可用作聚合反应的催化剂。BeO、 与足量C在600~800℃制备 的化学方程式
为 。
(5)沉铍时,将pH从8.0提高到8.5,则铍的损失降低至原来的 %。
10.(2023·重庆卷) 是一种用途广泛的磁性材料,以 为原料制备 并获得副产物 水
合物的工艺如下。
时各物质溶度积见下表:
物质
溶度积
回答下列问题:
(1) 中 元素的化合价是 和 。 的核外电子排布式为 。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是 。
(3)反应釜2中,加入 和分散剂的同时通入空气。
①反应的离子方程式为 。
②为加快反应速率,可采取的措施有 。(写出两项即可)。
(4)①反应釜3中, 时, 浓度为 ,理论上 不超过 。
②称取 水合物 ,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫
酸中,用 标准溶液滴定,消耗 。滴定达到终点的现象为 ,该副
8 / 18
学科网(北京)股份有限公司产物中 的质量分数为 。
11.(2023·全国甲卷) 是一种压电材料。以 为原料,采用下列路线可制备粉状 。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______。
(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要反应的离子
方程式为_______。
(3)“酸化”步骤应选用的酸是_______(填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_______,其原因是_______。
(5)“沉淀”步骤中生成 的化学方程式为_______。
(6)“热分解”生成粉状钛酸钡,产生的 _______。
12.(2023·全国乙卷)LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有少
2 4 3
量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______。为提高溶矿速率,可采取的措施_______(举1例)。
(2)加入少量MnO 的作用是_______。不宜使用HO 替代MnO ,原因是_______。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1;用石灰乳调节至pH≈7,
除去的金属离子是_______。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_______。
(5)在电解槽中,发生电解反应的离子方程式为_______。随着电解反应进行,为保持电解液成分稳
定,应不断_______。电解废液可在反应器中循环利用。
(6)缎烧窑中,生成LiMn O 反应的化学方程式是_______。
2 4
13.(2023·湖南卷)超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开
发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工
9 / 18
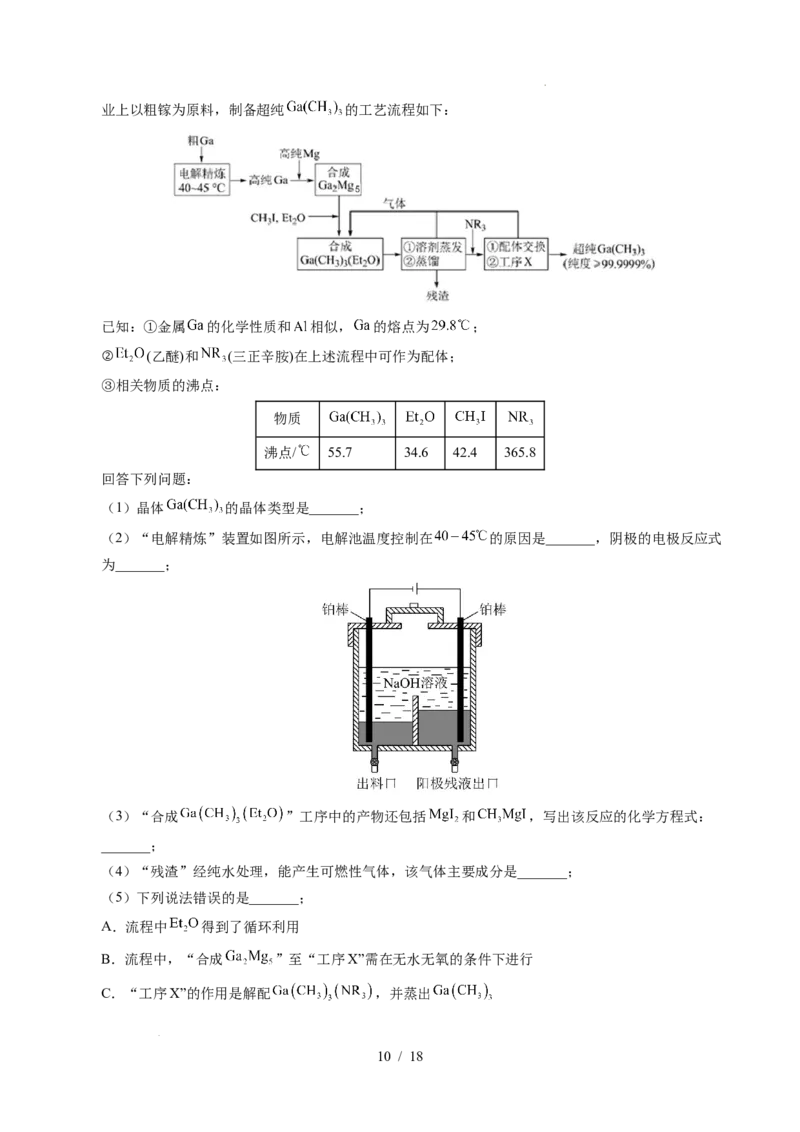
学科网(北京)股份有限公司业上以粗镓为原料,制备超纯 的工艺流程如下:
已知:①金属 的化学性质和 相似, 的熔点为 ;
② (乙醚)和 (三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
物质
沸点/ 55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体 的晶体类型是_______;
(2)“电解精炼”装置如图所示,电解池温度控制在 的原因是_______,阴极的电极反应式
为_______;
(3)“合成 ”工序中的产物还包括 和 ,写出该反应的化学方程式:
_______;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______;
(5)下列说法错误的是_______;
A.流程中 得到了循环利用
B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行
C.“工序X”的作用是解配 ,并蒸出
10 / 18
学科网(北京)股份有限公司D.用核磁共振氢谱不能区分 和
(6)直接分解 不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
的理由是_______;
(7)比较分子中的 键角大小: _______ (填“>”“<”或“=”),其
原因是_______。
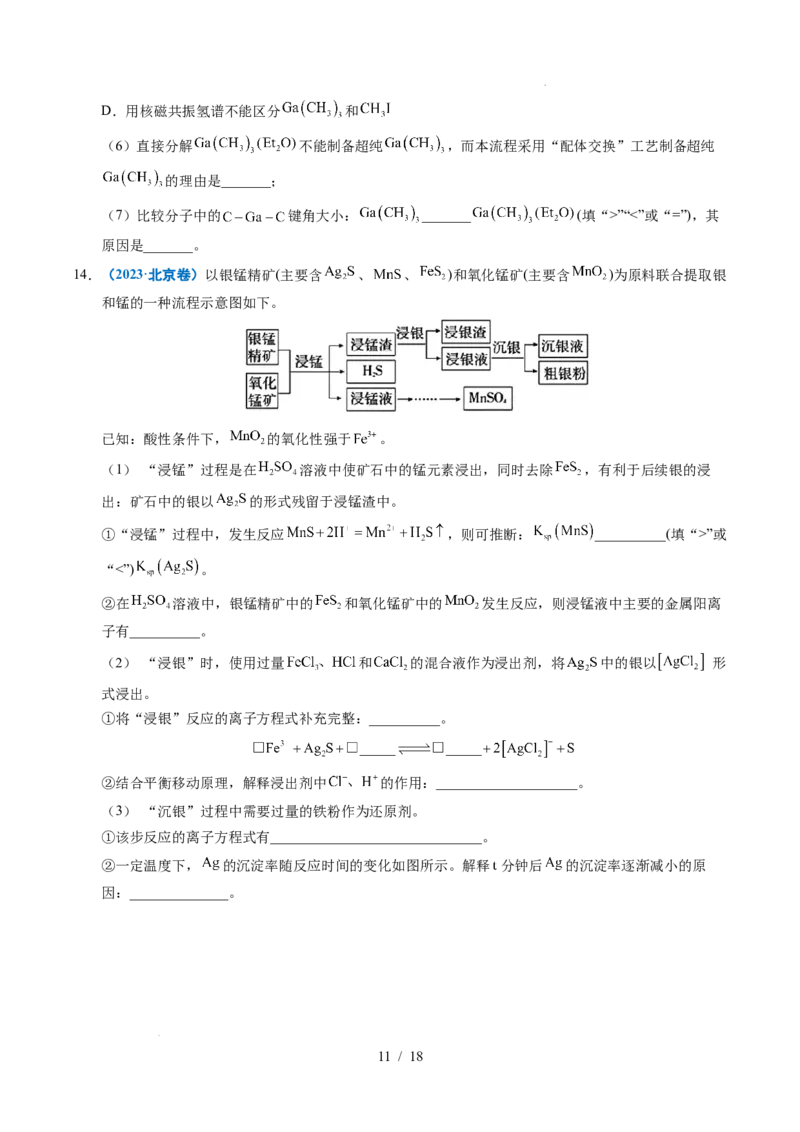
14.(2023·北京卷)以银锰精矿(主要含 、 、 )和氧化锰矿(主要含 )为原料联合提取银
和锰的一种流程示意图如下。
已知:酸性条件下, 的氧化性强于 。
(1) “浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸
出:矿石中的银以 的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,则可推断: __________(填“>”或
“<”) 。
②在 溶液中,银锰精矿中的 和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离
子有__________。
(2) “浸银”时,使用过量 和 的混合液作为浸出剂,将 中的银以 形
式浸出。
①将“浸银”反应的离子方程式补充完整:__________。
②结合平衡移动原理,解释浸出剂中 的作用:____________________。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有______________________________。
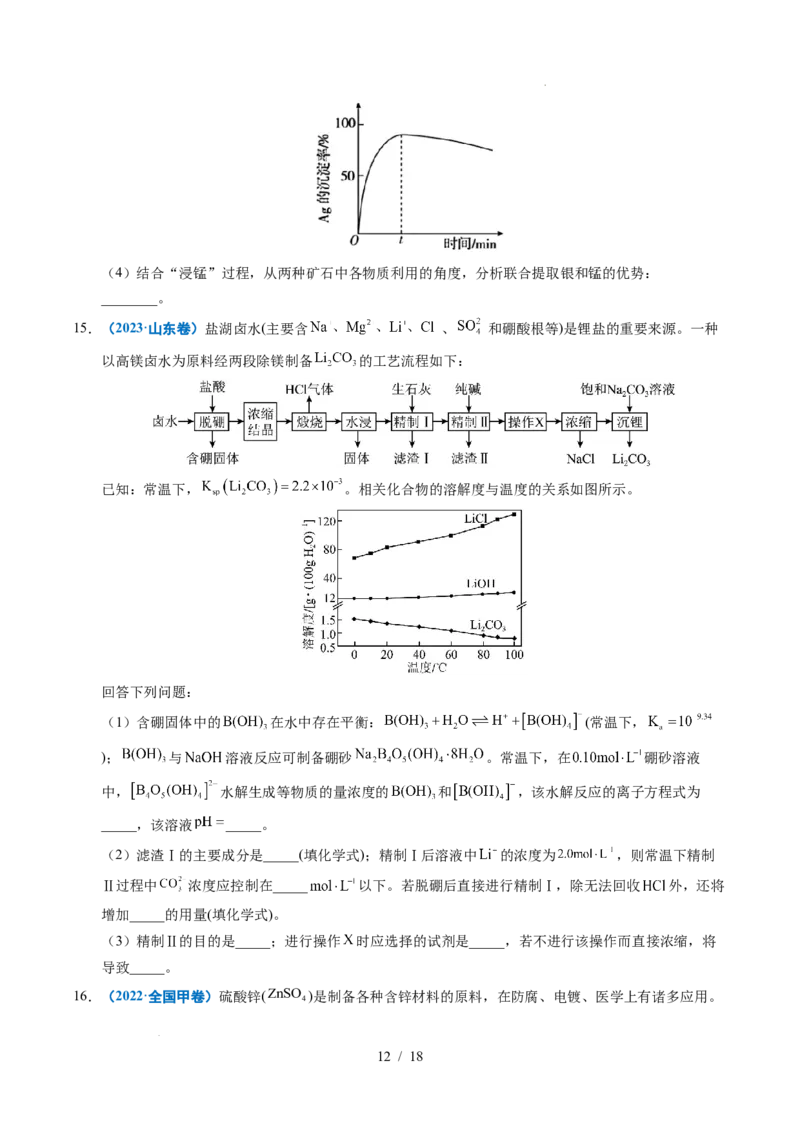
②一定温度下, 的沉淀率随反应时间的变化如图所示。解释 分钟后 的沉淀率逐渐减小的原
因:______________。
11 / 18
学科网(北京)股份有限公司(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:
________。
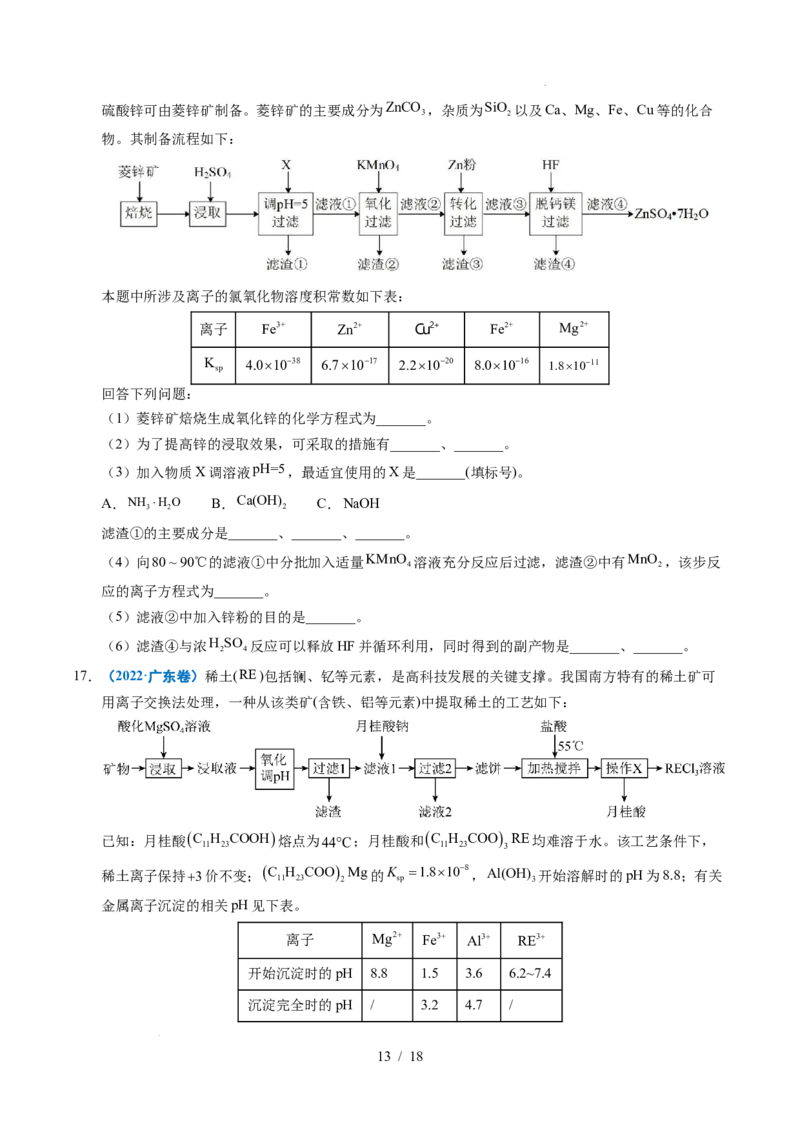
15.(2023·山东卷)盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来源。一种
以高镁卤水为原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下,
); 与 溶液反应可制备硼砂 。常温下,在 硼砂溶液
中, 水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为
_____,该溶液 _____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制
Ⅱ过程中 浓度应控制在_____ 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将
增加_____的用量(填化学式)。
(3)精制Ⅱ的目的是_____;进行操作 时应选择的试剂是_____,若不进行该操作而直接浓缩,将
导致_____。
16.(2022·全国甲卷)硫酸锌(ZnSO )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。
4
12 / 18
学科网(北京)股份有限公司硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合
3 2
物。其制备流程如下:
本题中所涉及离子的氯氧化物溶度积常数如下表:
离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
K
sp
4.01038 6.71017 2.21020 8.01016 1.81011
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液pH=5,最适宜使用的X是_______(填标号)。
A.NH H O B.Ca(OH) C.NaOH
3 2 2
滤渣①的主要成分是_______、_______、_______。
(4)向80~90℃的滤液①中分批加入适量KMnO 溶液充分反应后过滤,滤渣②中有MnO ,该步反
4 2
应的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓H SO 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
2 4
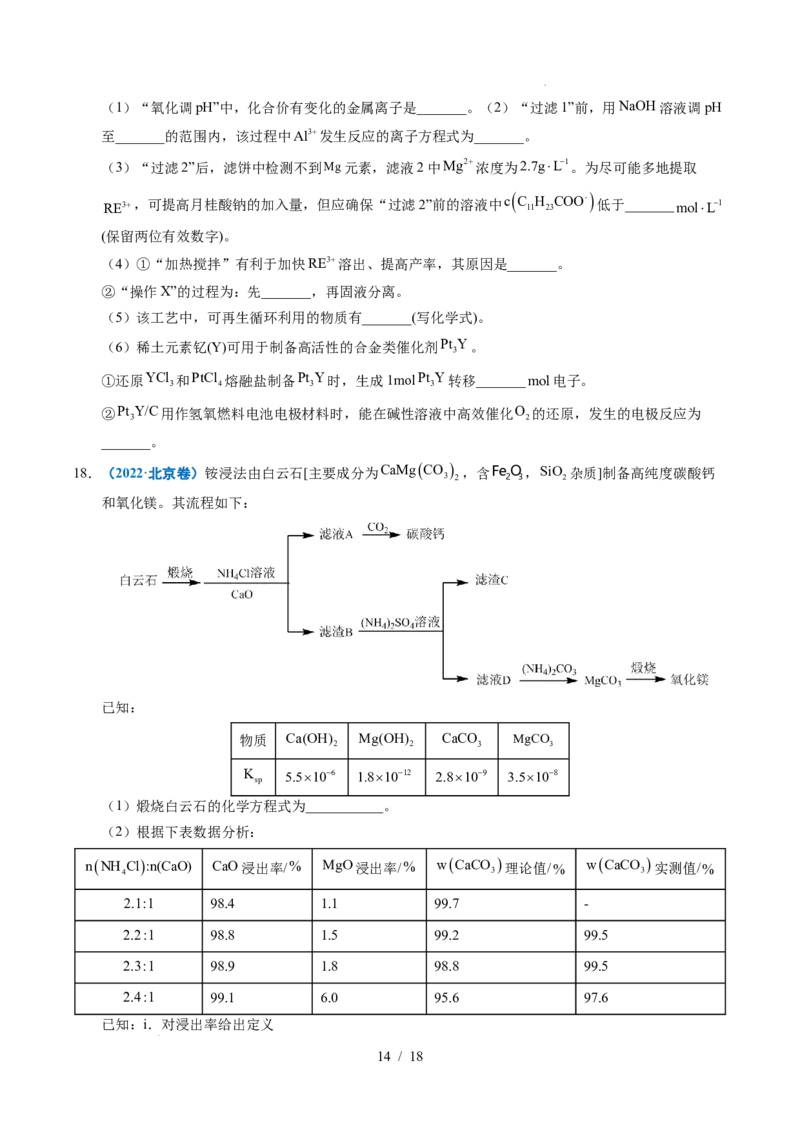
17.(2022·广东卷)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可
用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 C H COOH 熔点为44C;月桂酸和 C H COO RE均难溶于水。该工艺条件下,
11 23 11 23 3
稀土离子保持3价不变; C H COO Mg的K 1.8108 ,Al(OH) 开始溶解时的pH为8.8;有关
11 23 2 sp 3
金属离子沉淀的相关pH见下表。
离子 Mg2 Fe3 Al3 RE3
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
13 / 18
学科网(北京)股份有限公司(1)“氧化调pH”中,化合价有变化的金属离子是_______。(2)“过滤1”前,用NaOH溶液调pH
至_______的范围内,该过程中Al3发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到Mg元素,滤液2中Mg2浓度为2.7gL1。为尽可能多地提取
RE3,可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中c
C
11
H
23
COO-
低于_______molL1
(保留两位有效数字)。
(4)①“加热搅拌”有利于加快RE3溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y。
3
①还原YCl 和PtCl 熔融盐制备Pt Y时,生成1molPt Y转移_______mol电子。
3 4 3 3
②Pt Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化O 的还原,发生的电极反应为
3 2
_______。
18.(2022·北京卷)铵浸法由白云石[主要成分为CaMgCO
,含FeO,SiO 杂质]制备高纯度碳酸钙
3 2 2 3 2
和氧化镁。其流程如下:
已知:
物质 Ca(OH) Mg(OH) CaCO MgCO
2 2 3 3
K 5.5106 1.81012 2.8109 3.5108
sp
(1)煅烧白云石的化学方程式为___________。
(2)根据下表数据分析:
nNH Cl:n(CaO) CaO浸出率/% MgO浸出率/% wCaCO 理论值/% wCaCO 实测值/%
4 3 3
2.1:1 98.4 1.1 99.7 -
2.2:1 98.8 1.5 99.2 99.5
2.3:1 98.9 1.8 98.8 99.5
2.4:1 99.1 6.0 95.6 97.6
已知:i.对浸出率给出定义
14 / 18
学科网(北京)股份有限公司ii.对wCaCO
给出定义
3
①“沉钙”反应的化学方程式为___________。
②CaO浸出率远高于MgO浸出率的原因为___________。
③不宜选用的“nNH Cl:n(CaO)”数值为___________。
4
④wCaCO
实测值大于理论值的原因为___________。
3
⑤蒸馏时,随馏出液体积增大,MgO浸出率可出68.7%增加至98.9%,结合化学反应原理解释MgO
浸出率提高的原因为___________。
(3)滤渣C为___________。
(4)可循环利用的物质为___________。
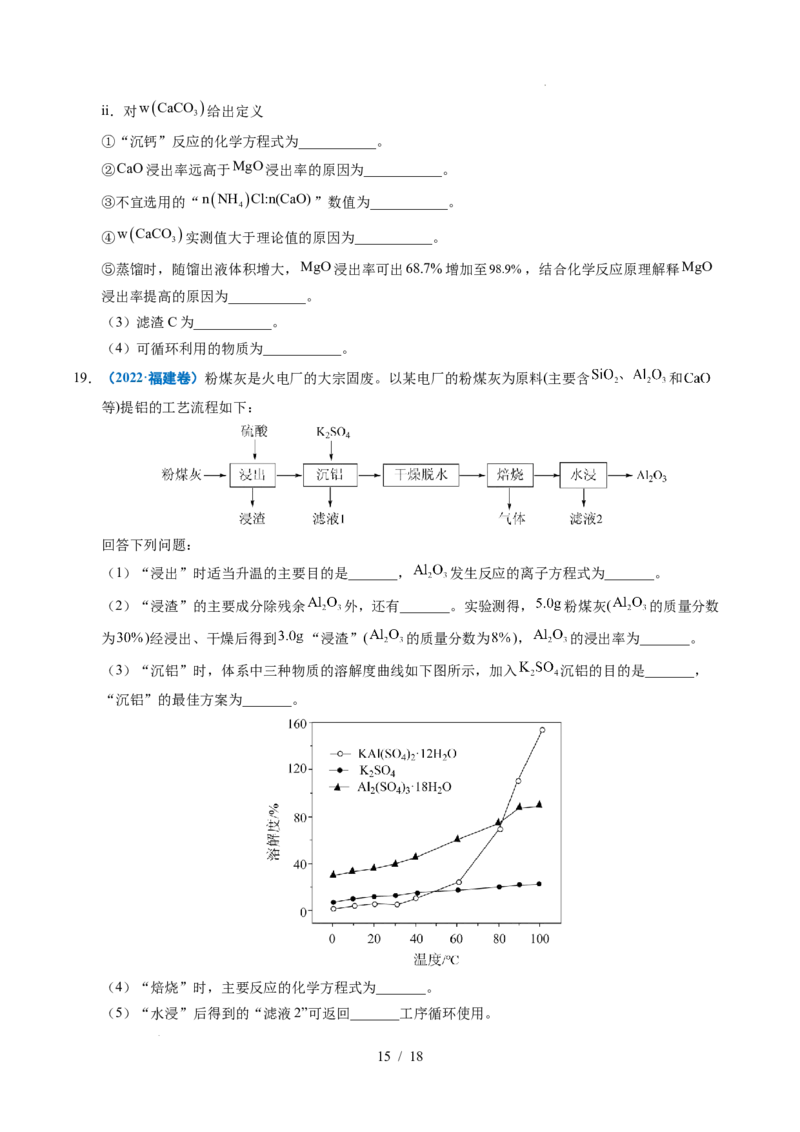
19.(2022·福建卷)粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含 和
等)提铝的工艺流程如下:
回答下列问题:
(1)“浸出”时适当升温的主要目的是_______, 发生反应的离子方程式为_______。
(2)“浸渣”的主要成分除残余 外,还有_______。实验测得, 粉煤灰( 的质量分数
为 )经浸出、干燥后得到 “浸渣”( 的质量分数为 ), 的浸出率为_______。
(3)“沉铝”时,体系中三种物质的溶解度曲线如下图所示,加入 沉铝的目的是_______,
“沉铝”的最佳方案为_______。
(4)“焙烧”时,主要反应的化学方程式为_______。
(5)“水浸”后得到的“滤液2”可返回_______工序循环使用。
15 / 18
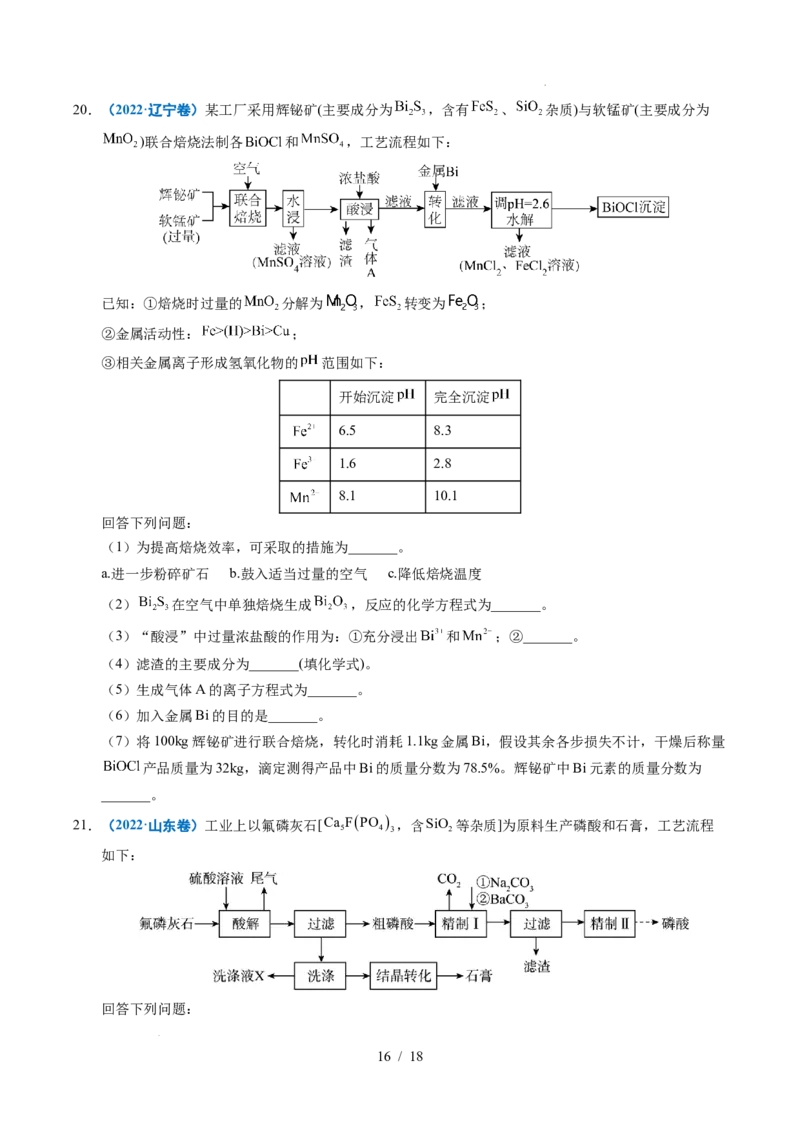
学科网(北京)股份有限公司20.(2022·辽宁卷)某工厂采用辉铋矿(主要成分为 ,含有 、 杂质)与软锰矿(主要成分为
)联合焙烧法制各 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀 完全沉淀
6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为_______。
a.进一步粉碎矿石 b.鼓入适当过量的空气 c.降低焙烧温度
(2) 在空气中单独焙烧生成 ,反应的化学方程式为_______。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出 和 ;②_______。
(4)滤渣的主要成分为_______(填化学式)。
(5)生成气体A的离子方程式为_______。
(6)加入金属Bi的目的是_______。
(7)将100kg辉铋矿进行联合焙烧,转化时消耗1.1kg金属Bi,假设其余各步损失不计,干燥后称量
产品质量为32kg,滴定测得产品中Bi的质量分数为78.5%。辉铋矿中Bi元素的质量分数为
_______。
21.(2022·山东卷)工业上以氟磷灰石[Ca FPO ,含SiO 等杂质]为原料生产磷酸和石膏,工艺流程
5 4 3 2
如下:
回答下列问题:
16 / 18
学科网(北京)股份有限公司(1)酸解时有HF产生。氢氟酸与SiO
2
反应生成二元强酸H
2
SiF
6
,离子方程式为_______。
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比nNa CO :n SiF2- =1:1加入Na CO
2 3 6 2 3
脱氟,充分反应后,c
Na+
=_______molL-1;再分批加入一定量的BaCO ,首先转化为沉淀的离子
3
是_______。
BaSiF Na SiF CaSO BaSO
6 2 6 4 4
K 1.0106 4.0106 9.0104 1.01010
sp
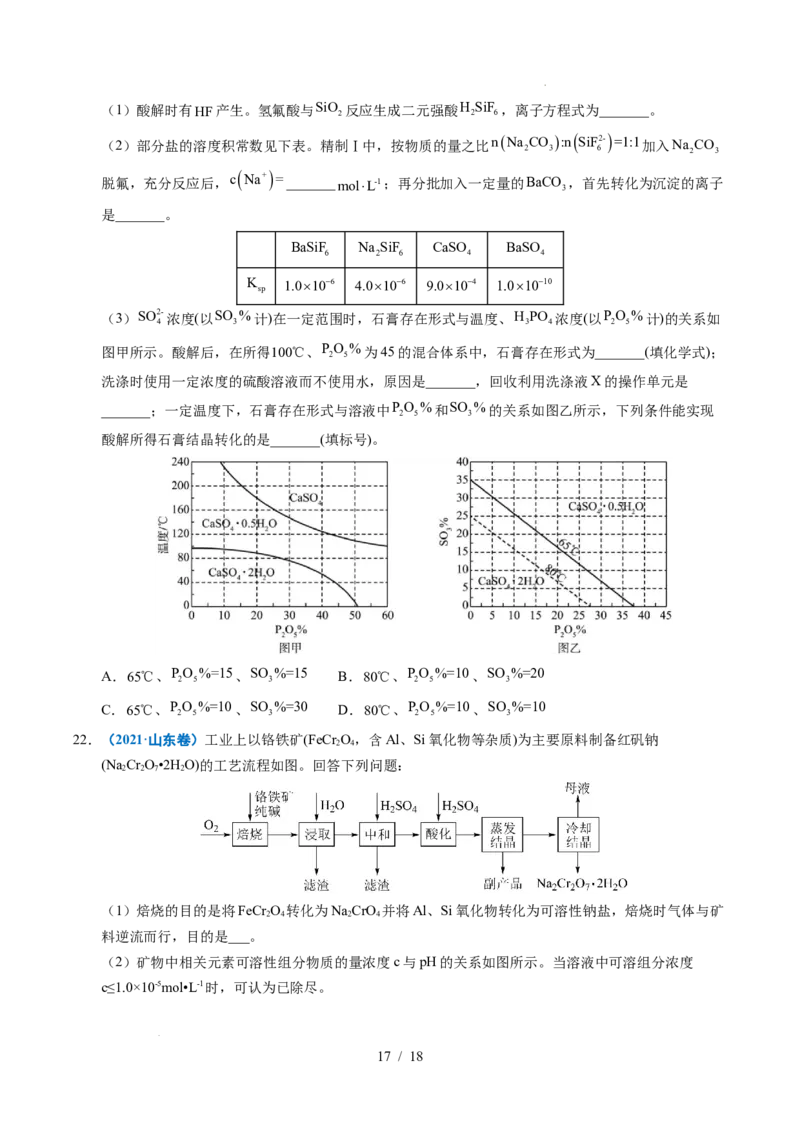
(3)SO2- 浓度(以SO %计)在一定范围时,石膏存在形式与温度、H PO 浓度(以PO %计)的关系如
4 3 3 4 2 5
图甲所示。酸解后,在所得100℃、PO %为45的混合体系中,石膏存在形式为_______(填化学式);
2 5
洗涤时使用一定浓度的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是
_______;一定温度下,石膏存在形式与溶液中PO %和SO %的关系如图乙所示,下列条件能实现
2 5 3
酸解所得石膏结晶转化的是_______(填标号)。
A.65℃、PO %=15、SO %=15 B.80℃、PO %=10、SO %=20
2 5 3 2 5 3
C.65℃、PO %=10、SO %=30 D.80℃、PO %=10、SO %=10
2 5 3 2 5 3
22.(2021·山东卷)工业上以铬铁矿(FeCr O,含Al、Si氧化物等杂质)为主要原料制备红矾钠
2 4
(NaCr O•2HO)的工艺流程如图。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCr O 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气体与矿
2 4 2 4
料逆流而行,目的是___。
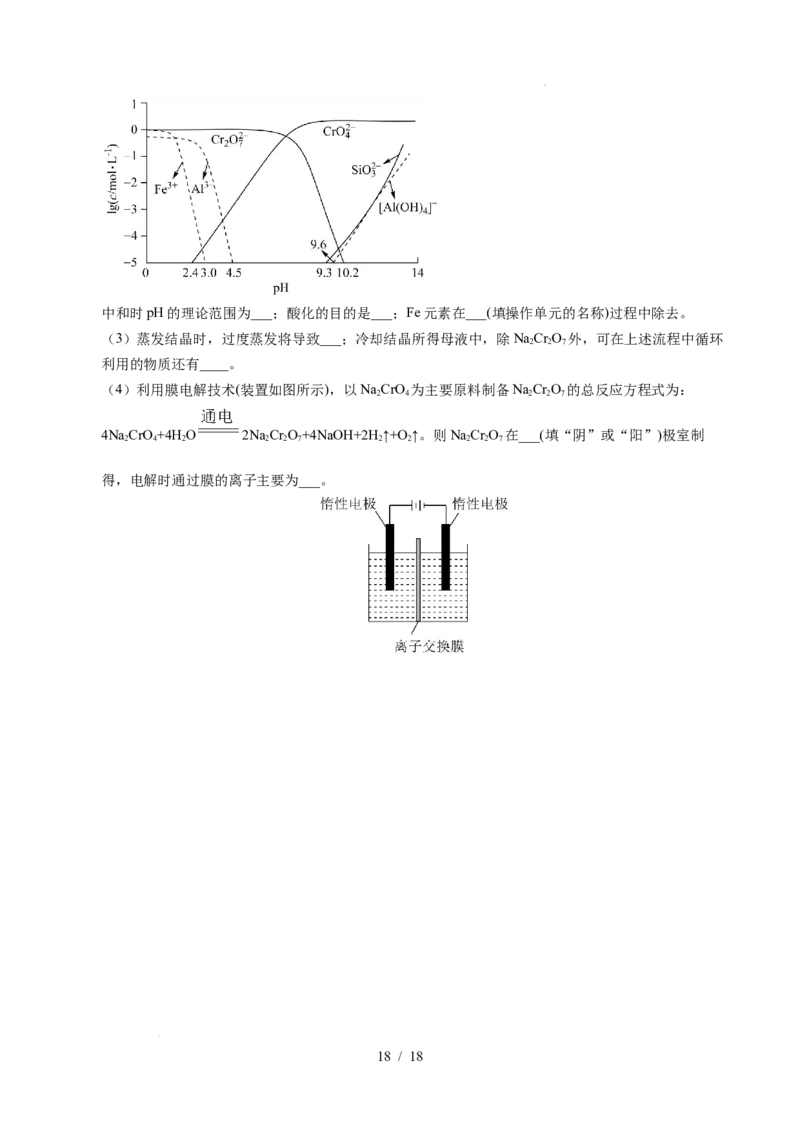
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度
c≤1.0×10-5mol•L-1时,可认为已除尽。
17 / 18
学科网(北京)股份有限公司中和时pH的理论范围为___;酸化的目的是___;Fe元素在___(填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致___;冷却结晶所得母液中,除NaCr O 外,可在上述流程中循环
2 2 7
利用的物质还有____。
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反应方程式为:
2 4 2 2 7
4NaCrO+4HO 2NaCr O+4NaOH+2H↑+O↑。则NaCr O 在___(填“阴”或“阳”)极室制
2 4 2 2 2 7 2 2 2 2 7
得,电解时通过膜的离子主要为___。
18 / 18
学科网(北京)股份有限公司