文档内容
2012 年江苏省高考化学试卷 C.催化剂能降低反应的活化能
D.逆反应的活化能大于正反应的活化能
一.单项选择题:本题包括10小题,每小题2分,共计20分.每小题只有一个选项符合题意.
5.(2分)下列有关物质的性质与应用不相对应的是( )
1.(2分)化学在资源利用、环境保护等与社会可持续发展密切相关的领域发挥着积极作用.下列做法与社会
A.明矾能水解生成Al(OH) 胶体,可用作净水剂
可持续发展理念相违背的是( ) 3
B.FeCl 溶液能与Cu 反应,可用于蚀刻印刷电路
A.改进汽车尾气净化技术,减少大气污染物的排放 3
C.SO 具有氧化性,可用于漂白纸浆
B.开发利用可再生能源,减少化石燃料的使用 2
D.Zn 具有还原性和导电性,可用作锌锰干电池的负极材料
C.研发可降解高分子材料,减少“白色污染”
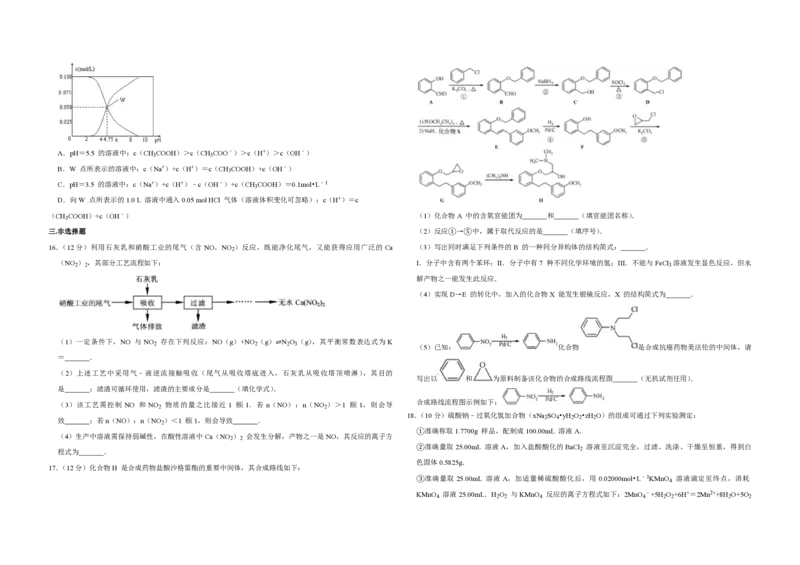
6.( 2分 ) 用 下 列 实 验 装 置 进 行 相 应 实 验 , 能 达 到 实 验 目 的 是 ( )
D.过度开采矿物资源,促进地方经济发展
2.(2分)下列有关化学用语表示正确的是( )
A.乙酸的结构简式:C H O
2 4 2
B.F﹣的结构示意图:
C.中子数为20 的氯原子:20 Cl
17
A.用图1所示装置除去Cl 中含有的少量HCl
2
D.NH 的电子式:
3
B.用图2所示装置蒸干NH Cl饱和溶液制备NH Cl晶体
3.(2分)常温下,下列各组离子在指定溶液中一定能大量共存的是( ) 4 4
C.用图3所示装置制取少量纯净的CO 气体
A.0.1mol•L﹣1NaOH 溶液:K+、Na+、SO 2﹣、CO 2﹣ 2
4 3
D.用图4所示装置分离CCl 萃取碘水后已分层的有机层和水层
B.0.1mol•L﹣1Na CO 溶液:K+、Ba2+、NO ﹣、Cl﹣ 4
2 3 3
7.(2分)下列物质的转化在给定条件下能实现的是( )
C.0.1mol•L﹣1FeCl 溶液:K+、NH +、I﹣、SCN﹣
3 4
𝑁𝑎𝑂𝐻(𝑎𝑞) 𝐶𝑂 2
D.c(H+)/c(OH﹣)=1×1014的溶液:Ca2+、Na+、ClO﹣、NO ﹣ ①Al 2 O 3 → NaAlO 2 (aq)→Al(OH) 3
3 △
4.(2分)某反应的反应过程中能量变化如图所示(图中 E 1 表示正反应的活化能,E 2 表示逆反应的活化 ②S 𝑂 2 → /点燃 SO 𝐻 → 2 𝑂 H SO
3 2 4
能).下列有关叙述正确的是( )
𝐻𝐶𝑙(𝑎𝑞) △
③Fe O → FeCl (aq)→无水FeCl
2 3 3 3
𝑁𝐻 3 ,𝐶𝑂 2 △
④饱和NaCl(aq) → NaHCO →Na CO
3 2 3
石灰乳 煅烧
⑤MgCl (aq) → Mg(OH) →MgO.
2 2
A.①③⑤ B.②③④ C.②④⑤ D.①④⑤
8.(2分)设N 表示阿伏加德罗常数的值.下列说法正确的是( )
A.该反应为吸热反应 A
A.标准状况下,0.1 mol Cl 溶于水,转移的电子数目为0.1N
B.催化剂能改变反应的焓变 2 AB.常温常压下,18 g H O 中含有的原子总数为3N D.1 mol 该物质最多可与1 mol NaOH 反应
2 A
C.标准状况下,11.2 L CH CH OH 中含有的分子数目为0.5N 12.(3分)短周期元素 X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的 3
3 2 A
D.常温常压下,2.24 L CO 和CO 混合气体中含有的碳原子数目为0.1N 倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是
2 A
9.(2分)下列表示对应化学反应的离子方程式正确的是( ) ( )
A.用KIO 氧化酸性溶液中的KI:5I﹣+IO ﹣+3H O=3I +6OH﹣ A.元素X的简单气态氢化物的热稳定性比W的强
3 3 2 2
△ B.元素W的最高价氧化物对应水化物的酸性比Z的弱
¯
B.向NH
4
HCO
3
溶液中加过量的NaOH溶液并加热:NH
4
++OH﹣ NH
3
↑+H
2
O C.化合物YX、ZX
2
、WX
3
中化学键的类型相同
D.原子半径的大小顺序:r >r >r >r
Y Z W X
C.将过量SO 通入冷氨水中:SO +NH •H O=HSO ﹣+NH +
2 2 3 2 3 4 13.(3分)下列根据实验操作和现象所得出的结论正确的是( )
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO ﹣=Ag++NO↑+H O
3 2 A.向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO 溶液均有固体析出蛋白质均发生变性
4
10.(2分)下列有关说法正确的是( )
B.向溶液X 中先滴加稀硝酸,再滴加Ba(NO ) 溶液出现白色沉淀溶液X 中一定含有SO 2﹣
3 2 4
A.CaCO (s)═CaO(s)+CO (g)室温下不能自发进行,说明该反应的△H<0
3 2
C.向一定浓度的Na SiO 溶液中通入适量CO 气体出现白色沉淀H SiO 的酸性比H CO 的酸性强
2 3 2 2 3 2 3
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
D.向浓度均为0.1 mol•L﹣1 NaCl 和NaI混合溶液中滴加少量AgNO 溶液出现黄色沉淀K (AgCl)>K
3 sp sp
C.N (g)+3H (g)⇌2NH (g)△H<0,其他条件不变时升高温度,反应速率v(H )和H 的平衡转
2 2 3 2 2 (AgI)
化率均增大
14.(3分)温度为T时;向2.0L恒容密闭容器中充入1.0mol PCl ;反应PCl (g)⇌PCl (g)+Cl (g)经过
5 5 3 2
D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
一段时间后达到平衡。反应过程中测定的部分数据见表:
二.不定项选择题:本题包括5小题,每小题3分,共计20分.每小题只有一个或两个选项符合题意.若正确
t/s 0 50 150 250 350
答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且
n(PCl )/mol 0 0.16 0.19 0.20 0.20
3
都正确的得满分,但只要选错一个,该小题就得0分.
下列说法正确的是( )
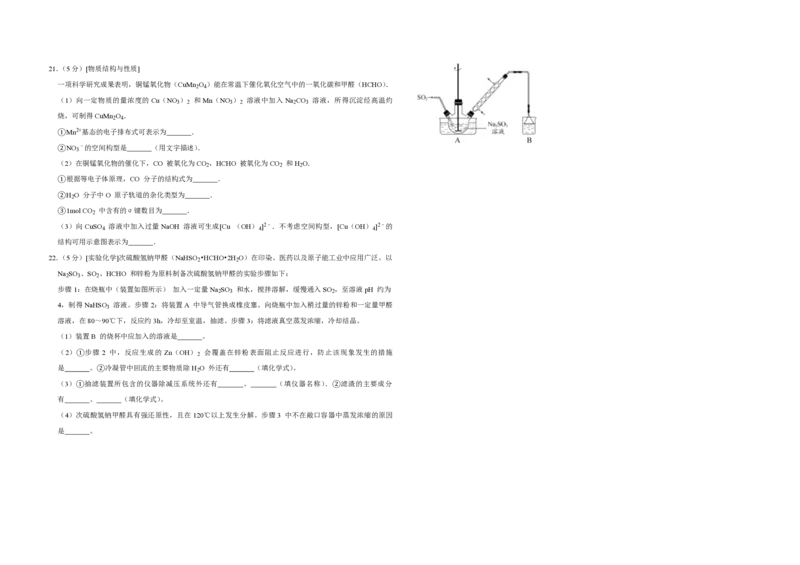
11.(3分)普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他
A.反应在前50 s的平均速率v(PCl )=0.0032 mol•L﹣1•s﹣1
3
汀的性质描述正确的是( )
B.保持其他条件不变;升高温度;平衡时c(PCl )=0.11 mol•L﹣1;则反应的△H<0
3
C.相同温度下;起始时向容器中充入1.0 mol PCl 、0.20 mol PCl 和0.20 mol Cl ;反应达到平衡前v(正)
5 3 2
>v(逆)
D.相同温度下;起始时向容器中充入2.0 mol PCl 和2.0 mol Cl ;达到平衡时;PCl 的转化率小于80%
3 2 3
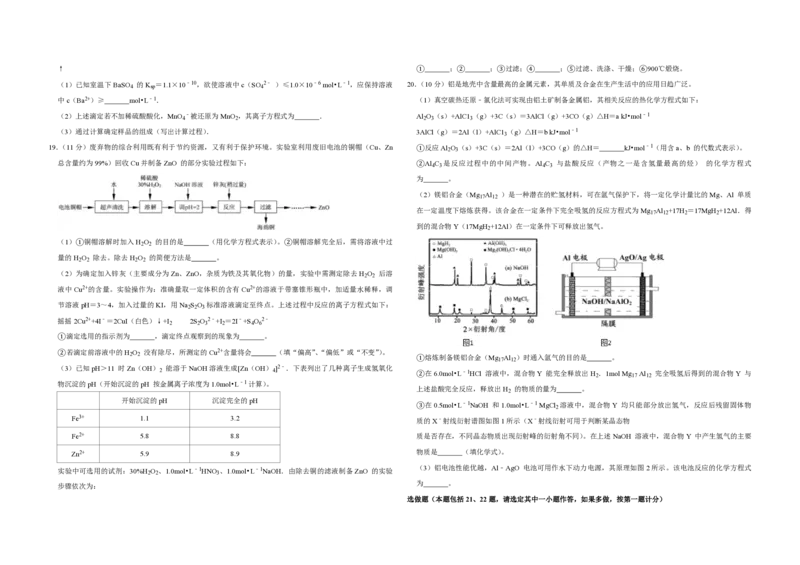
15.(3分)25℃时,有c(CH
3
COOH)+c(CH
3
COO﹣)=0.1mol•L﹣1的一组醋酸、醋酸钠混合溶液,溶液中
A.能与FeCl
3
溶液发生显色反应 c(CH
3
COOH)、c(CH
3
COO﹣)与 pH 的关系如图所示.下列有关溶液中离子浓度关系的叙述正确的是
B.能使酸性KMnO 溶液褪色 ( )
4
C.能发生加成、取代、消去反应A.pH=5.5 的溶液中:c(CH COOH)>c(CH COO﹣)>c(H+)>c(OH﹣)
3 3
B.W 点所表示的溶液中:c(Na+)+c(H+)=c(CH COOH)+c(OH﹣)
3
C.pH=3.5 的溶液中:c(Na+)+c(H+)﹣c(OH﹣)+c(CH COOH)=0.1mol•L﹣1
3
D.向W 点所表示的1.0 L 溶液中通入0.05 mol HCl 气体(溶液体积变化可忽略):c(H+)=c
(CH COOH)+c(OH﹣) (1)化合物A 中的含氧官能团为 和 (填官能团名称).
3
三.非选择题 (2)反应①→⑤中,属于取代反应的是 (填序号).
16.(12分)利用石灰乳和硝酸工业的尾气(含 NO、NO )反应,既能净化尾气,又能获得应用广泛的 Ca (3)写出同时满足下列条件的B 的一种同分异构体的结构简式: .
2
(NO ) ,其部分工艺流程如下: I.分子中含有两个苯环;II.分子中有7 种不同化学环境的氢;III.不能与FeCl 溶液发生显色反应,但水
2 2 3
解产物之一能发生此反应.
(4)实现D→E 的转化中,加入的化合物X 能发生银镜反应,X 的结构简式为 .
(1)一定条件下,NO 与 NO 存在下列反应:NO(g)+NO (g)⇌N O (g),其平衡常数表达式为 K
2 2 2 3
(5)已知: 化合物 是合成抗癌药物美法伦的中间体,请
= .
(2)上述工艺中采用气﹣液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的
写出以 和 为原料制备该化合物的合成路线流程图 (无机试剂任用).
是 ;滤渣可循环使用,滤渣的主要成分是 (填化学式).
(3)该工艺需控制 NO 和 NO 物质的量之比接近 1 颐 1.若 n(NO):n(NO )>1 颐 1,则会导
合成路线流程图示例如下:
2 2
18.(10分)硫酸钠﹣过氧化氢加合物(xNa SO •yH O •zH O)的组成可通过下列实验测定:
2 4 2 2 2
致 ;若n(NO):n(NO )<1 颐1,则会导致 .
2
①准确称取1.7700g 样品,配制成100.00mL 溶液A.
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO ) 会发生分解,产物之一是NO,其反应的离子方
2 2
②准确量取25.00mL 溶液A,加入盐酸酸化的BaCl 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白
程式为 . 2
色固体0.5825g.
17.(12分)化合物H 是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
③准确量取 25.00mL 溶液 A,加适量稀硫酸酸化后,用 0.02000mol•L﹣1KMnO 溶液滴定至终点,消耗
4
KMnO 溶液25.00mL.H O 与KMnO 反应的离子方程式如下:2MnO ﹣+5H O +6H+=2Mn2++8H O+5O
4 2 2 4 4 2 2 2 2↑ ① ;② ;③过滤;④ ;⑤过滤、洗涤、干燥;⑥900℃煅烧。
(1)已知室温下BaSO 的K =1.1×10﹣10,欲使溶液中c(SO 2﹣ )≤1.0×10﹣6 mol•L﹣1,应保持溶液 20.(10分)铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
4 sp 4
中c(Ba2+)≥ mol•L﹣1. (1)真空碳热还原﹣氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
(2)上述滴定若不加稀硫酸酸化,MnO ﹣被还原为MnO ,其离子方程式为 . Al O (s)+AlC1 (g)+3C(s)=3AlCl(g)+3CO(g)△H=a kJ•mol﹣1
4 2 2 3 3
(3)通过计算确定样品的组成(写出计算过程). 3AlCl(g)=2Al(l)+AlC1 (g)△H=b kJ•mol﹣1
3
19.(11分)废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn ①反应Al O (s)+3C(s)=2Al(l)+3CO(g)的△H= kJ•mol﹣1(用含a、b 的代数式表示)。
2 3
总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下: ②Al C 是反应过程中的中间产物。Al C 与盐酸反应(产物之一是含氢量最高的烃) 的化学方程式
4 3 4 3
为 。
(2)镁铝合金(Mg Al )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质
17 12
在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg Al +17H =17MgH +12Al.得
17 12 2 2
到的混合物Y(17MgH
2
+12Al)在一定条件下可释放出氢气。
(1)①铜帽溶解时加入H O 的目的是 (用化学方程式表示)。②铜帽溶解完全后,需将溶液中过
2 2
量的H O 除去。除去H O 的简便方法是 。
2 2 2 2
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H O 后溶
2 2
液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调
节溶液pH=3~4,加入过量的KI,用Na S O 标准溶液滴定至终点。上述过程中反应的离子方程式如下:
2 2 3
摇摇2Cu2++4I﹣=2CuI(白色)↓+I 2S O 2﹣+I =2I﹣+S O 2﹣
2 2 3 2 4 6
①滴定选用的指示剂为 ,滴定终点观察到的现象为 。
②若滴定前溶液中的H O 没有除尽,所测定的Cu2+含量将会 (填“偏高”、“偏低”或“不变”)。
2 2
①熔炼制备镁铝合金(Mg Al )时通入氩气的目的是 。
17 12
(3)已知pH>11 时Zn(OH) 能溶于NaOH溶液生成[Zn(OH) ]2﹣.下表列出了几种离子生成氢氧化
2 4 ②在6.0mol•L﹣1HCl 溶液中,混合物Y 能完全释放出H .1mol Mg Al 完全吸氢后得到的混合物Y 与
2 17 12
物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L﹣1计算)。
上述盐酸完全反应,释放出H 的物质的量为 。
2
开始沉淀的pH 沉淀完全的pH
③在0.5mol•L﹣1NaOH 和1.0mol•L﹣1 MgCl 溶液中,混合物Y 均只能部分放出氢气,反应后残留固体物
2
Fe3+ 1.1 3.2 质的X﹣射线衍射谱图如图1所示(X﹣射线衍射可用于判断某晶态物
Fe2+ 5.8 8.8 质是否存在,不同晶态物质出现衍射峰的衍射角不同)。在上述NaOH 溶液中,混合物Y 中产生氢气的主要
Zn2+ 5.9 8.9 物质是 (填化学式)。
实验中可选用的试剂:30%H O 、1.0mol•L﹣1HNO 、1.0mol•L﹣1NaOH.由除去铜的滤液制备ZnO 的实验
(3)铝电池性能优越,Al﹣AgO 电池可用作水下动力电源,其原理如图2所示。该电池反应的化学方程式
2 2 3
为 。
步骤依次为:
选做题(本题包括21、22题,请选定其中一小题作答,如果多做,按第一题计分)21.(5分)[物质结构与性质]
一项科学研究成果表明,铜锰氧化物(CuMn O )能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
2 4
(1)向一定物质的量浓度的 Cu(NO ) 和 Mn(NO ) 溶液中加入 Na CO 溶液,所得沉淀经高温灼
3 2 3 2 2 3
烧,可制得CuMn O .
2 4
①Mn2+基态的电子排布式可表示为 .
②NO ﹣的空间构型是 (用文字描述).
3
(2)在铜锰氧化物的催化下,CO 被氧化为CO ,HCHO 被氧化为CO 和H O.
2 2 2
①根据等电子体原理,CO 分子的结构式为 .
②H O 分子中O 原子轨道的杂化类型为 .
2
③1mol CO 中含有的σ键数目为 .
2
(3)向CuSO 溶液中加入过量NaOH 溶液可生成[Cu (OH) ]2﹣.不考虑空间构型,[Cu(OH) ]2﹣的
4 4 4
结构可用示意图表示为 .
22.(5分)[实验化学]次硫酸氢钠甲醛(NaHSO •HCHO•2H O)在印染、医药以及原子能工业中应用广泛。以
2 2
Na SO 、SO 、HCHO 和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
2 3 2
步骤1:在烧瓶中(装置如图所示) 加入一定量Na SO 和水,搅拌溶解,缓慢通入SO ,至溶液pH 约为
2 3 2
4,制得NaHSO 溶液。步骤2:将装置A 中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛
3
溶液,在80~90℃下,反应约3h,冷却至室温,抽滤。步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B 的烧杯中应加入的溶液是 。
(2)①步骤 2 中,反应生成的 Zn(OH) 会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施
2
是 。②冷凝管中回流的主要物质除H O 外还有 (填化学式)。
2
(3)①抽滤装置所包含的仪器除减压系统外还有 、 (填仪器名称).②滤渣的主要成分
有 、 (填化学式)。
(4)次硫酸氢钠甲醛具有强还原性,且在120℃以上发生分解。步骤3 中不在敞口容器中蒸发浓缩的原因
是 。