文档内容
2013年普通高等学校招生全国统一考试(安徽卷)(化学)
第I卷
(选择题 共120分)
本卷共20小题,每小题6分,共120分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
以下数据可供解题时参考
相对原子质量(原子量):H 1 C 12 N 14 O 16 Al 27 S 32 Cl 35.5 Ce 140
Pb 207
7.我国科学家研制出一种催化剂,能在室温下高效催化空气中的甲醛的氧化,其反应如下:
催
HCHO+O CO+H O。下列有关说法正确的是
2 2 2
A.该反应为吸热反应 B.CO 分子中的化学键为非极性键
2
C.HCHO分子中既含有σ键又含有π键 D.每生成1.8gH O消耗22.4LO
2 2
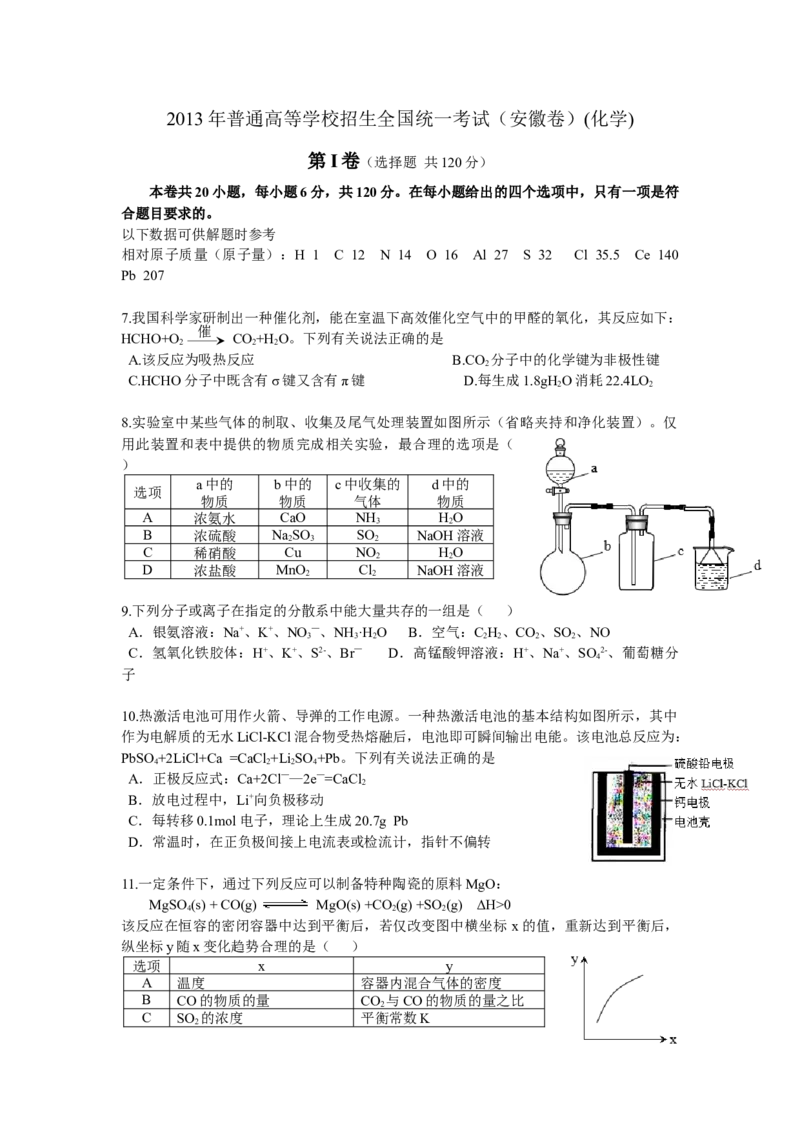
8.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅
用此装置和表中提供的物质完成相关实验,最合理的选项是(
)
a中的 b中的 c中收集的 d中的
选项
物质 物质 气体 物质
A 浓氨水 CaO NH HO
3 2
B 浓硫酸 NaSO SO NaOH溶液
2 3 2
C 稀硝酸 Cu NO HO
2 2
D 浓盐酸 MnO Cl NaOH溶液
2 2
9.下列分子或离子在指定的分散系中能大量共存的一组是( )
A.银氨溶液:Na+、K+、NO —、NH ·H O B.空气:C H、CO、SO 、NO
3 3 2 2 2 2 2
C.氢氧化铁胶体:H+、K+、S2-、Br— D.高锰酸钾溶液:H+、Na+、SO 2-、葡萄糖分
4
子
10.热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中
作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:
PbSO +2LiCl+Ca =CaCl +Li SO +Pb。下列有关说法正确的是
4 2 2 4
A.正极反应式:Ca+2Cl——2e—=CaCl
2
B.放电过程中,Li+向负极移动
C.每转移0.1mol电子,理论上生成20.7g Pb
D.常温时,在正负极间接上电流表或检流计,指针不偏转
11.一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:
MgSO (s) + CO(g) MgO(s) +CO (g) +SO (g) ΔH>0
4 2 2
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标 x的值,重新达到平衡后,
纵坐标y随x变化趋势合理的是( )
选项 x y
A 温度 容器内混合气体的密度
B CO的物质的量 CO 与CO的物质的量之比
2
C SO 的浓度 平衡常数K
2D MgSO 的质量(忽略体 CO的转化率
4
积)
12.我省盛产矿盐(主要成分是NaCl,还含有SO 2—等其他可溶性杂质的离子)。下列有关说
4
法正确的是
A.由矿盐生成食盐,除去SO 2—最合适的试剂是Ba(NO )
4 3 2
B.工业上通过电解氯化钠溶液制备金属钠和氯气
C.室温下,AgCl在水中的溶解度小于在食盐中的溶解度
D用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液
13.已知NaHSO 溶液显酸性,溶液中存在以下平衡:
3
HSO —+ H O HSO + OH— ①
3 2 2 3
HSO — H+ + SO 2— ②
3 3
向0.1mol·L-1的NaHSO 溶液中分别加入以下物质,下列有关说法正确的是
3
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO —)增大
3
B.加入少量NaSO 固体,则c(H+) + c(Na+) = c(HSO —) + c(OH—) + c(SO 2—)
2 3 3 3
C.加入少量NaOH溶液, 、 的值均增大
D.加入氨水至中性,则2c(Na+) = c(SO 2—)>c(H+) = c(OH—)
3
25.(15分)X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关
信息如下表:
元素 相关信息
X X的最高价氧化物对应的水化物化学式为HXO
2 3
Y Y是地壳中含量最高的元素
Z Z的基态原子最外层电子排布式为3s23p1
W W的一种核素的质量数为28,中子数为14
(1)W位于元素周期表第 周期第 族;W的原子半径比X的 (填
“大”或“小”)。
(2)Z的第一电离能比W的 (填“大”或“小”);XY 由固态变为气态所需克
2
服的微粒间作用力是 ;氢元素、X、Y的原子可共同形成多种分子,写出其中一
种能形成同种分子间氢键的物质名称 。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的
现象是
;
W 的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是
。
13.在25°、101kPa下,已知13.5g的Z固体单质在Y 气体中完全燃烧后恢复至原状态,放
2
热419kJ,
该反应的热化学方程式是 。26.(16分)
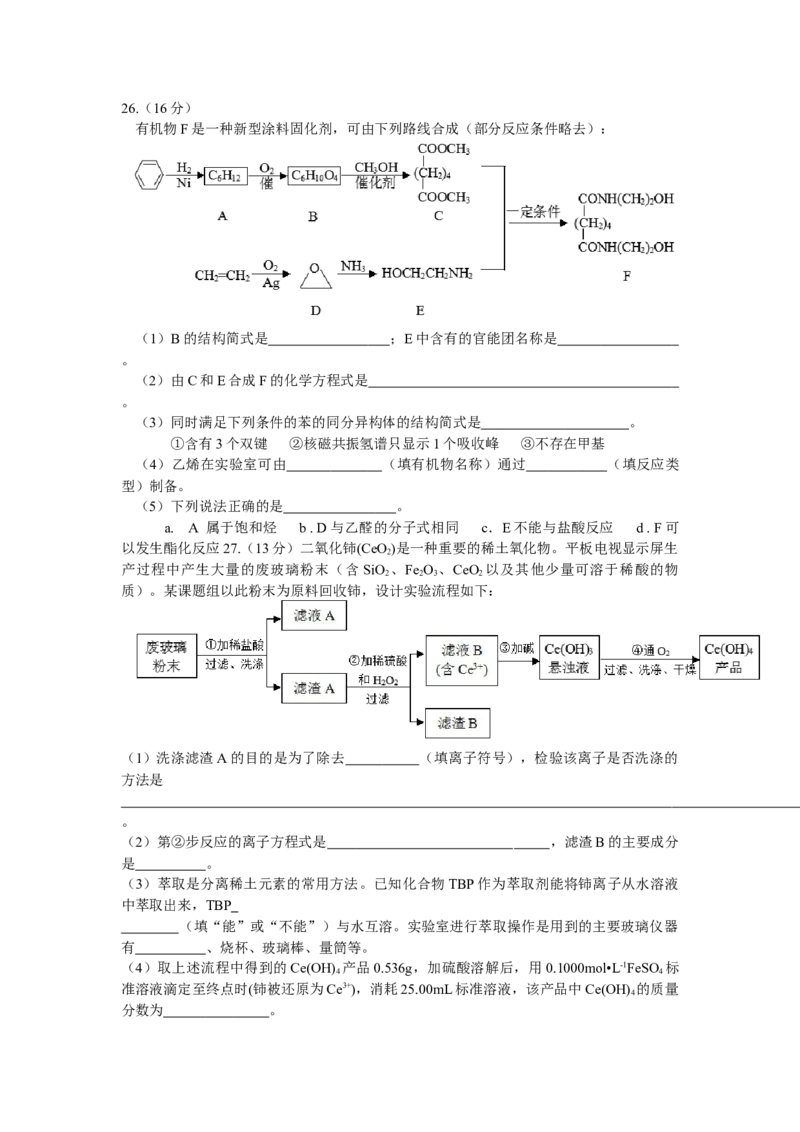
有机物F是一种新型涂料固化剂,可由下列路线合成(部分反应条件略去):
(1)B的结构简式是 ;E中含有的官能团名称是
。
(2)由C和E合成F的化学方程式是
。
(3)同时满足下列条件的苯的同分异构体的结构简式是 。
①含有3个双键 ②核磁共振氢谱只显示1个吸收峰 ③不存在甲基
(4)乙烯在实验室可由 (填有机物名称)通过 (填反应类
型)制备。
(5)下列说法正确的是 。
a. A 属于饱和烃 b . D与乙醛的分子式相同 c.E不能与盐酸反应 d . F可
以发生酯化反应27.(13分)二氧化铈(CeO)是一种重要的稀土氧化物。平板电视显示屏生
2
产过程中产生大量的废玻璃粉末(含 SiO 、Fe O 、CeO 以及其他少量可溶于稀酸的物
2 2 3 2
质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
(1)洗涤滤渣A的目的是为了除去 (填离子符号),检验该离子是否洗涤的
方法是
。
(2)第②步反应的离子方程式是 ,滤渣B的主要成分
是 。
(3)萃取是分离稀土元素的常用方法。已知化合物TBP作为萃取剂能将铈离子从水溶液
中萃取出来,TBP
(填“能”或“不能”)与水互溶。实验室进行萃取操作是用到的主要玻璃仪器
有 、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的Ce(OH) 产品0.536g,加硫酸溶解后,用0.1000mol•L-1FeSO 标
4 4
准溶液滴定至终点时(铈被还原为Ce3+),消耗25.00mL标准溶液,该产品中Ce(OH) 的质量
4
分数为 。28.(14分)某酸性工业废水中含有KCr O 。光照下,草酸(H C O)能将其中的Cr O2—转
2 2 7 2 2 4 2 7
化为Cr3+。某课题组研究发现,少量铁明矾[AlFe(SO )•24HO]即可对该反应堆起催化作用。
2 4 4 2
为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始
pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
实验编号 初始pH 废水样品体积/mL 草酸溶液体积/mL 蒸馏水体积/mL
① 4 60 10 30
② 5 60 10 30
③ 5 60
测得实验①和②溶液中的Cr O2—浓度随时间变化关系如图所示。
2 7
(2)上述反应后草酸被氧化为 (填化学式)。
(3)实验①和②的结果表明 ;
实验①中0~t 时间段反应速率 (Cr3+)= mol•L-1•min-1(用代数式表示)。
1
(4)该课题组对铁明矾[AlFe(SO )•24HO]中起催化作用的成分提出如下假设,请你完成
2 4 4 2
假设二和假设三:
假设一:Fe2+起催化作用;
假设二: ;
假设三: ;
…………
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可
供选择的药品有KSO 、FeSO 、KSO •Al (SO )•24HO、Al (SO ) 等。溶液中Cr O2—的
2 4 4 2 4 2 4 3 2 2 4 3 2 7
浓度可用仪器测定)
实验方案(不要求写具体操作过程) 预期实验结果和结论2013年普通高等学校招生全国统一考试(安徽卷)
理科综合能力测试【参考答案】
第I卷共20小题,每小题6分,共120分。
1.A 2.B 3.D 4.C 5.B 6.D 7.C 8.B 9.A 10.D
11.A 12.D 13.C 14.A 15.B 16.B 17.C 18.A 19.C 20.D
第II卷共11题,共180分。
25.(15分)
(1)三 IVA 大
(2)小 分子间作用力 乙酸(合理均可)
(3)先生成白色沉淀,后沉淀逐渐溶解,最后变成无色溶液
Si+4HF=SiF ↑+2H ↑
4 2
(4)4Al(s)+3O (g)=2Al O(s) ΔH=—3352kJ/mol(合理即可)
2 2 3
26.(16分)
(1)HOOC(CH )COOH 氨基、羧基
2 4
(2)CHOOC(CH )COOCH +2H NCH CHOH→
3 2 4 3 2 2 2
2CHOH+HOCH CHNHOC(CH )CONHCH CHOH
3 2 2 2 4 2 2
CH
2
CH
CH 2
2
(3)
(4)乙醇 消去反应合理即可)
(5)a、b、d
27.(13分)
(1)Fe3+ 取最后一次洗涤液,加入KSCN溶液,如果不出现红色,则已洗净;反之,未
洗净。(合理即可)
(2)2CeO+H O+6H+=2Ce3++O ↑+4H O SiO(合理即可)
2 2 2 2 2 2
(3)不能 分液漏斗
(4)97.0%
28.(14分)
(1)
实验编号 初始pH 废水样品体积/mL 草酸溶液体积/mL 蒸馏水体积/mL
③ 20 20
(2)CO
2
(3)溶液pH对该反应的速率有影响
(4)Al3+起催化作用 SO 2—起催化作用
4
(5)
实验方案(不要求写具体操作过程) 预期实验结果和结论用等物质的量的 KSO •Al (SO )•24HO 代 反应进行相同时间后,若溶液中 c(Cr O2—)
2 4 2 4 3 2 2 7
替实验①中的铁明矾,控制其他反应条件与 大于实验①中的 c(Cr O2—),则假设一成
2 7
实验①相同,进行对比实验 立;若两溶液中的c(Cr O2—)相同,则假设
2 7
一不成立。
(本题属于开放性试题)