文档内容
江苏省 2022 年普通高中学业水平选择性考试
化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56
Cu 64 Ce 140
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 我国为人类科技发展作出巨大贡献。下列成果研究的物质属于蛋白质的是
A. 陶瓷烧制 B. 黑火药 C. 造纸术 D. 合成结晶牛胰岛素
【答案】D
【解析】
【详解】A.陶瓷的主要成分是硅酸盐,陶瓷烧制研究的物质是硅的化合物,A不符合题意;
B.黑火药研究的物质是硫、碳和硝酸钾,B不符合题意;
C.造纸术研究的物质是纤维素,C不符合题意;
D.胰岛素的主要成分是蛋白质,故合成结晶牛胰岛素研究的物质是蛋白质,D符合题意;
答案选D。
2. 少量 与 反应生成 和 。下列说法正确的是
A. 的电子式为 B. 的空间构型为直线形
C. 中O元素的化合价为-1 D. 仅含离子键
【答案】AC
【解析】
【详解】A.过氧化钠是离子化合物,电子式是 ,A正确;
B. 中氧原子的成键电子对是2,孤电子对是2,根据价层电子对为4,根据价层电子对互斥理论,其
空间构型为V形,B错误;
C. 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,C正确;
D. 中O和H之间是共价键,D错误;
故选AC。3. 工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是
A. 半径大小: B. 电负性大小:
C. 电离能大小: D. 碱性强弱:
【答案】A
【解析】
【详解】A.核外电子数相同时,核电荷数越大半径越小,故半径大小为 ,故A正确;
B.同周期元素核电荷数越大电负性越大,故 ,故B错误;
C.同周期从左往右第一电离能呈增大趋势,同主族从上往下第一电离能呈减小趋势,故电离能大小为
,故C错误;
D.元素金属性越强,其最高价氧化物对应水化物的碱性越强,故碱性强弱为 ,故D错
误;
故选A 。
4. 实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验目的的是
A. 用装置甲制取 气体 B. 用装置乙制取 水溶液
C. 用装置丙吸收尾气中的 D. 用干燥pH试纸检验 水溶液的酸性
【答案】C
【解析】
【详解】A.60%硫酸和NaHSO3(s)可发生反应:HSO +2NaHSO =Na SO +2SO↑+2H O,因此装置甲可
2 4 3 2 4 2 2以制取 气体,A正确;
B.气体通入液体时“长进短处”,装置乙可以制取 水溶液,B正确;
C.SO 不会与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的 ,C错误;
2 3
D. 水溶液显酸性,可用干燥的pH试纸检验其酸性,D正确;
答案选C。
5. 下列说法正确的是
A. 金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C. 锗原子( )基态核外电子排布式为
D. ⅣA族元素单质的晶体类型相同
【答案】B
【解析】
【详解】A.金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误;
B. 的化学键为Si-H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键
为Si-Cl,为极性键,为正四面体,正负电荷中心重合,为非极性分子,故B正确;
C.锗原子( )基态核外电子排布式为[Ar] ,故C错误;
D.ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为原子晶体,故D错误;
故选B。
6. 周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热 ,是常见燃料;
Si、Ge是重要的半导体材料,硅晶体表面 能与氢氟酸(HF,弱酸)反应生成 ( 在水中完
全电离为 和 );1885年德国化学家将硫化锗 与 共热制得了门捷列夫预言的类硅—锗;
下列化学反应表示正确的是A. 与HF溶液反应:
B. 高温下 还原 :
C. 铅蓄电池放电时的正极反应:
D. 甲烷的燃烧:
【答案】A
【解析】
【详解】A.由题意可知,二氧化硅与氢氟酸溶液反应生成强酸 和水,反应的离子方程式为
,故A正确;
B.硫化锗与氢气共热反应时,氢气与硫化锗反应生成锗和硫化氢,硫化氢高温下分解生成硫和氢气,则
反应的总方程式为 ,故B错误;
C.铅蓄电池放电时,二氧化铅为正极,酸性条件下在硫酸根离子作用下二氧化铅得到电子发生还原反应
生成硫酸铅和水,电极反应式为正极反应 ,故C错误;
D.由题意可知,1mol甲烷完全燃烧生成二氧化碳和液态水放出热量为890.3kJ,反应的热化学方程式为
,故D错误;
故选A。
7. 我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜器;Pb、 是铅蓄电
池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料,下列物质性质与用途具有对应
关系的是
A. 石墨能导电,可用作润滑剂
B. 单晶硅熔点高,可用作半导体材料
C. 青铜比纯铜熔点低、硬度大,古代用青铜铸剑
D. 含铅化合物颜色丰富,可用作电极材料【答案】C
【解析】
【详解】A.石墨是过渡型晶体,质软,可用作润滑剂,故A错误
B.单晶硅可用作半导体材料与空穴可传递电子有关,与熔点高无关,故B错误;
C.青铜是铜合金,比纯铜熔点低、硬度大,易于锻造,古代用青铜铸剑,故C正确;
D.含铅化合物可在正极得到电子发生还原反应,所以可用作电极材料,与含铅化合物颜色丰富无关,故
D错误;
故选C。
8. 氮及其化合物的转化具有重要应用。下列说法不正确的是
A. 自然固氮、人工固氮都是将 转化为
B. 侯氏制碱法以 、 、 、 为原料制备 和
C. 工业上通过 催化氧化等反应过程生产
的
D. 多种形态 氮及其化合物间的转化形成了自然界的“氮循环”
【答案】A
【解析】
【详解】A.自然固氮是将N 转化为含氮化合物,不一定是转化为NH ,比如大气固氮是将N 会转化为
2 3 2
NO,A错误;
B.侯氏制碱法以HO、NH 、CO、NaCl为原料制备NaHCO 和NH Cl,反应的化学方程式为
2 3 2 3 4
HO+NH +CO +NaCl=NaHCO ↓+NHCl,B正确;
2 3 2 3 4
C.工业上通过NH 催化氧化等反应过程生产HNO,相关的化学反应方程式为4NH +5O
3 3 3 2
4NO+6H O、2NO+O =2NO、3NO +H O=2HNO +NO、4NO +O +2H O=4HNO ,C正确;
2 2 2 2 2 3 2 2 2 3
D.氮元素在自然界中既有游离态又有化合态,多种形态的氮及其化合物间的转化形成了自然界的“氮循
环”,D正确;
故选A。
9. 精细化学品Z是X与 反应的主产物,X→Z的反应机理如下:下列说法不正确的是
A. X与 互为顺反异构体
B. X能使溴的 溶液褪色
C. X与HBr 反应有副产物生成
D. Z分子中含有2个手性碳原子
【答案】D
【解析】
【详解】A.X与 互为顺反异构体,故A正确;
B.X中含有碳碳双键,故能使溴的 溶液褪色,故B正确;
C.X中的碳碳双键可以和HBr发生加成反应生成 ,故C正确;
D.Z分子中含有的手性碳原子如图: ,含有1个手性碳原子,故D错误;
故选D。
10. 用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是A. 上述反应
B. 上述反应平衡常数
C. 上述反应中消耗 ,转移电子的数目为
D. 实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】
【详解】A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,故A错
误;
B.由方程式可知,反应平衡常数 ,故B正确;
C.由方程式可知,反应每消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数
目为3mol×4× ×6.02×1023=3×6.02×1023,故C错误;
D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴油机车辆排放的氨气对空气污染程度
增大,故D错误;
故选B。
11. 室温下,下列实验探究方案不能达到探究目的的是
选
探究方案 探究目的
项
向盛有 溶液的试管中滴加几滴 溶液,振荡,
A 具有还原性
再滴加几滴新制氯水,观察溶液颜色变化
向盛有 水溶液的试管中滴加几滴品红溶液,振荡,加
B 具有漂白性
热试管,观察溶液颜色变化
向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶 的氧化性比
C
液颜色变化
的强
是弱
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小
电解质A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.向盛有 溶液的试管中滴加几滴 溶液,无现象,振荡,再滴加几滴新制氯水,
溶液变为红色,亚铁离子被新制氯水氧化,说明 具有还原性,A正确;
B.向盛有 水溶液的试管中滴加几滴品红溶液,品红溶液褪色,振荡,加热试管,溶液又恢复红色,
说明 具有漂白性, B正确;
C.向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,溶液变为蓝色,说明 的氧化性比 的强,C正
确;
D.用pH计测量醋酸、盐酸的pH用以证明 是弱电解质时,一定要注明醋酸和盐酸的物质的
量浓度相同,D错误。
故选D。
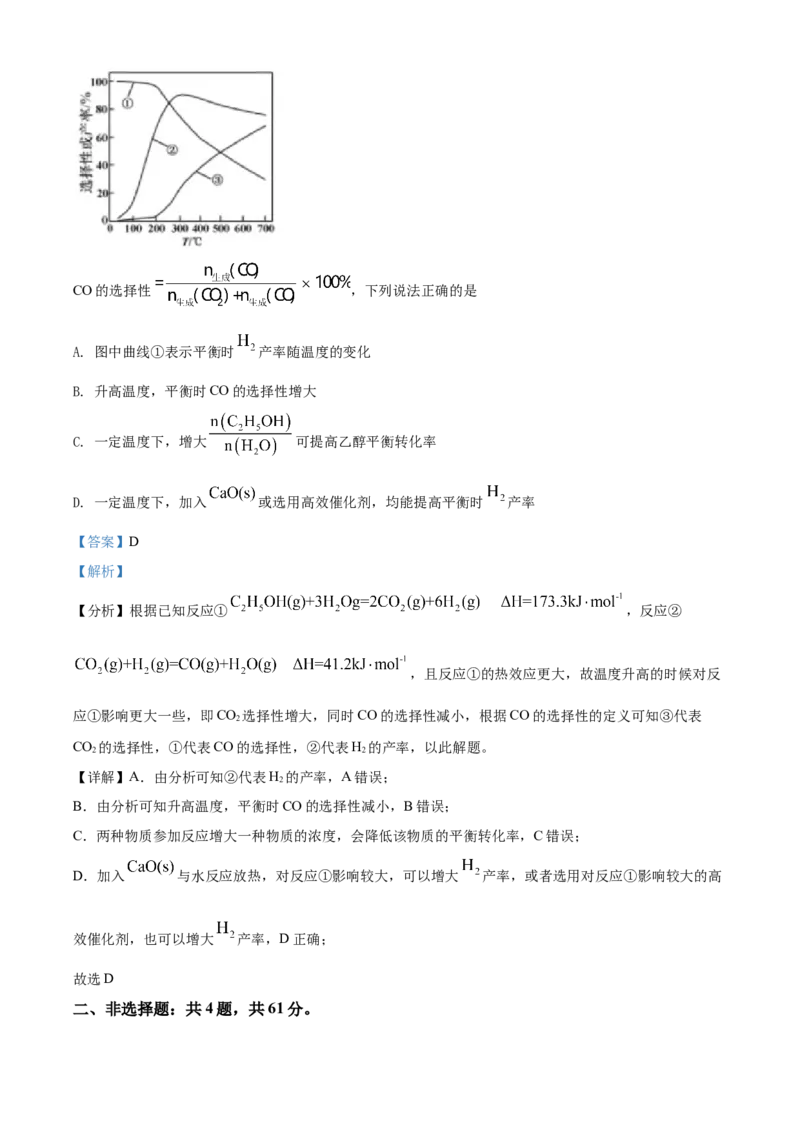
12. 一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通入CO 所引起的溶
2 2 2
液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c( )+c( )。HCO 电离常
2 总 2 3 2 3
数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
a1 a2
A. KOH吸收CO 所得到的溶液中:c(H CO)>c( )
2 2 3
B. KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C. KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3D. 如图所示的“吸收”“转化”过程中,溶液的温度下降
【答案】C
【解析】
【详解】A.KOH吸收CO 所得到的溶液,若为NaCO 溶液,则 主要发生第一步水解,溶液中:
2 2 3
c(H CO)<c( ),若为NaHCO 溶液,则 发生水解的程度很小,溶液中:c(H CO)<c(
2 3 3 2 3
),A不正确;
B.KOH完全转化为KCO 时,依据电荷守恒,溶液中:c(K+)+ c(H+)=c(OH-)+ +c( )+2c( ),依
2 3
据物料守恒,溶液中:c(K+)=2[c( )+c( )+c(H CO)],则c(OH-)= c(H+)+c( )+2c(H CO),B
2 3 2 3
不正确;
C.KOH溶液吸收CO,c(KOH)=0.1mol∙L-1,c =0.1mol∙L-1,则溶液为KHCO 溶液, K = =
2 总 3 h2
2.3×10-8>K =4.4×10-11,表明 以水解为主,所以溶液中:c(H CO)>c( ),C正确;
a2 2 3
≈
D.如图所示的“吸收”“转化”过程中,发生反应为:CO+2KOH=K CO+H O、
2 2 3 2
KCO+CaO+H O=CaCO ↓+2KOH(若生成KHCO 或KCO 与KHCO 的混合物,则原理相同),二式相加得:
2 3 2 3 3 2 3 3
CO+CaO=CaCO ↓,该反应放热,溶液的温度升高,D不正确;
2 3
故选C。
13. 乙醇-水催化重整可获得 。其主要反应为
,
,在 、
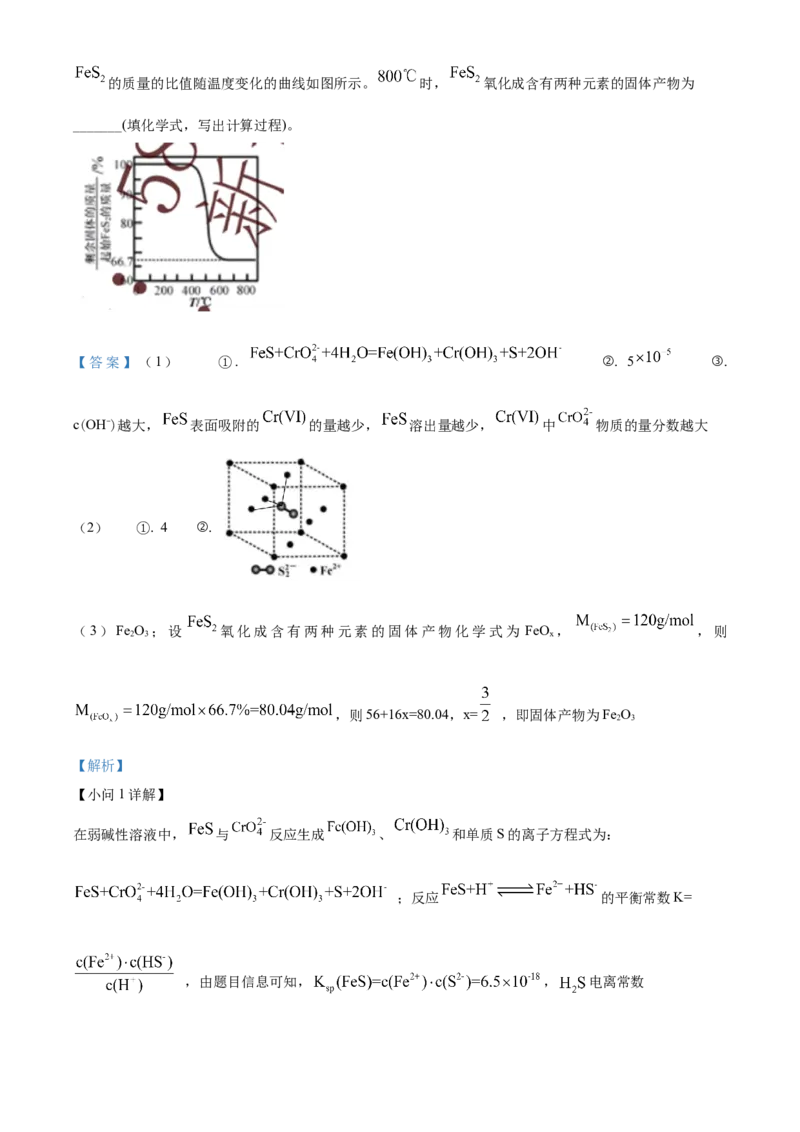
时,若仅考虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。CO的选择性 ,下列说法正确的是
A. 图中曲线①表示平衡时 产率随温度的变化
B. 升高温度,平衡时CO的选择性增大
C. 一定温度下,增大 可提高乙醇平衡转化率
D. 一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】D
【解析】
【分析】根据已知反应① ,反应②
,且反应①的热效应更大,故温度升高的时候对反
应①影响更大一些,即CO 选择性增大,同时CO的选择性减小,根据CO的选择性的定义可知③代表
2
CO 的选择性,①代表CO的选择性,②代表H 的产率,以此解题。
2 2
【详解】A.由分析可知②代表H 的产率,A错误;
2
B.由分析可知升高温度,平衡时CO的选择性减小,B错误;
C.两种物质参加反应增大一种物质的浓度,会降低该物质的平衡转化率,C错误;
D.加入 与水反应放热,对反应①影响较大,可以增大 产率,或者选用对反应①影响较大的高
效催化剂,也可以增大 产率,D正确;
故选D 。
二、非选择题:共4题,共61分。14. 硫铁化合物( 、 等)应用广泛。
(1)纳米 可去除水中微量六价铬 。在 的水溶液中,纳米 颗粒表面带正电荷,
主要以 、 、 好形式存在,纳米 去除水中 主要经过“吸附→反应→
沉淀”的过程。
已知: , ; 电离常数分别为 、
。
①在弱碱性溶液中, 与 反应生成 、 和单质S,其离子方程式为_______。
②在弱酸性溶液中,反应 的平衡常数K的数值为_______。
③在 溶液中,pH越大, 去除水中 的速率越慢,原因是_______。
(2) 具有良好半导体性能。 的一种晶体与 晶体的结构相似,该 晶体的一个晶胞中
的数目为_______,在 晶体中,每个S原子与三个 紧邻,且 间距相等,如图给出了
晶胞中的 和位于晶胞体心的 ( 中的 键位于晶胞体对角线上,晶胞中的其他 已省略)。
如图中用“-”将其中一个S原子与紧邻的 连接起来_______。
的
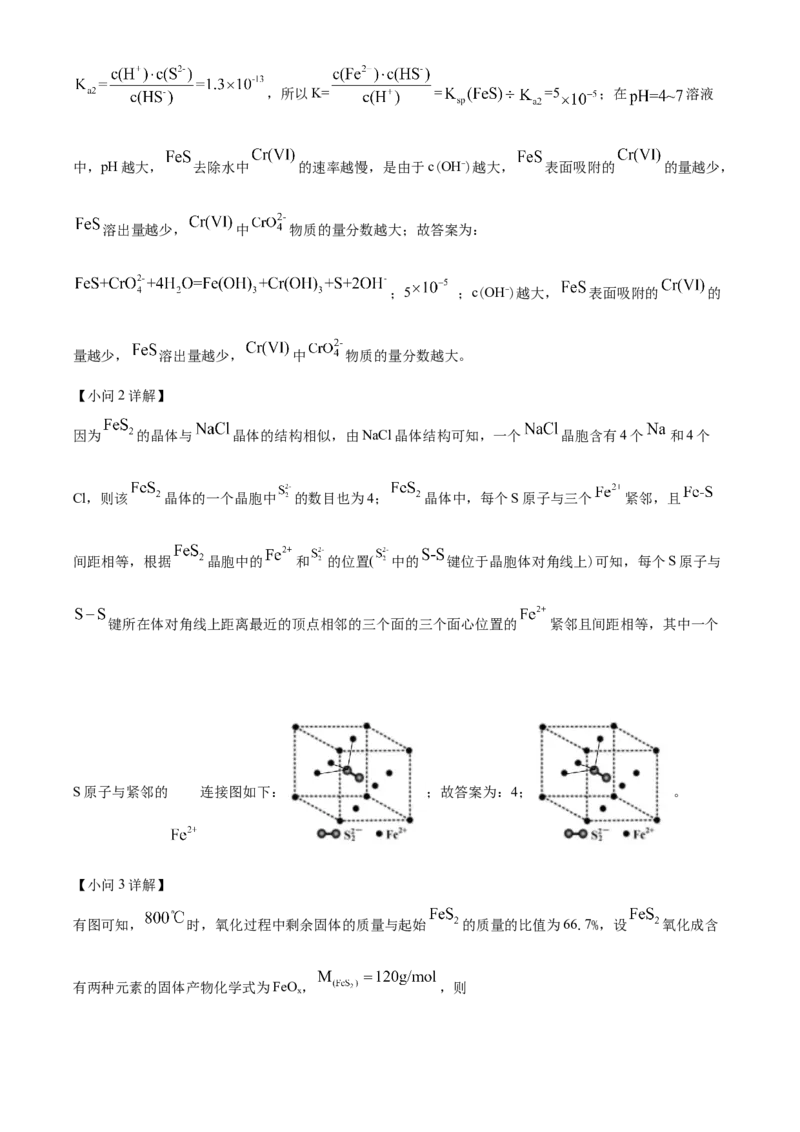
(3) 、 在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体 质量与起始的质量的比值随温度变化的曲线如图所示。 时, 氧化成含有两种元素的固体产物为
_______(填化学式,写出计算过程)。
【答案】(1) ①. ②. 5 ③.
c(OH-)越大, 表面吸附的 的量越少, 溶出量越少, 中 物质的量分数越大
(2) ①. 4 ②.
(3)Fe O ;设 氧化成含有两种元素的固体产物化学式为 FeO , ,则
2 3 x
,则56+16x=80.04,x= ,即固体产物为Fe O
2 3
【解析】
【小问1详解】
在弱碱性溶液中, 与 反应生成 、 和单质S的离子方程式为:
;反应 的平衡常数K=
,由题目信息可知, , 电离常数,所以K= = =5 ;在 溶液
中,pH越大, 去除水中 的速率越慢,是由于c(OH-)越大, 表面吸附的 的量越少,
溶出量越少, 中 物质的量分数越大;故答案为:
;5 ;c(OH-)越大, 表面吸附的 的
量越少, 溶出量越少, 中 物质的量分数越大。
【小问2详解】
因为 的晶体与 晶体的结构相似,由NaCl晶体结构可知,一个 晶胞含有4个 和4个
Cl,则该 晶体的一个晶胞中 的数目也为4; 晶体中,每个S原子与三个 紧邻,且
间距相等,根据 晶胞中的 和 的位置( 中的 键位于晶胞体对角线上)可知,每个S原子与
键所在体对角线上距离最近的顶点相邻的三个面的三个面心位置的 紧邻且间距相等,其中一个
S原子与紧邻的 连接图如下: ;故答案为:4; 。
【小问3详解】
有图可知, 时,氧化过程中剩余固体的质量与起始 的质量的比值为66.7%,设 氧化成含
有两种元素的固体产物化学式为FeO, ,则
x,56+16x=80.04,x= ,所以固体产物为Fe O;故答案为:
2 3
Fe O;设 氧化成含有两种元素的固体产物化学式为FeO, ,则
2 3 x
,则56+16x=80.04,x= ,即固体产物为Fe O。
2 3
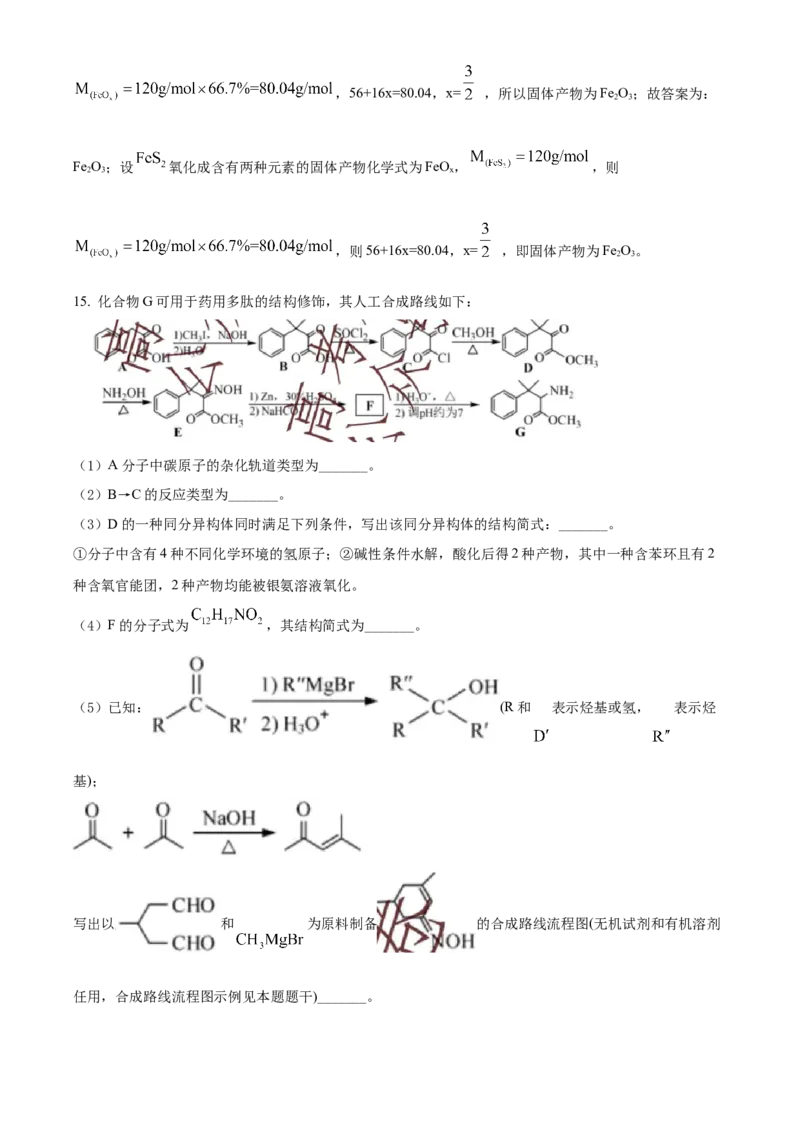
15. 化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)A分子中碳原子的杂化轨道类型为_______。
(2)B→C的反应类型为_______。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种含苯环且有2
种含氧官能团,2种产物均能被银氨溶液氧化。
(4)F的分子式为 ,其结构简式为_______。
(5)已知: (R和 表示烃基或氢, 表示烃
基);
写出以 和 为原料制备 的合成路线流程图(无机试剂和有机溶剂
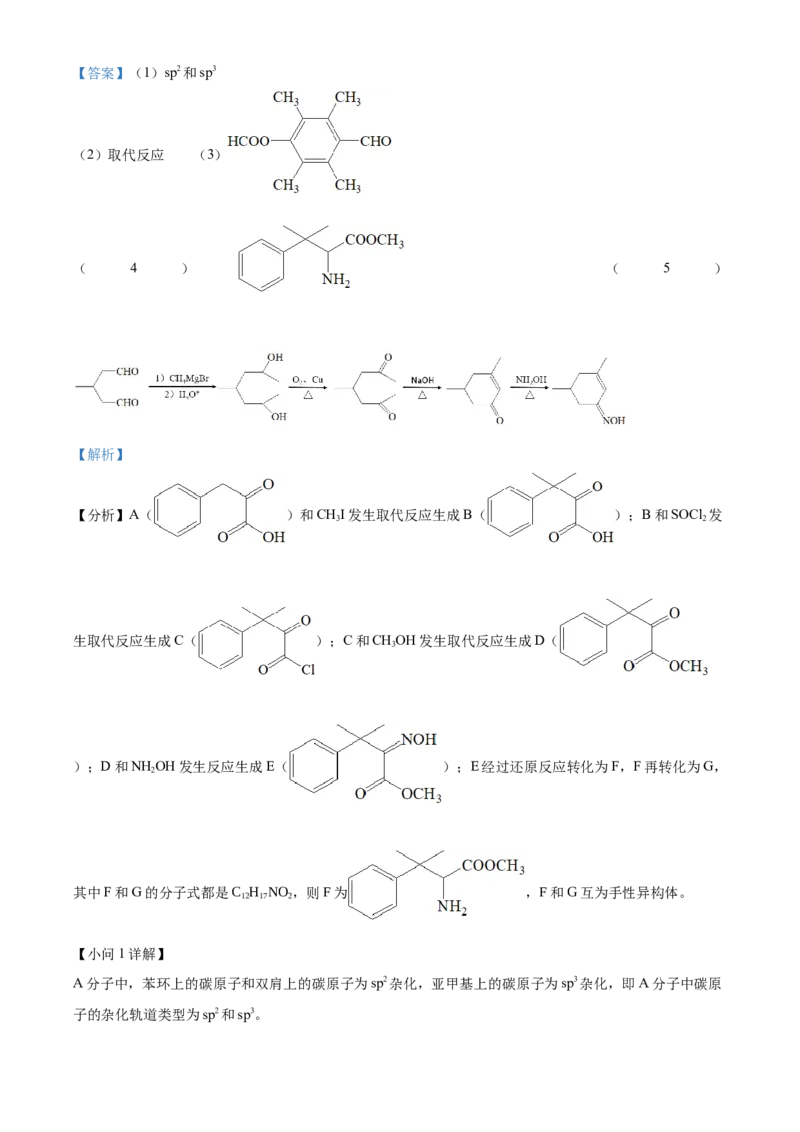
任用,合成路线流程图示例见本题题干)_______。【答案】(1)sp2和sp3
(2)取代反应 (3)
( 4 ) ( 5 )
【解析】
【分析】A( )和CHI发生取代反应生成B( );B和SOCl 发
3 2
生取代反应生成C( );C和CHOH发生取代反应生成D(
3
);D和NH OH发生反应生成E( );E经过还原反应转化为F,F再转化为G,
2
其中F和G的分子式都是C H NO ,则F为 ,F和G互为手性异构体。
12 17 2
【小问1详解】
A分子中,苯环上的碳原子和双肩上的碳原子为sp2杂化,亚甲基上的碳原子为sp3杂化,即A分子中碳原
子的杂化轨道类型为sp2和sp3。【小问2详解】
B→C的反应中,B中的羟基被氯原子代替,该反应为取代反应。
【小问3详解】
D的分子式为C H O,其一种同分异构体在碱性条件水解,酸化后得2种产物,其中一种含苯环且有2
12 14 3
种含氧官能团,2种产物均能被银氨溶液氧化,说明该同分异构体为酯,且水解产物都含有醛基,则水解
产物中,有一种是甲酸,另外一种含有羟基和醛基,该同分异构体属于甲酸酯;同时,该同分异构体分子
中含有4种不同化学环境的氢原子,则该同分异构体的结构简式为 。
【小问4详解】
由分析可知,F的结构简式为 。
【小问5详解】
根据已知的第一个反应可知, 与CHMgBr反应生成 , 再被氧
3
化为 ,根据已知的第二个反应可知, 可以转化为 ,根据流程图中D→E的反应可知, 和NH OH反应生成 ;综上所述,
2
的合成路线为:
。
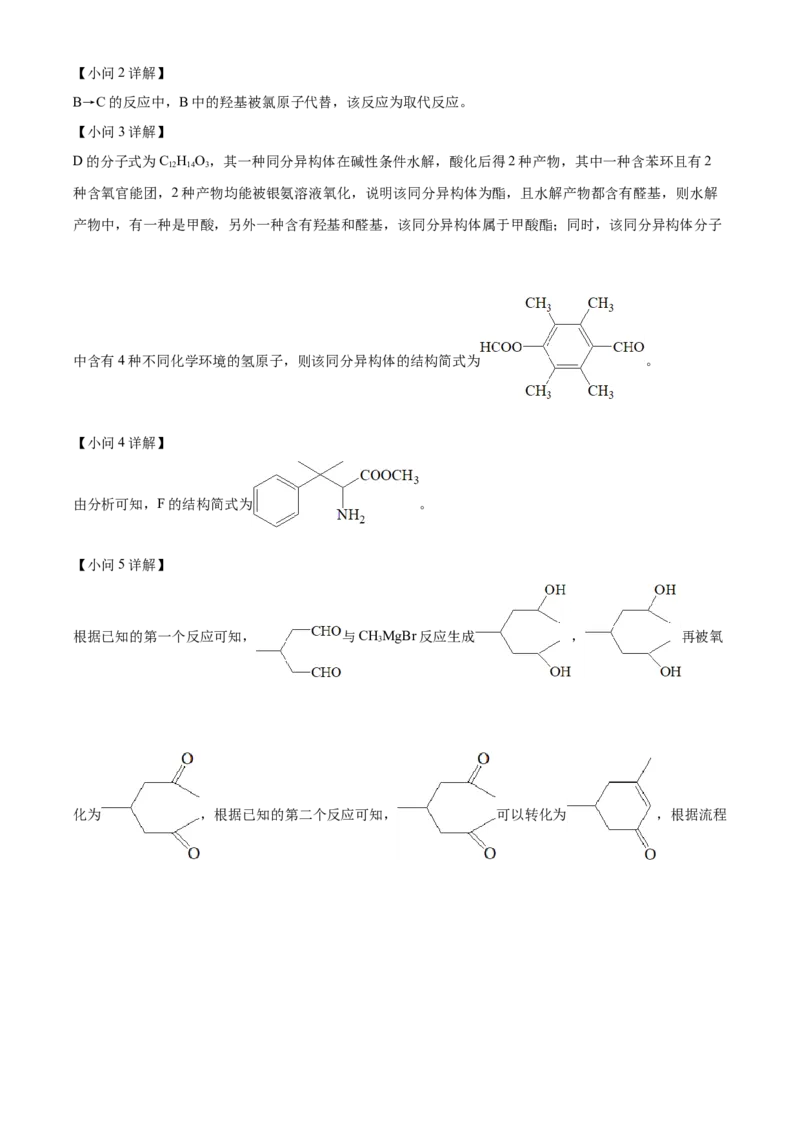
16. 实验室以二氧化铈( )废渣为原料制备 含量少的 ,其部分实验过程如下:
(1)“酸浸”时 与 反应生成 并放出 ,该反应的离子方程式为_______。
(2)pH约为7的 溶液与 溶液反应可生成 沉淀,该沉淀中 含量与加料方
式有关。得到含 量较少的 的加料方式为_______(填序号)。
A.将 溶液滴加到 溶液中 B.将 溶液滴加到 溶液中
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的 。已知 能被有机萃取
剂(简称HA)萃取,其萃取原理可表示为
(水层)+3HA(有机层) (有机层)+ (水层)
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______。
②反萃取的目的是将有机层 转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有_______(填两项)。
③与“反萃取”得到的水溶液比较,过滤 溶液的滤液中,物质的量减小的离子有_______(填化学
式)。
(4)实验中需要测定溶液中 的含量。已知水溶液中 可用准确浓度的 溶液滴
定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
。请补充完整实验方案:①准确量取 溶液[ 约为
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
容量瓶中后定容;②按规定操作分别将 和待测 溶液装入
如图所示的滴定管中:③_______。
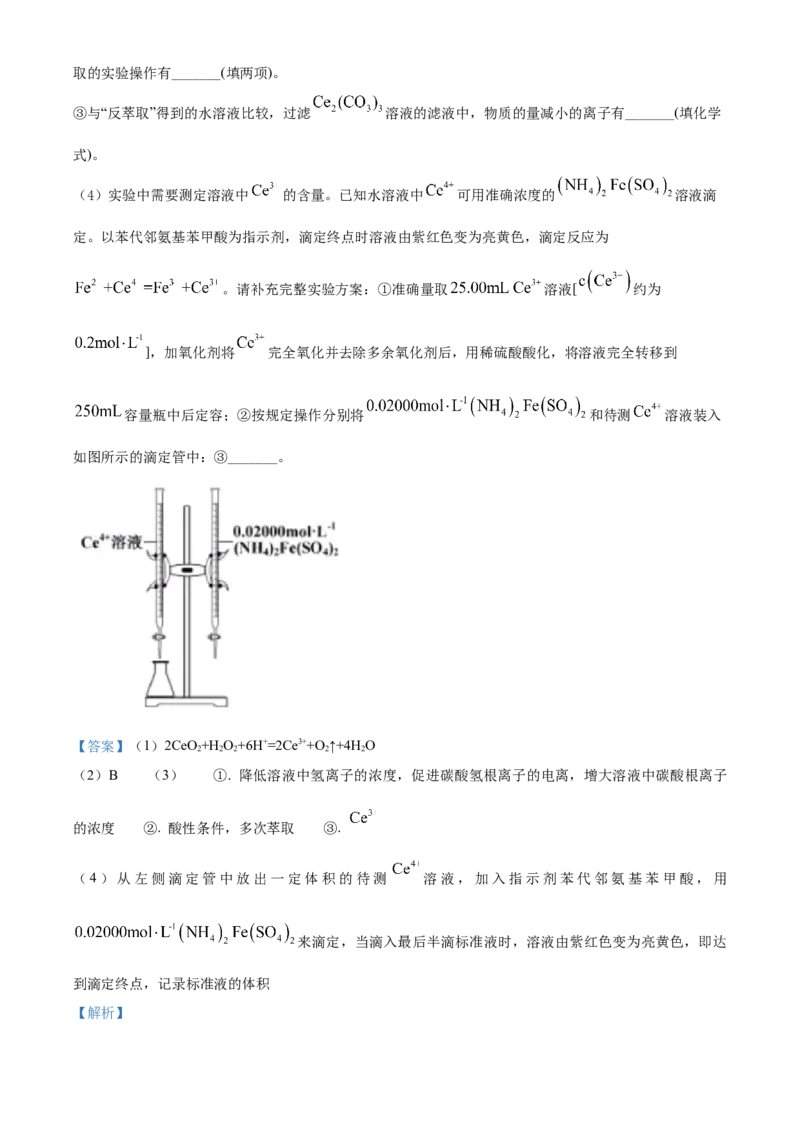
【答案】(1)2CeO+H O+6H+=2Ce3++O ↑+4H O
2 2 2 2 2
(2)B (3) ①. 降低溶液中氢离子的浓度,促进碳酸氢根离子的电离,增大溶液中碳酸根离子
的浓度 ②. 酸性条件,多次萃取 ③.
(4)从左侧滴定管中放出一定体积的待测 溶液,加入指示剂苯代邻氨基苯甲酸,用
来滴定,当滴入最后半滴标准液时,溶液由紫红色变为亮黄色,即达
到滴定终点,记录标准液的体积
【解析】【分析】首先用稀盐酸和过氧化氢溶液酸浸二氧化铈废渣,得到三价铈,加入氨水调节pH后用萃取剂萃
取其中的三价铈,增大三价铈浓度,之后加入稀硝酸反萃取其中的三价铈,再加入氨水和碳酸氢铵制备产
物,以此解题。
【小问1详解】
根据信息反应物为 与 ,产物为 和 ,根据电荷守恒和元素守恒可知其离子方程式为:
2CeO+H O+6H+=2Ce3++O ↑+4H O;
2 2 2 2 2
【小问2详解】
反应过程中保持 少量即可得到含 量较少的 ,故选B;
【小问3详解】
①增大碳酸根离子的浓度有助于生成产物,故答案为:降低溶液中氢离子的浓度,促进碳酸氢根离子的电
离,增大溶液中碳酸根离子的浓度;
②根据萃取原理可知,应选择的实验条件是酸性条件,为了使 尽可能多地发生上述转移,可以采用多
次萃取;
③“反萃取”得到的水溶液中含有浓度较大的 ,过滤后溶液中 离子浓度较小,故答案为: ;
【
小问4详解】
应该用标准液滴定待测 溶液,用苯代邻氨基苯甲酸作指示剂,故答案为:从左侧滴定管中放出一定体
积的待测 溶液,加入指示剂苯代邻氨基苯甲酸,用 来滴定,当滴
入最后半滴标准液时,溶液由紫红色变为亮黄色,即达到滴定终点,记录标准液的体积。
17. 氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。
(1)“ 热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图所示。
①电解在质子交换膜电解池中进行。阳极区为酸性 溶液,阴极区为盐酸,电解过程中 转化为。电解时阳极发生的主要电极反应为_______(用电极反应式表示)。
②电解后,经热水解和热分解的物质可循环使用。在热水解和热分解过程中,发生化合价变化的元素有
_______(填元素符号)。
(2)“ 热循环制氢和甲酸”的原理为:在密闭容器中,铁粉与吸收 制得的 溶
液反应,生成 、 和 ; 再经生物柴油副产品转化为Fe。
①实验中发现,在 时,密闭容器中 溶液与铁粉反应,反应初期有 生成并放出 ,
该反应的离子方程式为_______。
②随着反应进行, 迅速转化为活性 ,活性 是 转化为 的催化剂,其
可能反应机理如图所示。根据元素电负性的变化规律。如图所示的反应步骤Ⅰ可描述为_______。
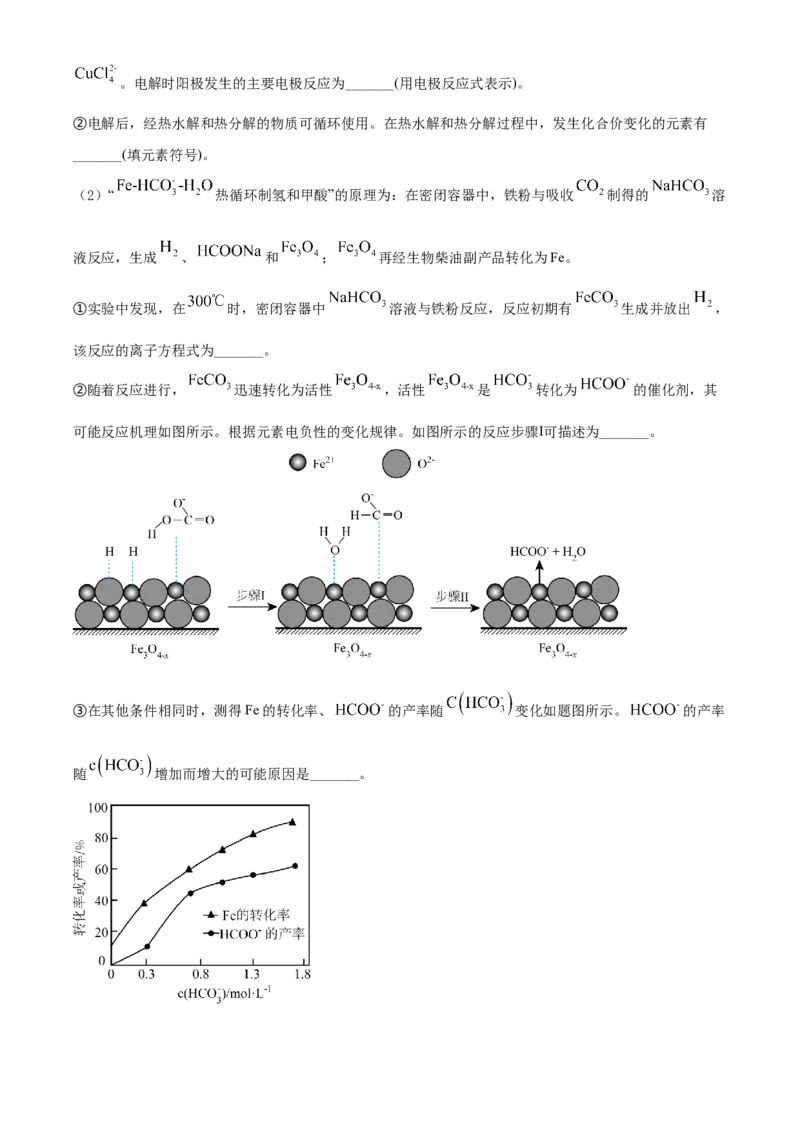
③在其他条件相同时,测得Fe的转化率、 的产率随 变化如题图所示。 的产率
随 增加而增大的可能原因是_______。(3)从物质转化与资源综合利用角度分析,“ 热循环制氢和甲酸”的优点是_______。
【答案】(1) ①. ②. Cu、O
(2) ①. ②. H的电负性大于Fe,小于O,在活性
表面,H 断裂为H原子,一个吸附在催化剂的铁离子上,略带负电,一个吸附在催化剂的氧离子
2
上,略带正电,前者与 中略带正电的碳结合,后者与 中略带负电的羟基氧结合生成HO,
2
转化为 ③. 随 增加,生成 和 H 的速率更快、产量增大,生成
2
的速率更快、产率也增大
(3)高效、经济、原子利用率高、无污染
【解析】
【小问1详解】
①电解在质子交换膜电解池中进行,H+可自由通过,阳极区为酸性 溶液,电解过程中 转化为
,电解时阳极发生的主要电极反应为: ;
②电解后,经热水解得到的HCl和热分解得到的CuCl等物质可循环使用,从图中可知,热分解产物还有
O,从详解①中得知,进入热水解的物质有 ,故发生化合价变化的元素有Cu、O。
2
【小问2详解】
①在 时,密闭容器中 溶液与铁粉反应,反应初期有 生成并放出 ,离子方程式
为: ;
②H的电负性大于Fe,小于O,在活性 表面,H 断裂为H原子,一个吸附在催化剂的铁离子上,
2略带负电,一个吸附在催化剂的氧离子上,略带正电,前者与 中略带正电的碳结合,后者与
中略带负电的羟基氧结合生成HO, 转化为 ;
2
③在其他条件相同时,随 增加,其与铁粉反应加快,从图中得知Fe的转化率也增大,即生成
和H 的速率更快,量更大,则得到活性 的速度更快,量也更多,生成 的速率更快,
2
产率也更大。
【小问3详解】
“ 热循环制氢和甲酸”系统将 转化为 和生成H 的速率快,原子利用率高,不
2
产生污染物,Fe初期生成 后迅速转化为活性 , 氧化为 再经生物柴油副产品
转化为Fe,得到循环利用,故该原理的优点是:高效、经济、原子利用率高、无污染。