文档内容
房山区 2020-2021 学年度第一学期期中检测试卷
九 年 级 化 学
考试须知:
1.本试卷共8页,共35道小题,满分70分。考试时间70分钟。
2.在试卷和答题卡上准确填写学校名称、姓名和考号。
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔作答
可能用到的相对原子质量:H 1 C 12 O 16 Ca 40
第一部分 选择题(共20分)
(每小题只有1个选项符合题意。每小题1分)
1. 下列做法中,不符合“节约用水,防治水污染”主张的是
A. 用洗菜水冲厕所 B. 城市生活污水任意排放
C. 推广使用节水器具 D. 农业上合理使用化肥农药
2. 地壳中含量最多的元素是( )
A. 硅 B. 氧 C. 铁 D. 铝
3. 下列元素符号书写正确的是
A. 钠NA B. 镁mg C. 氮Ne D. 铁Fe
4. 下列微粒数,能决定元素种类的是
.
A 电子数 B. 中子数 C. 质子数 D. 电子层数
5. 科学家发现月球土壤中含有较丰富的氦(He-3),其原子核内质子数为2,中子数为1,则氦原子的核
外电子数为( )
A. 1 B. 2 C. 3 D. 4
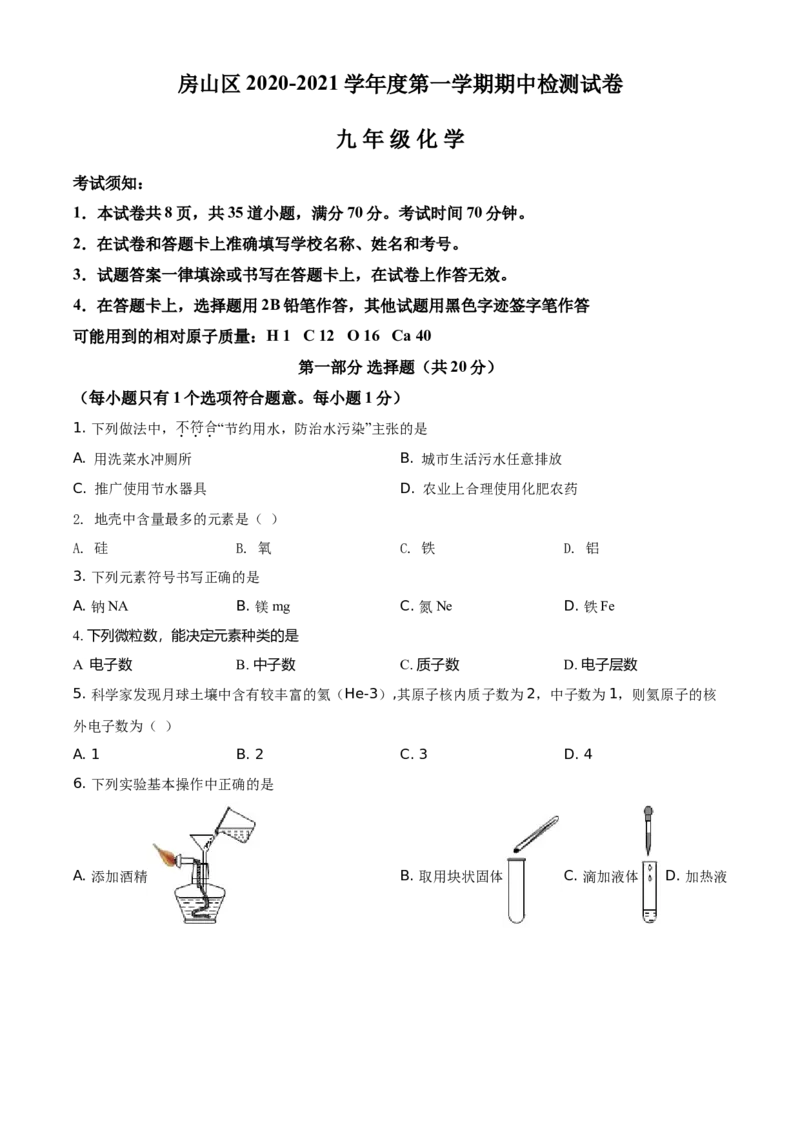
6. 下列实验基本操作中正确的是
A. 添加酒精 B. 取用块状固体 C. 滴加液体 D. 加热液体
7. 加碘盐中的“碘”指的是
A. 碘单质 B. 碘原子 C. 碘分子 D. 碘元素
8. 量取一定体积的水时需要用
A. 试管 B. 烧杯 C. 量筒 D. 托盘天平
9. 下列物质由分子构成的是
A. 氮气 B. 铁 C. 汞 D. 氯化钠
10. 下列符号表示2个氧分子的是
A. 2O B. 2O C. 2O2- D. O
2 2
11. 生活中软化硬水的常用方法为
A. 沉淀 B. 吸附 C. 煮沸 D. 搅拌
12. 在压强和温度保持不变的条件下,18mL的液态水完全蒸发成水蒸气后,体积扩大了约1700倍。这是
由于
A. 分子体积变大 B. 分子停止运动
C. 分子数目增多 D. 分子间空隙变大
13. 下列物质的性质中,属于化学性质的是
A. 氧气无色无味 B. 酒精易燃烧
C. 蔗糖易溶于水 D. 冰的密度比水的小
14. 下列物质中,属于氧化物的是
A. 氧气(O) B. 水(HO)
2 2
C. 甲烷(CH) D. 高锰酸钾(KMnO )
4 4
15. 医用双氧水的有效成分是过氧化氢,其化学式为HO,该化学式可获得的信息中正确的是
2 2
A. 过氧化氢由氢元素和氧元素组成
B. 过氧化氢分子中含有氢分子和氧分子
C. 过氧化氢由两个氢原子和两个氧原子构成
D. 过氧化氢中氢元素和氧元素的质量分数相等
16. 人们常用模型来表示分子.如果用 表示氧原子,用 表示碳原子,则下图中能表示二氧化碳分子
模型的是
A. B. C. D.17. 实验室用高锰酸钾制取氧气 的主要步骤有:①装药品;②检查装置气密性;③固定装置;④加热;⑤
收集气体;⑥撤酒精灯;⑦从水槽中撤出导管。正确的操作顺序为 ( )
A. ②①③④⑤⑥⑦ B. ①②③④⑤⑥⑦
C. ①②③④⑤⑦⑥ D. ②①③④⑤⑦⑥
18. 下列关于催化剂的说法中正确的是
A. 催化剂只能加快化学反应速率
B. 只有二氧化锰能作过氧化氢分解的催化剂
C. 加入催化剂可增加过氧化氢产生氧气的质量
D. 加入催化剂可加快过氧化氢产生氧气的速率
19. 某微粒的结构示意图为 ,下列有关该微粒的说法不正确的是
A. 该微粒的原子核内有11个质子
B. 该微粒的原子核外有3个电子层
C. 该微粒在化学反应中易失去1个电子
D. 该图表示的微粒是一种离子
20. 下图是氢分子与氧分子反应生成水分子的示意图。从该图获得的信息中不正确的是
A. 氢分子由氢原子构成
B. 一个水分子由两个氢原子和一个氧原子构成
C. 分子是化学变化中的最小粒子
D. 在化学变化中原子的种类不变
第二部分 非选择题(共50分)
〖生活现象解释〗
21. 空气是重要的自然资源。
(1)潜水员水下作业时需携带氧气瓶,因为氧气能________。
(2)氮气的化学性质不活泼,因此生活中常用作________。
22. 能源利用与社会可持续发展密切相关。
(1)目前人们使用的燃料大多来自于化石燃料,如煤、_______、天然气等。(2)天然气的主要成分是甲烷,其燃烧的文字表达式为_______。
(3)甲烷(CH)中碳、氢元素的质量比为________。
4
23. 搭篝火是露营的一项传统活动。
(1)从燃烧条件的角度分析,木柴属于________。
(2)搭篝火时通常将木柴架空燃烧,这是为了_______(填序号)。
A 加快散热
B 降低木柴的着火点
C 使木柴与空气充分接触
(3)用沙土可以盖灭篝火,其灭火原理为_________。
24. 我国科学家在利用镓进行肿瘤的早期精准诊断方面取得重大突破。元素周期表中镓元素的信息如图所
示。
(1)镓属于________(填“金属”或“非金属”)元素。
(2)镓的相对原子质量为__________。
25. 维生素C(C HO)主要存在于蔬菜水果中,它能促进人体发育、增强抵抗力。
6 8 6
(1)维生素C中碳、氢、氧原子的个数比为__________。
(2)维生素C相对分子质量的计算式为___________。
〖科普阅读理解〗
26. 阅读下面科普短文。
钙是人体内含量最高的金属元素,是构成人体的重要组分。成人体内约含钙1.2kg,其中99%存在于骨骼
和牙齿中,主要以羟基磷酸钙[Ca (PO )(OH)]晶体的形式存在,它使得骨骼和牙齿具有坚硬的结构
10 4 6 2
支架。
幼儿及青少年缺钙会患佝偻病和发育不良,老年人缺钙会发生骨质疏松,容易骨折。因此,人体每日必须
摄入足够量的钙。未成年人正处于生长发育阶段,钙的需要量也相对较大,可达成人需要量的2~4倍,要
特别注意补充。
人体对钙的需要可以从食物中获得,奶、奶制品、豆类、虾皮等食物中含钙丰富,是日常饮食中钙的较好来源。因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用补钙药品。体育运动可使肌肉互相
牵拉,刺激骨骼,加强血液循环和新陈代谢,减少钙质丢失,同时有利于人体对饮食中钙的吸收。阳光中
的紫外线能够促进体内维生素D的合成,有利于钙的吸收,因此多晒太阳对补钙有助益。
依据文章内容回答下列问题。
(1)羟基磷酸钙[Ca (PO )(OH)]的组成元素有_________种。
10 4 6 2
(2)青少年缺钙会患_________。
(3)下列食物可为人体补钙的是_________(填序号,下同)
A 牛奶 B 酸奶 C 豆腐 D 虾皮
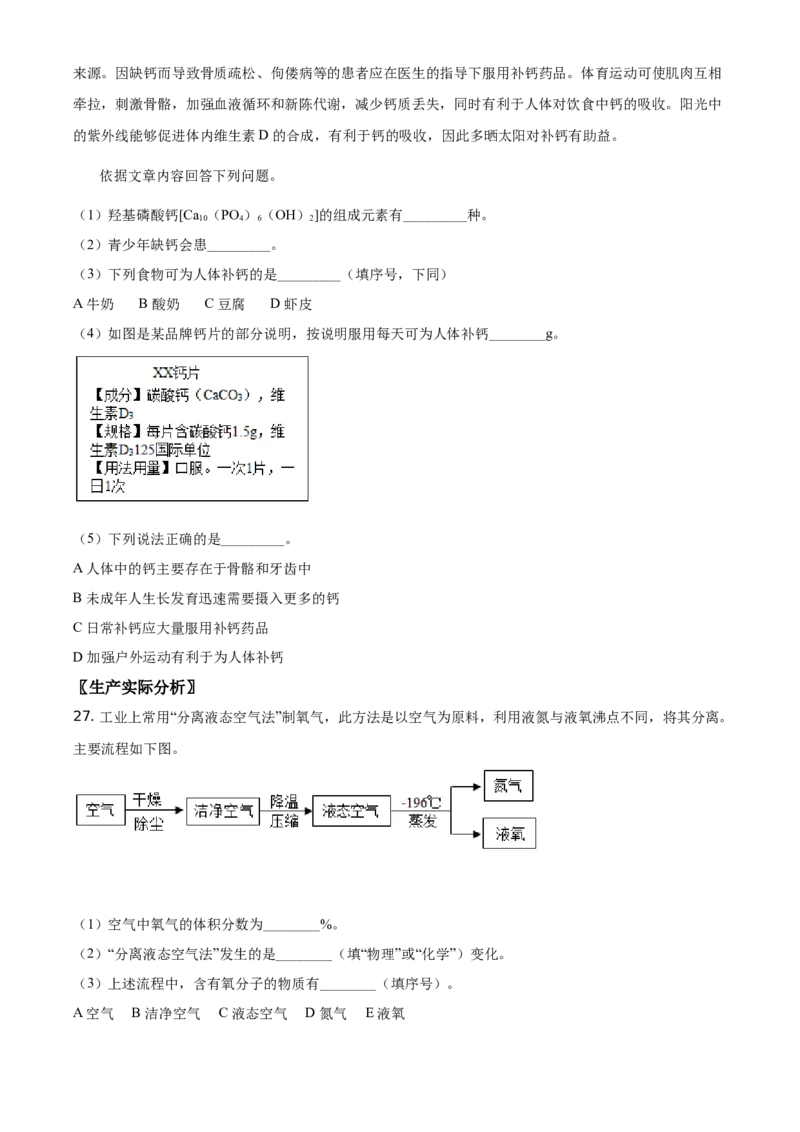
(4)如图是某品牌钙片的部分说明,按说明服用每天可为人体补钙________g。
(5)下列说法正确的是_________。
A 人体中的钙主要存在于骨骼和牙齿中
B 未成年人生长发育迅速需要摄入更多的钙
C 日常补钙应大量服用补钙药品
D 加强户外运动有利于为人体补钙
〖生产实际分析〗
27. 工业上常用“分离液态空气法”制氧气,此方法是以空气为原料,利用液氮与液氧沸点不同,将其分离。
主要流程如下图。
(1)空气中氧气的体积分数为________%。
(2)“分离液态空气法”发生的是________(填“物理”或“化学”)变化。
(3)上述流程中,含有氧分子的物质有________(填序号)。
A 空气 B 洁净空气 C 液态空气 D 氮气 E 液氧28. 水是生命之源,人类的日常生活与工农业生产都离不开水。城市生活用水的主要净化流程如下图。
(1)河水属于__________(填序号)。
A 纯净物 B 混合物 C 化合物
(2)常用 的净水絮凝剂为硫酸铝,其化学式为________。
(3)通过隔网和滤水池可去除水体中的________(填“可溶性”或“不溶性”)杂质。
(4)向清水池中投放二氧化氯(ClO ),可以消毒灭菌。二氧化氯中氯元素的化合价为_______ 。
2
〖基本实验及其原理分析〗
29. 下列装置可用于实验室制取气体。
(1)用高锰酸钾制取氧气的文字表达式为_________,该反应属于________(填“化合”或“分解”)反
应。
(2)用高锰酸钾制取氧气,应选用的发生装置和收集装置为_________(填序号)。
30. 用下图所示实验研究氧气的性质。
(1)实验1中,可观察到铁丝在氧气中剧烈燃烧,火星四射,放出大量热,_______。该反应的文字表达
式为_______。
(2)实验2中,可观察到木炭在氧气中燃烧,_______,放热。验证木炭燃烧后的生成物,需向集气瓶内倒入________。
31. 为研究分子的性质,进行如下实验。
(1)实验1中, A烧杯溶液无明显变化,B烧杯溶液由无色变为红色,该现象说明分子具有的性质是
_______。
(2)实验2中,品红在_______(填“冷”或“热”)水中扩散更快。
32. 电解水实验揭示了水的组成,装置如图所示。
(1)该反应的文字表达式为_________。
(2)得到氧气的试管是________(填“1”或“2”)。
(3)若试管1中产生10mL气体,则试管2中产生_____mL气体。
(4)该实验说明水是由_________(填序号)组成的。
A 氢元素和氧元素 B 氢原子和氧原子 C 氢分子和氧分子
33. 用如图所示装置探究可燃物的燃烧条件。
已知:白磷的着火点是40℃,红磷的着火点是240℃
(1)对比铜片上白磷燃烧、红磷不燃烧的现象,可知可燃物燃烧的条件之一是________。
(2)能说明可燃物燃烧需要与氧气接触的现象是________。
(3)要使烧杯中的白磷燃烧,可采用的操作是________(填序号)。A 将80℃水加热至90℃
B 将白磷从80℃水中取出
C 将导管对准烧杯中的白磷,通入氧气
34. 用如图所示装置测定空气中氧气的含量。
(1)该实验中红磷燃烧的文字表达式为_______。
(2)该实验操作的正确顺序是_______(填序号)。
① 用止水夹夹紧胶皮管。
② 待红磷熄灭并冷却至室温后,打开止水夹。
③ 点燃红磷,立即伸入瓶中并塞紧橡皮塞。
④ 检查装置 的气密性。在集气瓶中加入少量水,并将水面上方空间分成5等份。
(3)若实验中红磷的量不足,可导致测定结果_________(填“偏大”、“偏小”或“不变”)。
(4)能说明空气中氧气含量的现象是_______。
〖科学探究〗
35. 某化学小组同学用过氧化氢溶液进行相关实验。
Ⅰ.制取氧气
(1)过氧化氢溶液与二氧化锰制取氧气 的文字表达式为________。
(2)能用排水法收集氧气的原因是________。
(3)若要检验生成的气体是否为氧气,可将导管从水中取出,取带火星的木条放在导管口处,观察到
________,说明生成的气体是氧气。
Ⅱ.探究过氧化氢分解速率的影响因素
实验1:取6 mL30%的过氧化氢溶液进行实验,数据如下表:实验序号 1-1 1-2 1-3
温度/℃ 20 35 55
二氧化锰的用量/g 0 0 0
收集氧气的体积/mL 0 1.9 7.8
反应时间/分 40 40 40
(4)由此得出影响过氧化氢分解速率的因素之一是__________。
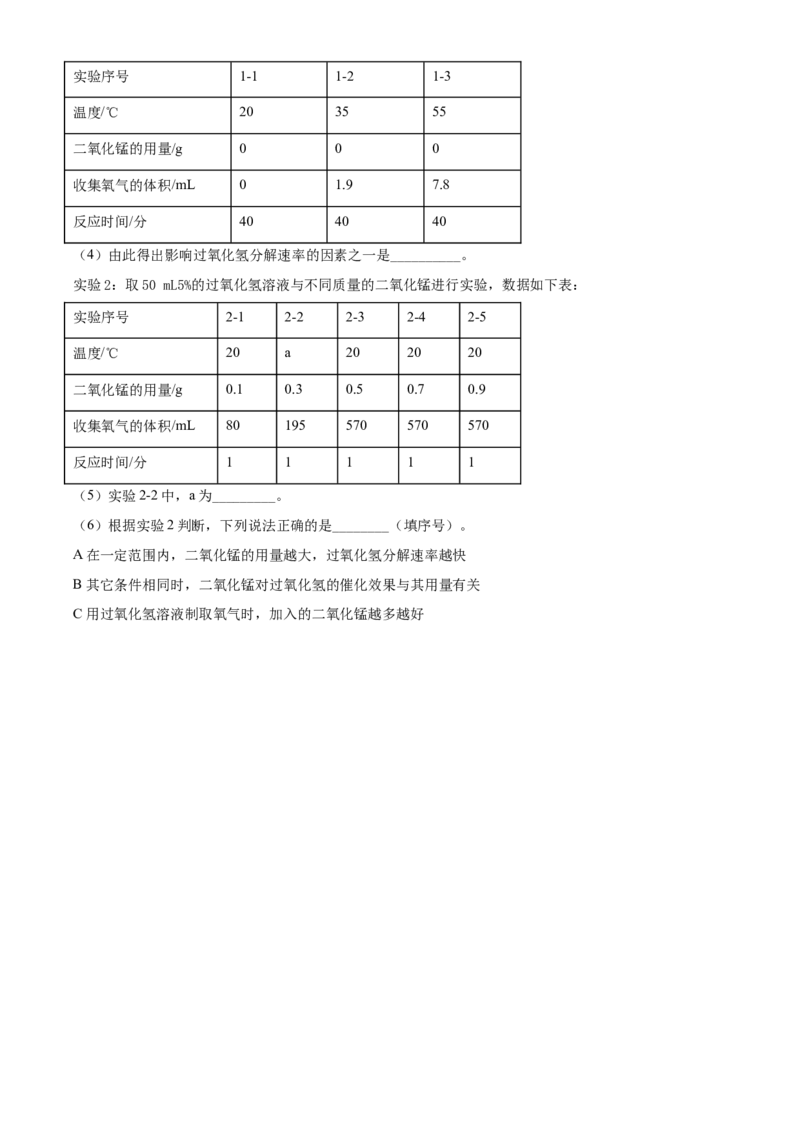
实验2:取50 mL5%的过氧化氢溶液与不同质量的二氧化锰进行实验,数据如下表:
实验序号 2-1 2-2 2-3 2-4 2-5
温度/℃ 20 a 20 20 20
二氧化锰的用量/g 0.1 0.3 0.5 0.7 0.9
收集氧气的体积/mL 80 195 570 570 570
反应时间/分 1 1 1 1 1
(5)实验2-2中,a为_________。
(6)根据实验2判断,下列说法正确的是________(填序号)。
A 在一定范围内,二氧化锰的用量越大,过氧化氢分解速率越快
B 其它条件相同时,二氧化锰对过氧化氢的催化效果与其用量有关
C 用过氧化氢溶液制取氧气时,加入的二氧化锰越多越好本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635