文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题五 化学计算题
(试题分值:100分 测试时间:80分钟)
可能用到的相对原子质量:C-12,H-1,O-16,N-14,S-32,Cl-35.5,Cu-64,Mg-24,
Ba-137,K-39,Fe-56,Ca-40,Na-23,Zn-65,Sn-119
一、选择题(本题包括13小题,1~5题每小题3分,6~13题每小题4分,共47分.1~11每小题
只有1个正确答案,12~13每小题有2个正确答案。)
1.【新考法】传统文化----典籍中的化学(2024·青海西宁·中考真题)《本草纲目》记载:“三七近时始
出,南人军中,用为金疮要药,云有奇功”。三七中止血的活性成分主要是三七氨酸 ,下列说
法错误的是
A.三七氨酸属于有机物
B.三七氨酸中含有氮分子
C.三七氨酸中氧元素的质量分数最大
D.三七氨酸分子中碳原子和氢原子的个数比为5:8
【答案】B
【详解】A、三七氨酸是含有碳元素的化合物,属于有机物,故正确;
B、三七氨酸是由三七氨酸分子构成的,不含有氮分子,故错误;
C、三七氨酸中碳、氢、氮、氧四种元素的质量比为(12×5):(1×8):(14×2):(16×5)=15:2:
7:20,其中氧元素的质量分数最大,故正确;
D、三七氨酸是由三七氨酸分子构成的,一个三七氨酸分子中含有5个碳原子、8个氢原子、2个氮原子和
5个氧原子,则三七氨酸分子中碳原子和氢原子的个数比为5:8,故正确;
故选B。
2.(2024·江苏无锡·中考真题)一定条件下,甲和乙反应的微观过程如图所示。下列叙述正确的是
A.甲、乙、丙、丁中有3种氧化物
B.反应前后原子种类改变
C.参加反应的甲和乙的分子个数比为1:1
D.反应生成的丙和丁的质量比为5:3
【答案】C
【分析】
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
发生反应为:
【详解】A、甲、乙、丙、丁都是纯净物,其中乙、丁含有两种元素,且其中一种元素是氧元素,属于氧
化物;甲含两种元素,但不含氧元素、丁含有三种元素,甲、丁不属于氧化物,说法不正确;
B、反应前后原子种类不改变,说法不正确;
C、参加反应的甲和乙的分子个数比为1:1,说法正确;
D、反应生成的丙和丁的质量比为 ,说法不正确。
故选:C。
3.(2024·四川达州·中考真题)实验室有部分被氧化的镁条8.0g与300.0g溶质质量分数为7.3%的稀盐酸
恰好完全反应,该镁条中镁元素的质量为
A.7.8g B.7.2g C.6.0g D.2.4g
【答案】B
【详解】氧化镁和稀盐酸反应生成氯化镁和水,镁和稀盐酸反应生成氯化镁和氢气,由质量守恒定律,反
应前后氯元素的质量不变,生成的氯化镁中氯元素的质量为300g×7.3%× ×100%=21.3g;氯化镁中镁元
素的质量即为样品中镁元素的质量,其质量为21.3g× =7.2g。故选B。
4.【新考法】循环转化图(2024·山东泰安·中考真题) 和 在一定条件下转化为 (反应过程如
图所示,虚线处部分中间产物略去),可实现 的再利用。下列说法错误的是
A. 是一种清洁能源
B.MgO起催化作用
C.参加反应的 和 质量比是
D.该反应中,除 外另一种生成物为
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【答案】C
【详解】A、甲烷(CH)只含有碳、氢两种元素,燃烧产物通常为二氧化碳和水,相对其他一些能源较为
4
清洁,是一种清洁能源,故选项说法正确;
B、从反应过程图示可以看出,氧化镁(MgO)在反应前后本身的质量和化学性质没有发生改变,符合催
化剂的特征,所以在反应中作催化剂,起催化作用,故选项说法正确;
C、根据题目信息可知,该反应的化学方程式为CO+4H CH+2H O,在化学反应中参加反应的
2 2 4 2
CO 与H 质量比为44:(1×2×4)=11:2,故选项说法不正确;
2 2
D、由反应的化学方程式CO+4H CH+2H O可知,该反应的生成物为甲烷和水,故选项说法正
2 2 4 2
确。
故选C。
5.(2024·四川绵阳·中考真题)将一定质量的水煤气(CO和 的混合物)在氧气中充分燃烧,燃烧产物
依次通过足量的浓硫酸和NaOH溶液,浓硫酸增重0.9g,NaOH溶液增重2.2g。该水煤气中CO和 的质
量比为
A.7:1 B.14:1 C.28:1 D.56:1
【答案】B
【详解】将一定质量的水煤气(CO和 H 的混合物)在氧气中充分燃烧,燃烧产物依次通过足量的浓硫酸
2
和NaOH溶液,浓硫酸增重0.9g,NaOH溶液增重2.2g,则生成水的质量为0.9g,生成二氧化碳的质量为
2.2g;
设该水煤气中CO的质量为 , 的质量为
该水煤气中CO和 的质量比为 ;
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选:B。
6.(2024·河南·一模)12.8 g MgO和CuO的混合物与足量的稀盐酸充分反应,所得溶液蒸发结晶并充分
干燥后称量固体的质量为23.8 g,则原混合物中金属元素的质量分数为
A.25% B.75% C.78% D.80%
【答案】B
【详解】氧化镁、氧化铜与稀盐酸反应的化学方程式分别为 、
,由上述化学方程式可知:1个氧化镁、1个氧化铜中的1个氧原子被2个氯原子
取代,1个氧原子相对原子质量是16,2个氯原子相对原子质量是71,2个氯原子和1个氧原子相对原子质
量相差=71-16=55,即完全反应后质量增加55份质量,氧化镁、氧化铜中氧原子占16份质量,实际反应中
固体增加质量=23.8g-12.8g=11g,设12.8 g MgO和CuO的混合物氧元素质量为
, ,原混合物中金属元素的质量分数= ;
故选:B。
7.(2024·黑龙江哈尔滨·中考真题)课堂上老师演示了镁条燃烧的实验,相关信息见卡片,下列分析正确
的是
参加反应的 的质量等于生成 的质量
称量到的 中氧元素的质量为
参加反应的 的质量等于未称量到的 的质量
未称量到的 的质量为
A. B. C. D.
【答案】B
【详解】 镁与氧气反应生成氧化镁,根据质量守恒定律可知,参加反应的镁的质量不等于生成的氧化镁
的质量,因为还有氧气参加反应,选项错误;
称量到的氧化镁中氧元素的质量为=4.8g× ×100%=1.92g,选项正确;
解:设参加反应的氧气的质量为x,生成氧化镁的质量为y
= x=3.2g
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
= y=8g
未称量到的氧化镁的质量=8g−4.8g=3.2g,所以参加反应的 的质量等于未称量到的氧化镁的质量,选项
正确;
未称量到的氧化镁的质量=8g−4.8g=3.2g,选项错误,故选B。
8.(2024·四川德阳·中考真题)向mg溶质质量分数为w%的BaCl 溶液中逐滴加入溶质质量分数为w%
1 2 2
的HSO 溶液,至恰好完全沉淀。将沉淀滤出,所得溶液的质量刚好为mg。下列结论正确的是
2 4
A.生成沉淀233 g B.可以确定m的值
C.w%=20.8% D.w%≈42. 06%
1 2
【答案】D
【分析】向mg溶质质量分数为w%的BaCl 溶液中逐滴加入溶质质量分数为w%的HSO 溶液,至恰好
1 2 2 2 4
完全沉淀,氯化钡与硫酸反应生成硫酸钡沉淀和盐酸,将沉淀滤出,所得溶液的质量刚好为mg,根据质
量守恒定律可知,化学反应前后物质的总质量不变,说明加入硫酸溶液的质量与生成硫酸钡沉淀的质量相
同,设生成硫酸钡沉淀的质量为x,参与反应的氯化钡质量为y,
已知加入mg溶质质量分数为w%的BaCl 溶液,则 ,但是这个等式并不能直接求出
1 2
m的值,因为不知道x(即硫酸溶液的质量,也等于硫酸钡沉淀的质量)的具体值。
【详解】A、由分析可知,由于不能直接求出m的值,所以也不能确定生成的硫酸钡沉淀就是233g,说法
错误,不符合题意;
B、由分析可知,不能直接求出m的值,说法错误,不符合题意;
C、由分析可知, ,则 ,由于不知道x和m的具体值,所以不能直接
得出 的结论,说法错误,不符合题意;
D、由分析可知,设生成硫酸钡沉淀的质量为x,则硫酸溶液中硫酸的质量为 ,
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
则 ,解得 ,说法正确,符合题意。
故选:D。
9.已知,4KO +2CO =2K CO+3O ,4KO +2H SO =2K SO +2H O+3O↑,现有28.4gKO 与一定量的CO 反
2 2 2 3 2 2 2 4 2 4 2 2 2 2
应后,固体质量变为27.8g,向反应后的固体中加入过量的200.0g稀硫酸,将产生的气体通入过量的石灰
水中,得到15.0gCaCO 。下列说法不正确的是
3
A.KO 应密封保存
2
B.与CO 反应生成O 的质量为7.2g
2 2
C.与CO 反后的固体中KO 和KCO 的质量比为71:207
2 2 2 3
D.与稀硫酸反应后所得溶液中KSO 的质量分数约为15.3%
2 4
【答案】D
【详解】A、由题意可知,KO 能与CO 反应,故应密封保存,故A正确;
2 2
B、解:设反应生成O 的质量为x
2
x=7.2g,故B正确;
C、解:设与二氧化碳反应的KO 的质量为y,反应生成碳酸钾的质量为z
2
y=21.3g
z=20.7g
则与CO 反应后的固体中KO 和KCO 的质量比为(28.4g﹣21.3g):20.7g=71:207,故C正确;
2 2 2 3
D、发生反应为: 、 、
,根据质量守恒定律,化学反应前后,元素的种类不变,则KO
2
中的钾元素完全转化到了硫酸钾中,则生成硫酸钾的质量为:
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
由化学方程式: 、 可知,碳酸钾与硫
酸反应生成的二氧化碳被石灰水完全吸收;
解:设反应生成二氧化碳的质量为m
m=6.6g
与硫酸反应的KO 的质量为28.4g-21.3g=7.1g,设KO 与硫酸反应生成O 的质量为n,则:
2 2 2
n=2.4g
故与硫酸反应后所得溶液中KSO 的质量分数约为: ,故D错
2 4
误。
故选:D。
10.(2024·江苏镇江·中考真题)已知:2NaHCO NaCO+CO ↑+H O,将16.8gNaHCO 固体加热一段时
3 2 3 2 2 3
间后,剩余固体质量为13.7g。下列说法正确的是
A.原固体加热生成3.1gCO
2
B.加热后,固体中钠元素的质量分数减小
C.剩余固体中NaHCO 和NaCO 的质量比为42:53
3 2 3
D.将13.7g剩余固体溶于足量盐酸后,蒸发结晶,得11.7gNaCl
【答案】D
【详解】A、解:设原固体加热生成二氧化碳的质量为x
x=2.2g,不符合题意;
B、碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,根据质量守恒定律,化学反应前后,元素的种类和质
量不变,故固体中钠元素的质量不变,由于生成了气体,加热后,固体的质量减小,故加热后,固体中钠
元素的质量分数增大,不符合题意;
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、解:设参加反应的碳酸氢钠的质量为y,反应生成碳酸钠的质量为z
y=8.4g
z=5.3g,则剩余固体中碳酸氢钠和碳酸钠的质量比为:(16.8g-8.4g):5.3g=84:53,不符合题
意;
D、碳酸氢钠受热分解: ,碳酸氢钠和稀盐酸反应:
,碳酸钠和稀盐酸反应: ,根据质量
守恒定律,化学反应前后,元素的种类和质量不变,由化学方程式可知,最后得到氯化钠中钠元素的质量
与16.8g碳酸氢钠中钠元素的质量相同,则生成氯化钠的质量为:
,符合题意。
故选D。
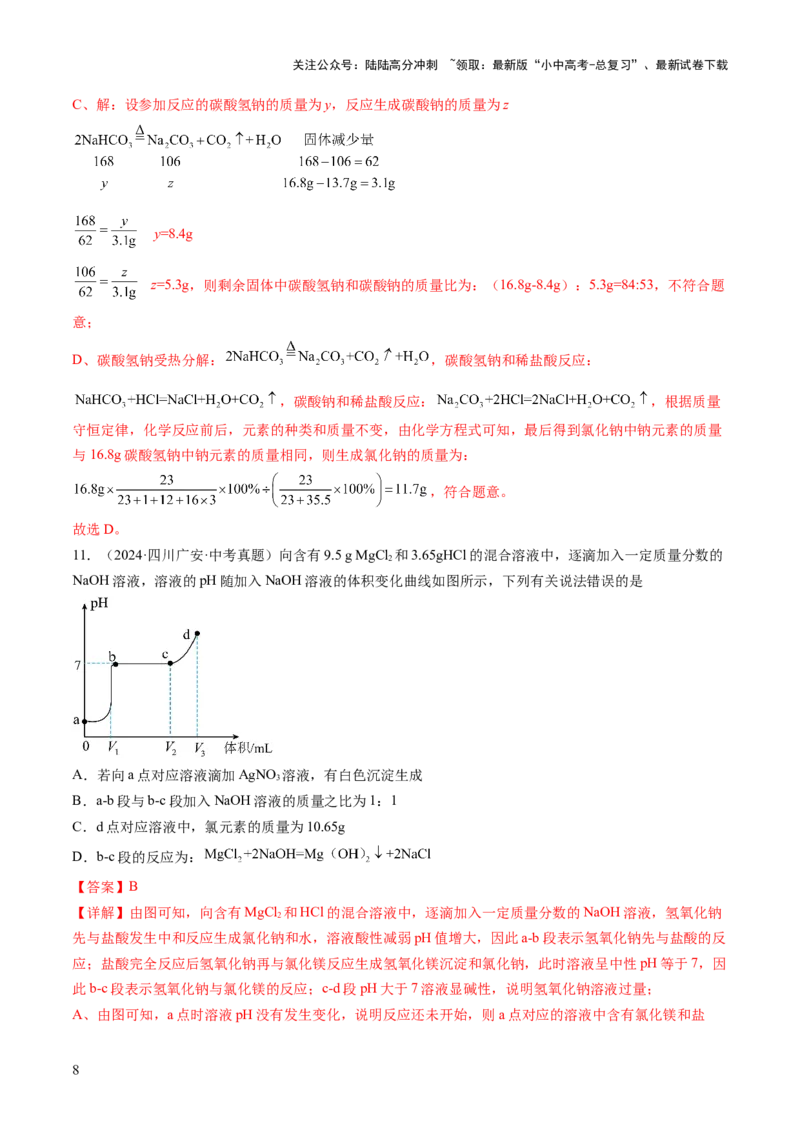
11.(2024·四川广安·中考真题)向含有9.5 g MgCl 和3.65gHCl的混合溶液中,逐滴加入一定质量分数的
2
NaOH溶液,溶液的pH随加入NaOH溶液的体积变化曲线如图所示,下列有关说法错误的是
A.若向a点对应溶液滴加AgNO 溶液,有白色沉淀生成
3
B.a-b段与b-c段加入NaOH溶液的质量之比为1:1
C.d点对应溶液中,氯元素的质量为10.65g
D.b-c段的反应为:
【答案】B
【详解】由图可知,向含有MgCl 和HCl的混合溶液中,逐滴加入一定质量分数的NaOH溶液,氢氧化钠
2
先与盐酸发生中和反应生成氯化钠和水,溶液酸性减弱pH值增大,因此a-b段表示氢氧化钠先与盐酸的反
应;盐酸完全反应后氢氧化钠再与氯化镁反应生成氢氧化镁沉淀和氯化钠,此时溶液呈中性pH等于7,因
此b-c段表示氢氧化钠与氯化镁的反应;c-d段pH大于7溶液显碱性,说明氢氧化钠溶液过量;
A、由图可知,a点时溶液pH没有发生变化,说明反应还未开始,则a点对应的溶液中含有氯化镁和盐
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
酸,向a点对应溶液滴加AgNO 溶液,氯离子和银离子结合生成氯化银白色沉淀,因此能观察到有白色沉
3
淀生成,说法正确,不符合题意;
B、由分析可知,a-b段发生的反应为盐酸与氢氧化钠反应生成氯化钠和水,设消耗氢氧化钠的质量为x,
b-c段发生的反应为氯化镁与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,设消耗氢氧化钠的质量为y,
设氢氧化钠溶液的溶质质量分数为m,则a-b段与b-c段加入NaOH溶液的质量之比为 ,说法
错误,符合题意;
C、由图可知,d点pH大于7,说明溶液显碱性,氢氧化钠溶液过量,则d点对应溶液中的溶质为氯化钠
和氢氧化钠,由质量守恒定律可知,化学反应前后元素种类及质量不变,则d点对应溶液中氯元素的质量
为氯化镁、盐酸中氯元素的质量总和,即 ,说法
正确,不符合题意;
D、由分析可知,b-c段发生的反应为氯化镁与氢氧化钠反应生成氢氧化镁沉淀和氯化钠,化学方程式为
,说法正确,不符合题意。
故选:B。
12.(2025·天津·模拟预测)常温下,向 由 组成的固体混合物中加入
稀盐酸,恰好完全反应,得到溶液的质量为 ,再向溶液中滴加 溶液至恰好完全反应,过滤,
将滤液蒸发结晶,得到 固体 。下列有关说法中,正确的是
A.生成 的质量为 B.原固体混合物中镁元素的质量为
C.原固体混合物中 的质量为 D.原固体混合物中氧元素的质量为
【答案】AB
【分析】氧化镁、氢氧化镁、碳酸镁和稀盐酸反应的化学方程式分别为MgO+2HCl=MgCl +H O、
2 2
Mg(OH) +2HCl=MgCl +2H O、MgCO +2HCl=MgCl +H O+CO↑,加入稀盐酸后,溶液中溶质是氯化镁,
2 2 2 3 2 2 2
再加入氢氧化钠,氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠MgCl +2NaOH= Mg(OH) ↓+2NaCl。
2 2
【详解】A、根据质量守恒定律,生成二氧化碳的质量为 + - =4.4g,故选项说法正确;
B、由反应的化学方程式可知,原混合物中镁元素与最终生成氯化钠的质量关系Mg~2NaCl,设原固体混
合物中镁元素的质量为x,
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
,故选项说法正确;
C、根据分析,设碳酸镁的质量为y,
碳酸镁中镁元素的质量为8.4g×( )=2.4g,氧化镁和氢氧化镁质量和是24g-8.4g=15.6g,设氧化镁质
量为m,氢氧化镁质量为15.6g-m,则有m×( )+(15.6g-m) ×( )=9.6g-2.4g,得m=4g,原
固体混合物中 的质量为15.6g-4g=11.6g,故选项说法不正确;
D、原固体混合物中氧元素的质量为4g×( )+11.6g×( )+8.4g×( )=12.8g,故选
项说法不正确。
故选AB。
13.(2025·山东济南·一模)取 某单质铜和单质锌的混合物样品放于烧杯中,向其中加入一定量的硫
酸铜溶液,搅拌,恰好完全反应,静置。一定温度下,在烧杯中得到不饱和溶液和 固体。下列说法
中正确的是
A.反应前后锌元素的化合价保持不变
B.加入的硫酸铜溶液中溶质质量为
C.该混合物样品中单质铜的质量分数为
D.反应后烧杯中溶液的质量比加入的硫酸铜溶液的质量小
【答案】BC
【详解】A、锌和硫酸铜反应生成硫酸锌和铜,反应物中锌是单质,锌元素的化合价为0;生成物硫酸锌中
锌元素的化合价为+2价,则反应前后锌元素的化合价发生了改变,故选项说法错误;
B、设加入的硫酸铜溶液中溶质质量为x,参加反应的心得质量为y,则有
, 解得x=16g, 解得y=6.5g,即加入的硫酸
铜溶液中溶质质量为16g,故选项说法正确;
C、由B分析可知,锌的质量为6.5g,则该混合物样品中单质铜的质量分数为 ,故
选项说法正确;
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、锌与硫酸铜溶液反应生成硫酸锌溶液和铜,反应后烧杯中固体质量比原来减少了26g-25.9g=0.1g,根据
质量守恒定律,则反应后烧杯中溶液的质量比加入的硫酸铜溶液的质量大0.1g,故选项说法错误;
故选BC。
二、填空题(本题1小题,除标注外,其余每空1分,共9分)
14.(9分)(2024·黑龙江哈尔滨·中考真题)氢气 在氯气 中燃烧生成氯化氢 的反应可用
于工业制备盐酸。请结合此反应回答下列问题:
(1)请写出该反应的化学方程式 ;
(2)参加反应的 和 的质量比为 ;
(3) (2分)若完全燃烧 ,理论上能生成 的质量为 ;
(4) (2分)若用 的浓盐酸稀释得到 的稀盐酸 ,所需水的质量为 ;
(5) (3分)取 质量分数为 的稀盐酸,理论上能处理铁锈(假设铁锈的成分是 和杂质,其
中杂质占 ,且不溶于水、不与其他物质反应)的质量是 。
【答案】(1)
(2) :
(3)365
(4)400
(5)25
【详解】(1)氢气和氯气在点燃的条件下反应生成氯化氢,该反应的化学方程式为:
;
(2)由化学方程式可知,参加反应的氢气和氯气的质量比为:2:71;
(3)解:设理论上能生成HCl的质量为x
x=365kg
答:理论上能生成HCl的质量为365kg;
(4)解:设需要水的质量为y,根据稀释前后,溶质的质量不变,可得:
,y=400g
答:所需水的质量为400g;
(5)解:设理论上能处理氧化铁的质量为z
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
z=24g
则理论上能处理铁锈的质量为:
答:理论上能处理铁锈的质量是25g。
二、计算题(本题8小题,共44分)
15.(6分)(2025·四川内江·一模)布洛芬(化学式为C H O)为解热镇痛类,非甾体抗炎药。本品通过抑制
12 18 2
环氧化酶,减少前列腺素的合成,产生镇痛、抗炎作用,通过下丘脑体温调节中框而起解热作用。
(1)布洛芬的相对分子质量为 。
(2)布洛芬中C、H元素的质量比为 (最简整数比)。
(3)多少克布洛芬中含有的氧元素质量与36g水中含有的氧元素质量相等?
【答案】(1)194
(2)8:1
(3)194g
解:设质量为x的布洛芬中含有的氧元素质量与36g水中含有的氧元素质量相等。
则有x×( )=36g×( ),得x=194g;
答:194g布洛芬中含有的氧元素质量与36g水中含有的氧元素质量相等。
【详解】(1)布洛芬的相对分子质量为12×12+1×18+16×2=194,故填:194;
(2)布洛芬中C、H元素的质量比为(12×12):(1×18)=8:1,故填:8:1;
(3)见答案。
16.(5分)(2025·湖北·模拟预测)《天工开物》记载了用锡砂(主要成分为SnO )冶炼金属锡的方法,其
2
化学反应原理为 。
(1)CO 中碳、氧元素的质量比为 (填最简整数比)。
2
(2)现有151kg含SnO 10%的锡砂,理论上可以炼出锡的质量是多少(写出计算过程)?
2
【答案】(1)3:8
(2)解:设理论上可以炼出锡的质量为x,
x=11.9kg
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答:理论上可以炼出锡的质量为11.9kg。
【详解】(1)CO 中碳、氧元素的质量比为12:(16×2)=3:8;
2
(2)见答案。
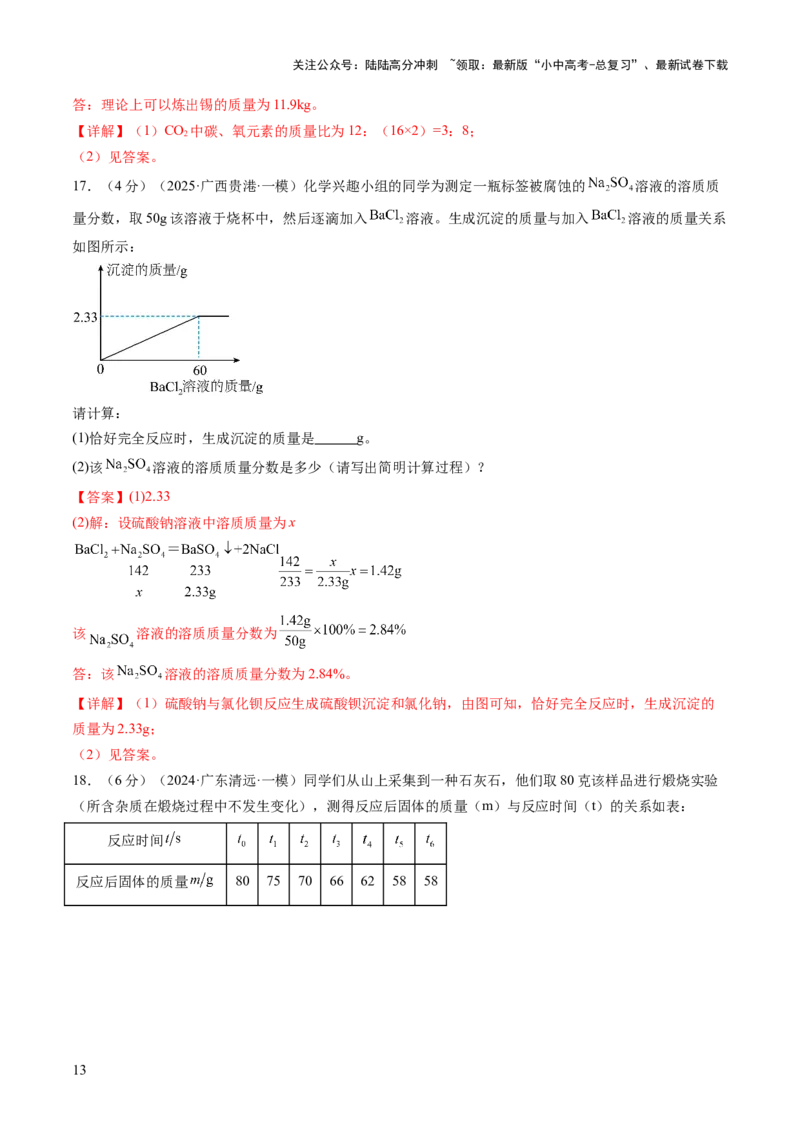
17.(4分)(2025·广西贵港·一模)化学兴趣小组的同学为测定一瓶标签被腐蚀的 溶液的溶质质
量分数,取50g该溶液于烧杯中,然后逐滴加入 溶液。生成沉淀的质量与加入 溶液的质量关系
如图所示:
请计算:
(1)恰好完全反应时,生成沉淀的质量是 g。
(2)该 溶液的溶质质量分数是多少(请写出简明计算过程)?
【答案】(1)2.33
(2)解:设硫酸钠溶液中溶质质量为x
该 溶液的溶质质量分数为
答:该 溶液的溶质质量分数为2.84%。
【详解】(1)硫酸钠与氯化钡反应生成硫酸钡沉淀和氯化钠,由图可知,恰好完全反应时,生成沉淀的
质量为2.33g;
(2)见答案。
18.(6分)(2024·广东清远·一模)同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验
(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如表:
反应时间
反应后固体的质量 80 75 70 66 62 58 58
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请回答下列问题:
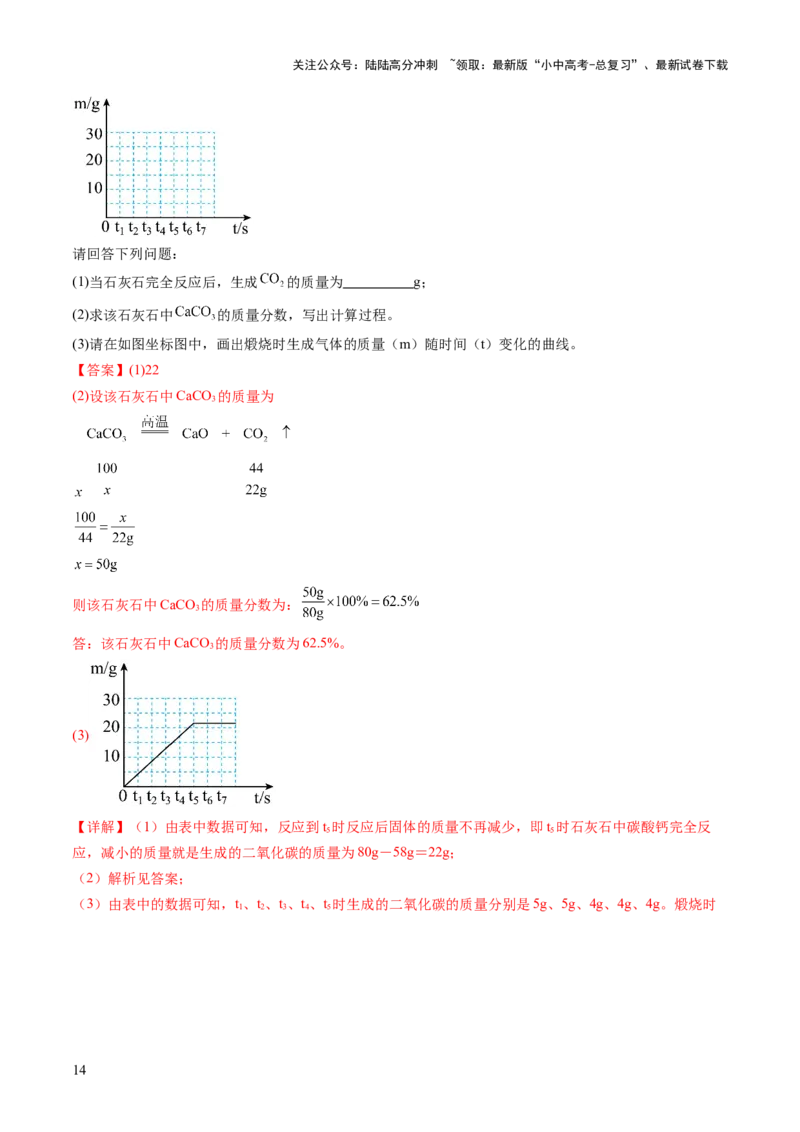
(1)当石灰石完全反应后,生成 的质量为 g;
(2)求该石灰石中 的质量分数,写出计算过程。
(3)请在如图坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线。
【答案】(1)22
(2)设该石灰石中CaCO 的质量为
3
则该石灰石中CaCO 的质量分数为:
3
答:该石灰石中CaCO 的质量分数为62.5%。
3
(3)
【详解】(1)由表中数据可知,反应到t 时反应后固体的质量不再减少,即t 时石灰石中碳酸钙完全反
5 5
应,减小的质量就是生成的二氧化碳的质量为80g-58g=22g;
(2)解析见答案;
(3)由表中的数据可知,t、t、t、t、t 时生成的二氧化碳的质量分别是5g、5g、4g、4g、4g。煅烧时
1 2 3 4 5
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
生成气体的质量(m)随时间(t)变化的曲线如下: 。
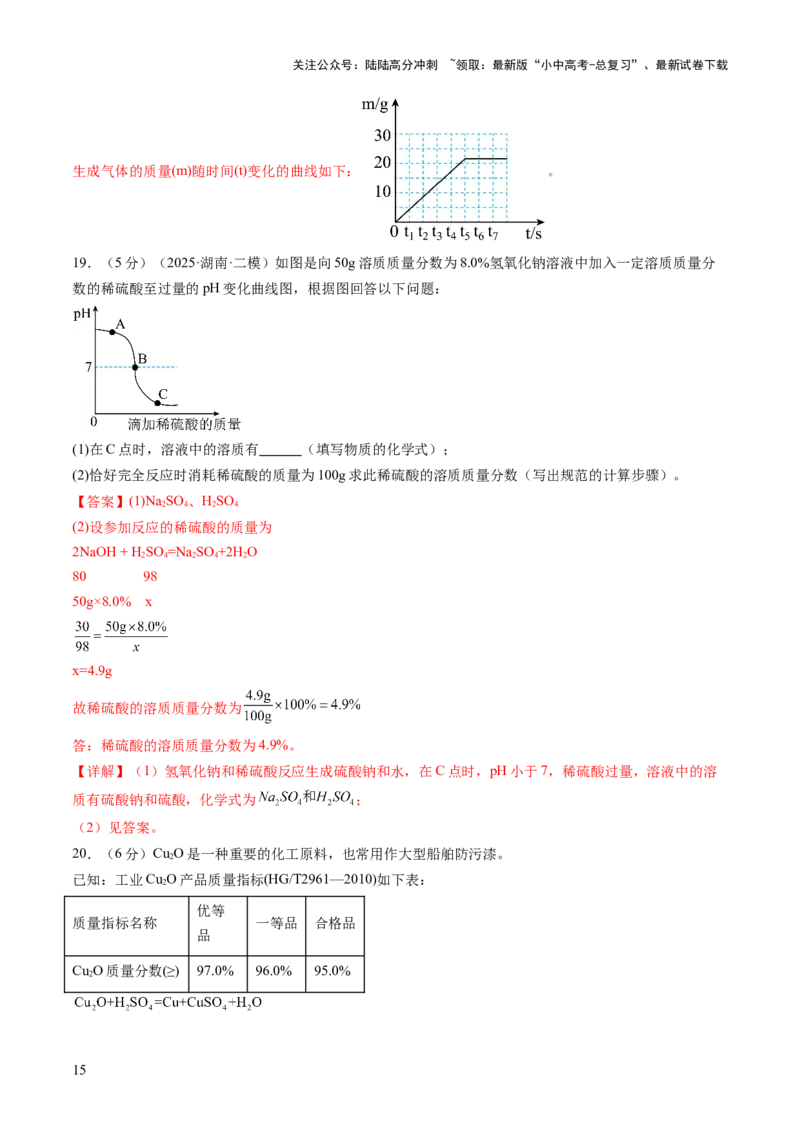
19.(5分)(2025·湖南·二模)如图是向50g溶质质量分数为8.0%氢氧化钠溶液中加入一定溶质质量分
数的稀硫酸至过量的pH变化曲线图,根据图回答以下问题:
(1)在C点时,溶液中的溶质有 (填写物质的化学式);
(2)恰好完全反应时消耗稀硫酸的质量为100g求此稀硫酸的溶质质量分数(写出规范的计算步骤)。
【答案】(1)Na SO 、HSO
2 4 2 4
(2)设参加反应的稀硫酸的质量为
2NaOH + H SO =Na SO +2H O
2 4 2 4 2
80 98
50g×8.0% x
x=4.9g
故稀硫酸的溶质质量分数为
答:稀硫酸的溶质质量分数为4.9%。
【详解】(1)氢氧化钠和稀硫酸反应生成硫酸钠和水,在C点时,pH小于7,稀硫酸过量,溶液中的溶
质有硫酸钠和硫酸,化学式为 ;
(2)见答案。
20.(6分)Cu O是一种重要的化工原料,也常用作大型船舶防污漆。
2
已知:工业Cu O产品质量指标(HG/T2961—2010)如下表:
2
优等
质量指标名称 一等品 合格品
品
Cu O质量分数(≥) 97.0% 96.0% 95.0%
2
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
某学习小组用工业Cu O产品进行如下实验:(注:产品中杂质全部视为Cu;不考虑实验过程中的损失)
2
步骤一:称取37.0g产品放入500.0g10%的(足量)稀硫酸中;
步骤二:充分反应后过滤,用280.0g蒸馏水洗涤固体(洗涤液全部并入滤液);
步骤三:干燥,称得固体质量为17.0g。
通过计算,回答下列问题:
(1)步骤二最终所得溶液中硫酸铜的质量分数是多少?
(2)判断该产品达到的质量指标。
【答案】(1)解:设骤二最终所得溶液中硫酸铜的质量为x,Cu O的质量为y。
2
x=40.0g
y=36.0g
则:步骤二最终所得溶液中硫酸铜的质量分数
答:则:步骤二最终所得溶液中硫酸铜的质量分数5%。
(2)Cu O质量分数为
2
答:该产品为优等品。
【详解】(1)见答案。
(2)见答案。
21.(5分)(2025·湖南长沙·模拟预测)某化学兴趣小组测定某石灰石样品中碳酸钙的质量分数(假定:
石灰石样品中除碳酸钙外,其余物质不与稀盐酸反应也不溶于水;且为了反应充分,尽可能地将石灰石粉
碎)。称取6g样品,把称取好的样品放入烧杯中(烧杯质量为10g)。将50g稀盐酸分5次加入,每次加入稀
盐酸后,用玻璃棒不断搅拌,充分反应后对烧杯(包括溶液和残余固体)进行了称量,记录如表:
第1次 第2次 第3次 第4次 第5次
加入稀盐酸的总质量(g) 10 20 30 40 50
烧杯和药品总质量(g) 25.56 35.12 44.68 54.24 64.24
(1)求样品完全反应后生成二氧化碳的质量为 g。
(2)求石灰石样品中碳酸钙的质量分数。(请写出计算过程,计算结果精确到0.1%)
【答案】(1)1.76
(2)解:设石灰石样品中碳酸钙的质量x
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
石灰石样品中碳酸钙的质量分数
答:石灰石样品中碳酸钙的质量分数为66.7%。
【详解】(1)碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,依据质量守恒定律可知,反应中烧杯和药
品总质量的减少就是生成的二氧化碳的质量;第1、2、3、4、5次生成二氧化碳质量总质量分别为
10g+6g+10g-25.56g=0.44g、10g+6g+20g-35.12g=0.88g、10g+6g+30g-44.68g=1.32g、
10g+6g+40g-54.24g=1.76g、6g+10g +50g-64.24g=1.76g;故样品完全反应后生成二氧化碳的质量1.76g。
(2)由上一步分析中第4次于第5次产生气体总质量相同,说明酸过量,样品中碳酸钙完全反应产生二氧
化碳的质为1.76g。据此进行计算,具体过程见答案。
22.(7分)(2025·天津宝坻·模拟预测)为了测定石灰石中碳酸钙的含量,小明称取20g干燥的石灰石放
入烧杯中,并向其中加入了100g稀盐酸。恰好完全反应(假设石灰石中除碳酸钙外的其他成分都不溶于
水,且不与稀盐酸反应),反应后烧杯中物质的总质量为115.6g。完成下列计算:
(1)石灰石中碳酸钙的质量分数。
(2)所用稀盐酸的溶质的质量分数。
(3)当碳酸钙恰好完全反应时,所得溶液中溶质的质量分数(结果精确到0.1%)。
【答案】(1)生成二氧化碳的质量为 。
解:设石灰石中碳酸钙的质量为x。
石灰石中碳酸钙的质量分数为
答:石灰石中碳酸钙的质量分数为50%。
(2)解:设参加反应的盐酸的质量为y。
所用稀盐酸的溶质的质量分数为
答:所用稀盐酸的溶质的质量分数为7.3%。
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)当碳酸钙恰好完全反应时,所得溶液中的溶质为氯化钙。
解:设碳酸钙恰好完全反应时生成的氯化钙质量为z。
当碳酸钙恰好完全反应时,所得溶液中溶质的质量分数为
答:当碳酸钙恰好完全反应时,所得溶液中溶质的质量分数为10.5%。
【详解】(1)见答案。
(2)见答案。
(3)见答案。
18