文档内容
理科综合参考答案
一、选择题:本题共13小题,每小题6分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13
答案 B C D C A D A B C D C D B
二、选择题:本题共8小题,每小题6分。在每小题给出的四个选项中,第14~18题只有一
项符合题目要求;第19~21题有多项符合题目要求,全部选对的给6分,选对但不全的给3
分,有选错的给0分。
题号 14 15 16 17 18 19 20 21
答案 C C B B D AD ABC ABD
【解析】
1.猴痘病毒是一种含有病毒包膜(来源于宿主细胞的细胞膜)的双链DNA病毒。其中含有
蛋白质、磷脂和DNA等化合物。
2.质壁分离过程中,由于细胞壁的伸缩性小,所以细胞的体积不会明显变小。
3.将R型活细菌与加热致死的S型细菌混合注射到小鼠体内后,从中分离得到的有S型活菌
和R型活菌,A错误。向S型细菌的细胞提取物中加入蛋白酶后再进行转化实验,该过程
利用了“减法原理”,B错误。用35S标记的噬菌体侵染未被标记的细菌,细菌裂解释放
出的噬菌体中不能检测到35S标记的蛋白质,C错误。
4.根据题目信息可知,A基因缺失突变体a的W基因表达量增加较少;但不能得出W基因
的表达产物能抑制A基因的表达。
5.年龄结构和性别比例不能直接决定种群密度。
6.TaqDNA聚合酶在PCR过程中只能沿引物的3′端延伸DNA子链。
7.含硫煤完全燃烧会产生二氧化硫污染大气,B错误。硫酸钡可用于胃肠X射线造影检查,
C错误。医用消毒酒精中乙醇的浓度(体积分数)为75%,D错误。
8.A项,25℃时,pH=9的CHCOONa溶液中,由于缺少溶液的体积,因此无法计算由水电
3
离出的H+数目。C项,1mol羟基与1mol氢氧根离子所含电子数分别为9N 、10N 。D项,
A A
SO 与O 的反应为可逆反应,不能进行到底。
2 2
9.X中的碳碳双键能发生加成反应,羧基能发生取代反应,A正确。根据X和Y的结构简
式看出,Y与乙酸发生酯化反应可得到X,B正确。Y的分子式为C H O,C错误。X、
21 22 4Y均含碳碳双键能与酸性KMnO 溶液反应,D正确。
4
10.根据分析可知,X为H,Y为N,Z为O,W为Cl。r为HCl,m为NH ,n为NO。A项,
3
N、O、Cl元素均处于元素周期表的p区。B项,非金属性NNO。C项,N的2p能级半充满,第一电离能N>O。D项,HCl与NH 形成
3 2 3
NH Cl,既含离子键,又含共价键。
4
11.A项,泡沫灭火器用Al (SO ) 和NaHCO 溶液。B项,SO 与ClO−会发生氧化还原反应。
2 4 3 3 2
D项,足量Fe粉与稀硝酸反应生成Fe2+。
12.CCl 在下层,所以先从分液漏斗下口放出有机层,后从上口倒出水层,A正确。少量钠
4
与水的反应比少量钠和乙醇的反应剧烈,说明水中氢的活泼性强于乙醇中氢的活泼性,
B正确。碘单质微溶于水,易溶于酒精,所以清洗碘升华实验所用试管,先用酒精清洗,
再用水清洗,C正确。将铁钉放入试管中用盐酸浸没,发生的是析氢腐蚀,D错误。
13.该电池是原电池,电池在微生物作用下将化学能转化为电能,A 错误。负极
HN(CH)NH 失 去 电 子 , 发 生 氧 化 反 应 , 产 生 N 、 CO , 电 极 反 应 式 为
2 2 2 2 2 2
H N(CH ) NH −16e−+4H O
2 2 2 2 2
=2CO↑+N↑+16H+,B正确。状况未知,无法由气体的体积求物质的量,所以无法
2 2
求通过质子交换膜的质子数,C错误。该电池中M为负极,电子由M经导线流向N,D
错误。
14.略
15.由 ,得 ,故A错误。减速时,有 ,得 ,故B错误。
, ,故C正确。 , , ,故
D错误。
16. ,得 , , ,可知B正确。
17.由 ,可知a→b、c→d都是等容变化,且图像斜率越大,气体体积越小,故B正
确。
18.由等质量弹性碰撞发生速度交换,可得D正确。
19.对B做受力分析,可得轻绳上的拉力和杆对B的弹力都减小。对A、B整体做受力分析,
可得F减小,杆对A的支持力增大。
20.由乙从B到C先加速后减速,BC之间某处合力为零,此时 ,到达C点后库仑力减小,则乙与斜面间静摩擦力小于 ,故A、B错误。电势能
和重力势能减小量之和为内能增加量,故C错误。 ,可
知D正确。
21. ,得 ,故 A 正确。 , ,得
,故B正确,C错误。 ,得 ,故D正确。
三、非选择题(共174分)
22.(每空2分,共10分)
(1)AE
(2)0.17 0.50
(3)
23.(每空2分,共10分)
(1) 分压
(2)甲
24.(10分)
解:(1)由对称性可知
对M,有 ①
②
解得 ③
(2)对m,有 ④
解得 ⑤
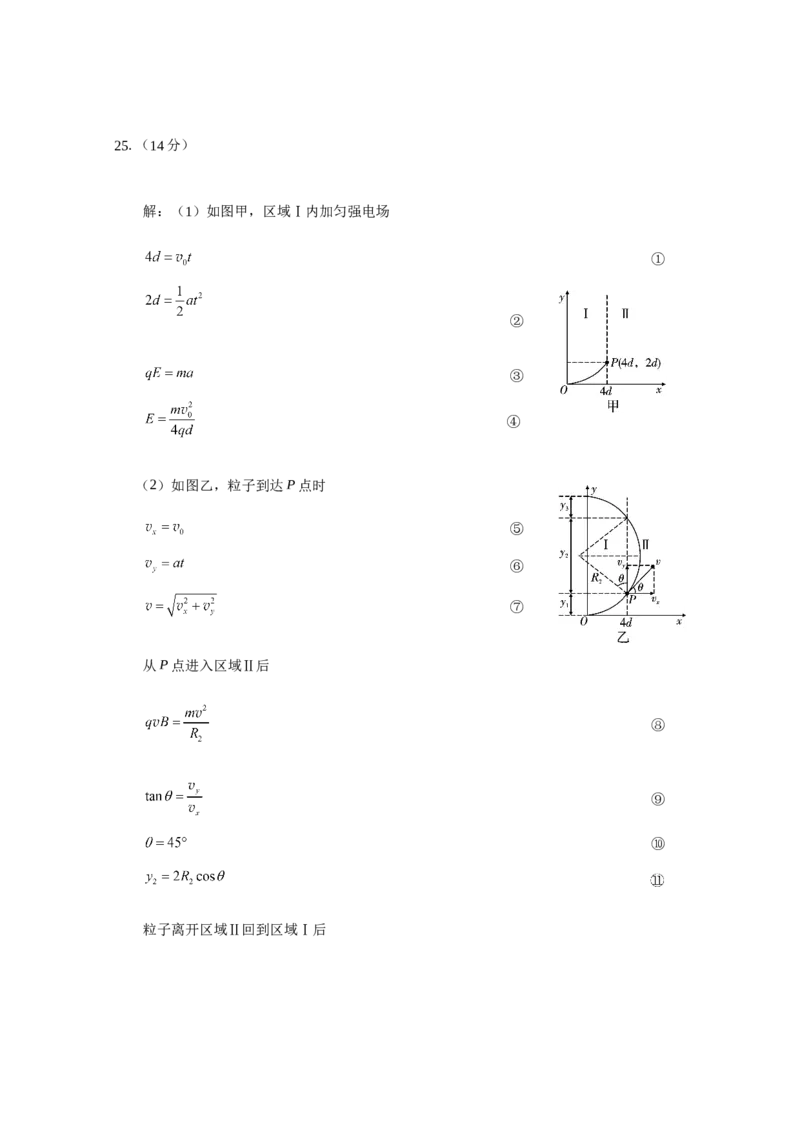
评分标准:本题共10分。正确得出①~⑤式各给2分。25.(14分)
解:(1)如图甲,区域Ⅰ内加匀强电场
①
②
③
④
(2)如图乙,粒子到达P点时
⑤
⑥
⑦
从P点进入区域Ⅱ后
⑧
⑨
⑩
粒子离开区域Ⅱ回到区域Ⅰ后粒子回到y轴时的位置坐标为(0,14d)
评分标准:本题共14分。正确得出①~ 式各给1分。
26.(18分)
解:(1)小球从A到B
、 ①
由几何关系有 、 ②
解得 ③
(2)小球到B点时,水平分速度因为绳子作用瞬间变为0,故小球到C点时
, ,解得 ④
小球与木板发生弹性碰撞,有
⑤
解得 ⑥
(3)对木板M,有 ⑦
对物块 ,有 ⑧
解得 、 ⑨
共速时,有 ,得 ⑩
1s内,解得
木板至少长
共速后,对木板M,有 ,物块 ,有 ,
距右端的距离
评分标准:本题共18分。正确得出④、 式各给2分,其余各式各给1分。
27.(除特殊标注外,每空2分,共15分)
(1)检查装置的气密性(1分)
(2)饱和NaHSO 溶液 吸收SO
3 2
(3)MnO +SO =====MnSO 三颈烧瓶中黑色粉末完全消失
2 2 4
(4)温度过高时,SO 在水中的溶解度减小,反应速率减慢
2
(5)2.5
(6)操作简单(1分) 有多孔球泡,吸收SO 更充分(或氢氧化钠溶液吸收尾气更充
2
分)
(1分)(合理答案均给分)
【解析】(2)浓盐酸和亚硫酸钠反应生成的二氧化硫气体中含有杂质气体氯化氢,B中
盛放饱和NaHSO 溶液除去二氧化硫中的氯化氢,C作安全瓶防止倒吸,二氧化硫通入
3
D中与二氧化锰反应生成MnSO ,同时用E装置吸收尾气。
4
(3)D中二氧化硫与二氧化锰反应生成MnSO ,要获得纯净的MnSO ·HO,应该在观
4 4 2
察到三颈烧瓶中黑色粉末完全消失时停止通入SO 。
2
(5)向含有1mol Na S的溶液中通入足量的SO ,发生反应5SO +2Na S+2H O=
2 2 2 2 2
3S↓+4NaHSO,则最多消耗2.5mol SO 。
3 2
(6)浓硫酸和亚硫酸钠反应生成的二氧化硫气体不含杂质气体,直接通入三颈烧瓶中与
二氧化锰反应生成MnSO ,同时设计有多孔球泡,吸收SO 更充分。
4 2
28.(除特殊标注外,每空2分,共14分)
(1)3d104s2
(2)延长浸泡时间或充分搅拌或适量增加硫酸的量或适当加热(合理答案均给分)(1
分)
(3)将Fe2+氧化为Fe3+(4)5.0≤pH < 5.4
(5)3Zn2++ =Zn(PO ) ↓+ 2H+
3 4 2
(6)热水(1分) 取最后一次洗涤液,滴入盐酸酸化的BaCl 溶液,无白色沉淀生成
2
(合理答案均给分)
(7)6.3×10−36
【解析】烧渣灰(主要含ZnO,还含少量FeO、Al O 、CuO及SiO )中加入稀硫酸,烧
2 3 2
渣灰中的ZnO,FeO、Al O 、CuO溶解,SiO 不溶,形成滤渣。溶液1中加入HO 溶液,
2 3 2 2 2
将亚铁离子氧化生成铁离子,并加入氢氧化钠溶液调节pH,除去铁离子和铝离子,生成
氢氧化铁和Al(OH) 沉淀,溶液2中金属阳离子主要为Cu2+、Zn2+,通入硫化氢,生成
3
CuS沉淀,溶液3含ZnSO ,加入NaHPO 可生成[Zn(PO )]沉淀,经过滤、洗涤、干燥
4 2 4 3 4 2
得到磷酸锌。根据提示信息,磷酸锌[Zn (PO ) ]在水中几乎不溶,其在水中的溶解度随
3 4 2
温度的升高而降低,水洗时,用热水洗涤磷酸锌沉淀比用冷水洗涤损耗更少。沉铜过程
中,当通入H 2 S达到饱和时测得溶液的pH=1,H 2 S H++HS−,HS− H++S2−。
根据H S的电离平衡常数K =1×10−7,K =1×10−15,可知K ×K = ×
2 a1 a2 a1 a2
= ,可得 c(S2−)= =
=1×10−21mol/L,CuS的溶度积K = c(Cu2+)·c(S2−)=1×10−21mol/L×6.3×10−15mol·L−1=
sp
6.3×10−36。
29.(每空2分,共14分)
(1)CO(g)+ O(g)=CO(g) ΔH=−283.0kJ·mol−1
2 2
(2)催化剂
(3)BC
(4)增大 反应②为放热反应,降低温度,化学平衡向正反应方向移动,导致n(CO)
2
增多,θ值增大
(5)① 或 ②62.51
【解析】(1)根据盖斯定律, (①+2×②)得,CO(g)+ O(g)=CO(g)
10 2 2
ΔH=−283.0kJ·mol−1,故表示CO燃烧热的热化学方程式为CO(g)+ O (g)=
2
CO (g) ΔH=−283.0kJ·mol−1。
2
(2)结合反应①和反应②分析,I 在反应①中作反应物,在反应②中是生成物,所以在
2
CO转化为CO 的反应中所起的作用是催化剂。
2
(3)达到化学平衡状态的标志之一是正逆反应速率相等,但CO和CO 的物质的量不一
2
定相等,故B错误。C中未标明正反应和逆反应,故C错误。反应②中气体的计量数之
和不变,体积不变,但是质量发生变化,因此平均分子量、密度不变时可以判断反应达
到平衡。
(5)①IO(s)→I(s),相当于减少了5个O原子,反应消耗掉IO 物质的量为n(IO)=
2 5 2 2 5 2 5
,对于反应IO(s)+5CO(g) 5CO(g)+I (s),反应开始时CO的
2 5
2 2
物质的量是 2mol,反应的 IO(s)物质的量是 0.1mol,则反应消耗 CO的物质的量是
2 5
0.5mol , 产 生 CO 的 物 质 的 量 是 0.5mol , 平 衡 时 CO 的 物 质 的 量 为
2
1.5mol
2mol−0.5mol=1.5mol , 物 质 的 平 衡 浓 度 c(CO)= =0.75mol/L, c(CO)=
2L 2
0.5mol 0.255 1
=0.25mol/L,则该反应的化学平衡常数K= 。
2L 0.755 243
②反应开始时加入的CO物质的量是2mol,根据图像可知:在温度为10℃时,当CO 移
2
出率是 0 时,CO 的转化率为 50%,则平衡时 n(CO)=n(CO)=1mol,c (CO)=c(CO)=
2 2
=0.5mol/L,故此时的化学平衡常数 。当CO的转化率是a%时,反应产生
CO 的物质的量是2a%mol,剩余CO的物质的量是(2−2a%)mol,由于CO 的移出率是
2 2
40%,则此时容器内CO 的物质的量是2a%mol×(1−40%)=1.2a%mol,由于该反应达到
2
平衡时化学平衡常数K =1,所以(2−2a%)mol=1.2a%mol,解得a%=0.625,则a=
1
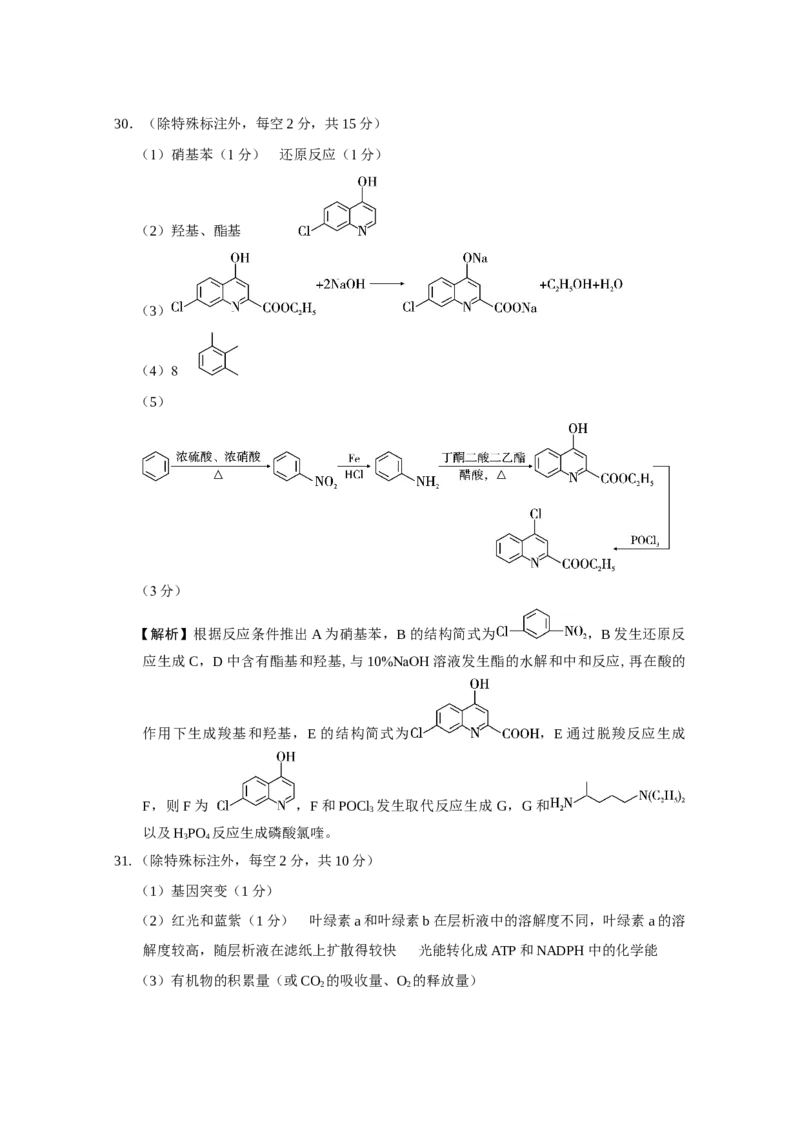
62.5。30.(除特殊标注外,每空2分,共15分)
(1)硝基苯(1分) 还原反应(1分)
(2)羟基、酯基
(3)
(4)8
(5)
(3分)
【解析】根据反应条件推出A为硝基苯,B的结构简式为 ,B发生还原反
应生成C,D中含有酯基和羟基,与10%NaOH溶液发生酯的水解和中和反应,再在酸的
作用下生成羧基和羟基,E的结构简式为 ,E通过脱羧反应生成
F,则F为 ,F和POCl 发生取代反应生成G,G和
3
以及HPO 反应生成磷酸氯喹。
3 4
31.(除特殊标注外,每空2分,共10分)
(1)基因突变(1分)
(2)红光和蓝紫(1分) 叶绿素a和叶绿素b在层析液中的溶解度不同,叶绿素a的溶
解度较高,随层析液在滤纸上扩散得较快 光能转化成ATP和NADPH中的化学能
(3)有机物的积累量(或CO 的吸收量、O 的释放量)
2 2(4)与对照组相比,实验组作物的叶绿素含量和气孔导度相对值(Gs)均明显下降,使
光反应速率和暗反应速率都下降;而两组呼吸速率相同,因此实验组作物净光合速率低
于对照组
32.(除特殊标注外,每空2分,共12分)
(1)两者碱基排列顺序不同 抗病
(2)用F 中高产(或低产)植株自交,观察后代是否发生性状分离
1
(3)两对 基因A/a与B/b之间遵循自由组合定律;F 中抗病高产的基因型为AaBb,
1
产生的配子为AB∶Ab∶aB∶ab=1∶1∶1∶1;抗病低产的基因型为Aabb,产生的配子
为Ab∶ab=1∶1;二者杂交时,雌雄配子随机结合,使得F 中出现抗病高产∶抗病低产
2
∶感病高产∶感病低产=3∶3∶1∶1(4分)
33.(除特殊标注外,每空1分,共9分)
(1)下丘脑 汗腺的分泌量减少(或皮肤血管收缩,皮肤的血流量减少) 非条件
(2)甲状腺激素、肾上腺素(2分) 神经—体液
(3)当运动排汗丢失Na+导致血钠含量降低时,肾上腺皮质会增加分泌醛固酮,促进肾
小管和集合管对Na+的重吸收,从而维持血钠含量的平衡(2分)
(4)做好保温措施;运动前充分热身;运动初期避免剧烈运动;在专业教练指导下进行
运动等
34.(除特殊标注外,每空2分,共8分)
(1)分解者、非生物的物质和能量
(2)三、四、五(1分) 营养级越多,在能量流动过程中消耗的能量就越多(1分)
(3)肉食性鱼类往往捕食个体数量多的物种,为其他物种的生存提供机会
(4)人类大量捕食牡蛎导致其绝迹后,该生态系统的组分减少,食物网复杂程度降低,
使其抵抗力稳定性降低
35.(除特殊标注外,每空2分,共15分)
(1)马铃薯琼脂 细菌(原核微生物) 选择 湿热(1分)
(2)单个微生物繁殖 通过接种环在固体培养基表面连续划线的操作,将聚集的菌种
逐步稀释分散到培养基表面,经数次划线培养,可以分离得到单菌落
(3)a 初始氧气浓度高,酵母菌进行有氧呼吸的时间长,酒精发酵的起始时间较晚
(或初始氧气浓度高,酵母菌有氧呼吸大量繁殖,在酒精发酵的初期,产生酒精的速率
较快)