文档内容
第 8 讲 化学计量(下)
达标练习01.
★☆☆☆☆
将11.7gNaCl 配制成400mL 溶液,该溶液的浓度为( )
A.0.2mol/L B.0.5mol/L C.1.0mol/L D. 2.0mol/L
【考点】物质的量浓度基本计算
【答案】B
【解答】解: mol/L。
� ���Ǥ�
� � �ͺ���ͷ�݃�
� = � = � = ���⺁ =���
达标练习02.
★☆☆☆☆
下列说法正确的是( )
A.将40gNaOH 配制成500mL 溶液,所得溶液浓度为0.5mol/L
B.将标况下11.2LNH 配制成浓度为 0.25mol/L的溶液,最终溶液体积为2L
3
C.500mL0.5mol/LMgCl 溶液中所含Cl-的物质的量为0.25mol
2
D.500mL2mol/L 稀盐酸中含氢原子约6.02×1023个
【考点】物质的量浓度基本计算
【答案】B
【解答】解:A. 2mol/L,故A错误;B. 2L,
� ��� ���Ǥ⺁
� � ���ͷ�݃� � ǤǤ��⺁ͷ�݃�
故B 正确;C.�n= �2= � =0.5�m��o⺁l,=故C错误;D.稀盐酸中�的=水� =也含��Ǥ有��氢݃� 原=子,
故条件不足无法计
=
算
�
,
�
故
=
D错误,故选B。
达标练习03.
★★☆☆☆
与50mL0.1mol•L ﹣1 Na2CO3 溶液中Na +的物质的量浓度相同的溶液是( )
A.50mL0.2mol•L
﹣1的NaCl
溶液
B.100mL0.1mol•L
﹣1的NaCl
溶液
C.25mL0.2mol•L
﹣1的Na2SO4
溶液
D.10mL0.5mol•L
﹣1的Na2CO3
溶液
【考点】物质的量浓度
第1页(共9页)【答案】A
【解答】解:50mL 0.1mol•L﹣1Na CO 溶液中Na+的物质的量浓度为0.2mol/L。
2 3
A.50 mL 0.2mol•L﹣1的NaCl 溶液中Na+的物质的量浓度为0.2mol/L,故A 正确;
B.100 mL0.1mol•L﹣1的NaCl溶液中Na+的物质的量浓度为0.1mol/L,故B错误;
C.25 mL 0.2 mol•L﹣1的 Na SO 溶液中 Na+的物质的量浓度为 0.4mol/L,故 C 错
2 4
误;
D.10 mL 0.5mol•L﹣1的Na CO 溶液中Na+的物质的量浓度为1mol/L,故D错误。
2 3
故选:A。
达标练习04
★★☆☆☆
有体积相同的两份营养液,其配方如下:
KCl
K2SO4 ZnSO4 ZnCl2
第一份 0.3mol 0.2mol 0.1mol ﹣﹣
第二份 0.1mol 0.3mol ﹣﹣ 0.1mol
两份营养液中各离子浓度( )
A.完全不同 B.完全相同
C.仅c(K +)相同 D.仅c(Cl ﹣ )相同
【考点】物质的量浓度
【答案】B
【解答】解:第一份营养液中,0.3molKCl 里面有 0.3mol 钾离子和 0.3mol 氯离
子,0.2mol 硫酸钾里面有 0.2mol×2=0.4mol 钾离子和 0.2mol 硫酸根离子,0.1mol
硫酸锌里面有0.1mol 锌离子和0.1mol硫酸根离子,那么总共此营养液里面有:
n(K +)=0.3mol+0.4mol=0.7mol,n(SO4 2﹣ )=0.2mol+0.1mol=0.3mol,n(Zn 2+)
﹣
=0.1mol,n(Cl )=0.3mol;
第二份营养液中,0.1molKCl 里面有 0.1mol 钾离子和 0.1mol 氯离子,0.3mol 硫
酸钾里面有 0.3mol×2=0.6mol钾离子和 0.3mol 硫酸根离子,0.1mol 氯化锌里面
有 0.1mol 锌离子和 0.1mol×2=0.2mol 氯离子,则第二份营养液内有:n(K +)
第2页(共9页)=0.1mol+0.6mol=0.7mol,n(SO4 2﹣ )=0.3mol,n(Zn 2+)=0.1mol,n(Cl ﹣ )
=0.1mol+0.2mol=0.3mol;
对比以上可知:因体积相同,两种营养液相同离子的物质的量相同,则两种营养
液离子浓度完全相同,故选:B。
达标练习05.
★★☆☆☆
下列溶液中氯离子浓度最大的是( )
A.150mL1mol/LNaCl B.75mL2mol/LNH4Cl
C.150mL3mol/LKCl D.75mL2mol/LCaCl2
【考点】物质的量浓度
【答案】D
﹣
【解答】解:A. 150mL1mol/L的NaCl 溶液中,Cl 浓度为:1mol/L×1=1mol/L;
﹣
B. 75mL2mol/L的NH4Cl溶液中,Cl 浓度为:2mol/L×1=2mol/L;
﹣
C. 150mL3mol/LKCl 溶液中,Cl 浓度为:1mol/L×3=3mol/L;
﹣
D. 75mL2mol/LCaCl2 溶液中,Cl 浓度为:2mol/L×2=4mol/L;
所以氯离子浓度最大的是D,故选:D。
达标练习06.
★★☆☆☆
﹣
与100mL0.2mol/LCaCl2 溶液中Cl 浓度相同的是( )
A.50mL0.1mol/LFeCl3 溶液
B.200mL0.4mol/LNaCl 溶液
C.200mL0.1mol/LMgCl2 溶液
D.200mL0.2mol/LKCl 溶液
【考点】物质的量浓度
【答案】B
﹣
【解答】解:100mL0.2mol/LCaCl2 溶液中Cl 浓度是0.4mol/L。
﹣
A.50mL0.1mol/LFeCl3 溶液中Cl 浓度是0.3mol/L,不相同,故A 错误;
第3页(共9页)﹣
B.200mL0.4mol/LNaCl 溶液中Cl 浓度是0.4mol/L,相同,故B 正确;
﹣
C.200mL0.1mol/LMgCl2 溶液中Cl 浓度是0.2mol/L,不相同,故C 错误;
﹣
D.200mL0.2mol/LKCl 溶液中Cl 浓度是0.2mol/L,不相同,故D错误;
故选:B。
达标练习07.
★★☆☆☆
将4gNaOH 固体完全溶解在水里,配成100mL 溶液,从中取出10mL,加水稀
释至50mL,所得溶液的物质的量浓度是( )
A.1mol/L B.0.1mol/L C.0.2mol/L D.0.02mol/L
【考点】物质的量浓度的相关计算
【答案】C
【解答】解:4gNaOH 的物质的量为:4g÷40g/mol=0.1mol,完全溶解在水里,
配成100mL 溶液,所得溶液浓度为:0.1mol÷0.1L=1mol/L。稀释前后溶液中溶
质的物质的量不变,稀释后溶液的物质的量浓度= =0.2mol/L,
故选:C。
达标练习08.
★★★☆☆
VmL Al2 (SO4 ) 3 溶液中含agSO4
2﹣
,若把此溶液取一半加水稀释至2VmL,
则稀释后溶液中Al 3+的物质的量浓度为( )
A. mol/L B. mol/L C. mol/L D. mol/L
【考点】物质的量浓度的相关计算
【答案】D
【解答】解:ag SO4
2﹣
的物质的量= = mol, mL 溶液中 SO4
2﹣
的
物质的量= mol× = mol,根据电荷守恒可知 2n(SO4 2﹣ )=3n(Al 3+),
mL 溶液中 Al 3+的物质的量= × mol= mol,稀释为 2VmL,溶液中
第4页(共9页)Al 3+的物质的量不变,稀释后溶液中 Al 3+的物质的量浓度= =
mol/L,故选:D。
达标练习09.
★★★☆☆
把500mL 有BaCl2 和KCl的混合溶液分成2等份,一份加入含a mol硫酸钠的
溶液,恰好使钡离子完全沉淀;另一份加入含bmol硝酸银的溶液,恰好使氯离
子完全沉淀。则该混合溶液中钾离子浓度为( )
A.0.1(b﹣2a)mol/L B.0.4(2a﹣b)mol/L
C.10(b﹣2a)mol/L D.4(b﹣2a)mol/L
【考点】物质的量浓度的相关计算
【答案】D
【解答】解:混合溶液分成两等份,每份溶液的浓度相同,一份加入含a mol 硫
酸钠的溶液,发生反应 Ba 2+ +SO4 2﹣ =BaSO4↓,恰好使钡离子完全沉淀,可知该
份中n(Ba 2+)=(Na2SO4 )=amol;另一份加入含bmol 硝酸银的溶液,发生
反应Ag + +Cl ﹣ =AgCl↓,恰好使氯离子完全沉淀,则n(Cl ﹣ )=n(Ag +)=bmol,
根据电荷守恒可知每份中 2n(Ba 2+)+n(K +)=n(Cl ﹣ ),每份溶液中n(K +)
=bmol﹣2amol=(b﹣2a)mol,溶液具有均一性,则原溶液中钾离子浓度为:c
(K +)= =4(b﹣2a) mol•L -1,故选:D。
达标练习10.
★☆☆☆☆
配制一定物质的量浓度的NaCl 溶液时,下列操作不正确的是( )
A.接近称量质量 B.溶解时,用量 C.移液时,玻璃 D.接近刻度线1~2
时,轻振手腕,加 筒控制所加蒸馏 棒插在刻度线以 cm 时,用胶头滴管滴
够药品 水的量 上,防止液体洒出 加蒸馏水至刻度线
第5页(共9页)【考点】溶液的配制
【答案】C
【解答】解:A.称量固体时,当接近称量质量时,应用左手拿药匙,右手轻轻
振动左手手腕,加够药品,图示操作正确,故A不选;
B.为防止溶解和洗涤时所用蒸馏水的体积超过容量瓶容积,溶解时应用量筒控
制所加蒸馏水的量,图示操作正确,故B 不选;
C.图示移液操作中,玻璃棒插在刻度线以上,应插在刻度线以下,故C选;
D.定容时,当液面接近刻度线1~2cm 时,用胶头滴管滴加蒸馏水至刻度线,
图示正确,故D不选;故选:C。
达标练习11.
★★☆☆☆
实验室中需要配制2mol/L的NaCl 溶液950mL,配制时应选用的容量瓶的规格
和称量的NaCl 的质量分别是( )
A.950mL,111.2g B.500mL,117g
C.1000mL,l17g D.任意规格,117g
【考点】配制一定物质的量浓度的溶液
【答案】C
【解答】解:配制 2mol/L 的 NaCl 溶液950mL,选择1000mL 容量瓶,需要 NaCl
的质量为1L×2mol/L×58.5g/mol=117g,故选:C。
达标练习12.
★★★☆☆
在配制一定物质的量浓度溶液时,下列操作出现的后果是(填“偏低”、“偏高”或
“无影响”)。
(1)配制NaOH 溶液时,称取已吸潮的NaOH 固体: 。
(2)配制NaOH 溶液时,溶液不澄清,少量溶质不溶解: 。
(3)配制NaOH 溶液时,容量瓶中有少量水: 。
(4)定容时,液面上方与刻度线相齐时,停止加水: 。
(5)发现溶液液面超过刻度线,用滴管吸出少量水,使液面降至刻度
线: 。
(6)定容后摇匀溶液,静置后发现凹液面低于刻度线,加水补齐至与刻度线相
第6页(共9页)齐: 。(7)配制NaCl 溶液时,用托盘天平称取NaCl 时采取了“左码右
物” : 。
【考点】溶液配制误差分析
【答案】
(1)偏低(2)偏低(3)无影响(4)偏高(5)偏低(6)偏低(7)偏低
【解析】
(1)NaOH 的实际质量偏小,最终浓度偏低;
(2)NaOH 的实际质量偏小,最终浓度偏低;
(3)容量瓶后续还需加水,无影响;
(4)液体体积小于容量瓶容积,最终浓度偏高;
(5)吸出溶液无法改变溶液浓度,由于溶液体积已经超过容积,最终浓度偏低;
(6)定容摇匀后由于部分溶液挂在刻度线之上的内壁,低于刻度线为正常现象,
补水后最终浓度偏低;
(7)左码右物使得药品质量小于示数,最终浓度偏低。
达标练习13.
★★★★☆
如图是硫酸试剂瓶标签上的内容:
(1)某化学兴趣小组进行硫酸性质的实验探究时,需要490mL4.6mol•L
﹣1的稀
硫酸,现要配制该浓度的溶液所需要的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴
管外,还需要 (填仪器名称);需要量取98%浓硫酸 mL 进行配制。
(2)配制溶液时有如下操作:
a.稀释溶液b.摇匀c.洗涤d.冷却 e.量取f.将溶液移至容量瓶g.定容
实验操作顺序正确的是 。
A.e→a→f→d→c→f→g→b B.e→a→d→f→c→f→g→b
C.e→a→f→d→c→f→b→g D.e→a→d→f→c→f→b→g
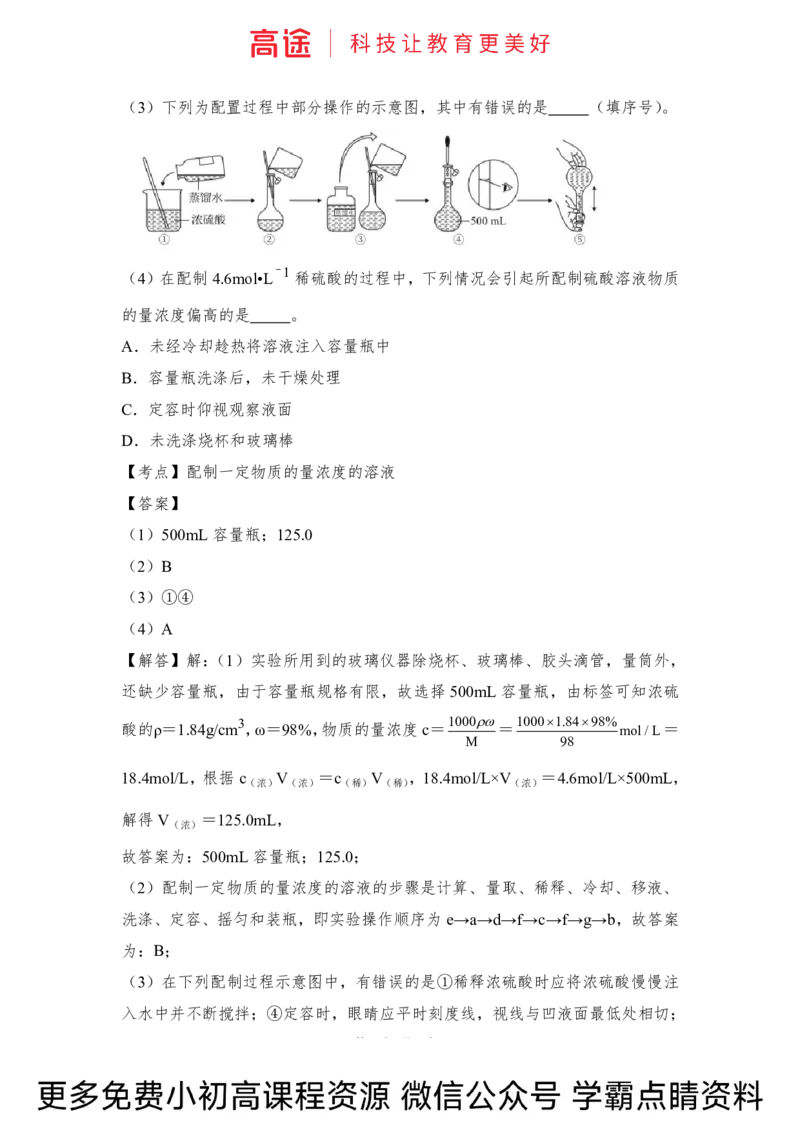
第7页(共9页)(3)下列为配置过程中部分操作的示意图,其中有错误的是 (填序号)。
(4)在配制4.6mol•L
﹣1稀硫酸的过程中,下列情况会引起所配制硫酸溶液物质
的量浓度偏高的是 。
A.未经冷却趁热将溶液注入容量瓶中
B.容量瓶洗涤后,未干燥处理
C.定容时仰视观察液面
D.未洗涤烧杯和玻璃棒
【考点】配制一定物质的量浓度的溶液
【答案】
(1)500mL 容量瓶;125.0
(2)B
(3)①④
(4)A
【解答】解:(1)实验所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管,量筒外,
还缺少容量瓶,由于容量瓶规格有限,故选择 500mL 容量瓶,由标签可知浓硫
酸的ρ=1.84g/cm 3,ω=98%,物质的量浓度c= 1000 = 10001.8498% mol/L=
M 98
18.4mol/L,根据c V =c V ,18.4mol/L×V =4.6mol/L×500mL,
(浓) (浓) (稀) (稀) (浓)
解得V =125.0mL,
(浓)
故答案为:500mL 容量瓶;125.0;
(2)配制一定物质的量浓度的溶液的步骤是计算、量取、稀释、冷却、移液、
洗涤、定容、摇匀和装瓶,即实验操作顺序为 e→a→d→f→c→f→g→b,故答案
为:B;
(3)在下列配制过程示意图中,有错误的是①稀释浓硫酸时应将浓硫酸慢慢注
入水中并不断搅拌;④定容时,眼睛应平时刻度线,视线与凹液面最低处相切;
第8页(共9页)故答案为:①④;
(4)A.未经冷却趁热将溶液注入容量瓶中,会导致溶液体积偏小,则浓度偏
高,故A正确;
B.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响,故B
错误;
C.定容时仰视观察液面,则加入的水偏多,使得溶液浓度偏低,故C错误;
D.将稀释的硫酸转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质的物质的量偏小,
溶液的浓度偏低,故D错误;故答案为:A。
第9页(共9页)