文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
精练 04 化学计算
知识点回顾(时间:5分钟)
知识点一、根据化学式的相关计算
以化合物AaBb为例,可推导出下列计算公式
1.相对分子质量:相对分子质量=A的相对原子质量×a+B的相对原子质量×b;
2.A、B原子个数比==
3.A、B元素质量比==
4.A元素的质量分数=A元素的质量分数=×100%
5.A元素的质量=化合物(AaBb)质量×A元素的质量分数
知识点二、有关溶液的计算
1.溶液质量=溶质质量+溶剂质量
溶质质量分数=×100% 变形后为:溶质质量=溶液质量×溶质质量分数
2.溶液稀释计算主要是根据稀释前后溶质质量相等列式:若浓溶液的质量为m ,质量分数
浓
为a%,加m 稀释后质量分数为b%,则可列式为:m ·a%=(m +m )·b%
水 浓 浓 水
3.化学方程式反映的是纯净物间的质量关系,涉及到的一般都是溶液中的溶质的质量,常要
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
用到的公式:
m =m ×a%,然后把得到的溶质的质量代入方程式计算。
溶质 溶液
知识点三、能根据化学方程式进行纯净物质间的计算
1.知道反应物(或生成物)的质量求生成物(或反应物)的质量。
2.根据质量守恒定律的化学方程式的计算
此内容是本课时的拓展,一类习题可根据质量守恒定律的定义或实质,利用反应物前后物质或
元素质量守恒进行计算。另一类习题还可根据反应前后物质质量之差,算出气体或沉淀物的质量,
再进行化学方程式的计算。
解题步骤:
(1)设未知量,用x、y等字母表示(不带单位);
(2)正确写出有关的化学方程式(注意配平);
(3)找出相关物质间的质量关系,写在对应化学式的下面;
(4)列出比例式,求出未知量;
(5)简明写出答案。
注意事项:
①根据化学方程式计算要注意解题格式化,准确列出有关反应物或生成物质量比,特别是相对
分子质量的计算;
②题设中未知数没有单位,求出的未知数应带单位;
③计算中已知量每步都要带单位。
【题型一】化学式的计算
[例题1] (2022•滨湖区一模)技术人员对甲醛(HCHO)、乙酸(CH COOH)和乳酸
3
(C H O )的混合水溶液进行测定,发现其中氧元素的质量分数为64%,则该溶液中溶剂水的
3 6 3
质量分数为( )
A.30% B.36% C.64% D.72%
【解答】解:根据甲醛(HCHO)、乙酸(CH COOH)和乳酸(C H O )和水的分子式,可以发
3 3 6 3
现四种物质中,H和O的原子个数比均为 2:1,则该混合物中氢元素和氧元素的质量比为
(1×2):(16×1)=1:8,其中氧元素的质量分数为64%,则氢元素质量分数为8%,故碳元素
的质量分数为1﹣64%﹣8%=28%,对甲醛(HCHO)、乙酸(CH COOH)和乳酸(C H O )三
3 3 6 3
种物质的化学式可以改写成CH O、(CH O) 、(CH O) ,因此可以将混合物看出是分子式为
2 2 2 2 3
CH O 的有机物与 H O 的结合,碳元素的质量分数为 28%,则 CH O 的质量分数为
2 2 2
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
28%×30
=70%,故水的质量分数为1﹣70%=30%。
12
故选:A。
[例题2] (2020•石首市模拟)由氧化镁和另一种金属氧化物组成的混合物 4g,已知含有氧
元素1.8g,则另一种氧化物可能是( )
A.CuO B.Fe O C.Al O D.CaO
2 3 2 3
1.8g
【解答】解:混合物中氧元素的质量分数为 ×100%=45%;
4g
16
氧化镁(MgO)中氧元素的质量分数为: ×100%=40%;
40
所以要达到混合物中氧元素的质量分数为 45%,另一种金属氧化物中氧元素的质量分数需大于
45%;
16
A、CuO中氧元素的质量分数为: ×100%=20%<45%,故A不适合。
80
16×3
B、Fe O 中氧元素的质量分数为: ×100%=30%<45%,故B不适合。
2 3 160
27×2
C、Al O 中氧元素的质量分数为: ×100%≈47.1%>45%,故C适合。
2 3 102
16
D、CaO中氧元素的质量分数为: ×100%≈28.6%<45%,故D不适合。
56
故选:C。
【题型二】溶液的计算
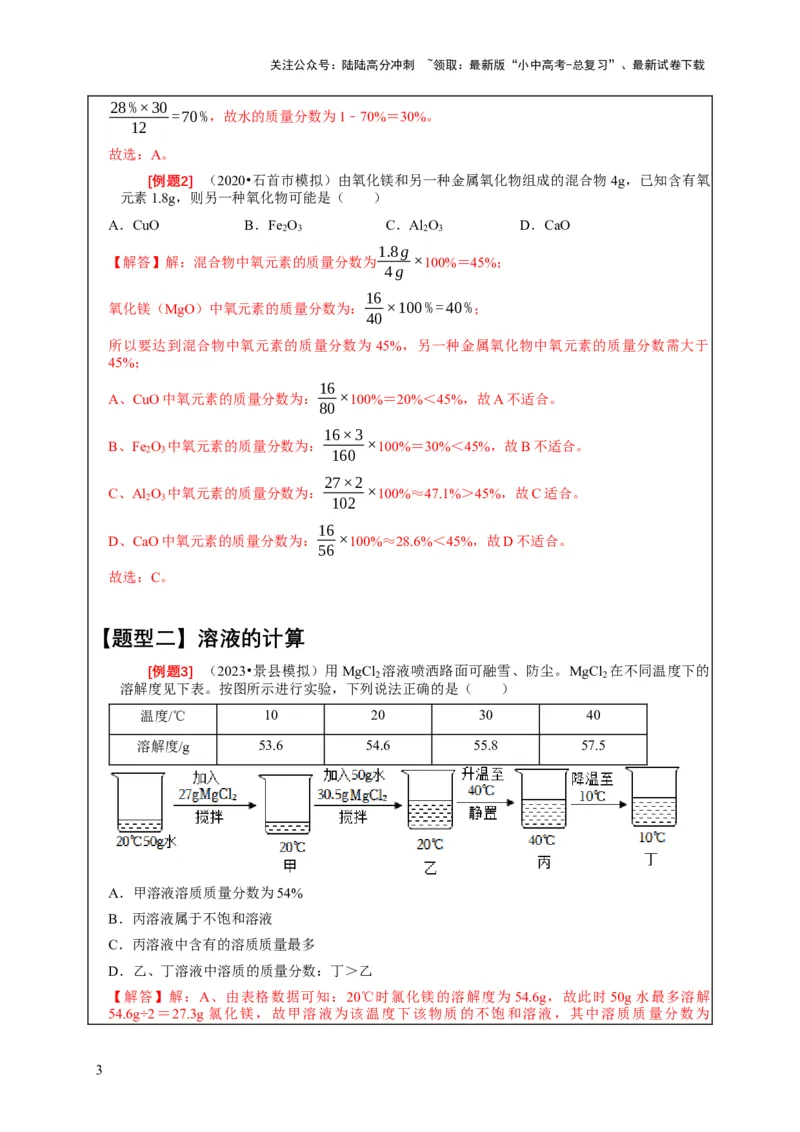
[例题3] (2023•景县模拟)用MgCl 溶液喷洒路面可融雪、防尘。MgCl 在不同温度下的
2 2
溶解度见下表。按图所示进行实验,下列说法正确的是( )
温度/℃ 10 20 30 40
溶解度/g 53.6 54.6 55.8 57.5
A.甲溶液溶质质量分数为54%
B.丙溶液属于不饱和溶液
C.丙溶液中含有的溶质质量最多
D.乙、丁溶液中溶质的质量分数:丁>乙
【解答】解:A、由表格数据可知:20℃时氯化镁的溶解度为54.6g,故此时50g水最多溶解
54.6g÷2=27.3g 氯化镁,故甲溶液为该温度下该物质的不饱和溶液,其中溶质质量分数为
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
27g
×100%≈35%,说法错误,不符合题意;
27g+50g
B、由表格数据可知:40℃时氯化镁的溶解度为57.5g,丙体系中有50g+50=100g水和27g+30.5g
=57.5g氯化镁,此时氯化镁恰好完全溶解,丙溶液属于饱和溶液,说法错误,不符合题意;
C、丙溶液中溶剂质量为100g、溶质质量为57.5g,而氯化镁溶解度随温度的升高而增大,丙溶液
温度为40℃,其温度最大,故丙溶液中含有的溶质质量最多,说法正确,符合题意;
D、由表格数据可知:20℃时氯化镁的溶解度为 54.6g,乙溶液的溶质质量分数为
54.6g
×100%≈35.3%,10℃时氯化镁的溶解度为 53.6g,丁溶液的溶质质量分数为
54.6g+100g
53.6g
×100%≈34.9%,乙、丁溶液中溶质的质量分数:丁<乙,说法错误,不符合题
53.6g+100g
意;
故选:C。
[例题4] (2023•镜湖区模拟)为探究硝酸钾的溶解性,某同学按如下步骤进行了实验。下
列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO 溶解 20.9 31.6 45.8 63.9 85.5 110.0
3
度/g
A.①③中的溶液均是不饱和溶液
B.②中的固体的质量是4.2g
C.保持温度不变,若在③中加入25gKNO 固体可得到饱和溶液
3
D.溶液的溶质质量分数满足③>②>①
【解答】解:A、由表格中的信息可知:硝酸钾在20℃时的溶解度是31.6g,则20℃中,50g水中
最多能溶解硝酸钾15.8g,因此①为不饱和溶液;60℃时,硝酸钾的溶解度为110g,50g水中最多
能溶解硝酸钾55g,③中只有硝酸钾20g,故③为不饱和溶液,故A说法正确;
B、由以上分析可知,20℃中,50g水中最多能溶解硝酸钾15.8g,②中未溶解的固体的质量是
10g+10g﹣15.8 g=4.2g,故B说法正确;
C、由以上分析可知,60℃时,硝酸钾的溶解度为110g,50g水中最多能溶解硝酸钾55g,③中只
有硝酸钾20g,保持温度不变,若在③中加入55g﹣20g=35g,硝酸钾固体可得到饱和溶液,故C
说法错误;
15.8g
D、②中硝酸钾的溶质质量分数是 ×100%≈24%,③中硝酸钾的溶质质量分数是
50g+15.8g
20g
×100%≈28.6%,②③溶液的溶质质量分数:③>②,①②溶液中的溶剂的质量
50g+20g
相等,②中溶质的质量比①中的多,故①②溶液的溶质质量分数:②>①,故D说法正确。
故选:C。
【题型三】化学方程式的计算
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
[例题5] (2023•镇江一模)已知Cu O+H SO ═Cu+CuSO +H O。现将仅含铜、硫元素组
2 2 4 4 2
成的纯净物16.0g敞口放在空气中充分加热,得16.0g两种元素组成的黑色固体纯净物。将该黑
色固体纯净物放在密闭容器中继续加热至t℃,固体全部变红,冷却得13.6g Cu与Cu O的固体
2
混合物。将此混合物放入96.0g足量稀H SO 中,充分反应,得蓝色溶液和红色固体。下列说法
2 4
正确的是( )
A.灼烧过程中产生3.2g SO
2
B.铜、硫元素组成的化合物的化学式为CuS
C.充分反应后所得蓝色溶液溶质质量分数为8%
D.若将13.6g固体混合物与足量的CO高温充分反应,可生成3.2g CO
2
【解答】解:依据题意可知,燃烧后得16.0g两种元素组成的黑色固体纯净物为CuO,则铜元素
64
的质量为16.0g× ×100%=12.8g,铜、硫元素组成的纯净物中硫元素的质量为16.0g﹣12.8g=
80
3.2g。
点燃
A.分析S+O 2 ¯ SO 2 反应可知,3.2g硫元素燃烧生成SO 2 的质量为6.4g,故A错误;
❑
12.8g 3.2g
B.通过上述分析可知,铜、硫元素组成的化合物中铜、硫元素的个数比为 : =2:1,
64 32
则化学式为Cu S,故B错误;
2
C.设13.6g固体混合物中铜的质量为x
128
x+(13.6g﹣x)× ×100%=12.8g x=6.4g,则Cu O的质量为7.2g,
144 2
设生成硫酸铜的质量为z,生成Cu的质量为y
Cu O+H SO ═Cu+CuSO +H O
2 2 4 4 2
144 64 160
7.2g y z
144 64 160
= =
7.2g y z
z=8.0g y=3.2g x=1.6g
8.0g
充分反应后所得蓝色溶液溶质质量分数为 ×100%=8%,
7.2g+96g−3.2g
故C正确;
D.设将13.6g固体混合物与足量的CO高温充分反应,生成CO 的质量为A
2
高温
Cu 2 O+CO ¯ 2Cu+CO 2
❑
144 44
7.2g A
144 7.2g
=
44 A
A=2.2g
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故D错误;
故选:C。
[例题6] (2023•巴南区模拟)甲醛(HCHO)是一种防腐剂,同时也是一种有毒物质。为
了测定溶液中甲醛的含量。某同学取含甲醛的溶液 10.0g,滴加过量酸性KMnO 溶液11.1g,
4
(反应的方程式为:4KMnO +5HCHO+6H SO ═2K SO +4MnSO +5CO ↑+11H O );整个过
4 2 4 2 4 4 2 2
程中无沉淀产生。将产生的气体用40.0g10%NaOH溶液恰好完全吸收,吸收后溶液的总质量为
41.1g;试计算。(已知MnSO 的相对分子质量为151)
4
(1)甲醛中碳、氢元素的质量比 。
(2)若用20%的溶液配制40.0g10%的NaOH,需要加入水的质量。
(3)所得溶液中MnSO 的质量分数。
4
【解答】解:(1)甲醛中碳、氢元素的质量比12:2=6:1;
40g×10%
(2)若用20%的溶液配制40.0g10%的NaOH,需要加入水的质量为:40g− =20g;
20%
答:需要加入水的质量为20g
(3)设所得溶液中MnSO 的质量分数为x。
4
4KMnO +5HCHO+6H SO ═2K SO +4MnSO +5CO ↑+11H O
4 2 4 2 4 4 2 2
604 220
x 41.1g﹣40.0g=1.1g
604 x
= 解得:x=3.02g
220 1.1g
3.02g
所得溶液中MnSO 的质量分数: ×100%=15.1%。
4 10.0g+11.1g−1.1g
答:所得溶液中MnSO 的质量分数为15.1%。
4
故答案为:(1)6:1;
(2)20g;
(3)15.1%。
难度:★★★ 建议时间:25分钟
1. (2021•广元模拟)取一定质量的碳酸钙,高温加热一段时间后,得到碳酸钙和氧化
钙的固体混合物,其中碳、氧元素质量比为 1:5,那么该固体混合物中碳酸钙和氧化钙的质
量比为( )
A.7:25 B.50:21 C.21:50 D.25:14
【解答】解:碳酸钙高温分解生成氧化钙和二氧化碳,反应后的碳元素全部存在于碳酸钙中,
碳酸钙中碳元素和氧元素的质量比为:12:(16×3)=3:12,假设碳元素的质量为3份质量,
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
则由碳、氧元素质量比为1:5=3:15可知,氧化钙中氧元素的质量为3份质量,因此碳酸钙的
12 16 21
质量为:3÷ =25,氧化钙的质量为:3÷ = ,故该固体混合物中碳酸钙和氧化钙的质量
100 56 2
21
比为:25: =50:21;
2
由以上计算可知,B符合题意
故选:B。
2. (2023•东莞市校级二模)高铁酸钾[K FeO ]能溶于水,是高效、多功能水处理剂.
2 4
K FeO 中铁元素的化合价为( )
2 4
A.﹣1 B.+2 C.+3 D.+6
【解答】解:钾元素显+1价,氧元素显﹣2价,设铁元素的化合价是x,根据在化合物中正负化
合价代数和为零,可得:(+1)×2+x+(﹣2)×4=0,则x=+6价。
故选:D。
3. (2023•双流区校级模拟)甲原子与乙原子的质量比为a:b,而乙原子与碳原子的质
量比为c:d,则甲原子的相对原子质量为( )
12ac bc 12bd ad
A. B. C. D.
bd 12ad ac 12bc
【解答】解:因为甲:乙=a:b,甲=(a•乙):b
又因 乙:碳原子=c:d,乙=(碳原子•c):d
甲=(a•c•碳原子):(b•d)
所以甲原子的相对原子质量为(12ac):(bd),
12ac
即
bd
故选:A。
4. (2023•临汾一模)氮元素对地球上的生命极其重要,它不仅是组成蛋白质必不可少
的元素,还是核酸等生命物质的重要成分。下列五种物质:NH 、N 、NO、X、HNO ,均含
3 2 3
有氮元素,且氮元素的化合价按照一定顺序排列,则物质X是( )
A.NaNO B.N O C.N O D.NO
3 2 2 5 2
【解答】解:已知氢元素的化合价为+1价,氧元素的化合价为﹣2价,根据化合价的原则(在
化合物中正、负化合价的代数和为零),则:NH 中氮元素的化合价为:﹣3价;N 中氮元素的
3 2
化合价为0;NO中氮元素的化合价为+2价;HNO 中氮元素的化合价为+5价。则X中氮元素的
3
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
化合价为+3或+4。
A、NaNO 中氮元素的化合价为:+5价,故A不符合题意。
3
B、N O中氮元素的化合价为:+1价,故B不符合题意;
2
C、N O 中氮元素的化合价为:+5价,故C不符合题意;
2 5
D、NO 中氮元素的化合价为:+4价,故D符合题意;
2
故选:D。
5. (2023•衡阳县模拟)在C H 、C H OH的混合物中,已知氧元素的质量分数为y,则
2 4 2 5
碳元素的质量分数为( )
3 8 6 9 3 9 6 8
A. (1− y) B. (1− y) C. (1− y) D. (1− y)
7 9 7 8 7 8 7 9
【解答】解:C H OH可以变形为C H •H O,所以C H 、C H OH可以视为C H 、H O组成的
2 5 2 4 2 2 4 2 5 2 4 2
18 y 9 y
混合物,因为氧元素的质量分数为y,故H O的质量分数为: = ,所以C H 的质量分
2 2 4
16 8
9 24 9 6 9
数为:(1− y),其中碳元素的质量分数为: (1− y)= (1− y);
8 28 8 7 8
故选:B。
6. (2023•古交市校级一模)笑气是人类最早应用于医疗的麻醉剂之一,如果长期过量
吸入笑气,就会对人体造成不可逆的伤害。笑气是氮的一种氧化物,该氧化物中氮元素的化合
价为+1,笑气的化学式是( )
A.N B.N O C.N O D.NO
2 2 2 4 2
【解答】解:笑气是氮的一种氧化物,该氧化物中氮元素的化合价为+1,氧元素的化合价为﹣2
价,化合价数值约到最简交叉写在元素右下角,其化学式为N O。
2
故选:B。
7. (2023•丰台区二模)如图是KNO 的溶解度曲线,下列说法正确的是( )
3
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.20℃时,向100g水中加入40gKNO ,得到140g溶液
3
B.40℃时,KNO 饱和溶液的溶质质量分数为63.9%
3
C.60℃时,KNO 饱和溶液中溶质与溶剂的质量比为11:10
3
D.将60℃的KNO 饱和溶液降温至40℃,溶液质量不变
3
【解答】解:A、20℃时,硝酸钾的溶解度为31.6g,20℃时,向100g水中加入40gKNO ,最多
3
能溶解31.6g,得到131.6g饱和溶液,故选项说法错误。
63.9g
B、40℃时,硝酸钾的溶解度为63.9g,KNO 饱和溶液的溶质质量分数为 ×100%
3 63.9g+100g
<63.9%,故选项说法错误。
C、60℃时,硝酸钾的溶解度为110g,60℃时,KNO 饱和溶液中溶质与溶剂的质量比为110g:
3
100g=11:10,故选项说法正确。
D、硝酸钾的溶解度随着温度的降低而减小,将60℃的KNO 饱和溶液降温至40℃,有晶体析
3
出,溶液质量减少,故选项说法错误。
故选:C。
8. (2023•民权县一模)固体硝酸钾、硝酸钠的溶解度曲线如图所示。下列说法正确的
是( )
A.在t ℃时,硝酸钾、硝酸钠溶液的溶质质量分数相等
1
B.硝酸钾、硝酸钠的溶液从t ℃降温至t ℃一定有晶体析出
2 1
C.t ℃时,向30 g硝酸钾的饱和溶液中加10 g水可得到20%的溶液
2
D.将t ℃时两固体的饱和溶液分别升温至t ℃,两溶液的溶质质量分数相等
1 2
【解答】解:A.在t ℃时,硝酸钾、硝酸钠的溶解度曲线相交于一点,即该温度下,硝酸钾、硝
1
酸钠的溶解度相等,但硝酸钾、硝酸钠溶液不一定是饱和溶液,所以溶质质量分数无法确定是
否相等,故A不正确;
B.硝酸钾、硝酸钠的溶液不一定饱和,所以从t ℃降温至t ℃不一定有晶体析出,故B不正确;
2 1
C.t ℃时,硝酸钾的溶解度为200g,向30 g硝酸钾的饱和溶液中加10 g水得到溶液的溶质质量
2
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
200g
30g× ×100%
分数为: 200g+100g 50%,故C不正确;
×100%=
30g+10g
D.t ℃时,硝酸钾、硝酸钠的溶解度曲线相交于一点,溶解度相等,溶质质量分数相等,将 t ℃
1 1
时两固体的饱和溶液分别升温至t ℃,两固体的溶解度增大,溶液由饱和变为不饱和溶液,溶液
2
的溶质质量分数不变,所以两溶液的溶质质量分数相等,故D正确。
故选:D。
9. (2023•南山区校级三模)t ℃时,将a、b两种固体物质各25g,分别加入盛有100g
1
水的烧杯中,充分搅拌后现象如图甲所示;升温到t ℃时(忽略水分蒸发),现象如图乙所示;
2
图丙是a、b两种固体物质在水中的溶解度曲线。下列说法正确的是( )
A.图丙中曲线N表示b物质的溶解度曲线
B.图甲中两烧杯内a、b溶液的溶质质量分数相等
C.图乙中烧杯内b溶液的溶质质量分数为25%
D.可用降温结晶的方法从饱和a溶液中得到固体a
【解答】解:A、结合图甲、图乙可知,b物质的溶解度随着温度升高而增大,故图丙中曲线M
表示b物质的溶解度曲线,则曲线N表示a物质的溶解度曲线,故A错误;
B、由图甲可知,t ℃时,a、b均是饱和饱和溶液,结合图丙可知,t ℃时a、b两物质溶解度相
1 1
等,故图甲中两烧杯内a、b溶液的溶质质量分数相等,故B正确;
25g
C、图乙中烧杯b内固体全部溶解,b溶液的溶质质量分数为 ×100%=20%,故C错
100g+25g
误;
D、a物质的溶解度随温度降低而增大,降低温度,a的溶解度增大,饱和溶液变成不饱和溶液,
故不能用降温结晶的方法从饱和a溶液中得到固体a,故D错误。
故选:B。
10. (2023•桐柏县三模)Mg、Al、Fe的固体混合物21.4g加入一定量的H SO 恰好完全
2 4
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
反应,反应后的溶液质量增加了21.2g,将反应后溶液蒸干得到固体的质量为( )
A.21.6g B.31.0g C.38.5g D.42.4g
【解答】解:Mg、Al、Fe的固体混合物21.4g加入一定量的硫酸恰好完全反应,反应后的溶液
质量增加了21.2g,则生成H 的质量为21.4g﹣21.2g=0.2g,根据反应前后元素的质量相等,产
2
生氢气中的氢元素的质量等于反应掉的硫酸中氢元素的质量,则硫酸中氢元素的质量为0.2g,
且硫酸中氢元素的质量与硫酸根离子的质量的质量比为2:96=1:48,则硫酸根离子的质量为:
0.2g×48=9.6g,将反应后溶液蒸发结晶、干燥,Mg、Al、Fe完全反应完后转化为MgSO 、Al
4 2
(SO ) 、FeSO ,故获得固体质量为9.6g+21.4g=31.0g。
4 3 4
故选:B。
11. (2023•东莞市二模)从微观上看,化学反应是微观粒子按一定的数目关系进行的。
某碳氢化合物(化学式为CxHy)在密闭容器内充分燃烧,生成二氧化碳和水。部分物质的分
子数随反应过程的变化如图所示。下列说法正确的是( )
A.该反应前后分子数目不变
B.t时刻,容器中O 和CO 的质量相等
2 2
C.该碳氢化合物的化学式为C H
3 8
D.该反应生成的二氧化碳和水的质量之比为22:9
【解答】解:由图可知,参加反应的有机物、氧气,生成的二氧化碳的分子个数比为:n:(6n
﹣n):3n=1:5:3,设化学方程式中水前面的化学计量数为m,则化学方程式为nC H +5nO
x y 2
点燃3nCO +mH O;根据质量守恒定律,化学反应前后,元素的种类不变,原子的种类、总个
2 2
¯
❑
数不变;根据氧原子个数守恒,反应物中有10n个氧原子,生成物二氧化碳中只含有6n个氧原
子,因此化学方程式中水前面的化学计量数为4n,即生成水分子个数为4n,故化学方程式为
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
点燃
C H +5O 3CO +4H O,根据质量守恒定律,则x=3,y=8,即有机物的化学式为C H ;
x y 2 2 2 3 8
¯
❑
A、由反应的化学方程式可知,反应前的分子个数发生变化,故错误;
B、t时刻,O 和CO 的分子数相等,质量不相等,故错误;
2 2
C、反应的氧原子个数是10n,生成的二氧化碳中的氧原子是6n,则生成的水分子中氧原子是
点燃
10n﹣6n=4n,该反应生成的水分子数目为 4n,由质量守恒定律可知,C H +5O
x y 2
¯
❑
3CO +4H O,即x=3,y=8,碳氢化合物的化学式是C H ,故正确;
2 2 3 8
D、该反应生成的二氧化碳和水的质量之比为:(3n×44):(4n×18)=11:6,故错误;
故选:C。
12. (2023•蕲春县模拟)氧化亚铜(Cu O)是鲜红色粉末状固体,可用作杀菌剂、陶瓷
2
和搪瓷的着色剂、红色玻璃染色剂等。现将Cu O和Cu的固体混合物6.8g放入烧杯中,加入
2
足量的稀硫酸,充分反应后,过滤、洗涤、干燥,得到 4.8g固体。(已知Cu O+H SO =
2 2 4
CuSO +Cu+H O)。则原混合物中的Cu O和Cu质量比为( )
4 2 2
A.9:8 B.17:12 C.1:1 D.9:4
【解答】解:设原混合物中的Cu O的质量为x,生成铜的质量为y,
2
Cu O+H SO =CuSO +Cu+H O,
2 2 4 4 2
144 64
x y
144 x
= ,
64 y
64x
y= ,
144
64x
根据题意有:6.8g﹣x+ =4.8g,
144
x=3.6g,
原混合物中的Cu的质量为:6.8g﹣3.6g=3.2g,
则原混合物中的Cu O和Cu质量比为:3.6g:3.2g=9:8,
2
故选:A。
13. (2023•天宁区校级模拟)“天宫课堂”中宇航员将维生素C泡腾片[含维生素C、柠
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
檬酸( C H O )和碳酸氢钠]塞入一个水球,水球里立即产生很多气泡,其中一个反应为:
6 8 7
C 6 H 8 O 7 +xNaHCO 3 ═Na x C 6 H 8﹣x O 7 +xH 2 O+xCO 2 ↑。为测定柠檬酸钠(Na x C 6 H 8﹣x O 7 )化学式中
的x,用4套相同装置加等量的水后,分别装入如表所示质量的柠檬酸和碳酸氢钠固体进行实
验测得该条件下数据如表,推测x的数值为( )
实验组别 柠檬酸/g 碳酸氢钠/g 气体体积/mL
1 1.92 0.84 224
2 1.92 1.68 448
3 1.92 2.52 672
4 1.92 3.36 672
A.4 B.3 C.2 D.1
【解答】解:由表格中的数据可知,加入0.84g碳酸氢钠产生气体的体积为224mL,加入1.68g
碳酸氢钠产生气体的体积为448mL,即每0.84g碳酸氢钠产生气体的体积为224mL,而加入
2.52g、3.36g碳酸氢钠产生气体的体积为672mL,说明在实验组别3中,1.92g柠檬酸和2.52g碳
酸氢钠恰好完全反应;
C 6 H 8 O 7 +xNaHCO 3 ═Na x C 6 H 8﹣x O 7 +xH 2 O+xCO 2 ↑
192 84x
1.92g 2.52g
192 1.92g
=
84x 2.52g
x=3
故选:B。
14. (2023•临沂一模)习近平总书记用“文明其精神,野蛮其体魄”来激励青少年多运
动,重视强身健体。因为运动时,身体可以产生多巴胺,让人心情舒畅,缓解焦虑,提高身体
免疫力。多巴胺的化学式为C H NO 。
8 11 2
(1)在多巴胺中,氮元素和氧元素的质量比为 (填最简整数比);
(2)多巴胺中碳元素的质量分数 (精确到0.1%)。
【解答】解:(1)在多巴胺中,氮元素和氧元素的质量比=14:(16×2)=7:16。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
12×8
(2)多巴胺中碳元素的质量分数= ×100%≈62.7%。
12×8+1×11+14+16×2
故答案为:(1)7:16;
(2)62.7%。
15. (2023•河西区一模)条形码的黏性主要来源于合成胶黏剂丙烯酸,化学式为
C H O 。计算:
3 4 2
(1)丙烯酸的相对分子质量为 ;
(2)丙烯酸中碳、氧元素的质量比为 (填最简比);
(3)丙烯酸中碳元素的质量分数为 ;
(4)3.6g丙烯酸中含有的碳元素的质量是 g。
【解答】解:(1)丙烯酸(C H O )的相对分子质量为12×3+1×4+16×2=72;故答案为:72;
3 4 2
(2)丙烯酸中碳元素与氧元素的质量比为(12×3):(16×2)=9:8,故答案为:9:8;
12×3
(3)丙烯酸中碳元素的质量分数为 ×100%=50%;故答案为:50%;
72
(4)3.6g丙烯酸中含有的碳元素的质量是3.6g×50%=1.8g;故答案为:1.8。
16. (2023•嘉禾县校级二模)山西老陈醋是中国四大名醋之一可促进胃液分泌,抑制血
糖升高,降低血脂。陈醋中含有乙酸(化学式CH COOH),如图是某品牌陈醋的部分标签。
3
(1)乙酸的相对分子质量为 。
(2)乙酸中氢、氧元素的质量比是 。
(3)一瓶陈醋中至少含有碳元素的质量是多少(写出计算过程)
【解答】解:(1)乙酸的相对分子质量为12×2+1×4+16×2=60;
故填:60;
(2)乙酸中氢、氧两种元素的质量比(1×4):(16×2)=1:8;
故填:1:8;
2×12
(3)一瓶陈醋中至少含有碳元素的质量是500mL×4g/100mL× ×100%=8g。
60
答:一瓶陈醋中至少含有碳元素的质量是8g。
故答案为:(1)60;(2)1:8;(3)8g。
17. (2023•魏县一模)在一定温度下,向100g水中依次加入一定质量的KCl固体,充分
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是 溶液(填“饱和”或“不饱和”)。
(2)实验③所得溶液中溶质的质量分数是 (写出计算过程)
(3)现有溶质质量分数为10%的KCl的溶液300g,若配制成溶质质量分数为3%的KCl的溶液,
问需要加水的质量是多少。(写出计算过程)
【解答】解:(1)饱和溶液是指一定温度下不能继续溶解某种溶质的溶液,还能继续溶解该溶
质的溶液是不饱和溶液。①能继续溶解这种溶质,所以是不饱和溶液;故答案为:不饱和;
(2)根据图示可知100g水中加入60g氯化钾所得溶液质量为140g,说明只溶解了40g,所以该
40g
温度下的溶解度是40g;实验③溶液的质量分数为 ×100%≈28.6%;故答案为:28.6%;
140g
(3)设需要加水的质量是x,根据题意可得:
300g×10%=(300g+x)×3%
解得:x=700g
答:需要加水的质量是700g。
18. (2023•邹平市二模)化学小组参与“铅蓄废电池中硫酸回收”的研学项目,回收时
需要测定电池废液中硫酸的质量分数。向装有50g废液的锥形瓶中加入质量分数为20%的氢氧
化钠溶液,并充分搅拌,利用温度传感器等电子设备采集信息并绘制成如图,请据图回答相关
问题。(杂质可溶但不参加反应)
(1)该反应是 (填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为 ℃。
(3)计算废液中硫酸的质量分数。(写出计算过程)
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:(1)由图像可知,溶液的温度升高,说明该反应是放热反应。
(2)该反应是放热反应,恰好完全反应时溶液温度最高,由图像可知,恰好完全反应时溶液的
温度为t ℃。
3
(3)设50g废液中硫酸的质量为x。
2NaOH+H SO =Na SO +2H O
2 4 2 4 2
80 98
40g×20% x
80 98
= 解得:x=9.8g
40g×20% x
9.8g
废液中硫酸的质量分数为: ×100%=19.6%
50g
答:废液中硫酸的质量分数19.6%。
故答案为:(1)放热;
(2)t ;
3
(3)19.6%。
19. (2023•唐山模拟)医学上常用过氧化氢溶液来清洗创口和局部抗菌,玲玲同学取
68.0g某医用过氧化氢溶液放入锥形瓶中,然后加入 2.0g二氧化锰,每隔一分钟观察并记录一
次锥形瓶及物质的质量(如表),直到实验结束。
时间/分钟 0 1 2 3 4 5
锥形瓶及物质质量/g 10 99.3 98.9 98.6 98.4 98.4
0
请计算:
(1)共生成氧气 g。
(2)过氧化氢溶液中溶质的质量分数。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【解答】解:(1)根据质量守恒定律,反应前后物质的总质量不变,则共生成氧气的质量为:
100g﹣98.4g=1.6g。
(2)设过氧化氢溶液中溶质的质量为x。
MnO
2H
2
O
2
22H
2
O+O
2
↑
¯
❑
68 32
x 1.6g
68 x
=
32 1.6g
x=3.4g
3.4g
则过氧化氢溶液中溶质的质量分数为: ×100%=5%。
68.0g
答:过氧化氢溶液中溶质的质量分数为5%。
20. (2023•重庆模拟)新冠疫情中常用84消毒液进行环境消毒,其主要成分是次氯酸钠
通电
(NaClO)。制备次氯酸钠的发生器中发生反应的总化学方程式为:NaCl+H O
2
¯
❑
NaClO+H ↑。现电解600g溶质的质量分数为26%的氯化钠溶液一段时间,溶液质量减少 4g
2
(假设不考虑其他副产物)。请计算:
(1)NaCl中氯元素的质量分数 (填“>”、“=”或“<”)NaClO中氯元素的质量
分数。
(2)电解所得溶液中次氯酸钠的质量分数。
(3)用于电解的600g26%的氯化钠溶液是通过在10%的氯化钠溶液中加入氯化钠固体的方式配
制的,计算需要加入NaCl固体的质量。(计算结果保留一位小数)
【解答】解:(1)NaCl和 NaClO中都是含有1个氯原子,但NaClO比NaCl多一个氧原子,
相对分子质量更大,所以NaCl中氯元素的质量分数>NaClO中氯元素的质量分数。
(2)根据质量守恒定律,氢气的质量为4g,
设生成的次氯酸钠的质量为x。
通电
NaCl+H O NaClO+H ↑
2 2
¯
❑
74.5 2
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
x 4g
74.5 x
=
2 4g
x=149g
149g
电解所得溶液中次氯酸钠的质量分数= ×100%=25%
600g−4g
答:电解所得溶液中次氯酸钠的质量分数25%。
(3)设需要加入NaCl固体的质量为y。
(600g﹣y)×10%+y=600g×26%
解得y≈106.7g。
18