文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
模块三 综合突破
速记一 中考必考化学方程式
01考情透视·目标导航
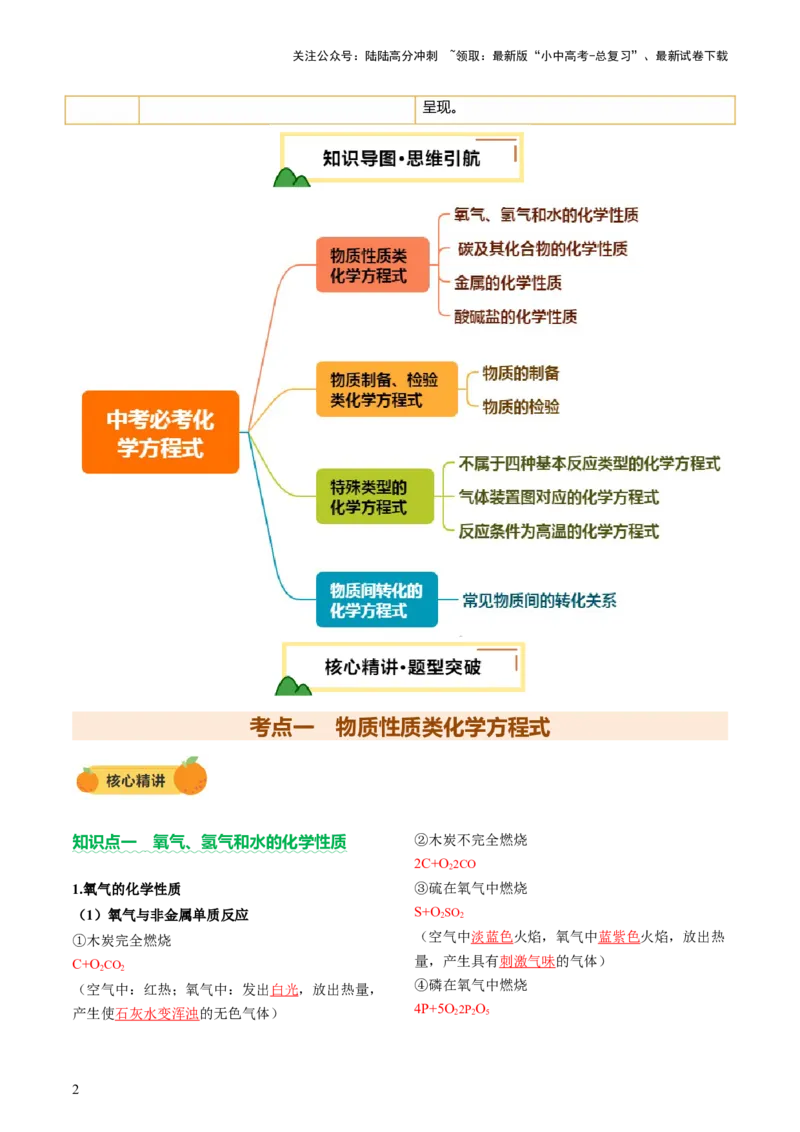
02知识导图·思维引航
03核心精讲·题型突破
考点一 物质性质类化学方程式
【核心精讲】
►知识点一 氧气、氢气和水的化学性质
►知识点二 碳及其化合物的化学性质
►知识点三 金属的化学性质
►知识点四 酸碱盐的化学性质
考点二 物质制备、检验类化学方程式
【核心精讲】
►知识点一 物质的制备
►知识点二 物质的检验
考点三 特殊类型的化学方程式
【核心精讲】
►知识点一 不属于四种基本反应类型的化学方程式
►知识点二 气体装置图对应的化学方程式
►知识点三 反应条件为高温的化学方程式
考点四 物质间转化的化学方程式
【核心精讲】
►知识点 常见物质间的转化关系
考点要求 课标要求 命题预测
化学方程式书写考点常以填空题的形式进行考
能根据实验事实用文字和符号描述、
化学方程 查,考查的命题点有:常见物质性质的化学方程
表示化学变化,并正确书写常见的化学方
式书写 式的书写、根据题目提供的新信息书写化学方程
程式。
式。化学方程式书写常以文字或图片结合的形式
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
呈现。
考点一 物质性质类化学方程式
知识点一 氧气、氢气和水的化学性质 ②木炭不完全燃烧
2C+O 2CO
2
1.氧气的化学性质 ③硫在氧气中燃烧
(1)氧气与非金属单质反应 S+O 2 SO 2
①木炭完全燃烧 (空气中淡蓝色火焰,氧气中蓝紫色火焰,放出热
C+O CO 量,产生具有刺激气味的气体)
2 2
④磷在氧气中燃烧
(空气中:红热;氧气中:发出白光,放出热量,
产生使石灰水变浑浊的无色气体) 4P+5O 2 2P 2 O 5
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(产生大量白烟,PO 污染空气) 浊)
2 5
⑤氢气在氧气中燃烧 ④葡萄糖在酶的作用下氧化
2H+O 2HO
2 2 2 C H O +6O 6CO +6H O
6 12 6 2 2 2
(产生淡蓝色火焰,罩在火焰上的干冷烧杯内壁有
2. 氢气的化学性质
小水株)
(1)氢气的可燃性(证明水由氢、氧元素组成)
(2)氧气与金属单质的反应
2H+O 2HO(点燃前必须验纯)
2 2 2
①铁丝在氧气中燃烧
(2)氢气的还原性
3Fe+2O Fe O
2 3 4
①氢气还原氧化铜
(氧气中剧烈燃烧,火星四射,放出大量热,生成
H+CuOCu+H O
2 2
黑色固体;瓶底留少量水或细沙,防止溅落的高温
②氢气还原氧化铁
熔化物炸裂瓶底)
3H
2
+Fe
2
O 32Fe+3H
2
O
②镁条在空气中燃烧
③一氧化碳还原四氧化三铁
2Mg+O 2MgO
2
4H
2
+Fe
3
O 43Fe+4H
2
O
(发出耀眼的白光,生成白色固体)
3.水的化学性质
③铜丝在氧气中加热
(1)电解水(证明水由氢、氧元素组成)
2Cu+O 22CuO
(红色固体变成黑色)
2H
2
O2H2 ↑+O
2
↑
(2)氧化钙和水反应(生石灰做干燥剂)
④铝在常温下与氧气反应
4Al+3O =2Al O CaO+H 2 O=Ca(OH) 2 (典型的放热反应)
2 2 3
(铝表面形成致密的氧化物薄膜、铝制品耐腐蚀的
(3)二氧化碳和水反应
原因) CO 2 +H 2 O=H 2 CO 3
⑤汞在空气中加热(拉瓦锡实验) (4)二氧化硫和水反应(酸雨的形成)
△ SO 2 +H 2 O=H 2 SO 3
2Hg +O 2 2HgO (5)三氧化硫和水反应
(3)氧气与化合物的反应 SO +H O=HSO
3 2 2 4
①一氧化碳燃烧 (6)水煤气的制取
2CO+O 2 2CO 2 C+H 2 O====CO+H 2
(产生蓝色火焰,罩在火焰上的烧杯内壁的澄清石
灰水变浑浊) 知识点 二 碳及其化合物的化学性质
②甲烷燃烧
CH+2O CO +2H O 1.碳的化学性质
4 2 2 2
(产生明亮的蓝色火焰,罩在火焰上的干冷烧杯内 (1)碳的可燃性
壁有小水株,罩在火焰上的烧杯内壁的澄清石灰水 充分燃烧:C+O — \s\up8(点燃)CO
2 — 2
变浑浊) 不充分燃烧:2C+O — \s\up8(点燃)2CO
2 —
③酒精(乙醇)燃烧 (2)碳的还原性
C 2 H 5 OH+3O 2 2CO 2 +3H 2 O ①木炭还原氧化铜
(产生蓝色火焰,罩在火焰上的干冷烧杯内壁有小
C+2CuO2Cu+CO2 ↑
水株,罩在火焰上的烧杯内壁的澄清石灰水变浑
②木炭还原氧化铁
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3C+2Fe 2 O 34Fe+3CO2 ↑ (2)乙醇燃烧
③木炭还原二氧化碳 C HOH+3O 2CO +3H O
2 5 2 2 2
C+CO 22CO (3)葡萄糖在酶的作用下氧化
(典型的吸热反应;CO既是氧化产物也是还原产
C H O +6O 6CO +6H O
6 12 6 2 2 2
物)
特别注意:木炭还原氧化物,反应条件均为高温。
知识点 三 金属的化学性质
2.二氧化碳的化学性质
(1)二氧化碳与水反应
1. 金属与氧气的反应
CO+H O=HCO
2 2 2 3 (1)铁丝在氧气中燃烧
(正常雨水pH小于7 的原因)
3Fe+2O Fe O
2 3 4
(2)二氧化碳与碱溶液反应
(2)镁条在氧气中燃烧
①二氧化碳与氢氧化钙反应
2Mg+O2MgO
2
CO+Ca(OH) =CaCO ↓+H O
2 2 3 2 (3)铜丝在氧气中加热
(用于检验 CO 气体;熟石灰变质的原因; 石灰浆
2 2Cu+O 22CuO
抹墙墙壁“出汗”的原因;石灰水保存鸡蛋的原
(4)铝在常温下与氧气反应
理;盛放石灰水的试剂瓶内壁有白膜的原因;)
4Al+3O =2Al O
2 2 3
②二氧化碳与氢氧化钠反应
2.常见金属与酸的反应
CO+2NaOH=NaCO+H O
2 2 3 2 (1)镁与稀盐酸反应
(用于吸收、除去 CO 气体;也是NaOH变质的原
2 Mg+2HCl=MgCl +H ↑
2 2
因)
(2)镁与稀硫酸反应
(3)二氧化碳与碳反应
Mg+HSO =MgSO +H ↑
2 4 4 2
C+CO 22CO (3)铝与稀盐酸反应
(4)植物的光合作用
2Al+6HCl=2AlCl +3H ↑
3 2
(4)铝与稀硫酸反应
6CO +6H O C H O +6O
2 2 6 12 6 2
2Al+3H SO =Al (SO )+3H ↑
2 4 2 4 3 2
3.一氧化碳的化学性质
(5)锌与稀盐酸反应
(1)一氧化碳的可燃性
Zn+2HCl=ZnCl+H ↑
2 2
2CO+O2CO
2 2
(6)锌与稀硫酸反应
(2)一氧化碳的还原性
Zn+H SO =ZnSO +H ↑
2 4 4 2
①一氧化碳还原氧化铜
(7)铁与稀盐酸反应
CO+CuOCu+ CO
2
Fe+2HCl=FeCl +H ↑
2 2
②一氧化碳还原氧化铁(高炉炼铁的反应原理)
(产生气泡,溶液由无色逐渐变为浅绿色)
3CO+Fe 2 O 32Fe+3CO2
(8)铁与稀硫酸反应
③一氧化碳还原四氧化三铁
Fe+H SO =FeSO +H ↑
4CO+Fe 3 O 43Fe+4CO2 2 4 4 2
(产生气泡,溶液由无色逐渐变为浅绿色)
4.有机物的化学性质
特别注意:铁与稀盐酸或稀硫酸反应,都生成亚铁
(1)甲烷燃烧
盐溶液。
CH+2O CO +2H O
4 2 2 2
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3. 常见金属与盐溶液的反应 见“知识点二 金属的化学性质”
(1)铝与硫酸铜溶液反应 2.常见金属氧化物与酸的反应
2Al+3CuSO=Al (SO )+3Cu (1)氧化铜与稀盐酸反应
4 2 4 3
(铝片表面覆盖一层红色物质,溶液由蓝色变为无 CuO+2HCl=CuCl
2
+H
2
O
色) (黑色固体消失,溶液由无色变为蓝色)
(2)铝和硝酸银溶液的反应 (2)氧化铜与稀硫酸反应
Al + 3AgNO Al (NO ) + 3Ag CuO+HSO =CuSO +H O
3 3 3 2 4 4 2
(铝片表面覆盖一层色银白色物质) (黑色固体消失,溶液由无色变为蓝色)
(3)锌与硝酸铜溶液反应 (3)氧化铁与稀盐酸反应(盐酸除铁锈)
Zn+ Cu(NO )=Zn(NO )+Cu Fe O+6HCl=2FeCl +3H O
3 2 3 2 2 3 3 2
(铝片表面覆盖一层红色物质,溶液由蓝色变为 (铁锈消失,溶液由无色变为黄色)
无色) (4)氧化铁与稀硫酸反应(硫酸除铁锈)
(4)锌与硫酸铜溶液反应 Fe O+3H SO =Fe (SO )+3H O
2 3 2 4 2 4 3 2
Zn +CuSO=ZnSO+Cu (铁锈消失,溶液由无色变为黄色)
4 4
(铝片表面覆盖一层红色物质,溶液由蓝色变为 3. 常见的酸碱中和反应
无色) (1)稀盐酸和氢氧化钠溶液反应
(5)锌与硫酸亚铁溶液反应 HCl+NaOH=NaCl+H O
2
Zn +FeSO =ZnSO+Fe (无明显现象,需借助酚酞判断反应是否发生或反
4 4
(锌片表面覆盖一层黑色物质,溶液由浅绿色变 应是否恰好完全进行)
为无色)
(2)稀硫酸和氢氧化钠溶液反应
(6)铜与硝酸银溶液反应 H 2 SO 4 +2NaOH=Na 2 SO 4 +2H 2 O
Cu+2AgNO =Cu(NO )+2Ag (无明显现象,需借助酚酞判断)
3 3 2
(3)稀盐酸和氢氧化钙溶液反应
(铜片表面覆盖一层色银白色物质,溶液由无色
变为蓝色) 2HCl+Ca(OH) 2 =CaCl 2 +2H 2 O
(无明显现象,需借助酚酞判断)
(7)铁与硫酸铜溶液反应
(4)稀硫酸和氢氧化钙溶液反应
(不能用铁制容器配制波尔多液的原因)
HSO +Ca(OH) =CaSO+2H O
Fe+CuSO=FeSO +Cu 2 4 2 4 2
4 4
(无明显现象,需借助酚酞判断)
(铁钉表面覆盖一层红色物质,溶液由蓝色变为
(5)稀盐酸和氢氧化铜反应
浅绿色)
2HCl+Cu(OH) =CuCl+2H O(蓝色固体消失,
(8)铁与硝酸银溶液反应 2 2 2
溶液由无色变为蓝色)
Fe+2AgNO =Fe(NO )+2Ag
3 3 2
(6)稀硫酸和氢氧化铜反应
(铁钉表面覆盖一层色银白色物质,溶液由无色
HSO + Cu(OH) =CuSO +2H O(蓝色固体消
变为浅绿色) 2 4 2 4 2
失,溶液由无色变为蓝色)
知识点 四 酸碱盐的化学性质 (7)稀盐酸和氢氧化铁反应
3HCl+Fe(OH) =FeCl+3HO(红褐色固体消失,
3 3 2
1.常见金属与酸的反应 溶液由无色变为黄色)
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(8)稀硫酸和氢氧化铁反应 SO+Ca(OH) =CaSO↓+H O
2 2 3 2
3HSO +2Fe (OH) =Fe (SO )+6H O(红褐色固 (用于燃煤脱硫处理)
2 4 3 2 4 3 2
体消失,溶液由无色变为黄色) (6)氢氧化钙与三氧化硫反应
4. 常见酸和盐的反应 SO+Ca(OH) =CaSO↓+H O
3 2 4 2
(1)盐酸和碳酸钠溶液反应 6. 常见碱和盐的反应
(水基型灭火器的原理) (1)氢氧化钠溶液和硫酸铜溶液反应
2HCl+Na 2 CO 3 =2NaCl+H 2 O+CO 2 ↑(产生大量气 2NaOH+CuSO 4 =Na 2 SO 4 +Cu(OH) 2 ↓(产生蓝色沉
泡;) 淀,溶液由蓝色变成无色)
(2)盐酸和碳酸氢钠溶液反应 (2)氢氧化钠溶液和氯化铁溶液反应
(小苏打治疗胃酸过多的原理) 3NaOH+FeCl =3NaCl +Fe(OH) ↓(产生红褐色
3 3
HCl+NaHCO 3 =NaCl+H 2 O+CO 2 ↑ 沉淀,溶液由黄色变成无色)
(产生大量气泡;等质量的NaHCO 比NaCO 与 (3)氢氧化钠溶液和氯化镁溶液反应(海水提取
3 2 3
盐酸反应产生气体又快又多) 镁)
(3)稀盐酸和硝酸银溶液反应 2NaOH+MgCl =2NaCl +Mg(OH) ↓
2 2
HCl+AgNO =AgCl↓+HNO (产生白色沉淀) (4)氢氧化钙溶液和硫酸铜溶液反应(配制波尔
3 3
(4)稀硫酸和碳酸钠溶液反应 多液)
HSO + Na CO =NaSO +H O+CO↑(产生大量 Ca(OH) +CuSO=CaSO+Cu(OH) ↓
2 4 2 3 2 4 2 2 2 4 4 2
气泡) (5)氢氧化钙溶液和碳酸钠溶液反应(制取少量
(5)稀硫酸和氯化钡溶液反应 氢氧化钠)
HSO +BaCl =BaSO↓+2HCl(产生白色沉淀) Ca(OH) +NaCO=2NaOH+CaCO ↓
2 4 2 4 2 2 3 3
(6)稀硫酸和硝酸钡溶液反应 (6)氢氧化钡溶液和硫酸钠溶液反应
HSO +Ba(NO)=BaSO↓+2HNO (产生白色沉 Ba(OH) +Na SO =2NaOH+ BaSO ↓
2 4 3 2 4 3 2 2 4 4
淀) 7. 常见盐和金属的反应
5. 常见碱和非金属氧化物的反应 见“知识点三 金属的化学性质”
(1)氢氧化钠与二氧化碳反应 8. 常见盐和盐的反应
CO+2NaOH=NaCO+H O (1)氯化钠溶液和硝酸银溶液反应
2 2 3 2
(用于除去、吸收二氧化碳;氢氧化钠变质的原 NaCl+AgNO =AgCl↓+NaNO
3 3
因;) (2)氯化钙溶液和碳酸钠溶液反应
(2)氢氧化钠与二氧化硫反应 CaCl +Na CO=CaCO ↓+2NaCl
2 2 3 3
SO 2 +2NaOH=Na 2 SO 3 +H 2 O (3)氯化钙溶液和碳酸钾溶液反应
(用于工厂吸收烟气中的二氧化硫) CaCl +KCO=CaCO ↓+2KCl
2 2 3 3
(3)氢氧化钠与三氧化硫反应
(4)氯化钡溶液和碳酸钠溶液反应
SO 3 +2NaOH=Na 2 SO 4 +H 2 O BaCl +Na CO=BaCO ↓+2NaCl
2 2 3 3
(4)氢氧化钙与二氧化碳反应
(5)氯化钡溶液和硫酸钠溶液反应
CO 2 +Ca(OH) 2 =CaCO 3 ↓+H 2 O BaCl + Na SO =BaSO↓+2NaCl
2 2 4 4
(用于检验二氧化碳;氢氧化钙变质的原因;)
(6)氯化钡溶液和硫酸铜溶液反应
(5)氢氧化钙与二氧化硫反应
BaCl +CuSO =BaSO↓+CuCl
2 4 4 2
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
9.盐类的分解反应 (2)碳酸氢钠分解
(1)碳酸钙分解(高温煅烧石灰石) 2NaHCO Na CO+H O+CO↑
3 2 3 2 2
CaCO 3CaO+CO2 ↑ (3)碳酸氢铵分解
NHHCO NH↑+H O+CO↑
4 3 3 2 2
考点二 物质制备、检验类化学方程式
知识点一 物质的制备 2.检验碳酸根离子(用稀盐酸和澄清石灰水检
验)
1.氧气的实验室制取
以碳酸钠(或碳酸氢钠)为例:
(1)高锰酸钾分解制取氧气
2HCl+Na CO = 2NaCl+H O+CO↑ ,
2KMnO KMnO +MnO+O ↑ 2 3 2 2
4 2 4 2 2
CO+Ca(OH) =CaCO ↓+H O
(2)过氧化氢分解制取氧气 2 2 3 2
( HCl+NaHCO = NaCl+H O+CO↑ ,
2H 2 O 22H2 O+O 2 ↑ 3 2 2
CO+Ca(OH) =CaCO ↓+H O)
2.二氧化碳的制取 2 2 3 2
3.检验氢氧化钠是否变质
(1)实验室制取二氧化碳
(1)加入过量的酸,观察是否产生气泡
CaCO +2HCl=CaCl+H O+CO↑
3 2 2 2
①加稀盐酸2HCl+Na CO=2NaCl+H O+CO↑
(2)工业制取二氧化碳(高温煅烧石灰石) 2 3 2 2
②加稀硫酸HSO +Na CO=NaSO +H O+CO↑
CaCO 3CaO+CO2 ↑ 2 4 2 3 2 4 2 2
(2)加入碱溶液,观察是否产生白色沉淀
3.实验室制取氢气
① 加 氢 氧 化 钙 Ca(OH) +Na CO =
Zn+HSO =ZnSO+H ↑ 2 2 3
2 4 4 2
2NaOH+CaCO ↓
4.其他物质的制备 3
② 加 氢 氧 化 钡 Ba(OH) +Na CO =
(1)氢氧化钙的制备(氧化钙和水反应) 2 2 3
2NaOH+BaCO↓
CaO+H O=Ca(OH) 3
2 2
(3)加入钡盐溶液或钙盐溶液,观察是否产生白
(2)氢氧化钠的制备(碳酸钠和氢氧化钙反应)
色沉淀
Ca(OH) +Na CO = 2NaOH+CaCO ↓
2 2 3 3
①加氯化钙CaCl+Na CO=2NaCl+CaCO ↓
2 2 3 3
知识点二 物质的检验
②加氯化钡BaCl+Na CO=2NaCl+BaCO↓
2 2 3 3
1.检验二氧化碳(用澄清石灰水检验)
③加硝酸钙Ca(NO )+Na CO=2NaNO +CaCO ↓
3 2 2 3 3 3
CO+Ca(OH) =CaCO ↓+H O
2 2 3 2 ④加硝酸钡Ba(NO )+Na CO=2NaNO +BaCO↓
3 2 2 3 3 3
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点三 特殊类型的化学方程式
知识点 一 不属于四种基本反应类型的化学 6CO 2 +6H 2 OC6 H 12 O 6 +6O 2
知识点 二 气体装置图对应的化学方程式
方程式
1.CO与金属氧化物的反应
(1)一氧化碳还原氧化铜
CO+CuOCu+ CO
2
(2)一氧化碳还原氧化铁
3CO+Fe 2 O 32Fe+3CO2 (1)实验室用装置A制氧气
(2)一氧化碳还原四氧化三铁 2KMnO KMnO +MnO+O ↑
4 2 4 2 2
4CO+Fe 3 O 43Fe+4CO2 (2)实验室用装置B制氧气
2.非金属氧化物与碱的反应 2H 2 O 22H2 O+O 2 ↑
(1)氢氧化钠与二氧化碳反应 (3)实验室用装置B制二氧化碳
CO 2 +2NaOH=Na 2 CO 3 +H 2 O CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2 ↑
(2)氢氧化钠与二氧化硫反应 (4)实验室用装置B制氢气
SO+2NaOH=NaSO+H O Zn+H SO =ZnSO+H ↑
2 2 3 2 2 4 4 2
(3)氢氧化钠与三氧化硫反应 (5)实验室用装置B和C组合制取气体
SO 3 +2NaOH=Na 2 SO 4 +H 2 O 2H 2 O 22H2 O+O 2 ↑
(4)氢氧化钙与二氧化碳反应 CaCO +2HCl=CaCl +H O+CO↑
3 2 2 2
CO+Ca(OH) =CaCO ↓+H O (6)实验室用装置B和D组合制取气体
2 2 3 2
(5)氢氧化钙与二氧化硫反应 Zn+H SO =ZnSO+H ↑
2 4 4 2
SO+Ca(OH) =CaSO↓+H O (7)实验室用装置B和E组合制取气体
2 2 3 2
(6)氢氧化钙与三氧化硫反应 2H 2 O 22H2 O+O 2 ↑
SO+Ca(OH) =CaSO↓+H O Zn+H 2 SO 4 =ZnSO 4 +H 2 ↑
3 2 4 2
知识点三 反应条件为高温的化学方程式
3.有机物与氧气的反应
1.单质碳参加的氧化还原反应
(1)甲烷在氧气中燃烧
(1)木炭还原氧化铜
CH+2O CO +2H O
4 2 2 2
(2)乙醇在氧气中加热
C+2CuO2Cu+CO2 ↑
(2)木炭还原氧化铁
C HOH+3O 2CO +3H O
2 5 2 2 2
(3)葡萄糖的氧化 3C+2Fe 2 O 34Fe+3CO2 ↑
(3)木炭还原二氧化碳
C H O +6O 6CO +6H O
6 12 6 2 2 2
C+CO 22CO
4.光合作用
2.铁的氧化物参加的氧化还原反应
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)氢气还原氧化铁、四氧化三铁 2C+Fe
3
O 43Fe+2CO
2
↑
3H
2
+Fe
2
O 32Fe+3H
2
O、 (5)一氧化碳还原氧化铁
(2)氢气还原四氧化三铁 3CO+Fe 2 O 32Fe+3CO2
4H
2
+Fe
3
O 43Fe+4H
2
O (6)一氧化碳四氧化三铁
(3)木炭还原氧化铁 4CO+Fe 3 O 43Fe+4CO2
3C+2Fe 2 O 34Fe+3CO2 ↑ 3.高温煅烧石灰石
(4)木炭还原四氧化三铁 CaCO 3CaO+CO2 ↑
考点四 物质间转化的化学方程式
知识点 常见物质间的转化关系 ① CO 2 +2NaOH=Na 2 CO 3 +H 2 O
1. 氧三角 ② Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑(合理即可)
③ CO+Ca(OH) =CaCO ↓+H O
2 2 3 2
④ CaCO +2HCl = CaCl +H O+CO↑ 或
3 2 2 2
CaCO 3CaO+CO2 ↑
⑤ Ca(OH) +Na CO=2NaOH+CaCO ↓
2 2 3 3
4. 钙三角
①2H 2 O 22H2 O+O 2 ↑
②2H
2
O2H2 ↑+O
2
↑
③2H+O 2HO(合理即可)
2 2 2
2. 碳三角1
①CaCO 3CaO+CO2 ↑
② Ca(OH) +Na CO = 2NaOH+CaCO ↓ 或
2 2 3 3
CO+Ca(OH) =CaCO ↓+H O(合理即可)
2 2 3 2
④ CaO+H O=Ca(OH)
2 2
①2C+O 2CO 5. 钠三角
2
② C+O CO
2 2
③ 2CO+O2CO (合理即可)
2 2
④CO
2
+C2CO
3. 碳三角2
①:HCl+NaOH=NaCl+H O(合理即可)
2
②:NaCO+2HCl=2NaCl+H O+CO↑(合理即可)
2 3 2 2
③:CO+2NaOH=NaCO+H O(合理即可)
2 2 3 2
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
④:Ca(OH) +Na CO =2NaOH+CaCO ↓(合理即
2 2 3 3
可)
6. 铜三角
① 2Cu+O 22CuO
②Fe+CuSO=FeSO +Cu
4 4
③ CuO+HSO =CuSO +H O
2 4 4 2
④ CO+CuOCu+CO2 (合理即可)
7.其他
① CaO+H O=Ca(OH)
2 2
② NaOH + HCl=NaCl+H O(合理即可)
2
③ Ca(OH) +Na CO =2NaOH+CaCO ↓(合理即
2 2 3 3
可)
10