文档内容
7 热重分析判断物质成分
方法思路
1.设晶体为1 mol,其质量为m。
2.失重一般是先失水,再失非金属氧化物。
3.计算每步固体剩余的质量(m )
余
×100%=固体残留率。
4.晶体中金属质量不再减少,仍在m 中。
余
5.失重最后一般为金属氧化物,由质量守恒得m ,由n ∶n ,即可求出失重后物质的
氧 金属 氧
化学式。
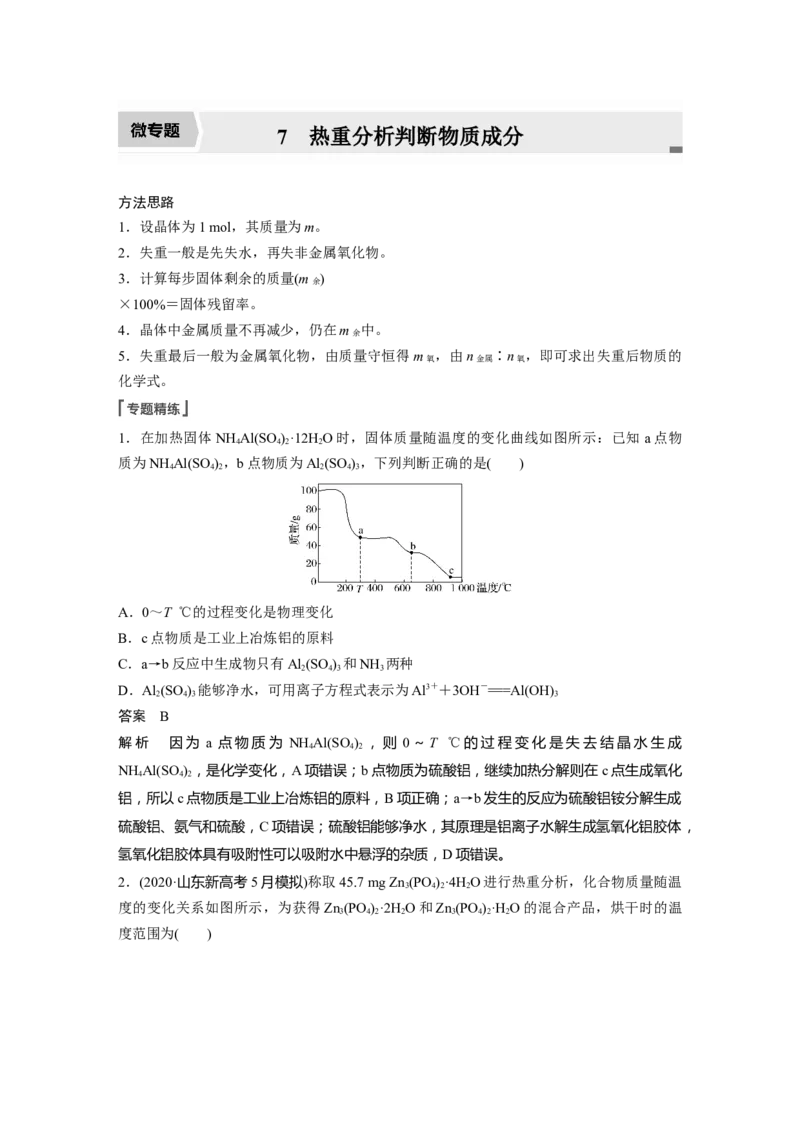
1.在加热固体NH Al(SO )·12H O时,固体质量随温度的变化曲线如图所示:已知 a点物
4 4 2 2
质为NH Al(SO ),b点物质为Al (SO ),下列判断正确的是( )
4 4 2 2 4 3
A.0~T ℃的过程变化是物理变化
B.c点物质是工业上冶炼铝的原料
C.a→b反应中生成物只有Al (SO ) 和NH 两种
2 4 3 3
D.Al (SO ) 能够净水,可用离子方程式表示为Al3++3OH-===Al(OH)
2 4 3 3
答案 B
解析 因为 a 点物质为 NH Al(SO ) ,则 0~T ℃的过程变化是失去结晶水生成
4 4 2
NH Al(SO ) ,是化学变化,A项错误;b点物质为硫酸铝,继续加热分解则在c点生成氧化
4 4 2
铝,所以c点物质是工业上冶炼铝的原料,B项正确;a→b发生的反应为硫酸铝铵分解生成
硫酸铝、氨气和硫酸,C项错误;硫酸铝能够净水,其原理是铝离子水解生成氢氧化铝胶体,
氢氧化铝胶体具有吸附性可以吸附水中悬浮的杂质,D项错误。
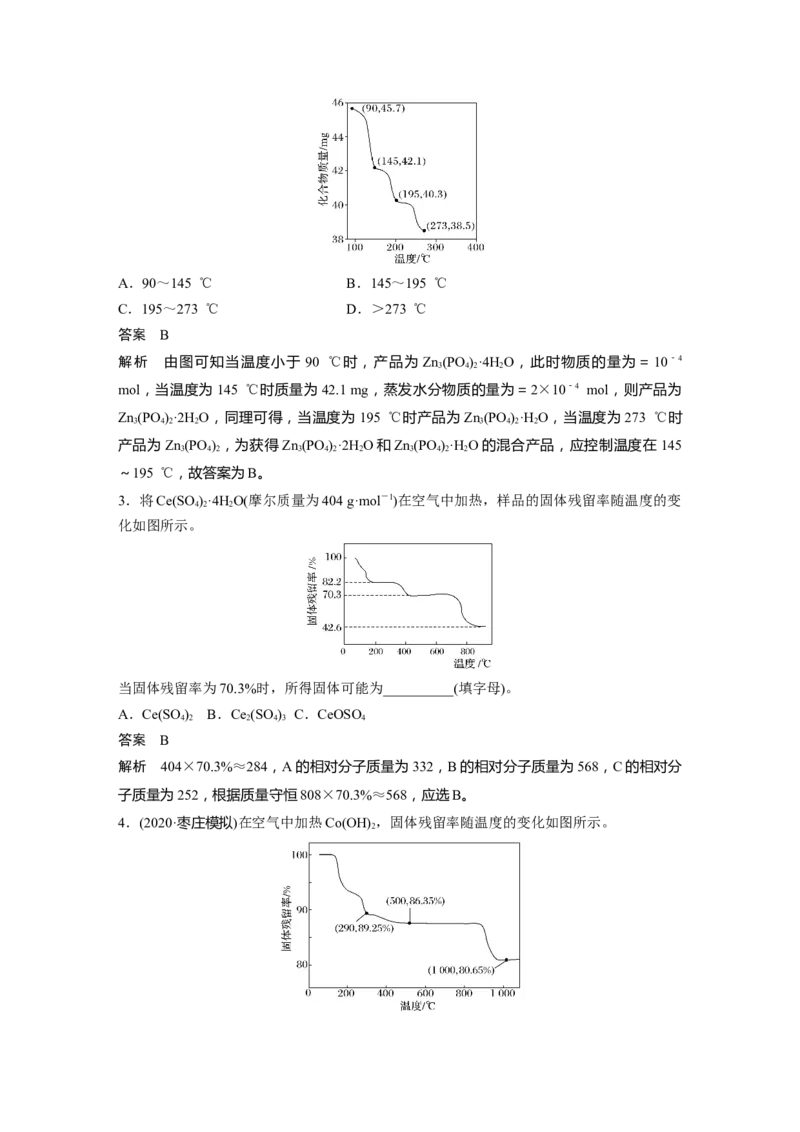
2.(2020·山东新高考5月模拟)称取45.7 mg Zn (PO )·4H O进行热重分析,化合物质量随温
3 4 2 2
度的变化关系如图所示,为获得Zn(PO )·2H O和Zn(PO )·H O的混合产品,烘干时的温
3 4 2 2 3 4 2 2
度范围为( )A.90~145 ℃ B.145~195 ℃
C.195~273 ℃ D.>273 ℃
答案 B
解析 由图可知当温度小于 90 ℃时,产品为 Zn(PO )·4H O,此时物质的量为=10-4
3 4 2 2
mol,当温度为145 ℃时质量为42.1 mg,蒸发水分物质的量为=2×10-4 mol,则产品为
Zn(PO )·2H O,同理可得,当温度为195 ℃时产品为Zn(PO )·H O,当温度为273 ℃时
3 4 2 2 3 4 2 2
产品为Zn(PO ) ,为获得Zn(PO )·2H O和Zn(PO )·H O的混合产品,应控制温度在 145
3 4 2 3 4 2 2 3 4 2 2
~195 ℃,故答案为B。
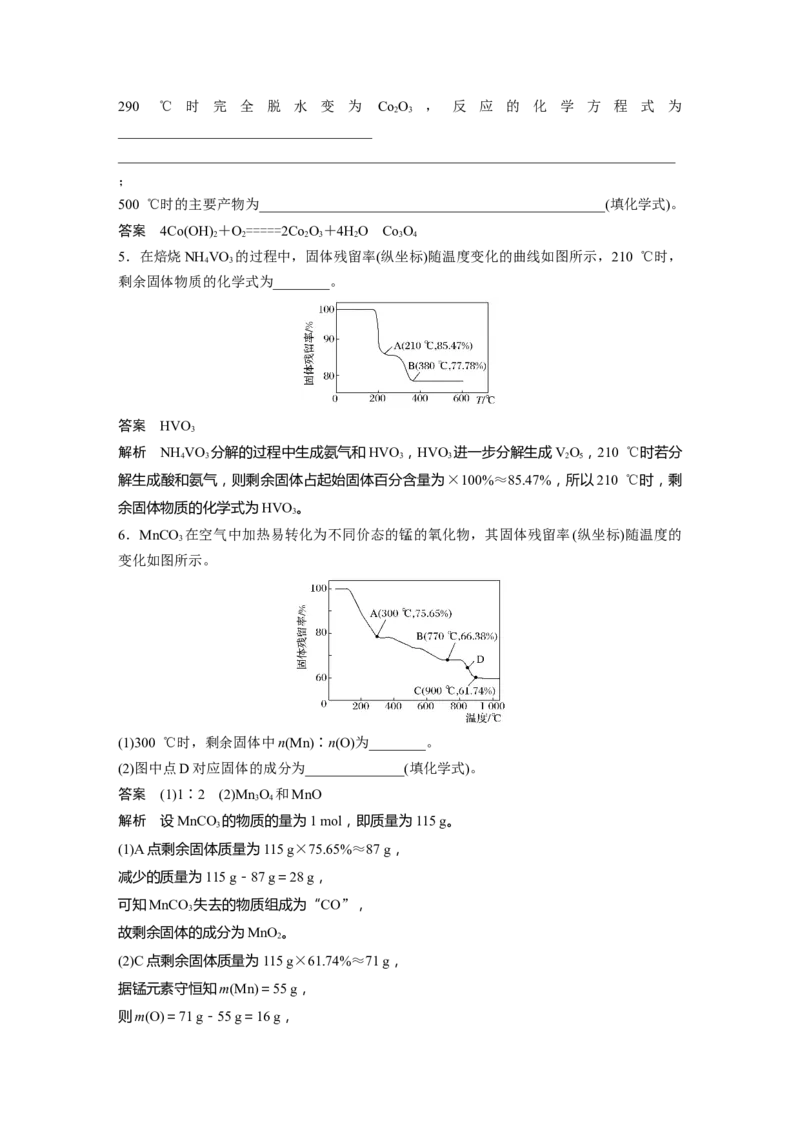
3.将Ce(SO)·4H O(摩尔质量为404 g·mol-1)在空气中加热,样品的固体残留率随温度的变
4 2 2
化如图所示。
当固体残留率为70.3%时,所得固体可能为__________(填字母)。
A.Ce(SO) B.Ce (SO ) C.CeOSO
4 2 2 4 3 4
答案 B
解析 404×70.3%≈284,A的相对分子质量为332,B的相对分子质量为568,C的相对分
子质量为252,根据质量守恒808×70.3%≈568,应选B。
4.(2020·枣庄模拟)在空气中加热Co(OH) ,固体残留率随温度的变化如图所示。
2290 ℃ 时 完 全 脱 水 变 为 Co O , 反 应 的 化 学 方 程 式 为
2 3
____________________________________
_______________________________________________________________________________
;
500 ℃时的主要产物为_________________________________________________(填化学式)。
答案 4Co(OH) +O=====2Co O+4HO Co O
2 2 2 3 2 3 4
5.在焙烧NH VO 的过程中,固体残留率(纵坐标)随温度变化的曲线如图所示,210 ℃时,
4 3
剩余固体物质的化学式为________。
答案 HVO
3
解析 NH VO 分解的过程中生成氨气和HVO,HVO 进一步分解生成VO,210 ℃时若分
4 3 3 3 2 5
解生成酸和氨气,则剩余固体占起始固体百分含量为×100%≈85.47%,所以210 ℃时,剩
余固体物质的化学式为HVO。
3
6.MnCO 在空气中加热易转化为不同价态的锰的氧化物,其固体残留率(纵坐标)随温度的
3
变化如图所示。
(1)300 ℃时,剩余固体中n(Mn)∶n(O)为________。
(2)图中点D对应固体的成分为______________(填化学式)。
答案 (1)1∶2 (2)Mn O 和MnO
3 4
解析 设MnCO 的物质的量为1 mol,即质量为115 g。
3
(1)A点剩余固体质量为115 g×75.65%≈87 g,
减少的质量为115 g-87 g=28 g,
可知MnCO 失去的物质组成为“CO”,
3
故剩余固体的成分为MnO 。
2
(2)C点剩余固体质量为115 g×61.74%≈71 g,
据锰元素守恒知m(Mn)=55 g,
则m(O)=71 g-55 g=16 g,则n(Mn)∶n(O)=∶=1∶1,
故剩余固体的成分为MnO,
同理,B点剩余固体质量为115 g×66.38%≈76 g,
因m(Mn)=55 g,则m(O)=76 g-55 g=21 g,
则n(Mn)∶n(O)=∶≈3∶4,
故剩余固体的成分为MnO,
3 4
因D点介于B、C之间,故D点对应固体的成分为MnO 与MnO的混合物。
3 4