文档内容
13 绿色化学与环境保护
一、环境污染及其防治
1.环境污染
(1)大气污染问题
大气污染是指由空气中的颗粒物、硫的氧化物(SO 、SO )、氮氧化物(NO)、CO、碳氢化合
2 3 x
物、氟氯代烃等造成的污染(其中SO 、NO 主要来源于化石燃料的大量使用)。大气污染的
2 x
具体表现主要有:形成酸雨、酸雾;臭氧层空洞;光化学烟雾;室内空气污染(指家用燃料
的燃烧、烹调、吸烟产生的CO、CO 、NO、NO 、SO 等,各种建筑材料和装饰材料释放
2 2 2
出的甲醛、苯等有机物造成的污染等;其中CO与血红蛋白作用会使血液失去输氧能力,导
致CO中毒)。
(2)水体污染
指过量有害物质进入水中造成的污染。导致水体污染的物质主要有两大类,一类是重金属污
染,如重金属Hg、Cd、Pb、Cr等进入水中形成的污染,这些重金属主要来自于化工、冶金、
电子、电镀等排放的工业废水。另一类是植物营养物质污染:水中高浓度的 N、P等植物营
养物质,导致水体富营养化而形成的污染。它主要是由进入水中腐烂的含蛋白质的物质、含
磷洗涤剂及大量使用的磷肥造成的。
(3)固体废弃物造成的污染
主要是指生活垃圾、工业废料随意堆放造成的污染。目前最引人注意的是由塑料制品造成的
白色污染及废旧电池造成的重金属污染。垃圾污染范围广泛,对环境及生物的不良影响途径
多样。
2.环境保护的措施
(1)工业废气携带颗粒物的回收利用。
(2)工业、生活污水经处理达标后排放,限制使用含磷洗涤剂。
(3)回收、限制难降解塑料,研制可降解塑料。
二、绿色化学
1.绿色化学有关概念
(1)核心:利用化学原理从源头上减少和消除工业生产对环境造成的污染。又称为“环境无
害化学”“环境友好化学”“清洁化学”。绿色化学的理想在于不再使用有毒有害的物质,
不再产生废物,不再处理废物,这是一门从源头上减少或消除污染的化学。
(2)绿色化学的研究主要是围绕化学反应、原料、催化剂、溶剂和产品的绿色化开展的,因
此化学反应及其产物具有以下特征:
①采用无毒、无害的原料;
②在无毒、无害的条件(包括催化剂、溶剂)下进行;
③产品应该是环境友好的;④具有“原子经济性”,即反应具有高选择性、极少副产物,甚至实现“零排放”。此外,
它还应当满足“物美价廉”的传统标准。
2.原子经济性
美国著名有机化学家B.M.Trost在1991年首先提出“原子经济性”的概念:认为高效的有机
合成应最大限度地利用原料分子的每一个原子,使之结合到目标分子中(如完全的加成反应:
A+B―→C),达到零排放。原子经济性可用原子利用率来衡量,其定义可表示为原子利用
率=×100%×100%。原子经济性的反应有两个显著优点:一是最大限度地利用了原料,二
是最大限度地减少了废物的排放。
1.(2019·石家庄质检)某研究小组采用如图所示电解法处理石油炼制过程中产生的大量HS
2
废气的工艺流程。该方法对HS的吸收率达99%以上,并可制取H 和S。下列说法正确的
2 2
是( )
A.吸收HS的离子方程式为Fe3++HS===Fe2++S↓+2H+
2 2
B.电解过程中的阳极反应主要为2Cl--2e-===Cl↑
2
C.该工艺流程体现绿色化学思想
D.实验室可用点燃充分燃烧的方法消除HS对环境的污染
2
答案 C
解析 A项,电荷不守恒;B项,由循环箭头可知,阳极电极反应为Fe2+-e-===Fe3+;D
项,HS完全燃烧的产物SO 仍是大气污染物。
2 2
2.食品、大气、工业尾气中SO 均需严格检测或转化吸收。下列有关SO 的检测或吸收方
2 2
法正确的是( )
A.滴定法:用酸性KMnO 溶液滴定葡萄酒试样以测定葡萄酒中SO 的浓度
4 2
B.沉淀法:用Ba(OH) 溶液沉淀SO ,然后将沉淀在空气中洗涤、过滤、干燥、称重以测
2 2
定大气中SO 的浓度
2
C.氨酸法:用氨水吸收尾气中的SO 后再将吸收液与硫酸反应,将富集后的SO 循环使用
2 2
D.石灰—石膏法:常温下用石灰石吸收尾气中的SO 得到CaSO ,再经氧化可用于生产石
2 3
膏
答案 C
解析 A项,葡萄酒中的乙醇能被酸性高锰酸钾溶液氧化,对 SO 的检测有干扰;B项,大
2
气中的CO 能与Ba(OH) 溶液形成沉淀,对SO 的检测有干扰;C项,氨水吸收SO 生成
2 2 2 2
(NH )SO 或NH HSO ,(NH )SO 或NH HSO 与硫酸反应能产生SO ,SO 可以循环使用;
4 2 3 4 3 4 2 3 4 3 2 2
D项,常温下石灰石不与SO 反应,不能吸收尾气中的SO 。
2 2
3.工业上常采用生物硝化法将NH转化为NO来处理氨氮废水,工作流程如图,下列说法错误的是( )
A.生物硝化法处理废水,会导致水体pH逐渐下降:NH+2O===NO+2H++HO
2 2
B.长期过量使用NH Cl等铵态化肥,易导致土壤酸化,水体富营养化
4
C.检验NH所需的试剂是浓NaOH溶液、湿润的蓝色石蕊试纸
D.微生物保持活性的pH范围为7~9,可以加入石灰石来调节水体的pH
答案 C
解析 NH Cl水解呈酸性,长期过量使用会导致土壤酸化,也会导致水体富营养化,B项正
4
确;检验NH应使用红色石蕊试纸,C项错误;生物硝化法处理废水会使水体呈酸性,可以
加入石灰石与H+反应来调节水体的pH,D项正确。
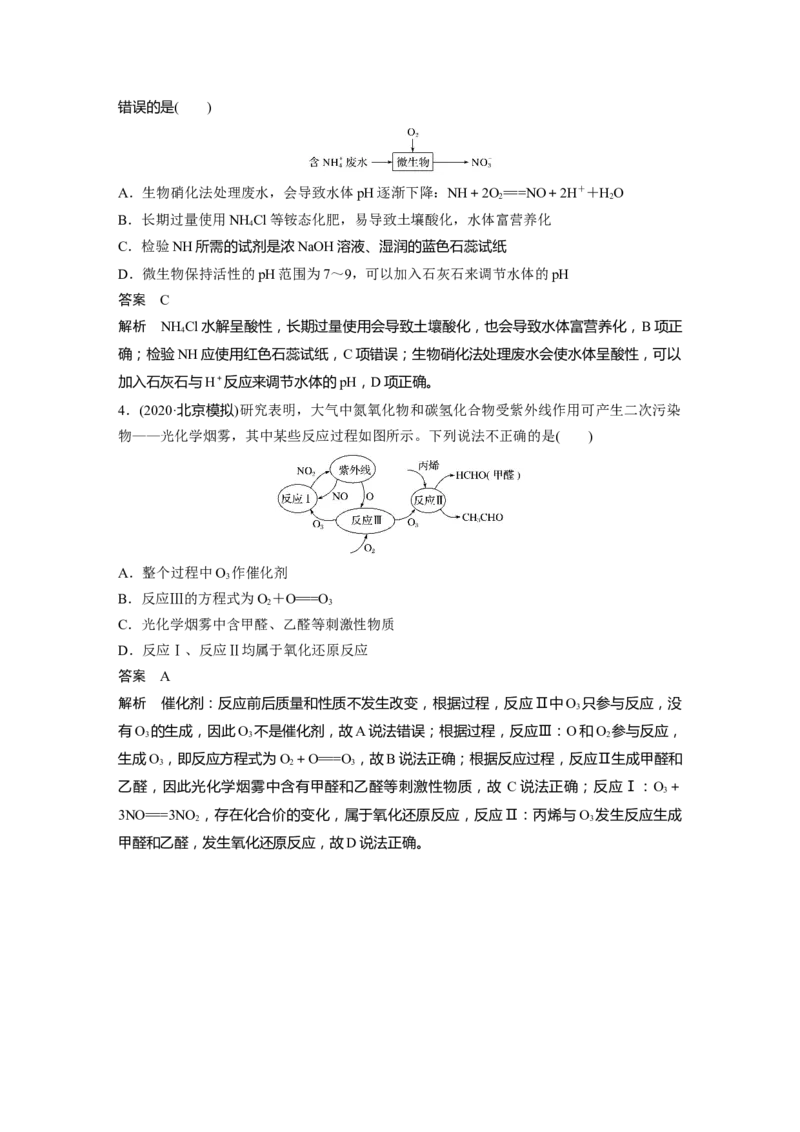
4.(2020·北京模拟)研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染
物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是( )
A.整个过程中O 作催化剂
3
B.反应Ⅲ的方程式为O+O===O
2 3
C.光化学烟雾中含甲醛、乙醛等刺激性物质
D.反应Ⅰ、反应Ⅱ均属于氧化还原反应
答案 A
解析 催化剂:反应前后质量和性质不发生改变,根据过程,反应Ⅱ中O 只参与反应,没
3
有O 的生成,因此O 不是催化剂,故A说法错误;根据过程,反应Ⅲ:O和O 参与反应,
3 3 2
生成O ,即反应方程式为O +O===O ,故B说法正确;根据反应过程,反应Ⅱ生成甲醛和
3 2 3
乙醛,因此光化学烟雾中含有甲醛和乙醛等刺激性物质,故 C说法正确;反应Ⅰ:O +
3
3NO===3NO ,存在化合价的变化,属于氧化还原反应,反应Ⅱ:丙烯与O 发生反应生成
2 3
甲醛和乙醛,发生氧化还原反应,故D说法正确。