文档内容
特色练 14 反应历程、机理图的分析应用
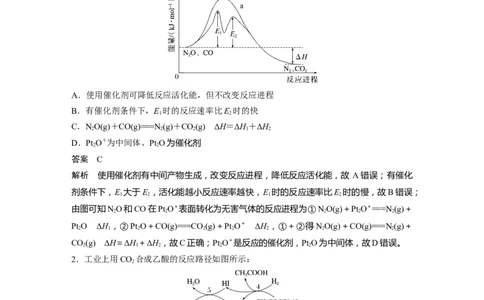
1.CO与NO气体均会造成环境污染,研究表明二者可在Pt O+表面转化为无害气体,其反
2 2
应进程及能量变化过程如图所示。下列说法正确的是( )
A.使用催化剂可降低反应活化能,但不改变反应进程
B.有催化剂条件下,E 时的反应速率比E 时的快
1 2
C.NO(g)+CO(g)===N(g)+CO(g) ΔH=ΔH+ΔH
2 2 2 1 2
D.Pt O+为中间体、Pt O为催化剂
2 2
答案 C
解析 使用催化剂有中间产物生成,改变反应进程,降低反应活化能,故 A错误;有催化
剂条件下,E 大于E ,活化能越小反应速率越快,E 时的反应速率比E 时的慢,故B错误;
1 2 1 2
由图可知NO和CO在Pt O+表面转化为无害气体的反应进程为①NO(g)+Pt O+===N(g)+
2 2 2 2 2
Pt O ΔH ,②Pt O+CO(g)===CO(g)+Pt O+ ΔH ,①+②得NO(g)+CO(g)===N(g)+
2 1 2 2 2 2 2 2
CO(g) ΔH=ΔH+ΔH,故C正确;Pt O+是反应的催化剂,Pt O为中间体,故D错误。
2 1 2 2 2
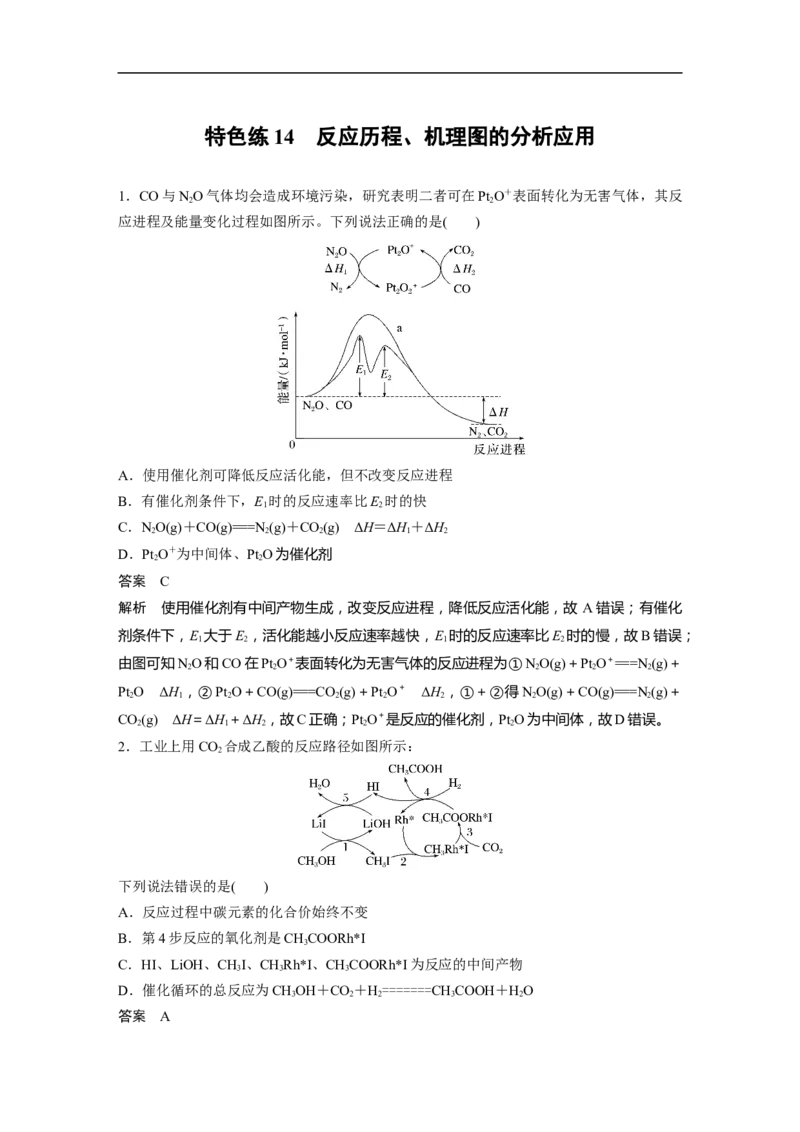
2.工业上用CO 合成乙酸的反应路径如图所示:
2
下列说法错误的是( )
A.反应过程中碳元素的化合价始终不变
B.第4步反应的氧化剂是CHCOORh*I
3
C.HI、LiOH、CHI、CHRh*I、CHCOORh*I为反应的中间产物
3 3 3
D.催化循环的总反应为CHOH+CO+H=======CHCOOH+HO
3 2 2 3 2
答案 A解析 碳元素在CHOH中显-2价,在CHCOOH中显0价,故A错误;第4步反应为
3 3
CHCOORh*I+H===CHCOOH+ Rh*+HI,氧化剂是CHCOORh*I,故B正确;根据每
3 2 3 3
一步的反应可知,中间产物有HI、LiOH、CHI、CHRh*I、CHCOORh*I,都是先生成后
3 3 3
反应的物质,故C正确;根据图示,循环的总反应为CHOH+CO +H=======CHCOOH
3 2 2 3
+HO,故D正确。
2
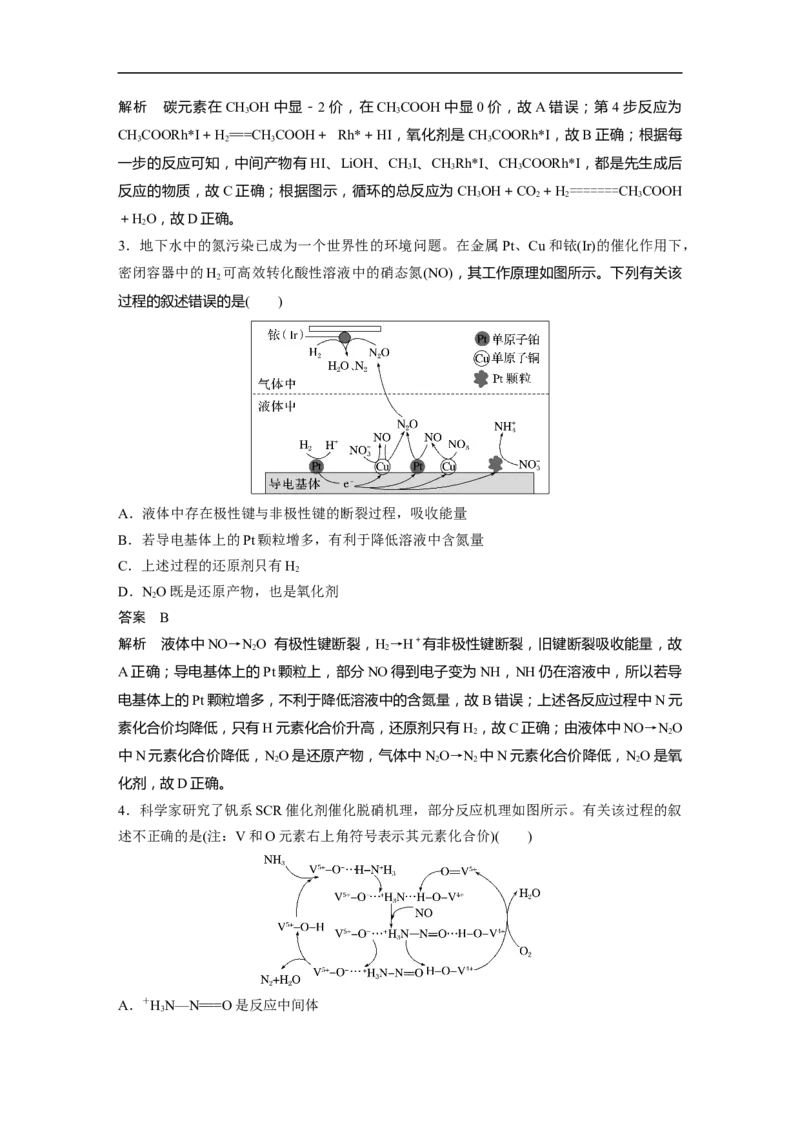
3.地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,
密闭容器中的H 可高效转化酸性溶液中的硝态氮(NO),其工作原理如图所示。下列有关该
2
过程的叙述错误的是( )
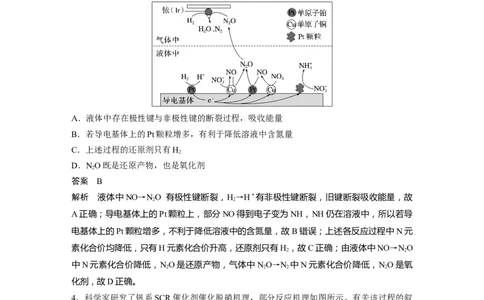
A.液体中存在极性键与非极性键的断裂过程,吸收能量
B.若导电基体上的Pt颗粒增多,有利于降低溶液中含氮量
C.上述过程的还原剂只有H
2
D.NO既是还原产物,也是氧化剂
2
答案 B
解析 液体中NO→NO 有极性键断裂,H→H+有非极性键断裂,旧键断裂吸收能量,故
2 2
A正确;导电基体上的Pt颗粒上,部分NO得到电子变为NH,NH仍在溶液中,所以若导
电基体上的Pt颗粒增多,不利于降低溶液中的含氮量,故B错误;上述各反应过程中N元
素化合价均降低,只有H元素化合价升高,还原剂只有H ,故C正确;由液体中NO→NO
2 2
中N元素化合价降低,NO是还原产物,气体中NO→N 中N元素化合价降低,NO是氧
2 2 2 2
化剂,故D正确。
4.科学家研究了钒系SCR催化剂催化脱硝机理,部分反应机理如图所示。有关该过程的叙
述不正确的是(注:V和O元素右上角符号表示其元素化合价)( )
A.+HN—N===O是反应中间体
3B.反应过程中V的成键数目发生变化
C.反应过程中O===V5+被还原
D.脱硝反应为4NH +3O===2N+6HO
3 2 2 2
答案 D
解析 由转化示意图可知,+HN—N===O是反应中间体,故A正确;O===V5+中V为双键,
3
H—O—V4+中V为单键,故B正确;反应过程中O===V5+中V由+5价降低到+4价,故被
还原,故C正确;由转化示意图可知,在催化剂作用下脱硝反应为 4NH +O +4NO===4N
3 2 2
+6HO,故D错误。
2
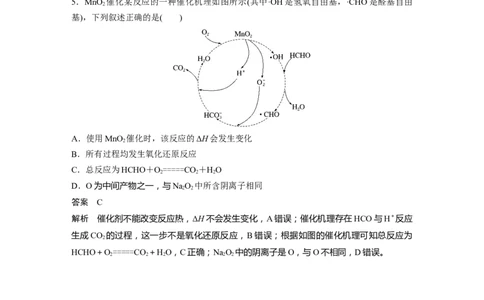
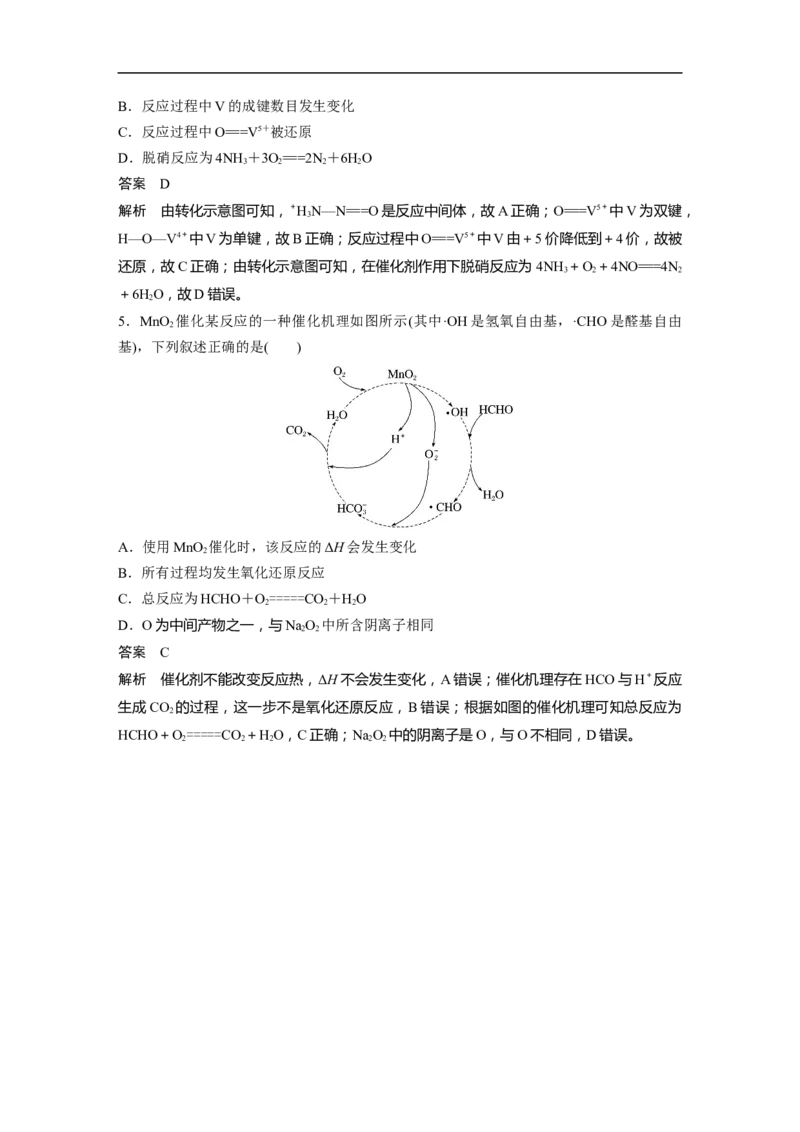
5.MnO 催化某反应的一种催化机理如图所示(其中·OH是氢氧自由基,·CHO是醛基自由
2
基),下列叙述正确的是( )
A.使用MnO 催化时,该反应的ΔH会发生变化
2
B.所有过程均发生氧化还原反应
C.总反应为HCHO+O=====CO+HO
2 2 2
D.O为中间产物之一,与NaO 中所含阴离子相同
2 2
答案 C
解析 催化剂不能改变反应热,ΔH不会发生变化,A错误;催化机理存在HCO与H+反应
生成CO 的过程,这一步不是氧化还原反应,B错误;根据如图的催化机理可知总反应为
2
HCHO+O=====CO+HO,C正确;NaO 中的阴离子是O,与O不相同,D错误。
2 2 2 2 2