文档内容
热点强化 7 含铁物质的转化与制备
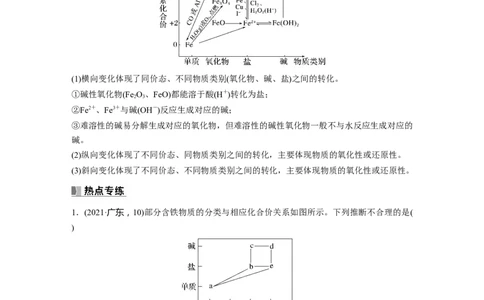
从物质类别和物质所含核心元素的化合价两个角度总结、预测物质的性质是学习化学的重要
方法之一。
(1)横向变化体现了同价态、不同物质类别(氧化物、碱、盐)之间的转化。
①碱性氧化物(Fe O、FeO)都能溶于酸(H+)转化为盐;
2 3
②Fe2+、Fe3+与碱(OH-)反应生成对应的碱;
③难溶性的碱易分解生成对应的氧化物,但难溶性的碱性氧化物一般不与水反应生成对应的
碱。
(2)纵向变化体现了不同价态、同物质类别之间的转化,主要体现物质的氧化性或还原性。
(3)斜向变化体现了不同价态、不同物质类别之间的转化,主要体现物质的氧化性或还原性。
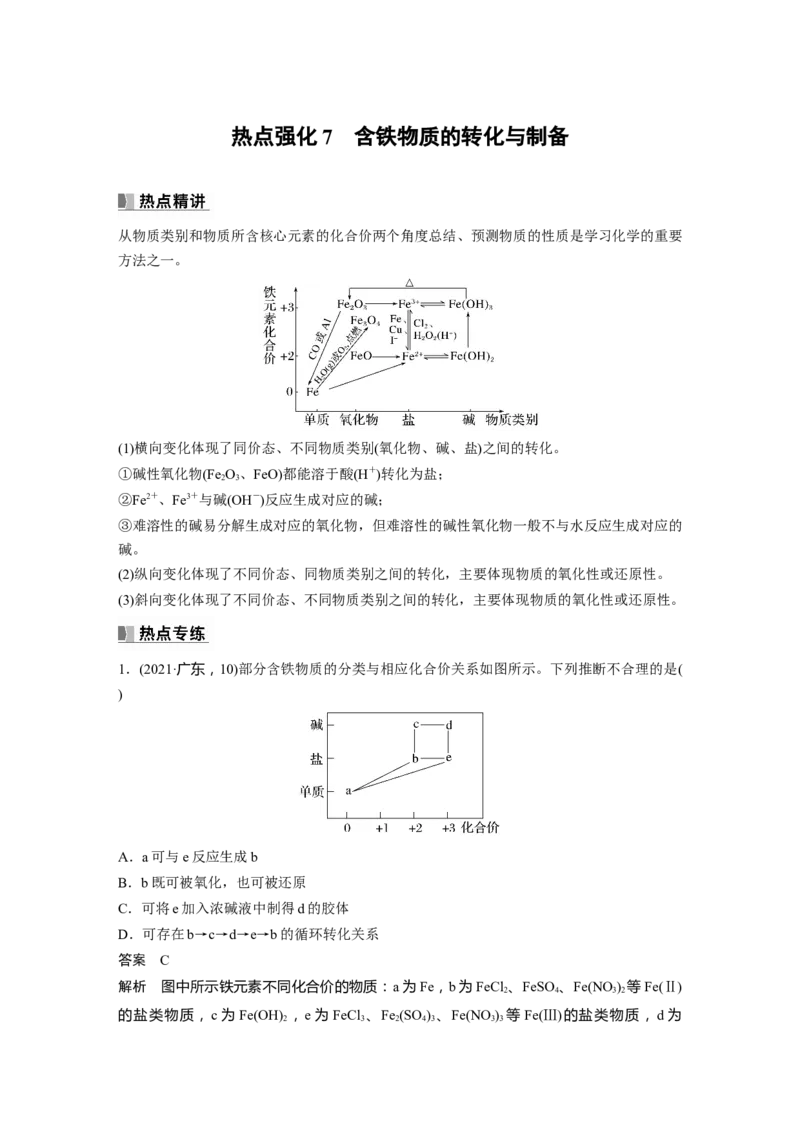
1.(2021·广东,10)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是(
)
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
答案 C
解析 图中所示铁元素不同化合价的物质:a为Fe,b为FeCl 、FeSO 、Fe(NO ) 等Fe(Ⅱ)
2 4 3 2
的盐类物质,c 为 Fe(OH) ,e 为 FeCl 、Fe (SO ) 、Fe(NO ) 等 Fe(Ⅲ)的盐类物质,d 为
2 3 2 4 3 3 3Fe(OH) 。Fe 与 Fe(Ⅲ)的盐类物质可发生反应生成 Fe(Ⅱ)的盐类物质,如 Fe+
3
2FeCl ===3FeCl ,故A不选;Fe(Ⅱ)为铁元素的中间价态,既有还原性也有氧化性,因此既
3 2
可被氧化,也可被还原,故B不选;Fe(Ⅲ)的盐类物质与浓碱液反应生成Fe(OH) 沉淀,制
3
备Fe(OH) 胶体操作为向沸水中滴加饱和FeCl 溶液,继续煮沸至溶液呈红褐色,停止加热,
3 3
故 C 选 ; b→c→d→e→b 转 化 如
FeCl ――→Fe(OH) ――→Fe(OH) ――→FeCl ――→FeCl ,故D不选。
2 2 3 3 2
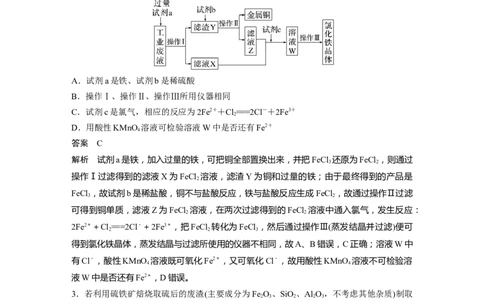
2.从某含有FeCl 、FeCl 、CuCl 的工业废液中回收铜并制备氯化铁晶体的流程如下,则下
2 3 2
列说法正确的是( )
A.试剂a是铁、试剂b是稀硫酸
B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C.试剂c是氯气,相应的反应为2Fe2++Cl===2Cl-+2Fe3+
2
D.用酸性KMnO 溶液可检验溶液W中是否还有Fe2+
4
答案 C
解析 试剂a是铁,加入过量的铁,可把铜全部置换出来,并把FeCl 还原为FeCl ,则通过
3 2
操作Ⅰ过滤得到的滤液X为FeCl 溶液,滤渣Y为铜和过量的铁;由于最终得到的产品是
2
FeCl ,故试剂b是稀盐酸,铜不与盐酸反应,铁与盐酸反应生成FeCl ,故通过操作Ⅱ过滤
3 2
可得到铜单质,滤液Z为FeCl 溶液,在两次过滤得到的FeCl 溶液中通入氯气,发生反应:
2 2
2Fe2++Cl===2Cl-+2Fe3+,把FeCl 转化为FeCl ,然后通过操作Ⅲ(蒸发结晶并过滤)便可
2 2 3
得到氯化铁晶体,蒸发结晶与过滤所使用的仪器不相同,故A、B错误,C正确;溶液W中
有Cl-,酸性KMnO 溶液既可氧化Fe2+,又可氧化Cl-,故用酸性KMnO 溶液不可检验溶
4 4
液W中是否还有Fe2+,D错误。
3.若利用硫铁矿焙烧取硫后的废渣(主要成分为Fe O 、SiO 、Al O ,不考虑其他杂质)制取
2 3 2 2 3
FeSO ·7H O,设计了如下流程:
4 2
下列说法错误的是( )
A.溶解废渣选用的酸是稀硫酸,试剂X选用铁粉
B.固体1中一定含有SiO,控制pH是为了使Al3+转化为Al(OH) ,进入固体2
2 3
C.从溶液2得到FeSO ·7H O产品的过程中,必须控制条件防止其被氧化和分解
4 2D.若改变方案,在溶液1中直接加入NaOH溶液至过量,得到的沉淀用硫酸溶解,其溶液
经结晶分离也可得到FeSO ·7H O
4 2
答案 D
解析 流程设计意图是用硫酸把Fe O 、Al O 转化为硫酸盐,除去SiO ,然后用试剂X(铁
2 3 2 3 2
粉)还原Fe3+得到硫酸亚铁,A正确;分离FeSO 和Al (SO ) 采用的是调控pH的方法,使
4 2 4 3
Al3+转化为 Al(OH) 沉淀从而与 FeSO 分离,B 正确;Fe2+容易被氧化,所以在制备
3 4
FeSO ·7H O产品的过程中,要防止其被氧化和分解,C正确;在溶液1中直接加过量的
4 2
NaOH得到的是Fe(OH) 沉淀,沉淀经溶解、结晶分离得到Fe (SO ),D不正确。
3 2 4 3
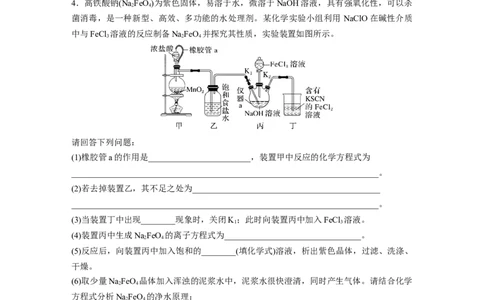
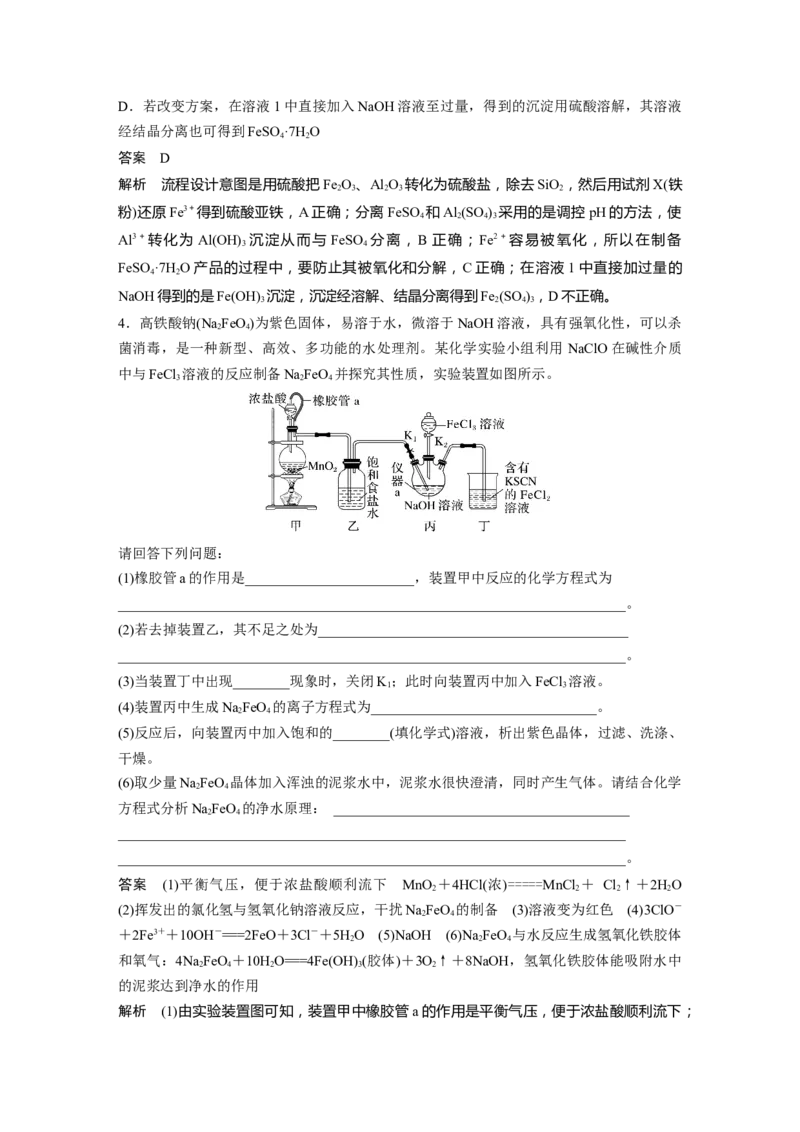
4.高铁酸钠(Na FeO)为紫色固体,易溶于水,微溶于NaOH溶液,具有强氧化性,可以杀
2 4
菌消毒,是一种新型、高效、多功能的水处理剂。某化学实验小组利用 NaClO在碱性介质
中与FeCl 溶液的反应制备NaFeO 并探究其性质,实验装置如图所示。
3 2 4
请回答下列问题:
(1)橡胶管a的作用是________________________,装置甲中反应的化学方程式为
________________________________________________________________________。
(2)若去掉装置乙,其不足之处为____________________________________________
________________________________________________________________________。
(3)当装置丁中出现________现象时,关闭K;此时向装置丙中加入FeCl 溶液。
1 3
(4)装置丙中生成NaFeO 的离子方程式为________________________________。
2 4
(5)反应后,向装置丙中加入饱和的________(填化学式)溶液,析出紫色晶体,过滤、洗涤、
干燥。
(6)取少量NaFeO 晶体加入浑浊的泥浆水中,泥浆水很快澄清,同时产生气体。请结合化学
2 4
方程式分析NaFeO 的净水原理: __________________________________________
2 4
________________________________________________________________________
________________________________________________________________________。
答案 (1)平衡气压,便于浓盐酸顺利流下 MnO +4HCl(浓)=====MnCl + Cl↑+2HO
2 2 2 2
(2)挥发出的氯化氢与氢氧化钠溶液反应,干扰NaFeO 的制备 (3)溶液变为红色 (4)3ClO-
2 4
+2Fe3++10OH-===2FeO+3Cl-+5HO (5)NaOH (6)Na FeO 与水反应生成氢氧化铁胶体
2 2 4
和氧气:4NaFeO +10HO===4Fe(OH) (胶体)+3O↑+8NaOH,氢氧化铁胶体能吸附水中
2 4 2 3 2
的泥浆达到净水的作用
解析 (1)由实验装置图可知,装置甲中橡胶管a的作用是平衡气压,便于浓盐酸顺利流下;装置甲中二氧化锰与浓盐酸共热反应生成氯化锰、氯气和水,反应的化学方程式为MnO +
2
4HCl(浓)=====MnCl + Cl↑+2HO。(3)若装置甲中生成的氯气将装置中的空气完全排出
2 2 2
后,过量的氯气将氯化亚铁氧化为氯化铁,FeCl 与溶液中的硫氰化钾反应生成硫氰化铁,
3
使溶液变为红色。(4)装置丙中碱性条件下,次氯酸根离子与铁离子发生氧化还原反应生成
高铁酸根离子、氯离子和水,反应的离子方程式为 3ClO—+2Fe3++10OH-===2FeO+3Cl-
+5HO。
2