文档内容
第 33 讲 价层电子对互斥模型、杂化轨道理论及应用
[复习目标] 1.掌握价层电子对互斥模型和杂化轨道理论的内容并能用其推测简单分子或离
子的空间结构。2.掌握键角大小原因并能作出规范描述。
1.价层电子对互斥模型
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
②孤电子对排斥力较大,孤电子对越多,排斥力越强,键角越小。
(2)价层电子对互斥模型推测分子(离子)的空间结构的关键——价层电子对数的计算
价层电子对数=σ键电子对数+中心原子的孤电子对数
说明:σ键电子对数=中心原子结合的原子数;
中心原子的孤电子对数=(a-xb),其中
①a表示中心原子的价电子数。
对于主族元素:a=原子的最外层电子数。
对于阳离子:a=中心原子的价电子数-离子的电荷数。
对于阴离子:a= 中心原子的价电子数+离子的电荷数 ( 绝对值 )。
②x表示与中心原子结合的原子数。
③b表示与中心原子结合的原子最多能接受的电子数(氢为1,其他原子= 8 -该原子的价电
子数。如氧和氧族元素中的S、Se等均为2,卤族元素均为1)。
例如,SOCl 的空间结构的判断:
2
SOCl 的中心原子为S,σ键电子对数为3,孤电子对数为×(6-1×2-2×1)=1,价层电子
2
对数为4,这些价层电子对互相排斥,形成四面体形的VSEPR模型,由于中心原子上有1
个孤电子对,则SOCl 的空间结构为三角锥形。
2
2.杂化轨道理论
(1)杂化轨道理论概述
中心原子上若干不同类型(主要是s、p轨道)、能量相近的原子轨道混合起来,重新组合成同
等数目、能量完全相同的新轨道。杂化轨道数不同,轨道间的夹角不同,形成分子的空间结
构不同。
(2)杂化轨道三种类型(3)由杂化轨道数判断中心原子的杂化类型
杂化轨道用来形成σ键和容纳孤电子对,所以有公式:杂化轨道数=中心原子的孤电子对数
+ 中心原子的 σ 键个数 =中心原子的价层电子对数。
3.VSEPR模型与微粒空间结构的关系
完成下列表格
价层电 σ键电 孤电子 中心原子杂 VSEPR 分子(离子)
实例
子对数 子对数 对数 化轨道类型 模型 空间结构
BeCl 、CS 2 2 0 sp 直线形 直线形
2 2
BF、SO 、CO 3 0 sp 2 平面三 平面三角形
3 3
3
O、SO 2 1 sp 2 角形 V 形
3 2
SnCl 、PO、NH 4 0 sp 3 正四面体形
4
四面体
PH 、SO 4 3 1 sp 3 三角锥形
3
形
HS、I 2 2 sp 3 V 形
2
1.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数( )
2.N 分子中N原子没有杂化,分子中有1个σ键、2个π键( )
2
3.只要分子的空间结构为平面三角形,中心原子均为sp2杂化( )
4.分子中中心原子通过sp3杂化轨道成键时,该分子一定为正四面体结构( )
5.SiF 与SO的中心原子均为sp3杂化( )
4
答案 1.√ 2.√ 3.√ 4.× 5.√
一、价层电子对数的判断
1.正误判断,正确的打“√”,错误的打“×”。
(1)XeF 的中心原子价层电子对数为6( × )
2
(2) 为四角锥结构, 中心原子I没有孤电子对( × )(3)六氟化硫分子空间结构呈正八面体形,其中心原子的价层电子对数为4( × )
(4)PhB(OH) 和 中B原子的价层电子对数相等(—Ph 代表苯基,—Pr 代表
2
异丙基)( × )
2.下列分子或离子的中心原子上未用于成键的价电子对最多的是( )
A.HO B.HCl
2
C.NH D.PCl
3
答案 A
解析 A项,氧原子有两对未成键的价电子对;B项,HCl分子属于AB型分子,没有中心
原子;C项,NH的中心原子的价电子全部参与成键;D项,磷原子有一对未成键的价电子
对。
二、杂化方式的判断
3.判断下列物质中心原子的杂化方式。
(1)PCl 分子中,P的杂化方式为________。
3
(2)[2019·全国卷Ⅰ,35(2)节选]乙二胺(H NCH CHNH )是一种有机化合物,分子中氮、碳的
2 2 2 2
杂化类型分别是______、______。
(3)HOCHCN分子中碳原子的杂化轨道类型是________。
2
(4)丙烯腈分子(H C==CH—C≡N)中碳原子杂化轨道类型为________。
2
(5)[2020·全国卷Ⅲ,35(2)节选]氨硼烷在催化剂作用下水解释放氢气:
3NH BH+6HO===3NH+B O+9H
3 3 2 3 2
B O 的结构为 。在该反应中,B 原子的杂化轨道类型由________变为
3
________。
答案 (1)sp3杂化 (2)sp3 sp3 (3)sp3和sp (4)sp2、sp (5)sp3 sp2
三、分子(离子)空间结构的判断
4.下列分子或离子中,中心原子的价层电子对的空间结构为正四面体形且分子或离子的空
间结构为V形的是( )
A.NO B.PH C.HO+ D.OF
3 3 2
答案 D
解析 NO的价层电子对的空间结构呈平面三角形,A错误;PH 的空间结构呈三角锥形,B
3
错误;HO+的空间结构呈三角锥形,C错误;OF 中心原子的价层电子对的空间结构为正四
3 2面体形且分子的空间结构为V形,D正确。
5.下列物质的分子与O 分子的结构最相似的是( )
3
A.HO B.CO C.SO D.BeCl
2 2 2 2
答案 C
解析 HO分子中氧原子采用sp3杂化方式;CO 中碳原子采用sp杂化方式;BeCl 中Be原
2 2 2
子采用sp杂化方式。
6.已知Zn2+的4s轨道和4p轨道可以形成sp3型杂化轨道,那么[ZnCl ]2-的空间结构为(
4
)
A.直线形 B.平面正方形
C.正四面体形 D.正八面体形
答案 C
解析 根据杂化轨道理论知,Zn2+的4s轨道和4p轨道形成的sp3杂化轨道为正四面体形,
Zn2+再结合4个Cl-形成[ZnCl ]2-,其中Zn2+的孤电子对数为0,所以[ZnCl ]2-的空间结构
4 4
为正四面体形。
答题规范(4) 键角大小原因解释的三种模型
模型1 价层电子对构型(或中心原子杂化方式)不相同,优先看杂化方式,键角:sp>sp2>sp3
例1 Si与C元素位于同一主族,SiO 键角小于CO 的原因是_____________________。
2 2
答案 SiO 中中心Si原子采取sp3杂化,键角为109°28′;CO 中中心C原子采取sp杂化,
2 2
键角为180°
答题模板:×××中心原子采取×××杂化,键角为×××,而×××中心原子采取×××
杂化,键角为×××。
变式训练1 比较下列分子或离子中的键角大小(填“>”“<”或“=”):
①HO________CS ,原因是_____________________________________________________。
2 2
②SO ______SO。③BF________NCl 。
3 3 3
答案 ①< HO中中心O原子采取sp3杂化,键角约为105°;CS 中中心C原子采取sp杂
2 2
化,键角为180° ②> ③>
模型2 价层电子对构型(或中心原子杂化方式)相同,看电子对间的斥力
(1)电子对排斥力大小顺序:孤电子对与孤电子对之间>孤电子对与成键电子对之间>成键电
子对与成键电子对之间
例2 已知HO、NH 、CH 三种分子中,键角由大到小的顺序是____________,原因为
2 3 4
________________________________________________________________________。
答案 CH >NH >HO CH 分子中无孤电子对,NH 分子中含有1个孤电子对,HO分子
4 3 2 4 3 2
中含有2个孤电子对,孤电子对对成键电子对的排斥作用依次增大,故键角逐渐减小答题模板: ×××分子中无孤电子对,×××分子中含有n个孤电子对,孤电子对对成键
电子对的排斥作用较大,因而键角较小。
变式训练2 比较下列分子或离子中的键角大小(填“>”“<”或“=”):
①PH ________PO,原因是_________________________________________________。
3
②SO______SO。
答案 ①< PH 与PO中中心P原子都采取sp3杂化,PO中无孤电子对,PH 分子中含有1
3 3
个孤电子对,孤电子对对成键电子对的排斥作用较大,因而键角较小 ②<
(2)三键、双键、单键之间的排斥力大小顺序:三键—三键>三键—双键>双键—双键>双键—
单键>单键—单键,举例:
分子 杂化轨道角度 排斥力分析 实际键角
C==O对C—Cl的排斥力大 形成两种键角分别为
COCl 120°
2
于C—Cl对C—Cl的排斥力 124°18′、111°24′
变 式 训 练 3 在 分 子 中 , 键 角 ∠ HCO________( 填 “ > ” “ < ” 或
“ = ” )∠HCH 。 理 由 是
________________________________________________________________________。
答案 > π键斥力大于σ键斥力
模型3 空间结构相同,中心原子相同或配位原子相同,看中心原子或配位原子的电负性
(1)中心原子不同,配位原子相同
例 3 AC 与 BC , 若 电 负 性 : A > B , 则 键 角 : AC ________BC 。 原 因 :
3 3 3 3
___________________
_____________________________________________________。
答案 > 中心原子的电负性A强于B,中心原子的电负性越大,成键电子对离中心原子越
近,斥力越大,键角也越大
(2)中心原子相同,配位原子不同
例 4 AB 与 AC ,若电负性: B>A>C,则键角: AB ______AC 。原因为
3 3 3 3
________________________________________________________________________
________________________________________________________________________。
答案 < 电负性:B>A>C,在AB 中成键电子对离中心原子较远,斥力较小,因而键角
3
较小
变式训练4 ①NH 的键角______PH 的键角,原因是________________________________。
3 3
②NF 的键角____NH 的键角,理由是______________________________________。
3 3
答案 ①> 中心原子的电负性N强于P,中心原子的电负性越大,成键电子对离中心原子
越近,斥力越大,键角也越大 ②< F的电负性比H大,NF 中成键电子对离中心原子较
3
远,斥力较小,因而键角也较小1.HBO 分子中的 O—B—O 的键角________(填“大于”“等于”或“小于”) BH中的
3 3
H—B—H 的键角,判断依据是____________________________________________。
答案 大于 HBO 分子中的B采取sp2杂化,而BH中的B采取sp3杂化,sp2杂化形成的键
3 3
角大于sp3杂化
2.高温陶瓷材料Si N 晶体中键角N—Si—N______(填“>”“<”或“=”)Si—N—Si,原
3 4
因是________________________________________________________________________。
答案 > N原子上有孤电子对,由于孤电子对与成键电子对的排斥力更大,使得 Si—N—
Si键角较小
3.SeO 中 Se—O 的键角比 SeO 的键角________(填“大”或“小”),原因是
3
________________________________________________________________________。
答案 小 SeO中中心Se原子采取sp3杂化,键角为109°28′,SeO 中中心Se原子采取sp2
3
杂化,键角为120°
1.(1)[2021·全国甲卷,35(1)节选]SiCl 是生产高纯硅的前驱体,其中Si采取的杂化类型为
4
________。SiCl 可发生水解反应,机理如下:
4
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl (H O)中Si采取的杂
4 2
化类型为________(填标号)。
(2)[2021·全国乙卷,35(3)节选]PH 中P的杂化类型是 ________。
3
(3)[2021·湖南,18(2)②节选]N-甲基咪唑( )中碳原子的杂化轨道类型为________。
答案 (1)sp3 ② (2)sp3 (3)sp3、sp2
解析 (1)根据 SiCl 的结构式可知,Si 的价层电子对数为 4,故 Si 采取 sp3杂化;根据
4
SiCl (H O)的结构式可知Si的价层电子对数为5,采取sp3d杂化。
4 2
(2)PH 中中心原子的价层电子对数为3+×(5-3×1)=4,故P原子的杂化方式为sp3。
3
(3)N-甲基咪唑分子中含有甲基和碳碳双键,则该分子中碳原子的杂化轨道类型为sp3、sp2。
2.[2022·河北,17(3)]SnCl的空间结构为________________________________________,
其中心离子杂化方式为__________。答案 三角锥形 sp3
3.[2022·北京,15(2)]比较SO和HO分子中的键角大小并给出相应解释:__________
2
_____________________________________________________________________________
____________________________________________________________________________。
答案 SO的键角大于HO分子的键角,SO中S原子的价层电子对数为4、孤电子对数为
2
0,离子的空间结构为正四面体形,HO分子中O原子的价层电子对数为4、孤电子对数为
2
2,分子的空间结构为V形
4.[2021·山东,16(3)]Xe是第五周期的稀有气体元素,与F形成的XeF 室温下易升华。
2
XeF 中心原子的价层电子对数为____________,下列对XeF 中心原子杂化方式推断合理的
2 2
是______________(填标号)。
A.sp B.sp2 C.sp3 D.sp3d
答案 5 D
解析 XeF 易升华,所以是分子晶体,其中心原子的价层电子对数为 2+=5,其中心原子
2
的杂化方式应为sp3d。
课时精练
1.下列描述正确的是( )
A.CS 为V形的极性分子
2
B.ClO的空间结构为平面三角形
C.SF 中有6对完全相同的成键电子对
6
D.SiF 和SO的中心原子均为sp2杂化
4
答案 C
解析 CS 与CO 的分子结构相似,是直线形的非极性分子,A错误;中心原子Cl有一个孤
2 2
电子对,所以ClO的空间结构为三角锥形,B错误;S有6个电子,正好与6个F形成6个
共价键,C正确;SiF 中Si有四个σ键,SO中S原子形成3个σ键,还有一个孤电子对,
4
所以Si、S均是sp3杂化,D错误。
2.科学家最近研制出有望成为高效火箭推进剂的N(NO)(如图所示)。
2 3
已知该分子中N—N—N键角都是108.1°,下列有关N(NO) 的说法正确的是( )
2 3
A.分子中N、O原子间形成的共价键是非极性键
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.分子中四个氮原子围成一个空间正四面体答案 C
3.下列关于BeF 和SF 的说法错误的是( )
2 2
A.BeF 分子中,中心原子Be的价层电子对数等于2,成键电子对数也等于2
2
B.BeF 分子的孤电子对数为0
2
C.SF 分子中,中心原子S的价层电子对数等于4,其空间结构为四面体形,成键电子对数
2
等于2,没有孤电子对
D.在气相中,BeF 是直线形而SF 是V形
2 2
答案 C
解析 SF 分子中,中心原子S的孤电子对数为=2,成键电子对数为2,故价层电子对数为
2
4,分子的空间结构为V形。
4.用价层电子对互斥模型(VSEPR)可以预测许多分子或离子的空间结构,有时也能用来推
测键角大小,下列判断正确的是( )
A.SO 、CS、HI都是直线形分子
2 2
B.BF 键角为120°,SnF 键角大于120°
3 2
C.COCl 、BF、SO 都是平面三角形分子
2 3 3
D.PCl 、NH 、PCl 都是三角锥形分子
3 3 5
答案 C
解析 SO 分子中含有孤电子对,不是直线形分子,是 V形分子,A错误;BF 键角为
2 3
120°,SnF 中有两个成键电子对,一个孤电子对,孤电子对会产生斥力,所以键角小于
2
120°,B错误;PCl 、NH 是三角锥形分子,PCl 是三角双锥形分子,D错误。
3 3 5
5.下列有关杂化轨道理论的说法不正确的是( )
A.杂化前后的轨道数不变,但轨道的形状发生了改变
B.杂化轨道全部参与形成化学键
C.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
D.四面体形、三角锥形的结构可以用sp3杂化轨道理论解释
答案 B
解析 杂化前后的轨道数不变,杂化后,各个轨道尽可能分散、对称分布,导致轨道的形状
发生了改变,故A正确;杂化轨道可以部分参与形成化学键,例如NH 中N发生了sp3杂化,
3
形成了4个sp3杂化轨道,但是只有3个参与形成了化学键,故B错误;sp3、sp2、sp杂化轨
道其空间结构分别是正四面体形、平面三角形、直线形,所以其夹角分别为 109°28′、
120°、180°,故C正确;四面体形、三角锥形分子的结构可以用 sp3杂化轨道理论解释,如
甲烷、氨气分子,故D正确。
6.下列分子或离子中键角由大到小排列的顺序是( )
①BCl ②NH ③HO ④PCl ⑤HgCl
3 3 2 2
A.⑤④①②③ B.⑤①④②③C.④①②⑤③ D.③②④①⑤
答案 B
解析 ①BCl 中中心B原子为sp2杂化,键角为120°;②NH 中中心N原子为sp3杂化,
3 3
NH 分子中有孤电子对存在,使键角小于109°28′;③HO中中心O原子为sp3杂化,HO
3 2 2
分子中存在两个孤电子对,使键角比NH 分子的键角还小;④PCl中中心P原子为sp3杂化,
3
键角为109°28′;⑤HgCl 中中心Hg原子为sp杂化,键角为180°;综上,键角由大到小的
2
顺序为⑤①④②③。
7.下列说法正确的是( )
①S 分子中S原子采用的杂化轨道类型为sp3
8
②C H 分子中只有以s轨道与sp2杂化轨道“头碰头”方式重叠而成的σ键
2 4
③SnBr 分子中Br—Sn—Br的键角<120°
2
④HO+中H—O—H的键角比HO中H—O—H的键角大
3 2
A.①② B.③④
C.①②③ D.①③④
答案 D
解析 ①S 是一个环形分子,每个S与另外两个S原子相连,S原子形成2个孤电子对,2
8
个σ键,所以S是sp3杂化,正确;②碳碳双键中一个是σ键,还有一个是π键,错误;
③SnBr 分子中,Sn原子的价层电子对数是×(4-2×1)+2=3,含有1个孤电子对,SnBr
2 2
的空间结构为V形,根据价层电子对互斥模型可以判断其键角小于 120°,正确;④HO+和
3
HO中氧原子均采取sp3杂化,HO中O原子有2个孤电子对,HO+中O原子有1个孤电子
2 2 3
对,导致HO+中H—O—H的键角比HO中H—O—H的键角大,正确。
3 2
8.CH、—CH、CH都是重要的有机反应中间体,下列有关它们的说法错误的是( )
3
A.CH与HO+的空间结构均为三角锥形
3
B.它们的C均采取sp2杂化
C.CH中的所有原子均共面
D.CH与OH-形成的化合物中不含有离子键
答案 B
解析 CH与HO+中C原子与O原子的价层电子对数都是4,且都含有1个孤电子对,均为
3
三角锥形结构,A项正确;CH、—CH 、CH中C的价层电子对数分别是3、4、4,根据价
3
层电子对互斥模型知,C原子的杂化类型分别是sp2、sp3、sp3,B项错误;CH中的碳原子
采取sp2杂化,所有原子均共面,C项正确;CH与OH-形成的化合物是CHOH,属于共价
3
化合物,不含离子键,D项正确。
9.根据价层电子对互斥模型填空:
(1)OF 分子中,中心原子上的σ键电子对数为______,孤电子对数为________,价层电子对
2
数为________,中心原子的杂化方式为________杂化,VSEPR模型为____________,分子的空间结构为______________。
(2)BF 分子中,中心原子上的σ键电子对数为________,孤电子对数为__________,价层电
3
子对数为________,中心原子的杂化方式为________杂化,VSEPR模型为____________,
分子的空间结构为____________。
(3)SO中,中心原子上的σ键电子对数为______,孤电子对数为______,价层电子对数为
________,中心原子的杂化方式为________杂化,VSEPR模型为____________,分子的空
间结构为______________。
答案 (1)2 2 4 sp3 四面体形 V形
(2)3 0 3 sp2 平面三角形 平面三角形
(3)4 0 4 sp3 正四面体形 正四面体形
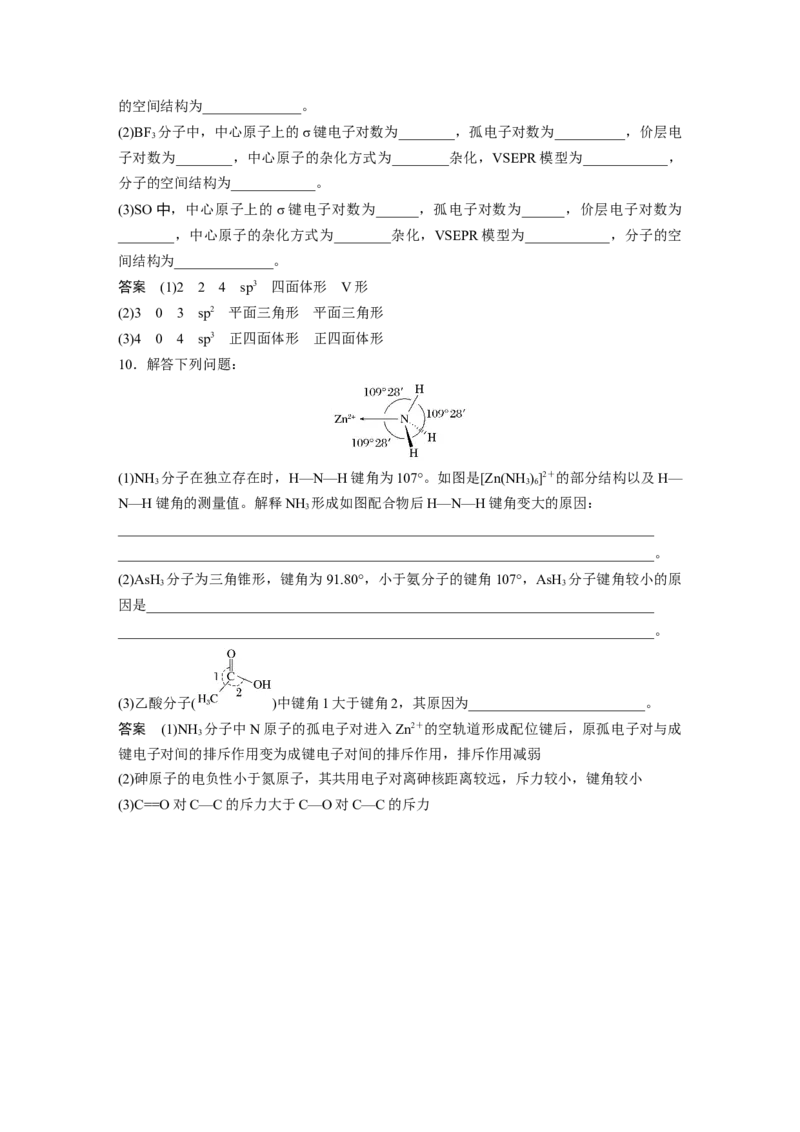
10.解答下列问题:
(1)NH 分子在独立存在时,H—N—H键角为107°。如图是[Zn(NH )]2+的部分结构以及H—
3 3 6
N—H键角的测量值。解释NH 形成如图配合物后H—N—H键角变大的原因:
3
____________________________________________________________________________
____________________________________________________________________________。
(2)AsH 分子为三角锥形,键角为91.80°,小于氨分子的键角107°,AsH 分子键角较小的原
3 3
因是________________________________________________________________________
____________________________________________________________________________。
(3)乙酸分子( )中键角1大于键角2,其原因为_________________________。
答案 (1)NH 分子中N原子的孤电子对进入Zn2+的空轨道形成配位键后,原孤电子对与成
3
键电子对间的排斥作用变为成键电子对间的排斥作用,排斥作用减弱
(2)砷原子的电负性小于氮原子,其共用电子对离砷核距离较远,斥力较小,键角较小
(3)C==O对C—C的斥力大于C—O对C—C的斥力