文档内容
课时检测(七十) 物质的检验、分离和提纯
1.我国明代《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二
次……价值数倍也”。这里用到的实验方法可用于分离( )
A.苯和水 B.乙酸乙酯和乙酸
C.食盐水和泥沙 D.硝酸钾和硫酸钠
2.(2023·海南等级考)化学实验中的颜色变化,可将化学抽象之美具体为形象之美。下列叙述错误
的是( )
A.土豆片遇到碘溶液,呈蓝色
B.蛋白质遇到浓硫酸,呈黄色
C.CrO 溶液(0.1 mol·L-1)中滴加乙醇,呈绿色
3
D.苯酚溶液(0.1 mol·L-1)中滴加FeCl 溶液(0.1 mol·L-1),呈紫色
3
3.下列关于离子检验的说法正确的是( )
A.向某溶液中加入稀盐酸,将产生的无色无味气体通入澄清石灰水中,石灰水变浑浊,则原溶液
中一定含有CO或HCO
B.向某溶液中加入Ba(NO ) 溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有
3 2
SO
C.向溶液中先加入HO 溶液,再滴加KSCN溶液,溶液变红,则原溶液中含Fe2+而不含Fe3+
2 2
D.向某溶液中加入AgNO 溶液产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有Cl-
3
4.(2023·湖南等级考)取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为
0.1 mol·L-1),反应现象没有明显差别的是( )
选项 试剂① 试剂②
A 氨水 AgNO 溶液
3
B NaOH溶液 Al (SO ) 溶液
2 4 3
C HCO 溶液 酸性KMnO 溶液
2 2 4 4
D KSCN溶液 FeCl 溶液
3
5.下列实验中,所采取的分离方法与对应原理都正确的是( )
选项 目的 分离方法 原理
A 除去KCl中的MnO 蒸发结晶 溶解度不同
2
B 除去碘中的NaCl 加热、升华 NaCl的熔点高,碘易升华
C 分离KNO 和NaCl 重结晶 KNO 的溶解度大于NaCl
3 3
D 分离食用油和汽油 分液 食用油和汽油的密度不同
6.(2023·菏泽一模)一定量的甲苯和KMnO 溶液发生反应得到混合物,按如下流程分离出苯甲酸、
4
回收未反应的甲苯。下列说法错误的是( )
A.苯甲酸可反应形成盐、酯、酰胺、酸酐等
B.操作Ⅰ和操作Ⅱ依次为蒸发浓缩、冷却结晶和蒸馏C.甲苯、苯甲酸依次由①②获得
D.苯甲酸100 ℃时迅速升华,故其粗品精制除采用重结晶方法外,还可用升华法
7.200 mL某无色溶液中只可能含有以下离子中的若干种(忽略水的电离):K+、Al3+、Fe3+、Fe2+、
Mg2+、Ba2+、NH、Cl-、CO、SO、CrO。将此溶液分为两等份并进行如下实验:①向第一份溶液中加入
2
过量NaOH溶液并加热,只收集到448 mL(标准状况)气体,无沉淀生成;再向冷却后的溶液中通入过
量的CO ,有白色沉淀生成,经过滤、洗涤、灼烧后可得到1.02 g固体。②向第二份溶液中加入足量
2
BaCl 溶液后,有白色沉淀生成,经过滤、洗涤(足量盐酸洗涤)、干燥后可得到11.65 g固体;再向滤液中
2
加入AgNO 溶液有白色沉淀产生。下列判断错误的是( )
3
A.溶液中一定不存在的离子是Fe3+、Fe2+、Mg2+、Ba2+、CO、CrO、Cl-
2
B.不能确定溶液中是否存在的离子是Cl-
C.原溶液中NH、Al3+的物质的量均为0.04 mol
D.原溶液中SO的浓度是0.5 mol·L-1
8.(2024·福建平潭翰英中学)有一瓶澄清的溶液,其中可能含有NH、Mg2+、Ba2+、Al3+、Cl-、I-、
NO、CO、SO、[Al(OH) ]-、SO,取该溶液进行以下实验:
4
(1)取pH试纸检验,溶液呈强酸性,可以排除________、________、________的存在。(填离子符号,
下同)
(2)取出部分溶液,加入少量CCl 及数滴新制氯水,经振荡后CCl 层呈紫红色,可以判断
4 4
__________不存在。
(3)另取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕
后,溶液均无沉淀产生,则又可以排除________、________的存在。
(4)取出部分上述碱性溶液加Na CO 溶液后,有白色沉淀生成,可以判断________不存在。
2 3
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定:该溶液中肯定存在的离子是__________,还不能确定是否存在的离子是
_________。
9.(2023·全国甲卷)钴配合物[Co(NH )]Cl 溶于热水,在冷水中微溶,可通过如下反应制备:
3 6 3
2CoCl +2NH Cl+10NH +HO――→2[Co( NH )]Cl+2HO
2 4 3 2 2 3 6 3 2
具体步骤如下:
Ⅰ.称取2.0 g NH Cl,用5 mL水溶解。
4
Ⅱ.分批加入3.0 g CoCl ·6HO后,将溶液温度降至10 ℃以下,加入1 g活性炭、7 mL浓氨水,搅
2 2
拌下逐滴加入10 mL 6%的双氧水。
Ⅲ.加热至55~60 ℃反应20 min。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的25 mL沸水中,趁热过滤。
Ⅴ.滤液转入烧杯中,加入4 mL浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题。
(1)步骤Ⅰ中使用的部分仪器如下:
仪器a的名称是________。加快NH Cl溶解的操作有______________________。
4(2)步骤Ⅱ中,将温度降至10 ℃以下以避免__________________、________________;可选用
________降低溶液温度。
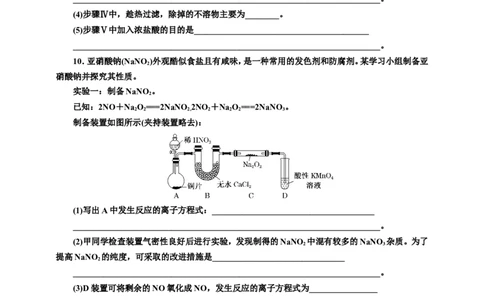
(3)
指出如图过滤操作中不规范之处。
________________________________________________________________________
________________________________________________________________________。
(4)步骤Ⅳ中,趁热过滤,除掉的不溶物主要为________。
(5)步骤Ⅴ中加入浓盐酸的目的是_________________________________________
________________________________________________________________________。
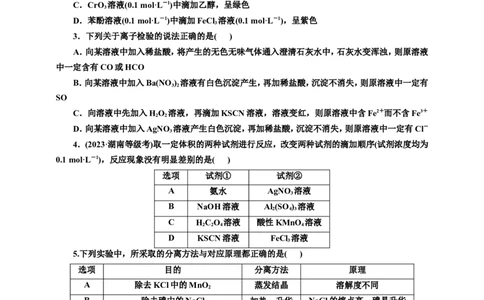
10.亚硝酸钠(NaNO )外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。某学习小组制备亚
2
硝酸钠并探究其性质。
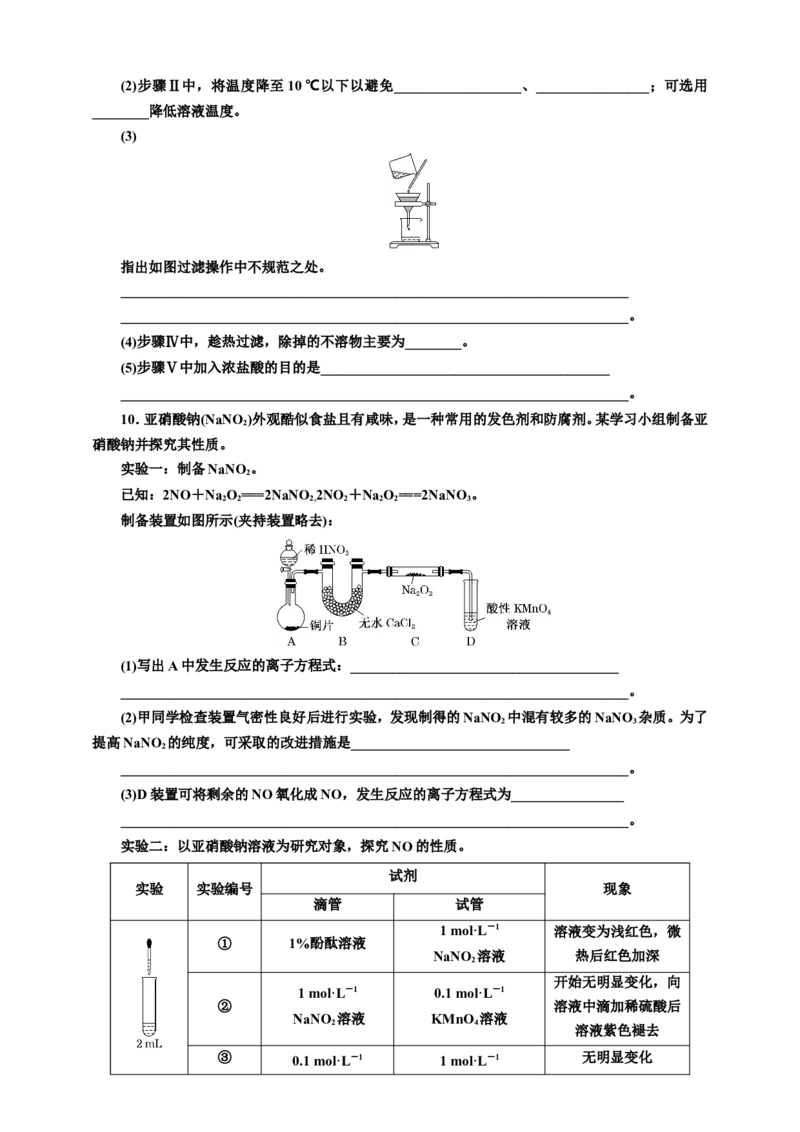
实验一:制备NaNO 。
2
已知:2NO+Na O===2NaNO 2NO +Na O===2NaNO 。
2 2 2, 2 2 2 3
制备装置如图所示(夹持装置略去):
(1)写出A中发生反应的离子方程式:______________________________________
________________________________________________________________________。
(2)甲同学检查装置气密性良好后进行实验,发现制得的NaNO 中混有较多的NaNO 杂质。为了
2 3
提高NaNO 的纯度,可采取的改进措施是_______________________________
2
________________________________________________________________________。
(3)D装置可将剩余的NO氧化成NO,发生反应的离子方程式为________________
________________________________________________________________________。
实验二:以亚硝酸钠溶液为研究对象,探究NO的性质。
试剂
实验 实验编号 现象
滴管 试管
1 mol·L-1 溶液变为浅红色,微
① 1%酚酞溶液
NaNO 溶液 热后红色加深
2
开始无明显变化,向
1 mol·L-1 0.1 mol·L-1
② 溶液中滴加稀硫酸后
NaNO 溶液 KMnO 溶液
2 4
溶液紫色褪去
③ 0.1 mol·L-1 1 mol·L-1 无明显变化KSCN溶液 FeSO 溶液(pH=0.5)
4
溶液变黄后迅速变为
1 mol·L-1 1 mol·L-1
④ 棕色,再滴加KSCN
NaNO 溶液 FeSO 溶液(pH=0.5)
2 4
溶液,溶液变红
已知:[Fe(NO)]2+在溶液中呈棕色。
(4)结合化学用语解释实验①“微热后红色加深”的原因:____________________
________________________________________________________________________
________________________________________________________________________。
(5)解释实验④中“溶液变黄后迅速变为棕色”的原因:_____________________
________________________________________________________________________(用离子方程
式表示)。
(6)取一支试管,加入少量实验④中的棕色溶液,加热,有无色气体逸出,在近试管口处变为红棕色,
溶液中有红褐色沉淀生成。解释上述现象产生的原因:________________
________________________________________________________________________。
课时检测(七十)
1.B 烧酒的制造工艺是蒸馏,蒸馏可用于分离沸点不同的液体混合物。苯和水互不相溶,可用分
液的方法分离,A项错误;乙酸乙酯和乙酸互溶且沸点差别较大,可用蒸馏的方法分离,B项正确;泥
沙不溶于水,食盐水和泥沙可用过滤的方法分离,C项错误;硝酸钾和硫酸钠的溶解度随温度变化不
同,可用重结晶的方法分离,D项错误。
2.B 土豆片中含有淀粉,淀粉遇到碘单质会变蓝,A正确;结构中含苯环的蛋白质遇到浓硝酸,
呈黄色,B错误;CrO 会被乙醇还原为三价铬,呈绿色,C正确;苯酚遇到氯化铁会有显色反应,生成紫
3
色的配合物,D正确。
3.A 能使澄清石灰水变浑浊的无色无味气体是二氧化碳,所以原溶液中可能有CO或HCO,A
正确;向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸沉淀不消失,则原溶液中可能有SO或
SO,B错误;HO 具有强氧化性,能将亚铁离子氧化为铁离子,向某溶液中先滴加少量HO 溶液,再
2 2 2 2
滴加KSCN溶液,溶液呈血红色,不能说明原溶液中含有亚铁离子,也可能含铁离子,C错误;向某溶
液中加入AgNO 溶液产生白色沉淀后又加入HCl,该白色沉淀可能转化为AgCl白色沉淀,故原溶液
3
中不一定有Cl-,D错误。
4.D
选项 ①加入②中现象 ②加入①中现象
A 先产生白色沉淀,后白色沉淀溶解 先无明显现象,后产生白色沉淀
B 先产生白色沉淀,后白色沉淀溶解 先无明显现象,后产生白色沉淀
C 溶液紫色逐渐褪去,有气泡产生 紫色溶液迅速褪色,有气泡产生
D 溶液变为红色 溶液变为红色
5.B 除去KCl中的MnO 应采用过滤的方法,A错误;碘易升华,加热可分离,B正确;利用重结
2
晶方法分离KNO 和NaCl是利用KNO 的溶解度受温度的影响大于NaCl,C错误;食用油和汽油互
3 3
溶,因沸点不同而用蒸馏的方法分离,D错误。6.B 苯甲酸中含有羧基,能形成盐、酯、酰胺、酸酐等,A正确;滤液经过萃取分为有机相和水相,
有机相经无水硫酸钠干燥后,蒸馏得到甲苯,水相经蒸发浓缩、冷却过滤得到苯甲酸,B错误;据B项
分析可知,甲苯、苯甲酸依次由①②获得,C正确;苯甲酸在100 ℃左右开始升华,故除了重结晶方法
外,也可用升华法精制苯甲酸,D正确。
7.A 溶液是无色的,则溶液中一定不存在Fe3+、Fe2+和CrO。①向第一份溶液中加入过量
2
NaOH溶液并加热,能收集到标准状况下448 mL(0.02 mol)气体,说明原溶液中含有NH,且NH的物
质的量为0.02 mol×2=0.04 mol;无沉淀生成,则该溶液中不含Mg2+;再向冷却后的溶液中通入过量的
CO ,有白色沉淀[Al(OH) ]生成,经过滤、洗涤、灼烧后可得到1.02 g固体(Al O ),说明原溶液中含
2 3 2 3
有Al3+,不含CO,由铝原子守恒得原溶液中n(Al3+)=4n(AlO)=4×=0.04 mol。②向第二份溶液
2 3
中加入足量BaCl 溶液后,生成的白色沉淀经足量盐酸洗涤、干燥后可得到11.65 g固体(BaSO ),说明
2 4
原溶液中含有SO,不含Ba2+,则原溶液中n(SO)=2×=0.10 mol,故原溶液中c(SO)==0.5 mol·L-1;
再向滤液中加入AgNO 溶液有白色沉淀产生,由于加入了BaCl 溶液和盐酸,不能确定原溶液中是否
3 2
含有Cl-。溶液呈电中性,离子所带正电荷的物质的量为n(NH)+3n(Al3+)=1×0.04 mol+3×0.04 mol
=0.16 mol,离子所带负电荷的物质的量为2n(SO)=2×0.10 mol=0.20 mol,0.16 mol<0.20 mol,所以原
溶液中一定含有K+。故A项符合题意。
8.解析:澄清的溶液中可能含有NH、Mg2+、Ba2+、Al3+、Cl-、I-、NO、CO、SO、[Al(OH) ]-、SO;
4
取pH试纸检验,溶液呈强酸性,则不存在和氢离子反应的CO、[Al(OH) ]-、SO;取出部分溶液,加入
4
少量CCl 及数滴新制氯水,经振荡后CCl 层呈紫红色,说明氯气将碘离子氧化为碘单质,溶液中存在
4 4
I-,则不存在和I-反应的NO;另取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在
滴加过程中和滴加完毕后,溶液均无沉淀产生,则不存在和氢氧根离子反应的Mg2+、Al3+;取出部分
上述碱性溶液加Na CO 溶液后,有白色沉淀生成,说明存在和碳酸根离子反应的Ba2+,则不存在和
2 3
Ba2+反应的SO;将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,说明
生成了碱性气体氨气,则存在NH;不确定溶液中是否存在Cl-。
答案:(1)CO、[Al(OH) ]-、SO (2)NO
4
(3)Mg2+ Al3+ (4)SO (5)NH、Ba2+、I- Cl-
9.解析:由题意得步骤Ⅰ、Ⅱ为加入反应物,步骤Ⅲ中反应生成[Co(NH )]Cl ,冷却后
3 6 3
[Co(NH )]Cl 析出,过滤得到活性炭和[Co(NH )]Cl 的混合物,步骤Ⅳ中[Co(NH )]Cl 溶于沸水,趁
3 6 3 3 6 3 3 6 3
热过滤除去活性炭,步骤Ⅴ中得到[Co(NH )]Cl 晶体。(1)仪器a的名称为锥形瓶,根据题给步骤Ⅰ中
3 6 3
使用的部分仪器可知,加快NH Cl溶解的操作有用玻璃棒搅拌、用酒精灯加热。(2)根据所加试剂的性
4
质可分析步骤Ⅱ中将溶液温度降至10 ℃以下的原因,可选用冰水浴降温。(5)根据同离子效应可知,向
滤液中加入浓盐酸(提供Cl-),能抑制[Co(NH )]Cl 溶解,利于析出橙黄色晶体。
3 6 3
答案:(1)锥形瓶 用玻璃棒搅拌、用酒精灯加热 (2)H O 分解 浓氨水挥发 冰水浴
2 2
(3)玻璃棒末端没有靠在3层滤纸上、漏斗下端尖嘴部分没有紧贴烧杯内壁 (4)活性炭
(5)促进[Co(NH )]Cl 结晶析出
3 6 3
10.解析:A装置为气体发生装置,制备NO气体,发生反应为3Cu+8HNO ===3Cu(NO ) +
3 3 2
2NO↑+4HO;B装置为干燥装置,除去NO中的水蒸气;C装置为反应装置;D装置为尾气处理装置。
2
(2)装置内若含有较多的空气,会将NO氧化成NO ,故可在反应前将装置内的空气排尽,改进措施为
2
在A装置左边,从左到右持续通入氮气。(5)NO在酸性条件下具有氧化性,向酸性硫酸亚铁溶液中加
入亚硝酸钠,亚铁离子被氧化成铁离子,溶液变黄,生成的NO与亚铁离子结合成[Fe(NO)]2+,使溶液呈棕色,其反应为Fe2++NO===[Fe(NO)]2+。
答案:(1)3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
(2)在A装置左边,从左到右持续通入氮气 (3)5NO+3MnO+4H+===3Mn2++5NO+2HO
2
(4)亚硝酸钠属于强碱弱酸盐,在溶液中,NO水解呈碱性,加入酚酞溶液,溶液变为浅红色,加热使水
解平衡向右移动,溶液碱性增强,红色加深 (5)Fe2++NO===[Fe(NO)]2+ (6)加热使[Fe(NO)]2+分
解生成NO,NO在试管口遇空气被氧化为红棕色二氧化氮,溶液中铁离子水解平衡右移生成氢氧化铁
红褐色沉淀