文档内容
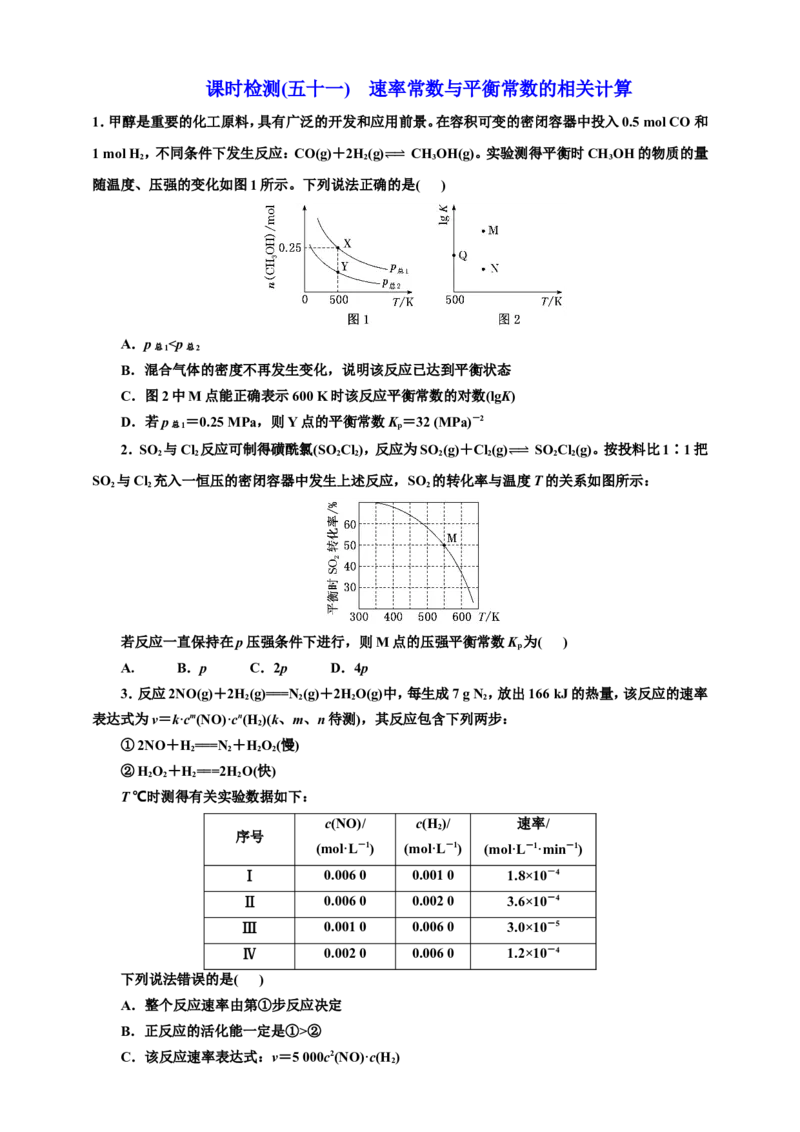
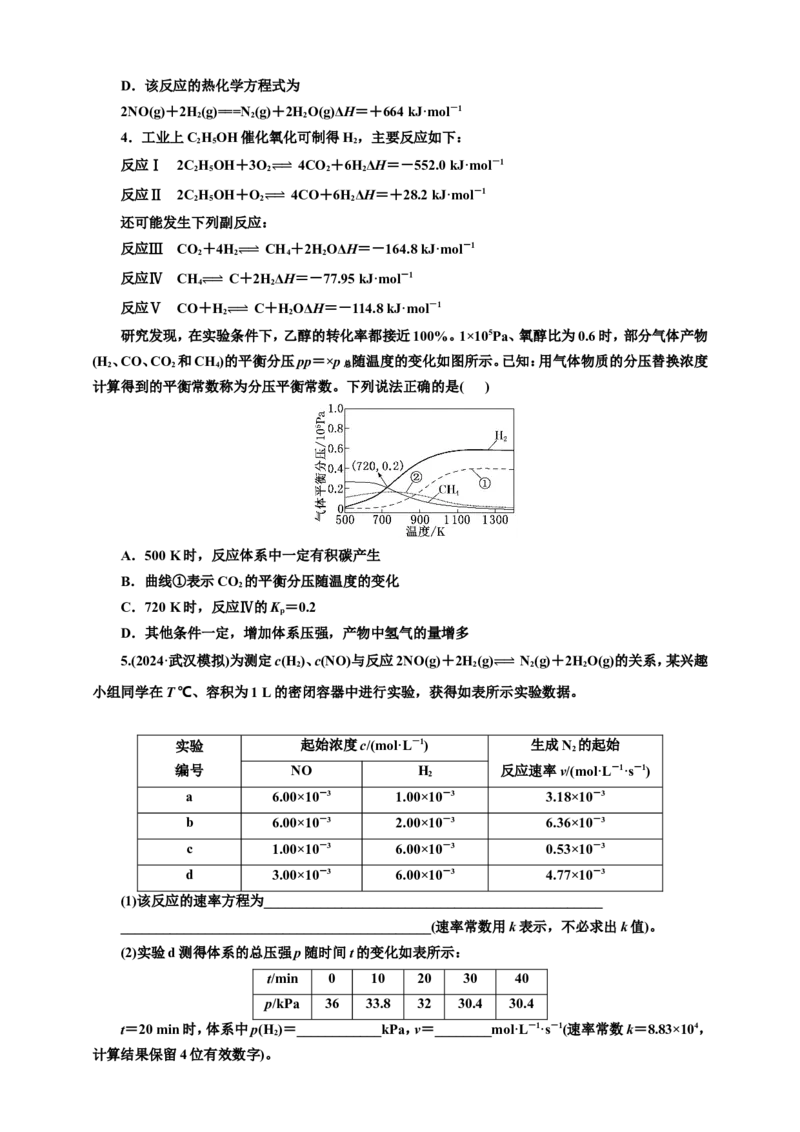
② C.该反应速率表达式:v=5 000c2(NO)·c(H ) 2D.该反应的热化学方程式为 2NO(g)+2H(g)===N (g)+2HO(g)ΔH=+664 kJ·mol-1 2 2 2 4.工业上CHOH催化氧化可制得H,主要反应如下: 2 5 2 反应Ⅰ 2CHOH+3O 4CO +6HΔH=-552.0 kJ·mol-1 2 5 2 2 2 反应Ⅱ 2C 2 H 5 OH+O 2 ⥫⥬ 4CO+6H 2 ΔH=+28.2 kJ·mol-1 还可能发生下列副反应: ⥫⥬ 反应Ⅲ CO +4H CH +2HOΔH=-164.8 kJ·mol-1 2 2 4 2 反应Ⅳ CH 4 C⥫+⥬2H 2 ΔH=-77.95 kJ·mol-1 反应Ⅴ CO+⥫⥬H 2 C+H 2 OΔH=-114.8 kJ·mol-1 研究发现,在实验 ⥫ 条 ⥬ 件下,乙醇的转化率都接近100%。1×105Pa、氧醇比为0.6时,部分气体产物 (H 、CO、CO 和CH )的平衡分压pp=×p 随温度的变化如图所示。已知:用气体物质的分压替换浓度 2 2 4 总 计算得到的平衡常数称为分压平衡常数。下列说法正确的是( ) A.500 K时,反应体系中一定有积碳产生 B.曲线①表示CO 的平衡分压随温度的变化 2 C.720 K时,反应Ⅳ的K =0.2 p D.其他条件一定,增加体系压强,产物中氢气的量增多 5.(2024·武汉模拟)为测定c(H )、c(NO)与反应2NO(g)+2H(g) N(g)+2HO(g)的关系,某兴趣 2 2 2 2 小组同学在T ℃、容积为1 L的密闭容器中进行实验,获得如表所⥫示⥬实验数据。 实验 起始浓度c/(mol·L-1) 生成N 的起始 2 编号 NO H 反应速率v/(mol·L-1·s-1) 2 a 6.00×10-3 1.00×10-3 3.18×10-3 b 6.00×10-3 2.00×10-3 6.36×10-3 c 1.00×10-3 6.00×10-3 0.53×10-3 d 3.00×10-3 6.00×10-3 4.77×10-3 (1)该反应的速率方程为________________________________________________ ____________________________________________(速率常数用k表示,不必求出k值)。 (2)实验d测得体系的总压强p随时间t的变化如表所示: t/min 0 10 20 30 40 p/kPa 36 33.8 32 30.4 30.4 t=20 min时,体系中p(H )=____________kPa,v=________mol·L-1·s-1(速率常数k=8.83×104, 2 计算结果保留4位有效数字)。6.碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。Bodensteins 研究了反应 2HI(g)H(g)+I(g),在716 K时气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如 2 2 表: t/min 0 20 40 60 80 120 x(HI) 1 0.91 0.85 0.815 0.795 0.784 x(HI) 0 0.60 0.73 0.773 0.780 0.784 回答下列问题: (1)根据上述实验结果,该反应的平衡常数K的计算式为________________________。 (2)上述反应中,正反应速率为v =k x2(HI),逆反应速率为v =k x(H )x(I ),其中k 、k 为速 正 正 逆 逆 2 2 正 逆 率常数,则120 min时,k 为______(以K和k 表示)。若k =0.002 7 min-1,在t=40 min时,v = 逆 正 正 正 ________min-1。 7.(2024·全国高三专题练习)在催化剂存在下用H 还原CO 是解决温室效应的重要手段之一,相 2 2 关反应如下: 主反应CO (g)+4H(g) CH (g)+2HO(g)ΔH=-164.0 kJ·mol-1 2 2 4 2 1 副反应CO 2 (g)+H 2 (g) ⥫⥬ CO(g)+H 2 O(g)ΔH 2 =+41.2 kJ·mol-1 T ℃时,若在体积恒为 ⥫⥬2 L的密闭容器中同时发生上述反应,将物质的量之和为 5 mol的H 2 和 CO 以不同的投料比进行反应,结果如图所示。若a、b表示反应物的转化率,则表示H 转化率的是 2 2 ___________,c、d分别表示CH (g)和CO(g)的体积分数,由图可知=__________时,甲烷产率最高。若 4 该条件下CO的产率趋于0,则T ℃时主反应的平衡常数K=__________。 8.机动车尾气的主要污染物是氮的氧化物,采用合适的催化剂可分解NO,反应为2NO(g) N(g)+O(g) ΔH,在T℃和T℃时,分别在容积均为1 L的密闭容器中通入1 mol NO,并发生上⥫⥬述 2 2 1 2 反应,NO的转化率随时间的变化曲线如图所示: (1)T______T,ΔH______0。(填“>”或“<”) 1 2 (2)温度为T℃时,该反应的平衡常数K=__________(结果保留3位小数)。已知反应速率v =k 1 正 正 c2(NO),v =k c(N )·c(O ),k 、k 分别为正反应速率常数和逆反应速率常数,则 a点处= 逆 逆 2 2 正 逆 __________。9.工业上用二氧化碳催化加氢可合成乙醇,其反应原理为 2CO (g)+6H(g) CHOH(g)+ 2 2 2 5 3HO(g) ΔH。 ⥫⥬ 2 (1)该反应的ΔH________(填“>”“<”或“=”) 0;其正反应在________(填“高温”“低温”或 “任何温度”)下能自发进行。 (2)该反应的反应速率表达式为v =k ·c2(CO)·c6(H ),v =k ·c(C HOH)·c3(H O),其中k 、k 正 正 2 2 逆 逆 2 5 2 正 为速率常数。则该反应的平衡常数K=________(用含k 、k 的代数式表示),若其他条件不变,降低 逆 正 逆 温度,则下列推断合理的是________(填标号)。 A.k 增大,k 减小 正 逆 B.k 减小,k 增大 正 逆 C.k 减小的倍数大于k 正 逆 D.k 减小的倍数小于k 正 逆 课时检测(五十一) 1.B 压强增大,CO(g)+2H(g) CH OH(g)平衡正向移动,甲醇物质的量增大,故p >p , 2 3 总1 总2 A错误;ρ=,气体质量不变,容器容积⥫可⥬变,达到平衡时,容器容积不变,则ρ不变,故混合气体的密度 不再发生变化可说明该反应已达到平衡状态,B正确;由题图1可知,压强一定时,升高温度,甲醇的 物质的量减少,平衡逆向移动,则lgK减小,由题图2知,500 K时,lgK对应的点为Q,升温lgK减小, 故N点能正确表示600 K时该反应平衡常数的对数(lgK),C错误;X、Y点温度相同,则平衡常数相同, X点甲醇的物质的量为0.25 mol,则列三段式可得: CO(g)+2H(g) CH OH(g) 2 3 起始量/mol 0.5 1 ⥫⥬ 0 转化量/mol 0.25 0.5 0.25 平衡量/mol 0.25 0.5 0.25 则K(Y)=K(X)= =64 (MPa)-2,D错误。 2.A 据图可知M点SO 的转化率为50%,设初始投料为2 mol SO 和2 mol Cl ,列三段式有 2 2 2 SO (g)+Cl (g) SO Cl (g) 2 2 2 2 起始/mol 2 2 0 ⥫⥬ 转化/mol 1 1 1 平衡/mol 1 1 1 所以p(SO )=p(Cl)=p(SO Cl )=p,所以K ==。 2 2 2 2 p 3.D 反应过程中反应慢的反应①决定整个反应速率,A正确;反应①慢,说明第①步反应的活化 能高,正反应的活化能一定是①>②,B正确;比较实验Ⅰ、Ⅱ数据可知,NO浓度不变,氢气浓度增大一 倍,反应速率增大一倍,比较实验Ⅲ、Ⅳ数据可知,H 浓度不变,NO浓度增大一倍,反应速率增大四倍, 2 据此得到速率方程:v=kc2(NO)·c(H ),依据实验Ⅰ中数据计算 k=5 000,则速率表达式为v=5 2 000c2(NO)·c(H ),C正确;反应2NO(g)+2H(g)===N (g)+2HO(g)中,每生成7 g N 放出166 kJ的热 2 2 2 2 2 量,生成28 g N 放热664 kJ,热化学方程式为2NO(g)+2H(g)===N (g)+2HO(g) ΔH=-664 2 2 2 2kJ·mol-1,D错误。 4.A 反应Ⅰ是放热反应,反应Ⅱ是吸热反应,升高温度,反应Ⅰ平衡逆向移动,反应Ⅱ平衡正向 移动,CO 的平衡分压减小,CO的平衡分压增大,因此曲线①表示CO的平衡分压随温度的变化,曲 2 线②表示CO 的平衡分压随温度的变化。由题图可知,500 K时,H、CO、CO 、CH 4种气体中H 和 2 2 2 4 2 CO的平衡分压最小,说明反应Ⅴ正向进行的程度大,反应体系中一定有积碳产生,故A正确;由分析 可知,曲线①表示CO的平衡分压随温度的变化,故B错误;反应Ⅳ的K =,由题图可知,720 K时,p p =p,则K =p(H )=0.2×105,故C错误;反应Ⅰ、Ⅱ均是气体体积增大的反应,增加体系压强,平衡均逆 p 2 向移动,产物中氢气的量减少,故D错误。 5.解析:(1)对比a、b组实验可知,反应速率与c(H )成正比,对比c、d组实验可知,反应速率与 2 c2(NO)成正比,故该反应的速率方程为v=k·c(H )·c2(NO)。(2)兴趣小组同学在T ℃、容积为1 L的密闭 2 容器中进行实验,根据表格所给数据,设生成N 的浓度为x mol·L-1,列三段式如下: 2 2H(g) + 2NO(g) N(g)+ 2HO(g) 2 2 2 0 0 ⥫⥬ 2x 2x x 2x x 2x 由此得20 min时气体总物质的量=(9×10-3-x)mol·L-1×1 L=(9×10-3-x)mol;恒温恒容下,气 体的压强之比等于物质的量之比,=,即=,解得x=1×10-3,故20 min 时,n(H )=(6×10-3-2x)mol·L 2 -1×1 L=4×10-3 mol,n(总)=(9×10-3-x)mol=8×10-3 mol,故p(H )=p(总)·=32 kPa×=16 kPa;20 2 min时,c(H )=4×10-3 mol·L-1,c(NO)=(3×10-3-2x)mol·L-1=1×10-3 mol·L-1,故反应速率v= 2 k·c(H )·c2(NO)=[8.83×104×4×10-3×(1×10-3)2]mol·L-1·s-1=3.532×10-4 mol·L-1·s-1。 2 答案:(1)v=kc(H )·c2(NO) (2)16 3.532×10-4 2 6.解析:(1)由表中数据可知,无论是从正反应方向开始,还是从逆反应方向开始,最终x(HI)均为 0.784,说明此时已达到了平衡状态。设HI的初始浓度为1 mol·L-1,则: 2HI(g) H(g)+I(g) 2 2 初始浓度/(mol·L-1) 1 ⥫ ⥬ 0 0 0.216 0.108 0.108 0.784 0.108 0.108 K== (2)建立平衡时,v =v ,即k x2(HI)=k x(H )·x(I ),k =k =k =。在40 min时,x(HI)= 正 逆 正 逆 2 2 逆 正 正 0.85,则v =0.002 7 min-1×0.852≈1.95×10-3 min-1。 正 答案:(1) (2) 1.95×10-3 7.解析:随着增大,H 的平衡转化率减小,CO 的平衡转化率增大,结合题图可得,b表示H 的平 2 2 2 衡转化率,a表示CO 的平衡转化率。c表示甲烷的体积分数,当=4时,甲烷产率最高,CO的产率趋于 2 0,由题意并结合题图得起始时c(CO)=0.5 mol·L-1,c(H )=2 mol·L-1,CO 、H 的平衡转化率均为 2 2 2 2 0.80,则列如下三段式: CO (g)+4H(g) CH (g)+2HO(g) 2 2 4 2 起始/ ⥫⥬ (mol·L-1) 0.5 2 0 0 转化/(mol·L-1) 0.4 1.6 0.4 0.8 平衡/ (mol·L-1) 0.1 0.4 0.4 0.8 平衡常数K===100。 答案:b 4 100 8.解析:(1)由图像可知,T℃下反应先达到化学平衡,故T>T,又T℃下NO的平衡转化率低于 1 1 2 1 T℃下NO的平衡转化率,即降低温度,平衡向正反应方向移动,故ΔH<0。(2)T℃条件下NO的平衡 2 1 转化率为21%,利用“三段式”法计算: 2NO(g) N(g)+O(g) 2 2 起始/(mol·L-1) 1 0 ⥫ ⥬ 0 转化/(mol·L-1) 0.21 0.105 0.105 平衡/(mol·L-1) 0.79 0.105 0.105 则平衡常数K=0.105 mol·L-1×0.105 mol·L-1÷(0.79 mol·L-1)2≈0.018。反应达到平衡时,v =v , 正 逆 故k c2(NO)=k c(N )·c(O ),即=K=0.018,a点对应的NO的转化率为20%,利用“三段式”法计 正 逆 2 2 算: 2NO(g) N(g)+O(g) 2 2 起始/(mol·L-1) 1 0 ⥫ ⥬ 0 转化/(mol·L-1) 0.2 0.1 0.1 平衡/(mol·L-1) 0.8 0.1 0.1 故a点处=K×=0.018×=1.152。 答案:(1)> < (2)0.018 1.152 9.解析:(1)反应2CO (g)+6H(g) CHOH(g)+3HO(g)生成气体物质的量减少,ΔS<0。该反 2 2 2 5 2 应能自发进行,根据ΔH-TΔS<0,该反应的ΔH<0;其正反应在低温下能自发进行。(2)反应达到平衡时 ⥫⥬ k ·c2(CO)·c6(H )=k ·c(C HOH)·c3(H O),K==。降低温度,正逆反应速率均减小,所以k 减小、k 正 2 2 逆 2 5 2 正 减小,故A错误,B错误;正反应放热,降低温度,平衡正向移动,v >v ,k 减小的倍数小于k 减小 逆 正 逆 正 逆 的倍数,故C错误,D正确。 答案:(1)< 低温 (2) D