文档内容
课时检测(五十二) 速率平衡的一般图像
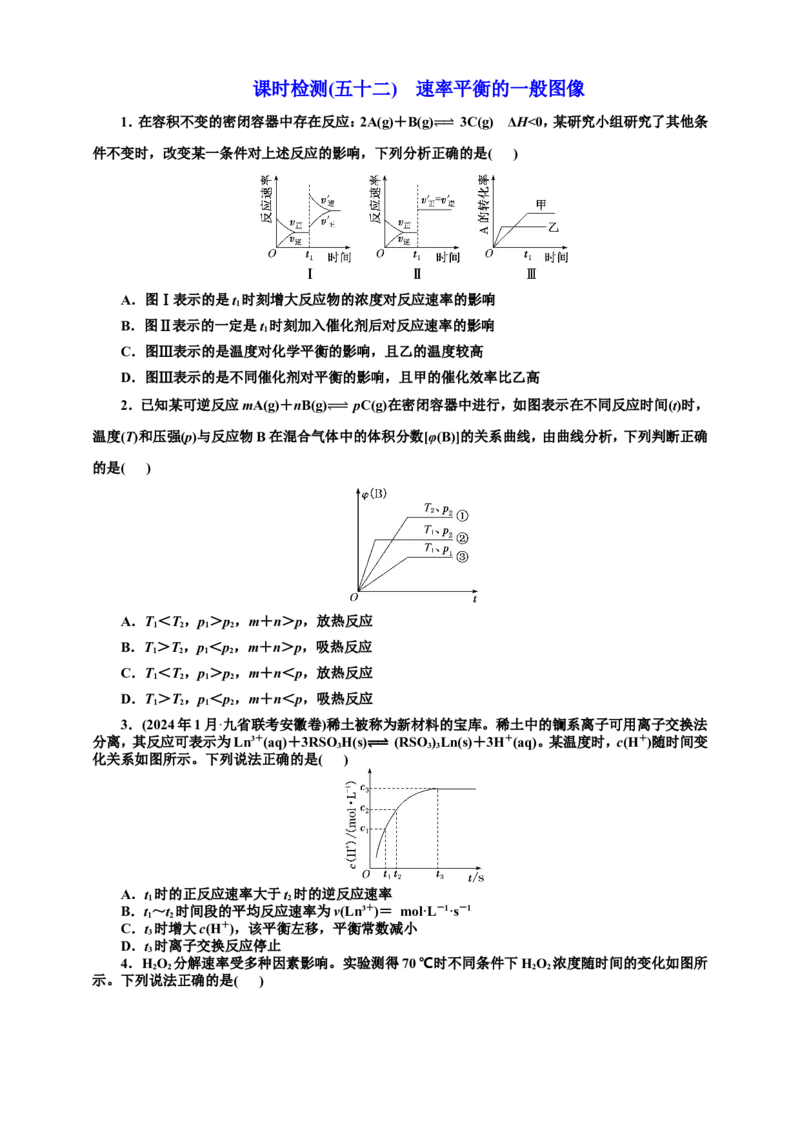
1.在容积不变的密闭容器中存在反应:2A(g)+B(g) 3C(g) ΔH<0,某研究小组研究了其他条
件不变时,改变某一条件对上述反应的影响,下列分析正⥫⥬确的是( )
A.图Ⅰ表示的是t 时刻增大反应物的浓度对反应速率的影响
1
B.图Ⅱ表示的一定是t 时刻加入催化剂后对反应速率的影响
1
C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D.图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高
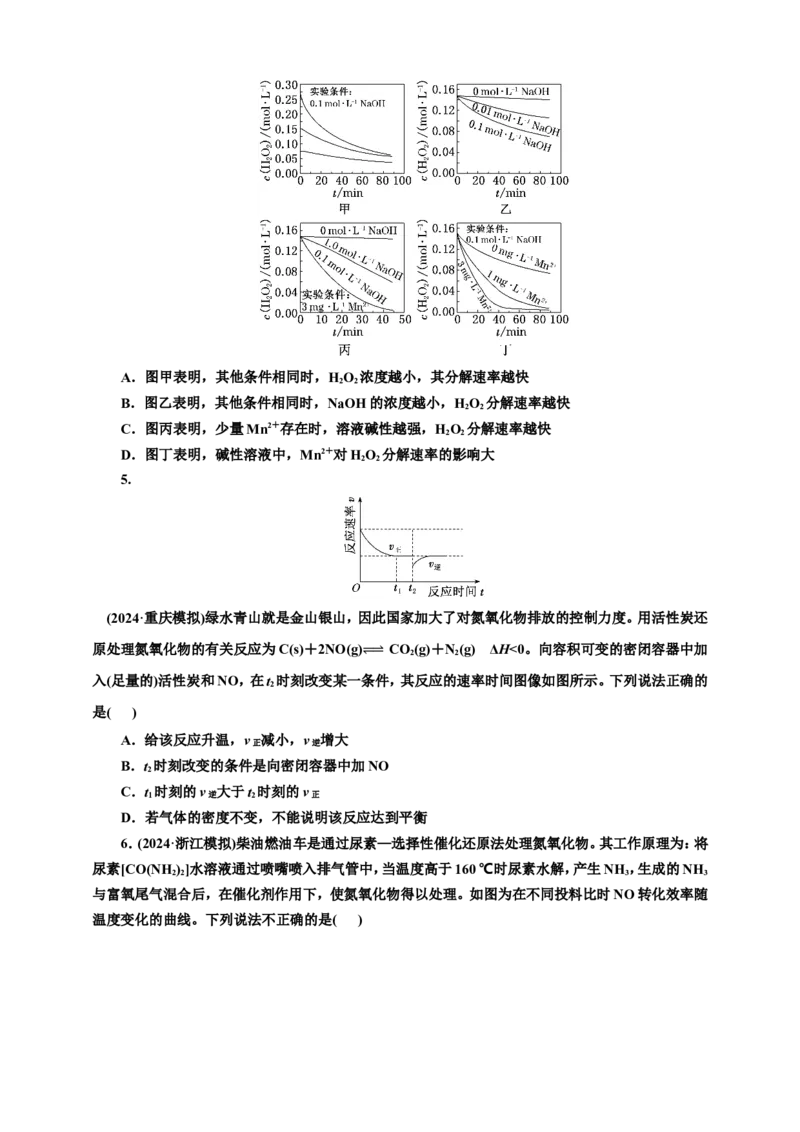
2.已知某可逆反应mA(g)+nB(g) pC(g)在密闭容器中进行,如图表示在不同反应时间(t)时,
温度(T)和压强(p)与反应物B在混合气体⥫⥬中的体积分数[φ(B)]的关系曲线,由曲线分析,下列判断正确
的是( )
A.T<T,p>p,m+n>p,放热反应
1 2 1 2
B.T>T,p<p,m+n>p,吸热反应
1 2 1 2
C.T<T,p>p,m+n<p,放热反应
1 2 1 2
D.T>T,p<p,m+n<p,吸热反应
1 2 1 2
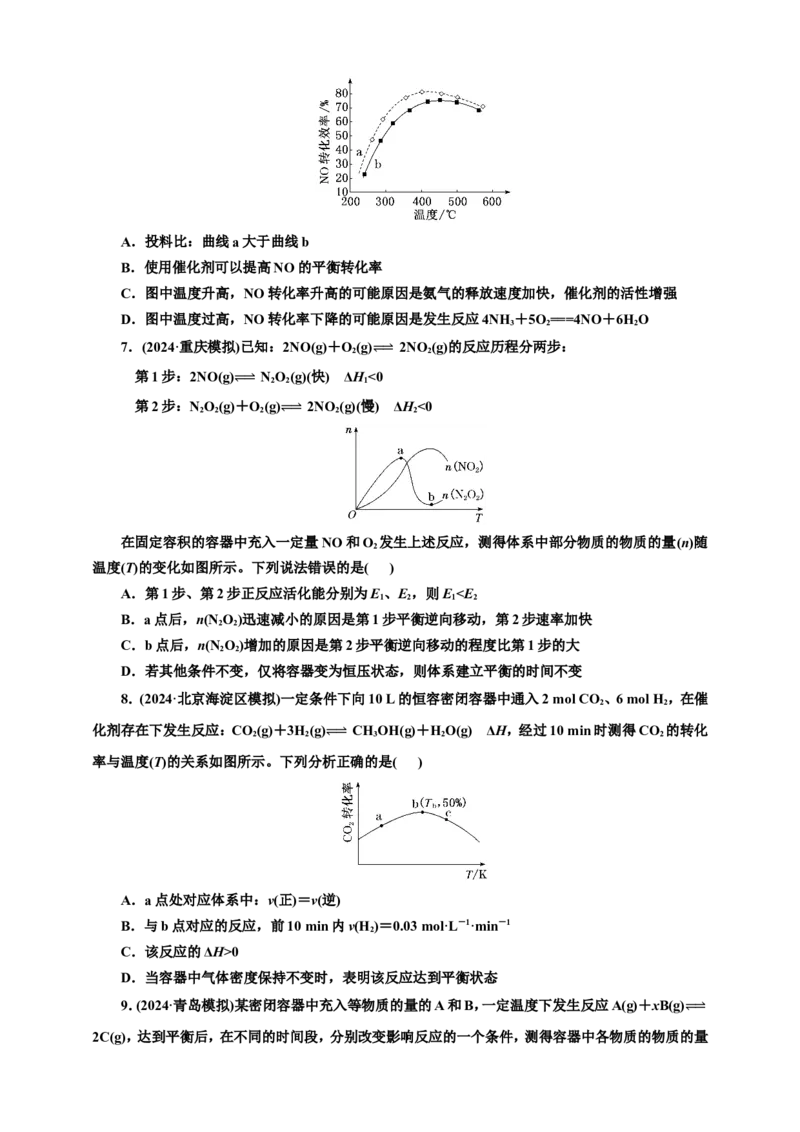
3.(2024年1月·九省联考安徽卷)稀土被称为新材料的宝库。稀土中的镧系离子可用离子交换法
分离,其反应可表示为Ln3+(aq)+3RSO H(s) (RSO )Ln(s)+3H+(aq)。某温度时,c(H+)随时间变
3 3 3
化关系如图所示。下列说法正确的是( )
⥫⥬
A.t 时的正反应速率大于t 时的逆反应速率
1 2
B.t~t 时间段的平均反应速率为v(Ln3+)= mol·L-1·s-1
1 2
C.t 时增大c(H+),该平衡左移,平衡常数减小
3
D.t 时离子交换反应停止
3
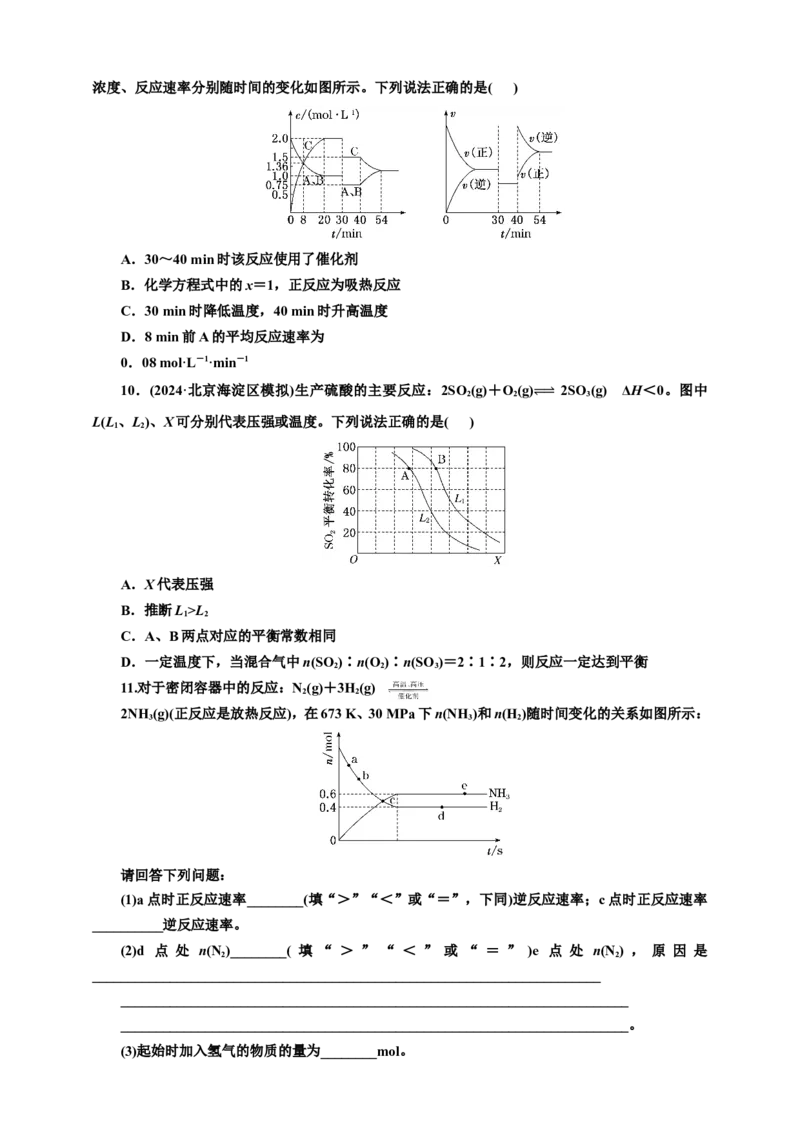
4.HO 分解速率受多种因素影响。实验测得70 ℃时不同条件下HO 浓度随时间的变化如图所
2 2 2 2
示。下列说法正确的是( )A.图甲表明,其他条件相同时,HO 浓度越小,其分解速率越快
2 2
B.图乙表明,其他条件相同时,NaOH的浓度越小,HO 分解速率越快
2 2
C.图丙表明,少量Mn2+存在时,溶液碱性越强,HO 分解速率越快
2 2
D.图丁表明,碱性溶液中,Mn2+对HO 分解速率的影响大
2 2
5.
(2024·重庆模拟)绿水青山就是金山银山,因此国家加大了对氮氧化物排放的控制力度。用活性炭还
原处理氮氧化物的有关反应为C(s)+2NO(g) CO (g)+N(g) ΔH<0。向容积可变的密闭容器中加
2 2
入(足量的)活性炭和NO,在t 时刻改变某一条⥫⥬件,其反应的速率时间图像如图所示。下列说法正确的
2
是( )
A.给该反应升温,v 减小,v 增大
正 逆
B.t 时刻改变的条件是向密闭容器中加NO
2
C.t 时刻的v 大于t 时刻的v
1 逆 2 正
D.若气体的密度不变,不能说明该反应达到平衡
6.(2024·浙江模拟)柴油燃油车是通过尿素—选择性催化还原法处理氮氧化物。其工作原理为:将
尿素[CO(NH )]水溶液通过喷嘴喷入排气管中,当温度高于160 ℃时尿素水解,产生NH ,生成的NH
2 2 3 3
与富氧尾气混合后,在催化剂作用下,使氮氧化物得以处理。如图为在不同投料比时NO转化效率随
温度变化的曲线。下列说法不正确的是( )A.投料比:曲线a大于曲线b
B.使用催化剂可以提高NO的平衡转化率
C.图中温度升高,NO转化率升高的可能原因是氨气的释放速度加快,催化剂的活性增强
D.图中温度过高,NO转化率下降的可能原因是发生反应4NH +5O===4NO+6HO
3 2 2
7.(2024·重庆模拟)已知:2NO(g)+O(g) 2NO (g)的反应历程分两步:
2 2
第1步:2NO(g) N
2
O
2
(g)(快) ΔH
1
<⥫0⥬
第2步:N
2
O
2
(g)⥫+⥬O
2
(g) 2NO
2
(g)(慢) ΔH
2
<0
⥫⥬
在固定容积的容器中充入一定量NO和O 发生上述反应,测得体系中部分物质的物质的量(n)随
2
温度(T)的变化如图所示。下列说法错误的是( )
A.第1步、第2步正反应活化能分别为E 、E ,则E 0
D.当容器中气体密度保持不变时,表明该反应达到平衡状态
9.(2024·青岛模拟)某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的⥫量⥬浓度、反应速率分别随时间的变化如图所示。下列说法正确的是( )
A.30~40 min时该反应使用了催化剂
B.化学方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的平均反应速率为
0.08 mol·L-1·min-1
10.(2024·北京海淀区模拟)生产硫酸的主要反应:2SO (g)+O(g) 2SO (g) ΔH<0。图中
2 2 3
L(L、L)、X可分别代表压强或温度。下列说法正确的是( ) ⥫⥬
1 2
A.X代表压强
B.推断L>L
1 2
C.A、B两点对应的平衡常数相同
D.一定温度下,当混合气中n(SO )∶n(O )∶n(SO )=2∶1∶2,则反应一定达到平衡
2 2 3
11.对于密闭容器中的反应:N(g)+3H(g)
2 2
2NH (g)(正反应是放热反应),在673 K、30 MPa下n(NH)和n(H )随时间变化的关系如图所示:
3 3 2
请回答下列问题:
(1)a点时正反应速率________(填“>”“<”或“=”,下同)逆反应速率;c点时正反应速率
__________逆反应速率。
(2)d 点 处 n(N )________( 填 “ > ” “ < ” 或 “ = ” )e 点 处 n(N ) , 原 因 是
2 2
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)起始时加入氢气的物质的量为________mol。(4)若温度、压强不变,反应在加入催化剂条件下进行,在上图的基础上画出n(NH)和n(H )随时间
3 2
变化的关系图。(已知催化剂不影响反应限度)。
12.向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s) yC(g) ΔH<0。
在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答⥫下⥬列问题:
(1)用A的浓度变化表示该反应在0~10 min内的平均反应速率v(A)=________。
(2)根据图示可确定x∶y=________。
(3)推测第10 min引起曲线变化的反应条件可能是________(填编号,下同);第16 min引起曲线变
化的反应条件可能是________。
①减压 ②增大A的浓度 ③增大C的量
④升温 ⑤降温 ⑥加催化剂
(4)若平衡Ⅰ的平衡常数为K ,平衡Ⅱ平衡常数为K ,则K ________K (填“>”“=”或“<”)。
1 2 1 2
13.工业上,常采用氧化还原方法处理尾气中的CO、NO。
氧化法:沥青混凝土可作为反应2CO(g)+O(g) 2CO (g)的催化剂。下图表示在相同的恒容密
2 2
闭容器、相同起始浓度、相同反应时间段下,使用同质⥫⥬量的不同沥青混凝土(α型、β型)催化时,CO的
转化率与温度的关系。
(1)在a、b、c、d四点中,未达到平衡状态的是________。
(2)已知c点时容器中O 浓度为0.04 mol·L-1,则50 ℃时,在α型沥青混凝土中CO转化反应的平
2
衡常数K=________(用含x的代数式表示)。
(3)下列关于上图的说法正确的是________(填字母)。
A.CO转化反应的平衡常数:K(a)<K(c)
B.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
C.b点时CO与O 分子之间发生有效碰撞的概率在整个实验过程中最高
2
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
课时检测(五十二)
1.C 增大反应物浓度瞬间,正反应速率增大,但逆反应速率不增大,故图Ⅰ不能表示t 时刻增大
1
反应物的浓度对反应速率的影响,故A错误;该反应增大压强或加入催化剂,都可以同等程度的增大反应速率,平衡不移动,故图Ⅱ可能表示的是t 时刻加入催化剂或加压对反应速率的影响,故B错误;
1
升温,化学反应速率加快,缩短达平衡的时间,平衡逆向移动,A的转化率降低,故图Ⅲ表示的是温度
对化学平衡的影响,且乙的温度较高,故C正确;催化剂能改变反应速率,影响达平衡的时间,但不会
影响平衡移动,不能影响反应物的转化率,故图Ⅲ不能表示不同催化剂对平衡的影响,故D错误。
2.D 由题图可知,压强一定时,温度T 先达到平衡,故温度:T>T,升高温度,B在混合气体中
1 1 2
的体积分数减小,说明平衡正向移动,正反应为吸热反应;温度一定时,压强p 先达到平衡,故压强:p
2 1
<p,增大压强,B在混合气体中的体积分数增大,说明平衡逆向移动,正反应为气体体积增大的反应,
2
则m+n<p。
3.A 随着反应的进行,反应物浓度逐渐下降,生成物浓度逐渐上升,直到达到平衡,即正反应逐
渐下降,逆反应逐渐上升,直到相等,期间正反应速率始终大于逆反应速率,A正确;化学反应速率之
比等于化学计量数之比,即v(Ln3+)= mol·L-1·s-1,B错误;温度不变,平衡常数不变,C错误;t 时反
3
应达到平衡,此时的平衡是一种动态平衡,v =v ,反应并未停止,D错误。
正 逆
4.D 由题图甲可知,起始时HO 的浓度越小,曲线下降越平缓,说明反应速率越慢,A项错误;
2 2
由题图乙可知0.1 mol·L-1NaOH对应的曲线下降最快,即HO 分解速率最快,B项错误;由题图丙可
2 2
知,相同时间内,0.1 mol·L-1NaOH条件下HO 分解速率最快,0 mol·L-1NaOH条件下HO 分解速
2 2 2 2
率最慢,而1.0 mol·L-1NaOH条件下HO 的分解速率处于中间,C项错误;由题图丁可知,Mn2+浓度
2 2
越大,HO 的分解速率越快,说明Mn2+对HO 分解速率影响较大,D项正确。
2 2 2 2
5.B 升高温度,任何反应的反应速率均增大,故给该反应升温,v 增大,v 增大,A错误;由图像
正 逆
可知,压强一定条件下,t 时刻改变条件以后,逆反应速率突然减小,达到新平衡时,与原反应速率相同,
2
故改变的条件是向密闭容器中加NO,B正确;由B项分析可知,t 时刻改变的条件是向密闭容器中加
2
NO,正反应速率增大,逆反应速率减小,则t 时刻的v 小于t 时刻的v ,C错误;由题干反应方程式
1 逆 2 正
可知,反应前后气体的物质的量保持不变,即恒温下容器的体积保持不变,正反应方向气体质量增加,
故若气体的密度不变,则气体质量不变,说明该反应达到平衡,D错误。
6.B 尿素分解产生氨气,氨气的浓度越大,越有利于NO的转化,则尿素与NO的比值为a曲线
大于b曲线,A项正确;催化剂可加快反应速率,但不会改变平衡转化率,B项错误;随着温度升高,尿
素分解氨气的速率加快,NH 的浓度变大,随着温度升高,催化剂活性增加,导致化学反应速率加快,C
3
项正确;温度过高,NO的转化效率下降,可能原因是发生反应4NH +5O===4NO+6HO,D项正确。
3 2 2
7.D 第2步是慢反应,由活化能越大反应速率越慢可知,第2步正反应活化能较大,即E L,故B正确;X代表温度,则A、B两点的温度不同,化学平衡常
1 2
数不同,故C错误;一定温度下,当混合气中n(SO )∶n(O )∶n(SO )=2∶1∶2时,反应混合物中各组
2 2 3
分的浓度不一定保持不变,不一定是平衡状态,故D错误。
11.解析:a、b、c三点反应都没有达到平衡状态,故正反应速率大于逆反应速率,但d、e点反应都
处于平衡状态,正、逆反应速率相等,各组分的含量保持不变。平衡时生成了0.6 mol氨气,则消耗了
0.9 mol 氢气,故起始时加入氢气的物质的量为0.4 mol+0.9 mol=1.3 mol。若加入催化剂,反应达到
平衡的时间缩短,但平衡时各物质的物质的量不变。
答案:(1)> > (2)= 当反应处于平衡状态时,混合物中各组分的含量保持不变 (3)1.3 (4)
如图虚线所示(只要体现出达到平衡的时间缩短,且平衡时NH 和H 的物质的量与原平衡一样即可)
3 2
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\5\\25HXCXYL6-70.TIF" \*
MERGEFORMATINET
12.解析:(1)0~10 min内v(A)==0.02 mol·L-1·min-1。(2)根据图像可知,0~10 min内A的物质
的量浓度减少量为0.2 mol·L-1,C的物质的量浓度增加量为0.4 mol·L-1,x、y之比等于A、C的浓度的
变化量之比,故x∶y=(0.2 mol·L-1)∶(0.4 mol·L-1)=1∶2。(3)根据图像可知,10 min 时改变条件后,
A、C的浓度瞬时不变且随后反应速率加快,故改变的条件可能是升温或加入催化剂;12~16 min,反
应处于平衡状态,16 min 时改变条件后,A、C的浓度瞬时不变,且随后A的浓度逐渐增大,C的浓度
逐渐减小,说明平衡逆向移动,故改变的条件可能是升温。(4)升高温度,平衡逆向移动,平衡常数减小。
由于16 min时升高温度,则K >K 。
1 2
答案:(1)0.02 mol·L-1·min-1 (2)1∶2 (3)④⑥ ④ (4)>
13.解析:(1)CO和O 的反应是放热反应,当达到平衡后升高温度,CO的转化率降低,所以,b、c、
2
d点表示平衡状态,a点对应的状态不是平衡状态。(2)令CO起始浓度为a mol·L-1。
2CO(g)+O(g) 2CO (g)
2 2
a 0
⥫⥬
ax ax
a(1-x) 0.04 ax
K==。(3)CO和O 的反应是放热反应,达到平衡后,温度升高,平衡向左移动,平衡常数K减小,
2
A项错误;观察图像知,β型催化剂作用下CO的转化速率大于α型催化剂,B项正确;有效碰撞概率
与反应速率有关,温度越高,反应速率越大,有效碰撞概率越高,故在图像中e点有效碰撞概率最高,C
项错误;催化剂需要一定活性温度,转化率出现突变,可能是因温度高而使催化剂失去活性,D项正确。答案:(1)a (2) (3)BD