文档内容
课时检测(五十六) 水的电离和溶液的pH的基本知能评价
1.下列说法正确的是( )
A.要量取18.90 mL溴水和双氧水均可选用碱式滴定管
B.25 mL的滴定管,若溶液的凹液面最低点处于10.00 mL,则滴定管内液体体积为15 mL
C.滴定时,眼睛注视滴定管液面,右手摇动锥形瓶
D.盐酸滴定氨水时用甲基橙作指示剂时,终点颜色变化为黄色变橙色,且30 s不变色
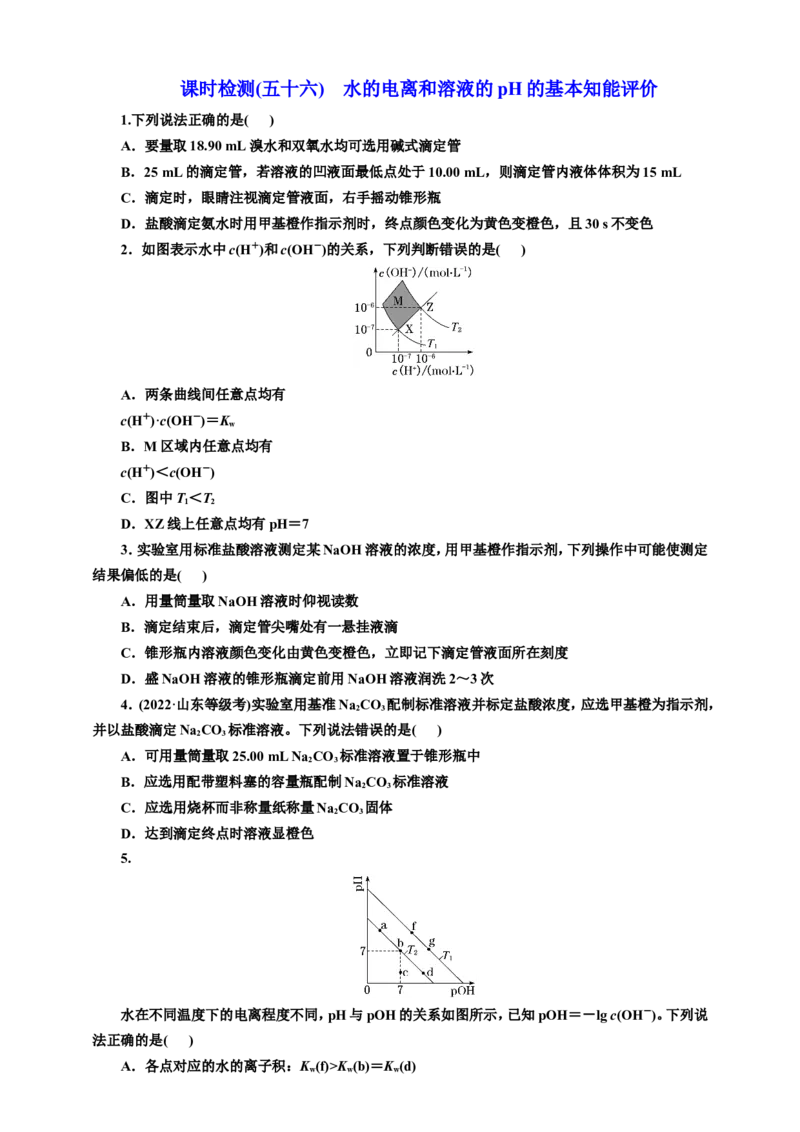
2.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有
c(H+)·c(OH-)=K
w
B.M区域内任意点均有
c(H+)<c(OH-)
C.图中T<T
1 2
D.XZ线上任意点均有pH=7
3.实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定
结果偏低的是( )
A.用量筒量取NaOH溶液时仰视读数
B.滴定结束后,滴定管尖嘴处有一悬挂液滴
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
4.(2022·山东等级考)实验室用基准Na CO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,
2 3
并以盐酸滴定Na CO 标准溶液。下列说法错误的是( )
2 3
A.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 3
B.应选用配带塑料塞的容量瓶配制Na CO 标准溶液
2 3
C.应选用烧杯而非称量纸称量Na CO 固体
2 3
D.达到滴定终点时溶液显橙色
5.
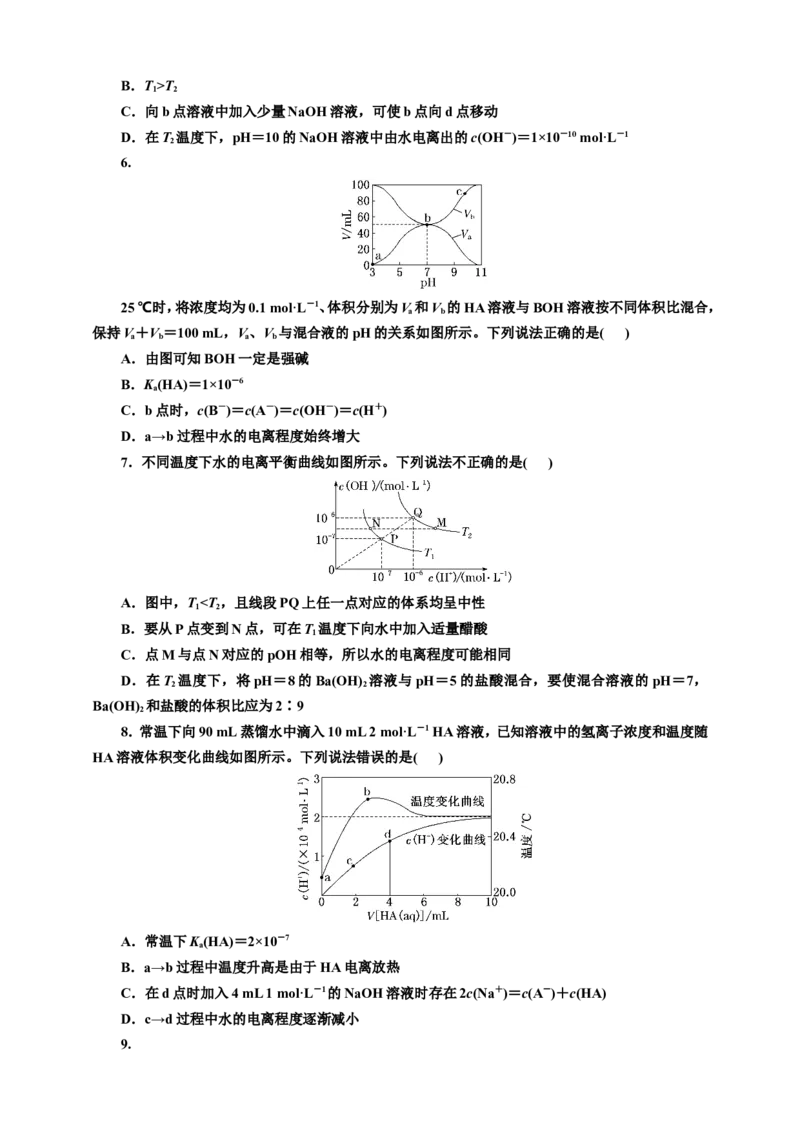
水在不同温度下的电离程度不同,pH与pOH的关系如图所示,已知pOH=-lg c(OH-)。下列说
法正确的是( )
A.各点对应的水的离子积:K (f)>K (b)=K (d)
w w wB.T>T
1 2
C.向b点溶液中加入少量NaOH溶液,可使b点向d点移动
D.在T 温度下,pH=10的NaOH溶液中由水电离出的c(OH-)=1×10-10 mol·L-1
2
6.
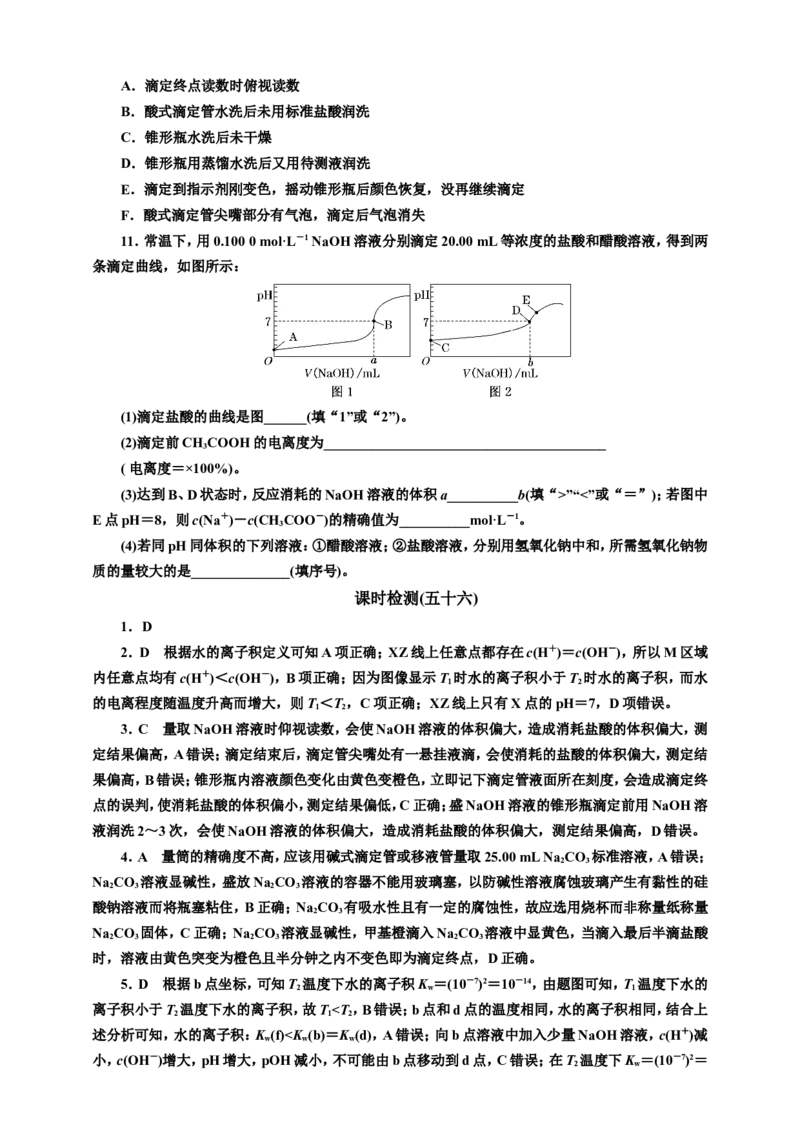
25 ℃时,将浓度均为0.1 mol·L-1、体积分别为V 和V 的HA溶液与BOH溶液按不同体积比混合,
a b
保持V+V =100 mL,V、V 与混合液的pH的关系如图所示。下列说法正确的是( )
a b a b
A.由图可知BOH一定是强碱
B.K (HA)=1×10-6
a
C.b点时,c(B-)=c(A-)=c(OH-)=c(H+)
D.a→b过程中水的电离程度始终增大
7.不同温度下水的电离平衡曲线如图所示。下列说法不正确的是( )
A.图中,T”“<”或“=”);若图中
E点pH=8,则c(Na+)-c(CHCOO-)的精确值为__________mol·L-1。
3
(4)若同pH同体积的下列溶液:①醋酸溶液;②盐酸溶液,分别用氢氧化钠中和,所需氢氧化钠物
质的量较大的是______________(填序号)。
课时检测(五十六)
1.D
2.D 根据水的离子积定义可知A项正确;XZ线上任意点都存在c(H+)=c(OH-),所以M区域
内任意点均有c(H+)<c(OH-),B项正确;因为图像显示T 时水的离子积小于T 时水的离子积,而水
1 2
的电离程度随温度升高而增大,则T<T,C项正确;XZ线上只有X点的pH=7,D项错误。
1 2
3.C 量取NaOH溶液时仰视读数,会使NaOH溶液的体积偏大,造成消耗盐酸的体积偏大,测
定结果偏高,A错误;滴定结束后,滴定管尖嘴处有一悬挂液滴,会使消耗的盐酸的体积偏大,测定结
果偏高,B错误;锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度,会造成滴定终
点的误判,使消耗盐酸的体积偏小,测定结果偏低,C正确;盛NaOH溶液的锥形瓶滴定前用NaOH溶
液润洗2~3次,会使NaOH溶液的体积偏大,造成消耗盐酸的体积偏大,测定结果偏高,D错误。
4.A 量筒的精确度不高,应该用碱式滴定管或移液管量取25.00 mL Na CO 标准溶液,A错误;
2 3
Na CO 溶液显碱性,盛放Na CO 溶液的容器不能用玻璃塞,以防碱性溶液腐蚀玻璃产生有黏性的硅
2 3 2 3
酸钠溶液而将瓶塞粘住,B正确;Na CO 有吸水性且有一定的腐蚀性,故应选用烧杯而非称量纸称量
2 3
Na CO 固体,C正确;Na CO 溶液显碱性,甲基橙滴入Na CO 溶液中显黄色,当滴入最后半滴盐酸
2 3 2 3 2 3
时,溶液由黄色突变为橙色且半分钟之内不变色即为滴定终点,D正确。
5.D 根据b点坐标,可知T 温度下水的离子积K =(10-7)2=10-14,由题图可知,T 温度下水的
2 w 1
离子积小于T 温度下水的离子积,故Tb;若题图中E点pH=8,则c(Na+)-c(CHCOO-)=c(OH-)-c(H+) = 1×10-6 mol·L-1-1×10-8
3
mol·L-1=9.9×10-7 mol·L-1。(4)同pH同体积的醋酸溶液与盐酸溶液,醋酸浓度远大于盐酸浓度,体积
相等,醋酸的物质的量大于盐酸的物质的量,因此所需氢氧化钠物质的量较大的是醋酸。
答案:(1)1 (2)1% (3)> 9.9×10-7 (4)①