文档内容
专练 19 氮及其化合物
一、单项选择题
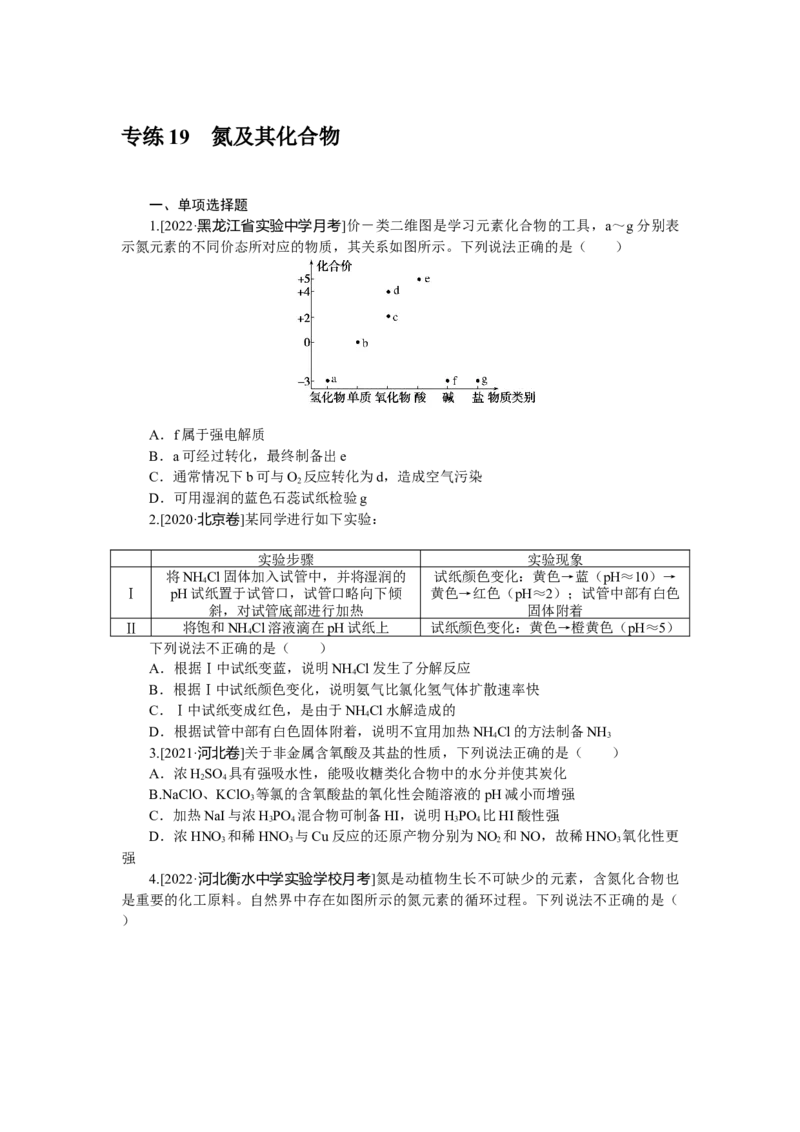
1.[2022·黑龙江省实验中学月考]价-类二维图是学习元素化合物的工具,a~g分别表
示氮元素的不同价态所对应的物质,其关系如图所示。下列说法正确的是( )
A.f属于强电解质
B.a可经过转化,最终制备出e
C.通常情况下b可与O 反应转化为d,造成空气污染
2
D.可用湿润的蓝色石蕊试纸检验g
2.[2020·北京卷]某同学进行如下实验:
实验步骤 实验现象
将NH Cl固体加入试管中,并将湿润的 试纸颜色变化:黄色→蓝(pH≈10)→
4
Ⅰ pH试纸置于试管口,试管口略向下倾 黄色→红色(pH≈2);试管中部有白色
斜,对试管底部进行加热 固体附着
Ⅱ 将饱和NH Cl溶液滴在pH试纸上 试纸颜色变化:黄色→橙黄色(pH≈5)
4
下列说法不正确的是( )
A.根据Ⅰ中试纸变蓝,说明NH Cl发生了分解反应
4
B.根据Ⅰ中试纸颜色变化,说明氨气比氯化氢气体扩散速率快
C.Ⅰ中试纸变成红色,是由于NH Cl水解造成的
4
D.根据试管中部有白色固体附着,说明不宜用加热NH Cl的方法制备NH
4 3
3.[2021·河北卷]关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更
3 3 2 3
强
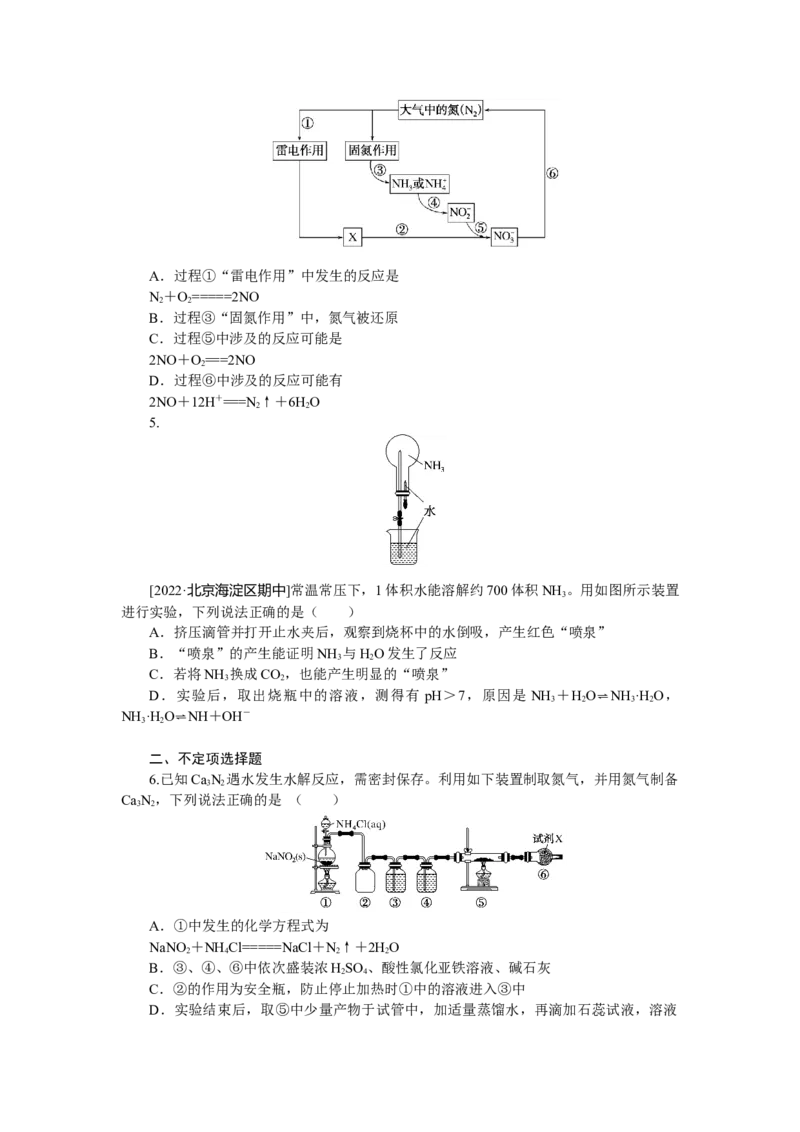
4.[2022·河北衡水中学实验学校月考]氮是动植物生长不可缺少的元素,含氮化合物也
是重要的化工原料。自然界中存在如图所示的氮元素的循环过程。下列说法不正确的是(
)A.过程①“雷电作用”中发生的反应是
N+O=====2NO
2 2
B.过程③“固氮作用”中,氮气被还原
C.过程⑤中涉及的反应可能是
2NO+O===2NO
2
D.过程⑥中涉及的反应可能有
2NO+12H+===N ↑+6HO
2 2
5.
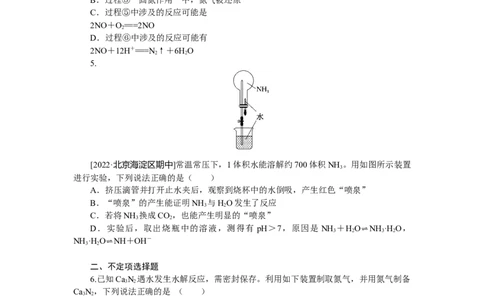
[2022·北京海淀区期中]常温常压下,1体积水能溶解约700体积NH 。用如图所示装置
3
进行实验,下列说法正确的是( )
A.挤压滴管并打开止水夹后,观察到烧杯中的水倒吸,产生红色“喷泉”
B.“喷泉”的产生能证明NH 与HO发生了反应
3 2
C.若将NH 换成CO,也能产生明显的“喷泉”
3 2
D.实验后,取出烧瓶中的溶液,测得有 pH>7,原因是 NH
3
+H
2
O⇌NH
3
·H
2
O,
NH
3
·H
2
O⇌NH+OH-
二、不定项选择题
6.已知Ca N 遇水发生水解反应,需密封保存。利用如下装置制取氮气,并用氮气制备
3 2
Ca N,下列说法正确的是 ( )
3 2
A.①中发生的化学方程式为
NaNO +NH Cl=====NaCl+N↑+2HO
2 4 2 2
B.③、④、⑥中依次盛装浓HSO 、酸性氯化亚铁溶液、碱石灰
2 4
C.②的作用为安全瓶,防止停止加热时①中的溶液进入③中
D.实验结束后,取⑤中少量产物于试管中,加适量蒸馏水,再滴加石蕊试液,溶液变蓝
7.一定量的浓硝酸与足量铜完全反应,得到硝酸铜溶液和NO 、NO的混合气体2.24 L
2
(标准状况),这些气体与一定体积O (标准状况)混合后通入水中,所有气体完全被水
2
吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,
则消耗NaOH溶液的体积是50 mL,下列说法正确的是( )
A.参加反应的硝酸是0.3 mol
B.消耗氧气的体积为1.68 L
C.混合气体中含NO 1.12 L
2
D.此反应过程中转移的电子为0.3 mol
8.[2022·西安五中高三期中测试]现用传感技术测定喷泉实验中的压强变化来认识喷泉
实验的原理。下列说法正确的是( )
A.制取氨气时烧瓶中的固体常用CaO或CaCl
2
B.将湿润的红色石蕊试纸置于三颈瓶口,试纸变蓝,说明NH 已经集满
3
C.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验
电脑绘制三颈瓶内压强变化曲线如图2,则E点时喷泉最剧烈
D.工业上,若出现液氨泄漏,喷稀盐酸比喷洒NaHCO 溶液处理效果好
3
三、非选择题
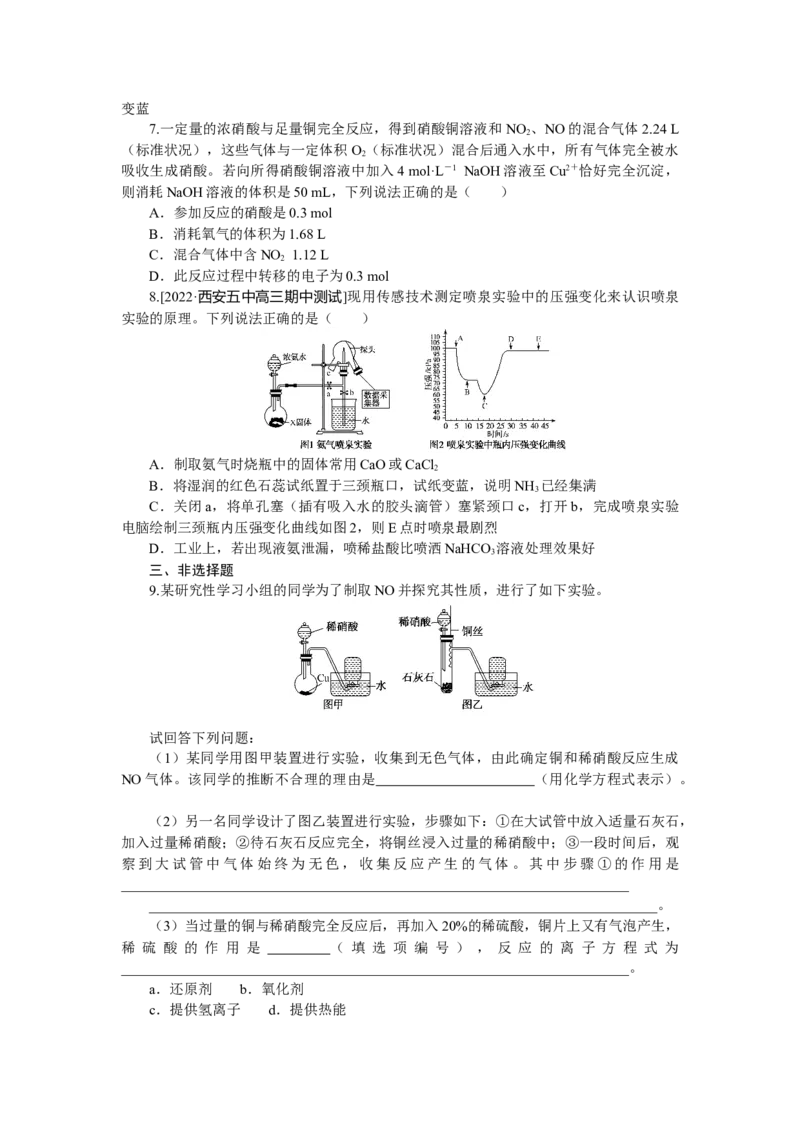
9.某研究性学习小组的同学为了制取NO并探究其性质,进行了如下实验。
试回答下列问题:
(1)某同学用图甲装置进行实验,收集到无色气体,由此确定铜和稀硝酸反应生成
NO气体。该同学的推断不合理的理由是 (用化学方程式表示)。
(2)另一名同学设计了图乙装置进行实验,步骤如下:①在大试管中放入适量石灰石,
加入过量稀硝酸;②待石灰石反应完全,将铜丝浸入过量的稀硝酸中;③一段时间后,观
察到大试管中气体始终为无色,收集反应产生的气体。其中步骤①的作用是
________________________________________________________________________
________________________________________________________________________。
(3)当过量的铜与稀硝酸完全反应后,再加入20%的稀硫酸,铜片上又有气泡产生,
稀 硫 酸 的 作 用 是 ( 填 选 项 编 号 ) , 反 应 的 离 子 方 程 式 为
________________________________________________________________________。
a.还原剂 b.氧化剂
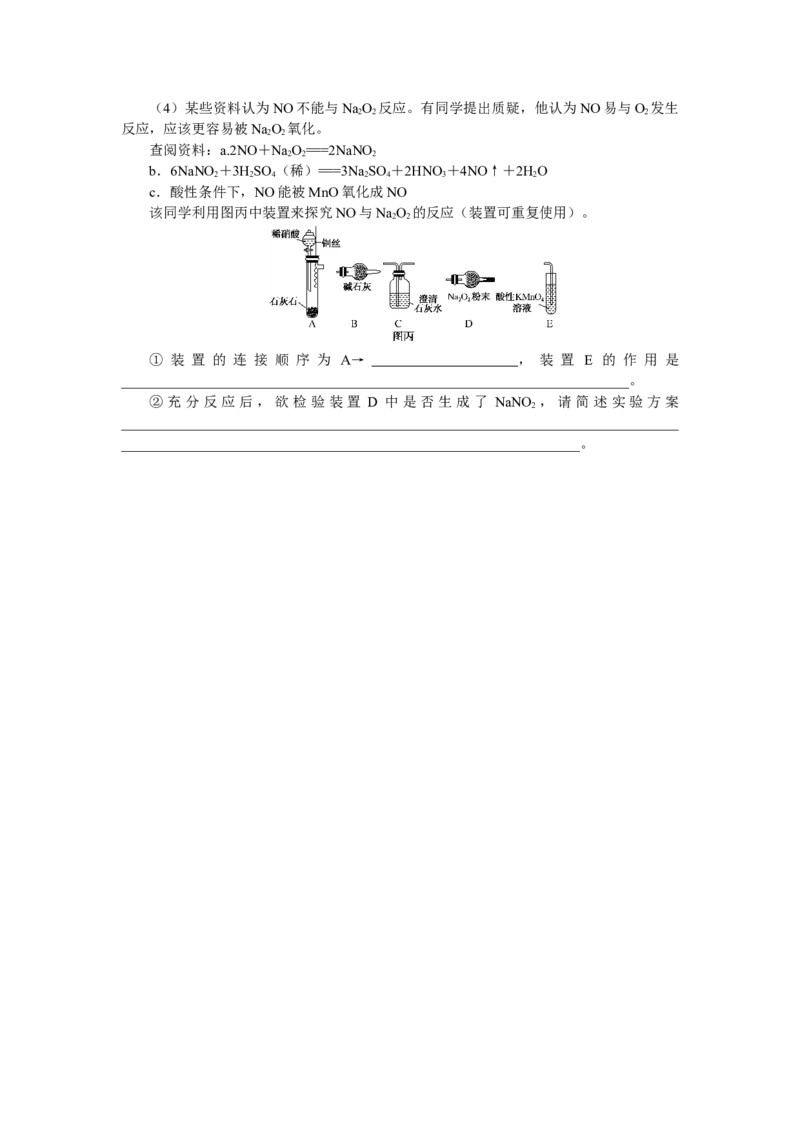
c.提供氢离子 d.提供热能(4)某些资料认为NO不能与NaO 反应。有同学提出质疑,他认为NO易与O 发生
2 2 2
反应,应该更容易被NaO 氧化。
2 2
查阅资料:a.2NO+NaO===2NaNO
2 2 2
b.6NaNO +3HSO (稀)===3Na SO +2HNO+4NO↑+2HO
2 2 4 2 4 3 2
c.酸性条件下,NO能被MnO氧化成NO
该同学利用图丙中装置来探究NO与NaO 的反应(装置可重复使用)。
2 2
① 装 置 的 连 接 顺 序 为 A→ , 装 置 E 的 作 用 是
________________________________________________________________________。
②充分反应后,欲检验装置 D 中是否生成了 NaNO ,请简述实验方案
2
_______________________________________________________________________________
_________________________________________________________________。