文档内容
专题 03 溶液
易错点1 误用胶体的特性
1.下列应用或事实与胶体的性质无关的是
A.清晨的阳光穿过茂密的林木枝叶所产生的美丽景象(美丽的光线)
B.用石膏或盐卤点制豆腐
C.向FeCl 溶液中滴加NaOH溶液出现红褐色沉淀
3
D.在海水与河水交界处,易形成沙洲
【错因分析】不能正确识记和理解胶体的概念及性质,而造成误选。
【试题解析】清晨的阳光穿过茂密的林木枝叶所产生的美丽景象,是胶体的丁达尔现象,与胶体有关,A
项正确;用石膏或盐卤点制豆腐,利用的是胶体的聚沉,和胶体性质有关,B项正确;在 FeCl 溶液中滴
3
加NaOH溶液出现红褐色沉淀,发生的是复分解反应,与胶体无关,C项错误;河流中的水含有泥沙胶粒,
海水中含有氯化钠、氯化钙等电解质,二者相遇是可以发生胶体凝聚,就形成三角洲,与胶体有关,D项
正确。答案选C。
【参考答案】C
【名师点拨】胶体区别于其它分散系的本质特征是分散质微粒直径在1nm-100nm之间;胶体具有丁达尔效
应,可以发生电泳现象,可以发生聚沉。
(1)丁达尔效应可以快速鉴别溶液与胶体,但胶体区别于其他分散系的本质特征是胶体粒子的直径介于
1~100 nm 之间,而不是丁达尔效应。
(2)胶体不带电荷,胶体粒子(分散质)带电荷,但淀粉胶体的胶体粒子也不带电荷。
(3)PM2.5是指环境空气中空气动力学当量直径小于或等于2.5 μm 的颗粒物,胶体粒子的直径在1~ 100
nm(10-9~10-7 m 或1 nm~0.1μm)之间,两者的颗粒大小有差异。
(4)胶体粒子是多个分子形成的聚集体或大分子。将含 1 mol FeCl 的饱和溶液逐滴滴入沸腾的蒸馏水中,
3
生成的Fe(OH) 胶体中胶粒数目远小于N 的原因有两个,一是Fe3+部分水解,二是胶粒为多个Fe(OH) 分
3 A 3
子的聚集体。1.下列说法正确的有
①“卤水点豆腐”“黄河入海口处三角洲的形成”都与胶体的聚沉有关
②提纯Fe(OH) 胶体,可以采用的方法是过滤
3
③明矾能作净水剂是因为铝离子与水作用生成的氢氧化铝胶体具有吸附悬浮杂质的作用
④在制备Fe(OH) 胶体实验中,可以长时间加热
3
⑤向Fe(OH) 胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解形成棕黄色溶液
3
A.2个 B.3个 C.4个 D.5个
【答案】B
【解析】①稀豆浆分散系属于胶体,加入卤水(含氯化镁等)发生聚沉,泥浆水属于胶体,海水中含有大量
的可溶性电解质,如氯化钠等,可以使泥浆水聚沉形成三角洲,①正确;②提纯胶体可用渗析的方法,溶
液和胶体都可以通过滤纸,不能通过过滤提纯胶体,②错误;③明矾能用于净水是因为铝离子与水作用生
成的氢氧化铝胶体具有吸附性,能够吸附水中悬浮杂质而达到净水效果,③正确;④在制备Fe(OH) 胶体
3
实验中,长时间加热会使生成的胶体聚沉,④错误;⑤向Fe(OH) 胶体中加入稀硫酸先发生Fe(OH) 胶体的
3 3
聚沉,HSO 过量时Fe(OH) 溶解,得到硫酸铁棕黄色溶液,⑤正确;①③⑤正确.答案选B。
2 4 3
易错点2 有关物质的量浓度的计算与换算公式出错
2.将50 g质量分数为w 、物质的量浓度为c 的浓硫酸加入V mL水(水的密度为1 g·cm-3)中,稀释后得到
1 1
质量分数为w 、物质的量浓度为c 的稀硫酸。下列说法中正确的是
2 2
A.若w =2w ,则c<2c=20
1 2 1 2
B.若w =2w ,则c>2c,V<50
1 2 1 2
C.若c =2c,则w <2w ,V<50
1 2 1 2
D.若c =2c,则w <2w ,V>50
1 2 1 2
【错因分析】一定的溶液中,物质的量浓度、溶液密度、质量分数等物理量有一定的换算关系,若掌握不
牢,容易无从下手或计算错误。浓硫酸稀释后密度变小,但溶质的质量不变,若不能利用此信息,则无法
解答。
【试题解析】设物质的量浓度为c 的浓硫酸的密度为ρ ,物质的量浓度为c 的稀硫酸的密度为ρ ,显然ρ
1 1 2 2 1>ρ。由 知, ,分别讨论:
2
(1)若w =2w ,则c>2c,V=50,A、B错误;
1 2 1 2
(2)若c=2c,则w <2 w ,而w = ,故V<50,C正确、D错误。
1 2 1 2 2
【 参 考 答 案 】 C
物质的量浓度的相关计算类型及公式
1.溶液稀释、同种溶质的溶液混合的计算
(1)稀释定律:cV=cV
1 1 2 2
(2)混合后溶液体积不变:c V+ c V=c (V+ V)
1 1 2 2 混 1 2
(3)混合后溶液体积改变:cV+ cV=c V
1 1 2 2 混 混
2.物质的量浓度与质量分数的换算
由定义出发,运用公式:c=、质量分数=×100%进行推理,c====(密度ρ的单位为g·mL-1;w为
溶质的质量分数;M为溶质的摩尔质量,单位为g·mol-1)。当溶液为饱和溶液时,因为w= ,可得
c= 。
3.溶液稀释定律(守恒观点)
(1)溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
(2)溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
(3)溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
4.同溶质不同物质的量浓度溶液的混合计算
(1)混合后溶液体积保持不变时,cV+cV=c ×(V+V)。
1 1 2 2 混 1 2
(2)混合后溶液体积发生改变时,cV+cV=c V ,其中V =。
1 1 2 2 混 混 混
5.溶质相同、质量分数不同的两溶液混合定律
同一溶质、质量分数分别为a%、b%的两溶液混合。
(1)等体积混合
①当溶液密度大于1 g·cm-3时,必然是溶液浓度越大,密度越大(如HSO 、HNO 、HCl、NaOH等多
2 4 3数溶液),等体积混合后质量分数w>(a%+b%)。
②当溶液密度小于1 g·cm-3时,必然是溶液浓度越大,密度越小(如酒精、氨水溶液),等体积混合后,
质量分数w<(a%+b%)。
(2)等质量混合
两溶液等质量混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),则混合后溶液中溶质的质量分数w=(a%+b%)。
以上规律概括为“计算推理有技巧,有大必有小,均值均在中间找,谁多向谁靠”。
6.气体溶于水后所得溶液的物质的量浓度的计算
(1)若在标准状况下,一定质量的水中溶解某气体的体积为 V′(单位为L),所得溶液的物质的量浓度的
计算公式为 (ρ的单位为g·mL-1)。
(2)若气体溶于水时体积变化忽略不计,1 L水中溶解V′ L 气体(标准状况)时,所得溶液的物质的量浓
度计算公式为 。
2.标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,
物质浓度为c mol/L,则下列关系中不正确的是
A.
B.
C.
D. =1000Vρ/(17V+22400)
【答案】A
【解析】将所给的式子的分子和分母同除以22.4可得ρ=,分子表示了溶液的质量,是合理的,但分母表
达的是将溶剂的体积与气体的体积直接进行加和得到溶液的体积,这显然是错误的,A项错误;假设取溶
液的体积为1L,根据溶质质量分数的本义有:ῳ=,分子表达了溶质质量,分母表达了溶液的质量,B项
正确;将所给的式子分子分母同除以22.4可得:ῳ==,分子表达了溶质质量,分母表达了溶液的质量,
C项正确;将所给式子变形得:c===,分子代表了溶质的物质的量,分母代表了溶液的体积(单位为L),D项正确。答案选A。
易错点3 一定物质的量浓度溶液的配制误差分析出错
3.使用容量瓶配制溶液时,由于操作不当,会引起误差。下列情况会使所配溶液浓度偏低的是
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①②⑤ B.①③⑤ C.③④⑤ D.②③⑤
【错因分析】一定物质的量浓度溶液的配制原理掌握不牢,出现操作失误时容易分析不清被影响的因素导
致出错。
【试题解析】利用公式 进行误差分析。①称量时,物品与砝码颠倒,在使用游码的情况下,
物品称少了,溶质的质量m偏低,c偏低,①符合题意;②烧杯及玻璃棒未用蒸馏水洗涤,说明有部分溶
质没有转移到容量瓶中,容量瓶中溶质的质量m偏低,c偏低,②符合题意;③容量瓶内有少量蒸馏水,
溶解之后的操作中需要往容量瓶中加水,所以原理有少量蒸馏水,不会带来影响,③不符合题意;④定容
时,俯视刻度,液面在刻度线以下,V偏小,c偏大,④不符合题;⑤定容后,再补加水相当于稀释,c偏
小,⑤符合题意;综上符合题意为①②⑤,本题答案选A。
【参考答案】A
一定物质的量浓度溶液配制的误差分析
1.误差分析的依据
若V不变,分析n的变化;若n不变,分析V的变化。2.常见的实验误差分析
根据c =可知,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n 和溶液的体积V引起的。
B B
误差分析时,关键要看溶液配制过程中引起了n 和V怎样的变化。在配制一定物质的量浓度溶液时,若n
B B
比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n 比理论值大,或V比理论值小时,都会
B
使所配溶液浓度偏大。
因变量
可能引起误差的操作 c/mol·L-1
n/mol V/L
天平砝码附着有其他物质或已生锈 增大 不变
用量筒量取需稀释的溶液时仰视读数 增大 不变
偏大
定容时俯视容量瓶刻度线 不变 减小
溶液未冷却就转入容量瓶进行定容 不变 减小
砝码残缺 减小 不变
药品和砝码位置颠倒(使用游码) 减小 不变
没有洗涤烧杯 减小 不变
定容时仰视容量瓶刻度线 不变 增大
溶质已潮解或含有其他杂质 减小 不变 偏小
定容摇匀后又加蒸馏水 不变 增大
用量筒量取需稀释的溶液时俯视读数 减小 不变
定容时蒸馏水加多后用吸管吸出 减小 不变
转移时有少量液体洒在容量瓶外 减小 不变
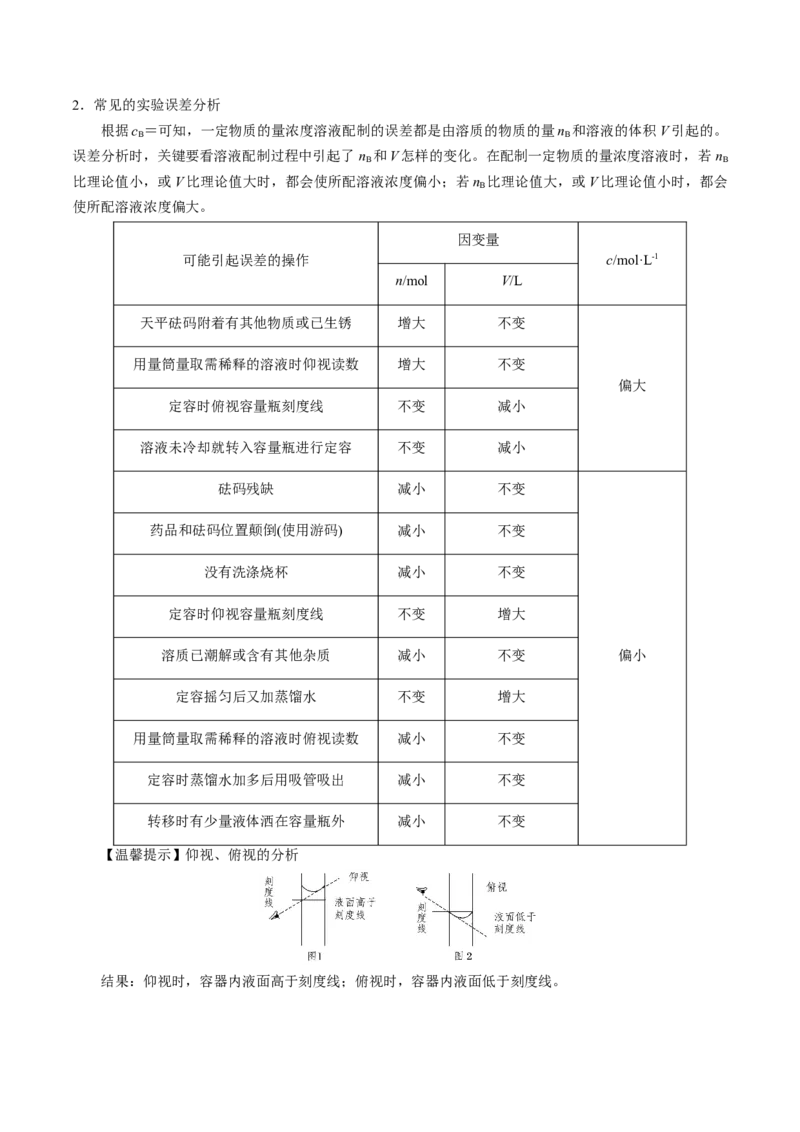
【温馨提示】仰视、俯视的分析
结果:仰视时,容器内液面高于刻度线;俯视时,容器内液面低于刻度线。3.某学生在配制一定物质的量浓度氢氧化钠溶液时,结果所配溶液浓度偏高,其原因可能是
A.所用氢氧化钠已经潮解
B.向容量瓶中加水未到刻度线
C.有少量氢氧化钠溶液残留在烧杯里
D.用带游码的托盘天平称2.4 g NaOH时误用了“左码右物”方法
【答案】B
【解析】所用NaOH已经潮解,实际称量的氢氧化钠的质量减小,氢氧化钠的物质的量减小,所配溶液浓
度偏低,A项错误;向容量瓶中加水未到刻度线时溶液的体积较小,溶液的浓度偏高,B项正确;有少量
氢氧化钠溶液残留在烧杯里,造成了溶质的损耗,溶液浓度偏低,C项错误;称量时误用“左码右物”,
若不使用游码,对称取氢氧化钠质量无影响,对所配溶液浓度无影响;若使用游码,实际称取氢氧化钠的
质量减小,所配溶液浓度偏低,D项错误。
易错点4 一定物质的量浓度溶液的配制答题不规范导致出错
4.用11.9 mol/L的浓盐酸配制80mL1.0 mol/L稀盐酸,有如下操作步骤:
①用量筒量取_______mL浓盐酸倒入小烧杯中,加适量蒸馏水稀释;
②继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,改用_______________小心滴加蒸馏水至溶液
凹液面的最低处与刻度线相切;
③将容量瓶塞紧,充分摇匀;
④把①中所得溶液小心地转入___________________中;
⑤用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液一并转移到容量瓶中。
(1)将上述操作步骤的空白处填写完整。
(2)本实验操作步骤的正确顺序是(填序号,不能重复)__________。
(3)使用玻璃棒在该实验中的作用是___________________________。
(4)配制过程中,下列情况会使配制结果偏高的是________(填序号)。
A.洗净后容量瓶内还残留蒸馏水未烘干
B.量取浓盐酸时,仰视刻度线观察液面
C.定容时,仰视刻度线
D.定容后,加盖倒转摇匀后,发现液面低于刻度线线
【 错 因分析】配制一定物质的量浓度溶液时应注意:①做需要补充仪器的实验题时,要学会“有序思考”——即
按照实验的先后顺序、步骤,思考每一步所需仪器,然后与已知仪器对比,就一定不会漏写某种仪器;②
容量瓶的规格,常见的有100 mL、250 mL、500 mL、1 000 mL;③所用定量仪器量筒、托盘天平的精确
度。
【试题解析】溶液配制一般步骤是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一
般用天平称量(用到药匙)称量,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻
璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量
蒸馏水,当加水至液面距离刻度线1~2 cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,
塞好瓶塞,反复上下颠倒摇匀。
(1)实验室配制80 mL1.0 mol/L稀盐酸应选用100mL容量瓶,由稀释定律可得:11.9 mol/L×V×10−3L=1.0
mol/L×100×10−3L,解得V=8.4 mL;向容量瓶中加蒸馏水至液面距刻度线1~2 cm处,为防止加水超过刻度
线,应改用胶头滴管小心滴加蒸馏水至溶液凹液面的最低处与刻度线相切;配制时一般用量筒量取浓盐酸,
在烧杯中稀释,冷却后转移到100mL容量瓶中,故答案为:8.4;胶头滴管;100mL容量瓶;
(2)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取浓盐酸,在烧杯中稀释,冷
却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯与玻璃棒2~3次,并将洗涤液移入容量瓶,继续
注入蒸馏水至液面距离刻度线1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线水平相切,盖好瓶
塞,反复颠倒摇匀,故实验操作顺序为:①④⑤②③,故答案为:①④⑤②③;
(3)配制过程中,溶解时用到玻璃棒,起搅拌作用;转移和定容时用到玻璃棒,起引流作用,故答案为:搅
拌、引流;
(4)洗净后容量瓶内还残留蒸馏水未烘干,对溶质的物质的量和溶液的体积都不会产生影响,溶液浓度不变,
A项错误;量取浓盐酸时,仰视刻度线观察液面,导致所取盐酸体积偏大,溶质的物质的量偏大,所测结
果偏高,B项正确;定容时仰视刻度线,导致溶液体积增大,所配溶液浓度偏低,C项错误;定容后,加
盖倒转摇匀后,容量瓶的壁上会残留部分溶液,液面会低于刻度线,对实验结果无影响,D项错误。答案
选B。
【参考答案】(1)8.4 胶头滴管 100 mL容量瓶
(2)①④⑤②③
(3)搅拌、引流
(4)B容量瓶使用的注意事项
(1)选用容量瓶时必须注明容量瓶规格。如500 mL容量瓶。
(2)选择容量瓶时遵循“大而近”的原则,所需溶质的量按所选用的容量瓶的规格进行计算。如配制
480 mL 1 mol/L NaOH溶液时应选用500 mL 的容量瓶,所需溶质NaOH的物质的量为0.5 mol。
(3)使用前要检查容量瓶是否漏水。
(4)向容量瓶中注入液体时,应沿细玻璃棒注入,以防操作时液体流出而造成损失。
(5)容量瓶使用应注意“五不”:不能溶解固体,不能稀释浓溶液,所配溶液温度不能高于或低于室温,
不能作反应容器,不能长期贮存所配溶液。
容量瓶检漏操作
往容量瓶中加入一定量的水,塞好瓶塞。用食指摁住瓶塞,另一只手托住瓶底,把瓶倒立过来,观察
瓶塞周围有无水漏出。如果不漏水,将瓶正立并将瓶塞旋转180度后塞紧,仍把瓶倒立过来,再检查是否
漏水。如果仍不漏水,即可使用。
4.高铁酸钠(Na FeO)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH) +4NaOH+
2 4 3
3NaClO=2NaFeO+3NaCl+5HO
2 4 2
(1)用单线桥在方程式中标出电子转移的情况: ;
(2)Na FeO 中铁元素的化合价是 价,NaFeO 具有较强的 (填“氧化性”或“还原性”)
2 4 2 4
(3)实验室欲配制250mL0.1 mol•L-1NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪
器为 ,下列操作配制的溶液浓度偏低的是 ;
A.称量NaOH时,将NaOH放在纸上称重
B.配制前,容量瓶中有少量蒸馏水
C.配制时,NaOH未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线(4)在容量瓶的使用方法中,下列操作正确的是 。
A.容量瓶用水洗净后,再用待配溶液洗涤
B.使用容量瓶前检验是否漏水
C.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线下1~2cm
处,用胶头滴管加蒸馏水至刻度线。
【答案】(1)
(2)+6 氧化性
(3)250mL容量瓶 AD
(4)BC
【解析】(1)2Fe(OH) +4NaOH +3NaClO=2Na FeO+3NaCl +5H O,NaClO中的氯元素从+1价降到-1价,
3 2 4 2
NaClO 是氧化剂,NaCl是还原产物,Fe(OH) 中的Fe元素化合价从+3价升高到+6价,被还原;
3
(2)NaFeO 中铁元素的化合价是+6 价,NaFeO 具有较强的氧化性;
2 4 2 4
(3) 配制氢氧化钠溶液需要的仪器有托盘天平、钥匙、烧杯、玻璃棒、250mL容量瓶,胶头滴管,实验室欲
配制250mL0.1 mol•L-1NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器为250mL
容量瓶;称量NaOH时,将NaOH放在纸上称重,NaOH吸收空气中的水分,造成溶质的物质的量减少,
浓度偏低,A项正确;配制前,容量瓶中有少量蒸馏水,定容时还需要加水,无影响,B项错误;配制时,
NaOH未冷却直接定容,氢氧化钠溶于水放热,液体热胀冷缩,定容时液体体积变小,浓度偏高,C项错
误;向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面,造成溶质的物质的量减少,浓度偏低,D项正确;
定容时俯视刻度线,液体体积变小,浓度偏高,E项错误。
(4)容量瓶用水洗净后,如果用待配溶液洗涤,会使所配溶液浓度偏高,A项错误;使用容量瓶前检验是否
漏水,B项正确;定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇
匀,符合容量瓶的使用方法,C项正确;配制溶液时,若试样是液体,用量筒取样后需在烧杯中稀释,再
用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线下1~2cm处,用胶头滴管加蒸馏水至刻度线,D项错误。
答案选BC。
【点睛】配制一定物质的量浓度的溶液时需要使用容量瓶,容量瓶在使用前需要检查是否漏液;容量瓶不
能用作反应容器,不能稀释溶液。易错点5 忽视溶液中的电荷守恒
5.某未知溶液X可能含有Al3+、Na+、NH +、Cl−、CO2−、SO 2−中的若干种,取该溶液进行如下实验,若
4 3 4
实验过程中所加试剂均过量,产生的气体全部逸出。则下列说法正确的是
A.原溶液中可能存在Na+,n(Cl−)≥0.01 mol
B.原溶液中一定存在CO2−、SO 2−、NH +,且均为0.01 mol
3 4 4
C.原溶液中一定存在Na+,Cl−
D.原溶液中一定不存在Al3+、Cl−
【错因分析】命题人常借用电荷守恒考查溶液中离子成分的确定,这样可增加试题的难度,解题时要熟练
运用电荷守恒而不落入陷阱。
【试题解析】滤液中加入烧碱溶液,通过颜色反应不能确定原溶液中是否存在Na+;加入BaCl 溶液生成沉
2
淀1,说明原溶液中至少含有CO2−、SO 2−中的一种,沉淀1部分溶于盐酸,所以沉淀1一定是BaSO、
3 4 4
BaCO 的混合物,故原溶液中一定存在CO2−、SO 2−,CO2−和Al3+不能大量共存,所以溶液中一定不存在
3 3 4 3
Al3+;沉淀2为硫酸钡沉淀,其物质的量为 =0.01 mol,CO2—的物质的量为 =0.01
3
mol;向所滤液中加入氢氧化钠溶液并加热生成了气体,则该气体为氨气,证明原溶液中一定含有NH +,
4
其物质的量为 =0.05 mol,CO2−、SO 2−所带负电荷的物质的量之和为0.01 mol 2+0.01 mol
3 4
2=0.04 mol,根据电荷守恒,原溶液中一定含有Cl−,不能确定是否存在Na+,所以n(Cl−)≥0.01 mol,据此
解答。根据以上分析,原溶液中可能存在Na+,n(Cl−)≥0.01 mol,A项正确;原溶液中一定存在CO2−、
3SO 2−、NH +,CO2−、SO 2−均为0.01 mol,而NH +为0.05 mol,B项错误;不能确定是否存在Na+,C项错
4 4 3 4 4
误;原溶液中一定不存在Al3+,一定含有Cl−,D项错误。答案选A。
【参考答案】A
离子检验的一般思路
1.离子检验一般是根据离子的特性(物理性质或化学性质),通过实验及实验现象确定离子的种类,在实验
时要注意排除干扰离子如检验SO时,要先用盐酸排除Ag+引起的干扰,且选用的钡试剂是BaCl 而不是
2
Ba(NO ) 溶液,以免酸性条件下NO将溶液中的SO氧化成SO而造成新的干扰。其一般检验流程为
3 2
先溶解后检验→先物理后化学→先取样后反应→排干扰加试剂→依现象得结论。
2.离子定量推断试题常根据离子的物质的量(或浓度)定量推断最后一种离子的存在:如果多种离子共存,
且只有一种离子的物质的量未知,可以用电荷守恒来确定最后一种离子是否存在,即阳离子所带的正电荷
总数等于阴离子所带的负电荷总数。
5.某溶液可能含有Cl-、SO、CO、NH、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加
热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.60 g固体;向上述滤液中加足
量BaCl 溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
2
A.至少存在5种离子
B.Cl-一定存在,且c(Cl-)≥0.4 mol·L-1
C.SO、NH一定存在,Cl-可能不存在
D.CO、Al3+一定不存在,K+可能存在
【答案】B
【解析】根据加入过量NaOH溶液,加热,得到0.02 mol气体,说明有NH,为0.02 mol,同时产生红褐色
沉淀,说明有Fe3+,而且为0.02 mol,则没有CO;根据不溶于盐酸的4.66 g 沉淀,说明有SO,且为0.02
mol,则根据电荷守恒可知一定有Cl-,至少有0.04 mol,B项正确。答案选B。
1.胶体
(1)当分散剂是水或其他液体时,根据分散质粒子直径的大小可把分散系分为溶液、胶体和浊液。(2)溶液、胶体、浊液的比较
浊液
分散系 溶液 胶体
悬浊液 乳浊液
分散质粒子直径 小于1 nm 1~100 nm 大于100 nm 大于100 nm
稳定性 稳定 介稳体系 不稳定 不稳定
分散质粒子能否透 能透过滤纸,不
均能透过 均不能透过 均不能透过
过半透膜或滤纸 能透过半透膜
植物油和水的混
实例 食盐水 淀粉胶体 泥浆水
合物
(3)胶体的性质及应用
①丁达尔效应
当一束光通过胶体时,形成一条光亮的“通路”,这是胶体粒子对光线散射造成的。利用丁达尔效应
是区别溶液和胶体的一种常用物理方法。
②介稳性
胶体的稳定性介于溶液与浊液之间,在一定条件下能稳定存在,属于介稳体系,但改变条件就有可能
发生聚沉。
③聚沉
加热、加入电解质或加入与胶体粒子带相反电荷的胶体等均能使胶体粒子聚集成为较大的颗粒,从而
形成沉淀从分散剂中析出。
④电泳
在外加电场作用下,胶体粒子在分散剂中做定向移动。电泳现象说明胶体粒子带电荷,工业上静电除
尘就是利用这个原理。
(4)胶体的制备
①物理方法:研磨法。如制豆浆。
②化学方法:利用水解反应、复分解反应等。
胶体 操作方法 制备原理
将饱和FeCl 溶液滴入沸水中, FeCl + 3HO Fe(OH) ( 胶 体 ) +
氢氧化铁胶体 3 3 2 3
得到透明的红褐色液体 3HCl
向稀KI溶液中滴加稀硝酸银溶
碘化银胶体 KI+AgNO AgI(胶体)+KNO
液,边滴加边振荡 3 3
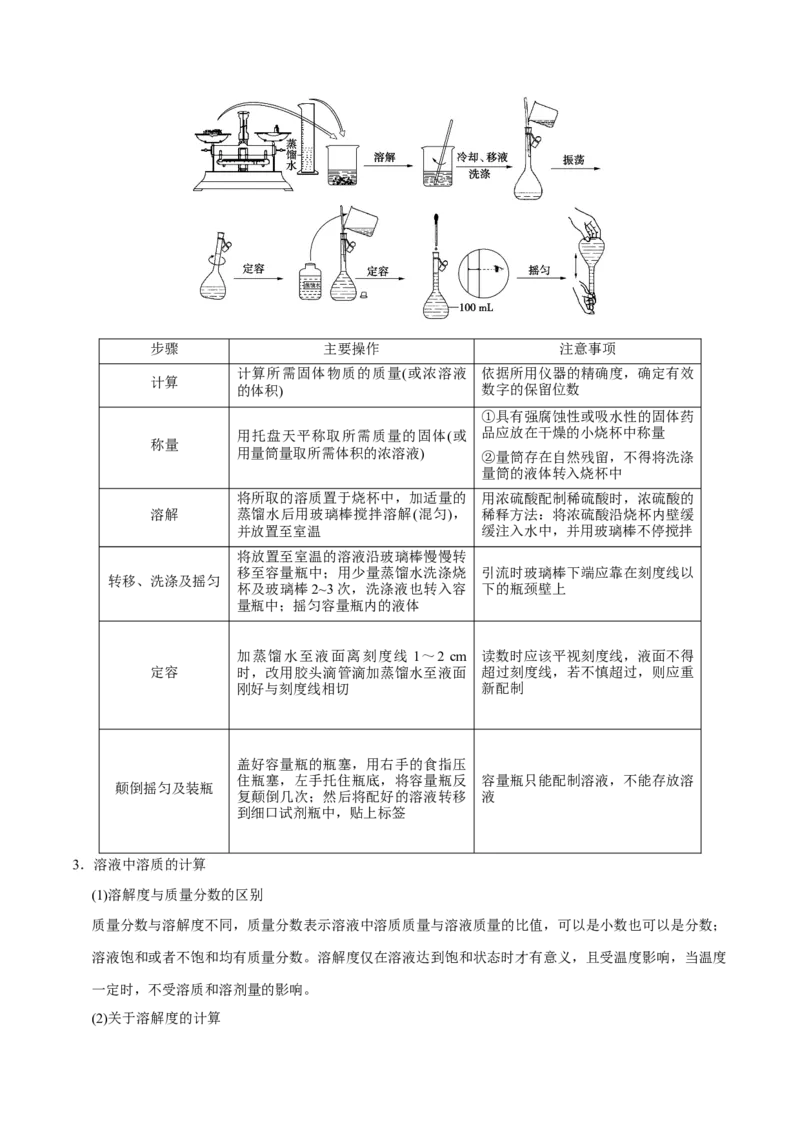
2.一定物质的量浓度溶液的配制步骤 主要操作 注意事项
计算所需固体物质的质量(或浓溶液 依据所用仪器的精确度,确定有效
计算
的体积) 数字的保留位数
①具有强腐蚀性或吸水性的固体药
用托盘天平称取所需质量的固体(或 品应放在干燥的小烧杯中称量
称量
用量筒量取所需体积的浓溶液) ②量筒存在自然残留,不得将洗涤
量筒的液体转入烧杯中
将所取的溶质置于烧杯中,加适量的 用浓硫酸配制稀硫酸时,浓硫酸的
溶解 蒸馏水后用玻璃棒搅拌溶解(混匀), 稀释方法:将浓硫酸沿烧杯内壁缓
并放置至室温 缓注入水中,并用玻璃棒不停搅拌
将放置至室温的溶液沿玻璃棒慢慢转
移至容量瓶中;用少量蒸馏水洗涤烧 引流时玻璃棒下端应靠在刻度线以
转移、洗涤及摇匀
杯及玻璃棒2~3次,洗涤液也转入容 下的瓶颈壁上
量瓶中;摇匀容量瓶内的液体
加蒸馏水至液面离刻度线 1~2 cm 读数时应该平视刻度线,液面不得
定容 时,改用胶头滴管滴加蒸馏水至液面 超过刻度线,若不慎超过,则应重
刚好与刻度线相切 新配制
盖好容量瓶的瓶塞,用右手的食指压
住瓶塞,左手托住瓶底,将容量瓶反 容量瓶只能配制溶液,不能存放溶
颠倒摇匀及装瓶
复颠倒几次;然后将配好的溶液转移 液
到细口试剂瓶中,贴上标签
3.溶液中溶质的计算
(1)溶解度与质量分数的区别
质量分数与溶解度不同,质量分数表示溶液中溶质质量与溶液质量的比值,可以是小数也可以是分数;
溶液饱和或者不饱和均有质量分数。溶解度仅在溶液达到饱和状态时才有意义,且受温度影响,当温度
一定时,不受溶质和溶剂量的影响。
(2)关于溶解度的计算关于溶解度的计算常有以下三种形式:
①温度不变时,某饱和溶液蒸发溶剂析出一定质量的晶体,求析出晶体的质量或蒸发的溶剂质量。
②饱和溶液的溶剂质量不变,改变温度时,求析出或可继续溶解溶质的质量。
③加入或析出的溶质带有结晶水时,求最终所得溶液中溶质的溶解度或质量分数。
计算原理:在一定温度下,溶质的溶解度不变,即溶液中溶质与溶剂的质量比不变。
(3)溶液的质量分数与密度的关系
①当溶液的ρ>1 g·cm−3时,质量分数(w)越大,则ρ越大,如烧碱溶液、硫酸等;
②当溶液的ρ<1 g·cm−3时,质量分数(w)越大,则ρ越小,如氨水、乙醇溶液。
(4)等体积或等质量的溶液混合后质量分数的变化规律
①两种不同质量分数的溶液等体积混合,若溶液的密度大于1 g·cm−3,则混合溶液的质量分数大于它们
和的一半;若溶液的密度小于1 g·cm−3,则混合溶液的质量分数小于它们和的一半。
②无论溶液的密度大于1 g·cm−3还是小于1 g·cm−3,等质量混合时,所得混合溶液的质量分数都等于它
们和的一半。
1.下列有关胶体的说法,正确的是
A.依据丁达尔效应可将分散系分为溶液、胶体和浊液
B.向沸水中滴加饱和氯化铁溶液至产生红褐色液体,用离子方程式表示为:Fe3++3H O=Fe(OH) ↓+3H+
2 3
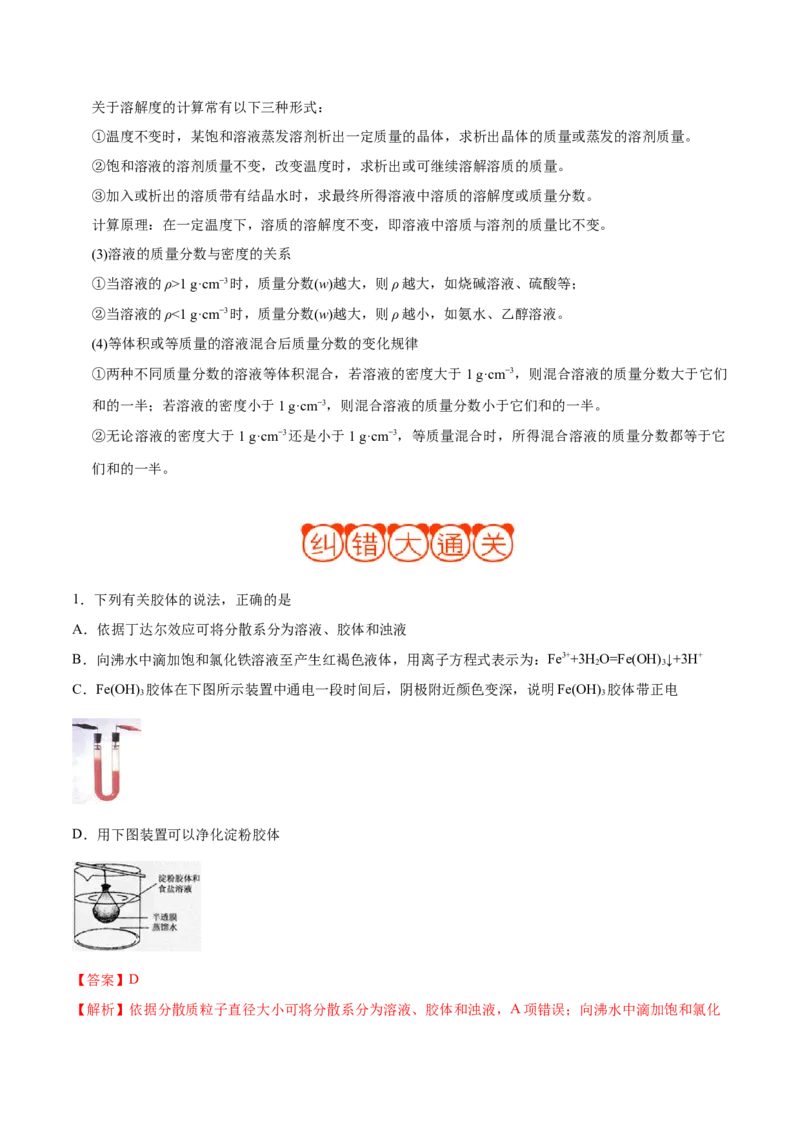
C.Fe(OH) 胶体在下图所示装置中通电一段时间后,阴极附近颜色变深,说明Fe(OH) 胶体带正电
3 3
D.用下图装置可以净化淀粉胶体
【答案】D
【解析】依据分散质粒子直径大小可将分散系分为溶液、胶体和浊液,A项错误;向沸水中滴加饱和氯化铁溶液至产生红褐色液体制得Fe(OH) 胶体,用离子方程式表示为:Fe3++3H O══Fe(OH) (胶体)+3H+,B
3 2 3
项错误;Fe(OH) 胶体在下图所示装置中通电一段时间后,阴极附近颜色变深,说明Fe(OH) 胶粒带正电,
3 3
胶体不带电,C项错误;根据淀粉胶体不能透过半透膜,溶液中的离子可以透过半透膜,所以能用该装置
净化淀粉胶体,D项正确。答案选D。
2.磁流体是电子材料的新秀,它是由直径为纳米量级(1~10nm之间)的磁性固体颗粒,基载液以及界面活
性剂混合而成的分散系,既具有液体的流动性,又具有固体磁性材料的磁性。下列关于纳米Fe O 磁流体
3 4
的说法不正确的是
A.纳米Fe O 磁流体分散系属于溶液
3 4
B.纳米Fe O 磁流体中分散质粒子可以透过滤纸
3 4
C.当一束可见光通过该磁流体时会出现光亮的“通路”
D.纳米Fe O 磁流体是介稳体系
3 4
【答案】A
【解析】纳米Fe O 磁流体的粒子直径在1~10nm之间,所以纳米Fe O 磁流体分散系属于胶体,A项错误;
3 4 3 4
纳米Fe O 磁流体分散系属于胶体,胶体的分散质粒子可以透过滤纸,B项正确;纳米Fe O 磁流体分散系
3 4 3 4
属于胶体,能产生丁达尔效应,所以当一束可见光通过该磁流体时会出现光亮的“通路”,C项正确;纳
米Fe O 磁流体分散系属于胶体,胶体具有介稳性,D项正确。答案选A。
3 4
3.用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有50 mL量筒、250 mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0 mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
【答案】C
【解析】稀释浓硫酸时,应将浓硫酸缓慢注入水中并不断搅拌,A项错误;该实验不需要托盘天平,B项
错误;根据溶质质量不变知,配制该稀硫酸需要浓硫酸的体积为V=
=25.0 mL,C项正确;不能在容量瓶里稀释浓硫酸,在烧杯里稀释并冷却后,再转移到容量瓶中,最后加
水定容,D项错误。
4.将物质的量均为a mol的Na和Al一同投入m g足量水中,所得溶液的密度为ρ g·cm-3,则此溶液的物
质的量浓度为
A. mol·L-1 B. mol·L-1 C. mol·L-1 D. mol·L-1
【答案】A
【解析】Na和Al一同投入m g足量水中时,发生反应的化学方程式为2Na+2HO=2NaOH+H↑、2Al+
2 2
2NaOH+2HO===2NaAlO +3H↑。由于Na、Al的物质的量均为a mol,结合化学方程式可知生成2a mol
2 2 2
H ,所得溶液中只有NaAlO 一种溶质,其物质的量为a mol。所得溶液的质量为m(Na)+m(Al)+m(H O)-
2 2 2m(H )=(46a+m)g,所得溶液的体积为 L,所得溶液的物质的量浓度为 mol·L-1,答案选A。
2
5.把V L含有MgSO 和KSO 的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使Mg2+完全
4 2 4
沉淀为Mg(OH) ;另一份加入含b mol BaCl 的溶液,恰好使 完全沉淀为BaSO。则原混合溶液中
2 2 4
K+的浓度为
A. mol·L−1 B. mol·L−1
C. mol·L−1 D. mol·L−1
【答案】D
【解析】把V L混合溶液分成两等份,每份为L,所含溶质各为原混合溶液的一半。根据题设条件可知:
L溶液中含mol MgSO ,含(b−) mol K SO ,则 L溶液中含K+的物质的量为2(b−) mol,从而算出原混合溶
4 2 4
液中K+的物质的量为4(b−) mol,即c(K+)=mol·L−1。
6.某校化学兴趣小组在实验中发现一瓶溶液,标签上标有“CaCl 0.1 mol·L−1”的字样,下面是该小组成员对
2
溶液的叙述,正确的是
A.配制1L溶液,可将0.1 mol的CaCl 溶于1L水
2
B.取少量该溶液加水至溶液体积为原来的二倍,所得溶液c(Cl−)=0.1 mol·L−1
C.Ca2+和Cl−的浓度都是1 mol·L−1
D.取该溶液的一半,则所取溶液c(CaCl )=0.05 mol·L−1
2
【答案】B
【解析】标签上标有“CaCl 0.1 mol·L−1”的字样,即在1L的溶液中含0.1 molCaCl 。将0.1 mol CaCl 溶于
2 2 2
1L水中,所得溶液的体积不是1L,无法计算浓度,A项错误;溶液中Cl−的浓度为0.2 mol/L,将溶液稀释
一倍,则浓度减半,故稀释后Cl−的浓度应为0.1 mol/L,B项正确;在CaCl 中,Ca2+和Cl−的物质的量之比
2
为1:2,则浓度之比也为1:2,故Ca2+的浓度为0.1 mol/L,而Cl−的浓度应为0.2 mol/L,C项错误;溶液
是均一稳定的,浓度与取出的溶液的体积是多少无关,D项错误。答案选B。
7.下列有关溶质的质量分数和物质的量浓度的计算结果错误的是
A.有KSO 和Al (SO ) 的混合溶液,已如其中Al3+的物质的量浓度为0.4mol/L, SO 的物质的量浓度
2 4 2 4 3
为0.7mol/L,则此溶液中K+的物质的量浓度为0.2mol/L
B.将5mol/L的Mg(NO ) 溶液a mL稀释至b mL,稀释后溶液中NO 的物质的量浓变为 mol/L
3 2C.将标准状况下,将VLA气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶
液的物质的量浓度为. mol/L
D.密度为0.91g/cm3的氨水,质量分数为25%。该氨水用等体积的水稀释后,所得溶液中溶质的质量分数
等于12.5%
【答案】D
【解析】由电荷守恒得3c(Al3+)+c(K+)=2c(SO 2-),即3×0.4mol/L+c(K+)=2×0.7mol/L,即c(K+)=
4
0.2mol/L,A项正确;稀释前后溶质的物质的量不变,则稀释后(NO -)==mol/L,B项正确;溶质的物质
3
的量n==mol,溶液的质量=溶质的质量+溶剂的质量=mol×Mg/mol+0.1L×1000g/L=g,溶液的体积==
mL=×10-3L,所以所得溶液的溶质的物质的量浓度==mol/L,C项正确;稀释前后溶质的质量不变,设稀
释前氨水的体积为Vcm3,稀释前溶液的质量=0.91Vg,则稀释前溶质的质量=稀释后溶质的质量
0.91V×25%g=0.2275Vg,稀释后溶液的质量=0.91Vg+Vcm3×1g/cm3 =1.91Vg,则稀释后溶质的质量分数
=×100%≈11.6%,D项错误。答案选D。
8.在标准状况下,将22.4LHCl完全溶于1L水中(水的密度近似为1g/mL),溶液的密度为ρg/cm3(ρ>
1),溶液的体积为VmL,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是
①w= ×100% ②c=1 mol·L−1 ③向上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w
④向上述溶液中再加入VmL水后,所得溶液的质量分数小于0.5w
A.①②③ B.①③④ C.①③ D.①④
【答案】C
【解析】①根据c= 可得w= ×100%,故正确;②36.5gHCl的物质的量为1 mol,1 mol氯化氢
溶解在1L水中,所得溶液体积不是1L,浓度不是1 mol/L,故错误;③盐酸的密度大于水的密度,则加入
等体积的水后,由于水的质量小于原盐酸的质量,根据质量分数公式可知混合液的总质量小于原先的2倍,
则混合液中溶质的质量分数大于原溶液的1半,即大于0.5w,故正确;④氯化氢为强电解质,溶液中完全
电离出氢离子和氯离子,所以溶液中不存在氯化氢分子,故④错误;所以正确的为①③。答案选C。
9.把200 mL NH HCO 和NaCO 的混合溶液分成两等份,取一份加入含a mol NaOH的溶液恰好反应完全;
4 3 2 3
取另一份加入含b mol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为
A.(10b-5a)mol·L-1 B.(2b-a)mol·L-1 C.(-)mol·L-1 D.(5b-)mol·L-1【答案】A
【解析】NH HCO 和a mol NaOH恰好完全反应,则NH HCO 的物质的量为0.5a mol,取另一份加入含b
4 3 4 3
mol HCl的盐酸恰好反应完全,由NH HCO 反应掉的盐酸为0.5a mol,则由NaCO 反应掉的盐酸为b mol
4 3 2 3
-0.5a mol,NaCO 的物质的量为(b mol-0.5a mol)×0.5,则c(Na+)=(b mol-0.5a mol)÷0.1 L=(10b-
2 3
5a)mol·L-1。答案选A。
10.取100 mL 0.3 mol·L-1的硫酸溶液和300 mL 0.25 mol·L-1的硫酸溶液加水稀释至500 mL,该混合溶液
中H+的物质的量浓度是
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
【答案】B
【解析】根据题意可知,容量瓶中 HSO 溶液的H+浓度关系如下:cV=cV +cV ,可得n(H+)=(0.1 L×
2 4 3 3 1 1 2 2
0.3 mol·L-1+0.3 L×0.25 mol·L-1)×2=0.21 mol,所以c(H+)= =0.42 mol·L-1。答案选B。
11.实验室常用98%(ρ=1.84 g·mL-1)的浓HSO 配制1∶4的稀HSO ,此稀HSO 的密度为1.23 g·mL-1,
2 4 2 4 2 4
其物质的量浓度为
A.4.6 mol·L-1 B.5.7 mol·L-1
C.3.88 mol·L-1 D.18.4 mol·L-1
【答案】C
【解析】实验室配制1∶4溶液的含义是指取1体积的浓硫酸与4体积的水混合。求算所得溶液溶质的质量
分数:w%=(1 mL×1.84 g·mL-1×98%)/(1 mL×1.84 g·mL-1+4 mL×1 g·mL-1)×100%≈30.9%,稀硫酸的物质的
量浓度为c(H SO )=(1 000 mL×1.23 g·mL-1×30.9%)/(98 g·mol-1)≈3.88 mol·L-1。答案选C。
2 4
12.某澄清水溶液,只可能含有以下离子中的若干种,且各离子物质的量浓度相等(忽略水的电离):
Na+、K+、Cl−、Ba2+、CO2−、SO 2−,取少量该溶液于试管,加BaCl 溶液后出现白色沉淀。一定存在
3 4 2
的离子有
A.Ba2+、Cl− B.SO 2−、Na+ C.Na+、K+ D.CO2−、SO 2−
4 3 4
【答案】C
【解析】取少量该澄清溶液于试管,加BaCl 溶液后出现白色沉淀,由于溶液中无Ag+,因此不可能与
2
Cl−发生沉淀反应的离子;可能与Ba2+发生沉淀反应形成白色沉淀的离子有CO2−、SO 2−,则由于可能含有
3 4
CO2−、SO 2−,则不能大量存在Ba2+;由于溶液中各离子物质的量浓度相等,则因为CO2−或SO 2−为阴离子,
3 4 3 4
则一定含有阳离子Na+、K+,CO2−和SO 2−只能有其中的一种离子。答案选C。
3 4
13.某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO−、CO2−、SiO2−、Cl−中的几种,现进行如下
2 3 3实验:
①取少量原溶液,加入氢氧化钠溶液过程中无沉淀生成;
②另取少量原溶液,逐滴加入盐酸, 发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产
生气体,最后沉淀逐渐减少至消失;
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀。
下列说法中正确的是
A.该溶液中一定不含有Ba2+、Mg2+、Al3+、SiO−、Cl−
3
B.该溶液中一定含有K+、AlO−、CO2−、Cl−
2 3
C.该溶液中是否含有K+需进行焰色反应(透过蓝色钴玻璃)
D.可能含有Cl−
【答案】D
【解析】①“溶液滴加氢氧化钠溶液过程中无沉淀生成”,故溶液中不含Al3+、Mg2+;②“溶液滴加盐酸,开
始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失”,故溶液中含有AlO−、
2
CO2−,不含SiO2−,由于Ba2+与CO2−不能共存(生成白色沉淀),故溶液中不含Ba2+,而由溶液电荷守恒,
3 3 3
必须有阳离子,故溶液中含有K+,无需焰色反应即可确定;③“在上述②沉淀消失后的溶液中,再加入足
量的硝酸银溶液可得到沉淀”,得到的沉淀为AgCl,而②中加入的是盐酸,故原溶液中可能含有Cl−。由以
上分析知该溶液中一定含有K+、AlO−、CO2−,一定不含Ba2+、Al3+、Mg2+、SiO2−,可能含有Cl−,D项正
2 3 3
确。答案选D。
14.在t ℃时,将a g NH 完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,质量分数为w,
3
其中含有NH的物质的量是b mol,下列叙述正确的是
A.溶质的质量分数w=×100%
B.溶质的物质的量浓度c= mol·L-1
C.溶液中c(OH-)= mol·L-1+c(H+)
D.向上述溶液中加入V mL水,所得溶液的质量分数大于0.5w
【答案】C
【解析】溶质的质量分数w=×100%,A项错误;氨水中的溶质是NH ,而不是NH ·H O,将w=×100%代
3 3 2
入公式c=,化简可得c= mol·L-1,B项错误;氨水中含有的阳离子为H+和NH,含有的阴离子只有OH
-,根据电荷守恒可知C项正确;由于氨水的密度小于水的密度,与水等体积混合所得稀氨水的质量大于
原氨水质量的2倍,故其质量分数小于0.5w,D项错误。答案选C。
15.下表是四种盐在不同温度下的溶解度(g/100 g水):(假设:盐类共存时不影响各自的溶解度,分离晶体
时,溶剂的损耗忽略不计)
NaNO KNO NaCl KCl
3 3
10 ℃ 80.5 21.2 35.7 31.0100 ℃ 175 246 39.1 56.6
用物质的量之比为1∶1的硝酸钠和氯化钾为原料,制取硝酸钾晶体,其流程如图所示
以下说法错误的是
A.①和②的实验过程中,都需要控制温度
B.①实验操作依次为加水溶解、蒸发浓缩结晶、趁热过滤
C.②实验操作依次为加水溶解、蒸发浓缩结晶、趁热过滤
D.用95%的酒精洗涤所得的硝酸钾晶体比较好
【答案】C
【解析】①为蒸发浓缩,②为冷却结晶,均需要控制温度,A项正确;①实验分离出NaCl,操作依次为加
水溶解、蒸发浓缩结晶、趁热过滤,B项正确;②实验操作为冷却结晶,C项错误;用95%的酒精洗涤所
得的硝酸钾晶体可减少硝酸钾的溶解,D项正确。答案选C。
16.实验室常用浓盐酸的质量分数为36.5%,密度为1.20 g/cm3。
(1)此盐酸的物质的量浓度为_____。
(2)需要230 mL3.0 mol·L-1的盐酸,配制时需以上浓盐酸的体积为_____mL。
(3)上述实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒以及_____(两种仪器)。
(4)用浓盐酸配制3.00 mol·L-1稀盐酸,操作步骤的正确顺序是________(填字母代号)。
a.计算需要浓盐酸的体积
b.用量筒量取浓盐酸
c.将烧杯中的溶液注入所需容积的容量瓶中,瓶用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容
量瓶
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却
e.盖好瓶塞,反复上下颠倒,摇匀
f.继续向容量瓶中加蒸馏水至刻度线下1~2 cm处,改用某仪器小心滴加蒸馏水至凹液面与刻度线相平
(5)下列操作使溶液物质的量浓度偏高的是:________。
A.量取浓盐酸时仰视刻度线
B.容量瓶洗净后未经干燥处理
C.未冷却至室温就转移定容D.将洗涤量筒的洗涤液转移到容量瓶中
E.定容时俯视刻度线
F.摇匀后立即观察,发现溶液未达到刻度线,再加几滴蒸馏水至刻度线
【答案】(1)12 mol/L (2)62.5 (3)250mL容量瓶、胶头滴管 (4)abdcfe (5)ACDE
【解析】(1)质量分数为36.5%,密度为1.20 g/cm3的浓盐酸的物质的量浓度c= mol/L=12 mol/L;
(2)配制230 mL3.0 mol·L-1的盐酸,应选择250mL的容量瓶,设需要浓盐酸的体积为V,稀释前后溶质
HCl的物质的量不变,则V×12 mol/L=250 mL ×3.0 mol·L-1,解得V=62.5mL;
(3)配制一定物质的量浓度溶液步骤为计算、称量、溶解、转移、洗涤、定容、摇匀、装瓶贴签等,用
到的玻璃仪器有250mL容量瓶、量筒、胶头滴管、烧杯、玻璃棒;
(4)配制一定物质的量浓度溶液步骤为计算、称量、溶解、转移、洗涤、定容、摇匀、装瓶贴签等,所
以正确的操作步骤为abdcfe;
(5)量取浓盐酸时仰视读数,浓盐酸体积偏大,溶质HCl物质的量偏大,根据c=,配制的溶液浓度偏高,
A项符合题意;定容时需要加入蒸馏水,所以将烧杯中溶液转移到容量瓶之前,容量瓶洗净后未经干燥处
理,对溶液浓度无影响,B项不符合题意;未冷却至室温就转移定容,冷却后溶液体积偏小,根据c=,
配制的溶液浓度偏高,C项符合题意;将洗涤量筒的洗涤液转移到容量瓶中,溶质HCl物质的量偏大,根
据c=,配制的溶液浓度偏高,D项符合题意;定容时俯视刻度线,溶液体积偏小,根据c=,配制的溶液
浓度偏高,E项符合题意;摇匀后立即观察,发现溶液未达到刻度线,再用滴管加几滴蒸馏水至刻度线,
导致溶液体积偏大,根据c=,配制的溶液浓度偏低,F项不符合题意;答案选ACDE。
【点睛】当所配制溶液体积与所选容量瓶体积不同时,应按所选容量瓶的体积计算。
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________