文档内容
专题 03 离子反应
一、选择题(每小题只有一个选项符合题意)
1.下列物质中,其水溶液能导电,但本身属于非电解质的是( )
A.金属铁 B.SO C.酒精 D.硫酸钡晶体
2
2.(2022·浙江省温州十校联合体高一期中)下列物质中能导电的是( )
A.无水乙醇 B.氯化氢气体 C.氢氧化钠固体 D.熔融氯化钠
3.(2022·浙江省绿谷高中联盟高一期中联考)下列物质属于电解质的是( )
A.硫酸 B.铜 C.氯化钠溶液 D.酒精
4.(2022·浙江省温州十校联合体高一期中)下列电离方程式中,正确的是( )
A.Ca(OH) =Ca2++OH- B.HClO H++Cl-+O2-
2
C.NaO=2Na++2O2- D.Al (SO )=2Al3++3SO2-
2 2 2 4 3 4
5.(2023·黔西南州同源中学高一期中)下列电离方程式错误的是( )
A.Al (SO )=2Al3++3 SO2- B.NaOH=Na++OH-
2 4 3 4
C.NaCO=2Na++CO2- D.HSO =H ++SO 2-
2 3 3 2 4 2 4
6.下列电离方程式书写正确的是( )
A.NaOH=Na++O2-+H+ B.FeCl =Fe3++Cl
3 2
C.Ca(NO )=Ca2++2(NO)2- D.HSO =2H++SO2-
3 2 3 2 4 4
7.关于NaSO 的电离方程式书写正确的是( )
2 4
A.NaSO =Na++ SO 2- B.NaSO =2Na++SO2-
2 4 4 2 4 4
C.2Na++ SO 2-=Na SO D.NaSO =Na2++ SO 2-
4 2 4 2 4 4
8.(2023·天津市部分区高三期中)加入(NH )Fe(SO )•6H O晶体后仍能大量存在的离子组是( )
4 2 4 2 2
A.Na+、H+、Cl-、NO - B.Na+、Mg2+、Cl-、SO 2-
3 4
C.K+、Ba2+、OH-、I- D.Na+、S2-、Br-、ClO-
9.(2023·湖北省黄冈市高三期中联考)下列各组离子在指定的溶液中,能大量共存的是( )
A.0.01mol/L HClO的溶液中: 、 、I-、SO 2-
4
B.pH=8的溶液中:Na+、K+、Cl-、HCO -
3
C.0.1mol/L NaCl的溶液中: 、H+、Ag+、SO 2-
4
D.水电离c(OH-)=1.0×10-11mol·L-1的溶液中,K+、Fe2+、NO -、SO 2-
3 4
10.(2023·天津市河北区高三期中质量检测)常温下,下列各组离子在指定溶液中能大量共存的是( )A.pH=1的溶液中:HCO -、K+、Na+、Cl-
3
B.无色溶液中:NH +、K+、MnO -、NO -
4 4 3
C.含有SO 2-的溶液中:NO -、OH-、Na+、Ba2+
4 3
D.c(OH-)=10-2mol·L-1的溶液中:Na+、Cl、CO2-、K+
3
11.(2023·广东省韶关市高三调研考试)下列关于微粒在溶液中表示正确的是( )
A.遇KSCN变红色的溶液中:Na+、Mg2+、CHCOOH、Cl-能大量共存
3
B.无色溶液中:Cu2+、Al3+、NH +、Cl-能大量共存
4
C.NaHCO 溶液中加入稀盐酸:CO2-+2H+=CO ↑+H O
3 3 2 2
D.向FeCl 溶液中通入Cl:Cl+Fe2+=2Cl-+Fe3+
2 2 2
12.(2023·江西省九江市十校高三联考)能正确表示下列反应的离子方程式为( )
A.硫氢化钠溶液和硝酸混合:HS-+H+=H S↑
2
B.碳酸钠溶液呈碱性:CO2-+2H O=HCO+2OH--
3 2 2 3
C.硅酸钠溶液中通入过量二氧化碳:SiO2-+H O+CO=HSiO-+HCO-
3 2 2 3 3
D.将等物质的量浓度的Ba(OH) 与NH HSO ,溶液以体积比1∶2混合:Ba2++2OH-+2H++SO2-
2 4 4 4
=BaSO ↓+2H O
4 2
13.(2022·辽宁省高三联考)下列表示对应化学反应的离子方程式正确的是( )
A.将SO 通入漂白粉溶液中:Ca2++SO+H O+2ClO-= CaSO↓+2HClO
2 2 2 4
B.将10滴0.1 mol·L-1盐酸逐滴滴入2mL0.2 mol·L-1 Na CO 溶液中:H++CO 2-=HCO-
2 3 3 3
C.FeSO 溶液与 溶液混合:Ba2++SO2-=BaSO ↓
4 4 4
D.醋酸与NaOH溶液反应:OH-+H+=H O
2
14.(2022·浙江省嘉兴市高三选考模拟预测)下列变化的离子方程式表示正确的是( )
A.少量SO 通入NaClO溶液中:SO +3ClO-+H O=SO 2-+Cl-+2HClO
2 2 2 4
B.碳酸钙溶于醋酸:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
C.酸性高锰酸钾溶液中滴入双氧水:2MnO -+3H O+6H+=2Mn2++4O ↑+6H O
4 2 2 2 2
D.向苯酚钠溶液中通入少量CO:2C HO-+H O+CO→2C HOH+CO 2-
2 6 5 2 2 6 5 3
15.(2022·浙江省缙云中学等高三联考)下列离子方程式正确的是( )
A.氯化铜溶液中加足量氨水:Cu2++2NH•H O=2NH ++Cu(OH) ↓
3 2 4 2
B.足量酸性KMnO 溶液与双氧水反应:2MnO -+7H O+6H+=2Mn2++6O ↑+10H O
4 4 2 2 2 2
C.向NaHSO 溶液中滴加Ba(OH)
4 2
溶液至中性: 2H++SO2-+ Ba2++2OH-=BaSO ↓+ 2HO
4 4 2
D.实验室用NH Cl 和Ca(OH) 制NH :NH ++OH- NH ↑+H O
4 2 3 4 3 216.(2022·湖北省公安县等六县教学研究中心高三联考)下列离子方程式符合题意且正确的是( )
A.在NaHCO 溶液中滴加过量的澄清石灰水:Ca2++2OH-+2 HCO -=CaCO ↓+CO 2-+2H O
3 3 3 3 2
B.在Mg(OH) 浊液中滴加CuSO 溶液产生蓝色沉淀:Mg(OH) +Cu2+=Mg2++Cu(OH)
2 4 2 2
C.在FeCl 溶液中通入HS:2Fe3++3H S=Fe S↓+6H+
3 2 2 2 3
D.磁性氧化铁溶于浓硝酸:Fe O+8H+=2Fe3++Fe2++4H O
3 4 2
17.(2022·辽宁省沈阳市重点高中联合体高三联考)下列过程中的化学反应,相应的离子方程式正确的是(
)
A.向CaCl 溶液中通入CO:Ca2++H O+CO=CaCO ↓+2H+
2 2 2 2 3
B.FeBr 溶液与等物质的量的Cl 反应:2Fe2++2Br-+2Cl=2Fe3++4Cl-+Br
2 2 2 2
C.过量铁粉加入稀硝酸中:Fe+4H++NO-=Fe3++NO↑+2HO
3 2
D.用惰性电极电解饱和MgCl 水溶液:2Cl-+2H O Cl↑+H ↑+2OH-
2 2 2 2
18.(2023·山西省运城市高三期中调研测试)对于下列实验,能正确描述其反应的离子方程式是( )
A.用NaSO 溶液吸收少量Cl:3SO 2-+Cl+H O=2HSO -+ 2Cl-+SO2-
2 3 2 3 2 2 3 4
B.向酸性KMnO 溶液中滴加HO 溶液:2MnO -+3H O+6H+=2Mn2++4O ↑+6H O
4 2 2 4 2 2 2 2
C.向CaCl 溶液中通入CO:Ca2++CO +H O=CaCO↓+2H+
2 2 2 2 3
D.用醋酸和淀粉―KI溶液检验加碘盐中的IO -:5I-+IO -+6H+=3I +3H O
3 3 3 2
19.(2023·山西省大同市高三第二次学情调研测试)对于下列实验,能正确描述其反应的离子方程式的是(
)
A.向碳酸氢铵溶液中加入足量的澄清石灰水:Ca2++2HCO-+2OH-=CaCO ↓+2H O+CO2-
3 3 2 3
B.用NaSO 溶液吸收少量Cl:3SO 2-+Cl+H O=2HSO -+ 2Cl-+SO2-
2 3 2 3 2 2 3 4
C.向水垢中滴加足量醋酸:CaCO +2H+=Ca2++H O+CO↑
3 2 2
D.向硫酸铝溶液中加过量氨水:Al3++4NH•H O=AlO-+4NH++2H O
3 2 2 4 2
20.(2023·辽宁省抚顺市六校协作体高三期中)化学创造美好生活。下列生产或探究活动中,相关操作或事
实合理且对应的离子方程式正确的是( )
A.用过量氨水吸收烟道气中的SO :SO + NH ·H O=HSO -+NH+
2 2 3 2 3 4
B.用白醋除铁锈:
C.向混有少量Fe Br 的FeCl 溶液中通入少量氯气除杂:2Br-+Cl=Br +2Cl-
2 2 2 2
D.用稀硝酸除去银镜实验中附着在试管内壁的银单质:3Ag+4H++NO-=3Ag++NO↑+2H O
3 2
21.(2023·江西省南昌市重点校高三第一次联考)宏观辨识与微观探析是化学学科核心素养之一。下列实验
现象对应的离子方程式正确的是( )
A.向NaClO溶液中通入NH 会有N 生成:3ClO-+2NH=3Cl-+N +3H O
3 2 3 2 2B.次氯酸钙溶液中通入少量的CO:ClO—+ H O+CO=HCO-+HClO
2 2 2 3
C.草酸与酸性高锰酸钾溶液反应:2MnO -+5C O2-+16H+═2Mn2++10CO ↑+8H O
4 2 4 2 2
D.明矾溶液中加入足量氢氧化钡溶液:A13++2SO2-+2Ba2++3OH-=Al(OH) ↓+2BaSO ↓
4 3 4
22.(2023·江西省上饶市、景德镇市六校高三联考)宏观辨识与微观探析是化学学科核心素养之一,下列离
子方程式能准确解释相应事实的是( )
A.工业上制漂白粉:Cl+2OH-═Cl-+ClO-+H O
2 2
B.明矾溶液通入过量氨气:Al3++4NH+2H O=AlO-+4NH+
3 2 2 4
C.向FeSO 溶液中加入NH HCO 溶液得到FeCO 沉淀:Fe2++2HCO-═FeCO ↓+CO ↑+H O
4 4 3 3 3 3 2 2
D.向NaHSO 溶液中加入足量Ba(OH) 溶液,得到白色沉淀:2H++SO2-+Ba2++2OH-═BaSO ↓+H O
4 2 4 4 2
23.(2022·湖南省雅礼中学高三月考)类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的
类推正确的是( )
选项 已知 类推
将Na加入到CuSO 溶液中:
将Na加入Fe (SO ) 溶液中: 4
A 2 4 3
6H 2 O+6Na+2Fe3+=2Fe(OH) 3 ↓+6Na++3H 2 ↑ 2HO+2Na+Cu2+=Cu(OH) ↓+2Na++H ↑
2 2 2
向Ca(ClO) 溶液中通入少量CO: 向Ca(ClO) 溶液中通入少量SO :
2 2 2 2
B
CO+Ca2++2ClO-+H O=CaCO ↓+2HClO SO +Ca2++2ClO-+H O=CaSO↓+2HClO
2 2 3 2 2 3
HCl溶液与Fe(OH) 反应:Fe(OH) +3H+= HI溶液与Fe(OH) 反应:
C 3 3 3
Fe3++3H O Fe(OH) +3H+= Fe3++3H O
2 3 2
稀盐酸与NaOH溶液反应至中性:H++OH- 稀HSO 与Ba(OH) 溶液反应至中
D 2 4 2
= HO 性:H++OH-= HO
2 2
24.(2022·江苏省镇江市高三期中)室温下,通过下列实验探究NaHCO 的性质。
3
实
实验操作和现象
验
1 用pH试纸测得0.1 mol·L-1 NaHCO 溶液的pH约为8.0
3
向10 mL 0.1 mol·L-1 NaHCO 溶液中加入10 mL 0.1 mol·L-1 NaOH 溶液,测得溶液pH约
2 3
11.3
3 向0.1 mol·L-1 NaHCO 溶液中加入过量0.1 mol·L-1 CaCl 溶液,产生白色沉淀
3 2
4 向10 mL 0.1 mol·L-1 NaHCO 溶液中加入10 mL 0.1 mol·L-1盐酸,产生无色气泡
3
下列有关说法正确的是( )
A.实验1得到的溶液中有:c(Na+)>c(HCO -)>c(CO2-)>c(HCO)
3 3 2 3
B.实验 2 得到的溶液中有 c(OH-)=c(H+)+c(HCO -)+2c(HCO)
3 2 3C.实验3反应后静置的上层清液中有c(Ca2+)·c(CO2-)>K (CaCO)
3 sp 3
D.实验4中反应的离子方程式:CO2-+2H+=CO ↑+HO
3 2 2
25.(2022·江西省赣州市十六县市十七校高三联考)中学常见的某反应的化学方程式为a+b→c+d+H O(未配
2
平,条件略去)。下列叙述不正确的是( )
A.若a是铁,b是稀硝酸(过量),且a可溶于c溶液中。则a与b反应的离子方程式为Fe+4H++NO-=Fe3+
3
+NO↑+2HO
2
B.若c、d均为气体,且都能使澄清石灰水变浑浊,则将混合气体通入溴水中,橙色褪去,其褪色过程的
离子方程式为SO +Br +2H O=4H++SO2-+2Br-
2 2 2 4
C.若a是造成温室效应的主要气体之一,c、d均为钠盐,参加反应的a、b物质的量之比为4:5,则上
述反应的离子方程式为4CO+5OH-= CO2-+3HCO-+H O
2 3 3 2
D.若c是无色有刺激性气味的气体,其水溶液呈弱碱性。在标准状况下用排空气法收集c气体得平均摩
尔质量为20g•mol-1的混合气体进行喷泉实验。假设溶质不扩散,实验完成后所得溶液的物质的量浓度约为
0.056mol•L-1
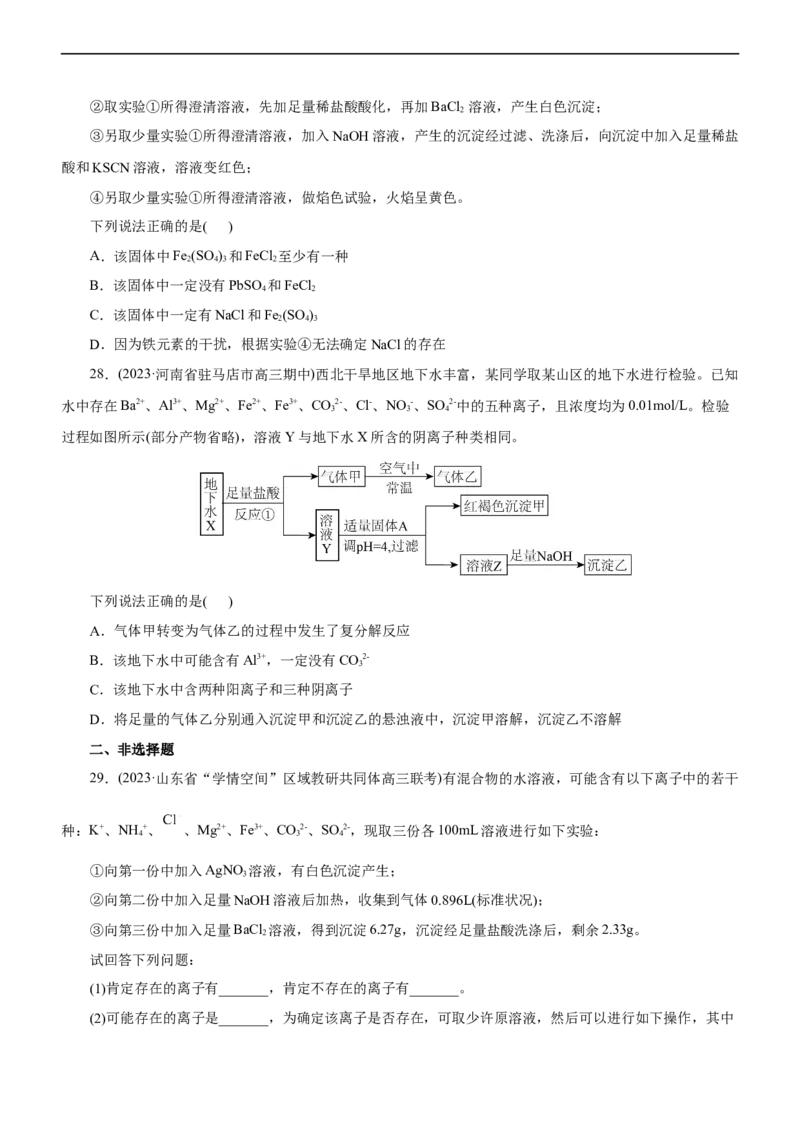
26.(2023·辽宁省葫芦岛·高三期中)某酸性溶液中可能含有 、SO 2-、SO 2-、CO2-、NH +、Fe3+、Fe2+、
4 3 3 4
Al3+和Na+。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是( )
A.反应①发生反应的离子方程式为3SO 2-+2NO-+2H+=3SO2-+2NO↑+HO
3 3 4 2
B.溶液中至少有6种离子大量存在,其中Cl-一定存在,且
C.溶液中可能含有Fe3+,一定含有Fe2+,可取少量原溶液加入 溶液检验
D.SO 2-、NH +、Na+一定存在,CO2-、Al3+一定不存在
4 4 3
27.(2023·安徽省A10联盟高三阶段性考试)某固体中可能含有Fe (SO )、FeCl、PbSO 、NaCl中一种或
2 4 3 2 4
者几种,现通过如下实验确定其成分。
①取少量该固体,加稀硫酸溶解,得到澄清溶液;②取实验①所得澄清溶液,先加足量稀盐酸酸化,再加BaCl 溶液,产生白色沉淀;
2
③另取少量实验①所得澄清溶液,加入NaOH溶液,产生的沉淀经过滤、洗涤后,向沉淀中加入足量稀盐
酸和KSCN溶液,溶液变红色;
④另取少量实验①所得澄清溶液,做焰色试验,火焰呈黄色。
下列说法正确的是( )
A.该固体中Fe (SO ) 和FeCl 至少有一种
2 4 3 2
B.该固体中一定没有PbSO 和FeCl
4 2
C.该固体中一定有NaCl和Fe (SO )
2 4 3
D.因为铁元素的干扰,根据实验④无法确定NaCl的存在
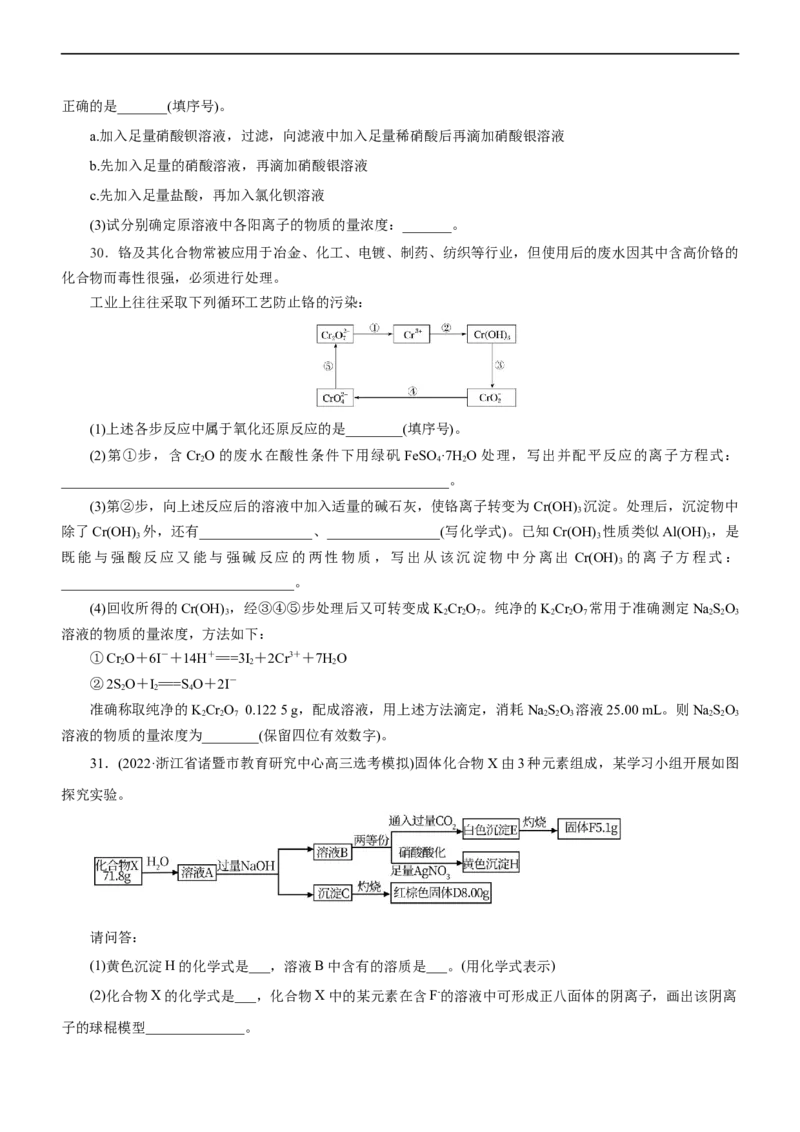
28.(2023·河南省驻马店市高三期中)西北干旱地区地下水丰富,某同学取某山区的地下水进行检验。已知
水中存在Ba2+、Al3+、Mg2+、Fe2+、Fe3+、CO2-、Cl-、NO -、SO 2-中的五种离子,且浓度均为0.01mol/L。检验
3 3 4
过程如图所示(部分产物省略),溶液Y与地下水X所含的阴离子种类相同。
下列说法正确的是( )
A.气体甲转变为气体乙的过程中发生了复分解反应
B.该地下水中可能含有Al3+,一定没有CO2-
3
C.该地下水中含两种阳离子和三种阴离子
D.将足量的气体乙分别通入沉淀甲和沉淀乙的悬浊液中,沉淀甲溶解,沉淀乙不溶解
二、非选择题
29.(2023·山东省“学情空间”区域教研共同体高三联考)有混合物的水溶液,可能含有以下离子中的若干
种:K+、NH +、 、Mg2+、Fe3+、CO2-、SO 2-,现取三份各100mL溶液进行如下实验:
4 3 4
①向第一份中加入AgNO 溶液,有白色沉淀产生;
3
②向第二份中加入足量NaOH溶液后加热,收集到气体0.896L(标准状况);
③向第三份中加入足量BaCl 溶液,得到沉淀6.27g,沉淀经足量盐酸洗涤后,剩余2.33g。
2
试回答下列问题:
(1)肯定存在的离子有_______,肯定不存在的离子有_______。
(2)可能存在的离子是_______,为确定该离子是否存在,可取少许原溶液,然后可以进行如下操作,其中正确的是_______(填序号)。
a.加入足量硝酸钡溶液,过滤,向滤液中加入足量稀硝酸后再滴加硝酸银溶液
b.先加入足量的硝酸溶液,再滴加硝酸银溶液
c.先加入足量盐酸,再加入氯化钡溶液
(3)试分别确定原溶液中各阳离子的物质的量浓度:_______。
30.铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价铬的
化合物而毒性很强,必须进行处理。
工业上往往采取下列循环工艺防止铬的污染:
(1)上述各步反应中属于氧化还原反应的是________(填序号)。
(2)第①步,含Cr O的废水在酸性条件下用绿矾 FeSO ·7H O处理,写出并配平反应的离子方程式:
2 4 2
_______________________________________________________。
(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为 Cr(OH) 沉淀。处理后,沉淀物中
3
除了Cr(OH) 外,还有________________、________________(写化学式)。已知Cr(OH) 性质类似Al(OH) ,是
3 3 3
既能与强酸反应又能与强碱反应的两性物质,写出从该沉淀物中分离出 Cr(OH) 的离子方程式:
3
_________________________________。
(4)回收所得的Cr(OH) ,经③④⑤步处理后又可转变成KCr O 。纯净的KCr O 常用于准确测定NaSO
3 2 2 7 2 2 7 2 2 3
溶液的物质的量浓度,方法如下:
①Cr O+6I-+14H+===3I +2Cr3++7HO
2 2 2
②2SO+I===S O+2I-
2 2 4
准确称取纯净的KCr O 0.122 5 g,配成溶液,用上述方法滴定,消耗NaSO 溶液25.00 mL。则NaSO
2 2 7 2 2 3 2 2 3
溶液的物质的量浓度为________(保留四位有效数字)。
31.(2022·浙江省诸暨市教育研究中心高三选考模拟)固体化合物X由3种元素组成,某学习小组开展如图
探究实验。
请问答:
(1)黄色沉淀H的化学式是___,溶液B中含有的溶质是___。(用化学式表示)
(2)化合物X的化学式是___,化合物X中的某元素在含F-的溶液中可形成正八面体的阴离子,画出该阴离
子的球棍模型______________。(3)溶液A用稀硫酸酸化后加入0.275molHO,用离子反应方程式表示发生的反应
2 2
_________________________,请设计实验验证反应后溶液中所含的金属阳离子_________________________。
32.(2022·山东省济宁市兖州区教学研究室高三期中)铈、铬、钛、镍虽不是中学阶段常见的金属元素,但
在工业生产中有着重要作用。
(1)二氧化铈(CeO)在平板电视显示屏中有着重要应用。CeO 在稀硫酸和HO 的作用下可生成Ce3+,CeO
2 2 2 2 2
在该反应中作___________剂。
(2)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的
铬。完成并配平下列离子方程式:___________
___________Cr O2-+___________ SO 2-+ =___________Cr3++___________ SO 2-+___________H O
2 7 3 4 2
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学
方程式是___________。
(4) NiSO ·xHO是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、
4 2
锌、铁等元素)为原料获得。操作步骤如下:
①向滤液Ⅰ中加入FeS是为了除去 、 等杂质。
②对滤液Ⅱ先加HO 再调pH,调pH的目的是___________。
2 2
③滤液Ⅲ溶质的主要成分是NiSO ,加NaCO 过滤后,再加适量稀硫酸溶解又生成NiSO ,这两步操作的
4 2 3 4
目的是___________。
④为测定NiSO ·xHO晶体中x的值,称取26.3g晶体加热至完全失去结晶水,剩余固体15.5g,则x的值
4 2
等于___________。
33.(2022·重庆市名校联盟高三第一次联考)某透明溶液中可能含有 、Fe3+、Al3+、NH +、 、I-、
4
NO -、SO 2-中的几种,为了确认溶液中离子的存在情况,分别取等量的试液装入5支试管里,做如下实验:
3 4
①测定溶液的pH,溶液呈强酸性;
②向溶液中加入足量稀硫酸和铜粉,振荡溶液充分反应,产生某种无色气体1.12L(标准状况),该气体遇
到空气立即变红棕色气体;
③向溶液中滴加过量氢氧化钠溶液,过滤、洗涤、灼烧、称重,得固体质量为3.2g;④向溶液中加入过量浓氢氧化钠溶液,加热,收集到气体1.12L(标准状况);
⑤向溶液中加入足量氯化钡溶液,过滤、洗涤、干燥、称重,得固体2.33g;
回答下列问题:
(1)请写出铝元素在元素周期表中的位置___________。
(2)由实验①和②可知,该溶液中一定不存在的离子是___________,写出实验②中反应生成无色气体的离
子方程式___________。
(3)实验④中收集到气体的电子式为:___________,该反应的离子方程式为:___________。
(4)根据以上实验,你认为该溶液中是否一定存在Cl-?___________(填“是”或者“否”);若存在 ,1
份溶液中其物质的量的范围为___________,如何用实验方法证明其存在___________(用简明的文字表述操作
方法、现象以及结论;若不存在 ,后面两空不用填写)
34.(2022·浙江省金华市十校联考)某兴趣小组对化合物X开展探究实验。
其中:X由4种短周期主族元素组成,B在标况下的密度为1.25g·L-1,A的焰色反应呈紫色,所有字母均
表示一种物质。(气体体积已折算为标况下的体积)
请回答:
(1)组成X的元素除了H、O外还有_______(填元素符号),X的化学式是_______。
(2)X与KClO 发生反应的化学方程式是_____________________________。
3
(3)少量A与足量Ba(OH) 反应也产生F,该反应的离子方程式是_______。
2
(4)请设计实验检验X中含有的阴离子:__________________。
35.(2023·江西省稳派名校高三统一调研考试)某溶液Q中含有如表所示离子中的5种离子,且离子浓度均
为0.5mol/L(不考虑水的电离与离子水解)。现向溶液Q中加入足量稀氢溴酸,有单一气体R产生,经分析,反
应前后阴离子种类不变。
阳离子 阴离子
K+、Fe3+、NH +、Ba2+、Fe2+、Mg2+、Al3+、Ag+ HSO -、OH-、NO -、CO2-、SO 2-、Br-、S2-、SO2-
4 3 3 3 4 2 3
已知SO2-在酸性溶液中会发生歧化反应。请回答下列问题:
2 3
(1)由“加入足量稀氢溴酸,……”“反应前后阴离子种类不变”推知:溶液Q中一定不含的阴离子有_______(填数字)种。
(2)综合推断,溶液Q中一定含有的阳离子有_______(填离子符号,下同)。产生气体R的反应中,原溶液
中过量的离子是_______,反应后溶液中物质的量一定发生变化的阳离子有_______。
(3)一定量溶液Q与氯气缓慢反应,反应后的溶液分为3份,分别进行以下操作,实验现象如图:
①铜粉参与的反应中,氧化产物是_______(填离子符号)。
②当V=448时,向溶液Q中通入氯气时发生反应的离子方程式为_______;假设不考虑Cl 与HO的反应,
2 2
则根据实验现象可推算出V的范围为_______