文档内容
专题 06 化学反应速率和化学平衡
2021年化学高考题
N O 100mL
1.(2021·浙江)一定温度下:在 2 5的四氯化碳溶液( )中发生分解反应:
2N O 4NO +O O N O
2 5 2 2。在不同时刻测量放出的 2体积,换算成 2 5浓度如下表:
t/s 0 600 1200 1710 2220 2820 x
cN O / molL1 1.40 0.96 0.66 0.48 0.35 0.24 0.12
2 5
下列说法正确的是
600~1200s NO 5.0104molL1s1
A. ,生成 2的平均速率为
2220s O 11.8L
B.反应 时,放出的 2体积为 (标准状况)
v NO =2v NO
C.反应达到平衡时, 正 2 5 逆 2
D.推测上表中的x为3930
2.(2021·浙江)相同温度和压强下,关于物质熵的大小比较,合理的是
1mol CH (g)<1mol H (g) 1mol H O(g)<2mol H O(g)
A. 4 2 B. 2 2
1mol H O(s)>1mol H O(l) 1mol C
s,
金刚石
1mol C
s,
石墨
C. 2 2 D.
X2Z XY Y2Z
3.(2021·广东高考真题)反应 经历两步:① ;② 。反应体系中
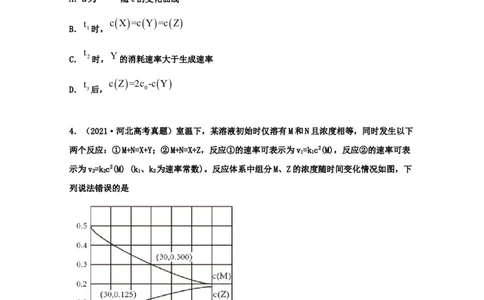
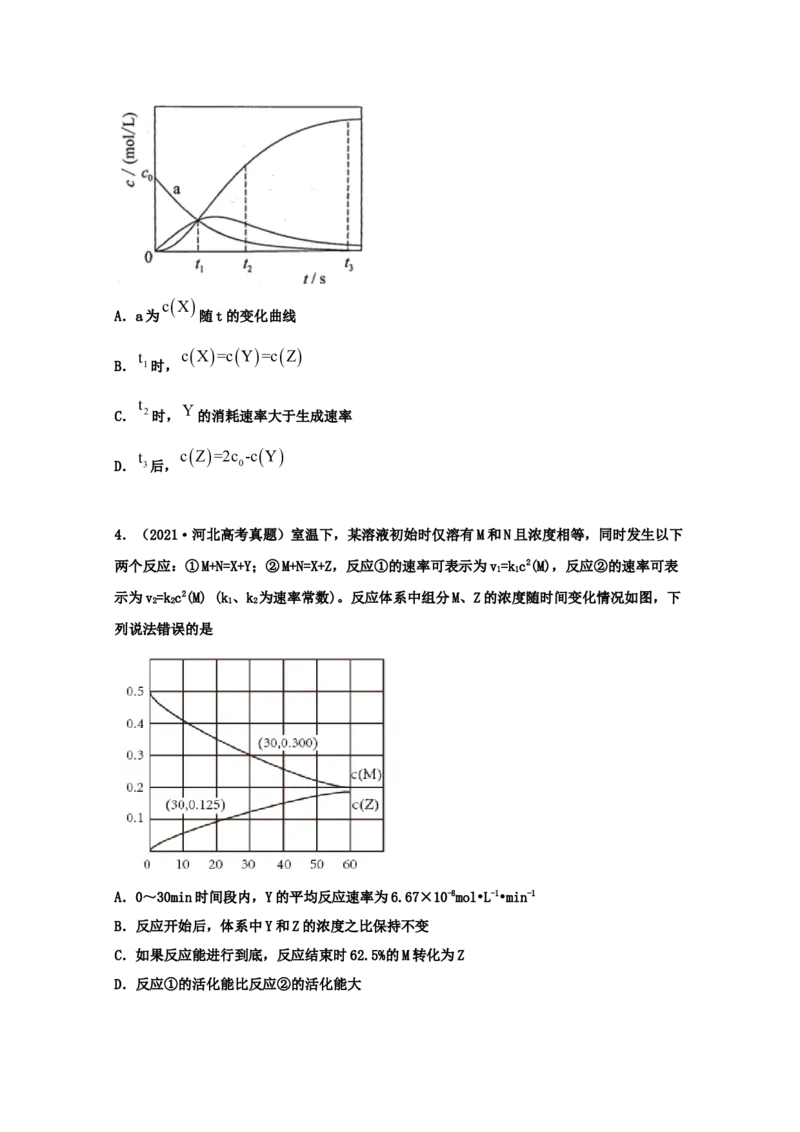
X、Y、Z的浓度c随时间t的变化曲线如图所示。下列说法不正确的是cX
A.a为 随t的变化曲线
t
cX=cY=cZ
B. 1时,
t
C. 2时, Y 的消耗速率大于生成速率
t
cZ=2c -cY
D. 3后, 0
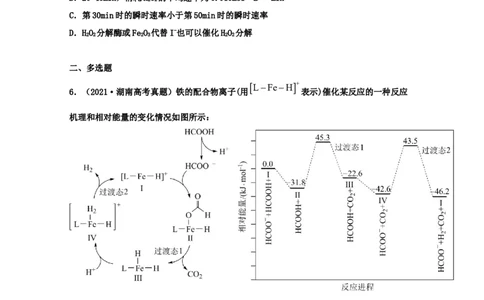
4.(2021·河北高考真题)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下
两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表
1 1
示为v=kc2(M) (k、k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下
2 2 1 2
列说法错误的是
A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大5.(2021·浙江高考真题)取50 mL过氧化氢水溶液,在少量I- 存在下分解:
2HO=2HO+O↑。在一定温度下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2 2 2 2 2
t/min 0 20 40 60 80
c/
0.80 0.40 0.20 0.10 0.050
(mol·L-1)
下列说法不正确的是
A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或FeO 代替I-也可以催化HO 分解
2 2 2 3 2 2
二、多选题
LFeH
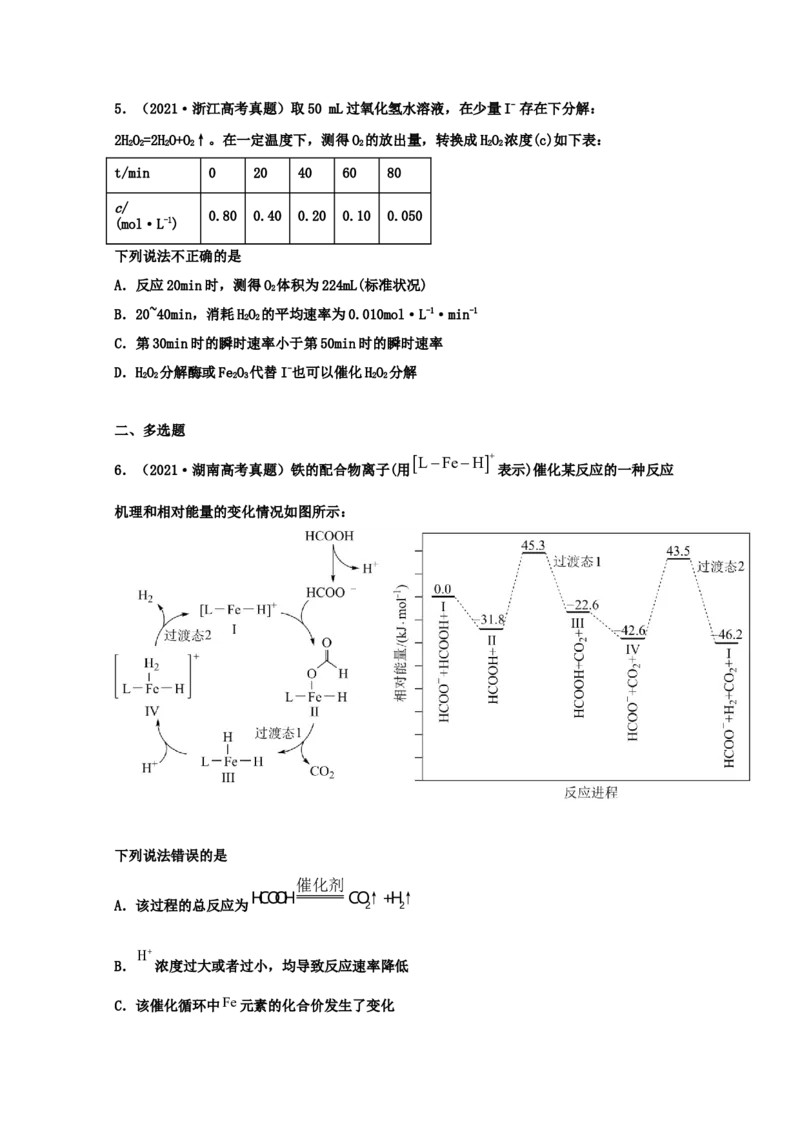
6.(2021·湖南高考真题)铁的配合物离子(用 表示)催化某反应的一种反应
机理和相对能量的变化情况如图所示:
下列说法错误的是
催化剂
HCOOH CO↑+H↑
A.该过程的总反应为 2 2
H
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中Fe元素的化合价发生了变化D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
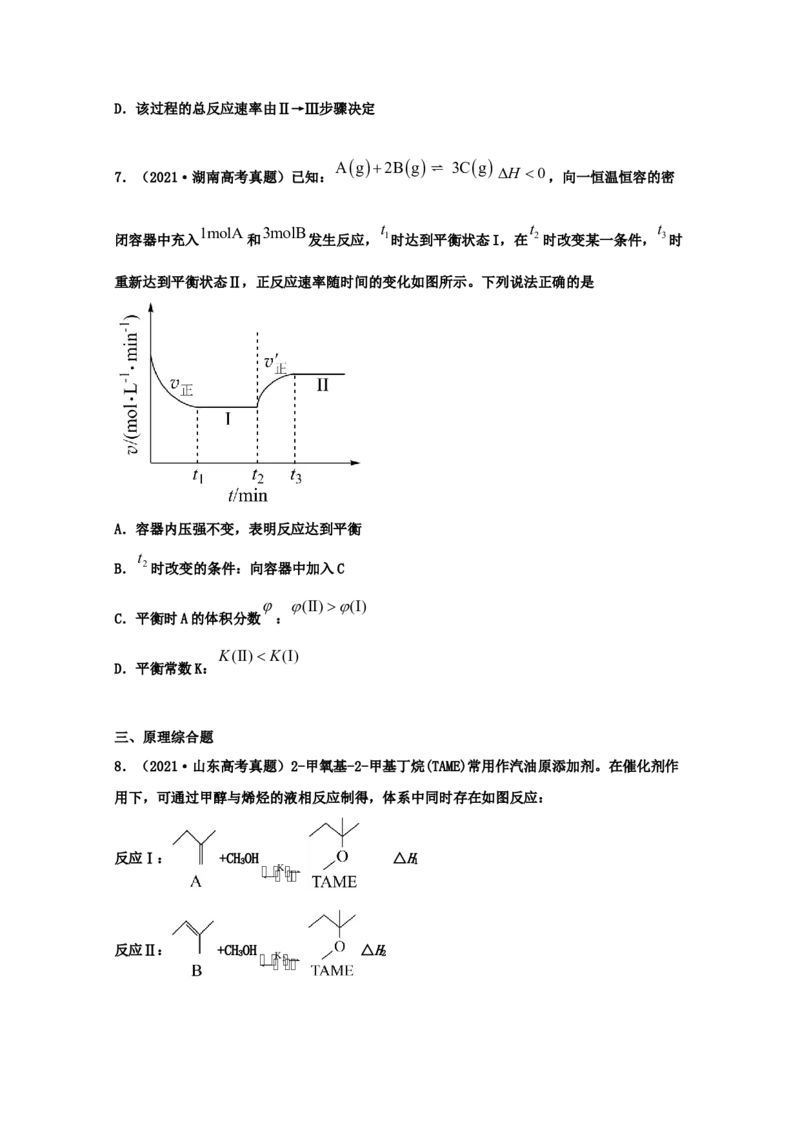
7.(2021·湖南高考真题)已知:
Ag2Bg
3Cg
H 0,向一恒温恒容的密
1molA 3molB t t t
闭容器中充入 和 发生反应, 1时达到平衡状态I,在 2时改变某一条件, 3时
重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡
t
B. 2时改变的条件:向容器中加入C
(II)(I)
C.平衡时A的体积分数 :
K(II) K(I)
D.平衡常数K:
三、原理综合题
8.(2021·山东高考真题)2-甲氧基-2-甲基丁烷(TAME)常用作汽油原添加剂。在催化剂作
用下,可通过甲醇与烯烃的液相反应制得,体系中同时存在如图反应:
反应Ⅰ: +CHOH △H
3 1
K 1
反应Ⅱ: +CHOH △H
3 K 2 2反应Ⅲ: K 3 △H 3
回答下列问题:
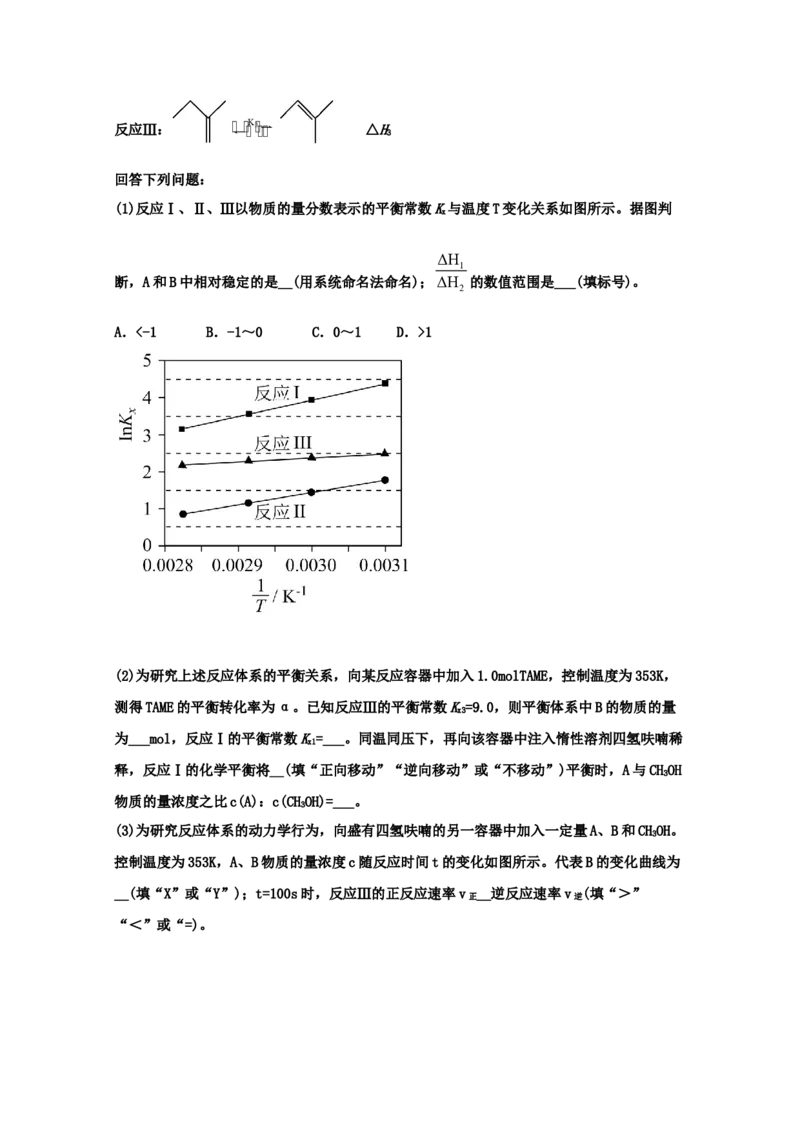
(1)反应Ⅰ、Ⅱ、Ⅲ以物质的量分数表示的平衡常数K与温度T变化关系如图所示。据图判
x
ΔH
1
断,A和B中相对稳定的是__(用系统命名法命名);ΔH 的数值范围是___(填标号)。
2
A.<-1 B.-1~0 C.0~1 D.>1
(2)为研究上述反应体系的平衡关系,向某反应容器中加入1.0molTAME,控制温度为353K,
测得TAME的平衡转化率为α。已知反应Ⅲ的平衡常数K=9.0,则平衡体系中B的物质的量
x3
为___mol,反应Ⅰ的平衡常数K=___。同温同压下,再向该容器中注入惰性溶剂四氢呋喃稀
x1
释,反应Ⅰ的化学平衡将__(填“正向移动”“逆向移动”或“不移动”)平衡时,A与CHOH
3
物质的量浓度之比c(A):c(CHOH)=___。
3
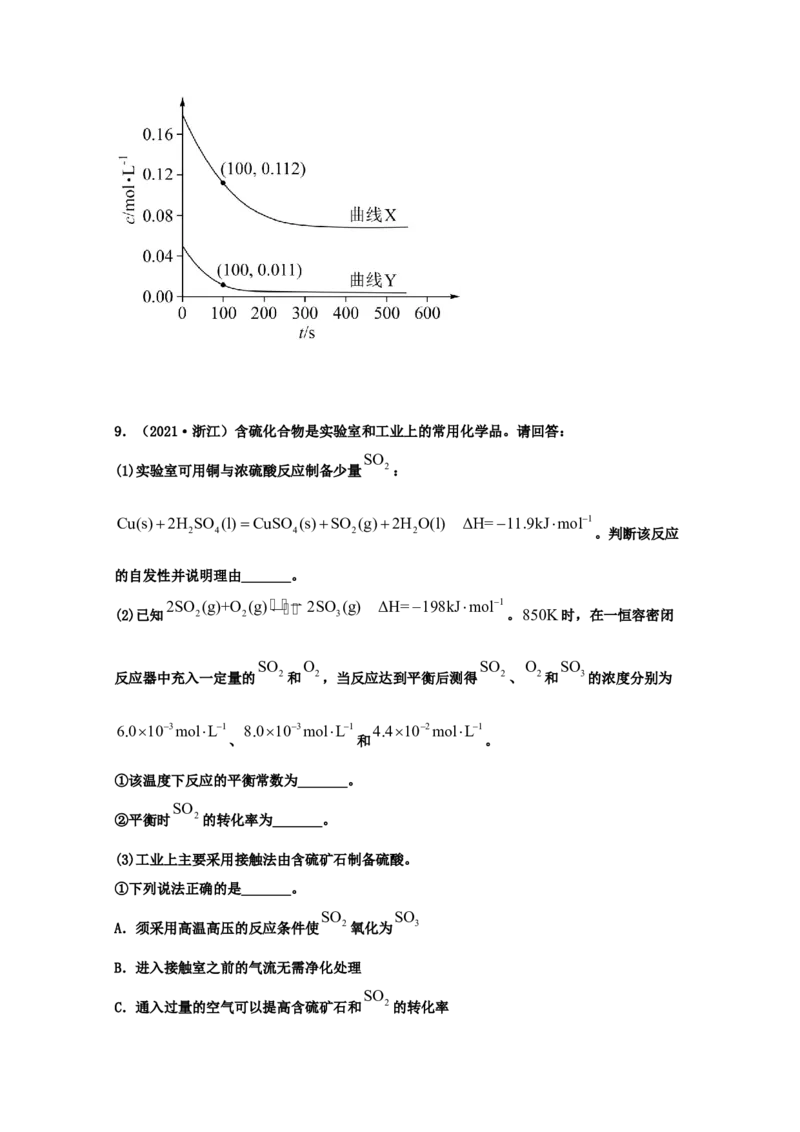
(3)为研究反应体系的动力学行为,向盛有四氢呋喃的另一容器中加入一定量A、B和CHOH。
3
控制温度为353K,A、B物质的量浓度c随反应时间t的变化如图所示。代表B的变化曲线为
__(填“X”或“Y”);t=100s时,反应Ⅲ的正反应速率v __逆反应速率v (填“>”
正 逆
“<”或“=)。9.(2021·浙江)含硫化合物是实验室和工业上的常用化学品。请回答:
SO
(1)实验室可用铜与浓硫酸反应制备少量 2:
Cu(s)2H SO (l)CuSO (s)SO (g)2H O(l) ΔH=11.9kJmol1
2 4 4 2 2 。判断该反应
的自发性并说明理由_______。
(2)已知
2SO
2
(g)+O
2
(g)
2SO
3
(g) ΔH=198kJmol1
。850K时,在一恒容密闭
SO O SO O SO
反应器中充入一定量的 2和 2,当反应达到平衡后测得 2、 2和 3的浓度分别为
6.0103molL1 8.0103molL1 4.4102molL1
、 和 。
①该温度下反应的平衡常数为_______。
SO
②平衡时 2的转化率为_______。
(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法正确的是_______。
SO SO
A.须采用高温高压的反应条件使 2氧化为 3
B.进入接触室之前的气流无需净化处理
SO
C.通入过量的空气可以提高含硫矿石和 2的转化率SO
D.在吸收塔中宜采用水或稀硫酸吸收 3以提高吸收速率
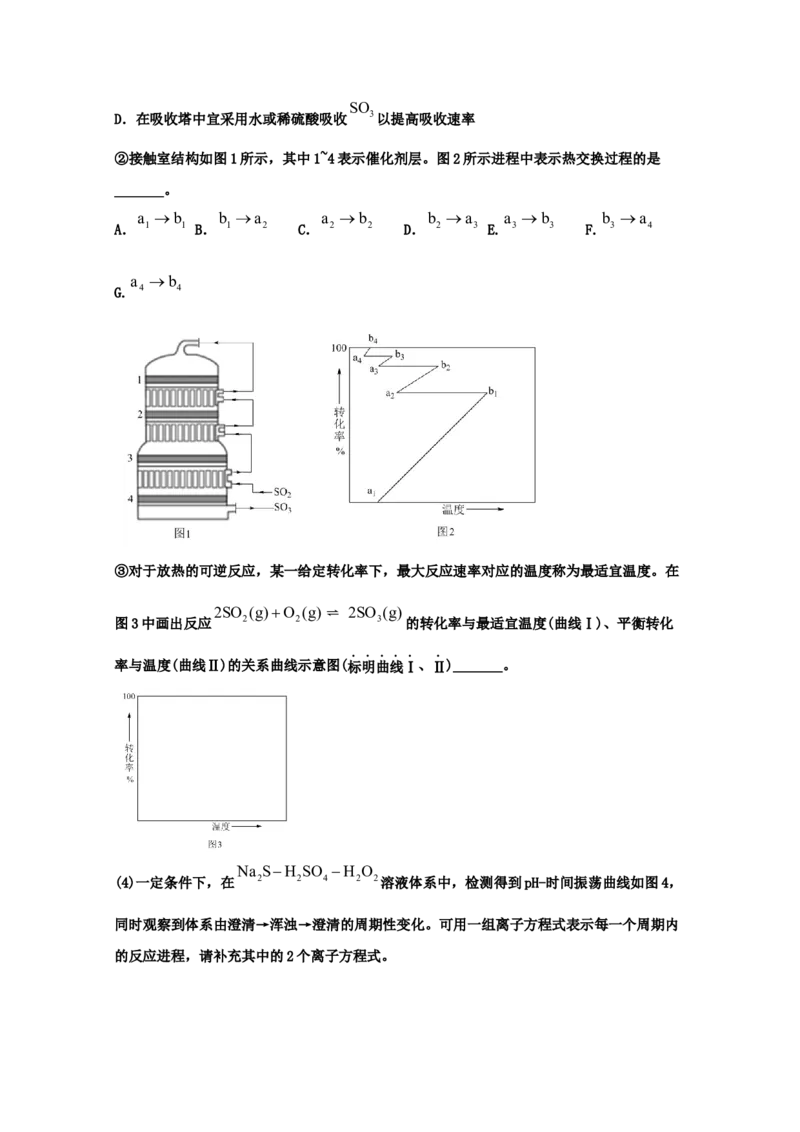
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是
_______。
a b b a a b b a a b b a
A. 1 1 B. 1 2 C. 2 2 D. 2 3 E. 3 3 F. 3 4
a b
G. 4 4
③对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。在
2SO (g)O (g) 2SO (g)
图3中画出反应 2 2 3 的转化率与最适宜温度(曲线Ⅰ)、平衡转化
率与温度(曲线Ⅱ)的关系曲线示意图(标明曲线Ⅰ、Ⅱ)_______。
Na SH SO H O
(4)一定条件下,在 2 2 4 2 2溶液体系中,检测得到pH-时间振荡曲线如图4,
同时观察到体系由澄清→浑浊→澄清的周期性变化。可用一组离子方程式表示每一个周期内
的反应进程,请补充其中的2个离子方程式。S2 H=HS
Ⅰ.
Ⅱ.①_______;
HS H O H=S2H O
Ⅲ. 2 2 2 ;
Ⅳ.②_______。
10.(2021·广东高考真题)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH
4
与CO 重整是CO 利用的研究热点之一。该重整反应体系主要涉及以下反应:
2 2
a)CH(g)+CO(g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
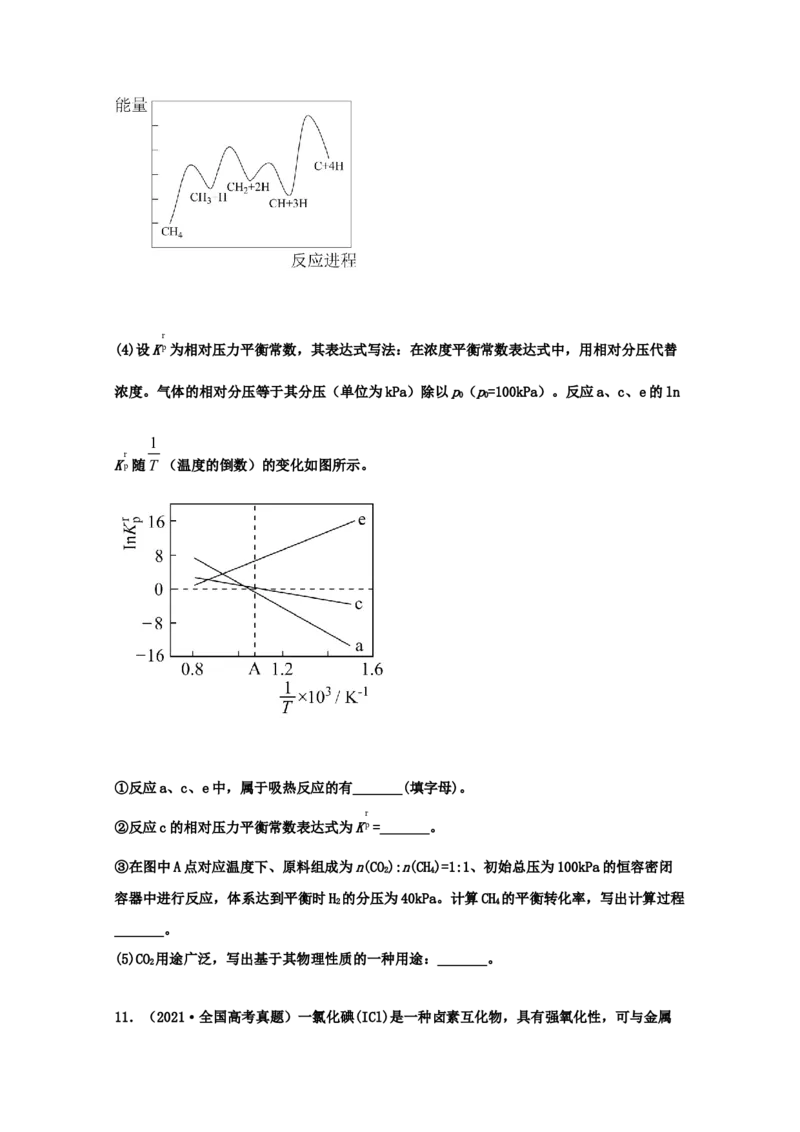
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第
4
_______步的正反应活化能最大。r
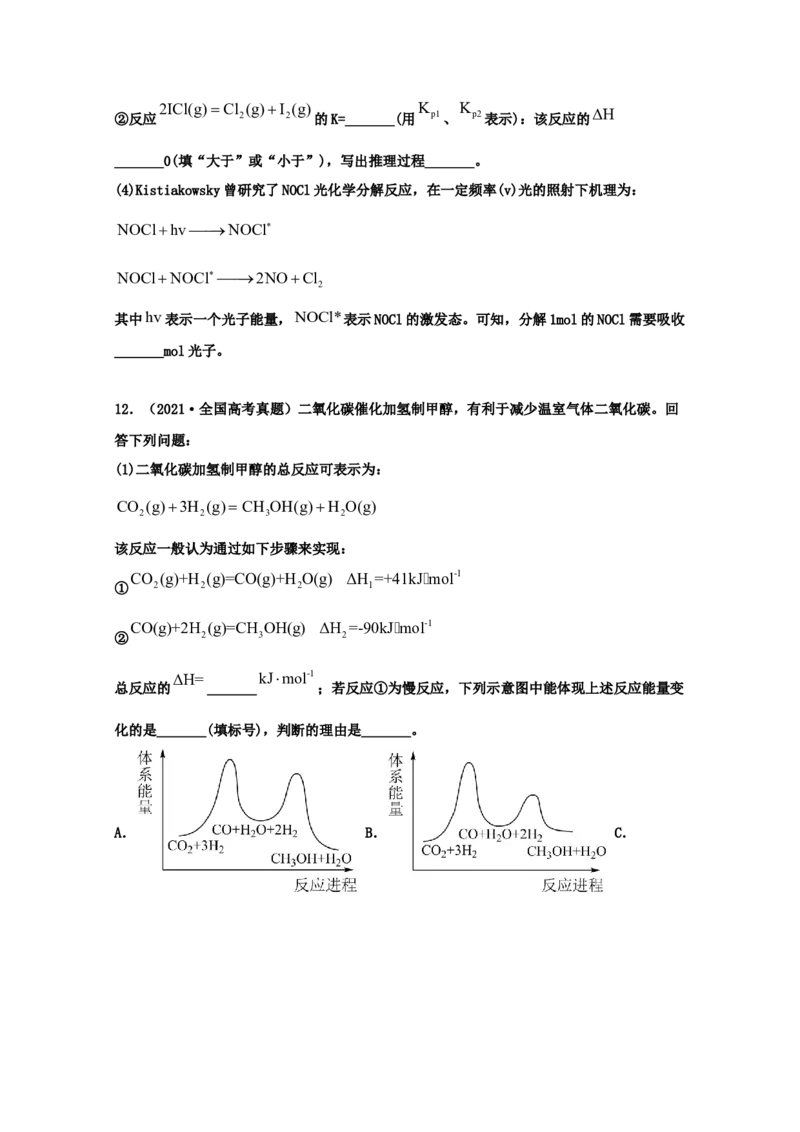
(4)设Kp为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替
浓度。气体的相对分压等于其分压(单位为kPa)除以p(p=100kPa)。反应a、c、e的ln
0 0
1
r
Kp随T (温度的倒数)的变化如图所示。
①反应a、c、e中,属于吸热反应的有_______(填字母)。
r
②反应c的相对压力平衡常数表达式为Kp=_______。
③在图中A点对应温度下、原料组成为n(CO):n(CH)=1:1、初始总压为100kPa的恒容密闭
2 4
容器中进行反应,体系达到平衡时H 的分压为40kPa。计算CH 的平衡转化率,写出计算过程
2 4
_______。
(5)CO 用途广泛,写出基于其物理性质的一种用途:_______。
2
11.(2021·全国高考真题)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过
了一种新元素的发现,该元素是_______。
BaPtCl BaCl Pt Cl
(2)氯铂酸钡( 6)固体加热时部分分解为 2、 和 2,376.8℃时平衡常数
K′1.0104Pa2
BaPtCl
p ,在一硬质玻璃烧瓶中加入过量 6,抽真空后,通过一支管通入碘
蒸气(然后将支管封闭),在376.8℃,碘蒸气初始压强为20.0kPa。376.8℃平衡时,测得烧
32.5kPa p = kPa 2ICl(g)Cl (g)I (g)
瓶中压强为 ,则 ICl _______ ,反应 2 2 的平衡常数
K=_______(列出计算式即可)。
K
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 p。
2NO(g)+2ICl(g) 2NOCl(g)+I (g) K
2 p1
2NOCl(g) 2NO(g)+Cl (g) K
2 p2
1 1
lgK ~ lgK ~
得到 p1 T 和 p2 T均为线性关系,如下图所示:
Cl
①由图可知,NOCl分解为NO和 2反应的 ΔH _______0(填“大于”或“小于”)2ICl(g)Cl (g)I (g) K K
②反应 2 2 的K=_______(用 p1、 p2表示):该反应的 ΔH
_______0(填“大于”或“小于”),写出推理过程_______。
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
NOClhvNOCl
NOClNOCl 2NOCl
2
其中hv表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
_______mol光子。
12.(2021·全国高考真题)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回
答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
CO (g)3H (g) CH OH(g)H O(g)
2 2 3 2
该反应一般认为通过如下步骤来实现:
CO (g)+H (g)=CO(g)+H O(g) ΔH =+41kJmol-1
① 2 2 2 1
CO(g)+2H (g)=CH OH(g) ΔH =-90kJmol-1
② 2 3 2
ΔH= kJmol-1
总反应的 _______ ;若反应①为慢反应,下列示意图中能体现上述反应能量变
化的是_______(填标号),判断的理由是_______。
A. B. C.D.
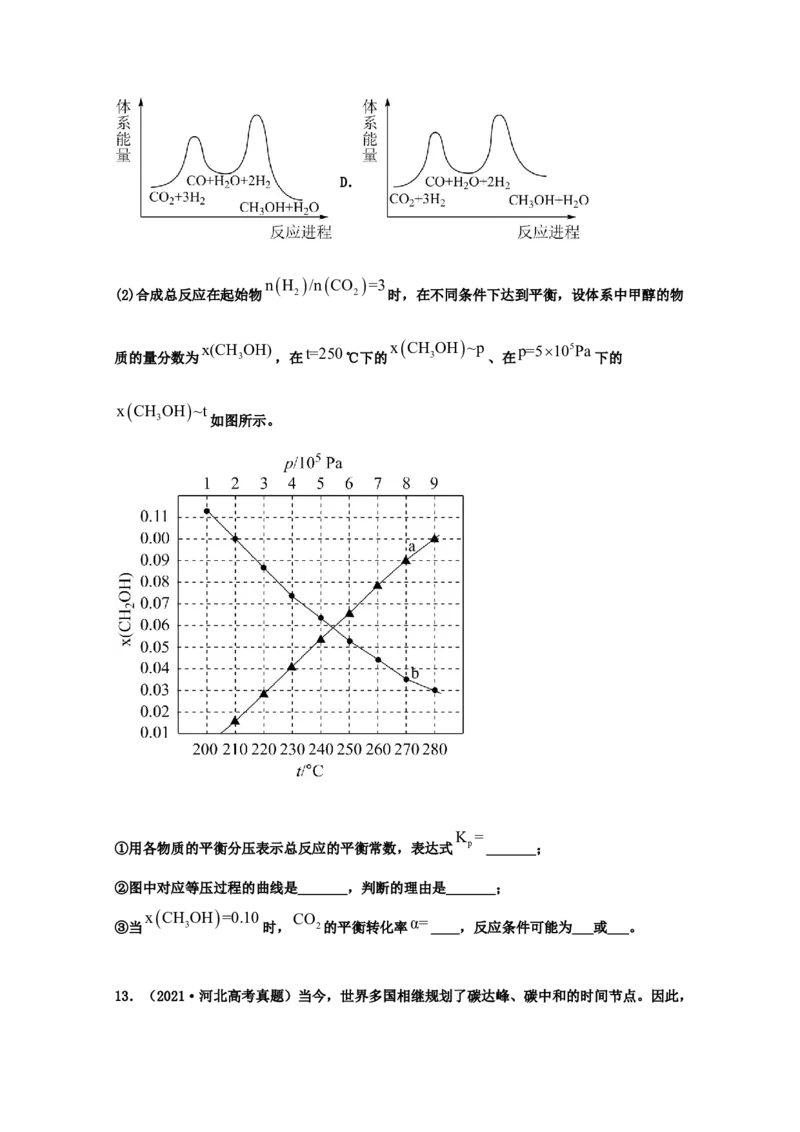
nH /nCO =3
(2)合成总反应在起始物 2 2 时,在不同条件下达到平衡,设体系中甲醇的物
x(CH OH) t=250 xCH OH~p p=5105Pa
质的量分数为 3 ,在 ℃下的 3 、在 下的
xCH OH~t
3 如图所示。
K =
①用各物质的平衡分压表示总反应的平衡常数,表达式 p _______;
②图中对应等压过程的曲线是_______,判断的理由是_______;
xCH OH=0.10
CO α=
③当 3 时, 2的平衡转化率 ____,反应条件可能为___或___。
13.(2021·河北高考真题)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物
质的燃烧热数据如表:
物质 H(g) C(石墨,s) CH(l)
2 6 6
燃烧热△H(kJ•mol-1) -285.8 -393.5 -3267.5
(1)则25℃时H(g)和C(石墨,s)生成CH(l)的热化学方程式为________。
2 6 6
(2)雨水中含有来自大气的CO,溶于水中的CO 进一步和水反应,发生电离:
2 2
①CO(g)=CO(aq)
2 2
②CO(aq)+HO(l)=H+(aq)+HCO3 (aq)
2 2
25℃时,反应②的平衡常数为K。
2
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
2
ymol•L-1•kPa-1,当大气压强为pkPa,大气中CO(g)的物质的量分数为x时,溶液中H+浓度为
2
________mol•L-1(写出表达式,考虑水的电离,忽略HCO3 的电离)
(3)105℃时,将足量的某碳酸氢盐(MHCO)固体置于真空恒容容器中,存在如下平衡:
3
Δ
2MHCO(s) MCO(s)+HO(g)+CO(g)。上述反应达平衡时体系的总压为46kPa。
3 2 3 2 2
保持温度不变,开始时在体系中先通入一定量的CO(g),再加入足量MHCO(s),欲使平衡时
2 3
体系中水蒸气的分压小于5kPa,CO(g)的初始压强应大于________kPa。
2
(4)我国科学家研究Li—CO 电池,取得了重大科研成果,回答下列问题:
2
①Li—CO 电池中,Li为单质锂片,则该电池中的CO 在___(填“正”或“负”)极发生电化
2 2
学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且CO 电还原后与锂离子结合形成
2
碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。
2 2 2
Ⅰ.2CO+2e-=CO4 Ⅱ.CO4 =CO+CO2
2 2 2 2
2
Ⅲ.__________ Ⅳ.CO3 +2Li+=LiCO
2 3
②研究表明,在电解质水溶液中,CO 气体可被电化学还原。
2
Ⅰ.CO 在碱性介质中电还原为正丙醇(CHCHCHOH)的电极反应方程式为_________。
2 3 2 2
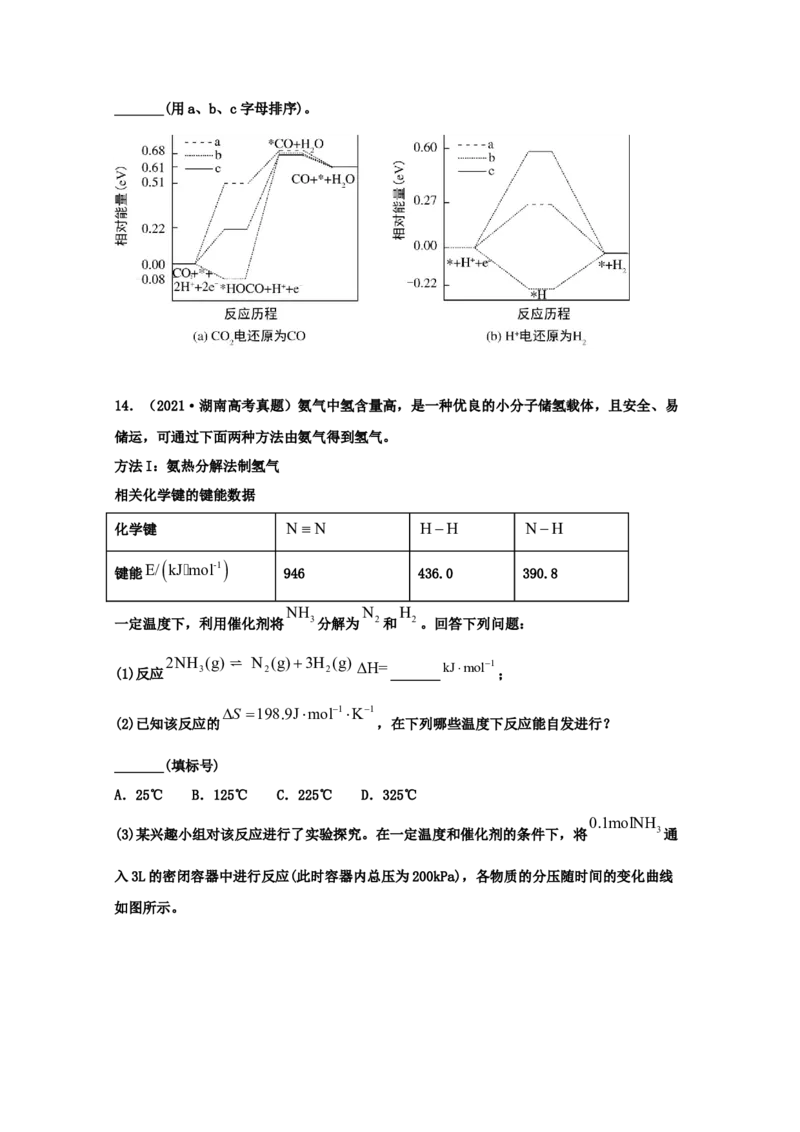
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO 电还原为CO的反应进程中(H+被还原
2
为H 的反应可同时发生),相对能量变化如图.由此判断,CO 电还原为CO从易到难的顺序为
2 2_______(用a、b、c字母排序)。
14.(2021·湖南高考真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易
储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键 N N HH NH
键能E/
kJmol-1
946 436.0 390.8
NH N H
一定温度下,利用催化剂将 3分解为 2和 2。回答下列问题:
(1)反应 2NH 3 (g) N 2 (g)3H 2 (g) ΔH= _______ kJmol1 ;
S 198.9Jmol1K1
(2)已知该反应的 ,在下列哪些温度下反应能自发进行?
_______(填标号)
A.25℃ B.125℃ C.225℃ D.325℃
0.1molNH
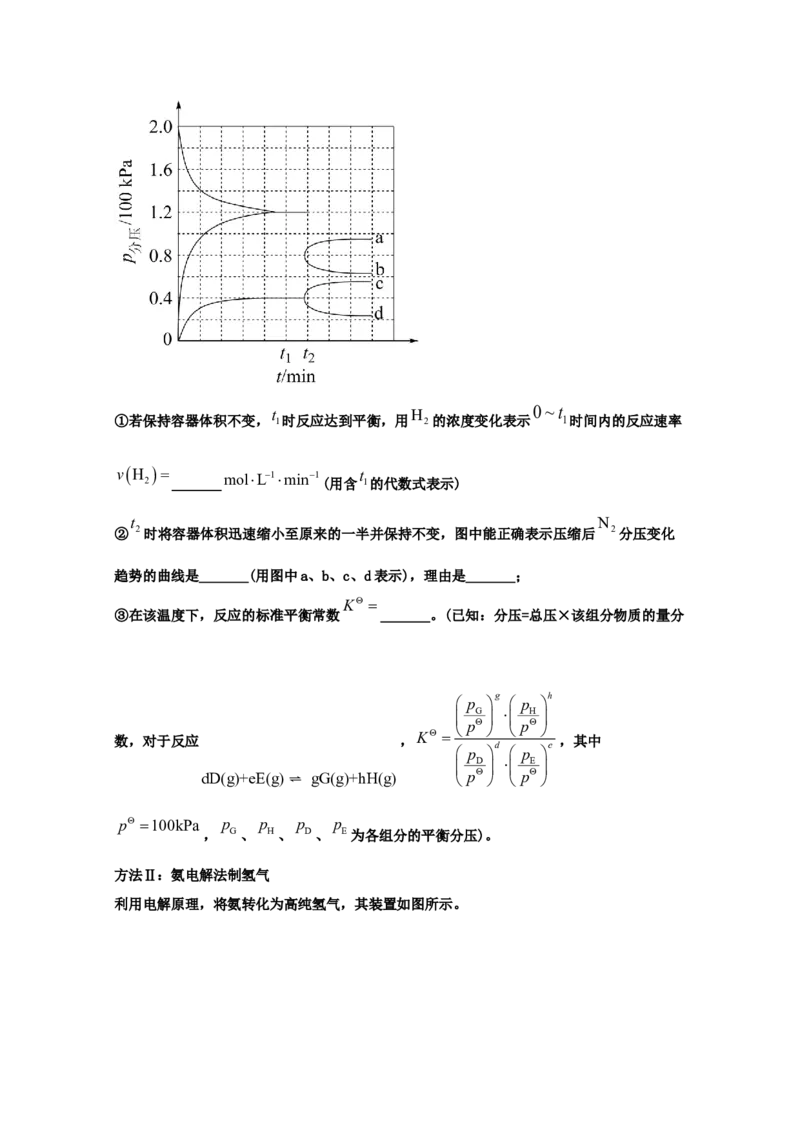
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将 3通
入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线
如图所示。0~t
t H
①若保持容器体积不变, 1时反应达到平衡,用 2的浓度变化表示 1时间内的反应速率
vH
2
_______
molL1min1
(用含
t
1的代数式表示)
t N
② 2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 2分压变化
趋势的曲线是_______(用图中a、b、c、d表示),理由是_______;
K
③在该温度下,反应的标准平衡常数 _______。(已知:分压=总压×该组分物质的量分
g h
p p
G H
p
p
数,对于反应 ,K ,其中
d e
p p
D E
dD(g)+eE(g) gG(g)+hH(g) p p
p 100kPa p p p p
, G 、 H、 D、 E为各组分的平衡分压)。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。OH
(4)电解过程中 的移动方向为_______(填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______。
KOH溶液KOH溶液
15.(2021·浙江高考真题)“氯碱工业”以电解饱和食盐水为基础制取氯气等产品, 氯
气是实验室和工业上的常用气体。请回答:
(1)电解饱和食盐水制取氯气的化学方程式是______。
(2)下列说法不正确的是______。
A.可采用碱石灰干燥氯气
B.可通过排饱和食盐水法收集氯气
C.常温下,可通过加压使氯气液化而储存于钢瓶中
D.工业上,常用氢气和氯气反应生成的氯化氢溶于水制取盐酸
(3)在一定温度下,氯气溶于水的过程及其平衡常数为:
Cl(g) Cl(aq) K=c(Cl)/p
2 2 1 2
Cl (aq) + HO(l) H+ (aq)+Cl- (aq) + HClO(aq) K
2 2 2
其中p为Cl(g)的平衡压强,c(Cl)为Cl 在水溶液中的平衡浓度。
2 2 2
①Cl(g) Cl(aq)的焓变ΔH______0。(填”>”、“=”或“<”)
2 2 1
②平衡常数K 的表达式为K=______。
2 2
③氯气在水中的溶解度(以物质的量浓度表示)为c,则c=______。(用平衡压强p和上述平衡
常数表示,忽略HClO的电离)
(4)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO)为原料生产TiCl,相应
2 4
的化学方程式为;
I.TiO(s)+2Cl(g) TiCl(g)+O(g) ΔH=181 mol·L-1,K=-3.4×10-29
2 2 4 2 I I
II.2C(s)+O(g) 2CO(g) ΔH= - 221 mol·L-1,K=1.2×1048
2 II II结合数据说明氯化过程中加碳的理由______ 。
(5)在一定温度下,以I 为催化剂,氯苯和Cl 在CS 中发生平行反应,分别生成邻二氯苯和
2 2 2
对二氯苯,两产物浓度之比与反应时间无关。反应物起始浓度均为0.5 mol·L-1,反应30
min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。保持其他条件不变,若要提高产物
中邻二氯苯的比例,可采用的措施是______。
A.适当提高反应温度 B.改变催化剂
C.适当降低反应温度 D.改变反应物浓度
2021年化学高考模拟题
1.(2021·九龙坡区·重庆市育才中学高三三模)均为1L的密闭容器中进行实验,测得气
体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如表:
容器编号 起始物质 t/min 0 20 40 60 80 100
0.5molI、
Ⅰ 2 ω(HI)/% 0 50 68 76 80 80
0.5molH
2
Ⅱ 1molHI ω(HI)/% 100 91 84 81 80 80
研究发现上述反应中v(正)=k·ω(H)·ω(I),v(逆)=k·ω2(HI),其中k、k 为常数。
a 2 2 b a b
下列说法正确的是
k
a =32
A.温度为T时该反应的k
b
B.容器Ⅰ中前20min的平均速率v(HI)=0.0125mol·L-1·min-1
C.若起始时,向容器I中加入物质的量均为0.1mol的H、I、HI,反应逆向进行
2 2
D.容器Ⅱ中达到平衡时的转化率为20%
2.(2021·重庆市第十一中学校高三二模)在体积可变的恒压密闭容器中,一定量的CO 与
2
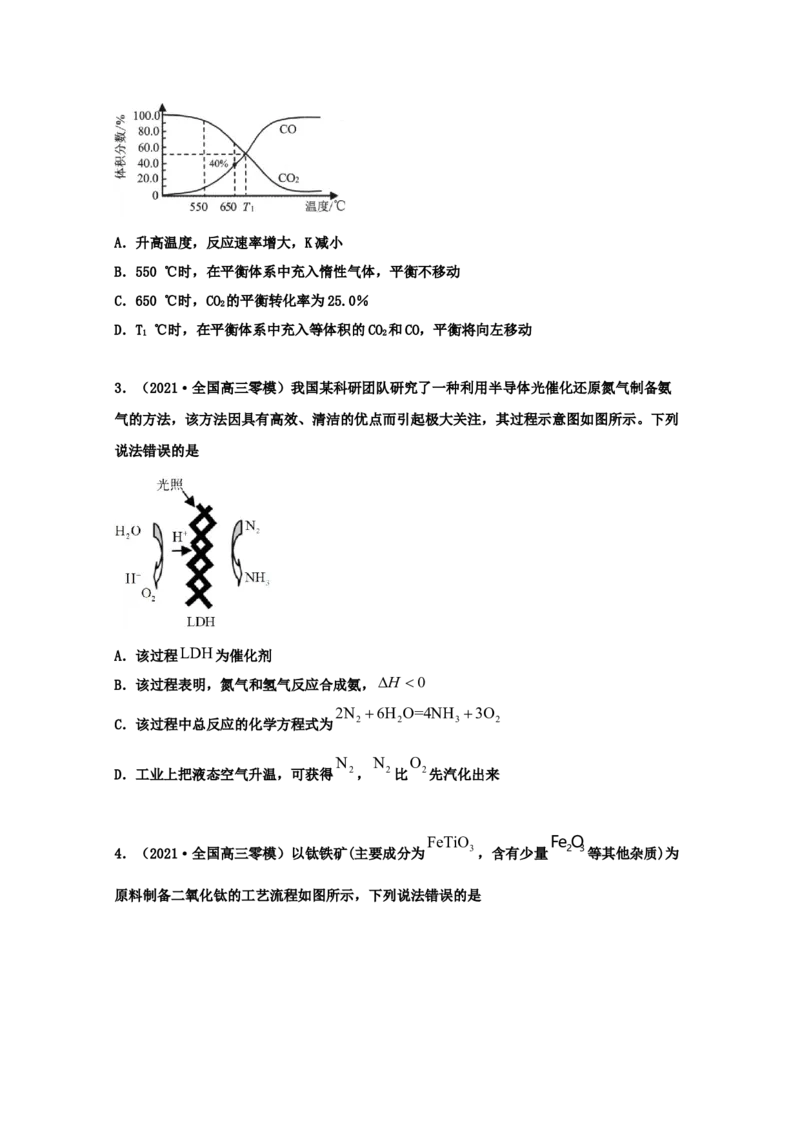
足量碳发生反应:C(s)+CO(g)
2CO(g)。平衡时,体系中气体体积分数与温度的关系
2
如图。下列说法正确的是A.升高温度,反应速率增大,K减小
B.550 ℃时,在平衡体系中充入惰性气体,平衡不移动
C.650 ℃时,CO 的平衡转化率为25.0%
2
D.T ℃时,在平衡体系中充入等体积的CO 和CO,平衡将向左移动
1 2
3.(2021·全国高三零模)我国某科研团队研究了一种利用半导体光催化还原氮气制备氨
气的方法,该方法因具有高效、清洁的优点而引起极大关注,其过程示意图如图所示。下列
说法错误的是
A.该过程LDH为催化剂
B.该过程表明,氮气和氢气反应合成氨,H 0
2N 6H O=4NH 3O
C.该过程中总反应的化学方程式为 2 2 3 2
N N O
D.工业上把液态空气升温,可获得 2, 2比 2先汽化出来
FeTiO FeO
4.(2021·全国高三零模)以钛铁矿(主要成分为 3,含有少量 2 3等其他杂质)为
原料制备二氧化钛的工艺流程如图所示,下列说法错误的是Fe2 Fe2
已知:水解时,若溶液中存在 ,则 会与溶液中的钛酸分离。
A.研磨的目的是增大接触面积,加快反应速率
Fe3
B.加入铁粉的目的是还原
TiO2 TiO2 2H O=H TiO 2H
C.“水解”时, 发生反应的离子方程式为: 2 2 3
K FeCN
D.洗涤步骤中,若向洗涤液中加入 3 6 溶液,无蓝色沉淀产生,说明已洗涤干
净
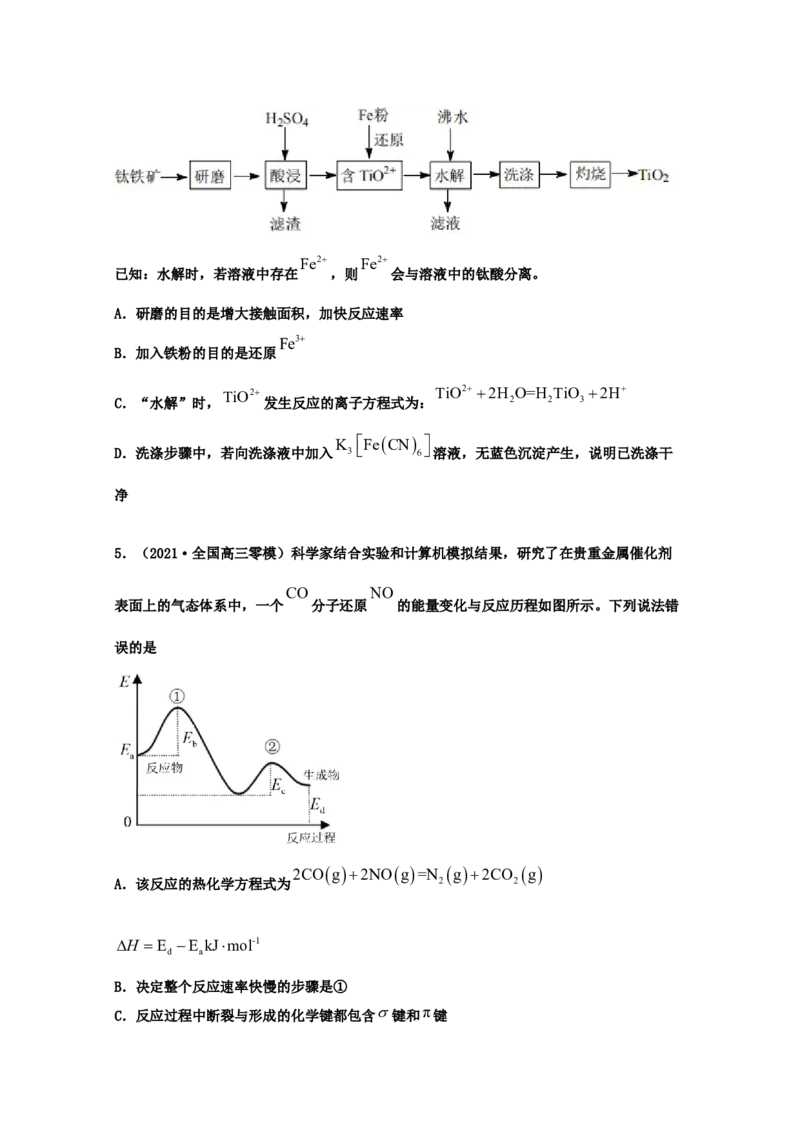
5.(2021·全国高三零模)科学家结合实验和计算机模拟结果,研究了在贵重金属催化剂
CO NO
表面上的气态体系中,一个 分子还原 的能量变化与反应历程如图所示。下列说法错
误的是
2COg2NOg=N g2CO g
A.该反应的热化学方程式为 2 2
H E E kJmol-1
d a
B.决定整个反应速率快慢的步骤是①
C.反应过程中断裂与形成的化学键都包含键和 π 键D.改变催化剂,不能使反应的焓变发生改变
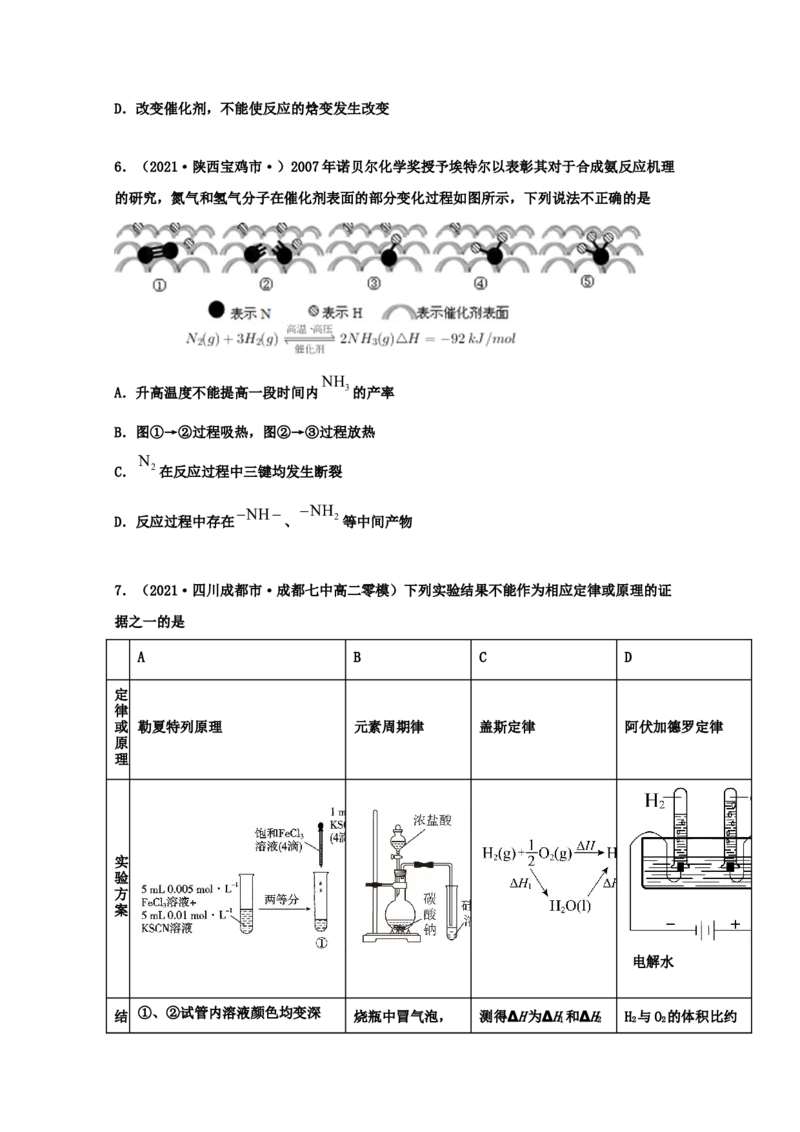
6.(2021·陕西宝鸡市·)2007年诺贝尔化学奖授予埃特尔以表彰其对于合成氨反应机理
的研究,氮气和氢气分子在催化剂表面的部分变化过程如图所示,下列说法不正确的是
NH
A.升高温度不能提高一段时间内 3的产率
B.图①→②过程吸热,图②→③过程放热
N
C. 2在反应过程中三键均发生断裂
NH NH
D.反应过程中存在 、 2等中间产物
7.(2021·四川成都市·成都七中高二零模)下列实验结果不能作为相应定律或原理的证
据之一的是
A B C D
定
律
或 勒夏特列原理 元素周期律 盖斯定律 阿伏加德罗定律
原
理
实
验
方
案
电解水
结 ①、②试管内溶液颜色均变深 烧瓶中冒气泡, 测得∆H为∆H和∆H H 与O 的体积比约
1 2 2 2果 试管中出现浑浊 的和 为2:1
A.A B.B C.C D.D
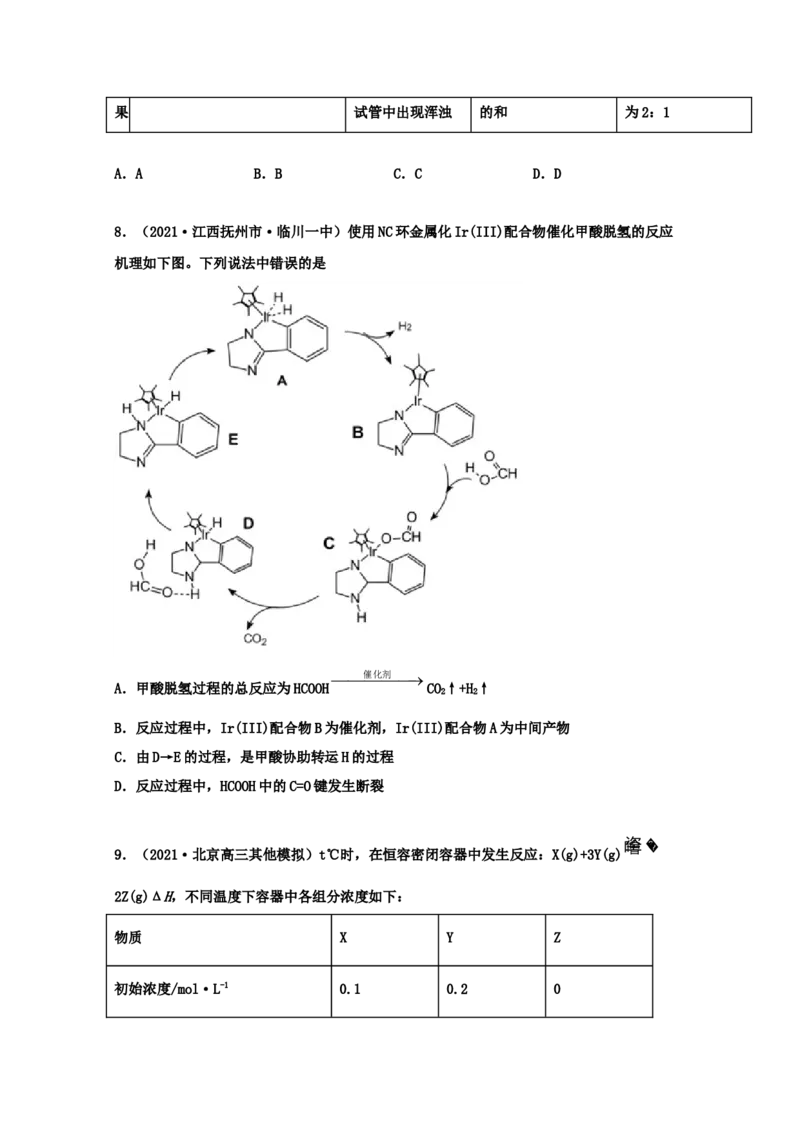
8.(2021·江西抚州市·临川一中)使用NC环金属化Ir(III)配合物催化甲酸脱氢的反应
机理如下图。下列说法中错误的是
催化剂
A.甲酸脱氢过程的总反应为HCOOH CO↑+H↑
2 2
B.反应过程中,Ir(III)配合物B为催化剂,Ir(III)配合物A为中间产物
C.由D→E的过程,是甲酸协助转运H的过程
D.反应过程中,HCOOH中的C=O键发生断裂
噲垐 ��
9.(2021·北京高三其他模拟)t℃时,在恒容密闭容器中发生反应:X(g)+3Y(g)
2Z(g)ΔH,不同温度下容器中各组分浓度如下:
物质 X Y Z
初始浓度/mol·L-1 0.1 0.2 0350℃ 0.05 0.05 0.1
平衡浓度/
mol·L-1
400℃ 0.08 0.14 0.04
已知:350℃时,反应经5min达到平衡状态。
下列说法不正确的是
A.该反应的ΔH<0
B.350℃时,5min内该反应平均速率v(Y)=0.03mol·L-1·min-1
C.350℃达到平衡后再通入少量Y(g),达到新平衡时,X转化率增大
D.350℃时,该反应的平衡常数K=40
10.(2021·北京高三其他模拟)Deacon催化氧化法将HCl转化为Cl 的反应为:4HCl(g)
2
+O(g)=2Cl(g)+2HO(g)ΔH=-116kJ·mol-1
2 2 2
研究发现CuCl(s)催化反应的过程如下:
2
1
反应i:CuCl(s)=CuCl(s)+2 Cl(g)ΔH=+83kJ·mol-1
2 2 1
1 1
反应ii:CuCl(s)+2 O(g)=CuO(s)+2 Cl(g)ΔH=-20kJ·mol-1
2 2 2
反应iii:……
下列表述不正确的是
A.反应i中反应物的总能量小于生成物的总能量
B.反应ii中,1molCuCl(s)反应时转移2mole-
C.推断反应iii应为CuO(s)+2HCl(g)=CuCl(s)+HO(g)ΔH=-242kJ·mol-1
2 2 3
D.由反应过程可知催化剂参与反应,通过改变反应路径提高反应速率
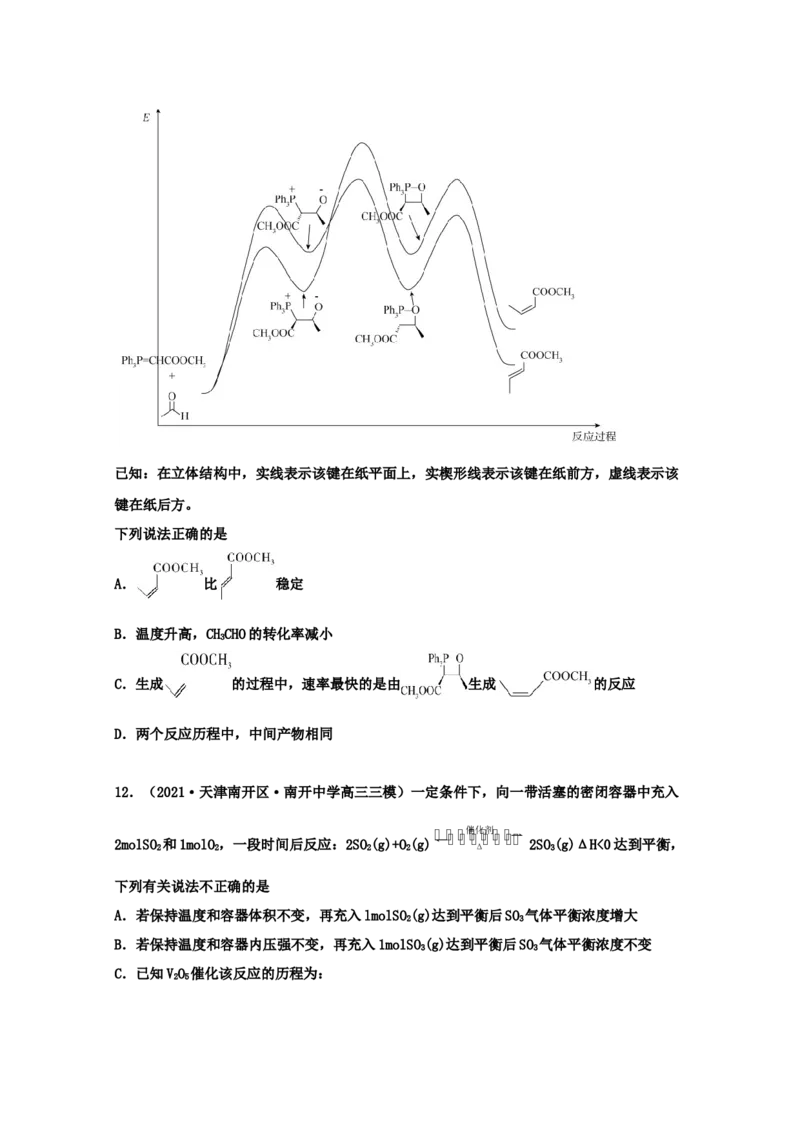
11.(2021·河南新乡市·新乡县一中高三其他模拟)CH-CH=CH-COOCH 有两种立体异构体
3 3
和 ,由CHCHO和PhP=CHCOOCH 反应制取这两种异构体的历程中能量变
3 3 3
化如图已知:在立体结构中,实线表示该键在纸平面上,实楔形线表示该键在纸前方,虚线表示该
键在纸后方。
下列说法正确的是
A. 比 稳定
B.温度升高,CHCHO的转化率减小
3
C.生成 的过程中,速率最快的是由 生成 的反应
D.两个反应历程中,中间产物相同
12.(2021·天津南开区·南开中学高三三模)一定条件下,向一带活塞的密闭容器中充入
2molSO 和1molO,一段时间后反应:2SO(g)+O(g) 催 化 剂 2SO(g)ΔH<0达到平衡,
2 2 2 2 Δ 3
下列有关说法不正确的是
A.若保持温度和容器体积不变,再充入lmolSO(g)达到平衡后SO 气体平衡浓度增大
2 3
B.若保持温度和容器内压强不变,再充入1molSO(g)达到平衡后SO 气体平衡浓度不变
3 3
C.已知VO 催化该反应的历程为:
2 5,由此可知,过程①的快慢
对该反应的速率起着决定性的影响。
D.假设平衡时SO 的物质的量为1mol,则该反应的化学平衡常数K一定为2
3
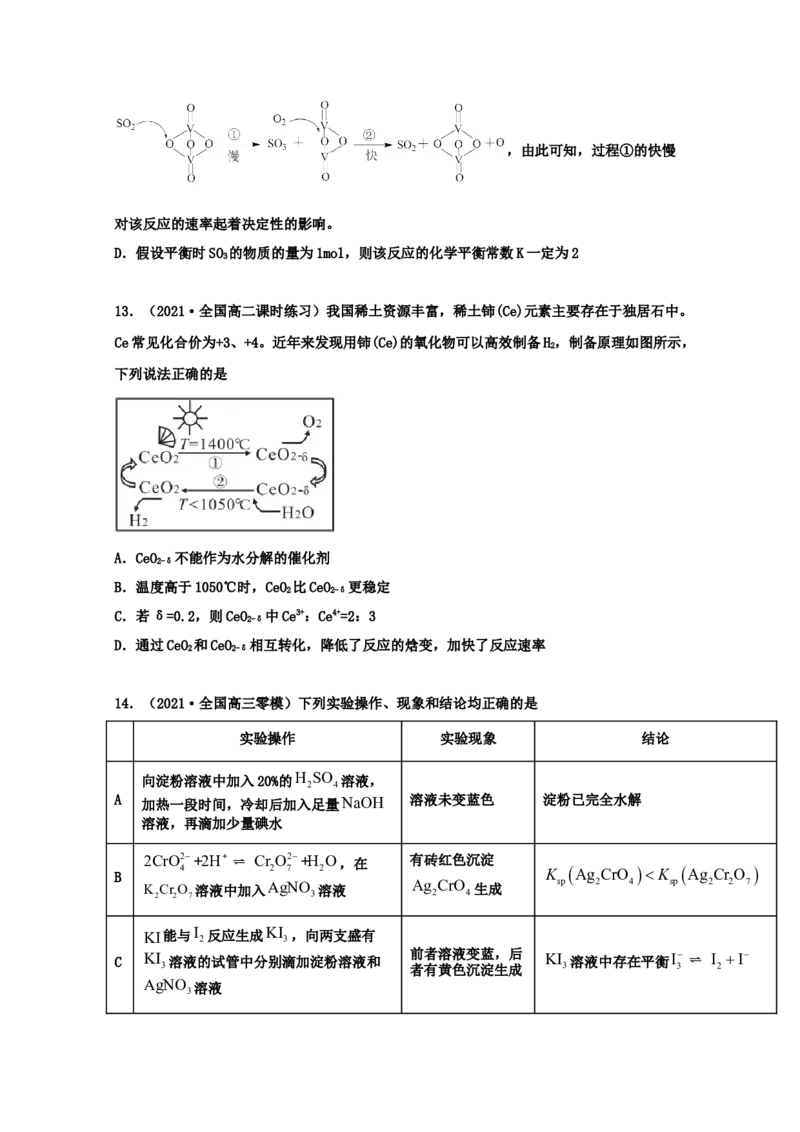
13.(2021·全国高二课时练习)我国稀土资源丰富,稀土铈(Ce)元素主要存在于独居石中。
Ce常见化合价为+3、+4。近年来发现用铈(Ce)的氧化物可以高效制备H,制备原理如图所示,
2
下列说法正确的是
A.CeO 不能作为水分解的催化剂
2-δ
B.温度高于1050℃时,CeO 比CeO 更稳定
2 2-δ
C.若δ=0.2,则CeO 中Ce3+:Ce4+=2:3
2-δ
D.通过CeO 和CeO 相互转化,降低了反应的焓变,加快了反应速率
2 2-δ
14.(2021·全国高三零模)下列实验操作、现象和结论均正确的是
实验操作 实验现象 结论
向淀粉溶液中加入20%的H SO 溶液,
2 4
A 加热一段时间,冷却后加入足量NaOH 溶液未变蓝色 淀粉已完全水解
溶液,再滴加少量碘水
2CrO2+2H+ Cr O2+H O,在 有砖红色沉淀
B 4 2 7 2 K Ag CrO K Ag Cr O
K CrO 溶液中加入AgNO 溶液 Ag CrO 生成 sp 2 4 sp 2 2 7
2 2 7 3 2 4
KI能与I
2
反应生成KI
3
,向两支盛有
C KI 溶液的试管中分别滴加淀粉溶液和 前者溶液变蓝,后 KI 溶液中存在平衡I I I
3 者有黄色沉淀生成 3 3 2
AgNO 溶液
3将Cu与浓硫酸反应后的混合液冷却,再
D 溶液变蓝 有Cu2生成
向其中加入蒸馏水
A.A B.B C.C D.D
15.(2021·九龙坡区·重庆市育才中学高三三模)CO 的回收与利用是科学家研究的热点课
2
题,可利用CH 与CO 制备“合成气”(CO、H),还可制备甲醇、二甲醚、碳基燃料等产品。
4 2 2
Ⅰ.制合成气
科学家提出制备“合成气”反应历程分两步:
噲垐 ��
第一步:CH(g) C(ads)+2H(g)(慢反应)
4 2
噲垐 ��
第二步:C(ads)+CO(g) 2CO(g)(快反应)
2
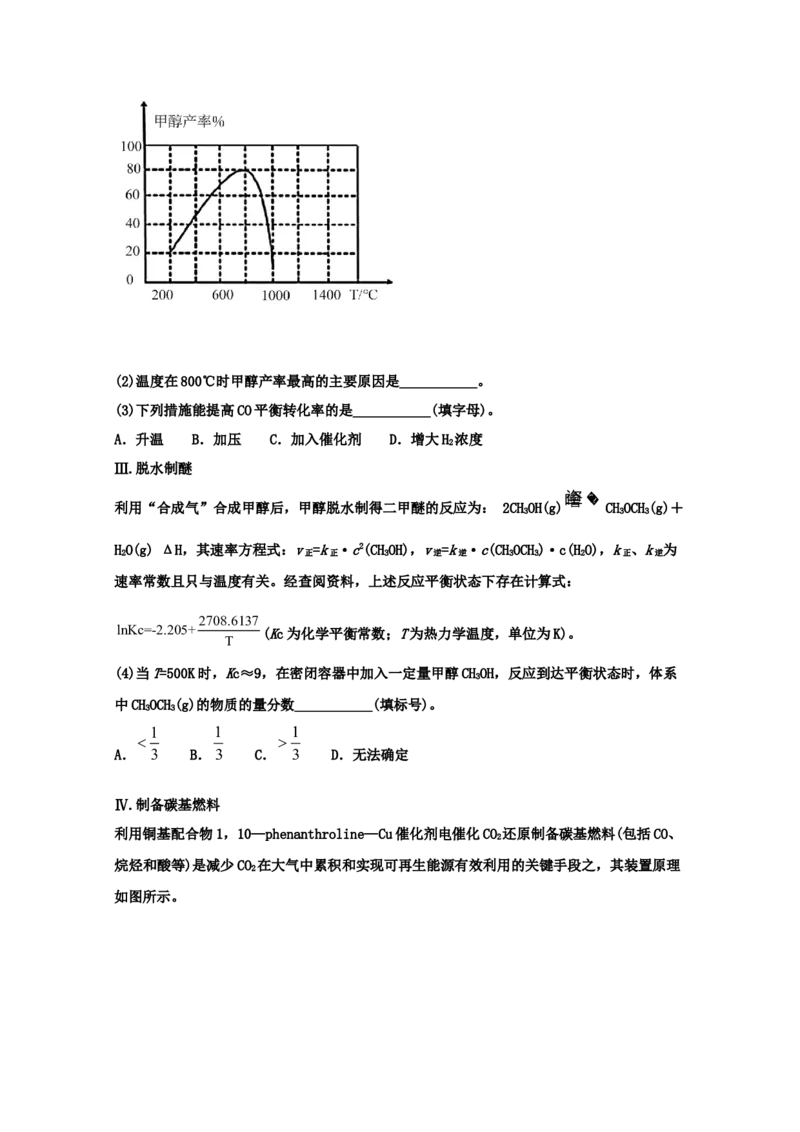
(1)决定制备“合成气”反应速率的是第___________步,上述反应中C(ads)为吸附性活性炭,
反应历程的能量变化如图:
CH 与CO 制备“合成气”的热化学方程式为___________。
4 2
Ⅱ.制备甲醇
噲垐 ��
“合成气”在催化剂作用下反应,可以直接合成甲醇:CO(g)+3H(g) CHOH(g)+
2 3
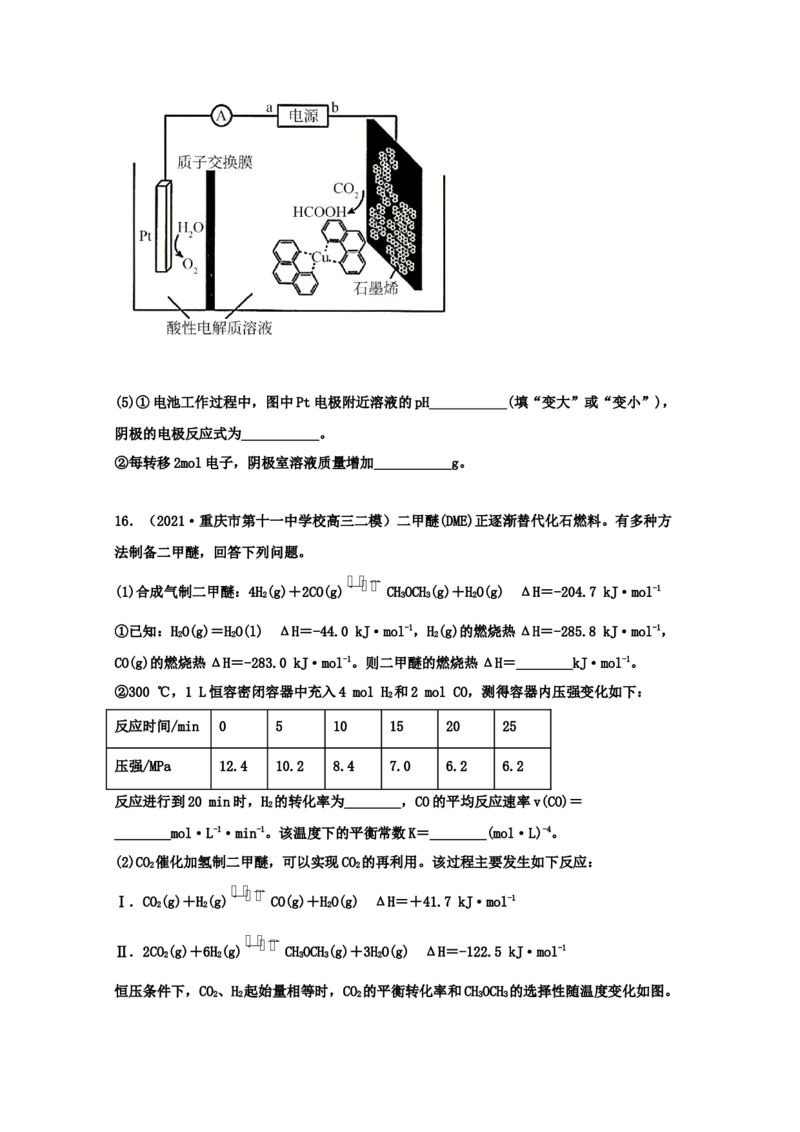
HO(g) △H<0,测得相同时间内甲醇产率与温度的关系如图所示。
2(2)温度在800℃时甲醇产率最高的主要原因是___________。
(3)下列措施能提高CO平衡转化率的是___________(填字母)。
A.升温 B.加压 C.加入催化剂 D.增大H 浓度
2
Ⅲ.脱水制醚
噲垐 ��
利用“合成气”合成甲醇后,甲醇脱水制得二甲醚的反应为: 2CHOH(g) CHOCH(g)+
3 3 3
HO(g) ΔH,其速率方程式:v =k ·c2(CHOH),v =k ·c(CHOCH)·c(HO),k 、k 为
2 正 正 3 逆 逆 3 3 2 正 逆
速率常数且只与温度有关。经查阅资料,上述反应平衡状态下存在计算式:
2708.6137
lnKc=-2.205+ (Kc为化学平衡常数;T为热力学温度,单位为K)。
T
(4)当T=500K时,Kc≈9,在密闭容器中加入一定量甲醇CHOH,反应到达平衡状态时,体系
3
中CHOCH(g)的物质的量分数___________(填标号)。
3 3
1 1 1
A. 3 B.3 C. 3 D.无法确定
Ⅳ.制备碳基燃料
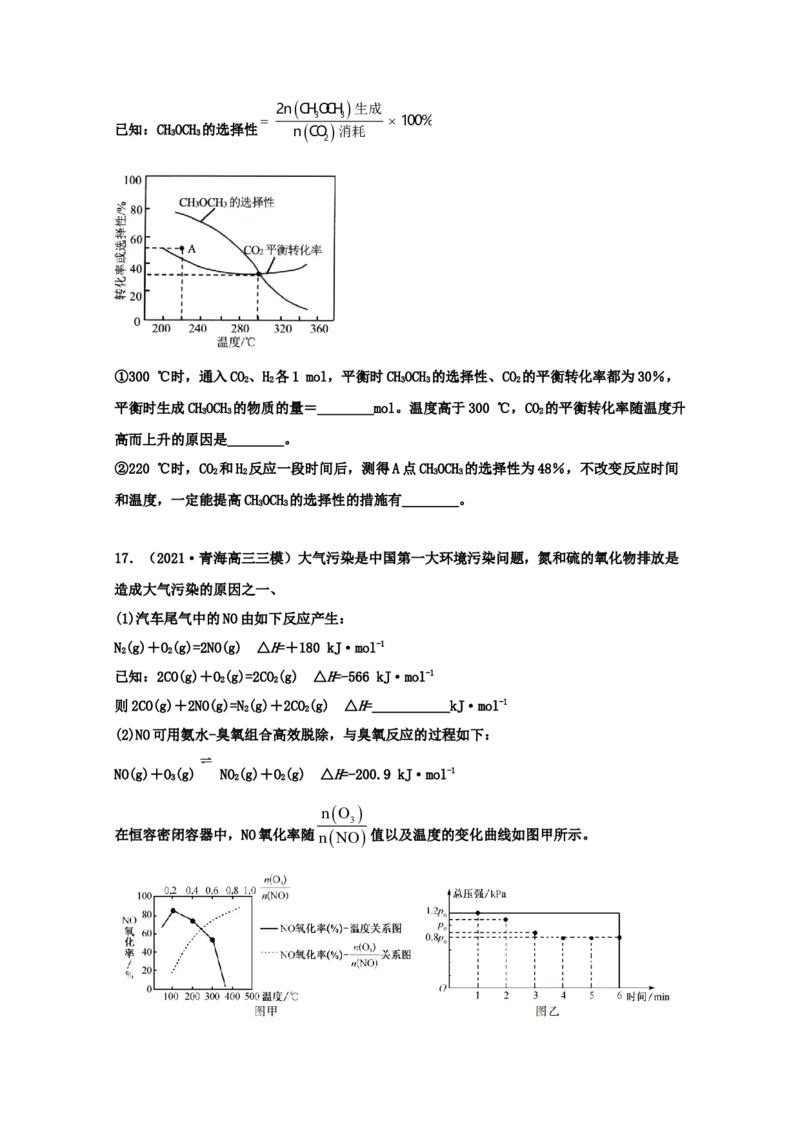
利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO 还原制备碳基燃料(包括CO、
2
烷烃和酸等)是减少CO 在大气中累积和实现可再生能源有效利用的关键手段之,其装置原理
2
如图所示。(5)①电池工作过程中,图中Pt电极附近溶液的pH___________(填“变大”或“变小”),
阴极的电极反应式为___________。
②每转移2mol电子,阴极室溶液质量增加___________g。
16.(2021·重庆市第十一中学校高三二模)二甲醚(DME)正逐渐替代化石燃料。有多种方
法制备二甲醚,回答下列问题。
(1)合成气制二甲醚:4H(g)+2CO(g)
CHOCH(g)+HO(g) ΔH=-204.7 kJ·mol-1
2 3 3 2
①已知:HO(g)=HO(l) ΔH=-44.0 kJ·mol-1,H(g)的燃烧热ΔH=-285.8 kJ·mol-1,
2 2 2
CO(g)的燃烧热ΔH=-283.0 kJ·mol-1。则二甲醚的燃烧热ΔH=________kJ·mol-1。
②300 ℃,1 L恒容密闭容器中充入4 mol H 和2 mol CO,测得容器内压强变化如下:
2
反应时间/min 0 5 10 15 20 25
压强/MPa 12.4 10.2 8.4 7.0 6.2 6.2
反应进行到20 min时,H 的转化率为________,CO的平均反应速率v(CO)=
2
________mol·L-1·min-1。该温度下的平衡常数K=________(mol·L)-4。
(2)CO 催化加氢制二甲醚,可以实现CO 的再利用。该过程主要发生如下反应:
2 2
Ⅰ.CO(g)+H(g)
CO(g)+HO(g) ΔH=+41.7 kJ·mol-1
2 2 2
Ⅱ.2CO(g)+6H(g)
CHOCH(g)+3HO(g) ΔH=-122.5 kJ·mol-1
2 2 3 3 2
恒压条件下,CO、H 起始量相等时,CO 的平衡转化率和CHOCH 的选择性随温度变化如图。
2 2 2 3 32n
CHOCH
生成
3 3 100%
已知:CH 3 OCH 3 的选择性 n CO 消耗
2
①300 ℃时,通入CO、H 各1 mol,平衡时CHOCH 的选择性、CO 的平衡转化率都为30%,
2 2 3 3 2
平衡时生成CHOCH 的物质的量=________mol。温度高于300 ℃,CO 的平衡转化率随温度升
3 3 2
高而上升的原因是________。
②220 ℃时,CO 和H 反应一段时间后,测得A点CHOCH 的选择性为48%,不改变反应时间
2 2 3 3
和温度,一定能提高CHOCH 的选择性的措施有________。
3 3
17.(2021·青海高三三模)大气污染是中国第一大环境污染问题,氮和硫的氧化物排放是
造成大气污染的原因之一、
(1)汽车尾气中的NO由如下反应产生:
N(g)+O(g)=2NO(g) △H=+180 kJ·mol-1
2 2
已知:2CO(g)+O(g)=2CO(g) △H=-566 kJ·mol-1
2 2
则2CO(g)+2NO(g)=N(g)+2CO(g) △H=___________kJ·mol-1
2 2
(2)NO可用氨水-臭氧组合高效脱除,与臭氧反应的过程如下:
NO(g)+O(g) NO(g)+O(g) △H=-200.9 kJ·mol-1
3 2 2
nO
3
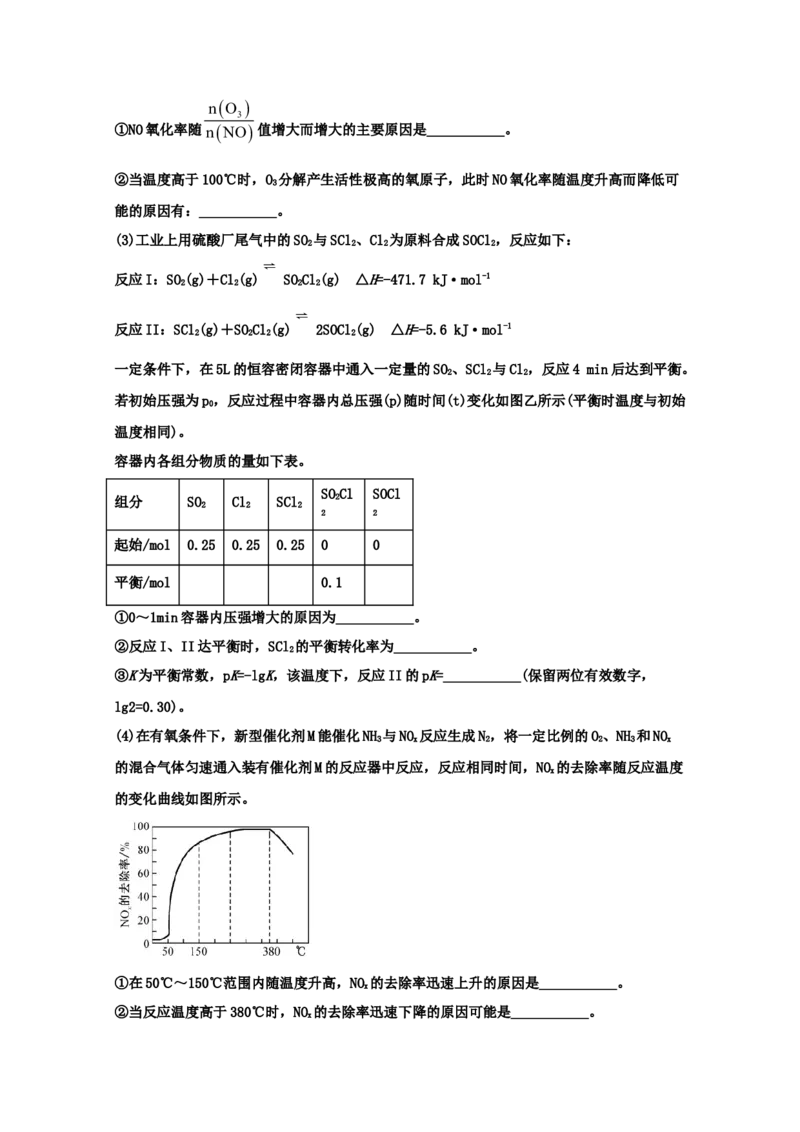
在恒容密闭容器中,NO氧化率随nNO 值以及温度的变化曲线如图甲所示。nO
3
①NO氧化率随nNO 值增大而增大的主要原因是___________。
②当温度高于100℃时,O 分解产生活性极高的氧原子,此时NO氧化率随温度升高而降低可
3
能的原因有:___________。
(3)工业上用硫酸厂尾气中的SO 与SCl、Cl 为原料合成SOCl,反应如下:
2 2 2 2
反应I:SO(g)+Cl(g) SOCl(g) △H=-471.7 kJ·mol-1
2 2 2 2
反应II:SCl(g)+SOCl(g) 2SOCl(g) △H=-5.6 kJ·mol-1
2 2 2 2
一定条件下,在5L的恒容密闭容器中通入一定量的SO、SCl 与Cl,反应4 min后达到平衡。
2 2 2
若初始压强为p,反应过程中容器内总压强(p)随时间(t)变化如图乙所示(平衡时温度与初始
0
温度相同)。
容器内各组分物质的量如下表。
SOCl SOCl
组分 SO Cl SCl 2
2 2 2
2 2
起始/mol 0.25 0.25 0.25 0 0
平衡/mol 0.1
①0~1min容器内压强增大的原因为___________。
②反应I、II达平衡时,SCl 的平衡转化率为___________。
2
③K为平衡常数,pK=-lgK,该温度下,反应II的pK=___________(保留两位有效数字,
lg2=0.30)。
(4)在有氧条件下,新型催化剂M能催化NH 与NO 反应生成N,将一定比例的O、NH 和NO
3 x 2 2 3 x
的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NO 的去除率随反应温度
x
的变化曲线如图所示。
①在50℃~150℃范围内随温度升高,NO 的去除率迅速上升的原因是___________。
x
②当反应温度高于380℃时,NO 的去除率迅速下降的原因可能是___________。
x18.(2021·全国高三零模)“一碳化学”是指研究分子中只含有一个碳原子的化合物为原
CO CO
料合成一系列化工产品的化学。研究和深度开发 、 2的应用对构建生态文明社会具有
重要的意义。
CO H
(1) 2和 2在催化剂作用下可发生以下两个反应:
Ⅰ. CO 2 g3H 2 g CH 3 OHgH 2 Og ΔH 48.5kJmol1
Ⅱ. 2CO 2 g5H 2 g C 2 H 2 g4H 2 Og ΔH 37.1kJmol1
反应 H 2 gC 2 H 2 g2H 2 Og 2CH 3 OHg 的ΔH ______。升高温度, C 2 H 2的
含量增大的原因是______。
CO H CO
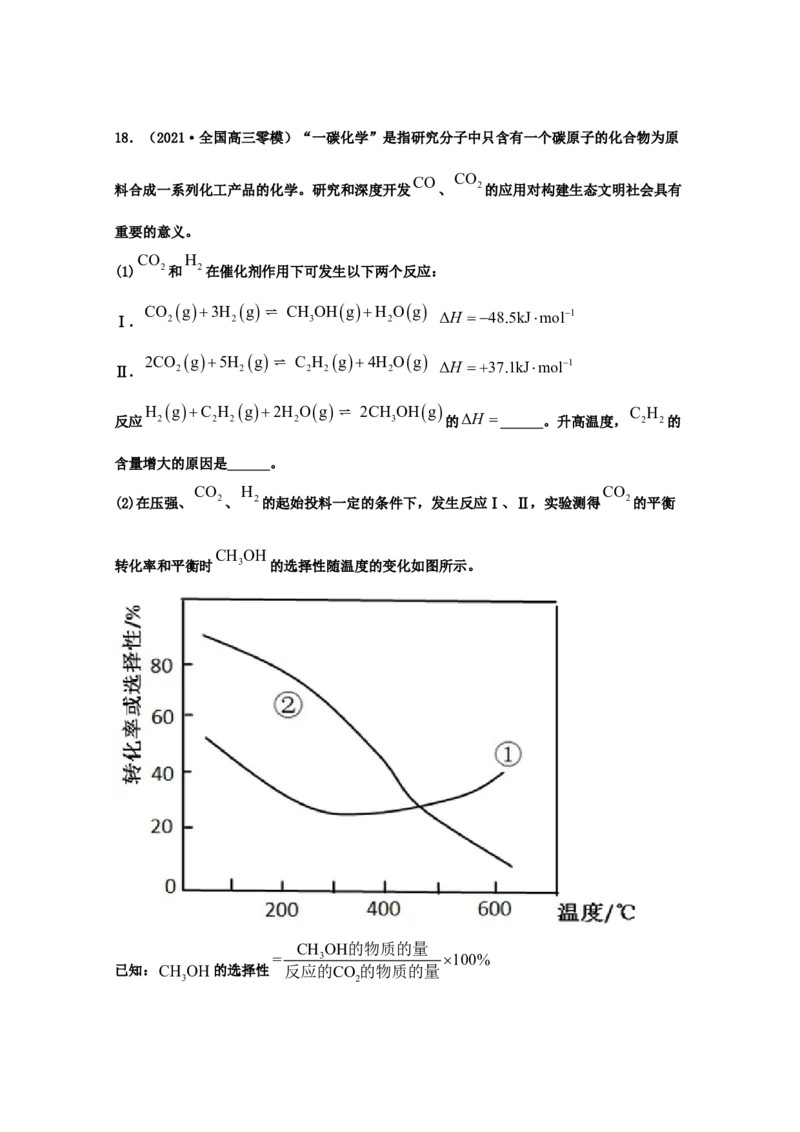
(2)在压强、 2、 2的起始投料一定的条件下,发生反应Ⅰ、Ⅱ,实验测得 2的平衡
CH OH
转化率和平衡时 3 的选择性随温度的变化如图所示。
CH OH的物质的量
= 3 100%
已知:CH OH的选择性 反应的CO 的物质的量
3 2CH OH
其中表示平衡时 3 的选择性的曲线是______(填“①”或“②”);温度高于280℃时,
CO CH OH
曲线①随温度升高而升高的原因是______;为同时提高 2的平衡转化率和平衡时 3
的选择性,应选择的反应条件为______(填标号)。
A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压
COgH Og CO gH g ΔH 41.1kJmol1
(3)对于反应 2 2 2 ,反应速率
vv v =k pCOpH O-k pCO pH k k
正 逆 正 2 逆 2 2 ,其中 正、 逆分别为正、逆反应
p
速率常数, 为气体的分压。
k -k
①降低温度, 正 逆______(填“增大”、“减小”或“不变”)。
k 4
正 =
②在 、 下,按照nCO:nH O=1:1投料,待达到平衡,k 9 ,用气体分
TK 101kPa 2 逆
K
压表示的平衡常数 p ______。
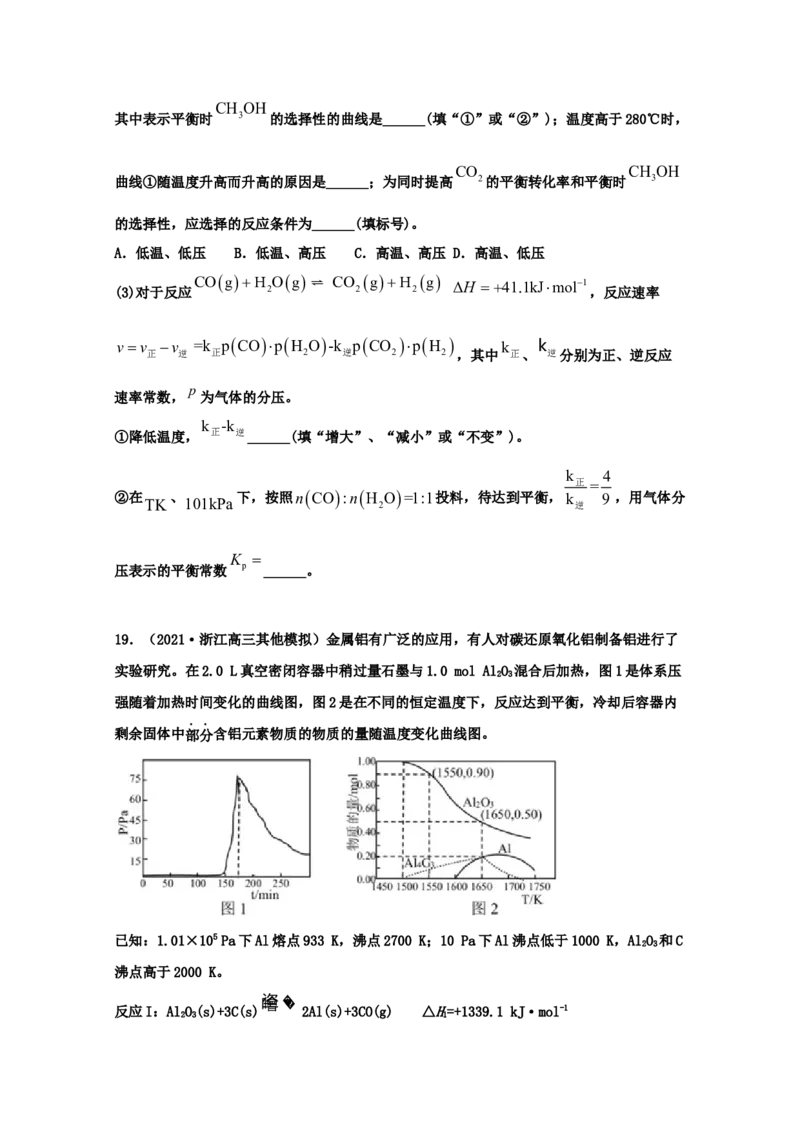
19.(2021·浙江高三其他模拟)金属铝有广泛的应用,有人对碳还原氧化铝制备铝进行了
实验研究。在2.0 L真空密闭容器中稍过量石墨与1.0 mol AlO 混合后加热,图1是体系压
2 3
强随着加热时间变化的曲线图,图2是在不同的恒定温度下,反应达到平衡,冷却后容器内
剩余固体中部分含铝元素物质的物质的量随温度变化曲线图。
已知:1.01×105 Pa下Al熔点933 K,沸点2700 K;10 Pa下Al沸点低于1000 K,AlO 和C
2 3
沸点高于2000 K。
噲垐 ��
反应I:AlO(s)+3C(s) 2Al(s)+3CO(g) △H=+1339.1 kJ·mol-1
2 3 1噲垐 ��
反应II:2AlO(s)+9C(s) AlC(s)+6CO(g) △H=+2249.5 kJ·mol-1
2 3 4 3 2
噲垐 ��
反应III:AlO(s)+AlC(s) 6Al(s)+3CO(g) △H
2 3 4 3 3
请回答下列问题:
(1)工业上电解法冶炼铝的化学方程式为___。
(2)△H=___。
3
(3)图1中石墨与AlO 混合物加热至150 min时容器内温度约为___。
2 3
(4)从反应自发性推测,实验室进行碳还原氧化铝制备铝的实验需要在真空容器中进行,可
能的原因是___。
(5)由图2可得1650 K时,反应I的平衡常数K=___。
(6)下列说法不正确的是___。
A.图1中约170 min后体系压强很快减小可能是反应I、II急剧发生,吸收了大量的热,容
器内温度降低,导致反应I、II平衡向逆方向移动
B.图2显示约1650~1700 K之间是石墨与AlO 反应制备Al的最佳温度
2 3
C.图2中T≥1700K时体系中一定还发生了其他副反应
D.综合分析可得,碳还原氧化铝制备铝比电解法成本更低,产率更高,适合大规模应用
(7)请在图3中画出温度在1450-1650 K之间2.0 L真空密闭容器中CO的浓度随温度变化曲
线图___。
20.(2021·四川树德中学高三其他模拟)甲醇不仅是重要的化工原料,还是性能优良的能
源和车用燃料。
(1)H(g)和CHOH(l)的燃烧热分别为285.8 kJ·mol-1和。726.5kJ·mo1-1,则由CO(g)和
2 3 2
H(g)生成液态甲醇和液态水的热化学方程式为___________。
2
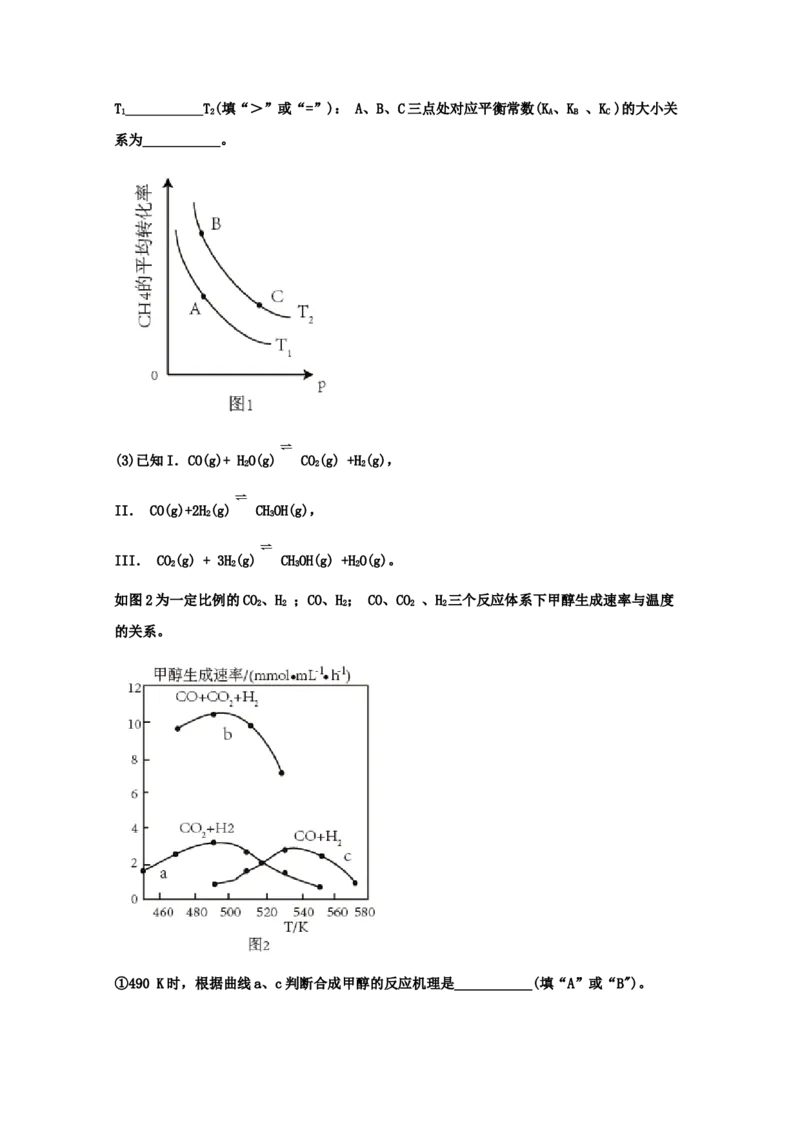
(2)CO与H 也可以合成CHOH,已知CO和H 可以利用如下反应制备:CH(g)+HO(g) CO(g)
2 3 2 4 2
+3H(g) ∆H>0, 定条件下CH 的平衡转化率与温度、压强的关系如图1所示。
2 4T___________T(填“>”或“=”): A、B、C三点处对应平衡常数(K、K 、K )的大小关
1 2 A B C
系为___________。
(3)已知I.CO(g)+ HO(g) CO(g) +H(g),
2 2 2
II. CO(g)+2H(g) CHOH(g),
2 3
III. CO(g) + 3H(g) CHOH(g) +HO(g)。
2 2 3 2
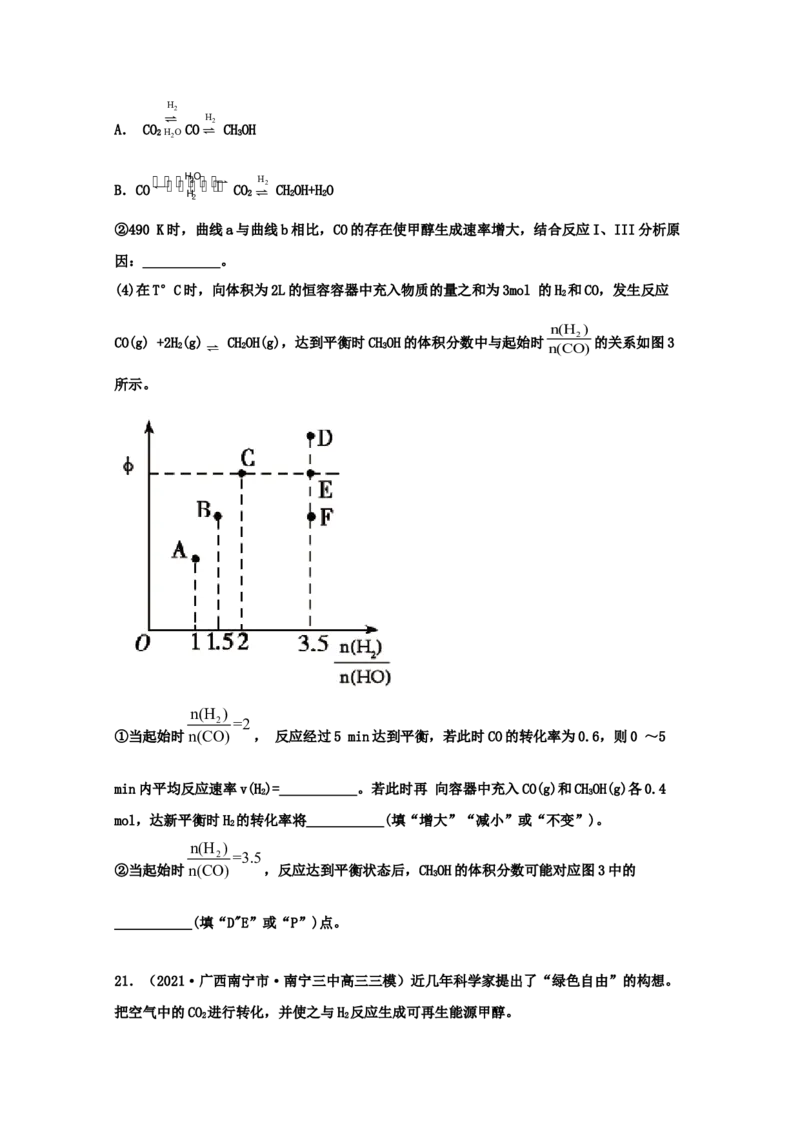
如图2为一定比例的CO、H ;CO、H; CO、CO 、H 三个反应体系下甲醇生成速率与温度
2 2 2 2 2
的关系。
①490 K时,根据曲线a、c判断合成甲醇的反应机理是___________(填“A”或“B")。H
2
H 2
A. CO CO CHOH
2H O 3
2
B.CO H2 O CO H 2 CHOH+HO
H 2 2 2
2
②490 K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原
因:___________。
(4)在T°C时,向体积为2L的恒容容器中充入物质的量之和为3mol 的H 和CO,发生反应
2
n(H )
2
CO(g) +2H(g) CHOH(g),达到平衡时CHOH的体积分数中与起始时 的关系如图3
2 2 3 n(CO)
所示。
n(H )
2 =2
①当起始时n(CO) , 反应经过5 min达到平衡,若此时CO的转化率为0.6,则0 ~5
min内平均反应速率v(H)=___________。若此时再 向容器中充入CO(g)和CHOH(g)各0.4
2 3
mol,达新平衡时H 的转化率将___________(填“增大”“减小”或“不变”)。
2
n(H )
2 =3.5
②当起始时n(CO) ,反应达到平衡状态后,CHOH的体积分数可能对应图3中的
3
___________(填“D"E”或“P”)点。
21.(2021·广西南宁市·南宁三中高三三模)近几年科学家提出了“绿色自由”的构想。
把空气中的CO 进行转化,并使之与H 反应生成可再生能源甲醇。
2 2(1)已知4.4kg CO 与足量H 恰好完全反应,生成气态的水和气态的甲醇,可放出4947kJ的
2 2
热量,试写出该反应的热化学方程式___________。
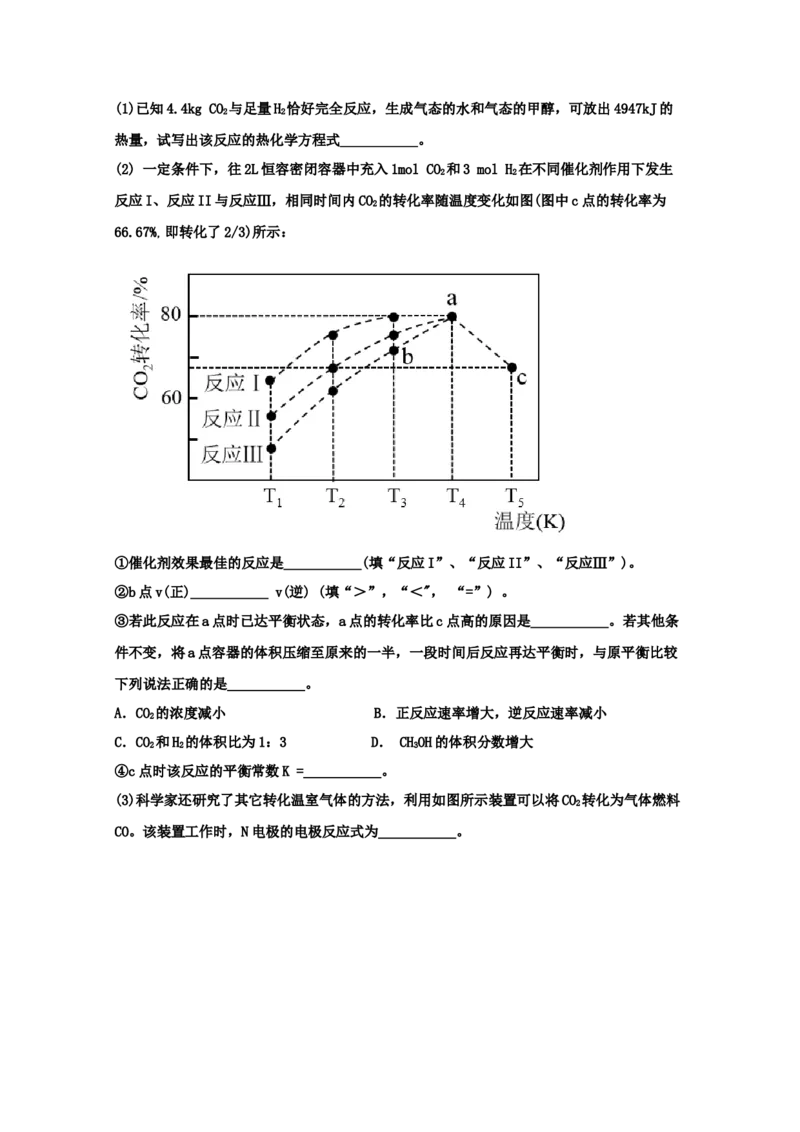
(2) 一定条件下,往2L恒容密闭容器中充入1mol CO 和3 mol H 在不同催化剂作用下发生
2 2
反应I、反应II与反应Ⅲ,相同时间内CO 的转化率随温度变化如图(图中c点的转化率为
2
66.67% 即转化了2/3)所示:
,
①催化剂效果最佳的反应是___________(填“反应I”、“反应II”、“反应Ⅲ”)。
②b点v(正)___________ v(逆) (填“>”,“<", “=”) 。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是___________。若其他条
件不变,将a点容器的体积压缩至原来的一半,一段时间后反应再达平衡时,与原平衡比较
下列说法正确的是___________。
A.CO 的浓度减小 B.正反应速率增大,逆反应速率减小
2
C.CO 和H 的体积比为1:3 D. CHOH的体积分数增大
2 2 3
④c点时该反应的平衡常数K =___________。
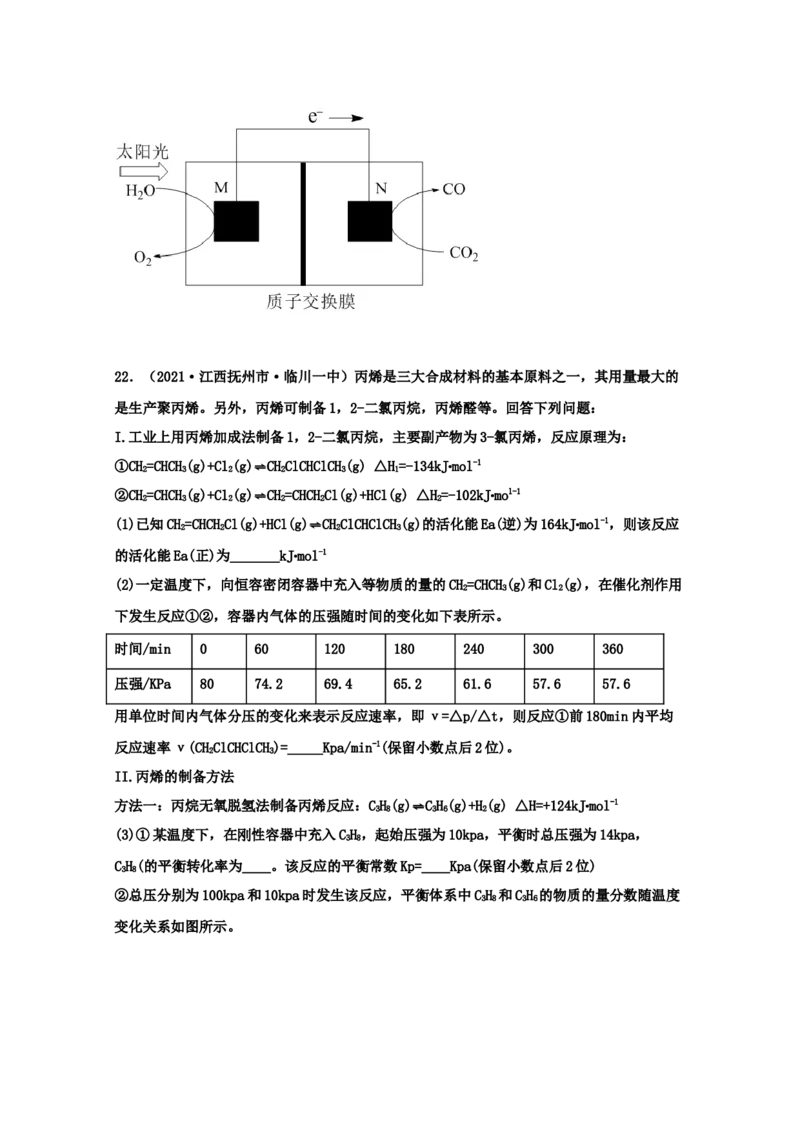
(3)科学家还研究了其它转化温室气体的方法,利用如图所示装置可以将CO 转化为气体燃料
2
CO。该装置工作时,N电极的电极反应式为___________。22.(2021·江西抚州市·临川一中)丙烯是三大合成材料的基本原料之一,其用量最大的
是生产聚丙烯。另外,丙烯可制备1,2-二氯丙烷,丙烯醛等。回答下列问题:
I.工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
①CH
2
=CHCH
3
(g)+Cl
2
(g)
CH
2
ClCHClCH
3
(g) △H
1
=-134kJ∙mol-1
②CH
2
=CHCH
3
(g)+Cl
2
(g)
CH
2
=CHCH
2
Cl(g)+HCl(g) △H
2
=-102kJ∙mol-1
(1)已知CH
2
=CHCH
2
Cl(g)+HCl(g)
CH
2
ClCHClCH
3
(g)的活化能Ea(逆)为164kJ∙mol-1,则该反应
的活化能Ea(正)为_______kJ∙mol-1
(2)一定温度下,向恒容密闭容器中充入等物质的量的CH=CHCH(g)和Cl(g),在催化剂作用
2 3 2
下发生反应①②,容器内气体的压强随时间的变化如下表所示。
时间/min 0 60 120 180 240 300 360
压强/KPa 80 74.2 69.4 65.2 61.6 57.6 57.6
用单位时间内气体分压的变化来表示反应速率,即ν=△p/△t,则反应①前180min内平均
反应速率ν(CHClCHClCH)=_____Kpa/min-1(保留小数点后2位)。
2 3
II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应:C
3
H
8
(g)
C
3
H
6
(g)+H
2
(g) △H=+124kJ∙mol-1
(3)①某温度下,在刚性容器中充入CH,起始压强为10kpa,平衡时总压强为14kpa,
3 8
CH(的平衡转化率为____。该反应的平衡常数Kp=____Kpa(保留小数点后2位)
3 8
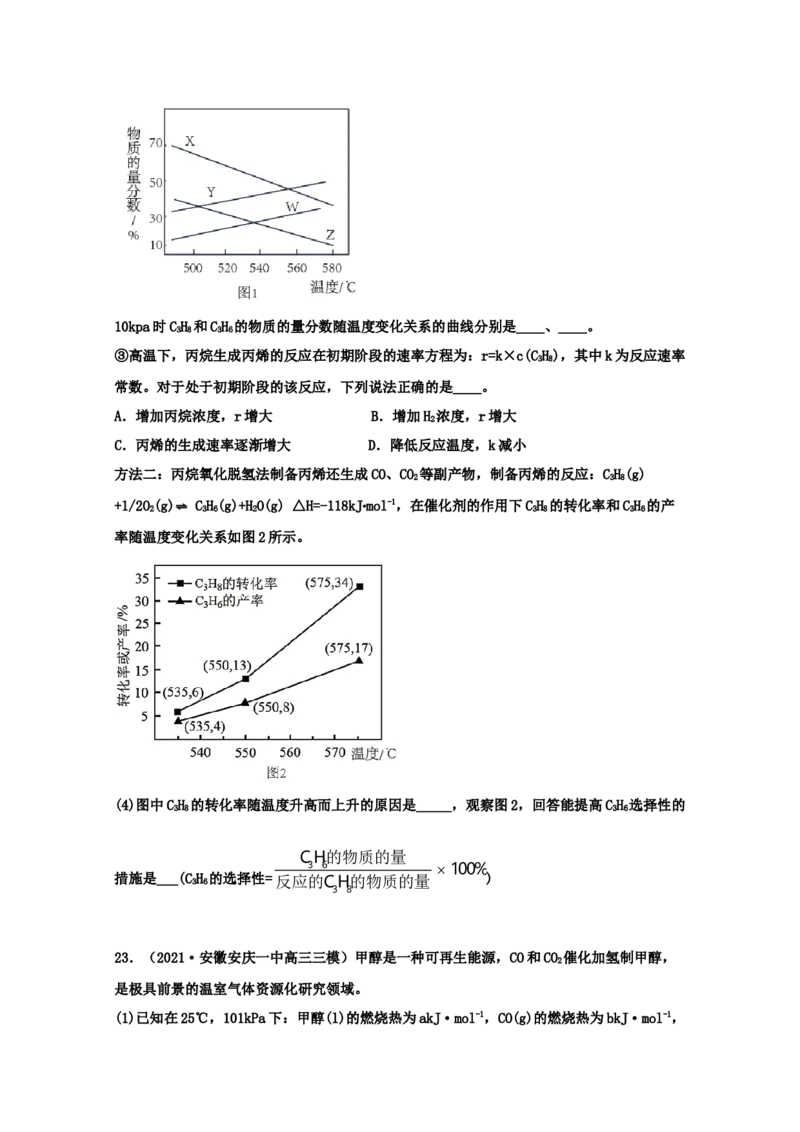
②总压分别为100kpa和10kpa时发生该反应,平衡体系中CH 和CH 的物质的量分数随温度
3 8 3 6
变化关系如图所示。10kpa时CH 和CH 的物质的量分数随温度变化关系的曲线分别是____、____。
3 8 3 6
③高温下,丙烷生成丙烯的反应在初期阶段的速率方程为:r=k×c(CH),其中k为反应速率
3 8
常数。对于处于初期阶段的该反应,下列说法正确的是____。
A.增加丙烷浓度,r增大 B.增加H 浓度,r增大
2
C.丙烯的生成速率逐渐增大 D.降低反应温度,k减小
方法二:丙烷氧化脱氢法制备丙烯还生成CO、CO 等副产物,制备丙烯的反应:CH(g)
2 3 8
+1/2O
2
(g)
C
3
H
6
(g)+H
2
O(g) △H=-118kJ∙mol-1,在催化剂的作用下C
3
H
8
的转化率和C
3
H
6
的产
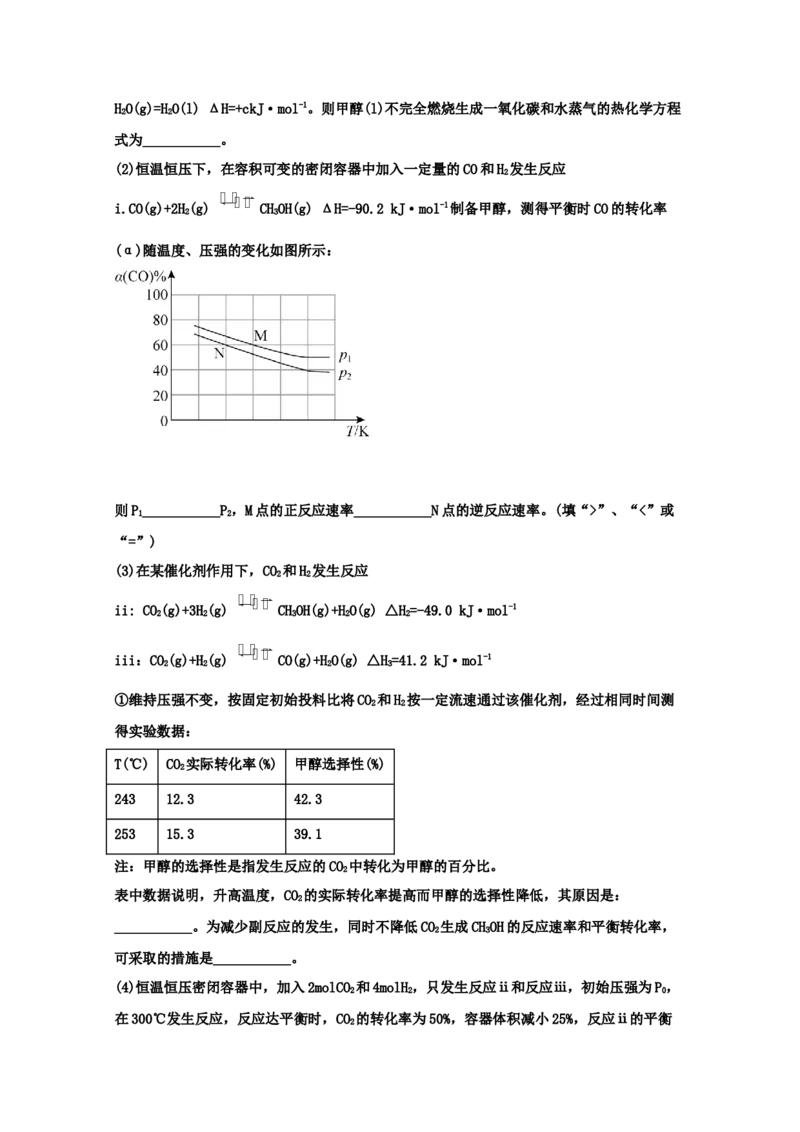
率随温度变化关系如图2所示。
(4)图中CH 的转化率随温度升高而上升的原因是_____,观察图2,回答能提高CH 选择性的
3 8 3 6
CH的物质的量
3 6 100%
措施是___(C
3
H
6
的选择性=反应的CH的物质的量 )
3 8
23.(2021·安徽安庆一中高三三模)甲醇是一种可再生能源,CO和CO 催化加氢制甲醇,
2
是极具前景的温室气体资源化研究领域。
(1)已知在25℃,101kPa下:甲醇(l)的燃烧热为akJ·mol-1,CO(g)的燃烧热为bkJ·mol-1,HO(g)=HO(l) ΔH=+ckJ·mol-1。则甲醇(l)不完全燃烧生成一氧化碳和水蒸气的热化学方程
2 2
式为___________。
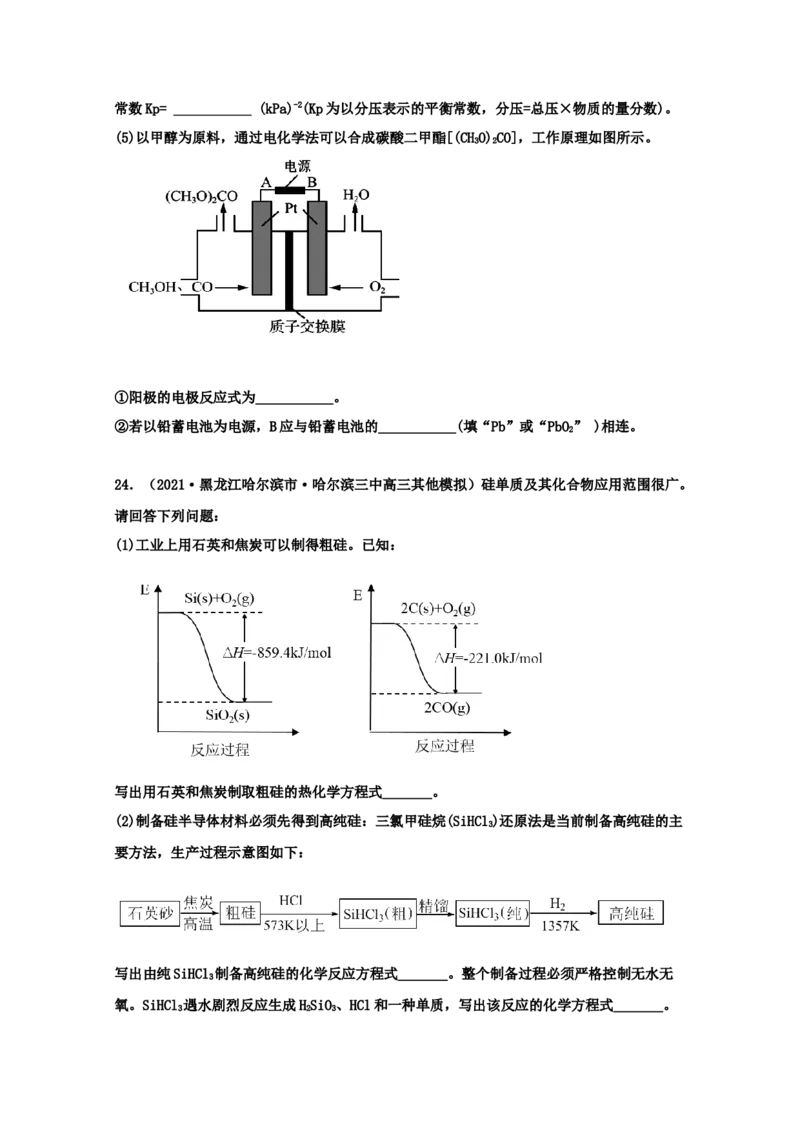
(2)恒温恒压下,在容积可变的密闭容器中加入一定量的CO和H 发生反应
2
i.CO(g)+2H(g)
CHOH(g) ΔH=-90.2 kJ·mol-1制备甲醇,测得平衡时CO的转化率
2 3
(α)随温度、压强的变化如图所示:
则P___________P,M点的正反应速率___________N点的逆反应速率。(填“>”、“<”或
1 2
“=”)
(3)在某催化剂作用下,CO 和H 发生反应
2 2
ii: CO(g)+3H(g)
CHOH(g)+HO(g) △H=-49.0 kJ·mol-1
2 2 3 2 2
iii:CO(g)+H(g)
CO(g)+HO(g) △H=41.2 kJ·mol-1
2 2 2 3
①维持压强不变,按固定初始投料比将CO 和H 按一定流速通过该催化剂,经过相同时间测
2 2
得实验数据:
T(℃) CO 实际转化率(%) 甲醇选择性(%)
2
243 12.3 42.3
253 15.3 39.1
注:甲醇的选择性是指发生反应的CO 中转化为甲醇的百分比。
2
表中数据说明,升高温度,CO 的实际转化率提高而甲醇的选择性降低,其原因是:
2
___________。为减少副反应的发生,同时不降低CO 生成CHOH的反应速率和平衡转化率,
2 3
可采取的措施是___________。
(4)恒温恒压密闭容器中,加入2molCO 和4molH,只发生反应ⅱ和反应ⅲ,初始压强为P,
2 2 0
在300℃发生反应,反应达平衡时,CO 的转化率为50%,容器体积减小25%,反应ⅱ的平衡
2常数Kp= ___________ (kPa)-2(Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(5)以甲醇为原料,通过电化学法可以合成碳酸二甲酯[(CHO)CO],工作原理如图所示。
3 2
①阳极的电极反应式为___________。
②若以铅蓄电池为电源,B应与铅蓄电池的___________(填“Pb”或“PbO” )相连。
2
24.(2021·黑龙江哈尔滨市·哈尔滨三中高三其他模拟)硅单质及其化合物应用范围很广。
请回答下列问题:
(1)工业上用石英和焦炭可以制得粗硅。已知:
写出用石英和焦炭制取粗硅的热化学方程式_______。
(2)制备硅半导体材料必须先得到高纯硅:三氯甲硅烷(SiHCl)还原法是当前制备高纯硅的主
3
要方法,生产过程示意图如下:
写出由纯SiHCl 制备高纯硅的化学反应方程式_______。整个制备过程必须严格控制无水无
3
氧。SiHCl 遇水剧烈反应生成HSiO、HCl和一种单质,写出该反应的化学方程式_______。
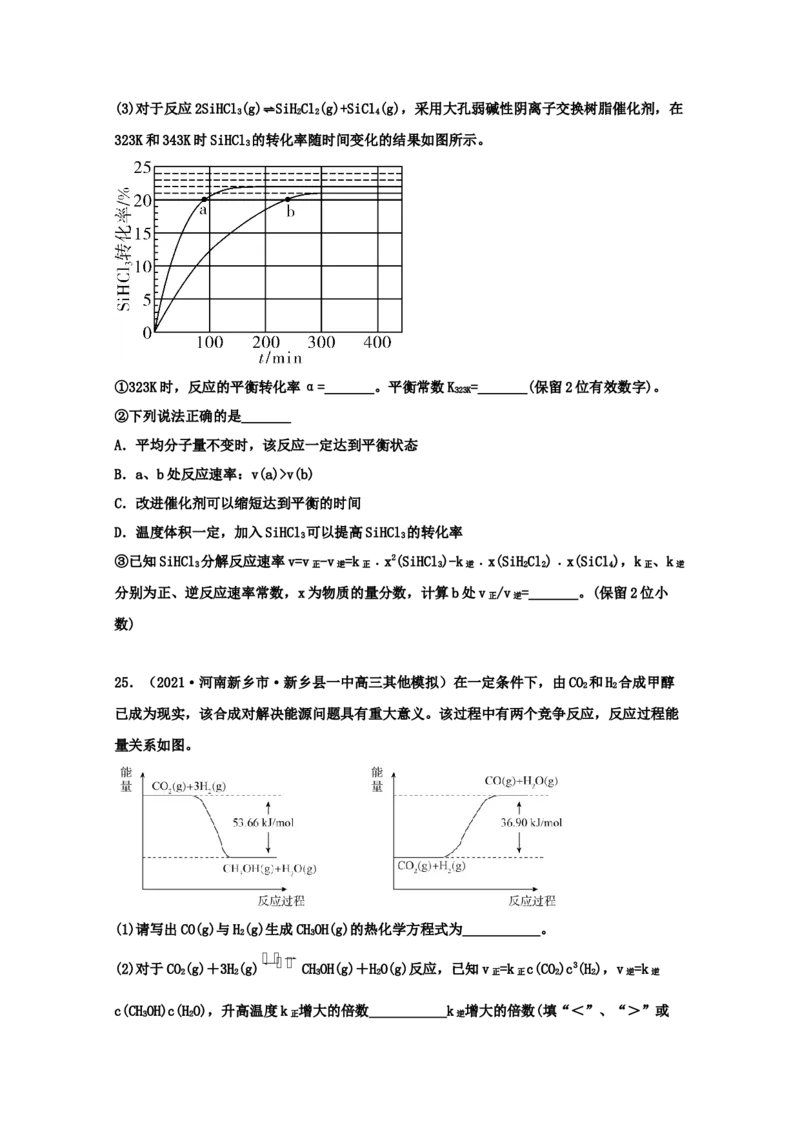
3 2 3(3)对于反应2SiHCl(g) SiHCl(g)+SiCl(g),采用大孔弱碱性阴离子交换树脂催化剂,在
3 2 2 4
323K和343K时SiHCl 的转化率随时间变化的结果如图所示。
3
①323K时,反应的平衡转化率α=_______。平衡常数K =_______(保留2位有效数字)。
323K
②下列说法正确的是_______
A.平均分子量不变时,该反应一定达到平衡状态
B.a、b处反应速率:v(a)>v(b)
C.改进催化剂可以缩短达到平衡的时间
D.温度体积一定,加入SiHCl 可以提高SiHCl 的转化率
3 3
③已知SiHCl 分解反应速率v=v -v =k ﹒x2(SiHCl)-k ﹒x(SiHCl)﹒x(SiCl),k 、k
3 正 逆 正 3 逆 2 2 4 正 逆
分别为正、逆反应速率常数,x为物质的量分数,计算b处v /v =_______。(保留2位小
正 逆
数)
25.(2021·河南新乡市·新乡县一中高三其他模拟)在一定条件下,由CO 和H 合成甲醇
2 2
已成为现实,该合成对解决能源问题具有重大意义。该过程中有两个竞争反应,反应过程能
量关系如图。
(1)请写出CO(g)与H(g)生成CHOH(g)的热化学方程式为___________。
2 3
(2)对于CO(g)+3H(g)
CHOH(g)+HO(g)反应,已知v =k c(CO)c3(H),v =k
2 2 3 2 正 正 2 2 逆 逆
c(CHOH)c(HO),升高温度k 增大的倍数___________k 增大的倍数(填“<”、“>”或
3 2 正 逆“=”),为了提高H 的转化率,可采取的措施有___________(填选项)。
2
A.加压B.升温C.加催化剂D.增加CO 的浓度
2
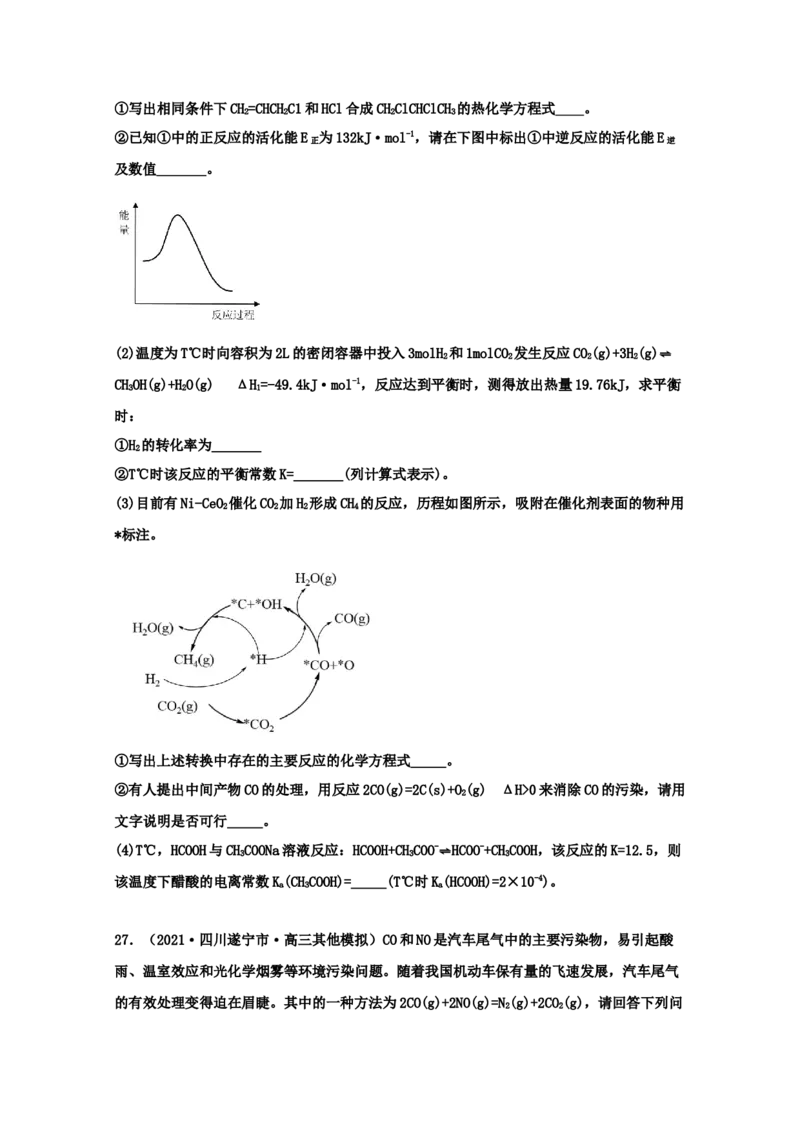
(3)在一容积可变的密闭容器中,充入1molCO 与3molH 发生反应:CO(g)+3H(g)
2 2 2 2
CHOH(g)+HO(g),CO 在不同温度下的平衡转化率与总压强的关系如下图所示,图中M点时
3 2 2
CHOH的物质的量分数为___________,该反应的压强平衡常数为K=___________atm-2(用平
3 p
衡分压代替平衡浓度计算,分压=总压×物质的量分数)
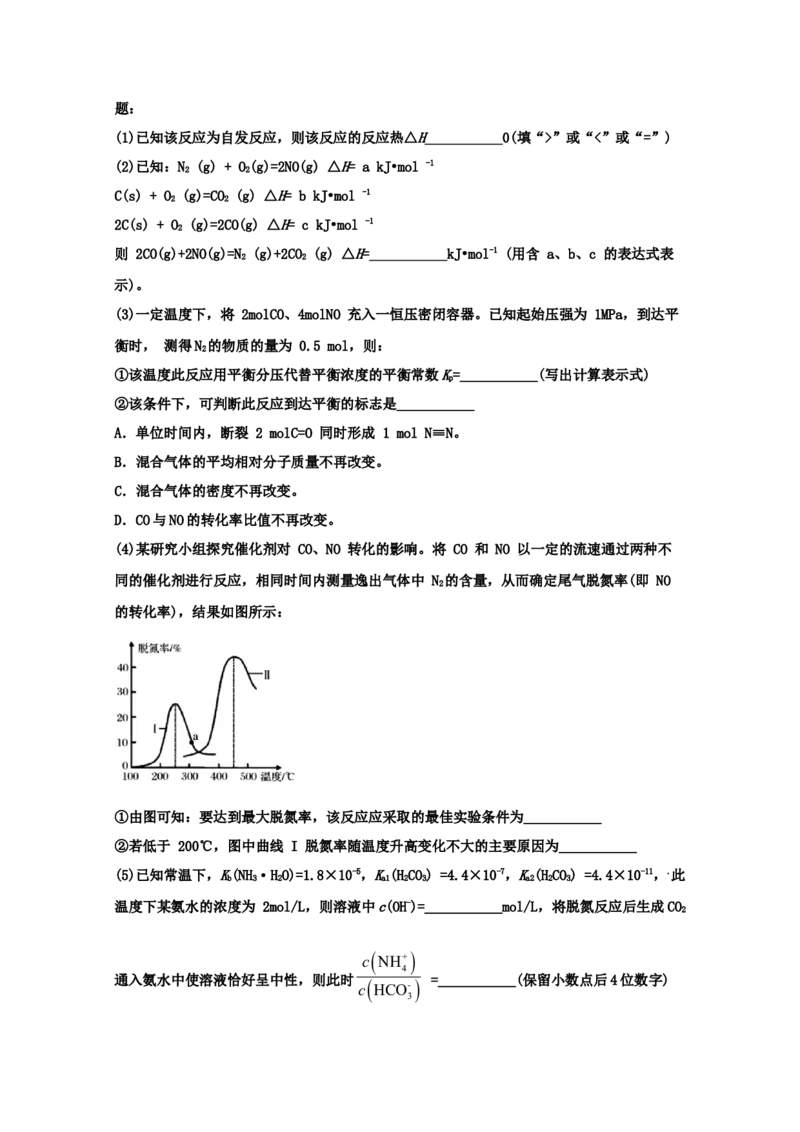
(4)由CO 和H 合成甲醇有两个竞争反应,为提高CHOH的选择性,在原料气中掺入一定量
2 2 3
CO,原因是___________。另外,可以通过控制双组份催化剂(CuO-ZnO)中CuO的含量,可提
高甲醇产率,根据下图判断,催化剂选择性最好的CuO的含量为___________。
26.(2021·天津高三一模)国务院总理李克强在2021年国务院政府工作报告中指出,扎实
做好碳达峰、碳中和各项工作,优化产业结构和能源结构,努力争取2060年前实现碳中和。
碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH=CHCH(g)+Cl(g)→CHClCHClCH(g) ΔH=-133kJ·mol-1
2 3 2 2 3
ii.CH=CHCH(g)+Cl(g)→CH=CHCHCl(g)+HCl(g) ΔH=-100kJ·mol-1
2 3 2 2 2①写出相同条件下CH=CHCHC1和HCl合成CHClCHClCH 的热化学方程式____。
2 2 2 3
②已知①中的正反应的活化能E 为132kJ·mol-1,请在下图中标出①中逆反应的活化能E
正 逆
及数值_______。
(2)温度为T℃时向容积为2L的密闭容器中投入3molH 和1molCO 发生反应CO(g)+3H(g)
2 2 2 2
CHOH(g)+HO(g) ΔH=-49.4kJ·mol-1,反应达到平衡时,测得放出热量19.76kJ,求平衡
3 2 1
时:
①H 的转化率为_______
2
②T℃时该反应的平衡常数K=_______(列计算式表示)。
(3)目前有Ni-CeO 催化CO 加H 形成CH 的反应,历程如图所示,吸附在催化剂表面的物种用
2 2 2 4
*标注。
①写出上述转换中存在的主要反应的化学方程式_____。
②有人提出中间产物CO的处理,用反应2CO(g)=2C(s)+O(g) ΔH>0来消除CO的污染,请用
2
文字说明是否可行_____。
(4)T℃,HCOOH与CHCOONa溶液反应:HCOOH+CHCOO- HCOO-+CHCOOH,该反应的K=12.5,则
3 3 3
该温度下醋酸的电离常数K(CHCOOH)=_____(T℃时K(HCOOH)=2×10-4)。
a 3 a
27.(2021·四川遂宁市·高三其他模拟)CO和NO是汽车尾气中的主要污染物,易引起酸
雨、温室效应和光化学烟雾等环境污染问题。随着我国机动车保有量的飞速发展,汽车尾气
的有效处理变得迫在眉睫。其中的一种方法为2CO(g)+2NO(g)=N(g)+2CO(g),请回答下列问
2 2题:
(1)已知该反应为自发反应,则该反应的反应热△H___________0(填“>”或“<”或“=”)
(2)已知:N (g) + O(g)=2NO(g) △H= a kJ•mol -1
2 2
C(s) + O (g)=CO (g) △H= b kJ•mol -1
2 2
2C(s) + O (g)=2CO(g) △H= c kJ•mol -1
2
则 2CO(g)+2NO(g)=N (g)+2CO (g) △H=___________kJ•mol-1 (用含 a、b、c 的表达式表
2 2
示)。
(3)一定温度下,将 2molCO、4molNO 充入一恒压密闭容器。已知起始压强为 1MPa,到达平
衡时, 测得N 的物质的量为 0.5 mol,则:
2
①该温度此反应用平衡分压代替平衡浓度的平衡常数K=___________(写出计算表示式)
p
②该条件下,可判断此反应到达平衡的标志是___________
A.单位时间内,断裂 2 molC=O 同时形成 1 mol N≡N。
B.混合气体的平均相对分子质量不再改变。
C.混合气体的密度不再改变。
D.CO与NO的转化率比值不再改变。
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不
同的催化剂进行反应,相同时间内测量逸出气体中 N 的含量,从而确定尾气脱氮率(即 NO
2
的转化率),结果如图所示:
①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为___________
②若低于 200℃,图中曲线 I 脱氮率随温度升高变化不大的主要原因为___________
(5)已知常温下,K(NH·HO)=1.8×10-5,K(HCO) =4.4×10-7,K(HCO) =4.4×10-11,.此
b 3 2 a1 2 3 a2 2 3
温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)=___________mol/L,将脱氮反应后生成CO
2
c
NH+
4
通入氨水中使溶液恰好呈中性,则此时 =___________(保留小数点后4位数字)
c
HCO-
3(6)电解NO制备NHNO,其工作原理如图所示,为使电解产物全部转化为NHNO,需要补充物
4 3 4 3
质A,A是___________,理由是___________
28.(2021·天津)氮和氮的化合物在国防建设、工农业生产和生活中都有极其广泛的用途。
请回答下列与氮元素有关的问题:
(1)已知部分化学键的键能如表
化学键 N≡N H —H N—H
键能/
946 436 391
(kJ·mol-1)
工业上合成氨反应当过程中转移3 mol电子时,理论上热量变化为 ___________kJ。
(2)在一个恒容密闭容器中充入2 mol NO(g)和1 mol Cl(g)发生反应:2NO(g)+Cl(g)
2 2
2ClNO(g) 在一定温度下测得NO的物质的量(单位:mol)与时间的关系如表所示:
t/min 0 5 8 13
NO的物质的量 2 1.15 1.0 1.0
217.5
①测得该反应平衡常数与温度关系为1gK=5.08+ T ,则该反应是___________(填“吸
p
热”或“放热”反应)。
②同温度下,起始时容器内的压强为P,则该反应的平衡常数K=___________(用平衡分压代
0 P
替平衡浓度计算,分压=总压×物质的量分数)。
③若同温度下,在相同容器中,充入1 mol NO(g)和0.5 molCl(g),则NO的平衡转化率
2
___________50%(填“大于”、“等于”或“小于”)。
(3)某研究小组将2 mol NH、3 mol NO和一定量的O 充入2 L密闭容器中,在AgO催化剂表
3 2 2面发生反应4NH(g)+6NO(g)
5N(g)+6HO(l);NO的转化率随温度变化的情况如图。5
3 2 2
min内,温度从420 K升高到580 K,此时段内NO的平均反应速率v(NO)___________,420 K
之前,NO生成N 的转化率偏低的原因可能是___________。
2
(4)若将NO 与O 通入如图所示甲装置,D电极上有红色物质析出,A电极的电极反应式为
2 2
___________。
29.(2021·安徽高三其他模拟)苯乙烯是重要的有机合成单体,常用乙苯为原料合成。
(1)以CO 和乙苯为原料合成的苯乙烯,其过程如图1,有“一步”途径1和“二步”途径2
2
的两种推测:则CO 2 (g)+ (g) 催 化 剂 (g)+CO(g)+H 2 O(g)的K 3 _______(用含K 1 、K 2 的代数式
表达)。
(2)向刚性容器中充入10 mol CO 2 和10 mol乙苯,发生反应CO 2 (g)+ (g) 催 化 剂
(g)+CO(g)+HO(g),在不同温度下测得平衡时各物质的体积分数如图2。可知
2
∆H_______0。相同温度下CO 转化率低于乙苯,推知发生了副反应CO(g)+HO(g) CO(g)
3 2 2 2
+H(g),由图像知该反应∆H_______0。
2
(3)某研究团队找到乙苯直接脱氢的高效催化剂,反应原理如图:
(g) H(g)+ (g) ∆H
催 化 剂 2 1
①已知部分化学键键能数据如表所示:
共价键 C-C C-H C=C H-H
键能(kJ/mol) 347.7 413.4 615 436
则∆H=_______。
1
②实际过程中,通常向乙苯中掺入水蒸气,保持体系总压为100 kPa的条件下进行。乙苯平
n(乙苯)
衡转化率与温度、投料比m[m= nHO ]的关系如图3。则投料比m
1
、m
2
、m
3
由大到小的关系
2
为_______。
③若m=5:1,则A点温度下,该反应的平衡常数K=_______。若其他条件不变,将恒压调整
2 p为恒容状态,则A点对应的乙苯的平衡转化率_______(填“增大”、“不变”或“减小”)。
(4)实验测得,乙苯脱氢的速率方程为 =k p , =k p p (k 、k 为速率常数,
正 正 乙苯 逆 逆 苯乙烯 氢气 正 逆
1 1
只与温度有关),图4中③代表lgk 随T 的变化关系,则能代表lgk 随T 的变化关系的是
逆 正
_______。
四、填空题
30.(2021·青海西宁市·高三二模)氮的化合物种类繁多,性质也各不相同。请回答下列
问题:
(1)已知:
①SO(g)+NO(g)=NO(g)+SO(g) ∆H =+41.8mol·L-1
3 2 2 1
②2SO(g)+O(g)=2SO(g) ∆H =-196.6mol·L-1
2 2 3 2
则2NO(g)=2NO(g)+O(g)的∆H=_______。
2 2
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO
进行吸附,并发生反应:C(s)+2NO(g)
N
2
(g)+CO
2
(g) ∆H<0.在恒压密闭容器中加入足量活
性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:图中a、b、c三点中,达到平衡的点是_______;温度为1100K时,N 的平衡体积分数为
2
_______。
(3)现代技术用氨气将汽车尾气中的NO 还原为N 和HO,反应原理是NO(g)+NO(g)+2NH(g)
x 2 2 2 3
催 化 剂 3HO(g)+2N(g) ∆H<0。
2 2
①实际生产中NO(g)+NO(g)+2NH(g) 催 化 剂 3HO(g)+2N(g)的反应温度不宜过高的原
2 3 2 2
因是_______。
②500℃时,在2L恒容密闭容器中充入1molNO、1molNO 和2molNH,8min时反应达到平衡,
2 3
此时NH 的转化率为40%,体系压强为pMPa,则0~8min内用N 表示的平均反应速率
3 0 2
v(N)=_______mol·L-1·min-1,500℃时该反应的平衡常数K=_______MPa(用含p 的代数式
2 p 0
表示,K 为以分压表示的平衡常数,分压=总压×物质的量分数)。
p