文档内容
专题 07 化学反应中的能量变化及反应机理
1.(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
能量/ kJmol-1 249 218 39 10 0 0 136 242
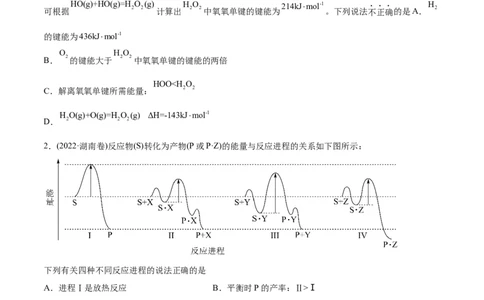
HO(g)+HO(g)=H O (g) H O 214kJmol-1 H
可根据 2 2 计算出 2 2中氧氧单键的键能为 。下列说法不正确的是A. 2
的键能为436kJmol-1
O H O
B. 2的键能大于 2 2中氧氧单键的键能的两倍
HOOⅠ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
1.(2022·重庆市育才中学模拟预测)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世嘱目的
成就。碳酰肼类化合物 是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知 ,则 为
A. B. C. D.
2.(2022·浙江·温州中学模拟预测)已知 固体溶于水放热,有关过程能量变化如图
下列说法正确的是
A.反应① , B.
C. D.
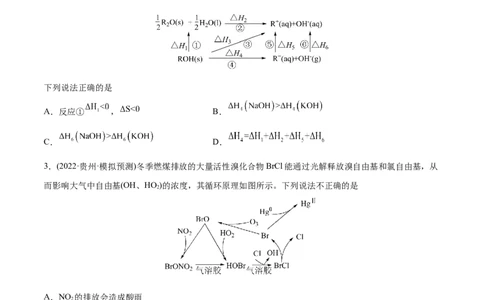
3.(2022·贵州·模拟预测)冬季燃煤排放的大量活性溴化合物BrCl能通过光解释放溴自由基和氯自由基,从
而影响大气中自由基(OH、HO )的浓度,其循环原理如图所示。下列说法不正确的是
2
A.NO 的排放会造成酸雨
2
B.向原煤中添加石灰石有利于实现“碳达峰、碳中和”
C.通过上述循环,大气中OH自由基的浓度升高
D.BrCl的排放会造成臭氧含量减小
4.(2022·安徽蚌埠·模拟预测)CO与NO在铁催化剂表面进行如下两步反应:
2
第一步:Fe*+N O=FeO*+N
2 2
第二步:FeO*+CO=Fe*+CO
2
其相对能量与反应历程如下图所示,下列说法不正确的是A.总反应是放热反应,化学方程式为CO+NO CO+N
2 2 2
B.在反应过程中,有极性键和非极性键的断裂和生成
C.总反应的反应速率由第一步反应决定
D.Fe*为反应的催化剂,FeO*为中间产物
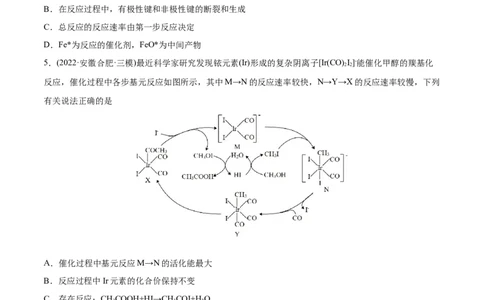
5.(2022·安徽合肥·三模)最近科学家研究发现铱元素(Ir)形成的复杂阴离子[Ir(CO) I]-能催化甲醇的羰基化
2 2
反应,催化过程中各步基元反应如图所示,其中M→N的反应速率较快,N→Y→X的反应速率较慢,下列
有关说法正确的是
A.催化过程中基元反应M→N的活化能最大
B.反应过程中Ir元素的化合价保持不变
C.存在反应:CHCOOH+HI→CH COI+HO
3 3 2
D.甲醇的羰基化反应原子利用率为100%
6.(2022·安徽师范大学附属中学模拟预测)如图分别代表溴甲烷和三级溴丁烷发生水解的反应历程。下列
说法不正确的是
I.CH Br+NaOH→CH OH+NaBr
3 3
II.(CH )CBr+NaOH→(CH )COH+NaBr
3 3 3 3A.反应I的 H<0
B.反应I有一△个过渡态,反应II有两个过渡态
C.反应I中C—Br键未断裂,反应II有C—Br键的断裂和C—O键的形成
D.增加NaOH的浓度,反应I速率增大,反应II速率不变
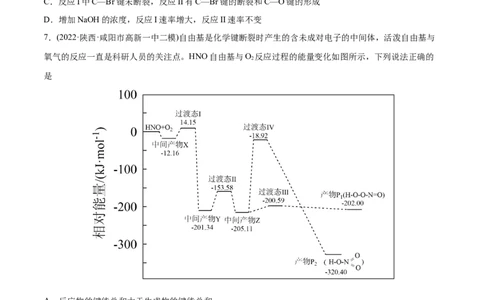
7.(2022·陕西·咸阳市高新一中二模)自由基是化学键断裂时产生的含未成对电子的中间体,活泼自由基与
氧气的反应一直是科研人员的关注点。HNO自由基与O 反应过程的能量变化如图所示,下列说法正确的
2
是
A.反应物的键能总和大于生成物的键能总和
B.产物P 与P 的分子式、氧元素的化合价均相同
1 2
C.该历程中最大正反应的活化能E =186.19 kJ
正
D.相同条件下,Z转化为产物的速率:v(P )>V(P )
1 2
8.(2022·陕西宝鸡·三模)我国科学家研究了不同含金化合物催化乙烯加氢[C H(g)+H(g)=C H(g)
2 4 2 2 6
H=akJ·mol-1]的反应历程如下图所示,下列说法正确的是
△A.1molC H(g)与1molH (g)具有的能量之和小于1molC H(g)的能量
2 4 2 2 6
B.过渡态物质的稳定性:过渡态1>过渡态2
C.该反应的焓变:ΔH=—129.6kJ·mol-1
D.相应的活化能:催化剂AuF<催化剂AuPF
9.(2022·安徽合肥·二模)某科研人员提出HCHO与O 在羟基磷灰石(HAP)表面催化氧化生成CO、HO的
2 2 2
历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列叙述错误的是( )
A.该历程中HCHO中所有的C-H键均断裂
B.该过程的总反应为HCHO+O CO+H O
2 2 2
C.该反应中反应物的总能量低于生成物的总能量
D.生成物CO 中的氧原子由HCHO和O 共同提供
2 2
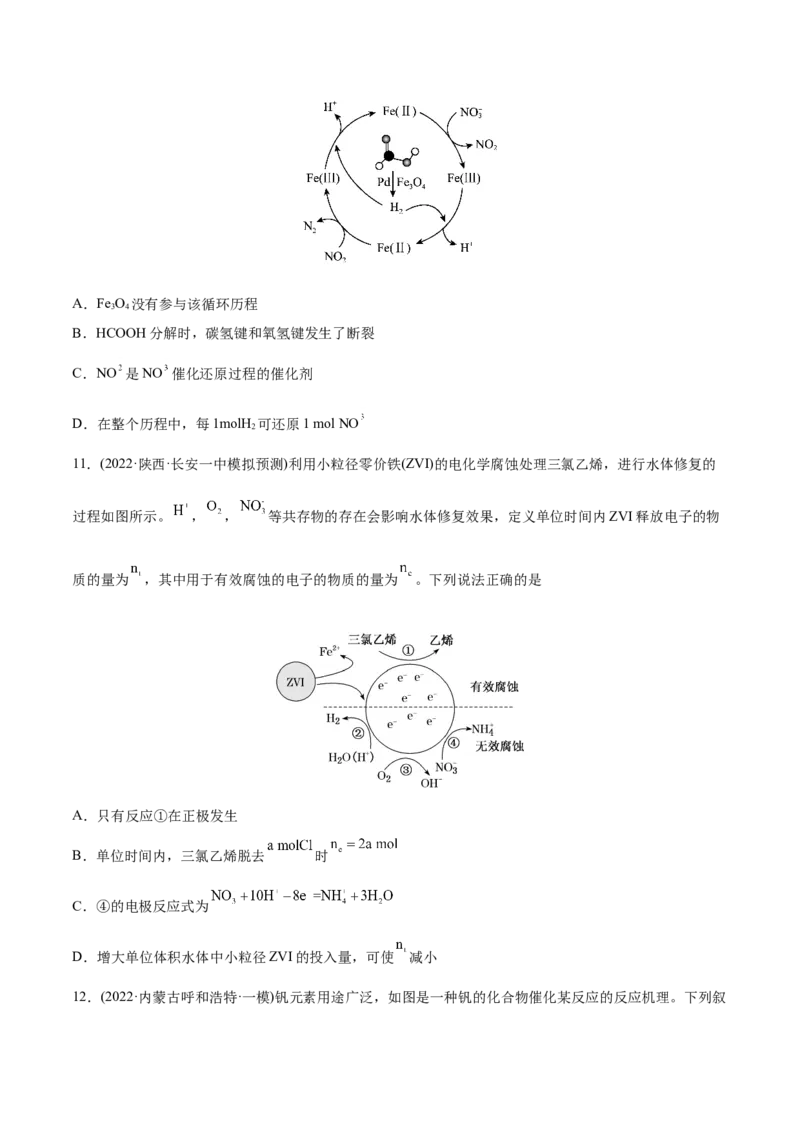
10.(2022·安徽蚌埠·模拟预测)硝酸盐污染已成为一个日益严重的环境问题,甲酸(HCOOH)在纳米级Pd表
面分解为活性H 和CO,再经下列历程实现NO 的催化还原,进而减少污染。已知Fe(II)、Fe(III)表示
2 2
Fe O 中二价铁和三价铁。下列说法正确的是
3 4A.Fe O 没有参与该循环历程
3 4
B.HCOOH分解时,碳氢键和氧氢键发生了断裂
C.NO 是NO 催化还原过程的催化剂
D.在整个历程中,每1molH 可还原1 mol NO
2
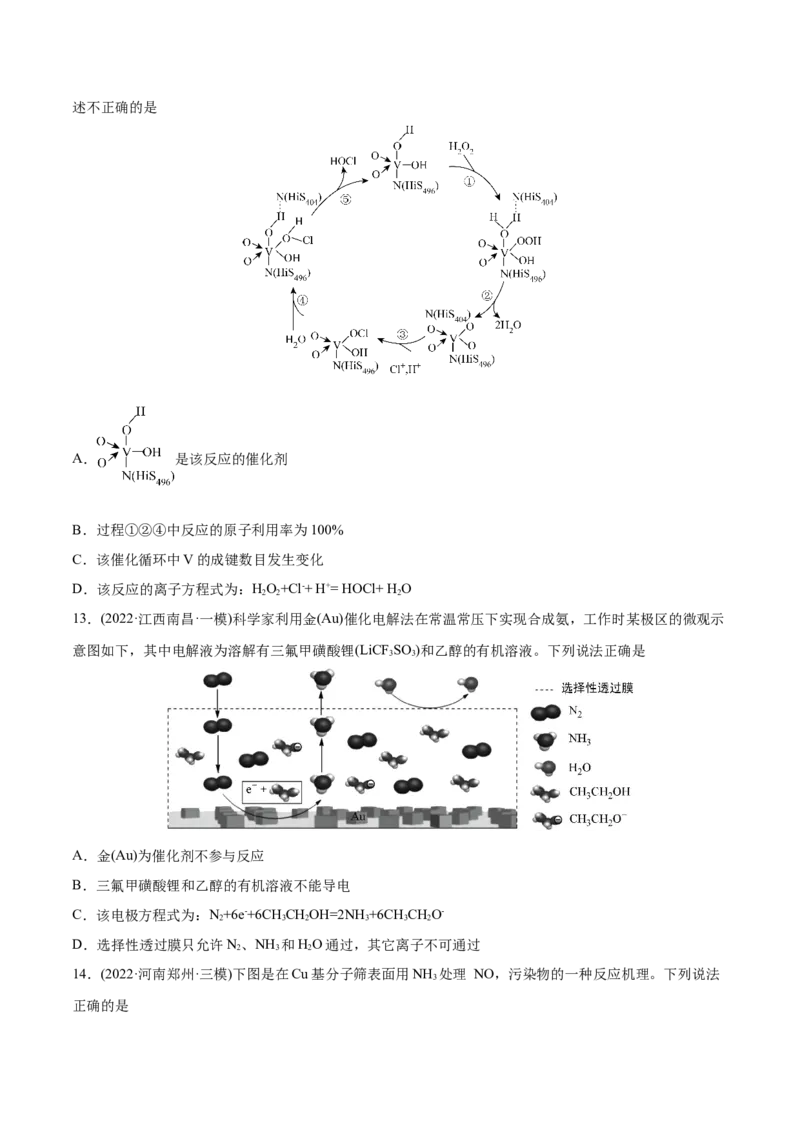
11.(2022·陕西·长安一中模拟预测)利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯,进行水体修复的
过程如图所示。 , , 等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物
质的量为 ,其中用于有效腐蚀的电子的物质的量为 。下列说法正确的是
A.只有反应①在正极发生
B.单位时间内,三氯乙烯脱去 时
C.④的电极反应式为
D.增大单位体积水体中小粒径ZVI的投入量,可使 减小
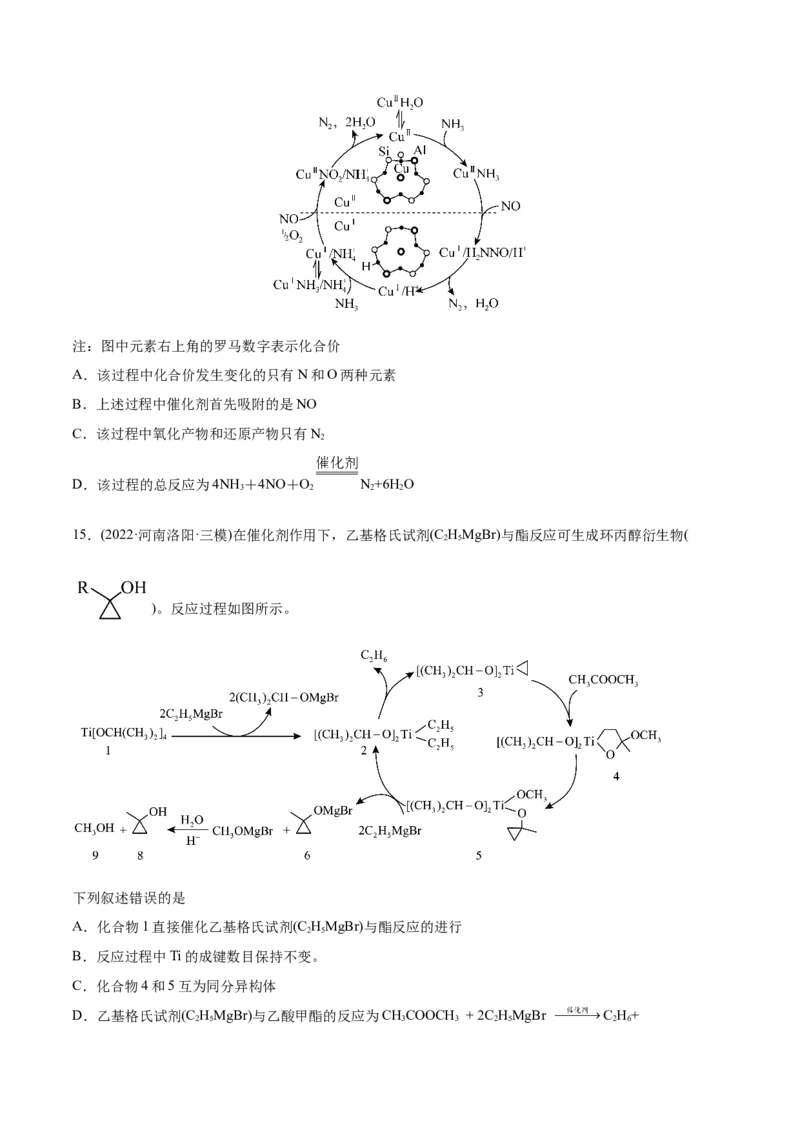
12.(2022·内蒙古呼和浩特·一模)钒元素用途广泛,如图是一种钒的化合物催化某反应的反应机理。下列叙述不正确的是
A. 是该反应的催化剂
B.过程①②④中反应的原子利用率为100%
C.该催化循环中V的成键数目发生变化
D.该反应的离子方程式为:HO+Cl-+ H+= HOCl+ H O
2 2 2
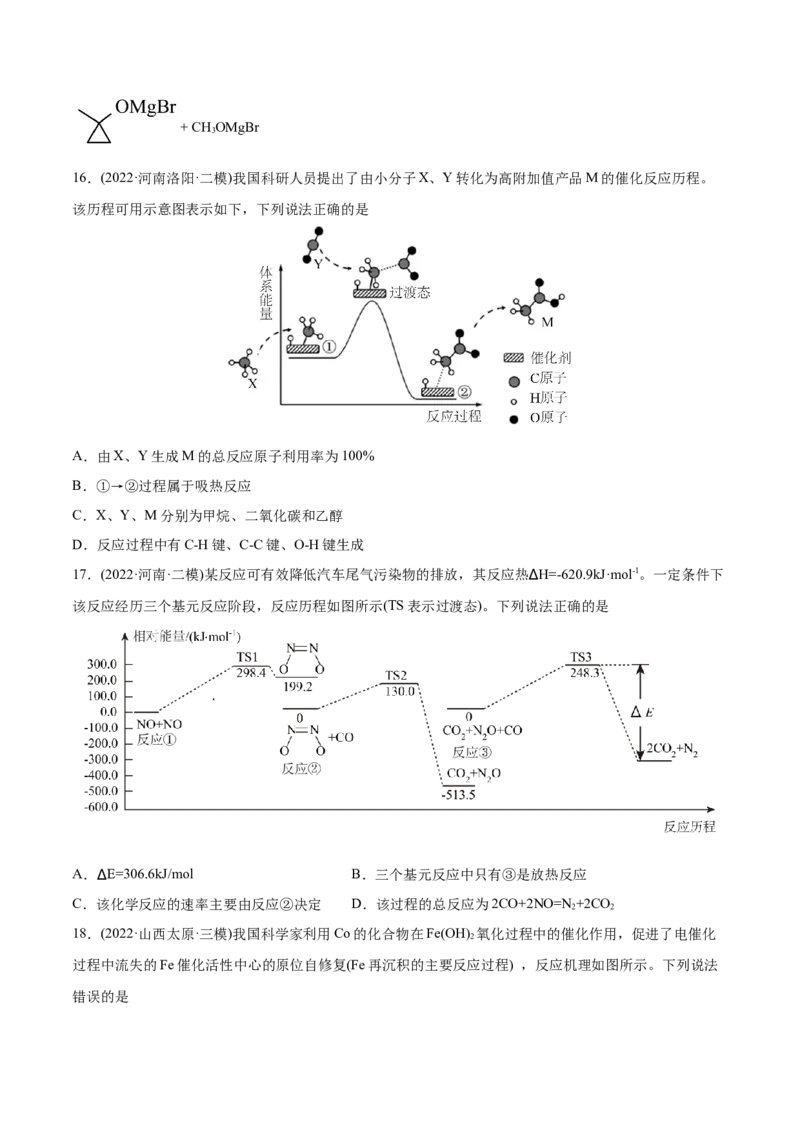
13.(2022·江西南昌·一模)科学家利用金(Au)催化电解法在常温常压下实现合成氨,工作时某极区的微观示
意图如下,其中电解液为溶解有三氟甲磺酸锂(LiCF SO )和乙醇的有机溶液。下列说法正确是
3 3
A.金(Au)为催化剂不参与反应
B.三氟甲磺酸锂和乙醇的有机溶液不能导电
C.该电极方程式为:N+6e-+6CH CHOH=2NH +6CH CHO-
2 3 2 3 3 2
D.选择性透过膜只允许N、NH 和HO通过,其它离子不可通过
2 3 2
14.(2022·河南郑州·三模)下图是在Cu基分子筛表面用NH 处理 NO,污染物的一种反应机理。下列说法
3
正确的是注:图中元素右上角的罗马数字表示化合价
A.该过程中化合价发生变化的只有N和O两种元素
B.上述过程中催化剂首先吸附的是NO
C.该过程中氧化产物和还原产物只有N
2
D.该过程的总反应为4NH +4NO+O N+6H O
3 2 2 2
15.(2022·河南洛阳·三模)在催化剂作用下,乙基格氏试剂(C HMgBr)与酯反应可生成环丙醇衍生物(
2 5
)。反应过程如图所示。
下列叙述错误的是
A.化合物1直接催化乙基格氏试剂(C HMgBr)与酯反应的进行
2 5
B.反应过程中Ti的成键数目保持不变。
C.化合物4和5互为同分异构体
D.乙基格氏试剂(C HMgBr)与乙酸甲酯的反应为CHCOOCH + 2C HMgBr C H+
2 5 3 3 2 5 2 6+ CHOMgBr
3
16.(2022·河南洛阳·二模)我国科研人员提出了由小分子X、Y转化为高附加值产品M的催化反应历程。
该历程可用示意图表示如下,下列说法正确的是
A.由X、Y生成M的总反应原子利用率为100%
B.①→②过程属于吸热反应
C.X、Y、M分别为甲烷、二氧化碳和乙醇
D.反应过程中有C-H键、C-C键、O-H键生成
17.(2022·河南·二模)某反应可有效降低汽车尾气污染物的排放,其反应热∆H=-620.9kJ·mol-1。一定条件下
该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是
A.∆E=306.6kJ/mol B.三个基元反应中只有③是放热反应
C.该化学反应的速率主要由反应②决定 D.该过程的总反应为2CO+2NO=N +2CO
2 2
18.(2022·山西太原·三模)我国科学家利用Co的化合物在Fe(OH) 氧化过程中的催化作用,促进了电催化
2
过程中流失的Fe催化活性中心的原位自修复(Fe再沉积的主要反应过程) ,反应机理如图所示。下列说法
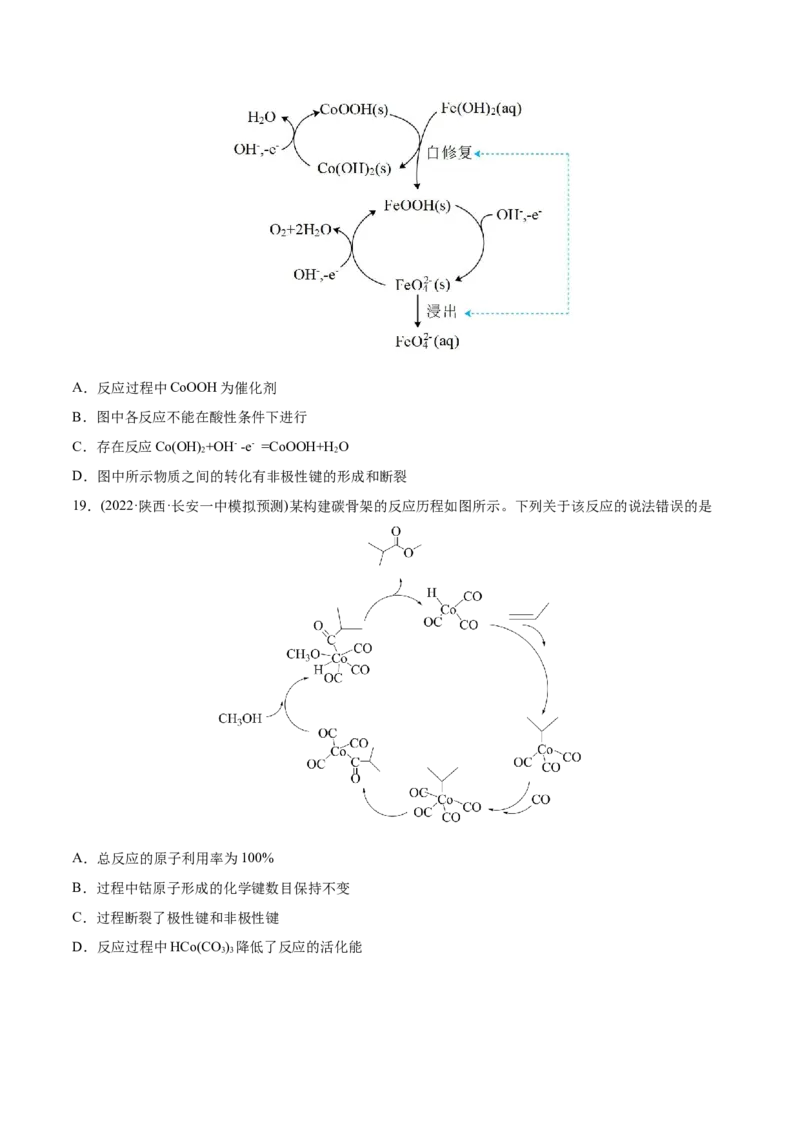
错误的是A.反应过程中CoOOH为催化剂
B.图中各反应不能在酸性条件下进行
C.存在反应Co(OH) +OH- -e- =CoOOH+H O
2 2
D.图中所示物质之间的转化有非极性键的形成和断裂
19.(2022·陕西·长安一中模拟预测)某构建碳骨架的反应历程如图所示。下列关于该反应的说法错误的是
A.总反应的原子利用率为100%
B.过程中钴原子形成的化学键数目保持不变
C.过程断裂了极性键和非极性键
D.反应过程中HCo(CO ) 降低了反应的活化能
3 3