文档内容
专题 08 电化学及其应用
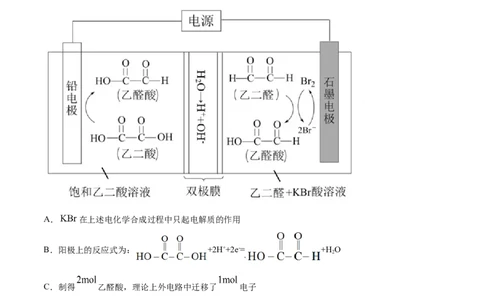
1.(2021·全国高考甲卷真题)乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。
图中的双极膜中间层中的 解离为 和 ,并在直流电场作用下分别问两极迁移。下列说法正确的
是
A. 在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +H O
2
C.制得 乙醛酸,理论上外电路中迁移了 电子
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
【答案】D
【分析】该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳极,阳
极上Br-被氧化为Br ,Br 将乙二醛氧化为乙醛酸,双极膜中间层的H+在直流电场作用下移向阴极,OH-移
2 2
向阳极。
【解析】A.KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生成的Br
2为乙二醛制备乙醛酸的中间产物,故A错误;
B.阳极上为Br-失去电子生成Br ,Br 将乙二醛氧化为乙醛酸,故B错误;
2 2
C.电解过程中阴阳极均生成乙醛酸,1mol乙二酸生成1mol乙醛酸转移电子为2mol,1mol乙二醛生成
1mol乙醛酸转移电子为2mol,根据转移电子守恒可知每生成1mol乙醛酸转移电子为1mol,因此制得
2mol乙醛酸时,理论上外电路中迁移了2mol电子,故C错误;
D.由上述分析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,故D正确;
综上所述,说法正确的是D项,故答案为D。
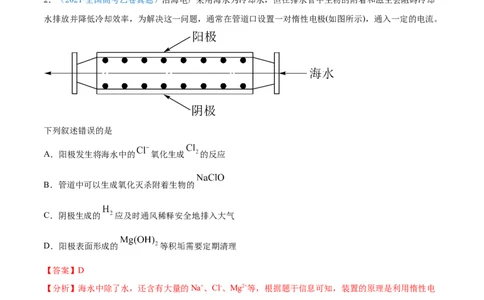
2.(2021·全国高考乙卷真题)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却
水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是
A.阳极发生将海水中的 氧化生成 的反应
B.管道中可以生成氧化灭杀附着生物的
C.阴极生成的 应及时通风稀释安全地排入大气
D.阳极表面形成的 等积垢需要定期清理
【答案】D
【分析】海水中除了水,还含有大量的Na+、Cl-、Mg2+等,根据题干信息可知,装置的原理是利用惰性电
极电解海水,阳极区溶液中的Cl-会优先失电子生成Cl,阴极区HO优先得电子生成H 和OH-,结合海水
2 2 2
成分及电解产物分析解答。
【解析】A.根据分析可知,阳极区海水中的Cl-会优先失去电子生成Cl,发生氧化反应,A正确;
2
B.设置的装置为电解池原理,根据分析知,阳极区生成的Cl 与阴极区生成的OH-在管道中会发生反应生
2
成NaCl、NaClO和HO,其中NaClO具有强氧化性,可氧化灭杀附着的生物,B正确;
2
C.因为H 是易燃性气体,所以阳极区生成的H 需及时通风稀释,安全地排入大气,以排除安全隐患,C
2 2
正确;D.阴极的电极反应式为:2HO+2e-=H ↑+2OH-,会使海水中的Mg2+沉淀积垢,所以阴极表面会形成
2 2
Mg(OH) 等积垢需定期清理,D错误。
2
故选D。
3.(2021·广东高考真题)火星大气中含有大量 ,一种有 参加反应的新型全固态电池有望为火星
探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B. 在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能
【答案】B
【解析】根据题干信息可知,放电时总反应为4Na+3CO =2Na CO+C。
2 2 3
A.放电时负极上Na发生氧化反应失去电子生成Na+,故A错误;
B.放电时正极为CO 得到电子生成C,故B正确;
2
C.放电时阳离子移向还原电极,即阳离子由负极移向正极,故C错误;
D.放电时装置为原电池,能量转化关系为化学能转化为电能和化学能等,故D正确;
综上所述,符合题意的为B项,故答案为B。
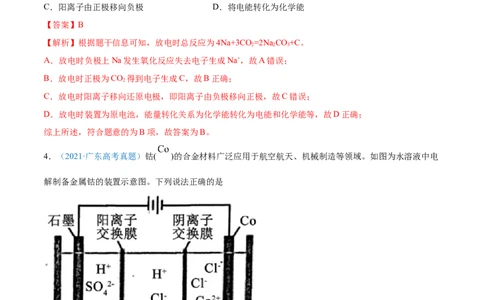
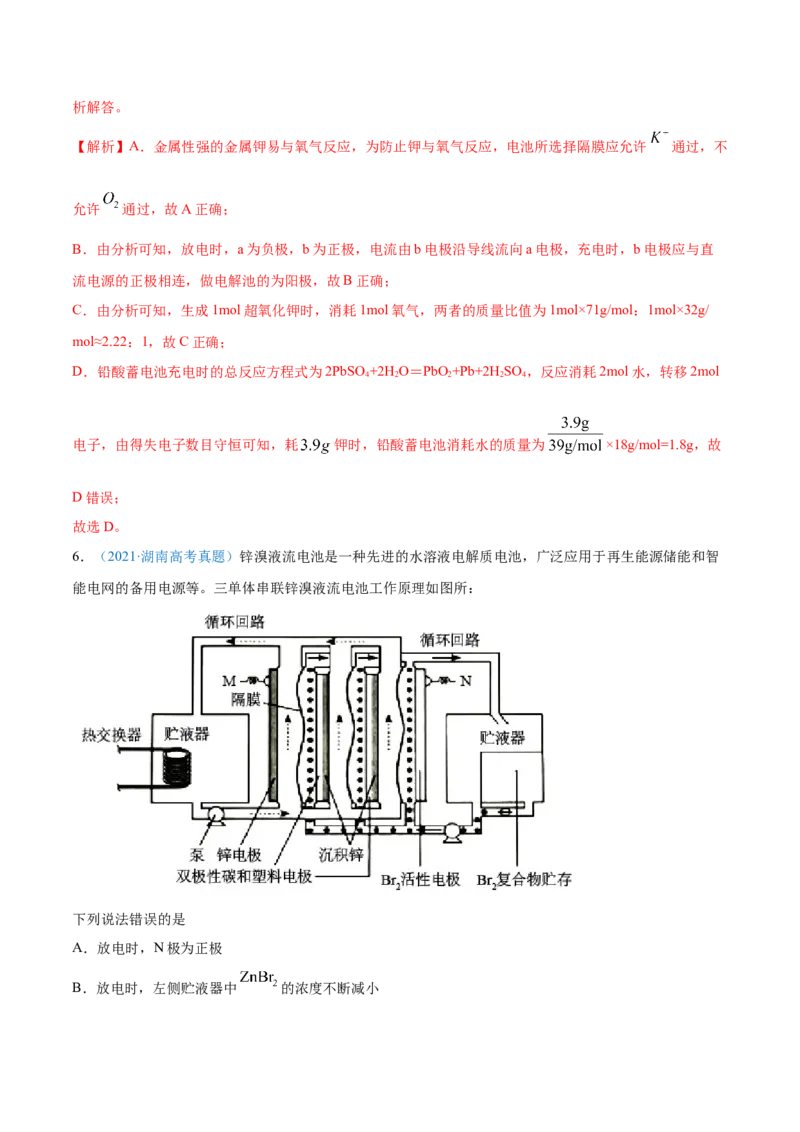
4.(2021·广东高考真题)钴( )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电
解制备金属钴的装置示意图。下列说法正确的是
A.工作时,Ⅰ室和Ⅱ室溶液的 均增大
B.生成 ,Ⅰ室溶液质量理论上减少
C.移除两交换膜后,石墨电极上发生的反应不变D.电解总反应:
【答案】D
【分析】由图可知,该装置为电解池,石墨电极为阳极,水在阳极失去电子发生氧化反应生成氧气和氢离
子,电极反应式为2HO-4e-=O ↑+4H+,Ⅰ室中阳离子电荷数大于阴离子电荷数,放电生成的氢离子通过阳
2 2
离子交换膜由Ⅰ室向Ⅱ室移动,钴电极为阴极,钴离子在阴极得到电子发生还原反应生成钴,电极反应式
为Co2++2e-=Co,Ⅲ室中阴离子电荷数大于阳离子电荷数,氯离子过阴离子交换膜由Ⅲ室向Ⅱ室移动,电解
的总反应的离子方程式为2Co2++2H O 2 Co +O ↑+4H+。
2 2
【解析】A.由分析可知,放电生成的氢离子通过阳离子交换膜由Ⅰ室向Ⅱ室移动,使Ⅱ室中氢离子浓度
增大,溶液pH减小,故A错误;
B.由分析可知,阴极生成1mol钴,阳极有1mol水放电,则Ⅰ室溶液质量减少18g,故B错误;
C.若移除离子交换膜,氯离子的放电能力强于水,氯离子会在阳极失去电子发生氧化反应生成氯气,则
移除离子交换膜,石墨电极的电极反应会发生变化,故C错误;
D.由分析可知,电解的总反应的离子方程式为2Co2++2H O 2 Co +O ↑+4H+,故D正确;
2 2
故选D。
5.(2021·河北高考真题)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,
2
下列说法错误的是
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【答案】D
【分析】由图可知,a电极为原电池的负极,单质钾片失去电子发生氧化反应生成钾离子,电极反应式为
K—e-=K+,b电极为正极,在钾离子作用下,氧气在正极得到电子发生还原反应生成超氧化钾;据以上分析解答。
【解析】A.金属性强的金属钾易与氧气反应,为防止钾与氧气反应,电池所选择隔膜应允许 通过,不
允许 通过,故A正确;
B.由分析可知,放电时,a为负极,b为正极,电流由b电极沿导线流向a电极,充电时,b电极应与直
流电源的正极相连,做电解池的为阳极,故B正确;
C.由分析可知,生成1mol超氧化钾时,消耗1mol氧气,两者的质量比值为1mol×71g/mol:1mol×32g/
mol≈2.22:1,故C正确;
D.铅酸蓄电池充电时的总反应方程式为2PbSO +2H O=PbO +Pb+2H SO ,反应消耗2mol水,转移2mol
4 2 2 2 4
电子,由得失电子数目守恒可知,耗 钾时,铅酸蓄电池消耗水的质量为 ×18g/mol=1.8g,故
D错误;
故选D。
6.(2021·湖南高考真题)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智
能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中 的浓度不断减小C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
【答案】B
【分析】由图可知,放电时,N电极为电池的正极,溴在正极上得到电子发生还原反应生成溴离子,电极
反应式为Br +2e—=2Br—,M电极为负极,锌失去电子发生氧化反应生成锌离子,电极反应式为Zn—2e—
2
=Zn2+,正极放电生成的溴离子通过离子交换膜进入左侧,同时锌离子通过交换膜进入右侧,维持两侧溴化
锌溶液的浓度保持不变;充电时,M电极与直流电源的负极相连,做电解池的阴极,N电极与直流电源的
正极相连,做阳极。
【解析】A.由分析可知,放电时,N电极为电池的正极,故A正确;
B.由分析可知,放电或充电时,左侧储液器和右侧储液器中溴化锌的浓度维持不变,故B错误;
C.由分析可知,充电时,M电极与直流电源的负极相连,做电解池的阴极,锌离子在阴极上得到电子发
生还原反应生成锌,电极反应式为Zn2++2e—=Zn,故C正确;
D.由分析可知,放电或充电时,交换膜允许锌离子和溴离子通过,维持两侧溴化锌溶液的浓度保持不变,
故D正确;
故选B。
7.(2021·浙江高考真题)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时
得电子成为Li嵌入该薄膜材料中;电极B为 薄膜;集流体起导电作用。下列说法不正确的是
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过 电子时, 薄膜电解质损失
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为【答案】B
【分析】由题中信息可知,该电池充电时 得电子成为Li嵌入电极A中,可知电极A在充电时作阴极,
故其在放电时作电池的负极,而电极B是电池的正极。
【解析】A.由图可知,集流体A与电极A相连,充电时电极A作阴极,故充电时集流体A与外接电源的
负极相连,A说法正确;
B.放电时,外电路通过a mol电子时,内电路中有a mol 通过LiPON薄膜电解质从负极迁移到正极,
但是LiPON薄膜电解质没有损失 ,B说法不正确;
C.放电时,电极B为正极,发生还原反应,反应可表示为 ,C说法正
确;
D.电池放电时,嵌入在非晶硅薄膜中的锂失去电子变成 ,正极上 得到电子和 变为
,故电池总反应可表示为 ,D说法正确。
综上所述,相关说法不正确的是B,本题选B。
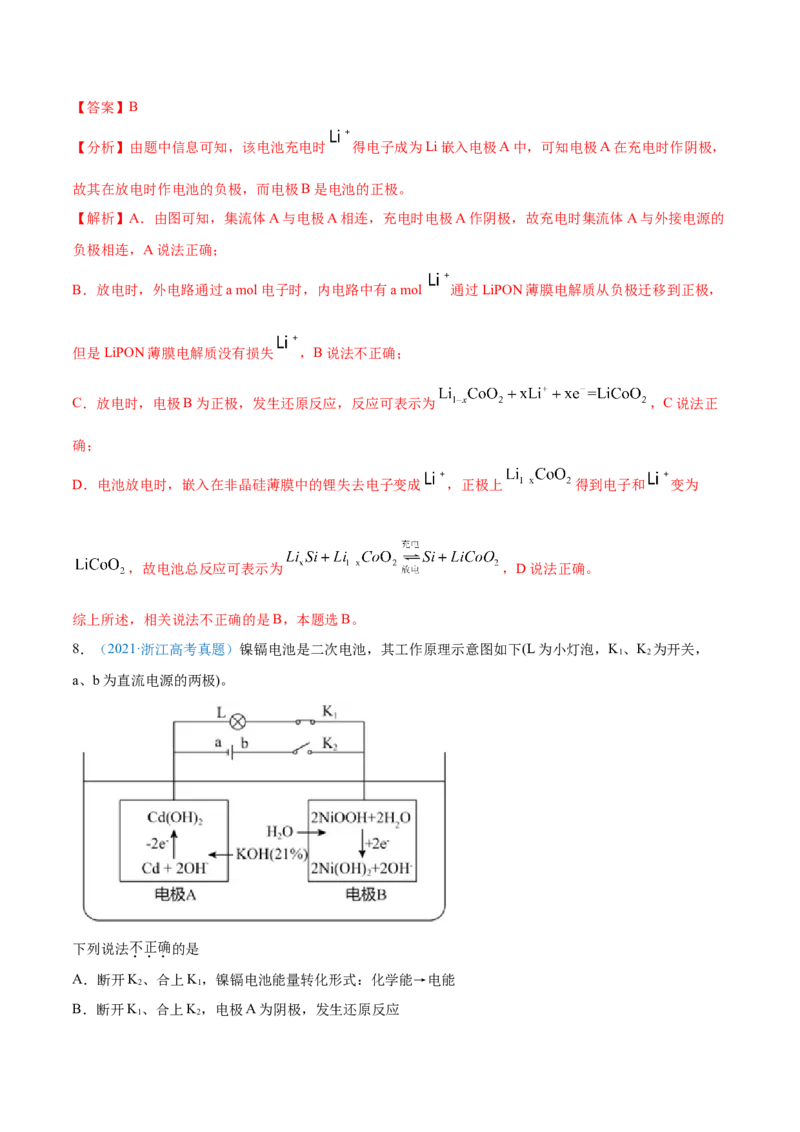
8.(2021·浙江高考真题)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开关,
1 2
a、b为直流电源的两极)。
下列说法不正确的是
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Cd(OH) +2Ni(OH)
2 2 2
【答案】C
【分析】根据图示,电极A充电时为阴极,则放电时电极A为负极,负极上Cd失电子发生氧化反应生成
Cd(OH) ,负极反应式为Cd-2e-+2OH-=Cd(OH) ,电极B充电时为阳极,则放电时电极B为正极,正极上
2 2
NiOOH得电子发生还原反应生成Ni(OH) ,正极反应式为2NiOOH+2e-+2H O=2Ni(OH) +2OH-,放电时总
2 2 2
反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) ,据此分析作答。
2 2 2
【解析】A.断开K、合上K,为放电过程,镍镉电池能量转化形式:化学能→电能,A正确;
2 1
B.断开K、合上K,为充电过程,电极A与直流电源的负极相连,电极A为阴极,发生还原反应,电极
1 2
反应式为Cd(OH) +2e-=Cd+2OH-,B正确;
2
C.电极B发生氧化反应的电极反应式为2Ni(OH) -2e-+2OH-=2NiOOH+2H O,则电极A发生还原反应的电
2 2
极反应式为Cd(OH) +2e-=Cd+2OH-,此时为充电过程,总反应为Cd(OH) +2Ni(OH)
2 2 2
Cd+2NiOOH+2H O,溶液中KOH浓度减小,C错误;
2
D.根据分析,放电时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) ,则镍镉二次电池总反应式为
2 2 2
Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) ,D正确;
2 2 2
答案选C。
1.(2021·黑龙江哈尔滨市·哈尔滨三中高三其他模拟)中国科学院大连化物所的研究团队创新性提出锌碘
单液流电池的概念,实现锌碘单液流中电解液的利用率近100%,其原理如图所示。下列说法正确的是A.放电时A电极反应式为:Zn2++2e-=Zn
B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜
D.充电时A极增重65g,C区增加离子数为2N
A
【答案】C
【解析】
A.放电时A电极是负极,A极反应式为:Zn-2e-=Zn2+,故A错误;
B.放电时,A区发生反应Zn-2e-=Zn2+,C区Cl-进入A区,所以电解质储罐中离子总浓度增大,故B错误;
C.放电时,C区Cl-进入A区、K+进入B区,所以M为阴离子交换膜,N为阳离子交换膜,故C正确;
D.充电时A极增重65g,A区发生反应Zn2++2e-=Zn,电路中转移2mol电子,根据电荷守恒,2molCl-自A
区进入C区,2molK+自B区进入C区,C区增加离子数为4N ,故D错误;
A
选C。
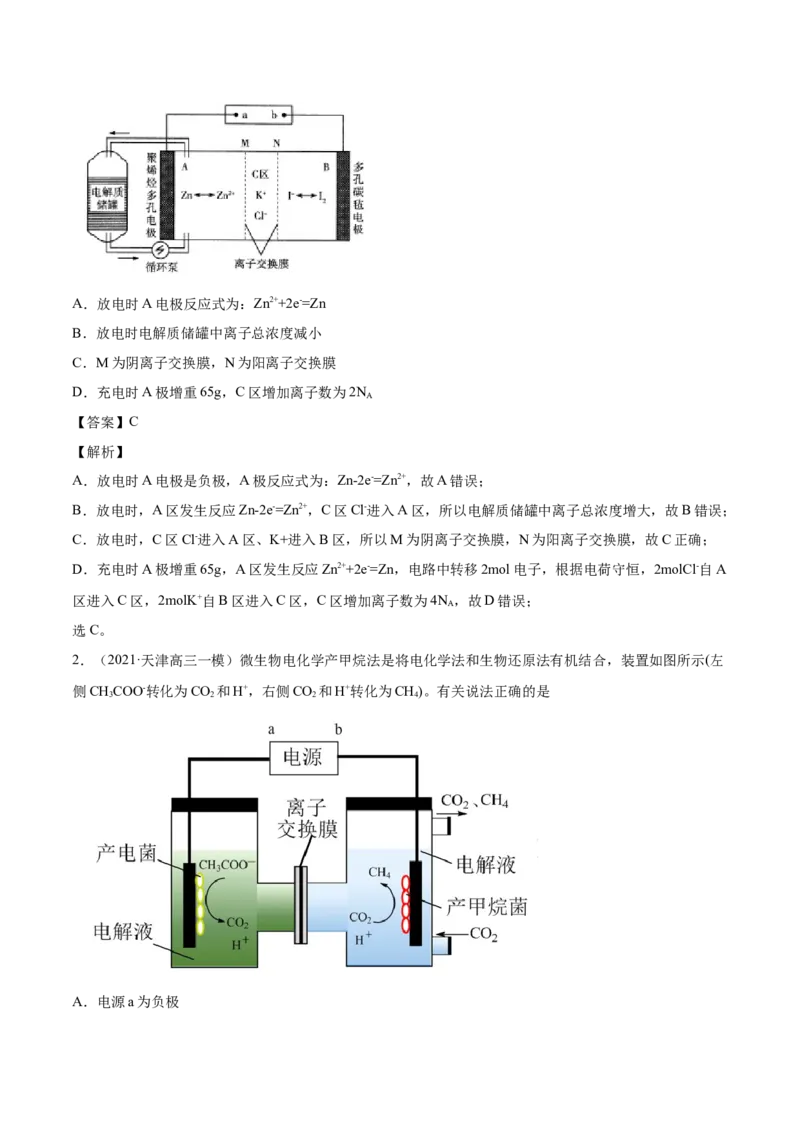
2.(2021·天津高三一模)微生物电化学产甲烷法是将电化学法和生物还原法有机结合,装置如图所示(左
侧CHCOO-转化为CO 和H+,右侧CO 和H+转化为CH)。有关说法正确的是
3 2 2 4
A.电源a为负极B.该技术能助力“碳中和”(二氧化碳“零排放”)的战略愿景
C.外电路中每通过lmol e-与a相连的电极将产生2.8L CO
2
D.b电极的反应为:CO+8e-+8H+=CH +2H O
2 4 2
【答案】D
【分析】
电解池中,与电源正极相连的电极是阳极,阳极上失去电子发生氧化反应,左侧电极上CHCOO-转化为
3
CO 和H+,发生氧化反应,左侧为阳极,与电源负极相连的电极是阴极,阴极上氧化剂得到电子发生还原
2
反应,右侧CO 和H+转化为CH;为还原反应,右侧为阴极;
2 4
【解析】
A. 据分析,左侧电极为阳极,则电源a为正极,A错误;
B.电化学反应时,电极上电子数守恒,则有左侧 ,右侧有 ,
二氧化碳不能零排放,B错误;
C. 不知道气体是否处于标准状况,则难以计算与a相连的电极将产生的CO 的体积,C错误;
2
D. 右侧为阴极区,b电极上发生还原反应,结合图示信息可知,电极反应为:CO+8e-+8H+=CH +2H O,
2 4 2
D正确;
答案选D。
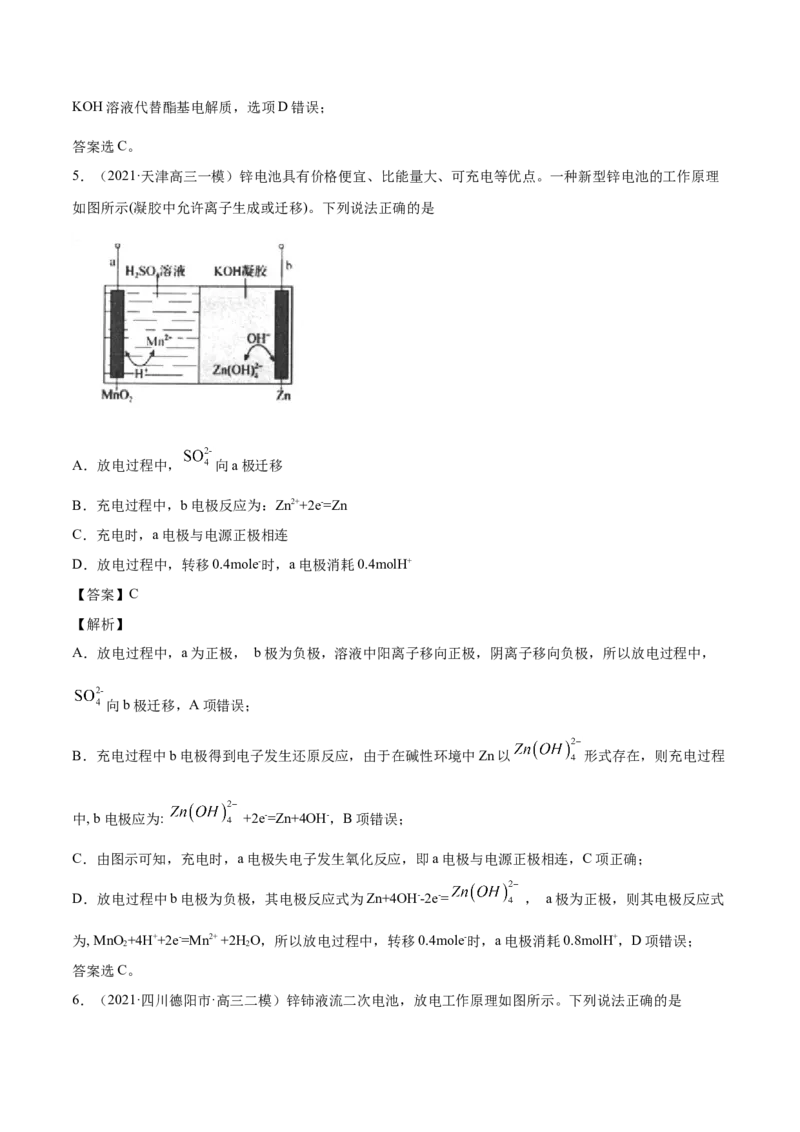
3.(2021·天津高三三模)我国化学工作者提出一种利用有机电极(PTO/HQ)和无机电极(MnO /石墨毡),在
2
酸性环境中可充电的电池其放电时的工作原理如图所示:
下列说法错误的是
A.放电时,MnO /石墨毡为正极,发生还原反应
2
B.充电时,有机电极和外接电源的负极相连
C.放电时,MnO /石墨毡电极的电极反应式为MnO +2e-+4H+=Mn2++2H O
2 2 2
D.充电时,有机电极的电极反应式为PTO+4e-+4H O=HQ+4OH-
2
【答案】D
【解析】A.从工作原理图可知,MnO 生成Mn2+,得到了电子,则MnO /石墨毡为电源正极,发生还原反应,故A
2 2
正确;
B.充电时,有机电极得到电子,PTO得到电子和H+生成HQ结构,则有机电极和外接电源的负极相连,
故B正确;
C.放电时,MnO /石墨毡电极为电源正极,MnO 的电子被还原成Mn2+,则其电极反应式为MnO +2e-
2 2 2
+4H+=Mn2++2H O,故C正确;
2
D.充电时,有机电极的电极反应式为PTO+4e-+4H+=HQ,故D错误;
本题答案D。
4.(2021·天津高三一模)近日,南开大学陈军院士团队以KSn合金为负极,以含羧基多壁碳纳米管
(MWCNTs—COOH)为正极催化剂构建了可充电K—CO 电池(如图所示),电池反应为4KSn+3CO
2 2
2KCO+C+4Sn,其中生成的KCO 附着在正极上。该成果对改善环境和缓解能源问题具有巨大潜力。下
2 3 2 3
列说法正确的是
A.放电时,电子由KSn合金经酯基电解质流向MWCNTs—COOH
B.电池每吸收22.4LCO ,电路中转移4mole-
2
C.充电时,阳极电极反应式为:C-4e-+2K CO=3CO ↑+4K+
2 3 2
D.为了更好的吸收温室气体CO,可用适当浓度的KOH溶液代替酯基电解质
2
【答案】C
【解析】
A.放电时,KSn合金作负极,MWCNTs-COOH作正极,在内电路中电流由负极流向正极,选项A错误;
B.气体未指明状况,无法根据体积确定其物质的量,选项B错误;
C.充电时,阳极发生氧化反应,电极反应为C-4e-+2K CO=3CO ↑+4K+,选项C正确;
2 3 2
D.若用KOH溶液代替酯基电解质,则KOH会与正极上的MWCNTs-COOH发生反应,因此不能使用KOH溶液代替酯基电解质,选项D错误;
答案选C。
5.(2021·天津高三一模)锌电池具有价格便宜、比能量大、可充电等优点。一种新型锌电池的工作原理
如图所示(凝胶中允许离子生成或迁移)。下列说法正确的是
A.放电过程中, 向a极迁移
B.充电过程中,b电极反应为:Zn2++2e-=Zn
C.充电时,a电极与电源正极相连
D.放电过程中,转移0.4mole-时,a电极消耗0.4molH+
【答案】C
【解析】
A.放电过程中,a为正极, b极为负极,溶液中阳离子移向正极,阴离子移向负极,所以放电过程中,
向b极迁移,A项错误;
B.充电过程中b电极得到电子发生还原反应,由于在碱性环境中Zn以 形式存在,则充电过程
中, b电极应为: +2e-=Zn+4OH-,B项错误;
C.由图示可知,充电时,a电极失电子发生氧化反应,即a电极与电源正极相连,C项正确;
D.放电过程中b电极为负极,其电极反应式为Zn+4OH--2e-= , a极为正极,则其电极反应式
为, MnO +4H++2e-=Mn2+ +2H O,所以放电过程中,转移0.4mole-时,a电极消耗0.8molH+,D项错误;
2 2
答案选C。
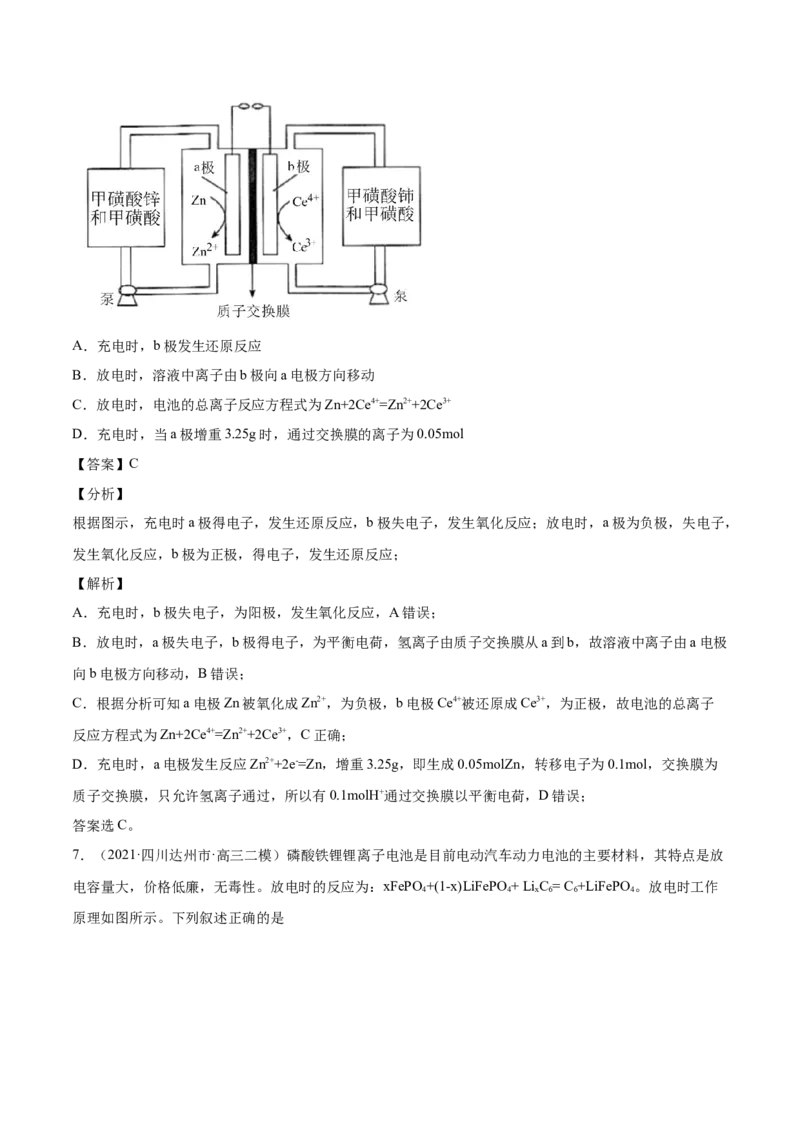
6.(2021·四川德阳市·高三二模)锌铈液流二次电池,放电工作原理如图所示。下列说法正确的是A.充电时,b极发生还原反应
B.放电时,溶液中离子由b极向a电极方向移动
C.放电时,电池的总离子反应方程式为Zn+2Ce4+=Zn2++2Ce3+
D.充电时,当a极增重3.25g时,通过交换膜的离子为0.05mol
【答案】C
【分析】
根据图示,充电时a极得电子,发生还原反应,b极失电子,发生氧化反应;放电时,a极为负极,失电子,
发生氧化反应,b极为正极,得电子,发生还原反应;
【解析】
A.充电时,b极失电子,为阳极,发生氧化反应,A错误;
B.放电时,a极失电子,b极得电子,为平衡电荷,氢离子由质子交换膜从a到b,故溶液中离子由a电极
向b电极方向移动,B错误;
C.根据分析可知a电极Zn被氧化成Zn2+,为负极,b电极Ce4+被还原成Ce3+,为正极,故电池的总离子
反应方程式为Zn+2Ce4+=Zn2++2Ce3+,C正确;
D.充电时,a电极发生反应Zn2++2e-=Zn,增重3.25g,即生成0.05molZn,转移电子为0.1mol,交换膜为
质子交换膜,只允许氢离子通过,所以有0.1molH+通过交换膜以平衡电荷,D错误;
答案选C。
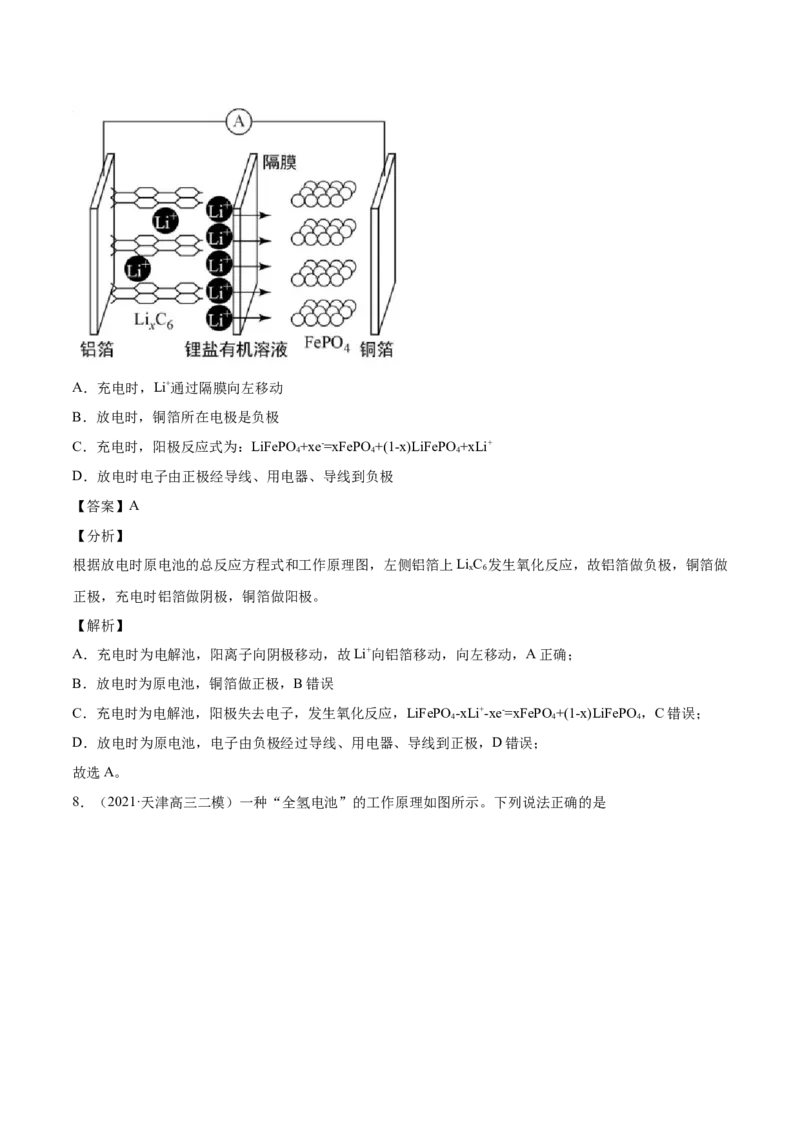
7.(2021·四川达州市·高三二模)磷酸铁锂锂离子电池是目前电动汽车动力电池的主要材料,其特点是放
电容量大,价格低廉,无毒性。放电时的反应为:xFePO +(1-x)LiFePO + LiC = C +LiFePO 。放电时工作
4 4 x 6 6 4
原理如图所示。下列叙述正确的是A.充电时,Li+通过隔膜向左移动
B.放电时,铜箔所在电极是负极
C.充电时,阳极反应式为:LiFePO +xe-=xFePO+(1-x)LiFePO +xLi+
4 4 4
D.放电时电子由正极经导线、用电器、导线到负极
【答案】A
【分析】
根据放电时原电池的总反应方程式和工作原理图,左侧铝箔上LiC 发生氧化反应,故铝箔做负极,铜箔做
x 6
正极,充电时铝箔做阴极,铜箔做阳极。
【解析】
A.充电时为电解池,阳离子向阴极移动,故Li+向铝箔移动,向左移动,A正确;
B.放电时为原电池,铜箔做正极,B错误
C.充电时为电解池,阳极失去电子,发生氧化反应,LiFePO -xLi+-xe-=xFePO+(1-x)LiFePO ,C错误;
4 4 4
D.放电时为原电池,电子由负极经过导线、用电器、导线到正极,D错误;
故选A。
8.(2021·天津高三二模)一种“全氢电池”的工作原理如图所示。下列说法正确的是A.电流方向是从吸附层M通过导线到吸附层N
B.放电时,吸附层M发生的电极反应:
C. 从右边穿过离子交换膜向左边移动
D.“全氢电池”放电时的总反应式为:
【答案】B
【分析】
由工作原理图可知,左边吸附层M上氢气失电子与氢氧根结合生成水,发生了氧化反应为负极,电极反应
是H-2e-+2OH-═2H O,右边吸附层N为正极,发生了还原反应,电极反应是2e-+2H+═H ,结合原电池中
2 2 2
阳离子移向正极,阴离子移向负极解答该题。
【解析】
A.由工作原理图可知,左边吸附层M为负极,右边吸附层N为正极,则电流方向为从吸附层N通过导线
到吸附层M,故A错误;
B.左边吸附层M为负极极,发生了氧化反应,电极反应是H-2e-+2OH-=2H O,故B正确;
2 2
C.原电池中阳离子移向正极,阴离子移向负极,所以电解质溶液中Na+向右正极移动,故C错误;
D.负极电极反应是H-2e-+2OH-═2H O,正极电极反应是2e-+2H+═H ,电池的总反应无氧气参加,故D错
2 2 2
误;
故选:B。
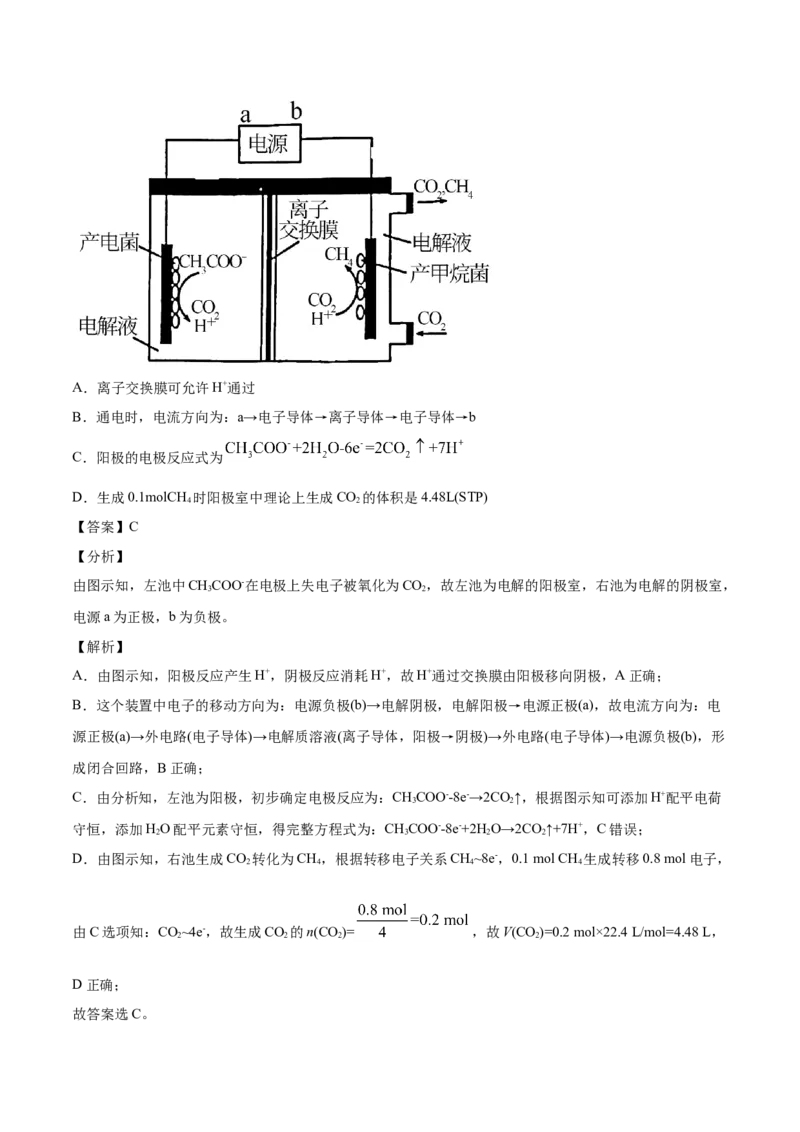
8.(2021·山东潍坊市·高三三模)将电化学法和生物还原法有机结合,利用微生物电化学方法生产甲烷,
装置如图所示。下列说法错误的是A.离子交换膜可允许H+通过
B.通电时,电流方向为:a→电子导体→离子导体→电子导体→b
C.阳极的电极反应式为
D.生成0.1molCH 时阳极室中理论上生成CO 的体积是4.48L(STP)
4 2
【答案】C
【分析】
由图示知,左池中CHCOO-在电极上失电子被氧化为CO,故左池为电解的阳极室,右池为电解的阴极室,
3 2
电源a为正极,b为负极。
【解析】
A.由图示知,阳极反应产生H+,阴极反应消耗H+,故H+通过交换膜由阳极移向阴极,A正确;
B.这个装置中电子的移动方向为:电源负极(b)→电解阴极,电解阳极→电源正极(a),故电流方向为:电
源正极(a)→外电路(电子导体)→电解质溶液(离子导体,阳极→阴极)→外电路(电子导体)→电源负极(b),形
成闭合回路,B正确;
C.由分析知,左池为阳极,初步确定电极反应为:CHCOO--8e-→2CO↑,根据图示知可添加H+配平电荷
3 2
守恒,添加HO配平元素守恒,得完整方程式为:CHCOO--8e-+2H O→2CO ↑+7H+,C错误;
2 3 2 2
D.由图示知,右池生成CO 转化为CH,根据转移电子关系CH~8e-,0.1 mol CH 生成转移0.8 mol电子,
2 4 4 4
由C选项知:CO~4e-,故生成CO 的n(CO)= ,故V(CO)=0.2 mol×22.4 L/mol=4.48 L,
2 2 2 2
D正确;
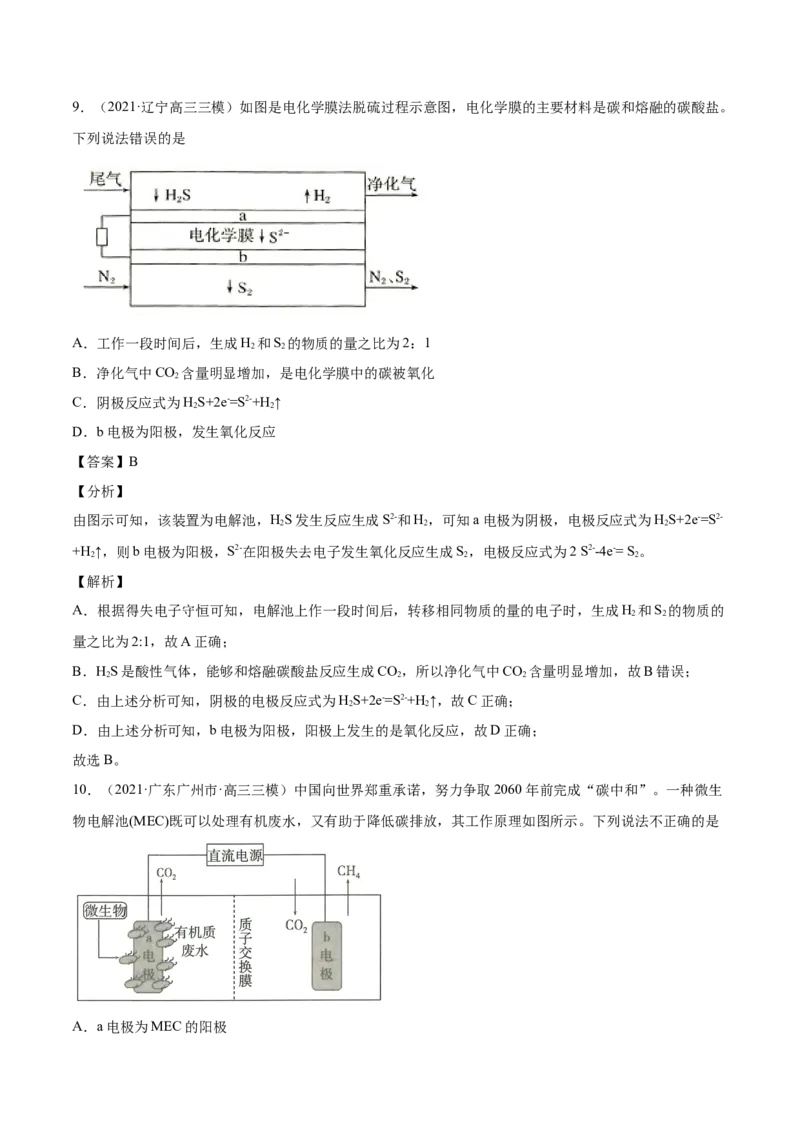
故答案选C。9.(2021·辽宁高三三模)如图是电化学膜法脱硫过程示意图,电化学膜的主要材料是碳和熔融的碳酸盐。
下列说法错误的是
A.工作一段时间后,生成H 和S 的物质的量之比为2:1
2 2
B.净化气中CO 含量明显增加,是电化学膜中的碳被氧化
2
C.阴极反应式为HS+2e-=S2-+H ↑
2 2
D.b电极为阳极,发生氧化反应
【答案】B
【分析】
由图示可知,该装置为电解池,HS发生反应生成S2-和H,可知a电极为阴极,电极反应式为HS+2e-=S2-
2 2 2
+H ↑,则b电极为阳极,S2-在阳极失去电子发生氧化反应生成S,电极反应式为2 S2--4e-= S 。
2 2 2
【解析】
A.根据得失电子守恒可知,电解池上作一段时间后,转移相同物质的量的电子时,生成H 和S 的物质的
2 2
量之比为2:1,故A正确;
B.HS是酸性气体,能够和熔融碳酸盐反应生成CO,所以净化气中CO 含量明显增加,故B错误;
2 2 2
C.由上述分析可知,阴极的电极反应式为HS+2e-=S2-+H ↑,故C正确;
2 2
D.由上述分析可知,b电极为阳极,阳极上发生的是氧化反应,故D正确;
故选B。
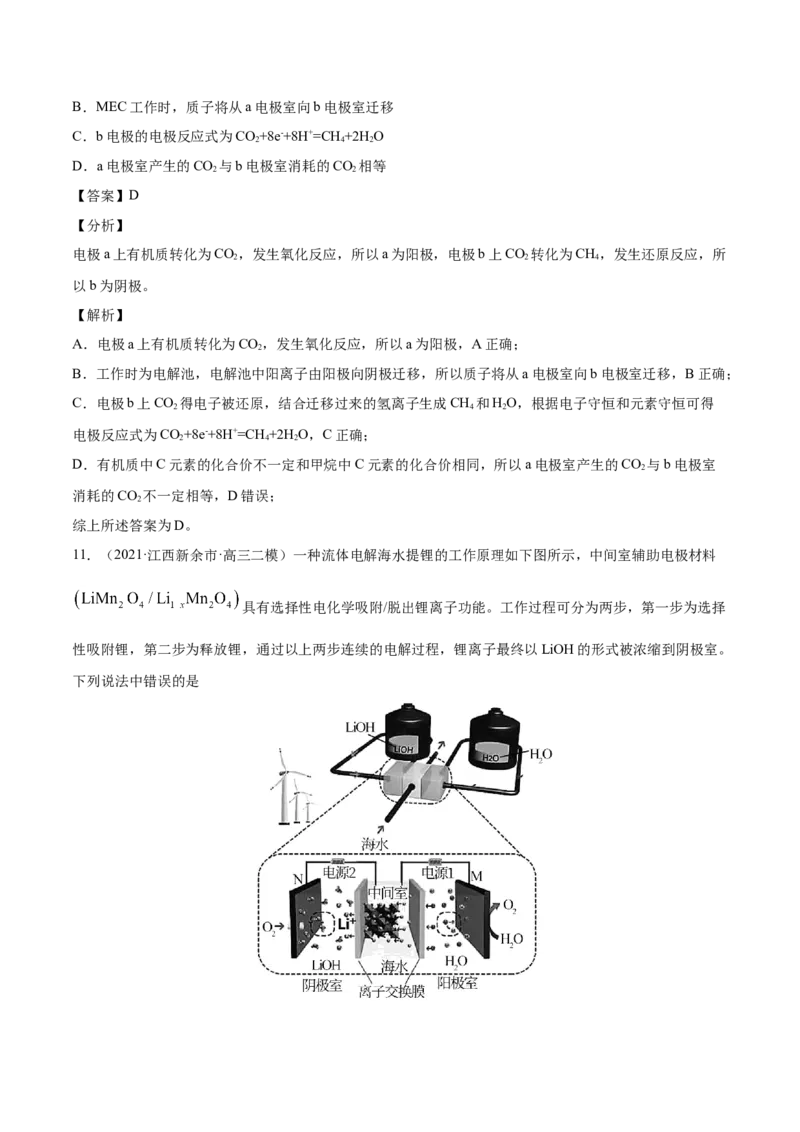
10.(2021·广东广州市·高三三模)中国向世界郑重承诺,努力争取2060年前完成“碳中和”。一种微生
物电解池(MEC)既可以处理有机废水,又有助于降低碳排放,其工作原理如图所示。下列说法不正确的是
A.a电极为MEC的阳极B.MEC工作时,质子将从a电极室向b电极室迁移
C.b电极的电极反应式为CO+8e-+8H+=CH +2H O
2 4 2
D.a电极室产生的CO 与b电极室消耗的CO 相等
2 2
【答案】D
【分析】
电极a上有机质转化为CO,发生氧化反应,所以a为阳极,电极b上CO 转化为CH,发生还原反应,所
2 2 4
以b为阴极。
【解析】
A.电极a上有机质转化为CO,发生氧化反应,所以a为阳极,A正确;
2
B.工作时为电解池,电解池中阳离子由阳极向阴极迁移,所以质子将从a电极室向b电极室迁移,B正确;
C.电极b上CO 得电子被还原,结合迁移过来的氢离子生成CH 和HO,根据电子守恒和元素守恒可得
2 4 2
电极反应式为CO+8e-+8H+=CH +2H O,C正确;
2 4 2
D.有机质中C元素的化合价不一定和甲烷中C元素的化合价相同,所以a电极室产生的CO 与b电极室
2
消耗的CO 不一定相等,D错误;
2
综上所述答案为D。
11.(2021·江西新余市·高三二模)一种流体电解海水提锂的工作原理如下图所示,中间室辅助电极材料
具有选择性电化学吸附/脱出锂离子功能。工作过程可分为两步,第一步为选择
性吸附锂,第二步为释放锂,通过以上两步连续的电解过程,锂离子最终以LiOH的形式被浓缩到阴极室。
下列说法中错误的是A.第一步接通电源1选择性提取锂:第二步接通电源2释放锂
B.释放锂过程中,中间室材料应接电源负极,发生的电极反应式为
C.中间室两侧的离子交换膜选用阳离子交换膜
D.当阴极室得到4.8gLiOH时,理论上阳极室产生1.12L气体(标准状态下)
【答案】B
【解析】
A. 第一步接通电源1,中间室为阴极,发生反应 ,选择性提取锂,
第二步接通电源2,中间室为阴极,发生反应 释放锂,故A正确;
B. 释放锂过程中,中间室材料应接电源正极,发生的电极反应式为 ,
故B错误;
C. 根据图示,第一步为选择性吸附锂过程中阳极室中的离子向中间室移动,第二步为释放锂的过程中锂离
子移向阴极室,所以中间室两侧的离子交换膜选用阳离子交换膜,故C正确;
D.当阴极室得到4.8gLiOH时,电路中转移0.2mol电子,阳极室电极反应式是 ,产
生氧气的体积是 1.12L气体(标准状态下),故D正确;
选B。
12.(2021·辽宁沈阳市·沈阳二中高三月考)目前,光电催化反应器(PEC)可以有效的进行能源的转换和储
存,一种PEC装置如图所示,通过光解水可由CO 制得主要产物异丙醇。下列说法中错误的是
2A.该装置的能量来源为光能
B.光催化剂电极反应为2HO-4e-=O ↑+4H+
2 2
C.每生成60g异丙醇,电路中转移电子数目一定为18N
A
D.H+从光催化剂电极一侧向左移动
【答案】C
【分析】
电池左侧CO 和H+得电子,做原电池的正极;右侧电极为HO失电子,做原电池的负极。
2 2
【解析】
A.由装置图可知,该装置的能量来源是光能,A正确;
B.由图中可知,光催化剂电极进入的物质为HO,出去的物质是O 和H+,故该电极的反应为
2 2
,B正确;
C.电化学催化剂电极中,CO 发生的电极反应为:3CO+18H++18e-=CH CH(OH)CH +5H O,故每生成60g
2 2 3 3 2
即 异丙醇,但电极上还会发生副反应产生氢气转移电子,所以电路中转移的电子数目
不一定为18 ,C错误;
D.由图中可知,左侧是电池的正极,右侧为负极,阳离子向阳极移动,故 从光催化剂电极一侧向左移
动,D正确;
故答案为:C。
13.(2021·辽宁沈阳市·沈阳二中高三月考)中山大学化学科研团队首次将CsPbBr 纳米晶锚定在氨基化
3RGO包覆的α-Fe O(α-Fe O/Amine-RGO/CsPbBr ),构筑Z-Scheme异质结光催化剂,可有效降低电荷复合,
2 3 2 3 3
促进电荷分离,从而提升光催化性能。光催化还原CO 和氧化HO的反应路径如图。下列说法正确的是
2 2
A.α-Fe O 表面发生了还原反应
2 3
B.该光催化转化反应可以消除温室效应
C.“CsPbBr 纳米晶”表面上CO 转化为CH 的电极反应式为CO+8e-+8H+=CH +2H O
3 2 4 2 4 2
D.该催化转化的总反应涉及到极性共价键、非极性共价键的断裂和形成
【答案】C
【分析】
HO能在 光催化剂材料作用下,被氧化成O,同时生成质子(H+),发生的氧化反应为:
2 2
;电子转移到“CsPbBr 纳米晶”用于还原CO,CO 被还原为CO、CH,发生的还原
3 2 2 4
反应为:CO+2e-+2H+=CO+H O、CO+8e-+8H+=CH +2H O。
2 2 2 4 2
【解析】
A.由图可知,HO能在 光催化剂材料作用下,被氧化成O,发生了氧化反应,A错误;
2 2
B. 该光催化转化反应生成了CH,CH 也能导致温室效应,故该反应不能阻止温室效应,B错误;
4 4
C. “CsPbBr 纳米晶“”表面上CO 转化为CO、CH,发生了还原反应:CO+2e-+2H+=CO+H O、CO+8e-
3 2 4 2 2 2
+8H+=CH +2H O,C正确;
4 2
D. 该催化转化的总反应:2CO 2CO+O、CO+2H O CH+2O ,CO、HO都只含有极性共
2 2 2 2 4 2 2 2
价键,CO、CH 都只含极性共价键,O 只含非极性共价键,故只有极性共价键断裂、有极性和非极性共价
4 2
键生成,D错误;答案选C。
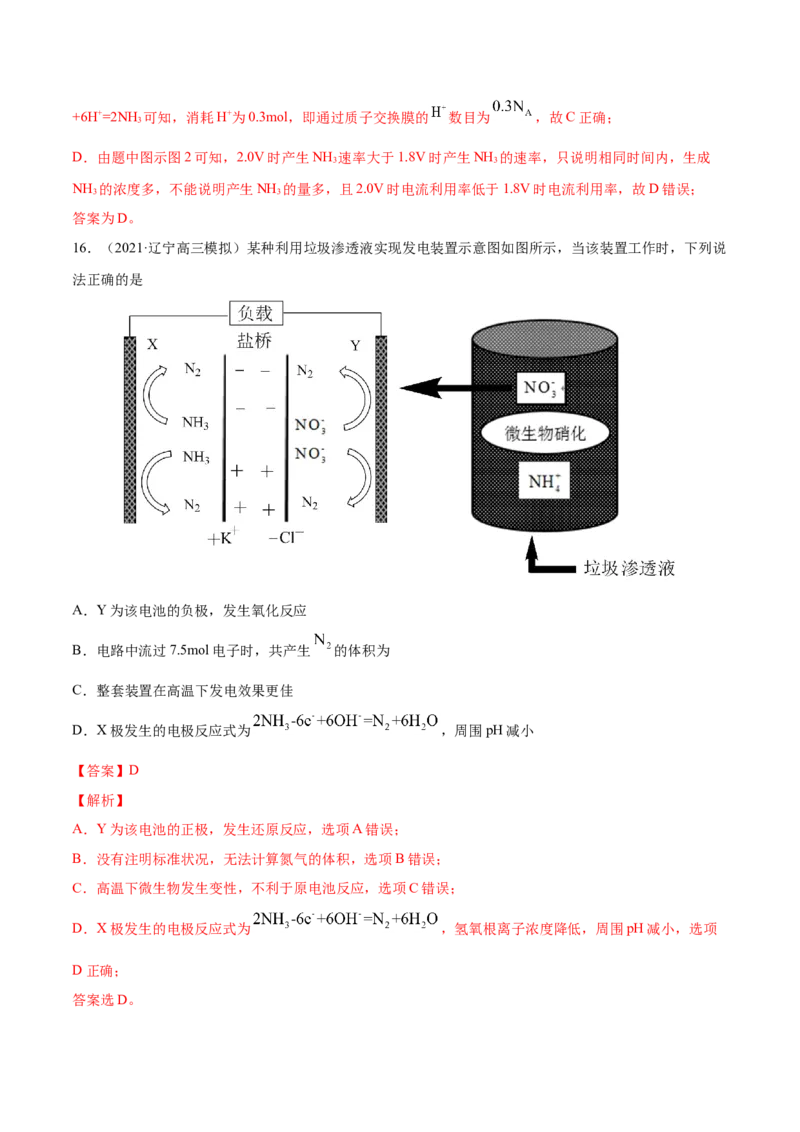
14.(2021·河南高三三模)目前,某研究团队对 基催化剂光催化还原 转化为燃料甲醇(原理如
图所示)进行研究,取得了大成果。下列说法正确的是
A.CB极的电势低于VB极的电势
B.CB极发生的反应是
C.光照下 基产生电子
D.总反应式为
【答案】C
【分析】
根据图示,VB极上水失去电子生成氧气,发生氧化反应,CB极上 得到电子生成甲醇,发生还原反应,
据此分析解答。
【解析】
A.在光照下,CB极表面聚集了由二氧化钛基转移过来的电子,因此CB极的电势高于VB极的电势,故
A错误;
B.CB极上 得到电子生成甲醇,发生还原反应,故B错误;
C.根据图示,反应过程中 在光照下产生电子,故C正确;
D.VB极上水失去电子生成氧气,发生氧化反应,CB极上 得到电子生成甲醇,发生还原反应,总反应式为 ,反应条件不是通电,故D错误;
故选C。
15.(2021·浙江高三三模)常温常压下用氮氧化铬纳米颗粒( )电催化氮气还原合成氨的工作
原理如图1所示,氨气生成速率、电流利用率与电压的关系如图2.下列说法不正确的是
A.电极 为阳极,发生氧化反应
B.该电催化装置的总反应为:2N+6H O 4NH +3O
2 2 3 2
C.当产生标准状况下 时,通过质子交换膜的 数目为
D.其他条件相同,用 电解比 电解在相同时间内产生的 多
【答案】D
【解析】
A.由题中图示图1可知,电极A中将HO O,氧元素由-2价失电子变为0价,发生氧化反应,电
2 2
极反应为2HO-4e-=O +4H+,电极A为阳极,电极B为阴极,故A正确;
2 2
B.由题中图示图1可知,电极A的电极反应为2HO-4e-=O +4H+,电极B的电极反应为N+6e-
2 2 2
+6H+=2NH,可得总反应为2N+6H O 4NH +3O ,故B正确;
3 2 2 3 2
C.当产生标准状况下 ,即n(NH )= =0.1mol,由阴极电极B的电极反应N+6e-
3 2+6H+=2NH 可知,消耗H+为0.3mol,即通过质子交换膜的 数目为 ,故C正确;
3
D.由题中图示图2可知,2.0V时产生NH 速率大于1.8V时产生NH 的速率,只说明相同时间内,生成
3 3
NH 的浓度多,不能说明产生NH 的量多,且2.0V时电流利用率低于1.8V时电流利用率,故D错误;
3 3
答案为D。
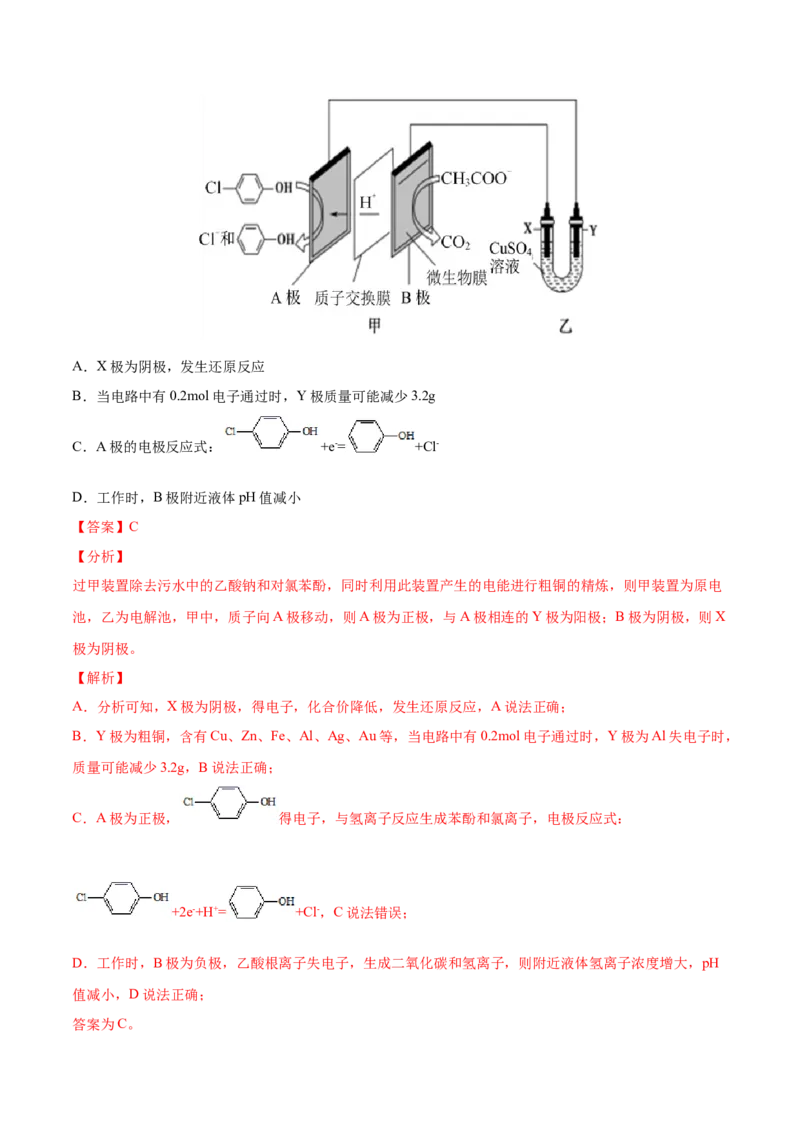
16.(2021·辽宁高三模拟)某种利用垃圾渗透液实现发电装置示意图如图所示,当该装置工作时,下列说
法正确的是
A.Y为该电池的负极,发生氧化反应
B.电路中流过7.5mol电子时,共产生 的体积为
C.整套装置在高温下发电效果更佳
D.X极发生的电极反应式为 ,周围pH减小
【答案】D
【解析】
A.Y为该电池的正极,发生还原反应,选项A错误;
B.没有注明标准状况,无法计算氮气的体积,选项B错误;
C.高温下微生物发生变性,不利于原电池反应,选项C错误;
D.X极发生的电极反应式为 ,氢氧根离子浓度降低,周围pH减小,选项
D正确;
答案选D。17.(2021·山东高三模拟)某电动汽车的锂离子电池的正极材料为层状的LiFePO 、负极材料为新型材料
4
石墨烯(Li C ),电解液为LiClO 的丙烯碳酸酯溶液,在充放电过程中,Li+在两个电极之间往返嵌入和脱出;
x 6 4
放电时,Li+从负极脱嵌,经过电解质溶液和离子交换膜嵌入正极;充电时则相反;其工作原理如图所示。
下列叙述正确的是
A.充电时,电极a与电源正极连接,电极b与电源负极连接
B.电池充电时,阳极的电极反应为LiFePO +xe−=Li FePO +xLi+
4 1-x 4
C.电池工作时,负极材料质量减少1.4g,转移0.4mol电子
D.充电时,阴极发生氧化反应,电极反应为xLi++xe−+C =Li C
6 x 6
【答案】A
【解析】
A.正极材料为层状的LiFePO ,负极材料为新型材料石墨烯(Li C ),a是正极、b是负极,故充电时,电
4 x 6
极a与电源正极连接,电极b与电源负极连接,故A正确;
B.电池充电时,a是阳极,阳极发生氧化反应,故其电极反应为LiFePO -xe−=Li FePO +xLi+,故B错误;
4 1-x 4
C.电池工作时,负极的电极反应为:LiC -xe−=xLi++C ,锂变成Li+离开负极,故材料质量减少1.4g是
x 6 6
Li+的质量,转移n(e−)=n(Li+)= =0.2mol,故C错误;
D.充电时,阴极发生还原反应,电极反应为xLi++xe−+C =Li C ,故D错误;
6 x 6
故选A。
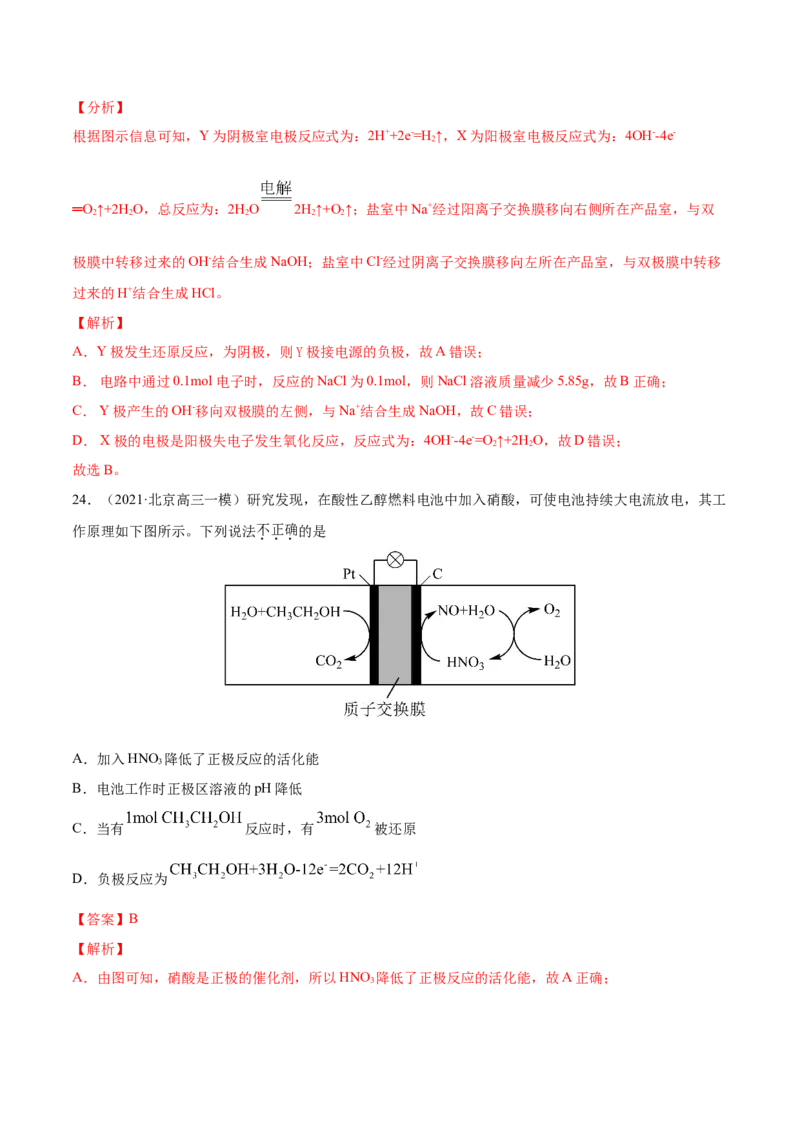
18.(2021·辽宁葫芦岛市·高三二模)如图为拟通过甲装置除去污水中的乙酸钠和对氯苯酚,同时利用此
装置产生的电能进行粗铜的精炼。下列说法不正确的是A.X极为阴极,发生还原反应
B.当电路中有0.2mol电子通过时,Y极质量可能减少3.2g
C.A极的电极反应式: +e-= +Cl-
D.工作时,B极附近液体pH值减小
【答案】C
【分析】
过甲装置除去污水中的乙酸钠和对氯苯酚,同时利用此装置产生的电能进行粗铜的精炼,则甲装置为原电
池,乙为电解池,甲中,质子向A极移动,则A极为正极,与A极相连的Y极为阳极;B极为阴极,则X
极为阴极。
【解析】
A.分析可知,X极为阴极,得电子,化合价降低,发生还原反应,A说法正确;
B.Y极为粗铜,含有Cu、Zn、Fe、Al、Ag、Au等,当电路中有0.2mol电子通过时,Y极为Al失电子时,
质量可能减少3.2g,B说法正确;
C.A极为正极, 得电子,与氢离子反应生成苯酚和氯离子,电极反应式:
+2e-+H+= +Cl-,C说法错误;
D.工作时,B极为负极,乙酸根离子失电子,生成二氧化碳和氢离子,则附近液体氢离子浓度增大,pH
值减小,D说法正确;
答案为C。19.(2021·四川成都市·石室中学高三三模)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以
触发电化学反应,该装置可有效减少碳的排放,其工作原理如图所示。下列有关说法中不正确的是
A.系统工作时,a极为电源负极,电子从a极流出
B.系统工作时,将电能转化成化学能
C.系统工作时,b极区可能会析出固体
D.系统工作时,b极区的电极反应式为2CO+2H O+2e-=2 +H
2 2 2
【答案】B
【分析】
金属Na为活泼金属,易失电子,所以d电极为负极,b电极为正极。
【解析】
A.该电池工作时,钠极(a极)为电源负极,电子从a极流出,流向b极,A描述正确;
B.由于是原电池,故系统工作时,将化学能转化成电能,B描述错误;
C.Na+移向正极,遇到 有可能形成溶解度较小的NaHCO ,故可能有固体析出,C描述正确;
3
D.由题图知b极上是CO、HO发生得电子的还原反应生成 、H,电极反应为2CO+2H O+2e-=2
2 2 2 2 2
+H ,D描述正确;
2
综上所述答案为B。
20.(2021·黑龙江哈尔滨市·哈九中高三二模)一种电化学“大气固碳”电池工作原理如图所示。该电池充
电时,通过催化剂的选择性控制,只有LiCO 发生氧化,释放出CO 和O。下列说法正确的是
2 3 2 2A.该电池放电时的正极反应为2Li-2e-+CO =LiCO
2 3
B.图中Li+的移动方向是充电时的移动方向
C.充电时阳极发生的反应为C+2LiCO-4e-=3CO+4Li+
2 3 2
D.该电池每放、充4mol电子一次,理论上能固定1molCO
2
【答案】D
【解析】
A.根据图中信息得到放电时Li为负极,电极B为正极,因此该电池放电时的正极反应为3CO+4e-+4Li
2
+=2LiCO+C,故A错误;
2 3
B.Li为负极,电极B为正极,因此图中Li+的移动方向是放电时的移动方向,故B错误;
C.根据信息电池充电时,通过催化剂的选择性控制,只有LiCO 发生氧化,释放出CO 和O,因此充电
2 3 2 2
时阳极发生的反应为2LiCO-4e-=2CO↑+4Li++O↑,故C错误;
2 3 2 2
D.根据放电正极电极反应式3CO+4e-+4Li+=2LiCO+C,充电阳极反应式2LiCO-4e-=2CO↑+
2 2 3 2 3 2
4Li++O↑,因此该电池每放、充4mol电子一次,理论上能固定1mol CO,故D正确。
2 2
综上所述,答案为D。
21.(2021·山东济宁市·高三二模)环氧乙烷是重要的有机合成原料,2020年《Science》报道科研人员研
发了一种将乙烯高效转化为环氧乙烷的电化学合成方法。反应在KCl电解液的流动池中进行,工作原理如
图。电解结束后,将阴阳极电解液输出混合,便可生成环氧乙烷。下列说法错误的是A.整个过程中,氯离子浓度一直不变
B.离子交换膜应为阴离子交换膜
C.泡沫镍电极为阳极,连接电源正极
D.当生成0.5 mol环氧乙烷时,阴极区溶液质量减少36.5 g
【答案】A
【解析】
A.根据图示可知:在反应过程中Cl-的物质的量不变,而反应会消耗水,因此整个过程中,c(Cl-)增大,A
错误;
B.阳极上Cl-失去电子发生氧化反应,2Cl--2e-=Cl↑,为维持溶液电中性,需Cl-从阴极向阳极定向移动,
2
故离子交换膜应为阴离子交换膜,B正确;
C.根据图示可知:泡沫镍电极为阳极,应该连接电源正极,C正确;
D.根据图示可知反应产生0.5 mol环氧乙烷时,需消耗0.5 mol的Cl,即消耗1 mol Cl-,阴极有1 molCl-
2
移向阳极,且2H++2e-=H ↑,生成H 0.5 mol,则溶液质量减少为35.5 g/mol×1 mol+0.5 mol×2 g/mol=36.5g,
2 2
D正确;
故合理选项是A。
22.(2021·福建南平市·高三二模)利用微生物燃料电池 处理氨氮废水原理如图。下列叙述正确的
是
A.微生物燃料电池工作时外电路的电流方向为
B. 极的电极反应式:
C.理论上参与反应的 和 的物质的量之比为
D.移去质子交换膜,可提高厌氧微生物电极的性能【答案】B
【解析】
A.根据氢离子的移动方向可判断A电极是负极,B电极是正极,则微生物燃料电池工作时外电路的电流
方向为 ,A错误;
B. 极是负极, 失去电子被氧化生成二氧化碳,电极反应式:
,B正确;
C.正极反应为2NO +10e-+12H+=N↑+6H O,根据氮原子守恒和电子得失守恒可知理论上参与反应的
2 2
和 的物质的量之比为 ,C错误;
D.移去质子交换膜后铵根离子会移向正极,在好氧微生物反应器中无法转化为硝酸根,所以不会提高厌
氧微生物电极的性能,D错误;
答案选B。
23.(2021·江西高三二模)双极膜是一种复合膜,在直流电场的作用下,复合层间的HO解离成H+和
2
OH-,并实现定向移动。该技术对淡水缺乏的地区有重大的意义,下图利用双极膜组合电解法模拟海水淡
化,下列说法正确的是
A.Y极接电源的正极
B.电路中通过0.1mol电子时,则NaCl溶液质量减少5.85g
C.OH-移向双极膜的右侧
D.X极的电极反应式为:4OH-+4e-=O ↑+2H O
2 2
【答案】B【分析】
根据图示信息可知,Y为阴极室电极反应式为:2H++2e-=H ↑,X为阳极室电极反应式为:4OH--4e-
2
═O ↑+2H O,总反应为:2HO 2H↑+O ↑;盐室中Na+经过阳离子交换膜移向右侧所在产品室,与双
2 2 2 2 2
极膜中转移过来的OH-结合生成NaOH;盐室中Cl-经过阴离子交换膜移向左所在产品室,与双极膜中转移
过来的H+结合生成HCl。
【解析】
A.Y极发生还原反应,为阴极,则Y极接电源的负极,故A错误;
B. 电路中通过0.1mol电子时,反应的NaCl为0.1mol,则NaCl溶液质量减少5.85g,故B正确;
C. Y极产生的OH-移向双极膜的左侧,与Na+结合生成NaOH,故C错误;
D. X极的电极是阳极失电子发生氧化反应,反应式为:4OH--4e-=O ↑+2H O,故D错误;
2 2
故选B。
24.(2021·北京高三一模)研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,其工
作原理如下图所示。下列说法不正确的是
A.加入HNO 降低了正极反应的活化能
3
B.电池工作时正极区溶液的pH降低
C.当有 反应时,有 被还原
D.负极反应为
【答案】B
【解析】
A.由图可知,硝酸是正极的催化剂,所以HNO 降低了正极反应的活化能,故A正确;
3B.电池工作时正极区的总反应为 ,氢离子浓度减小,溶液的pH升高,故B错
误;
C.1mol氧气得4mol电子,当有 被完全氧化为二氧化碳时转移12mol电子,根据电子
守恒,有 被还原,故C正确;
D.乙醇在负极失电子生成二氧化碳,负极反应为 ,故D正确;
选B。
25.(2021·山东日照市·高三三模)包覆纳米硅复合材料(GS-Si)的可充电石墨烯电池工作原理如图所示。
放电时,GS-Si包覆石墨烯电极上的物质变化为:C Li→C Li ;多元含锂过渡金属氧化物电极上的物质变
6 6 1-x
化为:Li MO →LiMO ,下列说法错误的是
1-x 2 2
A.放电时,胶状聚合物电解质和固体电解质的作用均为传导离子,构成闭合回路
B.若放电前两个电极质量相等,转移0.1mol电子后两个电极质量相差0.7g
C.充电时,与正极连接的电极反应为LiMO -xe-=Li MO +xLi+
2 l-x 2
D.为保护电池,GS-Si包覆石墨烯的电极反应不能进行至C Li-e-=C +Li+
6 6
【答案】B
【分析】
结合题意可知放电时,GS-Si包覆石墨烯电极上发生的反应为C Li-xe-=C Li +xLi+;多元含锂过渡金属氧
6 6 1-x
化物电极上的反应为xLi++xe-+Li MO =LiMO ,因此GS-Si包覆石墨烯电极为电池的负极,多元含锂过渡
1-x 2 2
金属氧化物电极为正极。
【解析】
A.放电时,电池内电路由胶状聚合物电解质、隔膜、固体电解质构成,放电时,胶状聚合物电解质和固
体电解质的作用均为传导Li+,构成闭合回路,A正确;B.由电极反应可知,放电时,转移0.1mol电子后,负极材料减少0.1molLi+,正极材料增加0.1molLi+,因
此转移0.1mol电子后两个电极质量相差0.1mol×2×7g/mol=1.4g,B错误;
C.放电时,正极反应式为xLi++xe-+Li MO =LiMO ,则充电时,与正极连接的电极反应式为LiMO -xe-
1-x 2 2 2
=Li MO +xLi+,C正确;
l-x 2
D.若GS-Si包覆石墨烯的电极反应进行至C Li-e-=C +Li+,石墨烯电极会被氧化,损伤电极,因此为保护
6 6
电池,GS-Si包覆石墨烯的电极反应不能进行至C Li-e-=C +Li+,D正确;
6 6
答案选B。
26.(2021·广东汕头市·高三二模)2021年3月5日,李克强总理在国务院政府报告中指出,扎实做好碳
达峰、碳中和各项工作。科研工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO 转化为
2
CO,实现节能减排的目标。如图所示,下列有关说法正确的是
A.N极为阴极
B.离子交换膜为阴离子交换膜
C.阳极的电极反应式为CO+2e-+2H+=CO+H O
2 2
D.理论上该装置在工作时,HPO 与KH PO 缓冲溶液的pH保持不变
3 4 2 4
【答案】D
【分析】
由图示知,该装置外电路有光伏电池(将太阳能转化为电能),故为电解池装置,在P极上,CO 得电子
2
转化为CO,故P极为阴极,N极为阳极,阴极电极反应为:CO+2H++2e-=CO+H O,需要缓冲溶液提供
2 2
H+,故离子交换膜为阳离子交换膜,阳极电极反应为:2HO-4e-=O ↑+4H+。
2 2
【解析】
A.由分析知,N极为阳极,A错误;
B.由分析知,离子交换膜为阳离子交换膜,B错误;
C.由分子知,CO 在阴极转化为CO,故选项所写电极反应为阴极电极反应,C错误;
2
D.根据得失电子守恒和阴阳极电极反应知,缓冲溶液流入阴极的H+和阳极流入缓冲溶液的H+数目相等,故缓冲溶液中c(H+)保持不变,故pH保持不变,D正确;
故答案选D。
27.(2021·陕西西安市·高三二模)对氨基苯甲酸( )是一种用途广泛的化工产品和医药中
间体,以对硝基苯甲酸( )为原料,采用电解法合成对氨基苯甲酸的装置如图。下列说法中
不正确的是
A.铅合金与电源负极相连
B.阴极的主要电极反应式为 +6e-+6H+→ +2H O
2
C.每转移1 mole-时,阳极电解质溶液的质量减少9 g
D.反应一段时间后阳极区pH不变
【答案】D
【分析】
该装置为电解池,右侧生成氧气,则右侧为阳极,电极反应式为 ,左侧为阴极,
据此分析解答。
【解析】
A. 该电解池右侧为阳极,则左侧为阴极,铅合金与电源负极相连,选项A正确;
B. 阴极得电子发生还原反应生成氨基苯甲酸,则阴极的主要电极反应式为 +6e-
+6H+→ +2H O,选项B正确;
2
C. 阳极发生反应 ,氢离子移动向阴极,当转移4mole-时,阳极电解质溶液减少
2mol水,则每转移1mole-时,阳极电解质溶液减少0.5mol水,质量为9g,选项C正确;D. 阳极发生反应 ,氢离子移动向阴极,则反应结束后阳极区硫酸浓度会增大,pH
减小,选项D错误;
答案选D。
28.(2021·河北石家庄市·高三二模)我国科学家报道了如图所示的可充电Na—Zn双离子电池体系。下列
说法正确的是
A.充电时,a为电源正极
B.充电时,Na+从正极中脱出进入溶液
C.放电时,负极附近溶液的碱性增强
D.放电时,正极反应式为Na MnO +xe-=Na MnO +xNa+
0.6 2 0.6-x 2
【答案】B
【分析】
根据图象信息可知,放电时,Zn失电子,与氢氧根离子反应生成[Zn(OH) ]2-,作负极;正极上,Mn化合
4
价降低,得电子,由Na MnO 变为Na MnO ;做电解池时与原电池相反,[Zn(OH) ]2-得电子生成Zn,
0.6-x 2 0.6 2 4
则a极为负极。
【解析】
A.由分析可知,充电时,a为电源负极,A说法错误;
B.充电时为电解池,此时的阳极(即放电时的正极)电极反应式为:Na MnO +xe-=Na MnO +xNa+,
0.6 2 0.6-x 2
Na+从电极上脱出进入溶液,B说法正确;
C.放电时,负极Zn失电子,与氢氧根离子反应生成[Zn(OH) ]2-,则负极附近溶液的碱性减弱,C说法错
4
误;
D.放电时,正极得电子,Mn的化合价降低,反应式为Na MnO +xNa++xe-= Na MnO ,D说法错误;
0.6-x 2 0.6 2
答案为B。
29.(2021·河南郑州市·高三三模)中国科学院唐永炳团队设计的新型铝一石墨双离子电池,工作原理如图,其放、充电的反应为:AlLi+C (PF ) LiPF +xC+Al,下列说法正确的是
x 6 6
A.放电时锂离子向负极移动
B.充电时阳极反应为Al-3e-=Al3+
C.该电池负极和正极的铝均未参与电极放电
D.该电池可用LiPF 水溶液做电解质溶液
6
【答案】C
【分析】
该电池反应为:AlLi+C (PF ) LiPF +xC+Al,放电时AlLi/Al电极为负极,失电子,石墨电极为正极,得
x 6 6
电子;放电时AlLi/Al电极为阴极,得电子,石墨电极为阳极,失电子。
【解析】
A.放电时阳离子向正极移动,锂离子向正极移动,A错误;
B.根据总反应AlLi+C (PF ) LiPF +xC+Al可知充电时阳极反应为: +xC-e-= C (PF ),B错误;
x 6 6 x 6
C.该电池负极和正极的铝均未参与电极放电,化合价始终为0,C正确;
D.因为AlLi合金中的Li常温下会与水反应,该电池不可用LiPF 水溶液做电解质溶液,D错误;
6
答案选C。
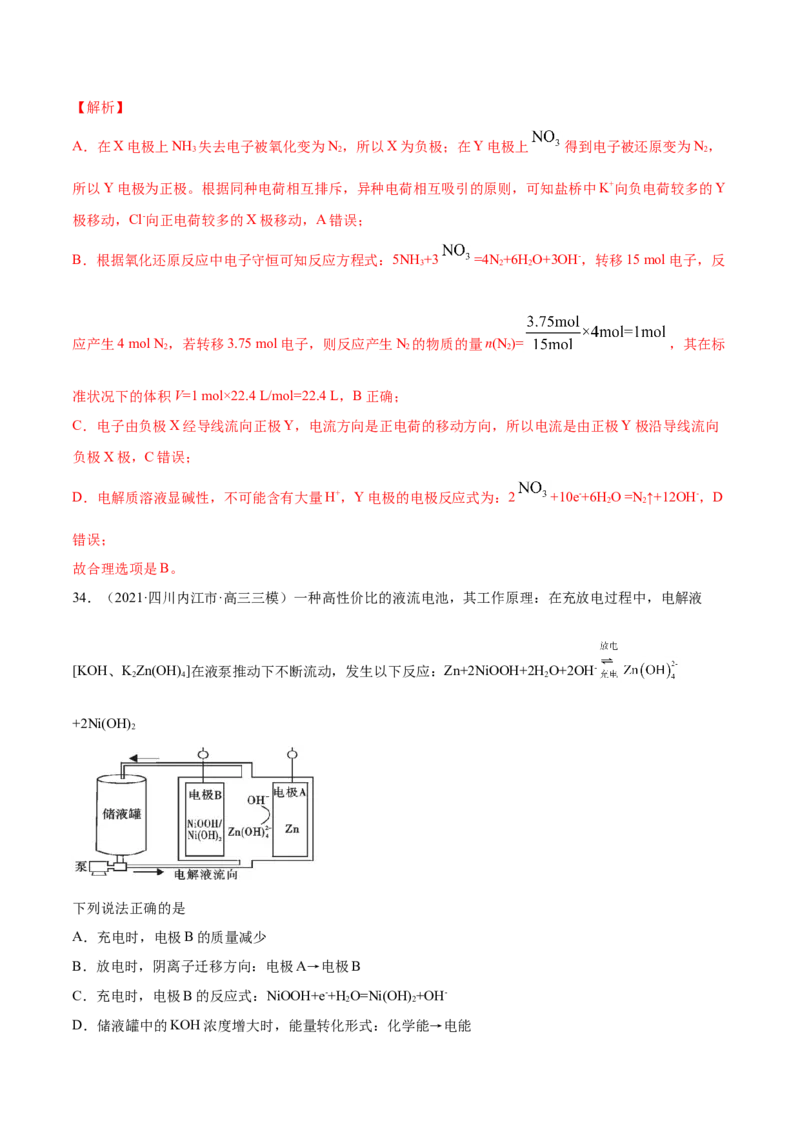
30.(2021·浙江杭州市·高三三模)某课外研究小组设计了一款可充电电池,在两惰性电极(多孔碳棒)上加
装两个玻璃罩,装置如图所示。先关闭K,打开K,工作一段时间后,再打开K,关闭K。下列说法不
1 2 1 2
正确的是A.打开K,关闭K 时,Na+向B极迁移
1 2
B.该装置电解过程总反应方程式为:2HO 2H+O
2 2 2
C.电极A发生还原反应过程中,A区域碱性增强
D.关闭K,打开K,转移2mol电子,左池增重44g
1 2
【答案】B
【解析】A.打开K,关闭K 时,形成氢氧燃料电池,A极是充满氢气负极,B极是充满氧气的正极,电
1 2
解质里的阳离子向电池的阳极移动,即 Na+向B极迁移,A项正确;
B.该装置电解过程总反应方程式为: ,B项错误;
C.电极A发生还原反应过程中,反应的电极方程式为:2HO+2e-=2OH-+H ↑,即A区域碱性增强,C项
2 2
正确;
D.关闭K,打开K,形成电解池,A极阴极,B极是阳极,Na+向A极移动,A极电极方程式为:
1 2
2HO+2e-=2OH-+H ↑,当转移2mol电子时,Na+也转移了2mol,即增重的质量为46g,但同时有1mol氢
2 2
气产生,即2g氢气,所以左池增重44g,D项正确;
答案选B。
31.(2021·四川绵阳市·高三三模)我国电动汽车产业发展迅猛,多种车型采用三元锂电池,该电池放电
时工作原理如图所示。下列说法错误的是A.无论充电或放电,A极电势均低于B极
B.充电时,外电路中流过0.1mol电子,A极质量减少0.7g
C.放电时,正极反应为Li Ni Co MnO+aLi++ae-=LiNi Co MnO
1-a x y z 2 x y z 2
D.失去活性锂元素的三元正极材料可采用化学方法再生,实现循环利用
【答案】B
【解析】
A.该电池放电时工作原理可知,放电时,A为负极B为正极,充电时,A为阴极B为阳极,故无论充电
或放电,A极电势均低于B极,故A正确;
B.充电时,A极电极反应为aLi++ae-+6C=LiC , 外电路中流过0.1mol电子,A极质量增加0.7g,故B错
a 6
误;
C.由该电池放电时工作原理可知,放电时B为正极,Li Ni Co MnO 得电子结合Li+生成
1- a x y z 2
LiNiCo MnO,正极反应为Li Ni Co MnO+aLi++ae-=LiNi Co MnO,故C正确;
x y z 2 1-a x y z 2 x y z 2
D.锂元素失去活性后,可采用化学方法再生,从而实现Li的循环利用,故D正确;
故选 B。
32.(2021·四川成都市·高三三模)锂空气电池因其比能量非常高,具有广阔应用前景。下图是两种不同
的锂空气(Li-O )电池,下列分析错误的是
2
A.放电时图1中电流从a电极经电解液流回b电极
B.放电时,两种电池负极反应式均为:Li-e-=Li+C.转移相同电子,两种电池正极产物的物质的量相同
D.两种不同的锂空气电池比能量不同
【答案】C
【分析】
根据化合价的变化判断电池的正负极,根据化合价的升降、电荷守恒及电解液进行书写电极反应。
【解析】
A.放电时,根据图1右侧充入的氧气判断,b为正极,a为负极,则电流从a电极经电解液流回b电极,
故A正确;
B.放电时,图1和图2中负极都为Li,根据电解质液传导离子判断,传导离子为锂离子,故电极反应为:
Li-e-=Li+,故B正确;
C.图1中正极反应为:O+2e-+2Li+=Li O,图2中正极反应为:O+4e-+2H O=4OH-,根据电子数相同判断
2 2 2 2 2
正极产物的物质的量不同,故C不正确;
D.比能量是指电池单位质量或单位体积所能输出的电能,根据正极氧气的化合价变化不同判断比能量不
同,故D正确;
故答案选C。
33.(2021·山东滨州市·高三二模)科学家利用垃圾渗透液研发出新型环保电池,实现发电、环保二位一
体化结合的装置如图。
当该装置工作时,下列说法正确的是
A.盐桥中K+向X极移动,Cl-向Y极移动
B.电路中流过3.75 mol电子时,产生N 的体积为22.4 L(标准状况)
2
C.电流由X极沿导线流向Y极
D.Y极反应式为2 +10e-+12H+=N ↑+6H O
2 2
【答案】B【解析】
A.在X电极上NH 失去电子被氧化变为N,所以X为负极;在Y电极上 得到电子被还原变为N,
3 2 2
所以Y电极为正极。根据同种电荷相互排斥,异种电荷相互吸引的原则,可知盐桥中K+向负电荷较多的Y
极移动,Cl-向正电荷较多的X极移动,A错误;
B.根据氧化还原反应中电子守恒可知反应方程式:5NH +3 =4N +6H O+3OH-,转移15 mol电子,反
3 2 2
应产生4 mol N ,若转移3.75 mol电子,则反应产生N 的物质的量n(N )= ,其在标
2 2 2
准状况下的体积V=1 mol×22.4 L/mol=22.4 L,B正确;
C.电子由负极X经导线流向正极Y,电流方向是正电荷的移动方向,所以电流是由正极Y极沿导线流向
负极X极,C错误;
D.电解质溶液显碱性,不可能含有大量H+,Y电极的电极反应式为:2 +10e-+6H O =N ↑+12OH-,D
2 2
错误;
故合理选项是B。
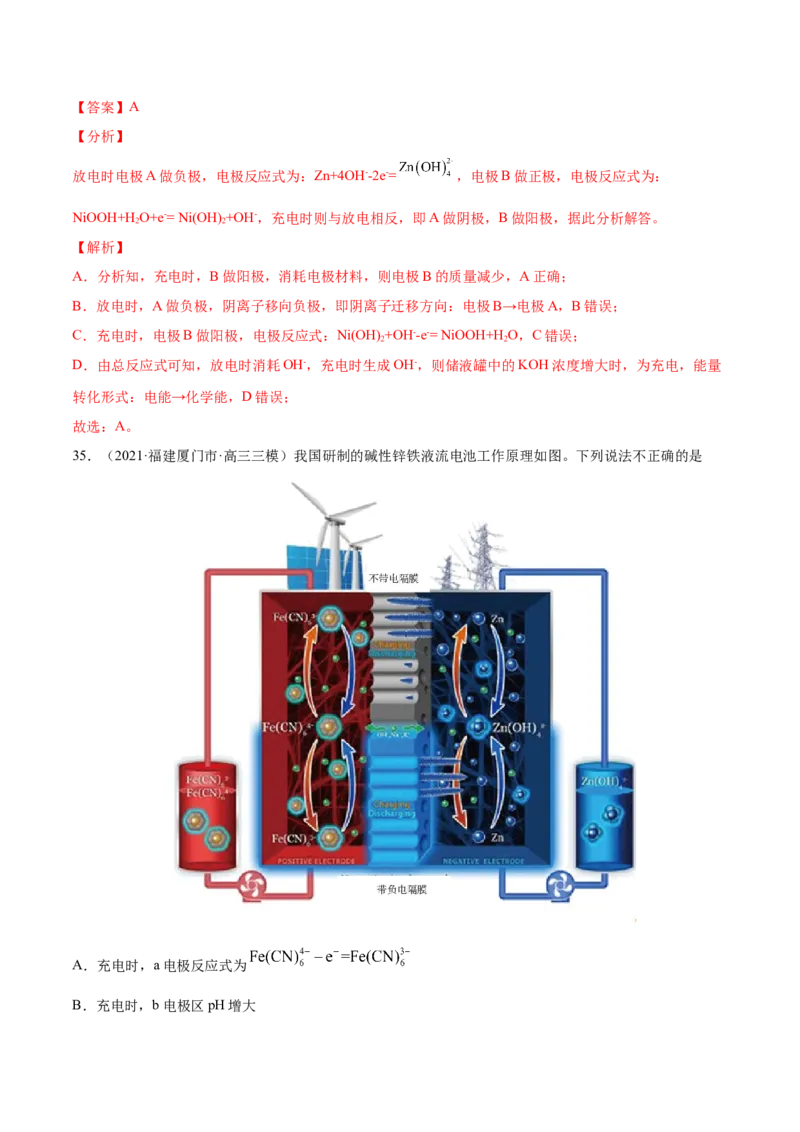
34.(2021·四川内江市·高三三模)一种高性价比的液流电池,其工作原理:在充放电过程中,电解液
[KOH、KZn(OH) ]在液泵推动下不断流动,发生以下反应:Zn+2NiOOH+2HO+2OH-
2 4 2
+2Ni(OH)
2
下列说法正确的是
A.充电时,电极B的质量减少
B.放电时,阴离子迁移方向:电极A→电极B
C.充电时,电极B的反应式:NiOOH+e-+H O=Ni(OH) +OH-
2 2
D.储液罐中的KOH浓度增大时,能量转化形式:化学能→电能【答案】A
【分析】
放电时电极A做负极,电极反应式为:Zn+4OH--2e-= ,电极B做正极,电极反应式为:
NiOOH+H O+e-= Ni(OH) +OH-,充电时则与放电相反,即A做阴极,B做阳极,据此分析解答。
2 2
【解析】
A.分析知,充电时,B做阳极,消耗电极材料,则电极B的质量减少,A正确;
B.放电时,A做负极,阴离子移向负极,即阴离子迁移方向:电极B→电极A,B错误;
C.充电时,电极B做阳极,电极反应式:Ni(OH) +OH--e-= NiOOH+HO,C错误;
2 2
D.由总反应式可知,放电时消耗OH-,充电时生成OH-,则储液罐中的KOH浓度增大时,为充电,能量
转化形式:电能→化学能,D错误;
故选:A。
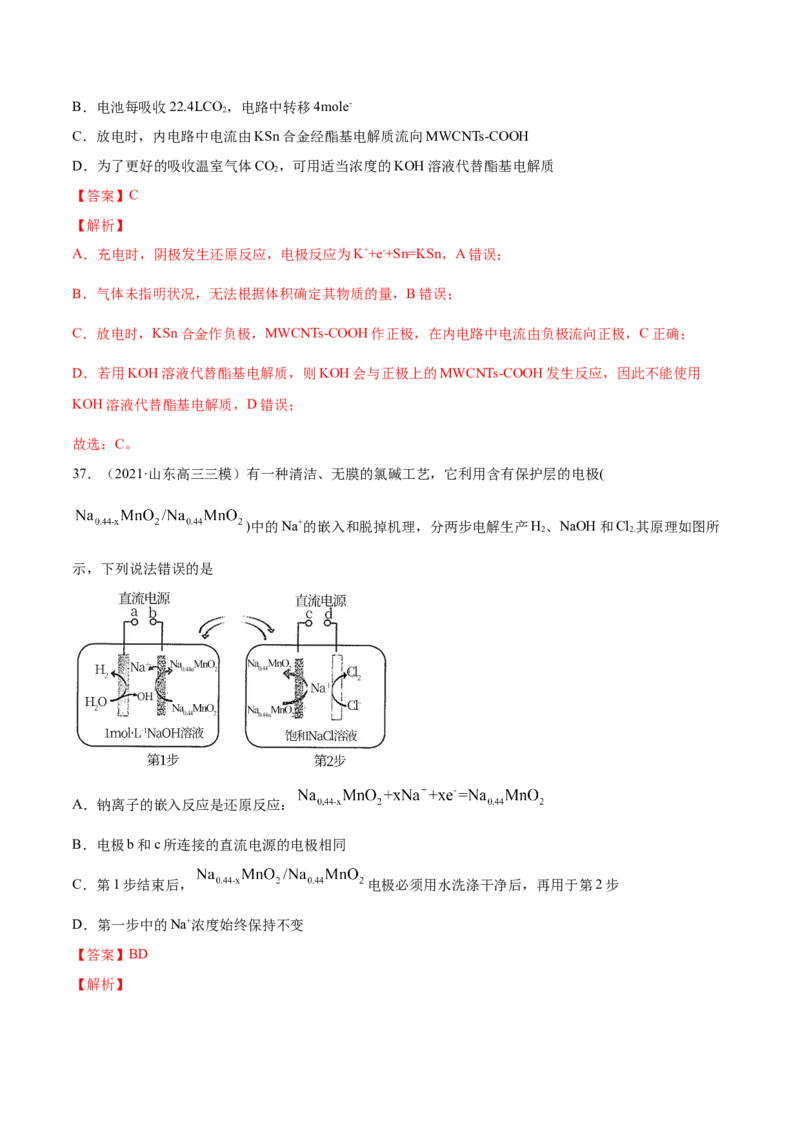
35.(2021·福建厦门市·高三三模)我国研制的碱性锌铁液流电池工作原理如图。下列说法不正确的是
A.充电时,a电极反应式为
B.充电时,b电极区pH增大C.理论上,每消耗6.5gZn,溶液中将增加0.1
D.采用带负电隔膜可减少充电时产生锌枝晶破坏隔膜
【答案】C
【分析】
Zn为活泼金属,所以放电时b电极为负极,发生氧化反应:Zn-2e-+4OH-=Zn(OH) ,a电极为正极发生还
原反应:Fe(CN) +e-=Fe(CN) ;则充电时a为阳极发生氧化反应,b为阴极发生还原反应。
【解析】
A.充电时,a为阳极发生氧化反应,电极反应为Fe(CN) -e-=Fe(CN) ,A正确;
B.充电时,b为阴极发生还原反应:Zn(OH) +2e-= Zn+4OH-,生成氢氧根,所以pH增大,B正确;
C.6.5gZn的物质的量为0.1mol,根据电极方程式可知此时转移0.2mol电子,生成0.2mol Fe(CN) ,C错
误;
D.带负电隔膜对Zn(OH) 离子有排斥作用,可实现碱性锌铁液流电池在充电过程中锌的沉积方向由沿离
子传导膜向沿电极侧转变,避免了锌枝晶对隔膜造成破坏,D正确;
答案为C。
36.(2021·福建高三模拟)近日,南开大学科研团队以KSn合金为负极,以含羧基多壁碳纳米管
(MWCNTs-COOH)为正极催化剂构建了可充电K-CO 电池(如图所示),电池反应为
2
4KSn+3CO 2KCO+C+4Sn,其中生成的KCO 附着在正极上。该成果对改善环境和缓解能源问题具有巨
2 2 3 2 3
大潜力。下列⇌说法正确的是
A.充电时,阴极反应为2KCO+C-4e-=4K++3CO ↑
2 3 2B.电池每吸收22.4LCO ,电路中转移4mole-
2
C.放电时,内电路中电流由KSn合金经酯基电解质流向MWCNTs-COOH
D.为了更好的吸收温室气体CO,可用适当浓度的KOH溶液代替酯基电解质
2
【答案】C
【解析】
A.充电时,阴极发生还原反应,电极反应为K++e-+Sn=KSn,A错误;
B.气体未指明状况,无法根据体积确定其物质的量,B错误;
C.放电时,KSn合金作负极,MWCNTs-COOH作正极,在内电路中电流由负极流向正极,C正确;
D.若用KOH溶液代替酯基电解质,则KOH会与正极上的MWCNTs-COOH发生反应,因此不能使用
KOH溶液代替酯基电解质,D错误;
故选:C。
37.(2021·山东高三三模)有一种清洁、无膜的氯碱工艺,它利用含有保护层的电极(
)中的Na+的嵌入和脱掉机理,分两步电解生产H、NaOH和Cl 其原理如图所
2 2.
示,下列说法错误的是
A.钠离子的嵌入反应是还原反应:
B.电极b和c所连接的直流电源的电极相同
C.第1步结束后, 电极必须用水洗涤干净后,再用于第2步
D.第一步中的Na+浓度始终保持不变
【答案】BD
【解析】A.钠离子的嵌入反应: ,得电子的反应是还原反应,故A正确;
B.第一步中,b电极发生Na+脱掉的反应,属于失去电子的氧化反应,作阳极,连接电源的正极,第二步
中,c电极发生Na+嵌入的反应,属于得电子的还原反应,作阴极,连接电源的正极,故B错误;
C.第1步结束后, 电极必须用水洗涤干净后,除去OH-,再用于第2步,防
止生成的氯气与之反应,故C正确;
D.如图所示,第一步中发生Na+脱掉的反应,所以Na+浓度增大,故D错误。
故选BD。
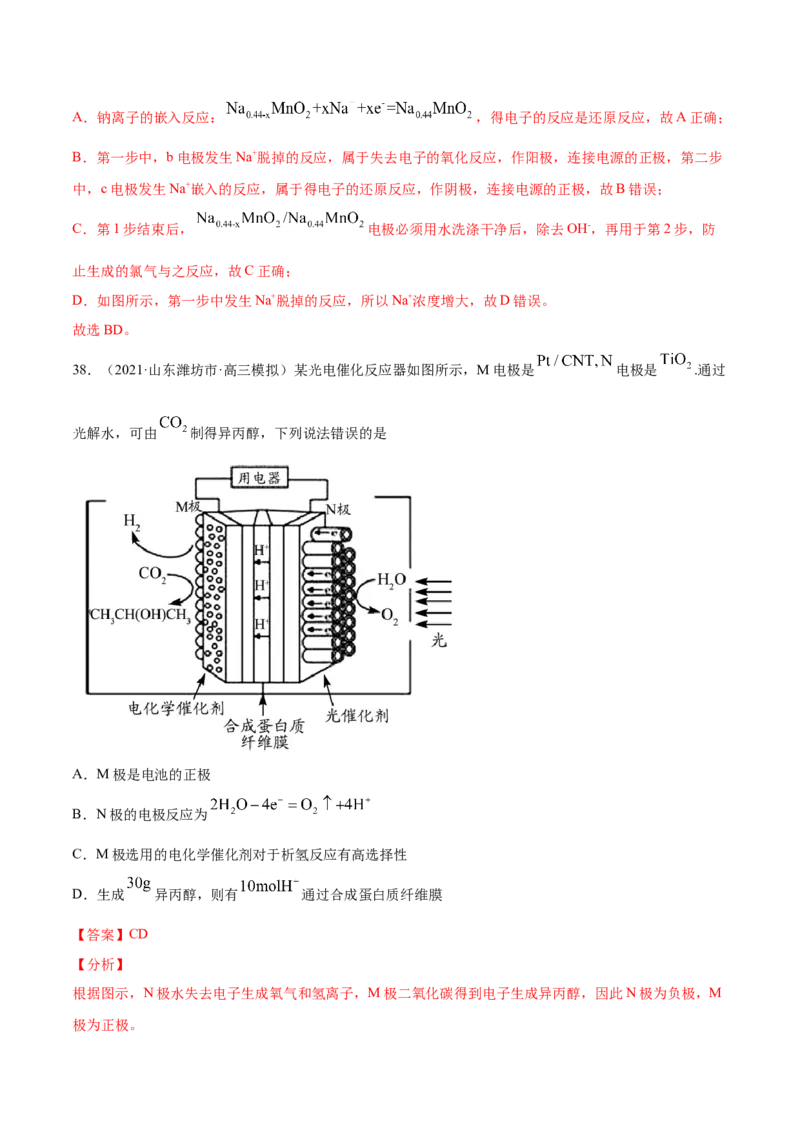
38.(2021·山东潍坊市·高三模拟)某光电催化反应器如图所示,M电极是 电极是 .通过
光解水,可由 制得异丙醇,下列说法错误的是
A.M极是电池的正极
B.N极的电极反应为
C.M极选用的电化学催化剂对于析氢反应有高选择性
D.生成 异丙醇,则有 通过合成蛋白质纤维膜
【答案】CD
【分析】
根据图示,N极水失去电子生成氧气和氢离子,M极二氧化碳得到电子生成异丙醇,因此N极为负极,M
极为正极。【解析】
A.根据上述分析可知,M极是电池的正极,故A正确;
B.N极上水失去电子生成氧气和氢离子,电极反应式为2HO-4e-=O ↑+4H+,故B正确;
2 2
C.M的选用高活性和高选择性的电化学催化剂能促进异丙醇的生成,有效抑制析氢反应,故C错误;
D.30g异丙醇的物质的量为0.5mol,M极的电极反应式为3CO+18H++18e-=CH CH(OH)CH +5H O,C元
2 3 3 2
素化合价由+4降低至-2,因此转移电子为0.5mol×3×6=9mol,若同时无析氢反应,则有9mol H+通过合成蛋
白质纤维膜,若同时有析氢反应,则通过合成蛋白质纤维膜的H+的物质的量大于9mol,故D错误;
故答案为CD。
39.(2021·山东济南市·高三二模)用质子导体固体氧化物燃料电池(P—SOFC)脱氢可得丙烯,可实现“烯
烃—电力”联产。
下列说法正确的是
A.催化剂促进电能转变为化学能
B.O2-由负极迁移至正极
C.负极上发生的电极反应为C H-2e-=C H+2H+
3 8 3 6
D.电池总反应为2C H+O =2C H+2H O
3 8 2 3 6 2
【答案】CD
【解析】
A.该装置为燃料电池,则催化剂能促进化学能转变为电能,A错误;
B.O 作正极,得电子后形成O2-,O2-带负电荷,会在正极上与H+结合形成HO,B错误;
2 2
C.通入燃料C H 的电极为负极,在负极上C H 失去电子变为C H,故负极的电极反应式为:C H-2e-
3 8 3 8 3 6 3 8
=C H+2H+,C正确;
3 6
D.在电池的正极上O 得到电子变为O2-,然后再与H+结合形成HO,故正极的电极反应式为O+4e-
2 2 2
+4H+=2H O。负极电极反应式为:C H-2e-=C H+2H+。由于同一闭合回路中电子转移数目相等,所以将正
2 3 8 3 6
极、负极电极反应式叠加,可得总反应方程式为:2C H+O =2C H+2H O,D正确;
3 8 2 3 6 2
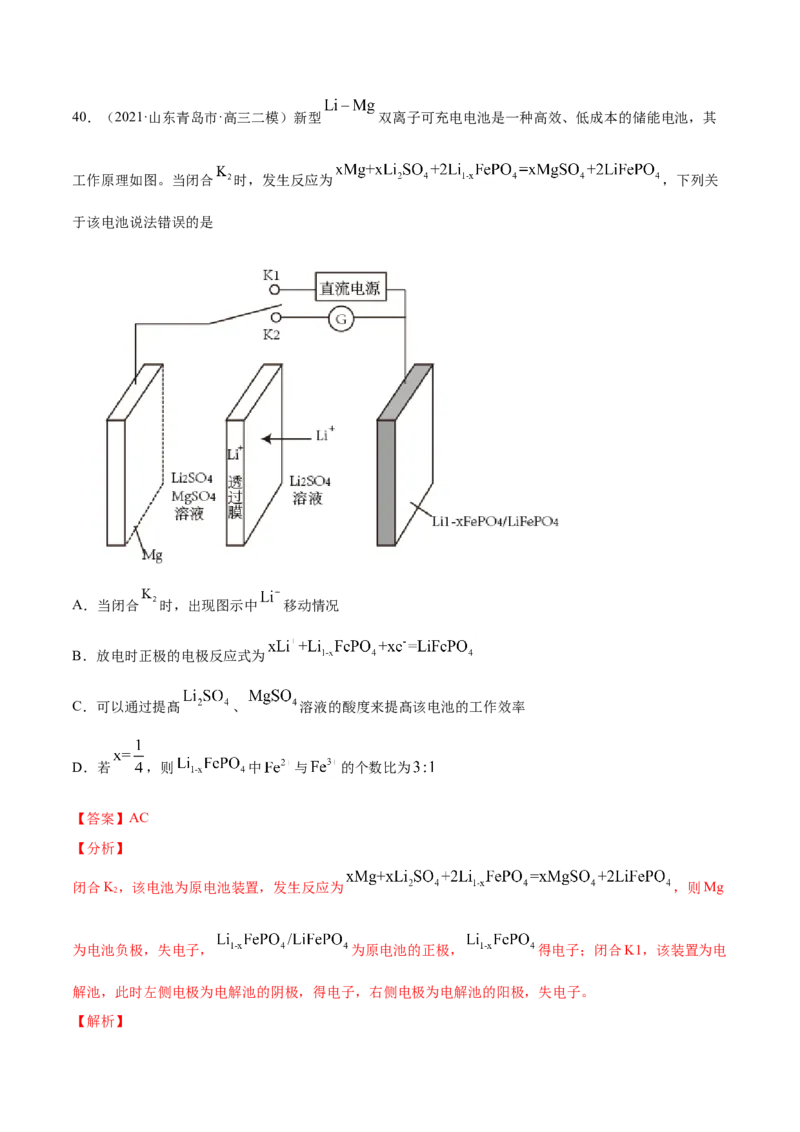
故合理选项是CD。40.(2021·山东青岛市·高三二模)新型 双离子可充电电池是一种高效、低成本的储能电池,其
工作原理如图。当闭合 时,发生反应为 ,下列关
于该电池说法错误的是
A.当闭合 时,出现图示中 移动情况
B.放电时正极的电极反应式为
C.可以通过提髙 、 溶液的酸度来提髙该电池的工作效率
D.若 ,则 中 与 的个数比为
【答案】AC
【分析】
闭合K,该电池为原电池装置,发生反应为 ,则Mg
2
为电池负极,失电子, 为原电池的正极, 得电子;闭合K1,该装置为电
解池,此时左侧电极为电解池的阴极,得电子,右侧电极为电解池的阳极,失电子。
【解析】A.当闭合 时,该装置为原电池, 移向电解池正极,根据分析可知, 电极为
原电池正极,所以不会出现图示中 移动情况,A错误;
B.放电时正极为 生成 ,所以电极反应式为: ,B
正确;
C.若提髙 、 溶液的酸度,Mg电极在断路时仍会自发的与电解质溶液反应从而造成损失,
从而降低了该电池的工作效率,C错误;
D.若 ,则该物质为 ,根据化合价代数和为零可知该物质中Fe的化合价为2.25,则
与 的个数比为 ,D正确;
答案选:AC。