文档内容
专题 08 非金属及其化合物
2021年化学高考题
一、单选题
1.(2021·广东高考真题)劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 社区服务:用84消毒液对图书馆桌椅消毒 含氯消毒剂具有氧化性
厨余垃圾含N、P、K等元
B 学农活动:用厨余垃圾制肥料
素
C 家务劳动:用白醋清洗水壶中的水垢 乙酸可由乙醇氧化制备
D 自主探究:以油脂为原料制肥皂 油脂可发生皂化反应
A.A B.B C.C D.D
2.(2021·河北高考真题)关于非金属含氧酸及其盐的性质,下列说法正确的是
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
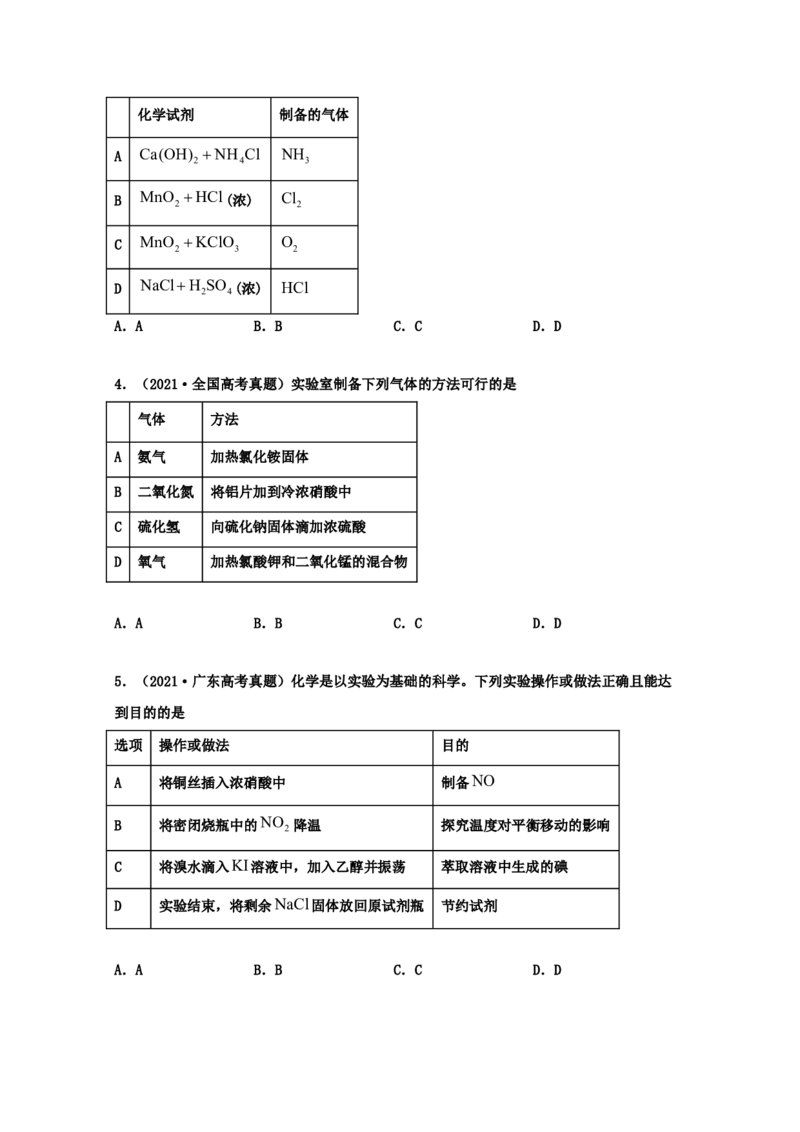
3.(2021·全国高考真题)在实验室采用如图装置制备气体,合理的是化学试剂 制备的气体
A Ca(OH) NH Cl NH
2 4 3
B MnO HCl(浓) Cl
2 2
C MnO KClO O
2 3 2
D NaClH SO (浓) HCl
2 4
A.A B.B C.C D.D
4.(2021·全国高考真题)实验室制备下列气体的方法可行的是
气体 方法
A 氨气 加热氯化铵固体
B 二氧化氮 将铝片加到冷浓硝酸中
C 硫化氢 向硫化钠固体滴加浓硫酸
D 氧气 加热氯酸钾和二氧化锰的混合物
A.A B.B C.C D.D
5.(2021·广东高考真题)化学是以实验为基础的科学。下列实验操作或做法正确且能达
到目的的是
选项 操作或做法 目的
A 将铜丝插入浓硝酸中 制备NO
B 将密闭烧瓶中的NO 降温 探究温度对平衡移动的影响
2
C 将溴水滴入KI溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余NaCl固体放回原试剂瓶 节约试剂
A.A B.B C.C D.D6.(2021·河北高考真题)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化
物和氮氧化物造成的环境问题也日益受到关注,下列说法正确的是
A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2
B.汽车尾气中的主要大气污染物为NO、SO 和PM2.5
2
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
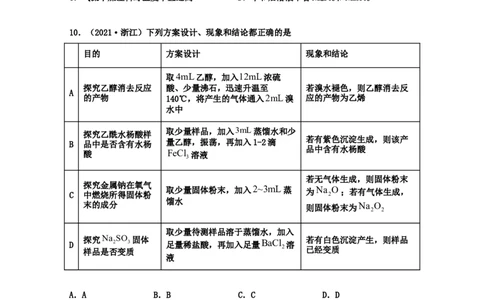
7.(2021·浙江高考真题)下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
检验某无色溶 若溶液变黄色且试管上
液中是否含有 取少量该溶液于试管中,加稀盐酸酸化,再 部产生红棕色气体,则
A
NO 加入FeCl 2 溶液 该溶液中含有NO
2 2
探究KI与 取5 mL 0.1 mol·L-1KI溶液于试管中,加 若溶液变血红色,则KI
B FeCl 反应的限 入1 mL 0.1 mol·L-1 FeCl 溶液,充分反应 与FeCl 的反应有一定限
3 3 3
度 后滴入5滴15% KSCN溶液 度
取2 mL卤代烃样品于试管中,加入5 mL 若产生的沉淀为白色,
判断某卤代烃
C 20% KOH水溶液混合后加热,再滴加AgNO 则该卤代烃中含有氯元
中的卤素 3
溶液 素
探究蔗糖在酸 取2mL20%的蔗糖溶液于试管中,加入适量稀 若没有生成砖红色沉淀
D 性水溶液中的 HSO 后水浴加热5 min;再加入适量新制 ,则蔗糖在酸性水溶液
2 4
稳定性 Cu(OH) 悬浊液并加热 中稳定
2
A.A B.B C.C D.D
8.(2021·浙江高考真题)下列说法不正确的是
A.某些胶态金属氧化物分散于玻璃中可制造有色玻璃
B.通常以海水提取粗食盐后的母液为原料制取溴
C.生物炼铜中通常利用某些细菌把不溶性的硫化铜转化为可溶性铜盐
D.工业制备硝酸的主要设备为沸腾炉、接触室和吸收塔
9.(2021·山东高考真题)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下
2 3
列说法错误的是A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高 D.中和后溶液中含NaSO 和NaHCO
2 3 3
10.(2021·浙江)下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
取4mL乙醇,加入12mL浓硫
探究乙醇消去反应 酸、少量沸石,迅速升温至 若溴水褪色,则乙醇消去反
A
的产物 140℃,将产生的气体通入2mL溴 应的产物为乙烯
水中
取少量样品,加入3mL蒸馏水和少
探究乙酰水杨酸样
若有紫色沉淀生成,则该产
B 品中是否含有水杨 量乙醇,振荡,再加入1-2滴
品中含有水杨酸
酸 FeCl 溶液
3
若无气体生成,则固体粉末
探究金属钠在氧气
取少量固体粉末,加入2~3mL蒸 为Na O;若有气体生成,
C 中燃烧所得固体粉 2
馏水
末的成分 则固体粉末为Na O
2 2
取少量待测样品溶于蒸馏水,加入
探究Na SO 固体 若有白色沉淀产生,则样品
D 2 3 足量稀盐酸,再加入足量BaCl 溶
样品是否变质 2 已经变质
液
A.A B.B C.C D.D
11.(2021·山东高考真题)某同学进行蔗糖水解实验,并检验产物中的醛基,操作如下:
向试管Ⅰ中加入1mL20%蔗糖溶液,加入3滴稀硫酸,水浴加热5分钟。打开盛有10%NaOH溶
液的试剂瓶,将玻璃瓶塞倒放,取1mL溶液加入试管Ⅱ,盖紧瓶塞;向试管Ⅱ中加入5滴
2%CuSO 溶液。将试管Ⅱ中反应液加入试管Ⅰ,用酒精灯加热试管Ⅰ并观察现象。实验中存在
4
的错误有几处?
A.1 B.2 C.3 D.412.(2021·广东高考真题)化学创造美好生活。下列生产活动中,没有运用相应化学原理
的是
选项 生产活动 化学原理
H O
A 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成CO 和
2 2
B 利用海水制取溴和镁单质
Br可被氧化、Mg2
可被还原
C 利用氢氟酸刻蚀石英制作艺术品 氢氟酸可与SiO 反应
2
D 公园的钢铁护栏涂刷多彩防锈漆 钢铁与潮湿空气隔绝可防止腐蚀
A.A B.B C.C D.D
13.(2021·广东高考真题)今年五一假期,人文考古游持续成为热点。很多珍贵文物都记
载着中华文明的灿烂成就,具有深邃的文化寓意和极高的学术价值。下列国宝级文物主要由
合金材料制成的是
选
A B C D
项
文
物
名
铸客大铜鼎 河姆渡出土陶灶 兽首玛瑙杯 角形玉杯
称
A.A B.B C.C D.D二、实验题
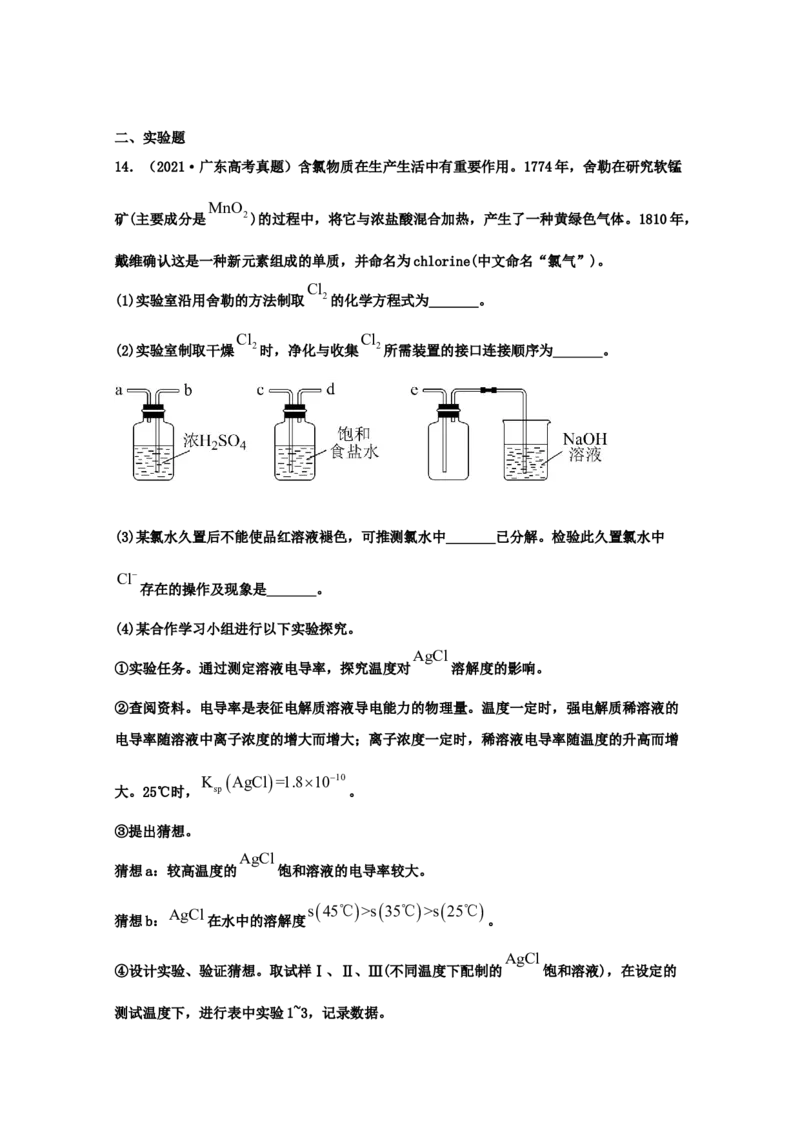
14.(2021·广东高考真题)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰
MnO
矿(主要成分是 2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,
戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
Cl
(1)实验室沿用舍勒的方法制取 2的化学方程式为_______。
Cl Cl
(2)实验室制取干燥 2时,净化与收集 2所需装置的接口连接顺序为_______。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中_______已分解。检验此久置氯水中
Cl
存在的操作及现象是_______。
(4)某合作学习小组进行以下实验探究。
AgCl
①实验任务。通过测定溶液电导率,探究温度对 溶解度的影响。
②查阅资料。电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的
电导率随溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增
K AgCl=1.81010
大。25℃时, sp 。
③提出猜想。
AgCl
猜想a:较高温度的 饱和溶液的电导率较大。
AgCl
s45℃>s35℃>s25℃
猜想b: 在水中的溶解度 。
AgCl
④设计实验、验证猜想。取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的 饱和溶液),在设定的
测试温度下,进行表中实验1~3,记录数据。实验序号 试样 测试温度/℃ 电导率/
μS/cm
1 Ⅰ:25℃的AgCl饱和溶液 25 A
1
2 Ⅱ:35℃的AgCl饱和溶液 35 A
2
3 Ⅲ:45℃的AgCl饱和溶液 45 A
3
c
Cl-
=
AgCl
⑤数据分析、交流讨论。25℃的 饱和溶液中, _______mol/L。
A A A a
实验结果为 3 2 1。小组同学认为,此结果可以证明③中的猜想 成立,但不足以证
明猜想b成立。结合②中信息,猜想b不足以成立的理由有_______。
⑥优化实验。小组同学为进一步验证猜想b,在实验1~3的基础上完善方案,进行实验4和
5。请在答题卡上完成表中内容。
实验序号 试样 测试温度/℃ 电导率/
μS/cm
4 Ⅰ _______ B
1
5 _______ _______ B
2
⑦实验总结。根据实验1~5的结果,并结合②中信息,小组同学认为猜想b也成立。猜想b
成立的判断依据是_______。
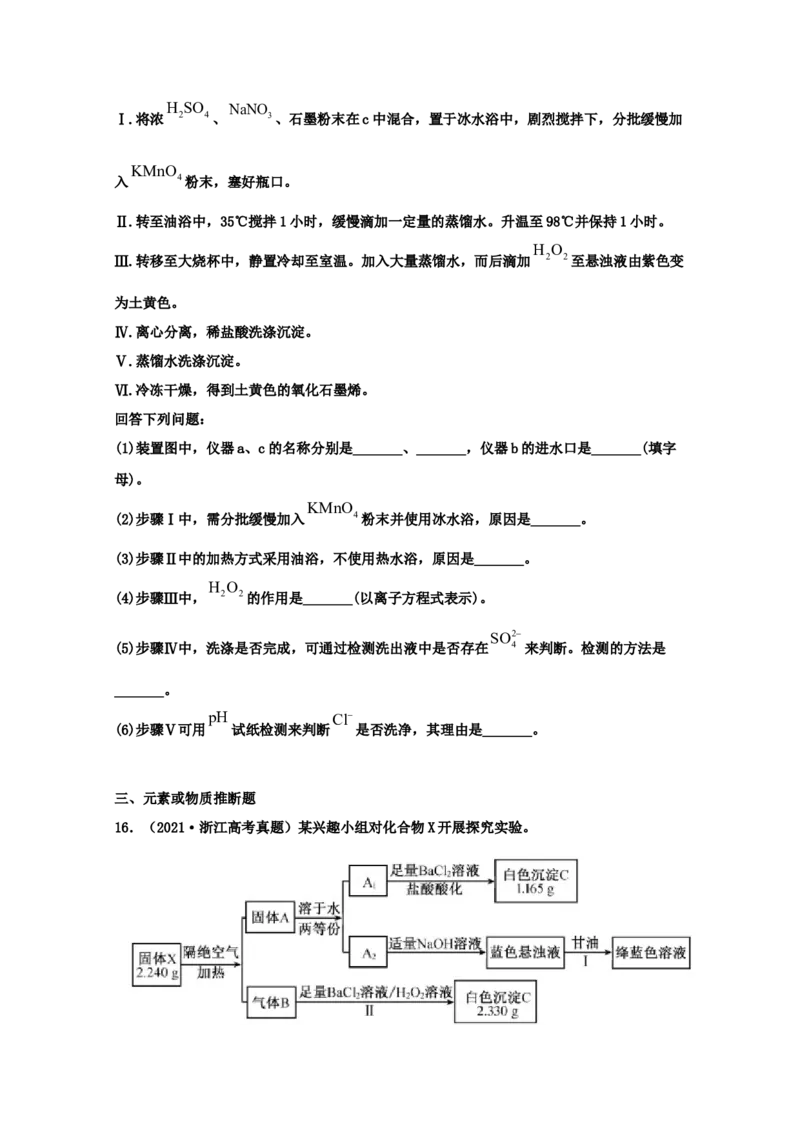
15.(2021·全国高考真题)氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重
要的应用前景,通过氧化剥离石墨制备氧化石墨烯的一种方法如下(装置如图所示):H SO NaNO
Ⅰ.将浓 2 4、 3、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加
KMnO
入 4粉末,塞好瓶口。
Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
H O
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加 2 2至悬浊液由紫色变
为土黄色。
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(1)装置图中,仪器a、c的名称分别是_______、_______,仪器b的进水口是_______(填字
母)。
KMnO
(2)步骤Ⅰ中,需分批缓慢加入 4粉末并使用冰水浴,原因是_______。
(3)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是_______。
H O
(4)步骤Ⅲ中, 2 2的作用是_______(以离子方程式表示)。
SO2
(5)步骤Ⅳ中,洗涤是否完成,可通过检测洗出液中是否存在 4 来判断。检测的方法是
_______。
pH Cl
(6)步骤Ⅴ可用 试纸检测来判断 是否洗净,其理由是_______。
三、元素或物质推断题
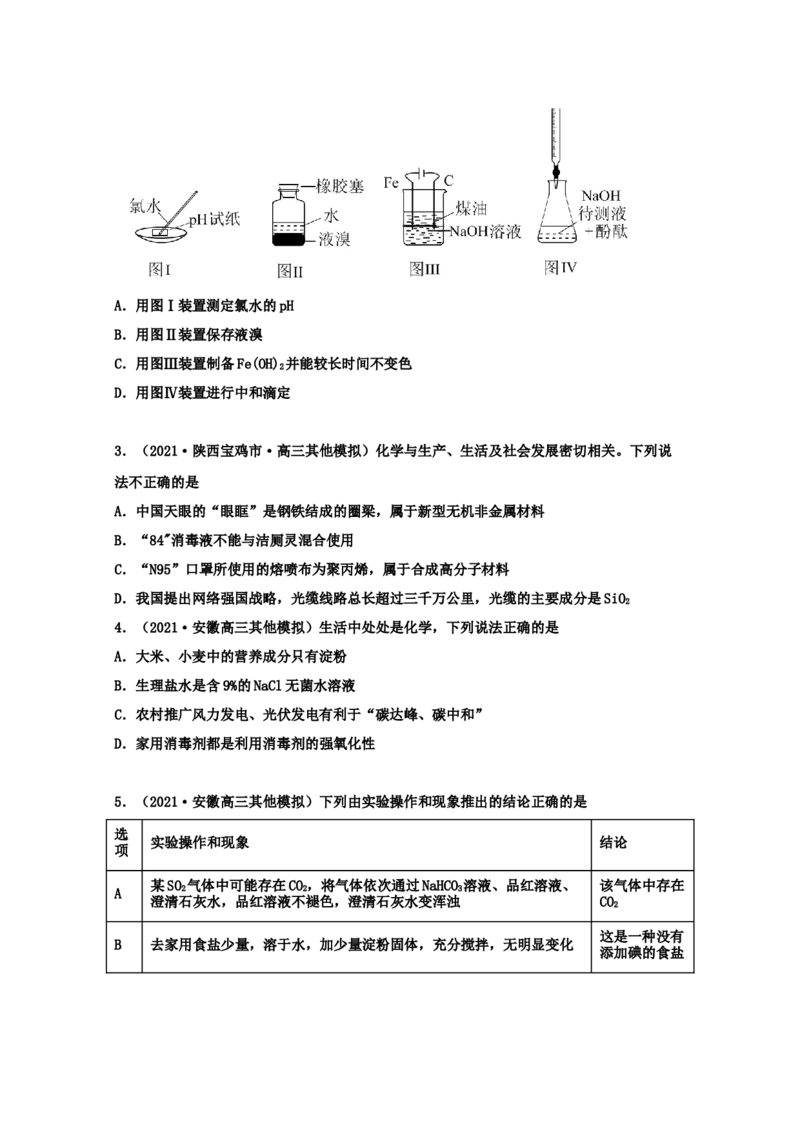
16.(2021·浙江高考真题)某兴趣小组对化合物X开展探究实验。其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。
请回答:
(1)组成X的3种元素是______(填元素符号),X的化学式是______。
(2)将固体X加入温热的稀HSO 中,产生气体B,该反应的离子方程式是______。
2 4
(3)步骤I,发生反应的化学方程式是______。
(4)步骤II,某同学未加HO 溶液,发现也会缓慢出现白色浑浊,原因是______。
2 2
(5)关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的
生成物使品红褪色。请设计实验证明______。
2021年化学高考模拟题
一、单选题
1.(2021·安徽高三一模)下列实验能达到目的的是
A.装置甲证明醋酸为弱酸 B.装置乙处理Cl 尾气
2
C.装置丙除去乙醇中少量的水 D.装置丁准确量取一定体积的酸性KMnO 标准
4
溶液
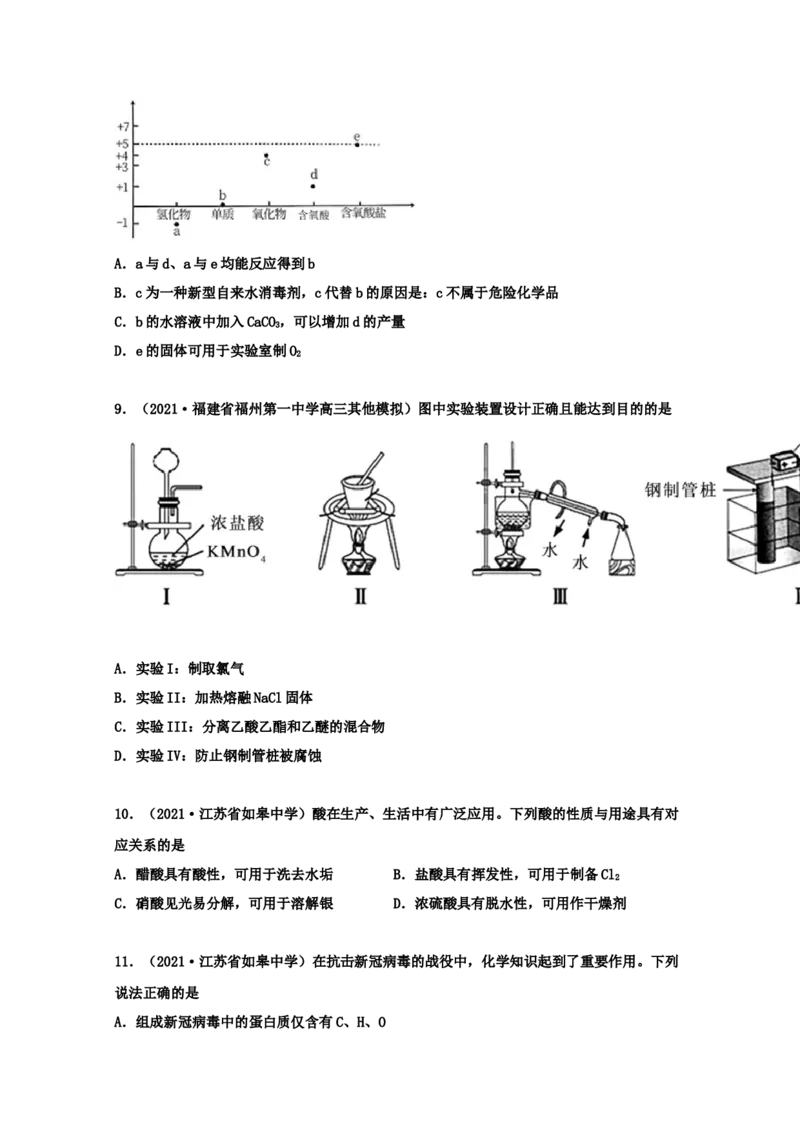
2.(2021·阜新市第二高级中学高三其他模拟)利用下列装置能达到相应实验目的的是A.用图Ⅰ装置测定氯水的pH
B.用图Ⅱ装置保存液溴
C.用图Ⅲ装置制备Fe(OH) 并能较长时间不变色
2
D.用图Ⅳ装置进行中和滴定
3.(2021·陕西宝鸡市·高三其他模拟)化学与生产、生活及社会发展密切相关。下列说
法不正确的是
A.中国天眼的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料
B.“84"消毒液不能与洁厕灵混合使用
C.“N95”口罩所使用的熔喷布为聚丙烯,属于合成高分子材料
D.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是SiO
2
4.(2021·安徽高三其他模拟)生活中处处是化学,下列说法正确的是
A.大米、小麦中的营养成分只有淀粉
B.生理盐水是含9%的NaCl无菌水溶液
C.农村推广风力发电、光伏发电有利于“碳达峰、碳中和”
D.家用消毒剂都是利用消毒剂的强氧化性
5.(2021·安徽高三其他模拟)下列由实验操作和现象推出的结论正确的是
选
实验操作和现象 结论
项
某SO 气体中可能存在CO,将气体依次通过NaHCO 溶液、品红溶液、 该气体中存在
A 2 2 3
澄清石灰水,品红溶液不褪色,澄清石灰水变浑浊 CO
2
这是一种没有
B 去家用食盐少量,溶于水,加少量淀粉固体,充分搅拌,无明显变化
添加碘的食盐取细铁丝在酒精灯上灼烧至红热,再伸入充满氯气的瓶中,剧烈反
Fe在Cl 中燃
C 应,产生大量红褐色的烟,结束后,加水振荡,使固体充分溶解,再 2
烧生成FeCl
滴加2滴KSCN溶液,溶液未变色 2
将钠块融化后,上面倒扣一个充满CO 的集气瓶,剧烈燃烧,产生大量 钠置换产生了
D 2
白烟,瓶壁有黑色固体 碳单质
A.A B.B C.C D.D
6.(2021·天津高三三模)以下实验设计能达到实验目的的是
实验目的 实验设计
将火柴头浸于水中,片刻后取少量溶液于试管中,只需加
A.检验火柴头中氯元素的存在
AgNO 溶液、稀硝酸
3
B.制备无水AlCl 蒸发Al与稀盐酸反应后的溶液
3
C.重结晶提纯苯甲酸 将粗品水溶、过滤、蒸发、结晶
D.鉴别NaBr和KI溶液 分别加新制氯水后,用CCl 萃取
4
A.A B.B C.C D.D
7.(2021·天津高三一模)用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)
选项 A B C D
X 浓盐酸 浓硫酸 双氧水 浓氨水
Y KMnO CHOH MnO NaOH
4 2 5 2
气体 Cl CH O NH
2 2 4 2 3
A.A B.B C.C D.D
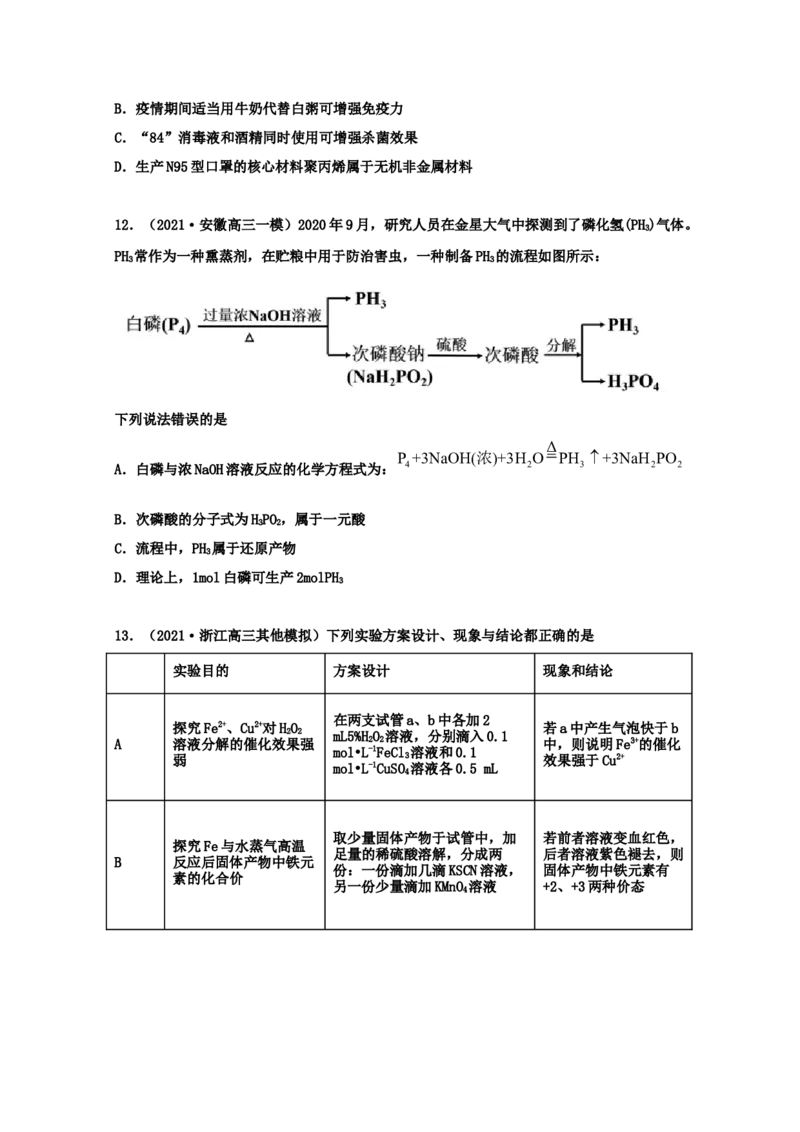
8.(2021·广东广州市·华南师大附中高三三模)部分含氯物质的分类与相应氯元素的化
合价关系如图所示。下列说法错误的是A.a与d、a与e均能反应得到b
B.c为一种新型自来水消毒剂,c代替b的原因是:c不属于危险化学品
C.b的水溶液中加入CaCO,可以增加d的产量
3
D.e的固体可用于实验室制O
2
9.(2021·福建省福州第一中学高三其他模拟)图中实验装置设计正确且能达到目的的是
A.实验I:制取氯气
B.实验II:加热熔融NaCl固体
C.实验III:分离乙酸乙酯和乙醚的混合物
D.实验IV:防止钢制管桩被腐蚀
10.(2021·江苏省如皋中学)酸在生产、生活中有广泛应用。下列酸的性质与用途具有对
应关系的是
A.醋酸具有酸性,可用于洗去水垢 B.盐酸具有挥发性,可用于制备Cl
2
C.硝酸见光易分解,可用于溶解银 D.浓硫酸具有脱水性,可用作干燥剂
11.(2021·江苏省如皋中学)在抗击新冠病毒的战役中,化学知识起到了重要作用。下列
说法正确的是
A.组成新冠病毒中的蛋白质仅含有C、H、OB.疫情期间适当用牛奶代替白粥可增强免疫力
C.“84”消毒液和酒精同时使用可增强杀菌效果
D.生产N95型口罩的核心材料聚丙烯属于无机非金属材料
12.(2021·安徽高三一模)2020年9月,研究人员在金星大气中探测到了磷化氢(PH)气体。
3
PH 常作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备PH 的流程如图所示:
3 3
下列说法错误的是
Δ
P +3NaOH(浓)+3H O PH +3NaH PO
A.白磷与浓NaOH溶液反应的化学方程式为: 4 2 3 2 2
B.次磷酸的分子式为HPO,属于一元酸
3 2
C.流程中,PH 属于还原产物
3
D.理论上,1mol白磷可生产2molPH
3
13.(2021·浙江高三其他模拟)下列实验方案设计、现象与结论都正确的是
实验目的 方案设计 现象和结论
在两支试管a、b中各加2
探究Fe2+、Cu2+对HO 若a中产生气泡快于b
2 2 mL5%HO 溶液,分别滴入0.1
A 溶液分解的催化效果强 2 2 中,则说明Fe3+的催化
mol•L-1FeCl 溶液和0.1
弱 3 效果强于Cu2+
mol•L-1CuSO 溶液各0.5 mL
4
取少量固体产物于试管中,加 若前者溶液变血红色,
探究Fe与水蒸气高温
足量的稀硫酸溶解,分成两 后者溶液紫色褪去,则
B 反应后固体产物中铁元
份:一份滴加几滴KSCN溶液, 固体产物中铁元素有
素的化合价
另一份少量滴加KMnO 溶液 +2、+3两种价态
4在小烧杯中加入约5 g动物脂
肪、6 mL95%的乙醇,再加入6
探究油脂在碱性条件下 若出现绛蓝色,则油脂
C mL 40%的氢氧化钠溶液,微热
的水解 已发生水解
一段时间后取少量清液,加入
新制氢氧化铜
未加KNO 固体前,无
3
探究Cu与硫酸的 铜粉加入稀硫酸中,加热,再 明显现象;加入KNO 3
D 固体后,产生大量气
反应 加入少量KNO 3 固体 泡,则说明KNO 起催
3
化作用
A.A B.B C.C D.D
14.(2021·广东佛山市·石门中学高三其他模拟)下列叙述I和II均正确并且有因果关系
的是
叙述I 叙述II
A NH 能使酚酞溶液变红 NH 可用于设计喷泉实验
3 3
B 1-己醇的沸点比己烷的沸点高 1-己醇和己烷可通过蒸馏初步分离
C KNO 的溶解度大 用重结晶法除去KNO 中混有的NaCl
3 3
D Na在Cl 中燃烧的生成物含离子键 NaCl固体可导电
2
A.A B.B C.C D.D
15.(2021·天津和平区·耀华中学高三二模)下列每组的叙述I、II都正确,且有因果关
系的是
叙述I 叙述II
A CH 中碳元素处于最低化合价,具有还原性 可燃冰是一种清洁能源
4
B Fe3+具有氧化性 NHFe(SO)·12HO作净水剂
4 4 2 2
C 断裂NH 分子中H-N键要吸收热量 工业上用液氨作制冷剂
3
D 有机玻璃(PMMA)透光性好、易加工 有机玻璃常作光学仪器A.A B.B C.C D.D
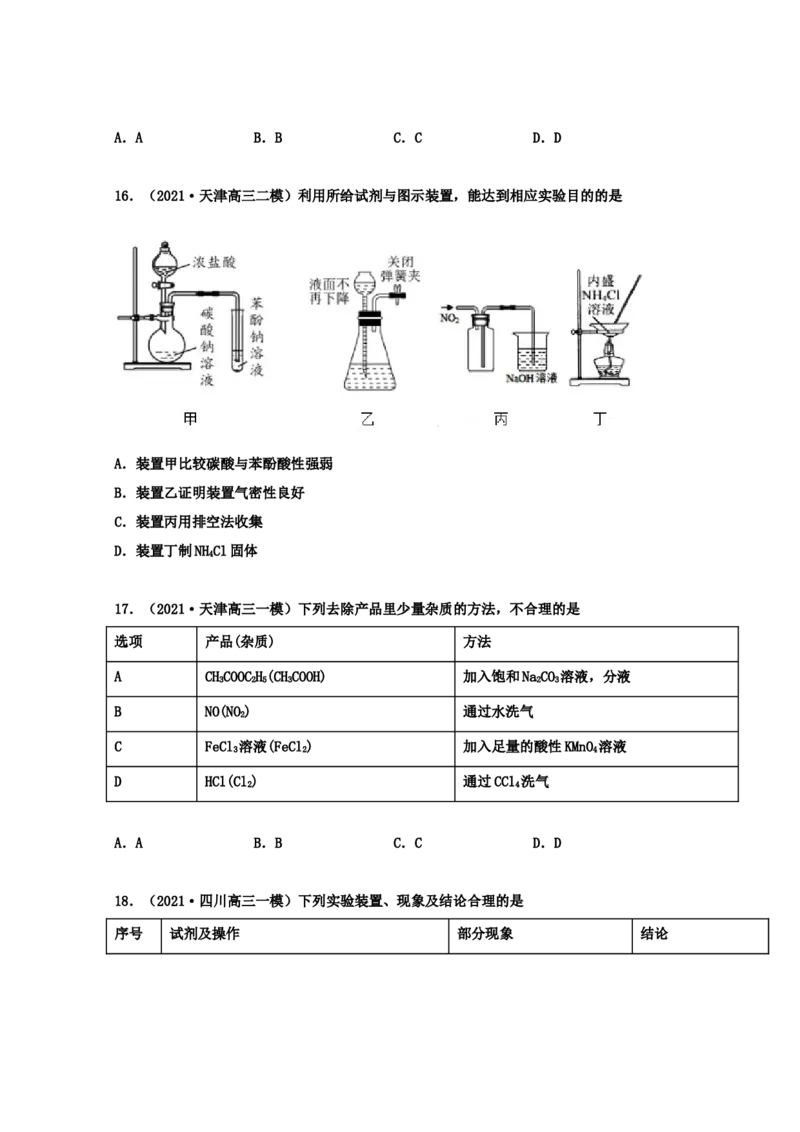
16.(2021·天津高三二模)利用所给试剂与图示装置,能达到相应实验目的的是
A.装置甲比较碳酸与苯酚酸性强弱
B.装置乙证明装置气密性良好
C.装置丙用排空法收集
D.装置丁制NHCl固体
4
17.(2021·天津高三一模)下列去除产品里少量杂质的方法,不合理的是
选项 产品(杂质) 方法
A CHCOOCH(CHCOOH) 加入饱和NaCO 溶液,分液
3 2 5 3 2 3
B NO(NO) 通过水洗气
2
C FeCl 溶液(FeCl) 加入足量的酸性KMnO 溶液
3 2 4
D HCl(Cl) 通过CCl 洗气
2 4
A.A B.B C.C D.D
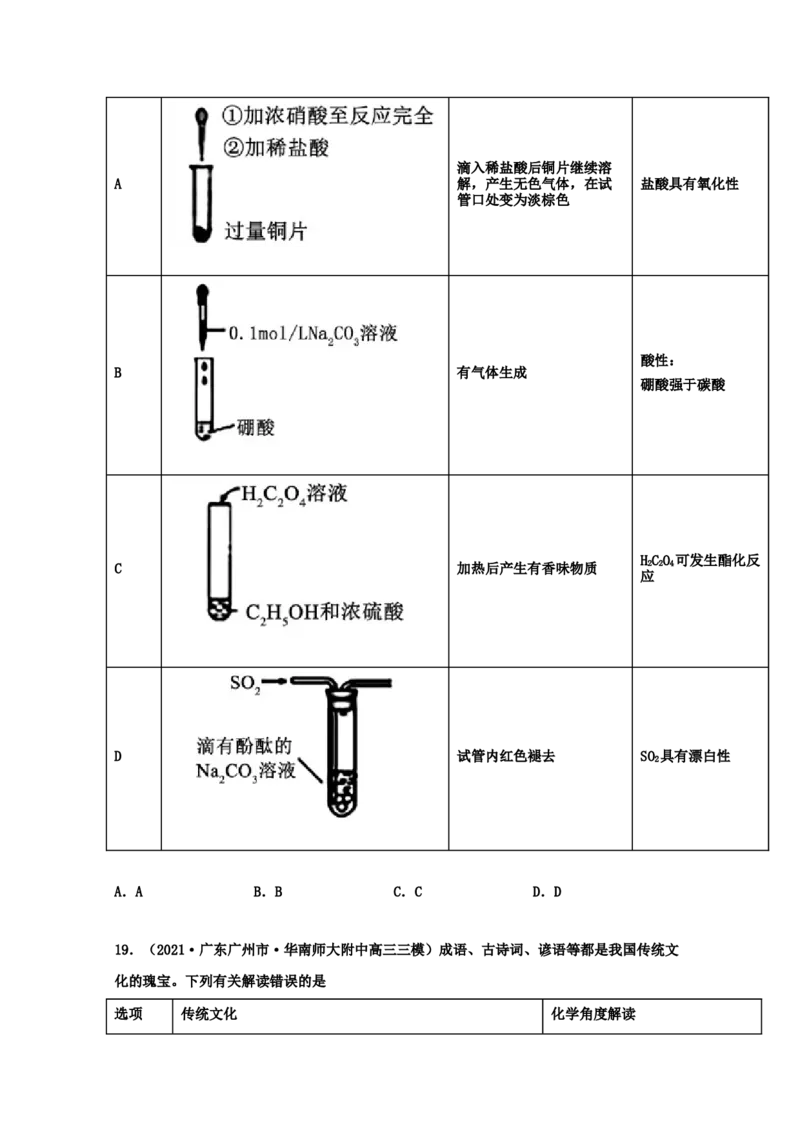
18.(2021·四川高三一模)下列实验装置、现象及结论合理的是
序号 试剂及操作 部分现象 结论滴入稀盐酸后铜片继续溶
A 解,产生无色气体,在试 盐酸具有氧化性
管口处变为淡棕色
酸性:
B 有气体生成
硼酸强于碳酸
HCO 可发生酯化反
C 加热后产生有香味物质 2 2 4
应
D 试管内红色褪去 SO 具有漂白性
2
A.A B.B C.C D.D
19.(2021·广东广州市·华南师大附中高三三模)成语、古诗词、谚语等都是我国传统文
化的瑰宝。下列有关解读错误的是
选项 传统文化 化学角度解读“香”的原因之一是美酒含有酯
A 兰陵美酒郁金香,玉碗盛来琥珀光
类物质
B “司南之杓(勺),投之于地,其柢(勺柄)指南” 司南中“杓”的材质为FeO
2 3
在雷电作用下N 最终转化成被作
C 三月打雷麦谷堆 2
物吸收的化合态氮
《本草经集注》记载“如握盐雪不冰,强烧之,紫青烟 利用物理方法(焰色反应)可以鉴
D
起…云是真硝石也 别钾盐
A.A B.B C.C D.D
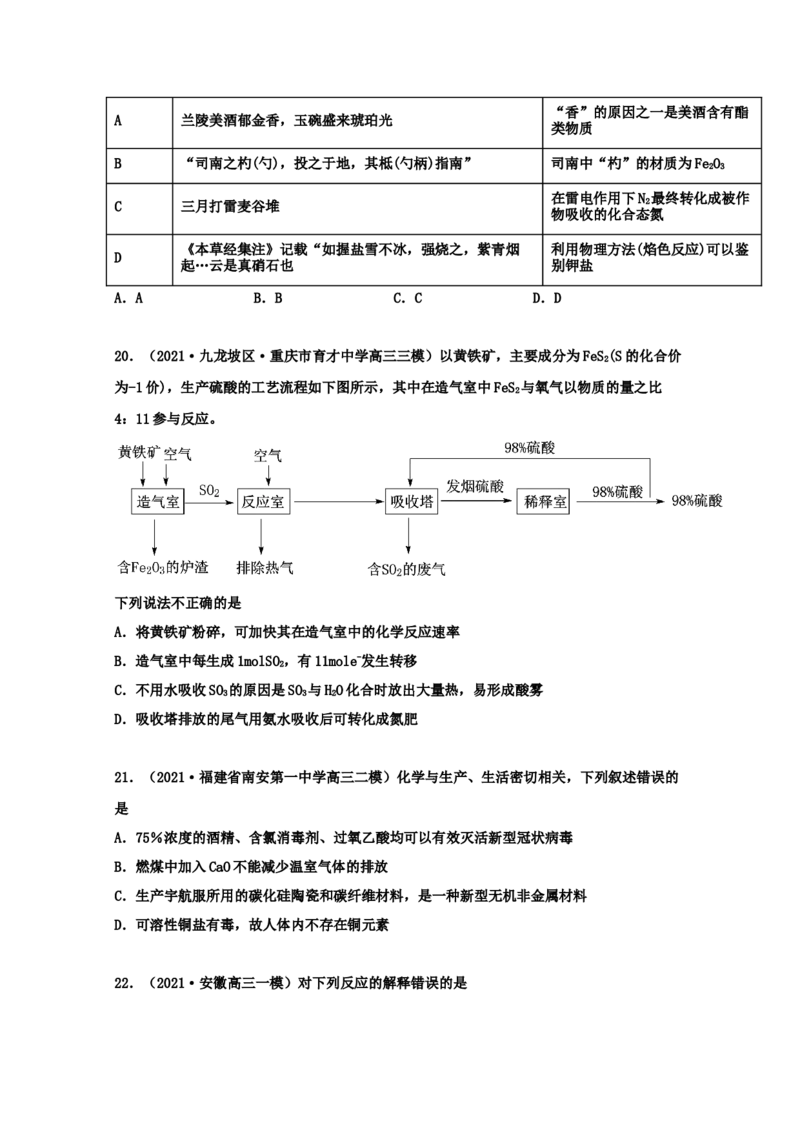
20.(2021·九龙坡区·重庆市育才中学高三三模)以黄铁矿,主要成分为FeS(S的化合价
2
为-1价),生产硫酸的工艺流程如下图所示,其中在造气室中FeS 与氧气以物质的量之比
2
4:11参与反应。
下列说法不正确的是
A.将黄铁矿粉碎,可加快其在造气室中的化学反应速率
B.造气室中每生成1molSO,有11mole-发生转移
2
C.不用水吸收SO 的原因是SO 与HO化合时放出大量热,易形成酸雾
3 3 2
D.吸收塔排放的尾气用氨水吸收后可转化成氮肥
21.(2021·福建省南安第一中学高三二模)化学与生产、生活密切相关,下列叙述错误的
是
A.75%浓度的酒精、含氯消毒剂、过氧乙酸均可以有效灭活新型冠状病毒
B.燃煤中加入CaO不能减少温室气体的排放
C.生产宇航服所用的碳化硅陶瓷和碳纤维材料,是一种新型无机非金属材料
D.可溶性铜盐有毒,故人体内不存在铜元素
22.(2021·安徽高三一模)对下列反应的解释错误的是反应 解释
A CuCl+HS=CuS↓+2HC1 反应体系中S2-浓度变小
2 2
B AgOH+2NH•HO=[Ag(NH)]OH+2HO [Ag(NH)]OH的碱性比NH•HO的弱
3 2 3 2 2 3 2 3 2
Δ
C 2NaCl(固)+HSO(浓) NaSO+2HC1↑ 生成HCl气体,熵增明显
2 4 2 4
该实验条件下,碳酸氢钠的溶解度比氯
D NaCl+NH+HO+CO=NHCl+NaHCO↓
3 2 2 4 3 化铵和氯化钠的小
A.A B.B C.C D.D
23.(2021·浙江高三其他模拟)下列物质对应组成正确的是
A.木醇:CHCHOH B.熟石灰:CaSO·2HO
3 2 4 2
C.油酸:C H COOH D.黄铁矿:FeS
15 31 2
24.(2021·北京高三其他模拟)降低硫含量是裂化汽油精制处理的关键。S—Zorb技术使
用Ni/ZnO作脱硫吸附剂脱除噻吩( )中硫原子的过程如图。
下列说法不正确的是
A.过程①涉及极性键和非极性键的断裂
B.过程③通入O 的主要目的是将ZnS转化为ZnO和SO
2 2
C.过程③中参加反应的O 和ZnS的物质的量之比是3∶2
2
D.过程④通入H 的主要目的是使脱硫吸附剂再生
2
25.(2021·吉林长春市·东北师大附中高三其他模拟)下列有关实验现象和解释或结论都
正确的选项是选
实验操作 现象 解释或结论
项
2-
原溶液中一定含有CO 或
向某无色溶液中加入稀盐酸,将产生 3
A 澄清石灰水变浑浊
的气体通入澄清石灰水中 -
HCO
3
B 将NaClO溶液滴到pH试纸上 测得pH=9.8 NaClO溶液水解显碱性
两支试管各盛0. 1 mol/L 4 mL酸性
加入0.2 mol/L草酸
高锰酸钾溶液,分别加入0.1 mol/L 反应物浓度越大,反应速
C 溶液试管中,高锰酸
2 mL草酸溶液和0.2mol/L2mL草酸溶 率越快
钾溶液褪色更快
液
D 把SO 通入紫色石蕊试液中 紫色溶液变红 SO 的水溶液呈酸性
2 2
A.A B.B C.C D.D
26.(2021·阜新市第二高级中学高三其他模拟)下列实验方案能达到实验目的的是
选
实验方案 实验目的
项
甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变 验证一氯甲烷
A
红 具有酸性
验证SO 的漂白
B 将纯净的SO 通入紫色石蕊试液中,观察颜色变化 2
2 性
验证氧化性:
C 向硫酸酸化的HO 溶液中滴入Fe(NO) 溶液,溶液变黄
2 2 3 2 HO>Fe3+
2 2
向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,冷却后向其中加
蔗糖水解产物
D 入足量稀NaOH溶液,再加入新制的银氨溶液,并水浴加热,产生了
具有还原性
银镜
A.A B.B C.C D.D
27.(2021·江西抚州市·临川一中)下列实验操作,不能达到实验目的是
选项 实验操作 实验目的
A 向少许蔗糖中滴入浓硫酸,并不断用玻璃棒搅拌 验证浓硫酸的脱水性
B 向苯中滴加浓溴水,并加入FeBr 作催化剂 验证苯的溴代反应
3
C 向NaSO 粉末中滴入足量浓盐酸,并加入BaCl 溶液 检验NaSO 粉末是否变质
2 3 2 2 3
D 浸透了石蜡油的石棉中加入碎瓷片,加热,并将产生 检验石蜡的分解产物中含有的气体通入酸性高锰酸钾溶液中 烯烃
A.A B.B C.C D.D
28.(2021·辽宁高三其他模拟)下列有关物质的检验和提纯叙述正确的是
A.麦芽糖在酸性条件下水解后,加入新制氢氧化铜悬浊液煮沸无现象,说明无葡萄糖生成
SO2
B.向某溶液中先加过量盐酸无现象,再加氯化钡产生白色沉淀,原溶液中一定含有 4
FeSO
C.检验 4是否变质可以用酸性高锰酸钾溶液
SO
D.除去乙烯中少量的 2气体,可将其通入盛有溴水的洗气瓶中
29.(2021·广东广州市·华南师大附中高三三模)实验室探究SO 与Fe(NO) 溶液反应的原
2 3 3
理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是
A.滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N
2
B.Y中产生的白色沉淀是BaSO 和BaSO
4 3
C.在X装置中浓硫酸不体现氧化性
D.若将Fe(NO) 换成氨水,Y中也能产生白色沉淀
3 3
30.(2021·四川德阳市·高三二模)下列实验方案中,能实现实验目的的是
实验目的 实验方案
检验露置的NaSO 是否变
A 2 3 用盐酸酸化的BaCl 溶液
质 2
B 缩短容量瓶干燥的时间 将洗净的容量瓶放在烘箱中烘干
测定NaCO(含NaCl)样品 取一定质量的样品与足量盐酸反应,用碱石灰吸
C 2 3
纯度 收产生的气体验证氧化性强弱: 向FeCl 和KSCN的混合溶液中滴入酸化的AgNO 溶
D 2 3
Ag+>Fe2+ 液
A.A B.B C.C D.D
31.(2021·阜新市第二高级中学高三其他模拟)下列说法错误的是
A.NH 的电子式为
2 4
B.“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的“碱”为KCO
2 3
C.二氧化硅的分子式为SiO
2
D.硅和锗都位于元素周期表中金属与非金属元素的交界区,都可以作半导体材料
32.(2021·长沙市明德中学高三三模)我国突飞猛进的新科技深刻改变着人类的生活、生
产方式。下列说法错误的是
A.“中国天眼”的镜片材料为SiC,属于新型无机非金属材料
B.北斗导航专用ASIC硬件结合国产处理器打造出一颗真正意义的“中国芯”,其主要成分
为SiO
2
C.港珠澳大桥设计使用寿命120年,水下钢柱镶铝块防腐的方法为牺牲阳极的阴极保护法
D.我国自主研发的东方超环(人造太阳)使用的氚、氘与氕互为同位素
33.(2021·广东佛山市·石门中学高三其他模拟)中华民族为人类文明进步做出了巨大贡
献,运用化学知识对下列事例进行分析,不合理的是
A.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
B.李白有诗云“日照香炉生紫烟”,这是描写“碘的升华”
C.北宋沈括《梦溪笔谈》中记载“熬胆矾铁釜,久之亦化为铜”,是发生了置换反应
D.屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作
34.(【一飞冲天】4.实验中学一模)新材料的发展充分体现了“中国技术”中国制造”和
“中国力量”。下列成果所涉及的材料为金属材料的是
A.“天问一号”火星探测器太阳翼的材料——石墨纤维复合聚酰胺薄膜
B.“长征五B”运载火箭中使用了耐热性、导热性好的材料——氮化铝陶瓷
C.“领雁”AG50飞机主体结构的复合材料——玻璃纤维复合材料
D..“奋斗者”号深潜器载人舱的外壳——钛合金35.(2021·四川德阳市·高三二模)中国传统文化博大精深,也蕴含着许多化学知识。下
列说法正确的是
A 宋代烧制出“明如镜、声如磬”的瓷器 瓷器主要原料是SiO
2
《梦溪笔谈》中“方家以磁石磨针锋,则能指
B 磁石主要成分是FeO
南” 2 3
古代四大发明之一的火药“乃焰硝、硫磺、杉
C 焰硝是指HNO
木炭所合” 3
D 《本草纲目》中记载石碱条:“彼人采蒿蓼之
属,晒干烧灰,以水淋汁,……浣衣发面,亦 石碱条主要成分是KCO
2 3
去垢发面”
A.A B.B C.C D.D
36.(2021·广东高三其他模拟)在给定的条件下,下列选项所示的物质间转化均能实现的
是
盐酸 H
A.SiO SiCl 2 Si
2 4 高温
N O 2NO H2 OHNO
B. 2 放电 2 3
Al O 盐酸AlCl (aq)过量氨水AlO
C. 2 3 3 2
SO O2 SO H2 OHSO
D. 2 催化剂,Δ 3 2 4
37.(2021·云南曲靖市·高三二模)从化学的视角分析,下列说法不正确的是
A.除去锅炉中的水垢时,可先用碳酸钠溶液处理,使水垢蓬松,再加入盐酸去除
Na O
B. 2 2可作供氧剂
C.人体摄入的油脂、蛋白质必须先经过水解才能被吸收
D.石英玻璃、分子筛的主要成分是硅酸盐
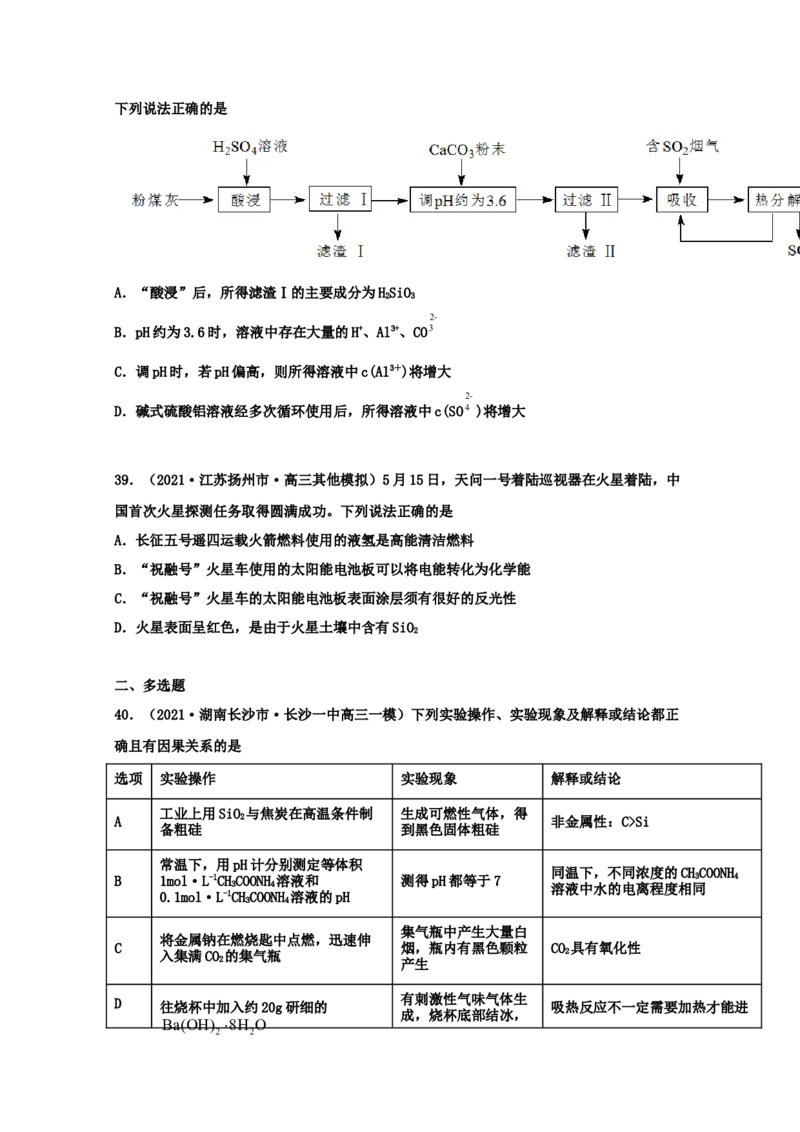
38.(2021·江苏扬州市·高三其他模拟)烟气脱硫能有效减少SO 的排放。实验室用粉煤
2
灰(主要含AlO、SiO 等)制备碱式硫酸铝[(1-x)Al(SO)·xAlO]溶液,并用于烟气脱硫。
2 3 2 2 4 3 2 3下列说法正确的是
A.“酸浸”后,所得滤渣Ⅰ的主要成分为HSiO
2 3
2-
B.pH约为3.6时,溶液中存在大量的H+、Al3+、CO3
C.调pH时,若pH偏高,则所得溶液中c(Al3+)将增大
2-
D.碱式硫酸铝溶液经多次循环使用后,所得溶液中c(SO4 )将增大
39.(2021·江苏扬州市·高三其他模拟)5月15日,天问一号着陆巡视器在火星着陆,中
国首次火星探测任务取得圆满成功。下列说法正确的是
A.长征五号遥四运载火箭燃料使用的液氢是高能清洁燃料
B.“祝融号”火星车使用的太阳能电池板可以将电能转化为化学能
C.“祝融号”火星车的太阳能电池板表面涂层须有很好的反光性
D.火星表面呈红色,是由于火星土壤中含有SiO
2
二、多选题
40.(2021·湖南长沙市·长沙一中高三一模)下列实验操作、实验现象及解释或结论都正
确且有因果关系的是
选项 实验操作 实验现象 解释或结论
工业上用SiO 与焦炭在高温条件制 生成可燃性气体,得
A 2 非金属性:C>Si
备粗硅 到黑色固体粗硅
常温下,用pH计分别测定等体积
同温下,不同浓度的CHCOONH
B 1mol·L-1CHCOONH 溶液和 测得pH都等于7 3 4
3 4 溶液中水的电离程度相同
0.1mol·L-1CHCOONH 溶液的pH
3 4
集气瓶中产生大量白
将金属钠在燃烧匙中点燃,迅速伸
C 烟,瓶内有黑色颗粒 CO 具有氧化性
入集满CO 的集气瓶 2
2 产生
有刺激性气味气体生
D 往烧杯中加入约20g研细的 吸热反应不一定需要加热才能进
成,烧杯底部结冰,
Ba(OH) 8H O
2 2Ba(OH) 8H O晶体和10gNHCl
2 2 4
与玻璃片粘在一起 行
晶体,并将烧杯放在滴有水的玻璃
片上,用玻璃棒迅速搅拌
A.A B.B C.C D.D
三、实验题
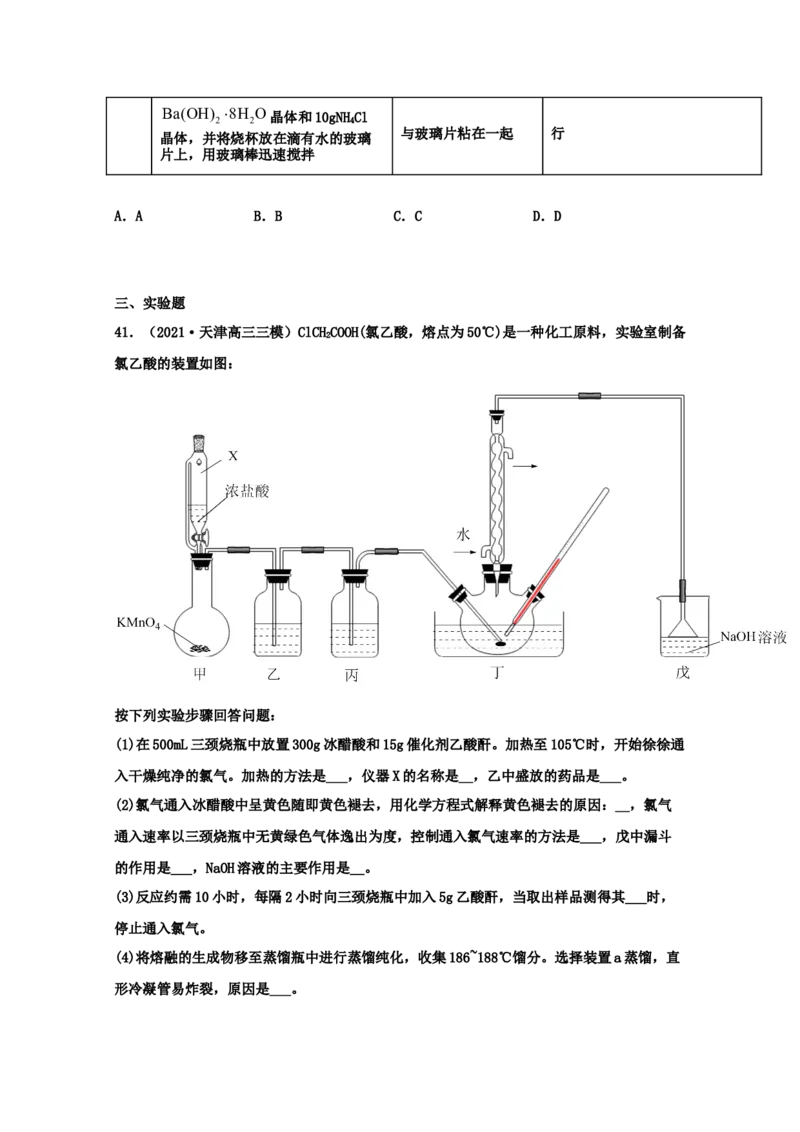
41.(2021·天津高三三模)ClCHCOOH(氯乙酸,熔点为50℃)是一种化工原料,实验室制备
2
氯乙酸的装置如图:
按下列实验步骤回答问题:
(1)在500mL三颈烧瓶中放置300g冰醋酸和15g催化剂乙酸酐。加热至105℃时,开始徐徐通
入干燥纯净的氯气。加热的方法是___,仪器X的名称是__,乙中盛放的药品是___。
(2)氯气通入冰醋酸中呈黄色随即黄色褪去,用化学方程式解释黄色褪去的原因:__,氯气
通入速率以三颈烧瓶中无黄绿色气体逸出为度,控制通入氯气速率的方法是___,戊中漏斗
的作用是___,NaOH溶液的主要作用是__。
(3)反应约需10小时,每隔2小时向三颈烧瓶中加入5g乙酸酐,当取出样品测得其___时,
停止通入氯气。
(4)将熔融的生成物移至蒸馏瓶中进行蒸馏纯化,收集186~188℃馏分。选择装置a蒸馏,直
形冷凝管易炸裂,原因是___。(5)冷凝后生成无色氯乙酸晶体425g,产率约为___(保留2位有效数字)。
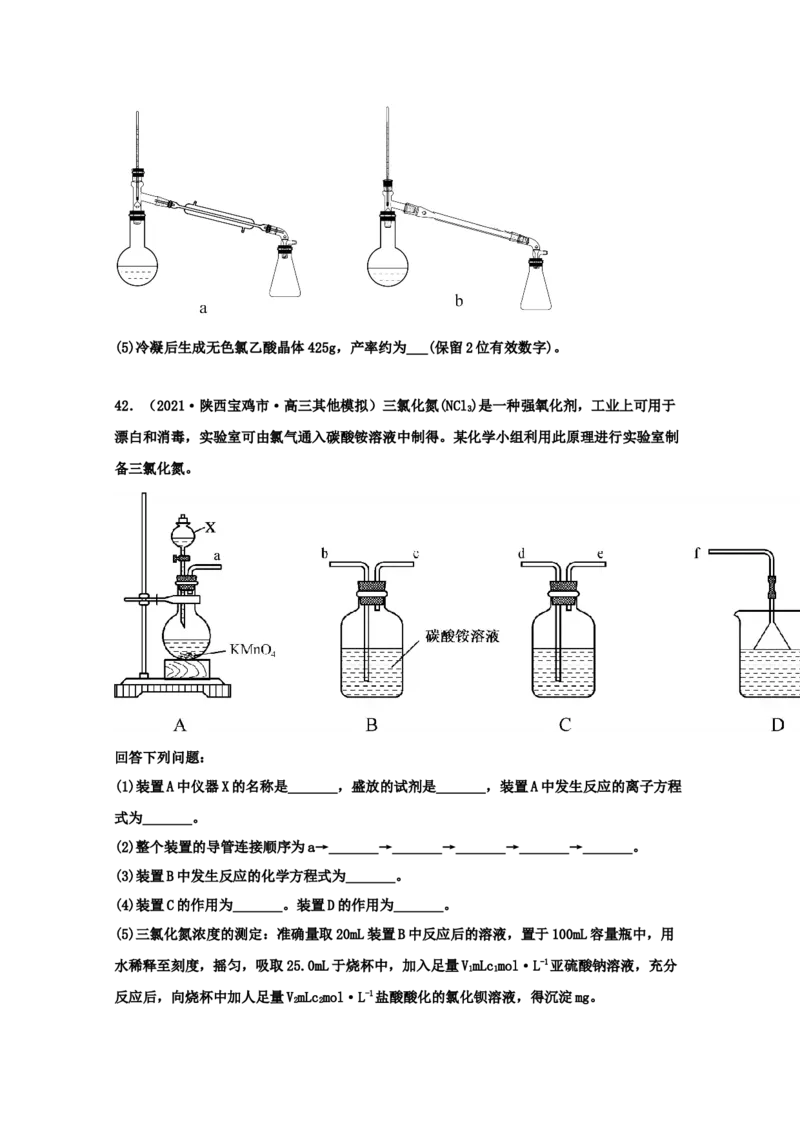
42.(2021·陕西宝鸡市·高三其他模拟)三氯化氮(NCl)是一种强氧化剂,工业上可用于
3
漂白和消毒,实验室可由氯气通入碳酸铵溶液中制得。某化学小组利用此原理进行实验室制
备三氯化氮。
回答下列问题:
(1)装置A中仪器X的名称是_______,盛放的试剂是_______,装置A中发生反应的离子方程
式为_______。
(2)整个装置的导管连接顺序为a→_______→_______→_______→_______→_______。
(3)装置B中发生反应的化学方程式为_______。
(4)装置C的作用为_______。装置D的作用为_______。
(5)三氯化氮浓度的测定:准确量取20mL装置B中反应后的溶液,置于100mL容量瓶中,用
水稀释至刻度,摇匀,吸取25.0mL于烧杯中,加入足量VmLcmol·L-1亚硫酸钠溶液,充分
1 1
反应后,向烧杯中加人足量VmLcmol·L-1盐酸酸化的氯化钡溶液,得沉淀mg。
2 2已知:i._______ NaSO+_______ NCl +_______=_______NaSO +_______ HCl+
2 3 3 2 4
_______NHCl;
4
ii. BaCl +NaSO=BaSO↓+ 2HCl。
2 2 4
①请完成反应i的化学方程式:i._______ NaSO+_______ NCl+_______=NaSO+_______
2 3 3 2 4
HCl+_______ NHCl
4
_______
②装置B反应后的溶液中三氯化氮的浓度为_______mol·L-1。
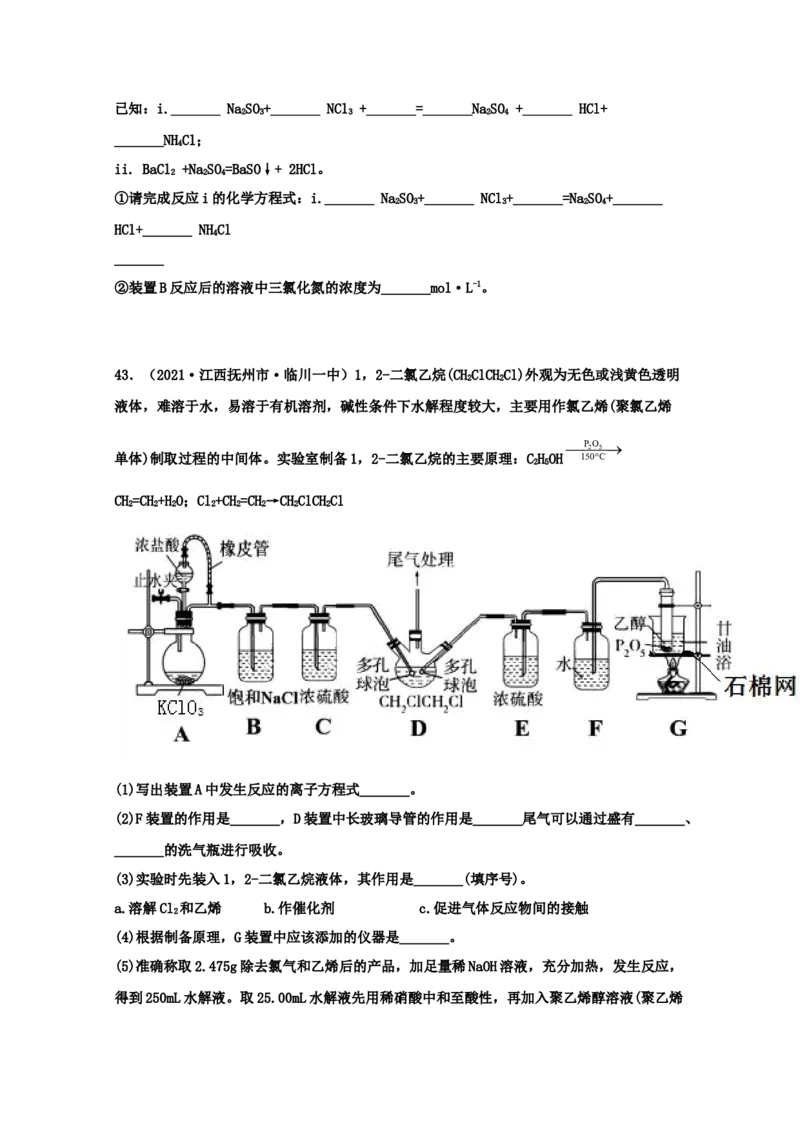
43.(2021·江西抚州市·临川一中)1,2-二氯乙烷(CHClCHCl)外观为无色或浅黄色透明
2 2
液体,难溶于水,易溶于有机溶剂,碱性条件下水解程度较大,主要用作氯乙烯(聚氯乙烯
P 2 O 5
单体)制取过程的中间体。实验室制备1,2-二氯乙烷的主要原理:CHOH 150C
2 5
CH=CH+HO;Cl+CH=CH→CHClCHCl
2 2 2 2 2 2 2 2
(1)写出装置A中发生反应的离子方程式_______。
(2)F装置的作用是_______,D装置中长玻璃导管的作用是_______尾气可以通过盛有_______、
_______的洗气瓶进行吸收。
(3)实验时先装入1,2-二氯乙烷液体,其作用是_______(填序号)。
a.溶解Cl 和乙烯 b.作催化剂 c.促进气体反应物间的接触
2
(4)根据制备原理,G装置中应该添加的仪器是_______。
(5)准确称取2.475g除去氯气和乙烯后的产品,加足量稀NaOH溶液,充分加热,发生反应,
得到250mL水解液。取25.00mL水解液先用稀硝酸中和至酸性,再加入聚乙烯醇溶液(聚乙烯醇的作用是阻止AgSCN和AgCl之间的转化),然后加入过量的50.00mL0.1000mol/LAgNO 溶液,
3
充分反应后用0.1000mol/LNHSCN标准液滴定过量的AgNO,重复实验三次,平均消耗标准液
4 3
10.00mL。已知:Ag++SCN-=AgSCN↓(白色沉淀)
①滴定时,应选用的指示剂为_______(填标号)。
a.FeSO b.Fe(NO) c.FeCl
4 3 3 3
②产品中Cl元素的质量分数为_______(保留三位有效数字),1,2-二氯乙烷的纯度为
≤_______。
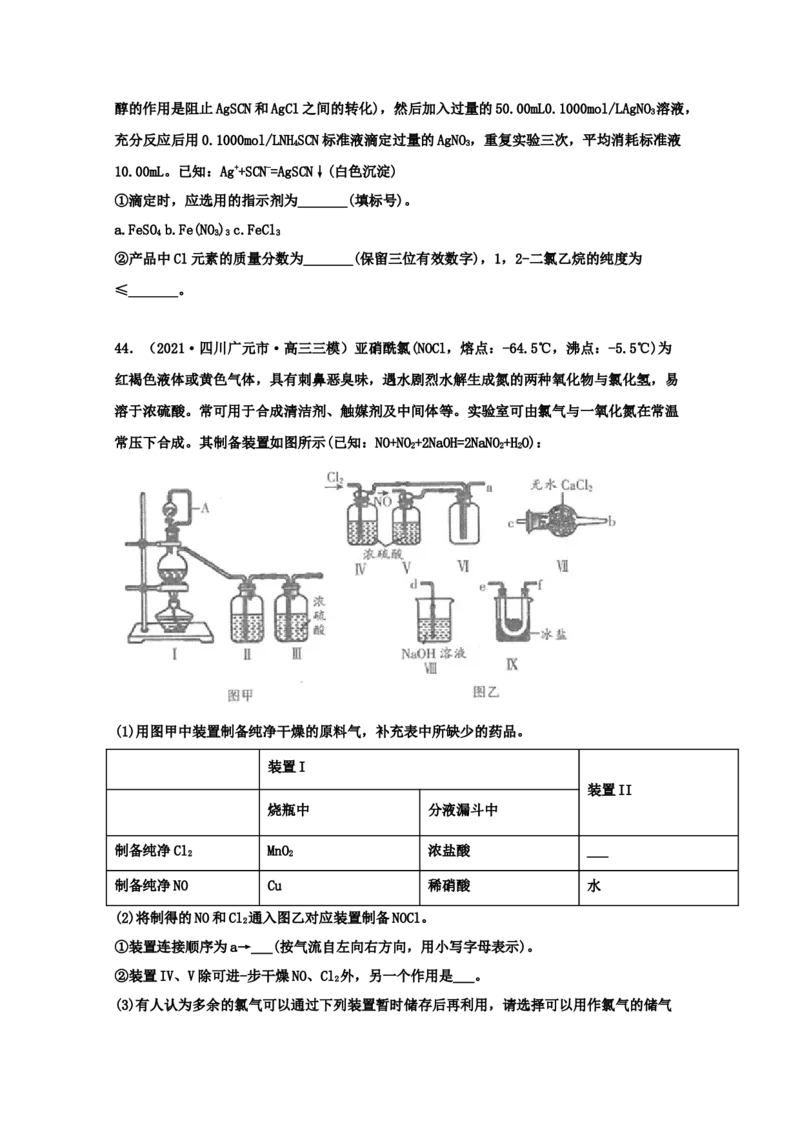
44.(2021·四川广元市·高三三模)亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)为
红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易
溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温
常压下合成。其制备装置如图所示(已知:NO+NO+2NaOH=2NaNO+HO):
2 2 2
(1)用图甲中装置制备纯净干燥的原料气,补充表中所缺少的药品。
装置I
装置II
烧瓶中 分液漏斗中
制备纯净Cl MnO 浓盐酸 ___
2 2
制备纯净NO Cu 稀硝酸 水
(2)将制得的NO和Cl 通入图乙对应装置制备NOCl。
2
①装置连接顺序为a→___(按气流自左向右方向,用小写字母表示)。
②装置IV、V除可进-步干燥NO、Cl 外,另一个作用是___。
2
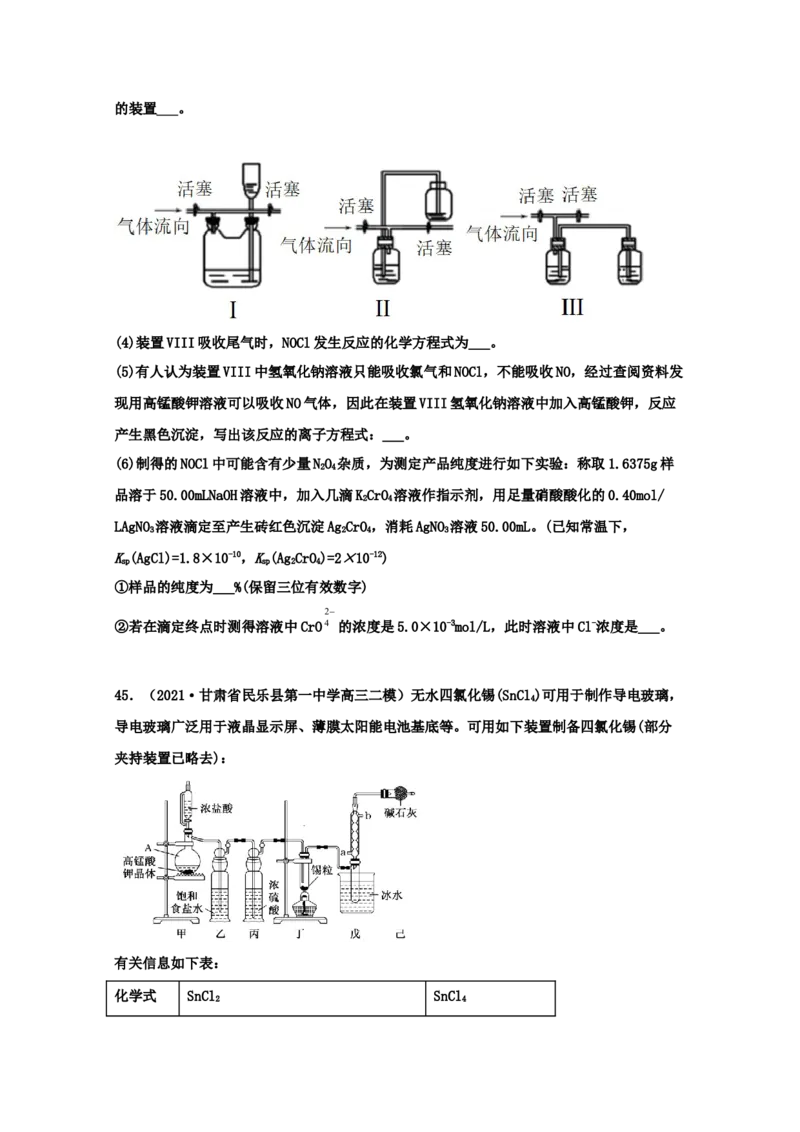
(3)有人认为多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置___。
(4)装置VIII吸收尾气时,NOCl发生反应的化学方程式为___。
(5)有人认为装置VIII中氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发
现用高锰酸钾溶液可以吸收NO气体,因此在装置VIII氢氧化钠溶液中加入高锰酸钾,反应
产生黑色沉淀,写出该反应的离子方程式:___。
(6)制得的NOCl中可能含有少量NO 杂质,为测定产品纯度进行如下实验:称取1.6375g样
2 4
品溶于50.00mLNaOH溶液中,加入几滴KCrO 溶液作指示剂,用足量硝酸酸化的0.40mol/
2 4
LAgNO 溶液滴定至产生砖红色沉淀AgCrO,消耗AgNO 溶液50.00mL。(已知常温下,
3 2 4 3
K(AgCl)=1.8×10-10,K(AgCrO)=2×10-12)
sp sp 2 4
①样品的纯度为___%(保留三位有效数字)
2
②若在滴定终点时测得溶液中CrO4 的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是___。
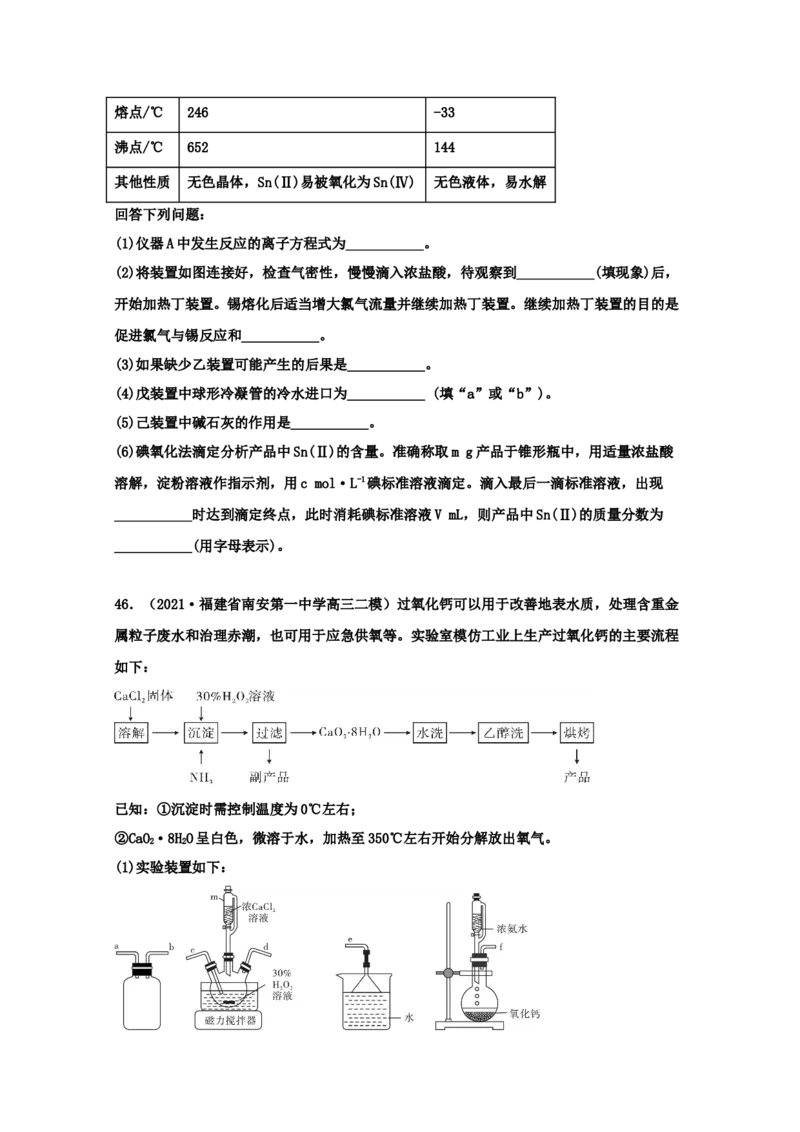
45.(2021·甘肃省民乐县第一中学高三二模)无水四氯化锡(SnCl)可用于制作导电玻璃,
4
导电玻璃广泛用于液晶显示屏、薄膜太阳能电池基底等。可用如下装置制备四氯化锡(部分
夹持装置已略去):
有关信息如下表:
化学式 SnCl SnCl
2 4熔点/℃ 246 -33
沸点/℃ 652 144
其他性质 无色晶体,Sn(Ⅱ)易被氧化为Sn(Ⅳ) 无色液体,易水解
回答下列问题:
(1)仪器A中发生反应的离子方程式为___________。
(2)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到___________(填现象)后,
开始加热丁装置。锡熔化后适当增大氯气流量并继续加热丁装置。继续加热丁装置的目的是
促进氯气与锡反应和___________。
(3)如果缺少乙装置可能产生的后果是___________。
(4)戊装置中球形冷凝管的冷水进口为___________ (填“a”或“b”)。
(5)己装置中碱石灰的作用是___________。
(6)碘氧化法滴定分析产品中Sn(Ⅱ)的含量。准确称取m g产品于锥形瓶中,用适量浓盐酸
溶解,淀粉溶液作指示剂,用c mol·L-1碘标准溶液滴定。滴入最后一滴标准溶液,出现
___________时达到滴定终点,此时消耗碘标准溶液V mL,则产品中Sn(Ⅱ)的质量分数为
___________(用字母表示)。
46.(2021·福建省南安第一中学高三二模)过氧化钙可以用于改善地表水质,处理含重金
属粒子废水和治理赤潮,也可用于应急供氧等。实验室模仿工业上生产过氧化钙的主要流程
如下:
已知:①沉淀时需控制温度为0℃左右;
②CaO·8HO呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
2 2
(1)实验装置如下:①沉淀步骤需控制温度为0℃左右,控温直接有效的方法是_______。
②仪器m的名称是_______;装置连接顺序为_______(填序号)。
③沉淀生成的反应方程式为_______。
(2)乙醇洗涤的目的是_______。
(3)请设计实验定性检验产品为CaO(简单地描述实验步骤和现象)_______。
2
(4)产品纯度测定实验步骤如下:
第一步:准确称取ag产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的(NH)CO,沉淀完全,过滤并洗涤沉淀;
4 2 2 4
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:向锥形瓶中滴入几滴MnSO 溶液,然后逐滴滴入浓度为cmol·L-1的KMnO 溶液至终
4 4
点,消耗KMnO 溶液VmL。
4
①滴定前,滴入MnSO 溶液的目的是_______。
4
②产品的纯度为_______(用字母表示)。
③若第三步用稀盐酸溶解,所测纯度_______(填“偏低”“不变”或“偏高”)
47.(2021·广西南宁市·南宁三中高三三模)高氯酸铵(NHClO)为白色晶体,具有不稳定
4 4
性,在400 ℃时开始分解产生多种气体,常用于生产火箭推进剂。某化学兴趣小组同学利用
下列装置对NHClO 的分解产物进行探究。(假设装置内药品均足量,部分夹持装置已省略。)
4 4
(1)在实验过程中发现C中铜粉由红色变为黑色,说明产物中有___________ (填化学式) 生
成。
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红
色石蕊试纸变蓝色的气体,产生该气体的化学方程式为___________。
(3)某同学认为产物中还应有HO和Cl 该同学从理论上分析认为有Cl 存在的理由是
2 2. 2
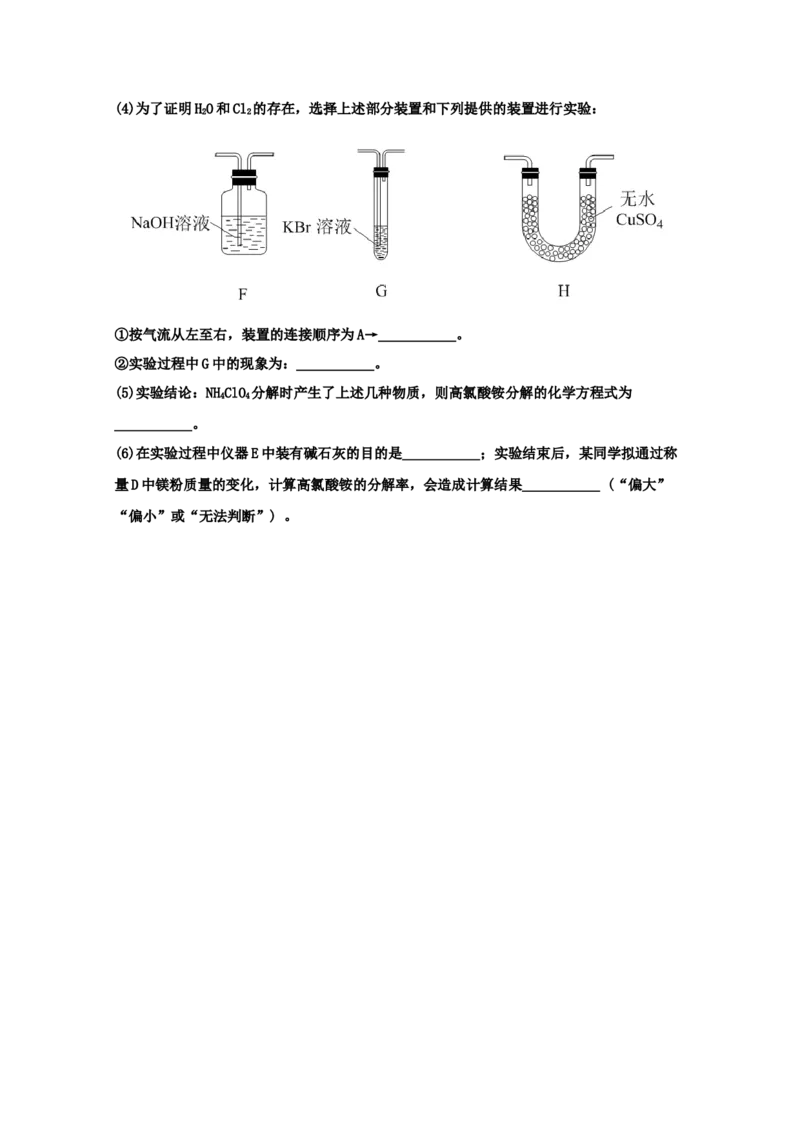
___________。(4)为了证明HO和Cl 的存在,选择上述部分装置和下列提供的装置进行实验:
2 2
①按气流从左至右,装置的连接顺序为A→___________。
②实验过程中G中的现象为:___________。
(5)实验结论:NHClO 分解时产生了上述几种物质,则高氯酸铵分解的化学方程式为
4 4
___________。
(6)在实验过程中仪器E中装有碱石灰的目的是___________;实验结束后,某同学拟通过称
量D中镁粉质量的变化,计算高氯酸铵的分解率,会造成计算结果___________ (“偏大”
“偏小”或“无法判断”) 。