文档内容
专题 10 化学工艺流程(题型突破)
(考试时间:90分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
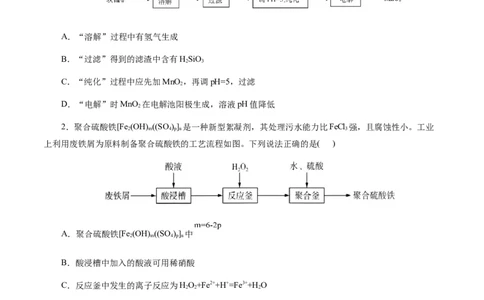
1.工业上常用软锰矿生产纯净的MnO ,工艺流程如图所示,已知软锰矿的主要成分为MnO ,还含
2 2
有少量SiO、Al O。下列说法错误的是( )
2 2 3
A.“溶解”过程中有氢气生成
B.“过滤”得到的滤渣中含有HSiO
2 3
C.“纯化”过程中应先加MnO ,再调pH=5,过滤
2
D.“电解”时MnO 在电解池阳极生成,溶液pH值降低
2
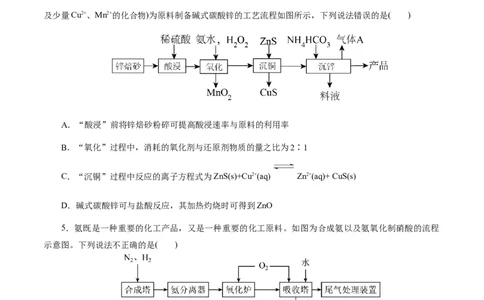
2.聚合硫酸铁[Fe (OH) ((SO )] 是一种新型絮凝剂,其处理污水能力比FeCl 强,且腐蚀性小。工业
2 m 4 p n 3
上利用废铁屑为原料制备聚合硫酸铁的工艺流程如图。下列说法正确的是( )
A.聚合硫酸铁[Fe (OH) ((SO )] 中
2 m 4 p n
B.酸浸槽中加入的酸液可用稀硝酸
C.反应釜中发生的离子反应为HO+Fe2++H+=Fe3++H O
2 2 2
D.聚合釜中控制溶液的pH越大越好
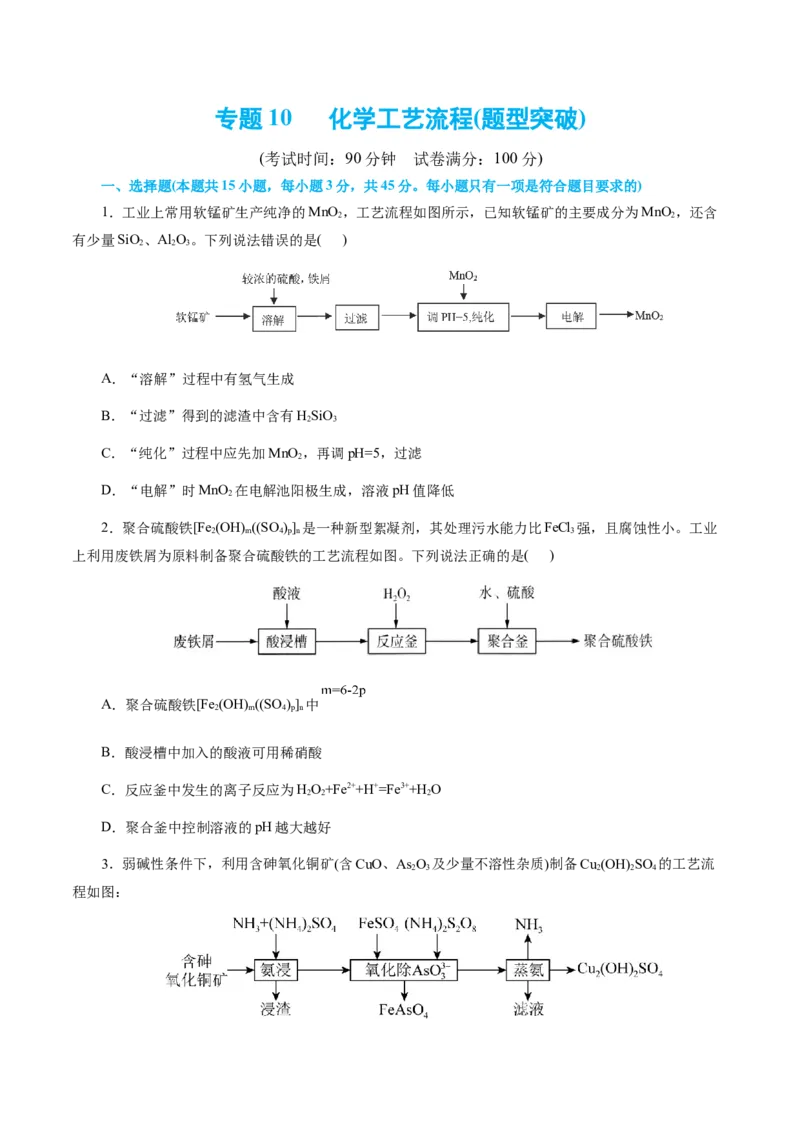
3.弱碱性条件下,利用含砷氧化铜矿(含CuO、As O 及少量不溶性杂质)制备Cu (OH) SO 的工艺流
2 3 2 2 4
程如图:下列说法不正确的是( )
A.“氨浸”时As O 发生的离子反应为:As O+6NH+3H O=6NH ++ 2AsO3-
2 3 2 3 3 2 4 3
B.“氨浸”时CuO转化为[Cu(NH )]2+
3 4
C.“氧化除As O”时每生成1 mol FeAsO ,转移的电子数目为6.02×1023
2 3 4
D.“蒸氨”后滤液中主要存在的离子为:NH +、SO 2-
4 4
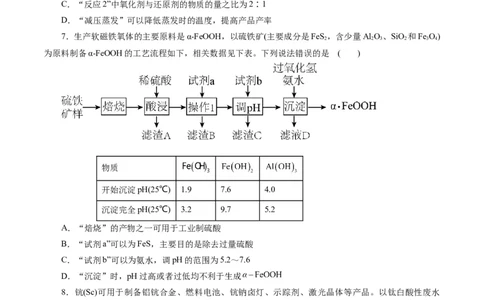
4.碱式碳酸锌 可被用于皮肤保护剂、饲料添加剂等,以锌焙砂(主要成分为ZnO
及少量Cu2+、Mn2+的化合物)为原料制备碱式碳酸锌的工艺流程如图所示,下列说法错误的是( )
A.“酸浸”前将锌焙砂粉碎可提高酸浸速率与原料的利用率
B.“氧化”过程中,消耗的氧化剂与还原剂物质的量之比为2∶1
C.“沉铜”过程中反应的离子方程式为ZnS(s)+Cu2+(aq) Zn2+(aq)+ CuS(s)
D.碱式碳酸锌可与盐酸反应,其加热灼烧时可得到ZnO
5.氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程
示意图。下列说法不正确的是( )
A.合成塔内发生的反应中有非极性键的断裂和极性键的生成
B.氧化炉内发生的反应氧化剂与还原剂的物质的量之比为5∶4
C.使用 溶液吸收尾气中的氮氧化物, 和NO 是酸性氧化物
2
D.向吸收塔中通入O 的作用是氧化
2
6.化学工业为疫情防控提供了强有力的物质支撑。亚氯酸钠(NaClO )具有强氧化性,受热易分解,可
2
作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如下图所示。已知:消毒能力即每克含氯消毒剂的氧化能力相当于多少克Cl 的氧化能力。
2
下列说法错误的是( )
A.“母液”中溶质的主要成分是NaSO
2 4
B.相同质量ClO 的消毒能力是Cl 的2.5倍
2 2
C.“反应2”中氧化剂与还原剂的物质的量之比为2∶1
D.“减压蒸发”可以降低蒸发时的温度,提高产品产率
7.生产软磁铁氧体的主要原料是α-FeOOH,以硫铁矿(主要成分是FeS,含少量Al O、SiO 和Fe O)
2 2 3 2 3 4
为原料制备α-FeOOH的工艺流程如下,相关数据见下表。下列说法错误的是 ( )
物质
开始沉淀pH(25℃) 1.9 7.6 4.0
沉淀完全pH(25℃) 3.2 9.7 5.2
A.“焙烧”的产物之一可用于工业制硫酸
B.“试剂a”可以为FeS,主要目的是除去过量硫酸
C.“试剂b”可以为氨水,调pH的范围为5.2~7.6
D.“沉淀”时,pH过高或者过低均不利于生成
8.钪(Sc)可用于制备铝钪合金、燃料电池、钪钠卤灯、示踪剂、激光晶体等产品。以钛白酸性废水
(主要含 、Fe2+、Sc3+)为原料制备氧化钪(ScO)的工艺流程如下。下列说法正确的是( )
2 3
A.酸洗时加入HO 的目的是将Ti 4+还原为Ti2+
2 2
B.“操作Ⅰ”需要的玻璃仪器有分液漏斗C.“滤渣Ⅰ”的主要成分是Ti (OH)、Fe(OH)
4 3
D.草酸钪焙烧时反应的化学方程式:2Sc(C O)+3O 2ScO+12CO
2 2 4 3 2 2 3 2
9.高铁酸钾(K FeO)具有杀菌消毒及净水作用,某实验小组在碱性条件下制备 KFeO 流程如图所
2 4 2 4
示:
下列说法错误的是( )
A.1molK FeO 消毒能力相当于1.5mol HClO
2 4
B.氧化反应:3NaClO+2Fe(NO )+10 NaOH=2Na FeO+3NaCl+6 NaNO +5H O
3 3 2 4 3 2
C.同温度时高铁酸钠溶解度大于高铁酸钾
D.提纯时,应用到的玻璃仪器有蒸发皿、玻璃棒、烧杯、酒精灯
10.硫代硫酸钠晶体(NaSO·5H O)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要
2 2 3 2
成分NaS,含少量NaSO )及纯碱等为原料制备NaSO·5H O的流程如下:
2 2 4 2 2 3 2
下列说法正确的是( )
A.NaSO 作脱氯剂时主要利用其氧化性
2 2 3
B.“净化”时加入的试剂X可选用BaCl 溶液
2
C.“反应”过程中体系pH大小对产品产率无影响
D.提纯NaSO·5H O时,应先用水洗,再用乙醇洗涤
2 2 3 2
11.为研究废旧电池的再利用,实验室利用旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的
部分实验过程如图所示。下列叙述错误的是( )A.“溶解” 操作中溶液温度不宜过高
B.铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的氧气或HO
2 2
C.过滤后滤液中只有ZnSO
4
D.本流程涉及置换反应
12.锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiC O 及少量Al,Fe等,处理该
O 2
废料的一种工艺流程如图所示:
已知LiC O 难溶于水,具有强氧化性。下列说法正确的是( )
O 2
A.滤液1中含有的阳离子主要是Al3+和Na+
B.“还原”时,参加反应n(C 3+):n(SO 2-)=2:1
O 3
C.“沉钴”离子方程式为C 2++HCO-= C CO↓+H+
O 3 O 3
D.滤渣主要是Fe(OH) ,滤液2中仅含有一种溶质
3
13.下图是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
已知:室温饱和HS溶液的pH的为3.9,SnS沉淀完全时溶液的pH为1.6,FeS开始沉淀时溶液的pH
2
为3.0,沉淀完全时的pH为5.5
根据以上流程图。下列说法错误的是( )
A.“溶解”中用到25%的稀硫酸,可用98%浓硫酸配制,需玻璃棒、烧杯、量筒、胶头滴管等仪器
B.操作II中用硫酸酸化至pH=2的主要目的是抑制Fe2+的水解
C.操作II中,通入HS至饱和的目的之一是防止Fe2+被氧化
2
D.操作IV中所得的晶体最后用乙醇洗去晶体表面附着的水分14.某废催化剂主要含Al、Ni、Mo(钼)等的氧化物,回收利用其金属资源的流程如下:
已知:碱性条件下,Mo元素以MoO 2-的形态存在;K (BaMoO )=3.5×10-8。
4 sp 4
下列有关说法不正确的是( )
A.焙烧时,Al O 与NaOH反应的化学方程式为Al O+2NaOH 2NaAlO +H O
2 3 2 3 2 2
B.水浸时,控制适当温度并不断搅拌,有利于提高铝、钼浸取率
C.沉铝后,过滤所得滤渣的主要成分是Al(OH)
3
D.沉钼后,过滤所得滤液中不存在MoO 2-
4
15.某废矿渣的主要成分有FeO、NiO、Al O、SiO,为节约和充分利用资源,通过如图工艺流程回
2 3 2
收铁、镍。下列说法错误的是( )
已知:ⅰ.常温下,K (NiCO)=1.4×10-7;K [Ni(OH) ]=1.0×10-15。
sp 3 sp 2
ⅱ.“萃取”可将金属离子进行富集与分离,原理如下:X2+(水相)+2RH(有机相) XR (有机相)
2
+2H+(水相)。
A.滤液①中,主要存在的钠盐有NaAlO 、NaSiO
2 2 3
B.“反萃取”应控制在酸性环境进行
C.“沉镍”过程中反应方程式为:Ni2++2HCO-=NiCO ↓+CO ↑+H O,“沉镍”时若溶液pH越大,越
3 3 2 2
能充分吸收二氧化碳,NiCO 的产率越高
3
D.已知“水相”中c(Ni2+)=2×10-2mol•L-1,加NaHCO “沉镍”,当沉镍率达到99%时,溶液中
3c(CO2-)=7×10-4mol•L-1
3
二、非选择题(本题包括4小题,共55分)
16.(12分)钒(V)是一种重要的金属,有金属“维生素”之称,用途涵盖了航空航天、电池、光学、医
药等众多领域,主要由五氧化二钒冶炼得到。某种由钒精矿(含VO 及少量MgO、SiO 等杂质)提取五氧化
2 5 2
二钒的工艺流程如下图所示。
【资料】+5价钒在溶液中的主要存在形式与溶液pH的关系:
PH 4~6 6~8 8~10 10~12
主要离子
(1)钒精矿磨细的目的是_______,浸出液中含有钒酸钠(Na VO )。VO 3-与PO 3-的空间构型相同,键角
3 4 4 4
的大小为_______。
(2)用硫酸缓慢调节浸出液的pH为7,得到净化液中主要的阴离子是_______。
(3)氨化沉钒:将净化液中的钒转化为NH VO 固体,其流程如下。
4 3
向(NH )VO 溶液中加入NHCl溶液的目的:_______。
4 3 4 4
(4)煅烧2.340g偏钒酸铵(NH VO ,摩尔质量为117g/mol)时,其固体质量的减少量随温度变化的曲线
4 3
如图所示:100~200℃时产生的一种气体的化学式为_______,300~350℃时发生反应的化学方程式为_______。
17.(13分)聚合硫酸铁(Ⅲ)[Fe (OH) (SO )] 是一种新型,优质、高效铁盐类无机高分子絮凝剂,极易
2 x 4 y n
溶于水,广泛应用于饮用水、各种工业废水、城市污水、污泥脱水等的净化处理。工业上用高硫铝土矿(主
要成分为Fe O、Al O、SiO,少量FeS)为原料制备聚合硫酸铁的部分工艺流程如下:
2 3 2 3 2 2
(1)写出焙烧产生的SO 气体在工业上的一种用途_______。
2
(2)“滤液”中存在的阴离子主要为OH-及_______(填离子符号)。
(3)氧化过程中加入双氧水的目的为_______,实际生产过程中温度不宜过高且要控制HO 的投加速
2 2
度,其原因为_______。
(4)在焙烧时若通入的空气量不足,Fe O 与FeS 之间可以反应生成Fe O 和SO 、Fe O 与FeS 之间反
2 3 2 3 4 2 2 3 2
应时理论上完全反应消耗的n(FeS ):n(Fe O)=_______。
2 2 3
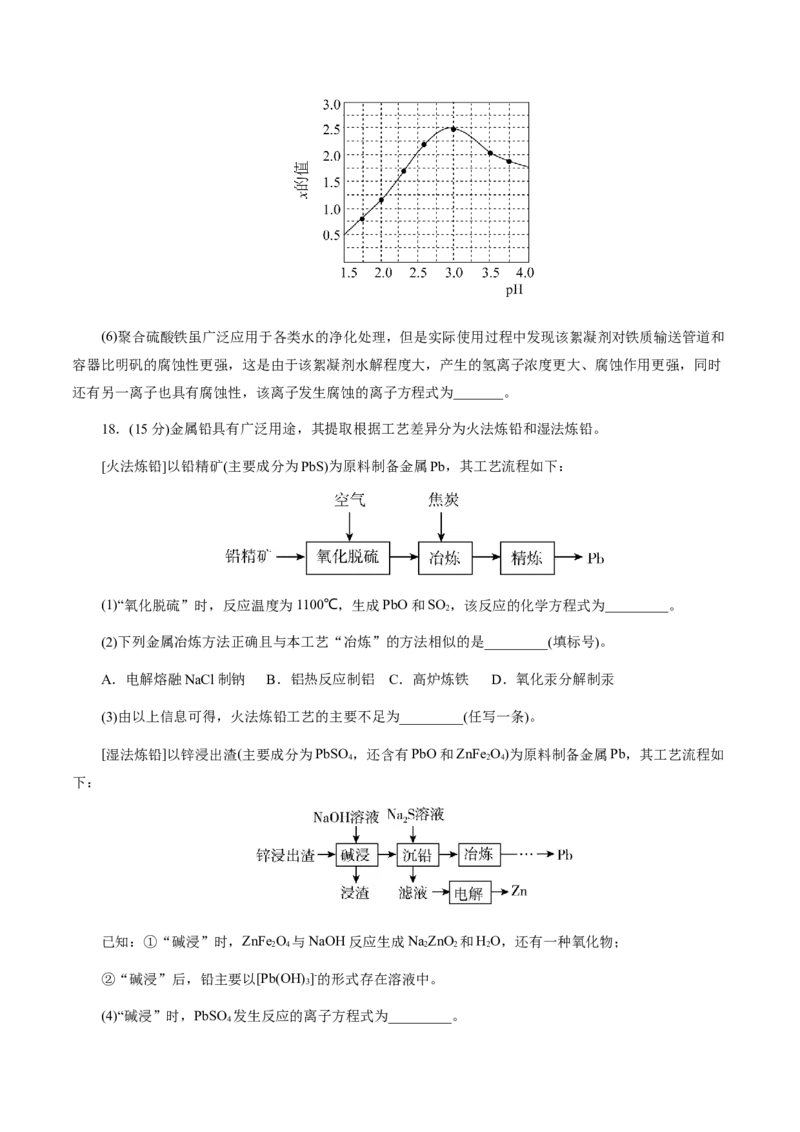
(5)加入试剂A的目的是通过调节pH促进聚合物的形成,所加试剂A为_______(填化学式),溶液的
pH对[Fe (OH) (SO )] 中x的值有较大影响(如下图所示),试分析pH过大(pH>3.0)导致聚合硫酸铁中x的
2 x 4 y n
值减小的原因_______。(6)聚合硫酸铁虽广泛应用于各类水的净化处理,但是实际使用过程中发现该絮凝剂对铁质输送管道和
容器比明矾的腐蚀性更强,这是由于该絮凝剂水解程度大,产生的氢离子浓度更大、腐蚀作用更强,同时
还有另一离子也具有腐蚀性,该离子发生腐蚀的离子方程式为_______。
18.(15分)金属铅具有广泛用途,其提取根据工艺差异分为火法炼铅和湿法炼铅。
[火法炼铅]以铅精矿(主要成分为PbS)为原料制备金属Pb,其工艺流程如下:
(1)“氧化脱硫”时,反应温度为1100℃,生成PbO和SO ,该反应的化学方程式为_________。
2
(2)下列金属冶炼方法正确且与本工艺“冶炼”的方法相似的是_________(填标号)。
A.电解熔融NaCl制钠 B.铝热反应制铝 C.高炉炼铁 D.氧化汞分解制汞
(3)由以上信息可得,火法炼铅工艺的主要不足为_________(任写一条)。
[湿法炼铅]以锌浸出渣(主要成分为PbSO ,还含有PbO和ZnFe O)为原料制备金属Pb,其工艺流程如
4 2 4
下:
已知:①“碱浸”时,ZnFe O 与NaOH反应生成NaZnO 和HO,还有一种氧化物;
2 4 2 2 2
②“碱浸”后,铅主要以[Pb(OH) ]-的形式存在溶液中。
3
(4)“碱浸”时,PbSO 发生反应的离子方程式为_________。
4(5)“浸渣”的主要成分为_________(填化学式)。
(6)“碱浸”液经处理后所得溶液[ 、 ]用于“沉铅”。
①“沉铅”时,理论上,当PbS完全沉淀时 ,ZnS_________(是或否)开始沉淀,通
过计算说明_________[已知: 、 ]。
②“滤液”中主要含有的金属阳离子有_________。
19.(15分)工业利用闪锌矿(主要成分ZnS,还含有FeS、CuFeS、石英及F-、Cl -等杂质)富氧酸浸提
2
取锌,同时实现环保除铁的工艺流程如下:
已知:①酸性条件下,亚铜离子易发生歧化反应;
②CaF 易形成胶体。
2
回答下列问题:
(1)“浸出”过程原理如图1a所示,ZnS “浸出”的总反应的化学方程式为___________。对比人造闪锌
矿浸出原理(如图1b所示),可知“浸出”过程中Fe2+的作用为___________。
(2)“滤渣1”主要成分为___________。
(3)“加热加压氧化”发生反应的离子方程式为___________。
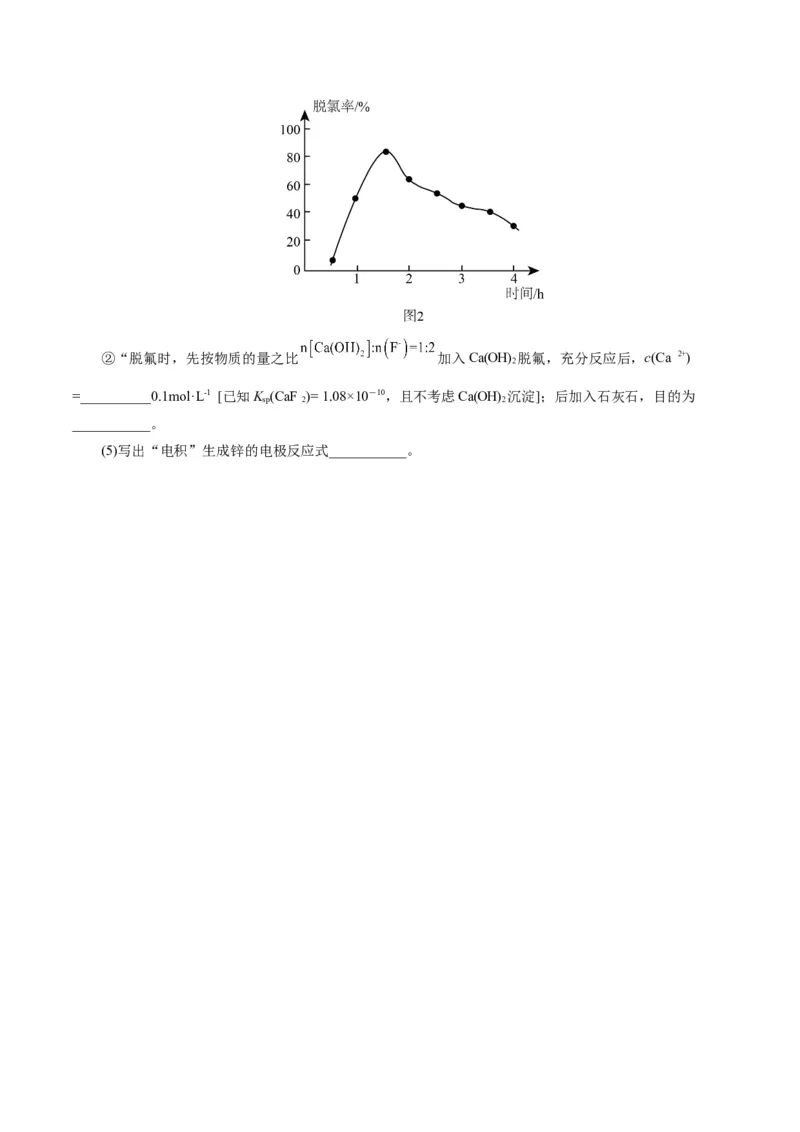
(4)“电积”时,F-、Cl -会腐蚀电极板,需提前除净。
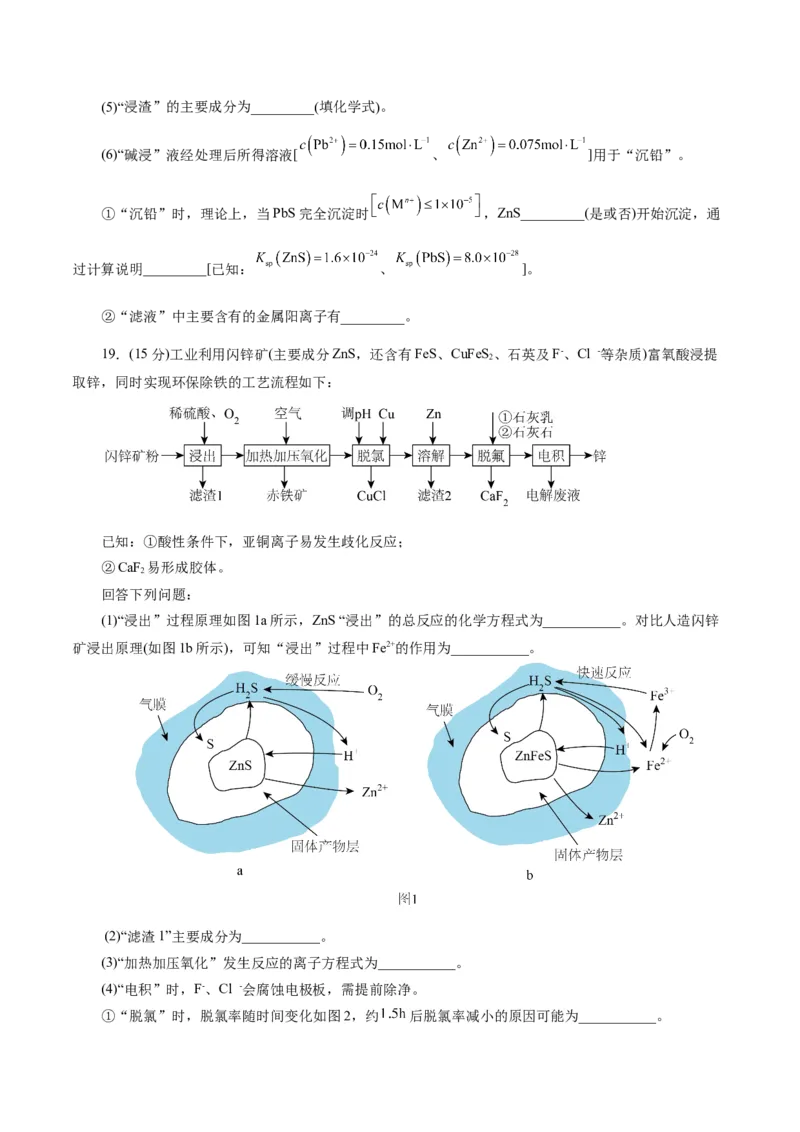
①“脱氯”时,脱氯率随时间变化如图2,约 后脱氯率减小的原因可能为___________。②“脱氟时,先按物质的量之比 加入Ca(OH) 脱氟,充分反应后,c(Ca 2+)
2
=__________0.1mol·L-1 [已知K (CaF )= 1.08×10-10,且不考虑Ca(OH) 沉淀];后加入石灰石,目的为
sp 2 2
___________。
(5)写出“电积”生成锌的电极反应式___________。