文档内容
专题 11 水溶液中离子反应
1.了解电解质的概念;了解强电解质和弱电解质的概念;
2.了解电解质在水溶液中的电离,以及电解质溶液的导电性;
3.了解弱电解质在水溶液中的电离平衡;
4.了解水的电离,水的离子积常数;
考纲
5.了解溶液pH的定义;了解测定溶液pH的方法,能进行pH的简单计算;
6.了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用;
7.了解难溶电解质的溶解平衡;
8.了解溶度积的含义,能用平衡移动原理分析沉淀溶解、生成和转化过程。
水溶液中的离子平衡是化学平衡的延伸和应用,也是高考中考点分布较多的内容之一。
一是在选择题某一选项中以图像或者文字的形式考查,二是在填空题中结合化学反应原
理综合考查。从高考命题的变化趋势来看,溶液中离子浓度的大小比较及沉淀的溶解平
考情预测 衡和转化是主流试题。此类题目考查的内容既与盐的水解有关,又与弱电解质的电离平
衡有关。题目不仅偏重考查粒子的浓度大小顺序,而且还侧重溶液中的各种守恒(电荷守
恒、物料守恒、质子守恒)关系的考查,从而使题目具有一定的综合性、灵活性和技巧
性。
核心素养 宏观辨识与微观探析 证据推理与模型认知高频考点一 弱电解质的电离平衡
1.弱电解质
(1)概念
(2)与化合物类型的关系
强电解质主要是大部分离子化合物及某些共价化合物,弱电解质主要是某些共价化合物。
2.弱电解质的电离平衡
(1)电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成弱电解质分子的速率相等
时,溶液中各分子和离子的浓度都不再发生变化,电离过程达到了平衡。
平衡建立过程的v-t图像如图所示。
(2)弱电解质电离平衡的特征
3.影响电离平衡的外界条件
外界条件 电离平衡移动方向 电离程度变化
温度 升高温度 向右移动 增大
浓度 稀释溶液 向右移动 增大加入与弱电解质相同离子
相同离子 向左移动 减小
的强电解质
加入能与弱电解质离子
向右移动 增大 增大
反应的物质
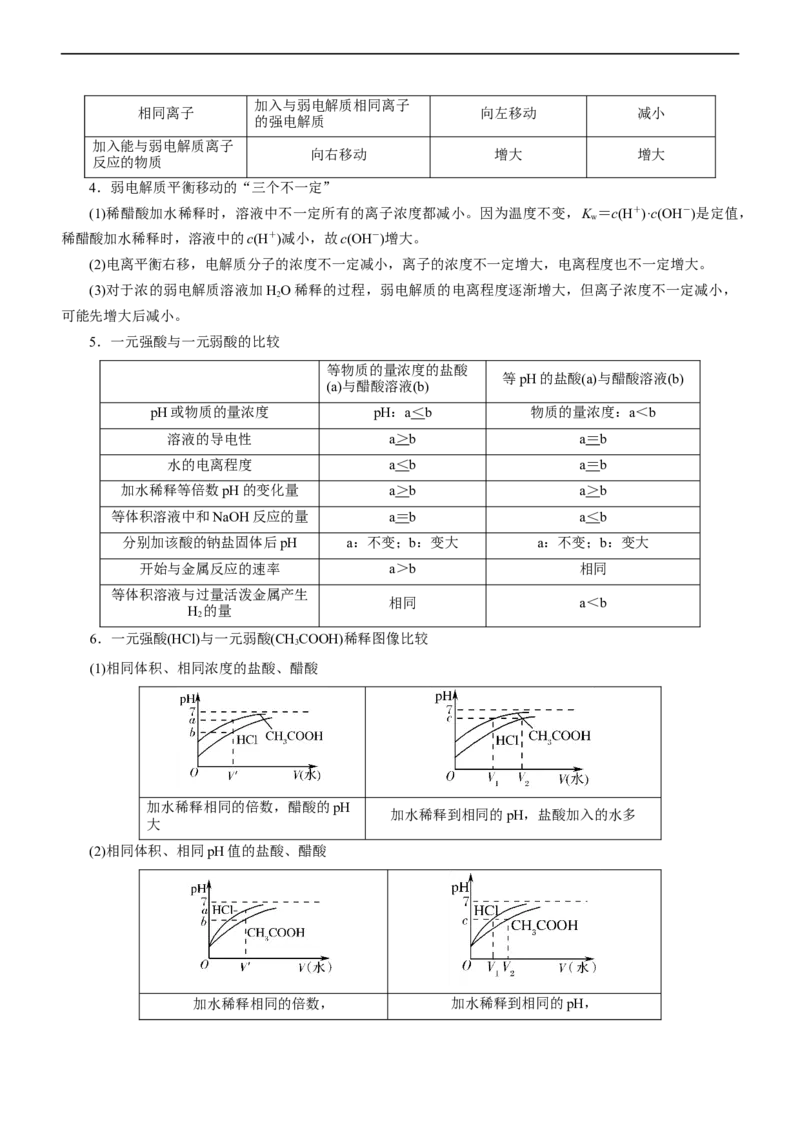
4.弱电解质平衡移动的“三个不一定”
(1)稀醋酸加水稀释时,溶液中不一定所有的离子浓度都减小。因为温度不变,K =c(H+)·c(OH-)是定值,
w
稀醋酸加水稀释时,溶液中的c(H+)减小,故c(OH-)增大。
(2)电离平衡右移,电解质分子的浓度不一定减小,离子的浓度不一定增大,电离程度也不一定增大。
(3)对于浓的弱电解质溶液加HO稀释的过程,弱电解质的电离程度逐渐增大,但离子浓度不一定减小,
2
可能先增大后减小。
5.一元强酸与一元弱酸的比较
等物质的量浓度的盐酸
等pH的盐酸(a)与醋酸溶液(b)
(a)与醋酸溶液(b)
pH或物质的量浓度 pH:a<b 物质的量浓度:a<b
溶液的导电性 a>b a=b
水的电离程度 a<b a=b
加水稀释等倍数pH的变化量 a>b a>b
等体积溶液中和NaOH反应的量 a=b a<b
分别加该酸的钠盐固体后pH a:不变;b:变大 a:不变;b:变大
开始与金属反应的速率 a>b 相同
等体积溶液与过量活泼金属产生
相同 a<b
H 的量
2
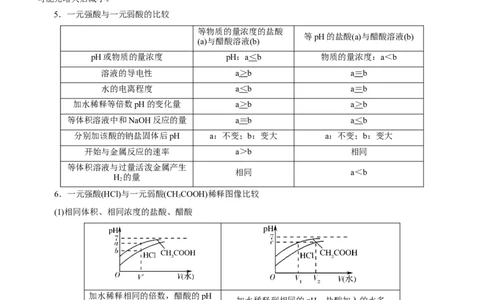
6.一元强酸(HCl)与一元弱酸(CHCOOH)稀释图像比较
3
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH
加水稀释到相同的pH,盐酸加入的水多
大
(2)相同体积、相同pH值的盐酸、醋酸
加水稀释相同的倍数, 加水稀释到相同的pH,盐酸的pH大 醋酸加入的水多
7.电离平衡常数
(1)①填写下表(25 ℃)
弱电解质 电离方程式 电离常数
NH ·H O NH ·H O NH+OH- K =1.8×10-5
3 2 3 2 b
CHCOOH CHCOOH CHCOO-+H+ K=1.8×10-5
3 3 3 a
HClO HClO H++ClO- K=3.0×10-8
a
②CHCOOH酸性大于(填“大于”“小于”或“等于”)HClO酸性,判断的依据:相同条件下,电离常
3
数越大,电离程度越大,c(H+)越大,酸性越强。
③电离平衡常数的意义:弱酸、弱碱的电离平衡常数能够反映酸碱性的相对强弱。电离平衡常数越大,电
离程度越大。多元弱酸的电离以第一步电离为主,各级电离平衡常数的大小差距较大。
④外因对电离平衡常数的影响:电离平衡常数与其他化学平衡常数一样只与温度有关,与电解质的浓度无
关,升高温度,K值增大,原因是电离是吸热过程。
(2)多元弱酸的分步电离,以碳酸为例,碳酸是二元弱酸,在水溶液中的电离是分步进行。
①电离方程式是HCO H++HCO,HCO H++CO。
2 3
②电离平衡常数表达式: , 。
③比较大小:K >K 。
a1 a2
【典例剖析】
【例1】(2021•浙江6月选考)某同学拟用pH计测定溶液pH以探究某酸HR是否为弱电解质。下列说法正确
的是( )
A.25℃时,若测得0.01mol·Lˉ1NaR溶液pH=7,则HR是弱酸
B.25℃时,若测得0.01mol·Lˉ1HR溶液pH>2且pH<7,则HR是弱酸
C.25℃时,若测得HR溶液pH= a,取该溶液10.0mL,加蒸馏水稀释至100.0mL,测得pH= b,b-a<
1,则HR是弱酸
D.25℃时,若测得NaR溶液pH= a,取该溶液10.0mL,升温至50℃,测得pH= b,a>b,则HR是弱
酸
【答案】B
【解析】A项,25℃时,若测得0.01mol·Lˉ1NaR溶液pH=7,可知NaR为强酸强碱盐,则HR为强酸,A
错误;B项,25℃时,若测得0.01mol·Lˉ1HR溶液pH>2且pH<7,可知溶液中c(H+)<0.01mol·Lˉ1,所以HR
未完全电离,HR为弱酸,B正确;C项,假设HR为强酸,取pH=6的该溶液10.0mL,加蒸馏水稀释至
100.0mL测得此时溶液pH<7,C错误;D项,假设HR为强酸,则NaR为强酸强碱盐,溶液呈中性,升温至50℃,促进水的电离,水的离子积常数增大,pH减小,D错误;故选B。
【例2】(2022•全国乙卷)常温下,一元酸 的K(HA)=1.0×10-3。在某体系中, 与A-离子不能穿过隔膜,
a
未电离的 可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
【答案】B
【解析】A项,常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A
错误;B项,常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)
a 总
+c(A-),则 =1.0×10-3,解得 = ,B正确;C项,根据题意,未电离的HA可自由穿过
隔膜,故溶液I和II中的c(HA)相等,C错误;D项,常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,
K = =1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶液I中c
a 总 总
(HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)
a 总+c(A-), =1.0×10-3,溶液II中c (HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液I
总
和II中的c(HA)相等,溶液I和II中c (HA)之比为[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;
总
故选B。
【变式探究】
1.能证明亚硝酸是弱酸的实验事实是( )
A.HNO 的酸性比CHCOOH强 B.0.1 mol·L-1NaNO 溶液的pH大于7
2 3 2
C.HNO 溶液与NaCO 反应生成CO D.HNO 不稳定可分解成NO和NO
2 2 3 2 2 2
【答案】B
【解析】A 项, HNO 的酸性比 CHCOOH 强,不能说明是弱酸,故 A 不符合题意;B 项,0.1
2 3
mol·L-1NaNO 溶液的pH大于7,说明亚硝酸根水解,亚硝酸是弱酸,故 B符合题意;C项,HNO 溶液与
2 2
NaCO 反应生成CO ,只能说明亚硝酸酸性大于碳酸,不能说明亚硝酸是弱酸,故 C不符合题意;D项,
2 3 2
HNO 不稳定可分解成NO和NO ,只能说明亚硝酸是不稳定性酸,不能说明亚硝酸是弱酸,故 D不符合题意。
2 2
故选B。
2.已知某温度下CHCOOH和NH ·H O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CHCOOH溶
3 3 2 3
液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B. 先增大再减小
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
【答案】D
【解析】A项,醋酸显酸性,水的电离平衡受到抑制,在滴加 NH ·H O的过程中,酸性减弱,水的电离
3 2
程度受到抑制的程度减小,电离程度增大,当CHCOOH反应完后,加入的NH ·H O会抑制水的电离,电离
3 3 2
程度减小,故该选项错误;B项,在向醋酸中滴加氨水的过程中,碱性增强酸性减弱,c(OH-)一直增大。由
NH ·H ONH+OH-可知,K=,则 ,而K是常数,故 直减小,该选
3 2
项错误;C 项,n(CHCOOH)与 n(CHCOO-)之和保持不变,但溶液的体积是增大的,故 c(CHCOOH)与
3 3 3
c(CHCOO-)之和逐渐减小,该选项错误;D 项,当加入氨水 10 mL 时,两者恰好完全反应生成
3
CHCOONH ,由CHCOOH和NH ·H O的电离常数相等可知,CHCOO-和NH的水解程度也相等,故c(NH)
3 4 3 3 2 3=c(CHCOO-),该选项正确。
3
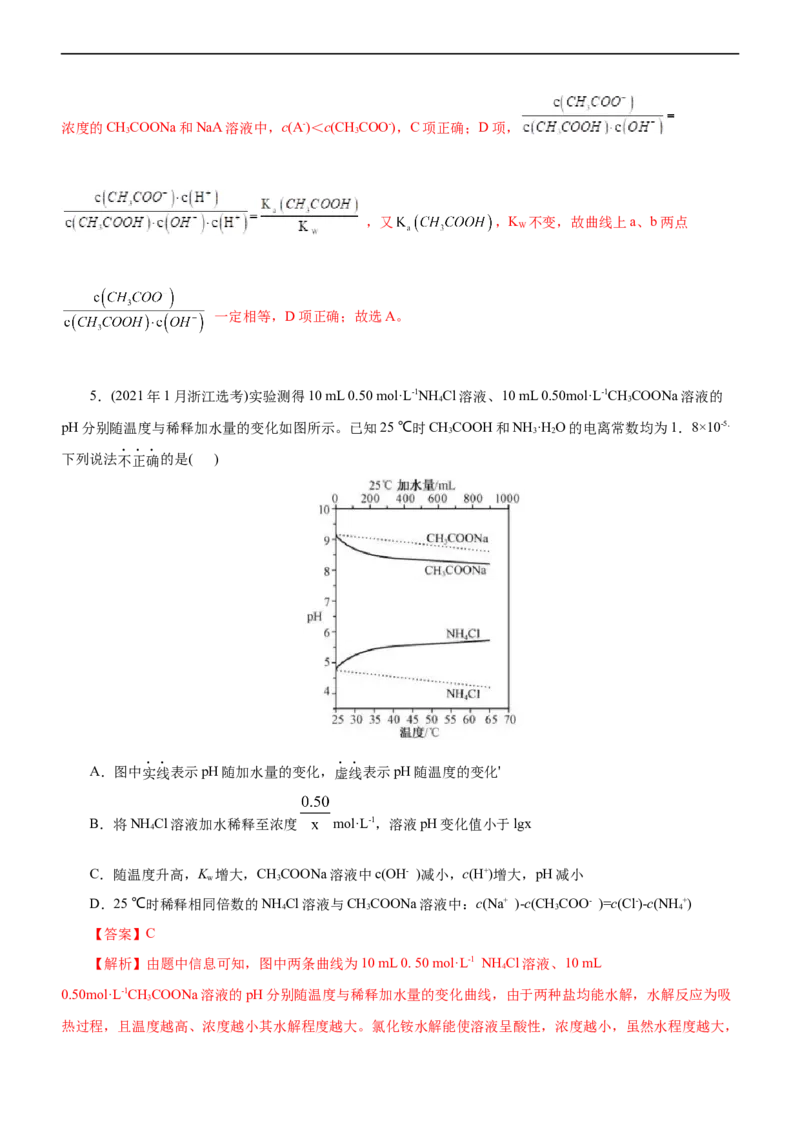
3.常温下pH=2的两种酸溶液A和B,分别加水稀释1 000倍,其pH与所加水的体积变化如图所示。下
列结论正确的是( )
A.B酸比A酸的电离度大 B.A为弱酸,B为强酸
C.B酸的物质的量浓度比A的小 D.A酸比B酸易电离
【答案】D
【解析】根据图示可知溶液稀释1 000倍后,A酸溶液pH变化大,说明A酸酸性大于B酸酸性。则B酸
为弱酸,其电离度应比A酸小,A酸易电离。同为pH=2,B酸溶液物质的量浓度一定比A酸溶液浓度大。
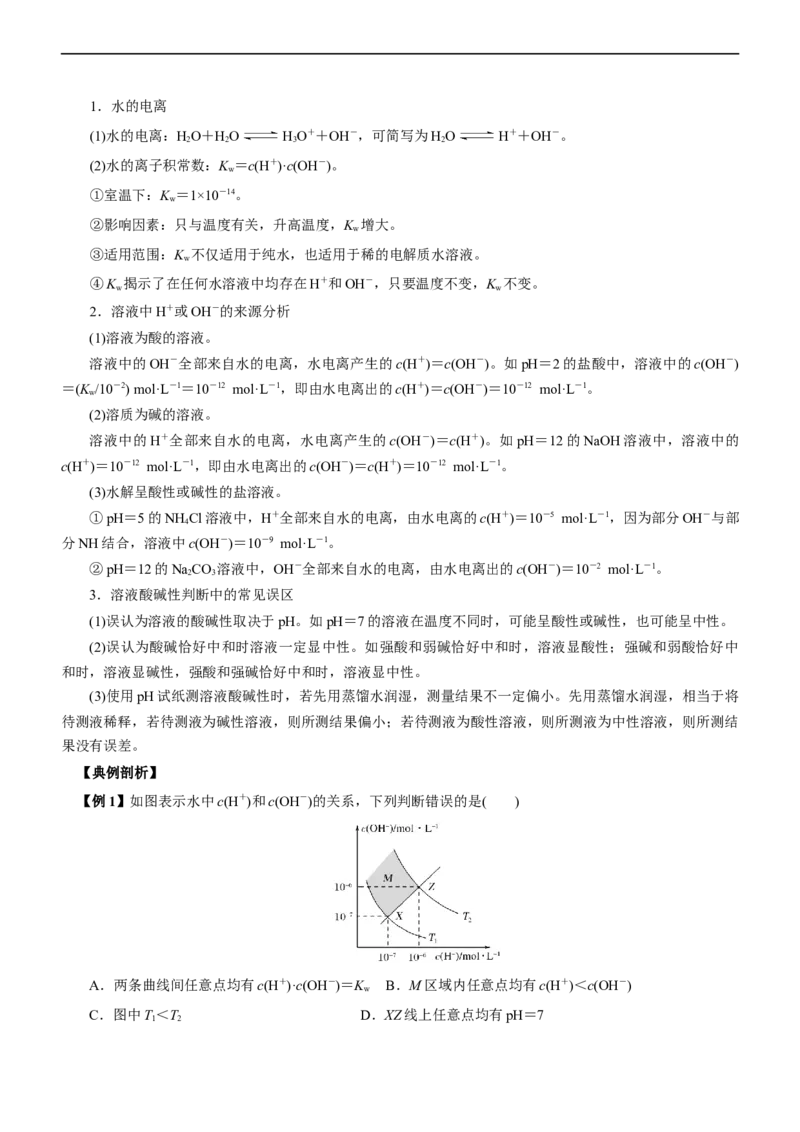
4.(2023·河北省部分学校高三联考)在25℃下,稀释CHCOOH和某酸HA的溶液,溶液pH变化的曲线
3
如图所示,其中V 表示稀释前的体积,V 表示稀释后的体积,下列说法错误的是( )
1 2
A. ,两种酸溶液pH相同时,c(HA)<c(CHCOOH)
3
B.a、b两点中,水的电离程度a小于b
C.25℃时,等浓度的CHCOONa与NaA溶液中,c(A-)<c(CHCOO-)
3 3
D.曲线上a、b两点中, 的比值一定相等
【答案】A
【解析】A项, m<4,两种酸都是弱酸,HA的酸性小于CHCOOH,故pH相同时, c(CHCOOH)<
3 3
c(HA),A项错误;B项,a点pH小于b点pH,则a溶液中c(H+)大,对水的电离抑制程度大,因此水的电离
程度:a小于b,B项正确;C项,CHCOOH和HA都是弱酸,其中HA的酸性弱于CHCOOH,25℃时,等
3 3浓度的CHCOONa和NaA溶液中,c(A-)<c(CHCOO-),C项正确;D项,
3 3
,又 ,K 不变,故曲线上a、b两点
W
一定相等,D项正确;故选A。
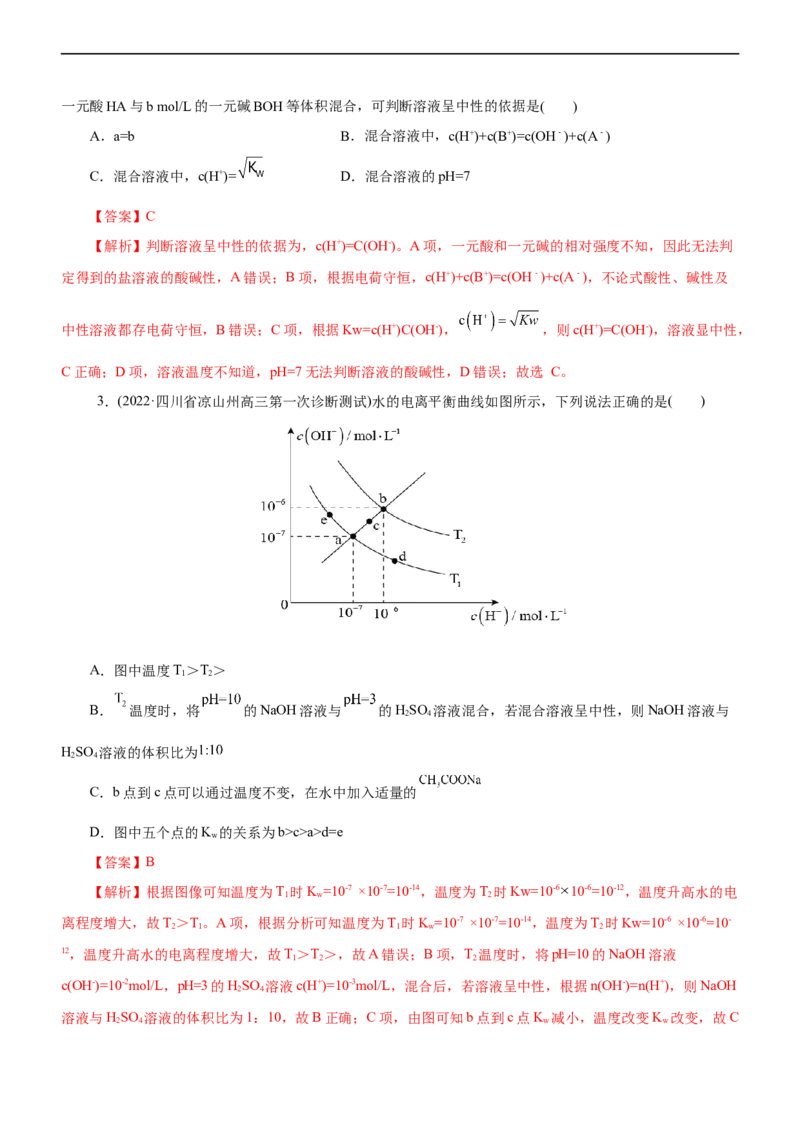
5.(2021年1月浙江选考)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的
4 3
pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-5.
3 3 2
下列说法不正确的是( )
A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B.将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH +)
4 3 3 4
【答案】C
【解析】由题中信息可知,图中两条曲线为10 mL 0. 50 mol·L-1 NH Cl溶液、10 mL
4
0.50mol·L-1CHCOONa溶液的pH分别随温度与稀释加水量的变化曲线,由于两种盐均能水解,水解反应为吸
3
热过程,且温度越高、浓度越小其水解程度越大。氯化铵水解能使溶液呈酸性,浓度越小,虽然水程度越大,但其溶液的酸性越弱,故其pH越大;醋酸钠水解能使溶液呈碱性,浓度越小,其水溶液的碱性越弱,故其pH
越小。温度越高,水的电离度越大。因此,图中的实线为pH随加水量的变化,虚线表示pH随温度的变化。A
项,由分析可知,图中实线表示pH随加水量的变化,虚线表示pH随温度的变化,A说法正确;B项,将
NH Cl溶液加水稀释至浓度 mol·L-1时,若氯化铵的水解平衡不发生移动,则其中的c(H+)变为原来的 ,
4
则溶液的pH将增大lgx,但是,加水稀释时,氯化铵的水解平衡向正反应方向移动,c(H+)大于原来的 ,因
此,溶液pH的变化值小于lgx,B说法正确;C项,随温度升高,水的电离程度变大,因此水的离子积变大,
即K 增大;随温度升高,CHCOONa的水解程度变大,溶液中c(OH-)增大,因此,C说法不正确;D项,
w 3
25℃时稀释相同倍数的NH C1溶液与CHCOONa溶液中均分别存在电荷守恒,c(Na+ ) +c(H+) =c(OH-)
4 3
+c(CHCOO- ) ,c(NH +)+c(H+ ) =c(Cl-)+c(OH- )。因此,氯化铵溶液中,c(Cl-)-c(NH +) =c(H+ )-c(OH- ),醋酸
3 4 4
钠溶液中,c(Na+ )-c(CHCOO- )= c(OH-) -c(H+) 。由于25 ℃时CHCOOH和NH ·H O的电离常数均为1.8
3 3 3 2
×10-5,因此,由于原溶液的物质的量浓度相同,稀释相同倍数后的NH C1溶液与CHCOONa溶液,溶质的物
4 3
质的量浓度仍相等,由于电离常数相同,其中盐的水解程度是相同的,因此,两溶液中c(OH-) -c(H+)(两者差
的绝对值)相等,故c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH +),D说法正确。故选C。
3 4
以一元强酸(HCl)与一元弱酸(CHCOOH)的比较为例
3
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较项
目 c(H+) pH 中和碱的能 与活泼金属反应产 开始与金属反
力 生H 的量 应的速率
2
酸
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较
中和碱的 与足量活泼金属反 开始与金属反
项目 c(H+) c(酸)
能力 应产生H 的量 应的速率
2
酸
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
高频考点二 水的电离和溶液的酸碱性1.水的电离
(1)水的电离:HO+HO HO++OH-,可简写为HO H++OH-。
2 2 3 2
(2)水的离子积常数:K =c(H+)·c(OH-)。
w
①室温下:K =1×10-14。
w
②影响因素:只与温度有关,升高温度,K 增大。
w
③适用范围:K 不仅适用于纯水,也适用于稀的电解质水溶液。
w
④K 揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K 不变。
w w
2.溶液中H+或OH-的来源分析
(1)溶液为酸的溶液。
溶液中的OH-全部来自水的电离,水电离产生的c(H+)=c(OH-)。如pH=2的盐酸中,溶液中的c(OH-)
=(K /10-2) mol·L-1=10-12 mol·L-1,即由水电离出的c(H+)=c(OH-)=10-12 mol·L-1。
w
(2)溶质为碱的溶液。
溶液中的H+全部来自水的电离,水电离产生的c(OH-)=c(H+)。如pH=12的NaOH溶液中,溶液中的
c(H+)=10-12 mol·L-1,即由水电离出的c(OH-)=c(H+)=10-12 mol·L-1。
(3)水解呈酸性或碱性的盐溶液。
①pH=5的NH Cl溶液中,H+全部来自水的电离,由水电离的c(H+)=10-5 mol·L-1,因为部分OH-与部
4
分NH结合,溶液中c(OH-)=10-9 mol·L-1。
②pH=12的NaCO 溶液中,OH-全部来自水的电离,由水电离出的c(OH-)=10-2 mol·L-1。
2 3
3.溶液酸碱性判断中的常见误区
(1)误认为溶液的酸碱性取决于pH。如pH=7的溶液在温度不同时,可能呈酸性或碱性,也可能呈中性。
(2)误认为酸碱恰好中和时溶液一定显中性。如强酸和弱碱恰好中和时,溶液显酸性;强碱和弱酸恰好中
和时,溶液显碱性,强酸和强碱恰好中和时,溶液显中性。
(3)使用pH试纸测溶液酸碱性时,若先用蒸馏水润湿,测量结果不一定偏小。先用蒸馏水润湿,相当于将
待测液稀释,若待测液为碱性溶液,则所测结果偏小;若待测液为酸性溶液,则所测液为中性溶液,则所测结
果没有误差。
【典例剖析】
【例1】如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)·c(OH-)=K B.M区域内任意点均有c(H+)<c(OH-)
w
C.图中T<T D.XZ线上任意点均有pH=7
1 2【答案】D
【解析】由水的离子积的定义知两条曲线间任意点均有c(H+)·c(OH-)=K ,A项正确;由图中纵横轴的大
w
小可知M区域内任意点均有c(H+)<c(OH-),B项正确;温度越高,水的电离程度越大,电离出的c(H+)与
c(OH-)越大,所以T >T ,C项正确;XZ线上任意点都有c(H+)=c(OH-),只有当c(H+)=10-7 mol·L-1时,
2 1
才有pH=7,D项错误。
【例2】 (2022·浙江省1月选考)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是(
2 a1 a2
)
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】A项,在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,
2
故A错误;B项,向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,
2
,则HA的电离度 0.013%,故B正确;C项,向
2
HA溶液中加入NaOH溶液至pH=11, ,则c(A2-)c>a>d=e
w
【答案】B
【解析】根据图像可知温度为T 时K =10-7 ×10-7=10-14,温度为T 时Kw=10-6 10-6=10-12,温度升高水的电
1 w 2
离程度增大,故T>T。A项,根据分析可知温度为T 时K =10-7 ×10-7=10-14,温度为T 时Kw=10-6 ×10-6=10-
2 1 1 w 2
12,温度升高水的电离程度增大,故T>T>,故A错误;B项,T 温度时,将pH=10的NaOH溶液
1 2 2
c(OH-)=10-2mol/L,pH=3的HSO 溶液c(H+)=10-3mol/L,混合后,若溶液呈中性,根据n(OH-)=n(H+),则NaOH
2 4
溶液与HSO 溶液的体积比为1:10,故B正确;C项,由图可知b点到c点K 减小,温度改变K 改变,故C
2 4 w w错误;D项,温度不变K ,温度升高K 增大,a、e、d三点温度相同故K 相同,从a到b温度依次升高,故
w w w
K 的关系为b>c>a=d=e,故D错误;故选B。
w
4.25 ℃时,K =1.0×10-14;100 ℃时,K =1×10-12,下列说法正确的是( )
w w
A.100 ℃时,pH=10的NaOH溶液和pH=2的HSO 恰好中和,所得溶液的pH=7
2 4
B.25 ℃时,0.2 mol·L-1 Ba(OH) 溶液和0.2 mol·L-1 HCl等体积混合,所得溶液的pH=7
2
C.25 ℃时,0.2 mol·L-1 NaOH溶液与0.2 mol·L-1 CHCOOH恰好中和,所得溶液的pH=7
3
D.25 ℃时,pH=12的氨水和pH=2的HSO 等体积混合,所得溶液的pH>7
2 4
【答案】D
【解析】100 ℃时,NaOH和HSO 恰好中和时,pH=6,A错误;25 ℃时,c(OH-)=0.4 mol·L-1,c(H+)
2 4
=0.2 mol·L-1,等体积混合后pH大于7,B错误;C项,由于CHCOO-的水解pH大于7,错误;D项,氨水
3
过量,pH>7,正确。
5.一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
【答案】C
【解析】c点、b点对应相同的温度,A项错误;根据b点对应的纵坐标和横坐标都为1.0×10-7 mol·L-1
可知,水的离子积常数为1.0×10-14,B项错误;FeCl 为强酸弱碱盐,可水解使溶液呈酸性,C项正确;c、d
3
点对应的c(H+)相同,c(OH-)不同,但由于K 只与温度有关,所以温度不变时,稀释溶液不可能引起 c向d的
w
变化,D项错误。
有关pH计算的一般思维模型高频考点三 酸碱中和滴定
1.概念:用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸)的方法。
2.原理:c =(以一元酸与一元碱的滴定为例)。
待
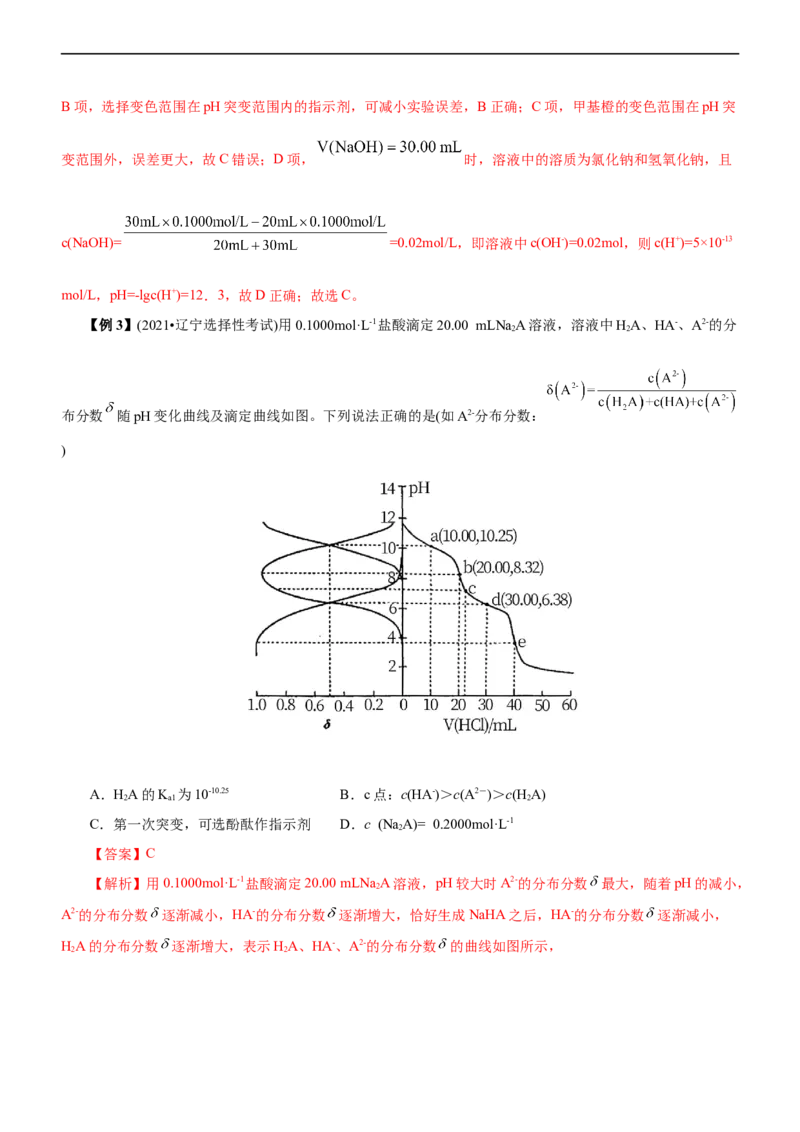
在酸碱中和滴定过程中,开始时由于被滴定的酸(或碱)浓度较大,滴入少量的碱(或酸)对其pH的影响不大。
当滴定接近终点(pH=7)时,很少量(一滴,约0.04 mL)的碱(或酸)就会引起溶液pH突变(如图所示)。
3.酸碱中和滴定的关键
(1)准确测定参加反应的酸、碱溶液的体积。
(2)选取适当指示剂,准确判断滴定终点。
4.实验用品
(1)仪器
图(A)是酸式滴定管,图B是碱式滴定管、滴定管夹、铁架台、锥形瓶。
(2)试剂
标准液、待测液、指示剂、蒸馏水。
指示剂 变色范围的pH甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
5.中和滴定实验操作(以酚酞作指示剂,用盐酸滴定氢氧化钠溶液)。
(1)滴定前的准备。
(2)滴定。
(3)终点判断:等到滴入最后一滴反应液,指示剂变色,且在半分钟内不能恢复原来的颜色,视为滴定终
点,并记录标准液的体积。
(4)数据处理:按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理计算。
c(NaOH)=
6.氧化还原滴定的原理及指示剂的选择:
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定一些本
身并没有还原性或氧化性,但能与某些还原剂或氧化剂反应的物质。
(2)试剂:常见用于滴定的氧化剂有KMnO 、KCr O 等;常见用于滴定的还原剂有亚铁盐、草酸、维生素
4 2 2 7
C等。
(3)指示剂:氧化还原滴定的指示剂有三类:
①氧化还原指示剂;
②专用指示剂,如在碘量法滴定中,可溶性淀粉溶液遇碘标准溶液变蓝;
③自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点为溶液由无色变为浅红色。
7.沉淀滴定:
(1)概念:沉淀滴定是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件的却
很少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比滴
定剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液测定溶液中Cl-的含量时常
3
以CrO为指示剂,这是因为AgCl比AgCrO 更难溶。
4【典例剖析】
【例1】下列有关滴定的说法正确的是( )
A.用标准的KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中混有NaOH杂质,则结果偏低
B.用c mol·L-1酸性高锰酸钾溶液滴定V mL未知浓度的HC O 溶液,至滴定终点用去酸性高锰酸钾溶
1 2 2 2 4
液体积为V mL,则HC O 溶液的浓度为 mol·L-1
1 2 2 4
C.用未知浓度的盐酸滴定已知浓度的NaOH溶液时,若读取读数时,滴定前仰视,滴定到终点后俯视,
会导致测定结果偏低
D.用25 mL滴定管进行中和滴定时,用去标准液的体积为21.7 mL
【答案】A
【解析】用标准的KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体 KOH中混有NaOH杂质,由于
氢氧化钠的摩尔质量较小,则所配标准溶液中 OH-浓度较大,滴定时消耗标准溶液体积偏小,所以测定结果
偏低,A正确;用c mol·L-1酸性高锰酸钾溶液滴定V mL未知浓度的HC O 溶液,至滴定终点用去高锰酸
1 2 2 2 4
钾溶液体积为V mL,由两者反应中化合价升降总数相等(或电子转移守恒)可得到关系式5HC O~2KMnO ,
1 2 2 4 4
则n(H C O)=2.5n(KMnO)=2.5×V mL×c mol·L-1,所以HC O 溶液的浓度为 mol·L-1,B不正确;用
2 2 4 4 1 1 2 2 4
未知浓度的盐酸滴定已知浓度的NaOH溶液时,若读取读数时,滴定前仰视,滴定到终点后俯视,则未知盐酸
的体积偏小,导致测定结果偏高,C不正确;滴定管的读数要精确到0.01 mL,D不正确。
【例2】(2020•浙江1月选考)室温下,向20.00 mL 0.1000mol·L−1盐酸中滴加0.1000mol·L−1 NaOH溶液,溶
液的pH随NaOH溶液体积的变化如图。已知lg5=0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
【答案】C
【解析】A项,NaOH与盐酸恰好完全反应时溶液中的溶质为NaCl,呈中性,室温下 ,故A正确;B项,选择变色范围在pH突变范围内的指示剂,可减小实验误差,B正确;C项,甲基橙的变色范围在pH突
变范围外,误差更大,故C错误;D项, 时,溶液中的溶质为氯化钠和氢氧化钠,且
c(NaOH)= =0.02mol/L,即溶液中c(OH-)=0.02mol,则c(H+)=5×10-13
mol/L,pH=-lgc(H+)=12.3,故D正确;故选C。
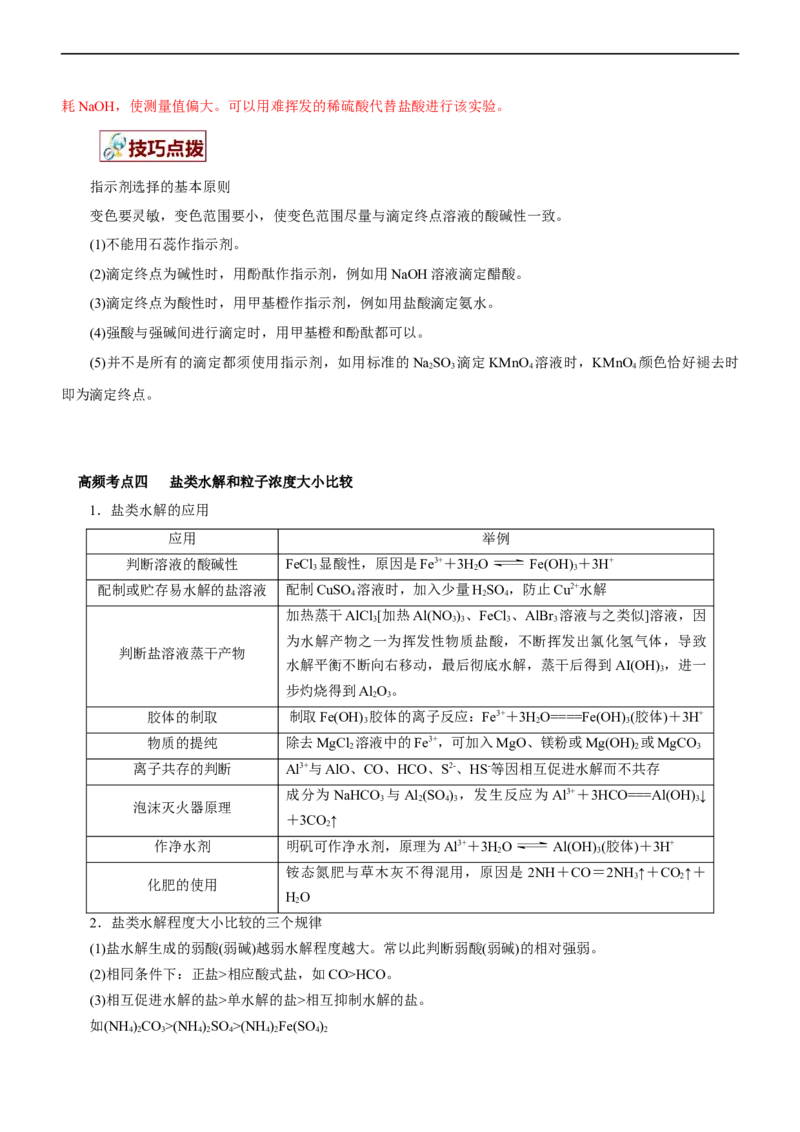
【例3】(2021•辽宁选择性考试)用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,溶液中HA、HA-、A2-的分
2 2
布分数 随pH变化曲线及滴定曲线如图。下列说法正确的是(如A2-分布分数:
)
A.HA的K 为10-10.25 B.c点:c(HA-)>c(A2-)>c(H A)
2 a1 2
C.第一次突变,可选酚酞作指示剂 D.c (NaA)= 0.2000mol·L-1
2
【答案】C
【解析】用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,pH较大时A2-的分布分数 最大,随着pH的减小,
2
A2-的分布分数 逐渐减小,HA-的分布分数 逐渐增大,恰好生成NaHA之后,HA-的分布分数 逐渐减小,
HA的分布分数 逐渐增大,表示HA、HA-、A2-的分布分数 的曲线如图所示,
2 2。A项,HA的 ,根据上图交点1计
2
算可知K =10-6.38,A错误;B项,根据图像可知c点中c(HA-)>c(H A)>c(A2-),B错误;C项,根据图像可知
a1 2
第一次滴定突跃溶液呈碱性,所以可以选择酚酞做指示剂,C正确;D项,根据图像e点可知,当加入盐酸
40mL时,全部生成HA,根据NaA+2HCl=2NaCl+H A计算可知c (Na A)= 0.1000mol·L-1,D错误;故选C。
2 2 2 2
【变式探究】
1.(2022·辽宁省沈阳二中高三第二阶段测试)下列滴定反应中,指示剂使用正确的是( )
A.用HO 溶液滴定KI溶液,淀粉做指示剂
2 2
B.用酸性KMnO 标准溶液滴定NaHSO 溶液以测量其浓度,用甲基橙做指示剂
4 3
C.用标准FeCl 溶液滴定KI溶液,KSCN溶液做指示剂
3
D.用强酸标准溶液滴定测量弱碱浓度,用酚酞做指示剂
【答案】C
【解析】A项,用过氧化氢滴定碘化钾溶液,若用淀粉作指示剂,反应开始生成的碘遇淀粉使溶液就变为
蓝色,继续滴加时,溶液蓝色的变化无法确定滴定终点,故A错误;B项,酸性高锰酸钾溶液与亚硫酸氢钠溶
液完全反应时,再滴入酸性高锰酸钾溶液,过量的酸性高锰酸钾会使溶液会变为浅紫色,则滴定时不需要指示
剂即可完成测量实验,故B错误;C项,氯化铁溶液与碘化钾溶液完全反应时,若用硫氰化钾溶液做指示剂,
过量的氯化铁溶液与硫氰化钾溶液反应生成硫氰化铁溶液,使溶液变为红色,可以确定滴定达到终点,故C
正确;D项,强酸溶液与弱碱溶液完全反应时生成强酸弱碱盐,强酸弱碱盐使溶液呈酸性,若用酚酞作指示剂
无法判断反应的终点,应选用甲基橙做指示剂,故D错误;故选C。
2.用标准的KOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是( )
A.配制标准溶液的固体KOH中混有NaOH杂质
B.滴定到终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液【答案】A
【解析】A项将会使标准碱液的c(OH-)偏大,滴定时耗用的V(OH-)偏小,导致结果偏低,A项正确;滴
定终点时仰视读数,将使读取碱液的体积偏大,测定结果偏高,B项错误;用未知液润洗锥形瓶将使测定结果
偏高,C项错误;尖嘴处悬挂溶液将使读取的标准液体积偏大,测定结果偏高,D项错误。
3.(2021•湖南选择性考试)常温下,用0.1000mol•L﹣1的盐酸分别滴定20.00mL浓度均为0.1000mol•L﹣1的
三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A.该NaX溶液中:c(Na+)>c(X﹣)>c(OH﹣)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X﹣)=c(Y﹣)=c(Z﹣)
D.分别滴加20.00mL盐酸后,再将三种溶液混合:c(X﹣)+c(Y﹣)+c(Z﹣)=c(H+)﹣c(OH﹣)
【答案】C
【解析】A项,因为HX为弱酸,NaX溶液存在水解:X﹣+H O HX+OH﹣,所以c(Na+)>c(X﹣)>c(OH﹣)
2
>c(H+),故A正确;B项,根据盐类水解的规律:越弱越水解可知,⇌相同浓度的强碱弱酸盐溶液中,一元弱
酸越弱,则其盐溶液碱性越强,结合图片可知溶液碱性强弱为:NaX<NaY<NaZ,则酸性强弱为:HX>HY
>HZ,一元弱酸中,酸性越强,电离程度越大,电离平衡常数K越大,所以有:K(HX)>K(HY)>K(HZ),
a a a
故B正确;C项,当pH=7时,c(H+)=c(OH﹣),根据电荷守恒,NaX溶液中有:c(H+)+c(Na+)=c(OH﹣)+c(X﹣)
+c(Cl﹣),则有:c(X﹣)=c(Na+)﹣c(Cl﹣),同理有:c(Y﹣)=c(Na+)﹣c(Cl﹣),c(Z﹣)=c(Na+)﹣c(Cl﹣),又因三种溶
液滴定到pH=7时,消耗的HCl的量是不一样的,即溶液中的c(Cl﹣)是不一样的,所以c(X﹣)≠c(Y﹣)≠c(Z﹣),
故C错误;D项,分别滴加20.00mL盐酸后,再将三种溶液混合后存在电荷守恒:c(X﹣)+c(Y﹣)+c(Z﹣)+c(OH﹣)
0.1mol/L×20mL×3
+c(Cl﹣)=c(H+)+c(Na+),又混合溶液中 c(Na+)= =0.05mol/L,混合溶液中 c(Cl﹣)
40mL×3
0.1mol/L×20mL×3
= =0.05mol/L,代入电荷守恒表达式,有c(X﹣)+c(Y﹣)+c(Z﹣)=c(H+)﹣c(OH﹣),故D正
40mL×3
确。故选C。4.中华人民共和国国家标准(GB 27602011)规定葡萄酒中SO 最大使用量为0.25 g·L-1。某兴趣小组用图1
2
装置(夹持装置略)收集某葡萄酒中SO ,并对其含量进行测定。
2
图1 图2
(1)仪器A的名称是____________,水通入A的进口为______。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO 全部逸出并与C中HO 完全反应,其化学方程式
2 2 2
为__________________________________。
(3)除去C中过量的HO ,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2
2 2
中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;若用50 mL滴定管进行实验,
当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)________(①=10 mL,②=40 mL,③<10
mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO 含量为________g·L-1。
2
(5) 该 测 定 结 果 比 实 际 值 偏 高 , 分 析 原 因 并 利 用 现 有 装 置 提 出 改 进 措 施 :
______________________________。
【答案】(1)冷凝管(或冷凝器) b (2)SO +HO===H SO (3)③ 酚酞 ④ (4)0.24
2 2 2 2 4
(5)原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸(或用蒸馏水代替葡萄酒进行对比实验,
扣除盐酸挥发的影响)
【解析】(1)A仪器的名称为冷凝管或冷凝器;为使冷却效果好,应将冷却水从处于低处的 b口通入。
(2)SO 具有强还原性,HO 具有强氧化性,二者发生氧化还原反应:SO +HO===H SO 。(3)NaOH盛装在碱
2 2 2 2 2 2 2 4
式滴定管中,应将橡皮管向上弯曲以排出气泡,选③。滴定至终点时溶液的pH=8.8,在酚酞的变色范围内,
故可选用酚酞作指示剂。液面在10 mL时滴定管中有刻度的液体为40 mL,因滴定管的下端有一段无刻度,故
管内液体的体积大于40 mL。(4)SO 与NaOH存在如下关系:
2
SO ~ HSO ~ 2NaOH
2 2 4
64 g 2 mol
m(SO ) 0.090 0 mol·L-1×0.025 L
2
解得:m(SO )==0.072 g,故葡萄酒中SO 的含量为=0.24 g·L-1。(5)盐酸为挥发性酸,挥发出的HCl消
2 2耗NaOH,使测量值偏大。可以用难挥发的稀硫酸代替盐酸进行该实验。
指示剂选择的基本原则
变色要灵敏,变色范围要小,使变色范围尽量与滴定终点溶液的酸碱性一致。
(1)不能用石蕊作指示剂。
(2)滴定终点为碱性时,用酚酞作指示剂,例如用NaOH溶液滴定醋酸。
(3)滴定终点为酸性时,用甲基橙作指示剂,例如用盐酸滴定氨水。
(4)强酸与强碱间进行滴定时,用甲基橙和酚酞都可以。
(5)并不是所有的滴定都须使用指示剂,如用标准的NaSO 滴定KMnO 溶液时,KMnO 颜色恰好褪去时
2 3 4 4
即为滴定终点。
高频考点四 盐类水解和粒子浓度大小比较
1.盐类水解的应用
应用 举例
判断溶液的酸碱性 FeCl 显酸性,原因是Fe3++3HO Fe(OH) +3H+
3 2 3
配制或贮存易水解的盐溶液 配制CuSO 溶液时,加入少量HSO ,防止Cu2+水解
4 2 4
加热蒸干AlCl [加热Al(NO ) 、FeCl 、AlBr 溶液与之类似]溶液,因
3 3 3 3 3
为水解产物之一为挥发性物质盐酸,不断挥发出氯化氢气体,导致
判断盐溶液蒸干产物
水解平衡不断向右移动,最后彻底水解,蒸干后得到AI(OH) ,进一
3
步灼烧得到Al O。
2 3
胶体的制取 制取Fe(OH) 胶体的离子反应:Fe3++3HO====Fe(OH) (胶体)+3H+
3 2 3
物质的提纯 除去MgCl 溶液中的Fe3+,可加入MgO、镁粉或Mg(OH) 或MgCO
2 2 3
离子共存的判断 Al3+与AlO、CO、HCO、S2-、HS-等因相互促进水解而不共存
成分为NaHCO 与Al (SO ) ,发生反应为Al3++3HCO===Al(OH) ↓
3 2 4 3 3
泡沫灭火器原理
+3CO↑
2
作净水剂 明矾可作净水剂,原理为Al3++3HO Al(OH) (胶体)+3H+
2 3
铵态氮肥与草木灰不得混用,原因是 2NH+CO=2NH ↑+CO↑+
3 2
化肥的使用
HO
2
2.盐类水解程度大小比较的三个规律
(1)盐水解生成的弱酸(弱碱)越弱水解程度越大。常以此判断弱酸(弱碱)的相对强弱。
(2)相同条件下:正盐>相应酸式盐,如CO>HCO。
(3)相互促进水解的盐>单水解的盐>相互抑制水解的盐。
如(NH )CO>(NH)SO >(NH)Fe(SO )
4 2 3 4 2 4 4 2 4 23.离子浓度大小比较
(1)微粒浓度大小比较的理论依据和守恒关系
A.两个理论依据
①弱电解质电离理论:电离粒子的浓度大于电离生成粒子的浓度。
例如,HCO 溶液中:c(H CO)>c(HCO) c(CO)(多元弱酸第一步电离程度远远大于第二步电离)。
2 3 2 3
②水解理论:水解离子的浓度大于水解生成粒子的浓度。
≫
例如,NaCO 溶液中:c(CO)>c(HCO) c(H CO)(多元弱酸根离子的水解以第一步为主)。
2 3 2 3
B.三个守恒关系
≫
①电荷守恒:电荷守恒是指溶液必须保持电中性,即溶液中所有阳离子的电荷总浓度等于所有阴离子的电
荷总浓度。
例如,NaHCO 溶液中:c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-)。
3
②物料守恒:物料守恒也就是元素守恒,变化前后某种元素的原子个数守恒。
例如,0.1 mol·L-1 NaHCO 溶液中:c(Na+)=c(HCO)+c(CO)+c(H CO)=0.1 mol·L-1。
3 2 3
③质子守恒:由水电离出的c(H+)等于由水电离出的c(OH-),在碱性盐溶液中OH-守恒,在酸性盐溶液
中H+守恒。例如,纯碱溶液中c(OH-)=c(H+)+c(HCO)+2c(H CO)。
2 3
(2)四种情况分析
①多元弱酸溶液
根据多步电离分析,如:在HPO 溶液中,c(H+)>c(H PO)>c(HPO)>c(PO)。
3 3 2
②多元弱酸的正盐溶液
根据弱酸根的分步水解分析,如:NaCO 溶液中:c(Na+)>c(CO)>c(OH-)>c(HCO)。
2 3
③不同溶液中同一离子浓度的比较
要看溶液中其他离子对其产生的影响。例如,在相同物质的量浓度的下列溶液中:①NH NO 溶液,
4 3
②CHCOONH 溶液,③NH HSO 溶液,c(NH)由大到小的顺序是③>①>②。
3 4 4 4
④混合溶液中各离子浓度的比较
要进行综合分析,如电离因素、水解因素等。例如,在0.1 mol·L-1的NH Cl和0.1 mol·L-1的氨水混合溶液
4
中,各离子浓度的大小顺序为c(NH)>c(Cl-)>c(OH-)>c(H+)。在该溶液中,NH ·H O的电离与NH的水解互相
3 2
抑制,但NH ·H O的电离程度大于NH的水解程度,溶液呈碱性,c(OH-)>c(H+),同时c(NH)>c(Cl-)。
3 2
1.电解质溶液中的守恒关系
(1)电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。
如NaHCO 溶液中:n(Na+)+n(H+)=n(HCO)+2n(CO)+n(OH-)
3
(2)物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分
子中某种特定元素的原子的总数是不会改变的。
如NaHCO 溶液中n(Na+)∶n(C)=1∶1,推出:c(Na+)=c(HCO)+c(CO)+c(H CO)
3 2 3
(3)质子守恒:电解质溶液中分子或离子得到或失去质子(H+)的物质的量应相等。
例如在NH HCO 溶液中HO+、HCO 为得到质子后的产物;NH ·H O、OH-、CO为失去质子后的产物,
4 3 3 2 3 3 2
故有以下关系:c(H O+)+c(H CO)===c(NH ·H O)+c(OH-)+c(CO)。
3 2 3 3 2
2.微粒浓度大小的比较(1)多元弱酸溶液,根据多步电离分析,如在HPO 的溶液中,c(H+)>c(H PO)>c(HPO)>c(PO)。
3 4 2
(2)多元弱酸的正盐溶液,根据弱酸根的分步水解分析,如 NaCO 的溶液中:c(Na+)>c(CO)>c(OH
2 3
-)>c(HCO)。
(3)不同溶液中同一离子浓度的比较,要看溶液中其他离子对其影响的因素。如在相同的物质的量浓度的
下列各溶液中A.NH Cl b.CHCOONH c.NH HSO 。c(NH)由大到小的顺序是c>a>b。
4 3 4 4 4
(4)混合溶液中各离子浓度的比较,要进行综合分析,如电解因素、水解因素等。如相同浓度的NH Cl溶
4
液和氨水等体积混合后,由于氨水的电离程度大于 NH的水解程度,所以溶液中离子浓度顺序为:c(NH)>c(Cl
-)>c(OH-)>c(H+)。
【典例剖析】
【例1】(2022·浙江省6月选考) 时,苯酚(C HOH)的K=1.0×10-10,下列说法正确的是( )
6 5 a
A.相同温度下,等 的C HONa和CHCOONa溶液中,c (C HO-)>c(CHCOO-)
6 5 3 6 5 3
B.将浓度均为0.1mol·L-1的C HONa和NaOH溶液加热,两种溶液的 均变大
6 5
C. 时,C HOH溶液与NaOH溶液混合,测得 ,则此时溶液中c (C HO-)= c (C HOH)
6 5 6 5 6 5
D. 时,0.1mol·L-1的C HOH溶液中加少量C HONa固体,水的电离程度变小
6 5 6 5
【答案】C
【解析】A项,醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的C HONa
6 5
和CHCOONa溶液中c(C HO-)3,故A错误;B项,稀释GHCl溶液时,GH+水解程度将增大,根据勒夏特列
原理可知溶液中c(H+)将减小,溶液pH将升高,故B正确;C项,GHCl为强酸弱碱盐,在水中电离方程式为
GHCl=GH++Cl-,故C错误;D项,根据电荷守恒可知,GHCl溶液中c(OH-)+c(Cl-)=c(H+)+c(GH+),故D错误;
故选B。
3.(2019•年4月浙江选考)高温高压液态水具有接近常温下弱酸的 c(H+)或弱碱的 c(OH-), 油脂在其中
能以较快的反应速率水解。与常温常压水相比,下列说法不正确的是( )
A.高温高压液态水中,体系温度升高,油脂水解反应速率加快
B.高温高压液态水中,油脂与水的互溶能力增强,油脂水解反应速率加快
C.高温高压液态水中,c(H+)增大,可催化油脂水解反应,且产生的酸进一步催化水解
D.高温高压液态水中的油脂水解,相当于常温下在体系中加入了相同 c(H+)的酸或相同c(OH-)的碱的
水解
【答案】D
【解析】对于任何化学反应,体系温度升高,均可加快反应速率,A 项正确;由于高温高压液态水中,
c(H+)和 c(OH−)增大,油脂水解向右移动的倾向变大,因而油脂与水的互溶能力增强, 反应速率加快,B 项
正确;油脂在酸性(H+做催化剂)条件下水解,高温高压液态水中,c(H+)增大,可催化油脂水解反应,且产生
的酸进一步催化水解,C 项正确;高温高压液态水中的油脂水解,其水环境仍呈中性,因而不能理解成相当
于常温下在体系中加入了相同 c(H+)的酸或相同 c(OH−)的碱的水解,而是以体系升温、增加水和油脂的互溶
以及提高水中 H+浓度的方式,促进油脂的水解,D 项不正确。
4.(2021•天津卷)常温下,下列有关电解质溶液的叙述正确的是( )
A.在0.1mol·L-1HPO 溶液中c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-)
3 4 3 4 2 4 4 4
B.在0.1mol·L-1NaC O 溶液中c(Na+)+c(H+)= c(OH―)+c(HC O-)+c(C O2-)
2 2 4 2 4 2 4
C.在0.1mol·L-1NaHCO 溶液中c(H CO)+ c(HCO -)=0.1mol·L-1
3 2 3 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH +)>c(OH―)>c(H+)
4 4
【答案】A
【解析】A项,由于磷酸为多元酸,第一步电离大于第二步电离大于第三步电离,所以在0.1mol·L-1HPO
3 4
溶液中,离子浓度大小为:c(H PO )>c(H PO -)>c(HPO 2-)>c(PO 3-),故A正确;B项,在0.1mol·L-1NaC O
3 4 2 4 4 4 2 2 4
溶液中,根据电荷守恒得到c(Na+)+c(H+)= c(OH―)+c(HC O-)+2c(C O2-),故B错误;C项,在
2 4 2 40.1mol·L-1NaHCO 溶液中,根据物料守恒得到c(H CO)+ c(HCO -)+ c(CO2-)=0.1mol·L-1,故C错误;D项,氨
3 2 3 3 3
水和NH Cl溶液混合,形成pH=9的溶液,则c(OH―)>c(H+),根据电荷守恒c(Cl-)+c(OH―)=c(NH +)+c(H+),
4 4
则c(Cl-)<c(NH +),故D错误;故选A。
4
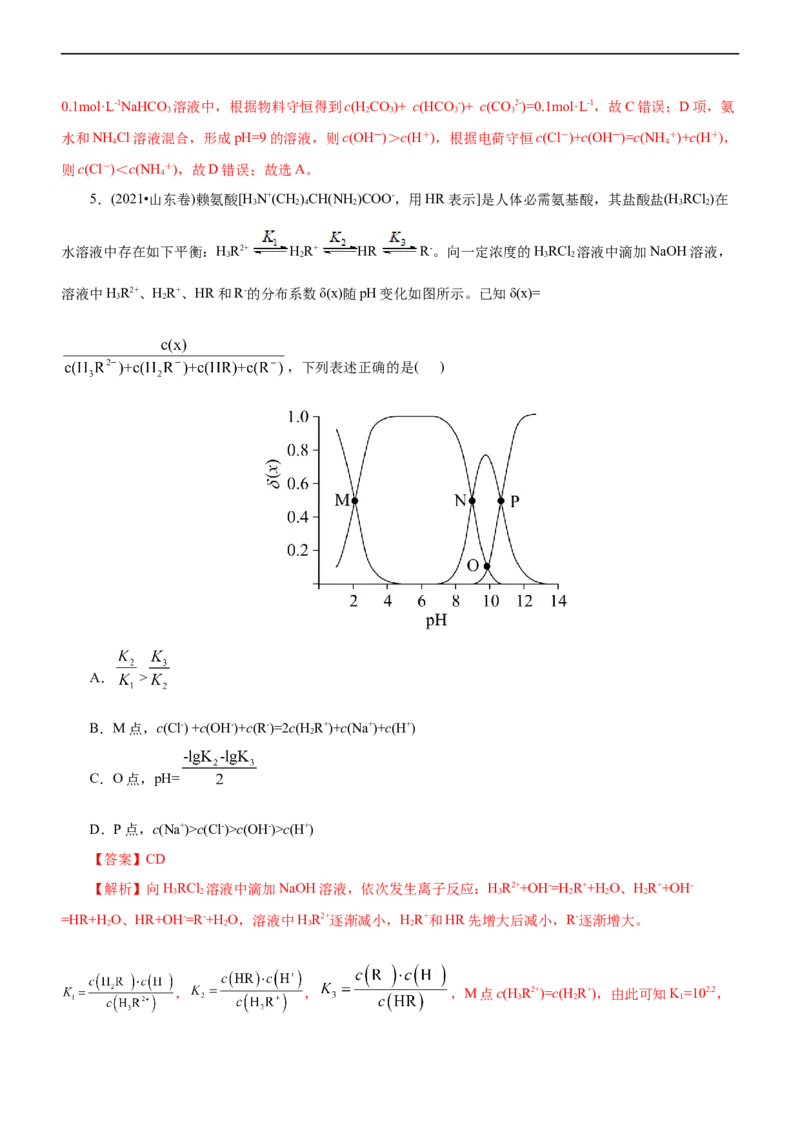
5.(2021•山东卷)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H RCl )在
3 2 4 2 3 2
水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴加NaOH溶液,
3 2 3 2
溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是( )
A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
【答案】CD
【解析】向HRCl 溶液中滴加NaOH溶液,依次发生离子反应:HR2++OH-=H R++H O、HR++OH-
3 2 3 2 2 2
=HR+H O、HR+OH-=R-+H O,溶液中HR2+逐渐减小,HR+和HR先增大后减小,R-逐渐增大。
2 2 3 2
, , ,M点c(H R2+)=c(H R+),由此可知K=102.2,
3 2 1N点c(HR)=c(H R+),则K=10-9.1,P点c(HR)=c(R-),则K=10-10.8。A项, ,
2 2 3
,因此 ,故A错误;B项,M点存在电荷守恒:c(Cl-) +c(OH-)+c(R-)=2c(H R2+)
3
+c(H R+)+c(Na+)+c(H+),此时c(H R2+)=c(H R+),因此c(Cl-) +c(OH-)+c(R-)=3c(H R+)+c(Na+)+c(H+),故B错误;
2 3 2 2
C项,O点c(H R+)=c(R-),因此 ,即 ,因此
2
,溶液 ,故C正确;D项,P点溶质为NaCl、HR、
NaR,此时溶液呈碱性,因此c(OH-)>c(H+),溶质浓度大于水解和电离所产生微粒浓度,因此
c(Na+)>c(Cl-)>c(OH-)>c(H+),故D正确;故选CD。
6.(2023·广东省深圳市龙岗区高三期中)25℃时,用0.1000mol∙L-1NaOH溶液滴定0.1000mol∙L-1醋酸溶液,
由水电离出的c(H+) 与加入NaOH溶液的体积V(NaOH)的关系如下图所示[已知 ]。下列
水
说法正确的是( )
A.图中x=10-11.13
B.b、d两点溶液组成相同,且均存在c(Na+)=c(CHCOO-)
3
C.c点溶液中存在c(CHCOOH)>c(OH-)
3D.稀释e点溶液时, 减小
【答案】A
【解析】CHCOOH溶液中加入NaOH溶液,CHCOOH的电离程度不断增大,溶液的酸性不断减弱,水
3 3
电离的程度不断增大,当有少量CHCOOH剩余时,溶液呈中性;继续加入NaOH溶液至c点时,CHCOOH
3 3
全部转化为CHCOONa,此时水的电离程度最大;继续加入NaOH,对CHCOONa的水解产生抑制,水解程
3 3
度不断减小,到达d点时,CHCOONa基本不发生水解,再往后,加入的NaOH使溶液呈碱性。A项,
3
,则K (CHCOOH)=1×10-4.74,图中x点,K (CHCOOH)= =
a 3 a 3
=1×10-4.74,c(H+)=1×10-2.87mol∙L-1,则x= =10-11.13,A正确;B项,b点溶液为CHCOONa与
3
CHCOOH的混合溶液,此时c(Na+)=c(CHCOO-),d点溶液为CHCOONa与NaOH的混合溶液,此时c(Na+)>
3 3 3
c(CHCOO-),B不正确;C项,c点,CHCOOH与NaOH刚好完全反应,此时溶液为CHCOONa溶液,
3 3 3
CHCOO-发生水解生成等量的CHCOOH和OH-,水电离又生成OH-,所以存在c(CHCOOH)<c(OH-),C不正
3 3 3
确;D项,e点溶液中, = ,温度不变时,K 不变,稀释e点溶液,溶液的碱性减弱,
a
c(H+)增大,所以 增大,D不正确;故选A。
7.向1 L含0.01 mol NaAlO 和0.02 mol NaOH的溶液中缓慢通入CO,随n(CO)增大,先后发生三个不同
2 2 2
的反应,当0.01 molc(AlO)+c(OH-)
B 0.01 c(Na+)>c(AlO)>c(OH-)>c(CO)
C 0.015 c(Na+)>c(HCO)>c(CO)>c(OH-)
D 0.03 c(Na+)>c(HCO)>c(OH-)>c(H+)
【答案】D【解析】A项,NaAlO 与NaOH的混合溶液,由电荷守恒有:c(Na+)+c(H+)=c(AlO)+c(OH-),有c(Na
2
+)c(AlO),错误;C项,继续通CO ,发生题给反应:2NaAlO +CO +
2 2 2
3HO===2Al(OH) ↓+NaCO ,当n(CO)=0.015 mol,此时为NaCO 溶液,有c(CO)>c(HCO),错误;D项,
2 3 2 3 2 2 3
继续通CO 发生反应:NaCO +CO +HO===2NaHCO ,当n(CO)=0.03 mol,此时为NaHCO 溶液,因
2 2 3 2 2 3 2 3
HCO水解程度大于电离程度,溶液呈碱性,正确。
离子浓度大小关系分析判断的基本解题框架
步骤一:
步骤二:
巧抓“四点”,突破图象中的“粒子”浓度关系
(1)抓反应“一半”点,判断是什么溶质的等量混合。
(2)抓“恰好”反应点,生成什么溶质,溶液的酸碱性,是什么因素造成的。
(3)抓溶液“中性”点,生成什么溶质,哪种反应物过量或不足。
(4)抓反应“过量”点,溶质是什么,判断谁多、谁少还是等量
高频考点五 难溶电解质的溶解平衡
1.溶度积和离子积
以A B (s) mAn+(aq)+nBm-(aq)为例
m n
溶度积 离子积
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp cK (A B )=cm(An+)·cn(Bm-),式中 Q(A B )=cm(An+)·cn(Bm-),式中
表达式 sp m n c m n
的浓度都是平衡浓度 的浓度是任意浓度
判断在一定条件下沉淀能否生成或溶解
①Q>K :溶液过饱和,有沉淀析出
c sp
应用
②Q=K :溶液饱和,处于平衡状态
c sp
③Q<K :溶液未饱和,无沉淀析出
c sp
2.K 的影响因素
sp
(1)内因:难溶物质本身的性质,这是主要因素。
(2)外因
①浓度:加水稀释,平衡向溶解方向移动,但K 不变。
sp
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,K 增大。
sp
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离物质或气体的离子时,平
衡向溶解方向移动,但K 不变。
sp
3.沉淀溶解平衡的应用
(1)沉淀的生成
①调节pH法
如除去NH Cl溶液中的FeCl 杂质,可加入氨水调节pH至7~8,离子方程式为Fe3++
4 3
3NH ·H O===Fe(OH) ↓+3NH。
3 2 3
②沉淀剂法
如用HS沉淀Cu2+,离子方程式为HS+Cu2+===CuS↓+2H+。
2 2
(2)沉淀的溶解
①酸溶解法
如CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++HO+CO↑。
3 3 2 2
②盐溶液溶解法
如Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
③氧化还原溶解法
如不溶于盐酸的硫化物Ag S溶于稀HNO。
2 3
④配位溶解法
如AgCl溶于氨水,离子方程式为AgCl+2NH ·H O===[Ag(NH)]++Cl-+2HO。
3 2 3 2 2
(3)沉淀的转化
①实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化)。
②应用:锅炉除垢、矿物转化等。
4.溶度积曲线
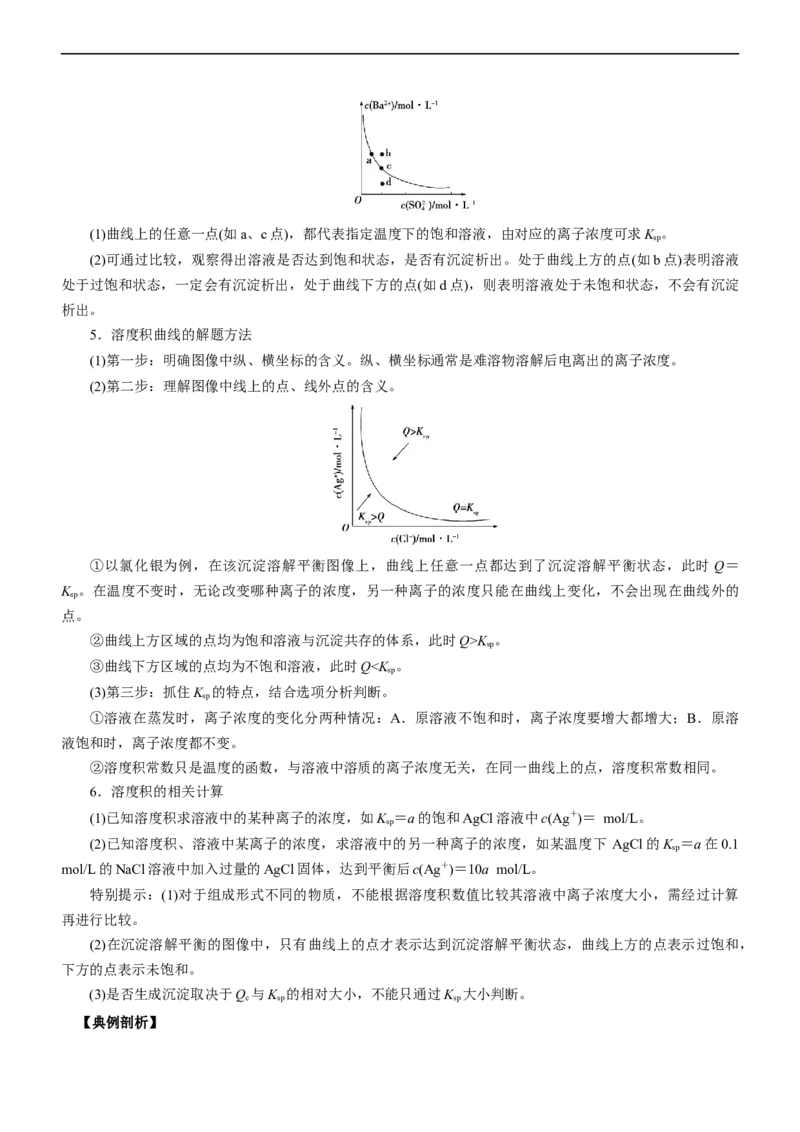
溶度积曲线是分别以阳、阴离子的浓度为坐标作出的曲线,不同温度下曲线形状不尽相同。如图是 BaSO
4
溶液中的离子浓度曲线。(1)曲线上的任意一点(如a、c点),都代表指定温度下的饱和溶液,由对应的离子浓度可求K 。
sp
(2)可通过比较,观察得出溶液是否达到饱和状态,是否有沉淀析出。处于曲线上方的点(如b点)表明溶液
处于过饱和状态,一定会有沉淀析出,处于曲线下方的点(如d点),则表明溶液处于未饱和状态,不会有沉淀
析出。
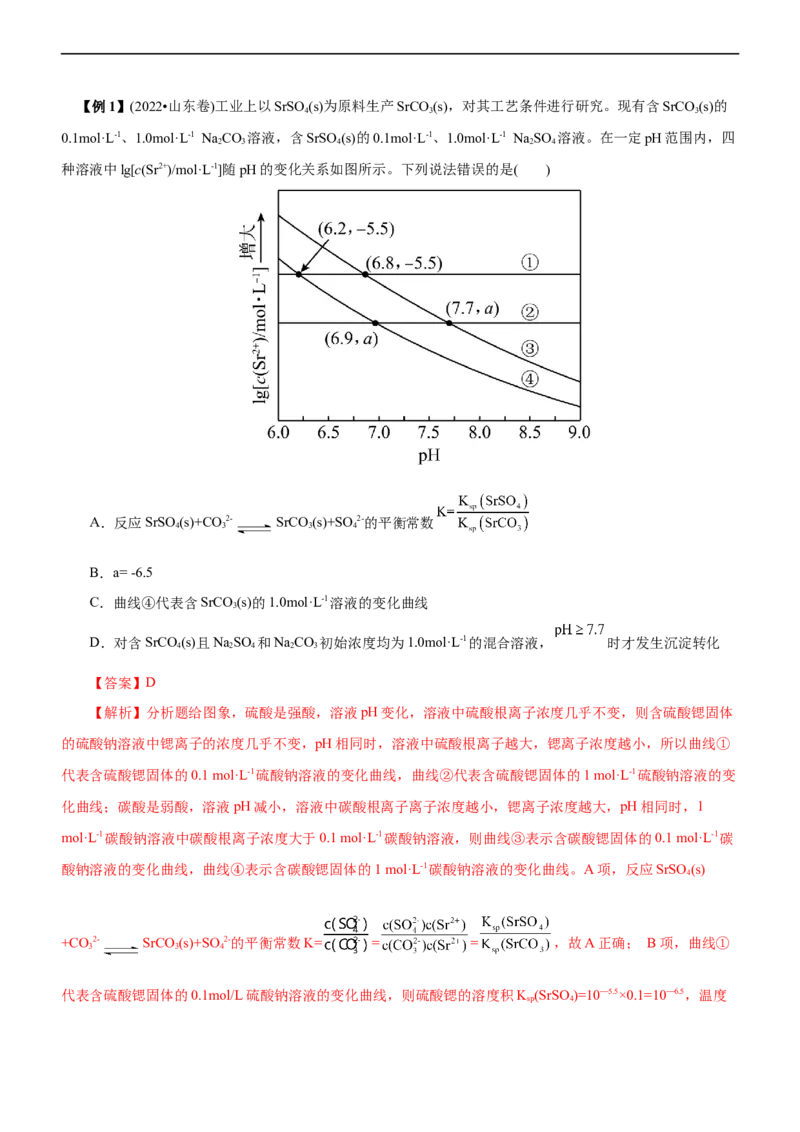
5.溶度积曲线的解题方法
(1)第一步:明确图像中纵、横坐标的含义。纵、横坐标通常是难溶物溶解后电离出的离子浓度。
(2)第二步:理解图像中线上的点、线外点的含义。
①以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时 Q=
K 。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不会出现在曲线外的
sp
点。
②曲线上方区域的点均为饱和溶液与沉淀共存的体系,此时Q>K 。
sp
③曲线下方区域的点均为不饱和溶液,此时QK (RCO),故向c(CO2-)=c(SO2-)的混合液中滴加RCl 溶液,首先析
4 3 sp 4 sp 3 3 4 2
出RCO 沉淀,A错误;B项,将浓度均为3×10-4.5mol•L-1的RCl 、NaCO 溶液等体积混合后,c(R2+)=1.5×10-
3 2 2 3
4.5mol•L-1、c(CO2-)=1.5×10-6mol•L-1,此时的离子积Q=c(R2+)•c(CO 2-)=1.5×10-6×1.5×10-6=2.25×10-12