文档内容
专题 12 物质结构与性质综合(题型突破)
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.含有N-、N+的材料Pb(N )、NAsF 可以用于炸药。下列说法正确的是( )
3 5 3 2 5 6
A.Pb属于d区元素
B.基态As原子的d轨道与p轨道上的电子数之比为3:2
C.N-的空间构型为直线形
3
D.基态F原子中,核外电子的空间运动状态有9种
2.(2024·江苏苏州高三期中)Na、Mg、Al均为第三周期元素。下列说法正确的是( )
A.离子半径:r(Na+)<r(Mg2+)<r(Al3+) B.第一电离能:I(Na)> I (Mg)> I (Al)
1 1 1
C.还原性:Na>Mg>Al D.碱性:NaOH<Mg(OH) <Al(OH)
2 3
3.(2024·山东淄博高三期中检测)下列关于物质结构和性质的说法正确的是( )
A.键角:HS>PH>SiH B.熔点:CsCl>KCl>NaCl
2 3 4
C.NO -、NO -的VSEPR模型相同 D.酸性:CHCOOH>CCl COOH>CF COOH
3 2 3 3 3
4.实验室中利用CoCl 制取配合物[Co(NH )]Cl 的反应为2CoCl + 10NH + 2NH Cl+H O
2 3 6 3 2 3 4 2 2
=2[Co(NH)]Cl +2H O。下列叙述正确的是( )
3 6 3 2
A.Co2+的价电子排布图为 B.1 mol [Co(NH)]3+中含σ键为18 mol
3 6
C.HO 中氧原子采用sp3杂化 D.氨分子间存在氢键,因而NH 易溶于水
2 2 3
5.(2024·山东菏泽高三期中)H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错
误是( )
A.该分子中不存在氢键
B.B.基态V原子的价电子轨道表示式为C.基态O原子中有3种能量不同的电子
D.该分子中的碳原子全部是sp2杂化
6.(2024·北京丰台高三期中)镍二硫烯配合物基元的COFs材料因具有良好的化学稳定性、热稳定性和
导电性而应用于电池领域。一种基于镍二硫烯配合物的单体结构简式如下图所示,下列关于该单体的说法
不正确的是( )
A.Ni属于d区元素 B.S与Ni形成配位键时,S提供孤电子对
C.组成元素中电负性最大的是O D.醛基中C原子的价层电子对数为4
7.NF 是微电子工业中一种优良的等离子蚀刻气体,可通过电解熔融氟化氢铵(NH HF )制得。下列有
3 4 2
关说法错误的是( )
A.NF 的空间构型为平面三角形
3
B.相关元素电负性由大到小的顺序为F>N>H
C.NF 和NH HF 中N原子的杂化方式均为sp3
3 4 2
D.NH HF 晶体中微粒间的作用有离子键、共价键、配位键、氢键
4 2
8.(2024·山东临沂市高三教学质量检测考试)六硝基合钴酸钾{K [Co(NO )]}是一种黄色难溶物。检验
3 2 6
K+或Co2+的反应原理如下:CoCl+NaNO +KCl+HCl→K[Co(NO )]↓+NO↑+NaCl+H O(未配平)。下列说法
2 2 3 2 6 2
错误的是( )
A.将上述反应设计成原电池,正极产物为NO
B.配合物K[Co(NO )]中配位原子是氧原子
3 2 6
C.基态Co原子的价层电子中,成对电子数与未成对电子数之比为2:1
D.上述反应的离子方程式为CoCl+7NO -+3K++2H+=K[Co(NO )]↓+NO↑+HO
2 2 3 2 6 2
9.(2024·安徽六安一中高三质检)在《是真的吗》节目《盐里面加进了亚铁氰化钾》案例中:有一位
老教授食用了添加抗结剂亚铁氰化钾的食盐后,肾脏受到严重危害。亚铁氰化钾K[Fe(CN)]俗名黄血盐,
4 6
制备方法为Fe+6HCN+2KCO= K[Fe(CN)]+H ↑+2CO ↑+2H O。设N 为阿伏加德罗常数的数值,下列说法
2 3 4 6 2 2 2 A
正确的是( )
A.27gHCN分子中含有π键数目为N
AB.配合物K[Fe(CN)]的中心离子价电子排布式为3d6,该中心离子的配位原子数为12
4 6
C.每生成1 CO 时,反应过程中转移电子数目为4N
2 A
D.1L1 的KCO 溶液,阳离子数目大于2N
2 3 A
10.(2024·江苏南京金陵中学高三期中)NH 是一种重要的化工原料,向NiSO 溶液中通NH 可制
3 4 3
[Ni(NH )]SO ,肼(N H)是一种火箭燃料推进剂,其燃烧热为624 kJ·mol-1,下列说法正确的是( )
3 6 4 2 4
A.[Ni(NH )]SO 、NH 中的 键角:前者大于后者
3 6 4 3
B.基态 核外电子排布式为 [Ar]3d64s2
C.表示肼燃烧热的热化学方程式:NH (g)+ O(g) N (g)+ 2HO(g) ΔH=-624 kJ·mol-1
2 4 2 2 2
D.[Ni(NH )]SO 中含有化学键有离子键、共价键、氢键、配位键
3 6 4
11.(2024·江苏泰州高三期中)海洋是一个巨大的化学资源宝库,含有80多种元素,其中含有较高的钠
和氯元素。化学家常用廉价氯化钠为原料制备纯碱,也可用于电解方法获得金属钠、氯气、氢气等,并进
一步将其转化为生产、生活和科学实验中用途更为广泛的新物质,如ClO 、NaO、NaClO等。下列说法
2 2 2
正确的是( )
A.键角:ClO ->ClO -
3 4
B.酸性:CClCOOH>CHCOOH
3 3
C.侯氏制碱的反应:2NaCl+2NH +CO +H O=NaCO+2NHCl
3 2 2 2 3 4
D.电解饱和食盐水时,若两极共产生气体 (标准状况下),转移电子数为
12.铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热
点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。下列有关说法中错误的是( )
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了sp2和sp3两种杂化方式C.该配离子中铜的配位数和所含配位键的数目均为4
D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)
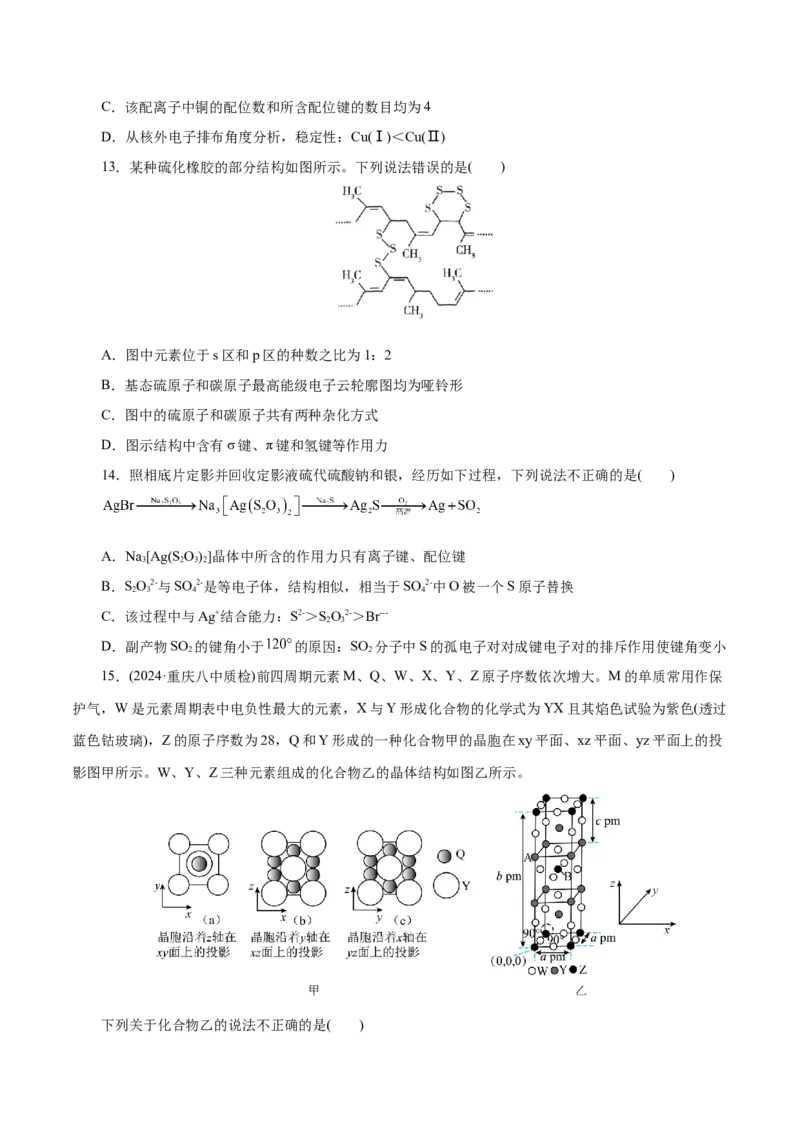
13.某种硫化橡胶的部分结构如图所示。下列说法错误的是( )
A.图中元素位于s区和p区的种数之比为1:2
B.基态硫原子和碳原子最高能级电子云轮廓图均为哑铃形
C.图中的硫原子和碳原子共有两种杂化方式
D.图示结构中含有σ键、π键和氢键等作用力
14.照相底片定影并回收定影液硫代硫酸钠和银,经历如下过程,下列说法不正确的是( )
A.Na[Ag(S O)]晶体中所含的作用力只有离子键、配位键
3 2 3 2
B.SO2-与SO 2-是等电子体,结构相似,相当于SO 2-中O被一个S原子替换
2 3 4 4
C.该过程中与Ag+结合能力:S2->SO2->Br---
2 3
D.副产物SO 的键角小于 的原因:SO 分子中S的孤电子对对成键电子对的排斥作用使键角变小
2 2
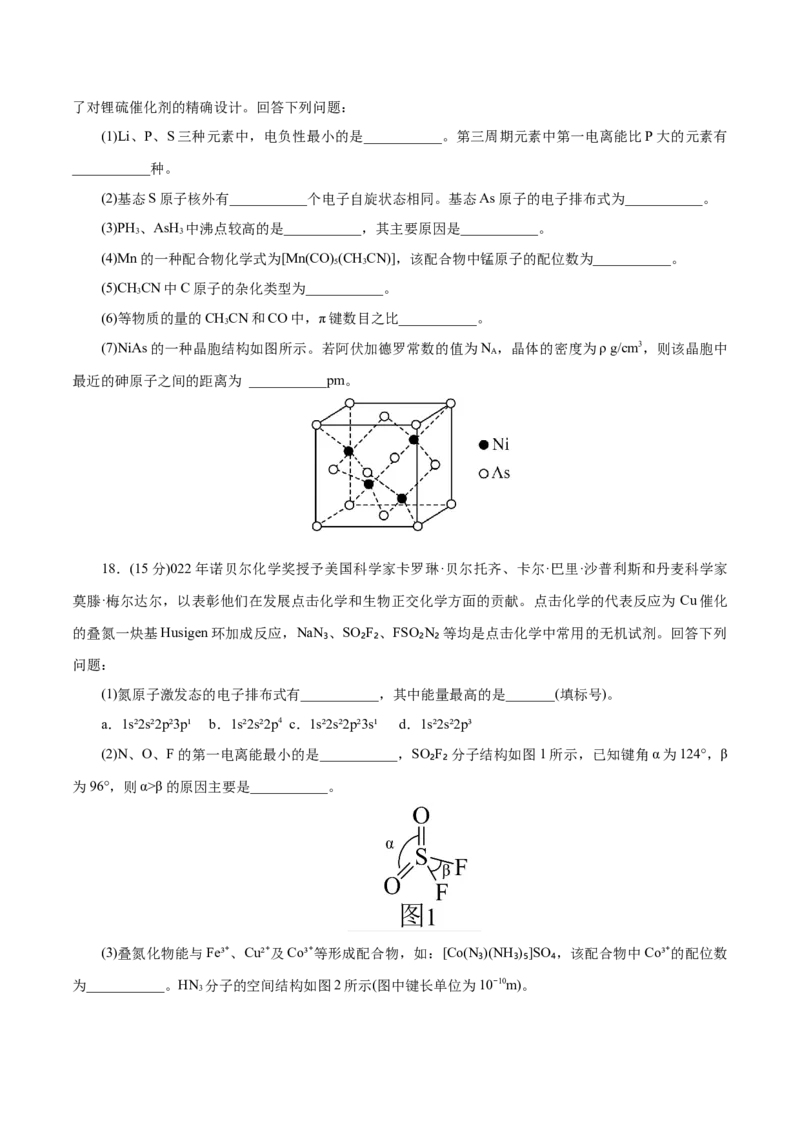
15.(2024·重庆八中质检)前四周期元素M、Q、W、X、Y、Z原子序数依次增大。M的单质常用作保
护气,W是元素周期表中电负性最大的元素,X与Y形成化合物的化学式为YX且其焰色试验为紫色(透过
蓝色钴玻璃),Z的原子序数为28,Q和Y形成的一种化合物甲的晶胞在xy平面、xz平面、yz平面上的投
影图甲所示。W、Y、Z三种元素组成的化合物乙的晶体结构如图乙所示。
下列关于化合物乙的说法不正确的是( )A.该晶体中Z的化合价为+2
B.与Z等距最近的W有6个
C.图中A、B原子间的距离为
D.图中B的原子分数坐标可表示为
二、非选择题(本题包括4小题,共55分)
16.(12分)含氮化合物在生活中占有重要地位。请回答:
(1)CN-可通过配位键与Co3+形成[Co(CN) ]3-。形成该配合物时,基态 的价层电子发生重排提供两
6
个空轨道,则重排后的Co3+价电子排布图为___________;CO 的金属配合物也已经制备成功,但为数不多,
2
如[Ni(PH )CO],已知该配合物的配位数与[[Ni(CO) ]]的配位数相同,测得其中存在两种碳氧键的键长,
3 2 2 4
一个为0.117mm,另一个为0.122nm。请画出[Ni(PH )CO]的结构示意图:___________。
3 2 2
(2)NF 和NH 是常见含氮化合物,其VSEPR构型均为___________,其中二者相比较,键角更大的是
3 3
___________。
(3)N、P、As同属于ⅤA族,下列说法正确的是___________。
A.原子半径:r(N) >r(P) >r(As)且电负性:N>P>As
B.N、P、As的最高价氧化物水化物的酸性依次减弱
C.简单氢化物的还原性:NH >PH >AsH
3 3 3
D.黑砷和黑磷的结构相似(如图1),每个砷原子最外层均形成8电子结构。其晶体单层中,As原子与
As—As键的个数比为2∶3
(4)已知NH F晶胞结构如图2所示,M处的NH + (其位于四个F-所构成的正四面体中心)有一定的朝向,
4 4
不能随意转动,请解释其原因___________,该晶胞的晶胞参数如图所示,设N 为阿伏伽德罗常数的值,
A
该晶体的密度ρ=___________ g· cm-3 (列出计算式即可)
17.(13分)中国科学院朱庆山团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP)型结构转变,实现了对锂硫催化剂的精确设计。回答下列问题:
(1)Li、P、S三种元素中,电负性最小的是___________。第三周期元素中第一电离能比P大的元素有
___________种。
(2)基态S原子核外有___________个电子自旋状态相同。基态As原子的电子排布式为___________。
(3)PH 、AsH 中沸点较高的是___________,其主要原因是___________。
3 3
(4)Mn的一种配合物化学式为[Mn(CO) (CHCN)],该配合物中锰原子的配位数为___________。
5 3
(5)CH CN中C原子的杂化类型为___________。
3
(6)等物质的量的CHCN和CO中,π键数目之比___________。
3
(7)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为N ,晶体的密度为ρ g/cm3,则该晶胞中
A
最近的砷原子之间的距离为 ___________pm。
18.(15分)022年诺贝尔化学奖授予美国科学家卡罗琳·贝尔托齐、卡尔·巴里·沙普利斯和丹麦科学家
莫滕·梅尔达尔,以表彰他们在发展点击化学和生物正交化学方面的贡献。点击化学的代表反应为 Cu催化
的叠氮一炔基Husigen环加成反应,NaN₃、SO₂F₂、FSO₂N₂等均是点击化学中常用的无机试剂。回答下列
问题:
(1)氮原子激发态的电子排布式有___________,其中能量最高的是_______(填标号)。
a.1s²2s²2p²3p¹ b.1s²2s²2p4 c.1s²2s²2p²3s¹ d.1s²2s²2p³
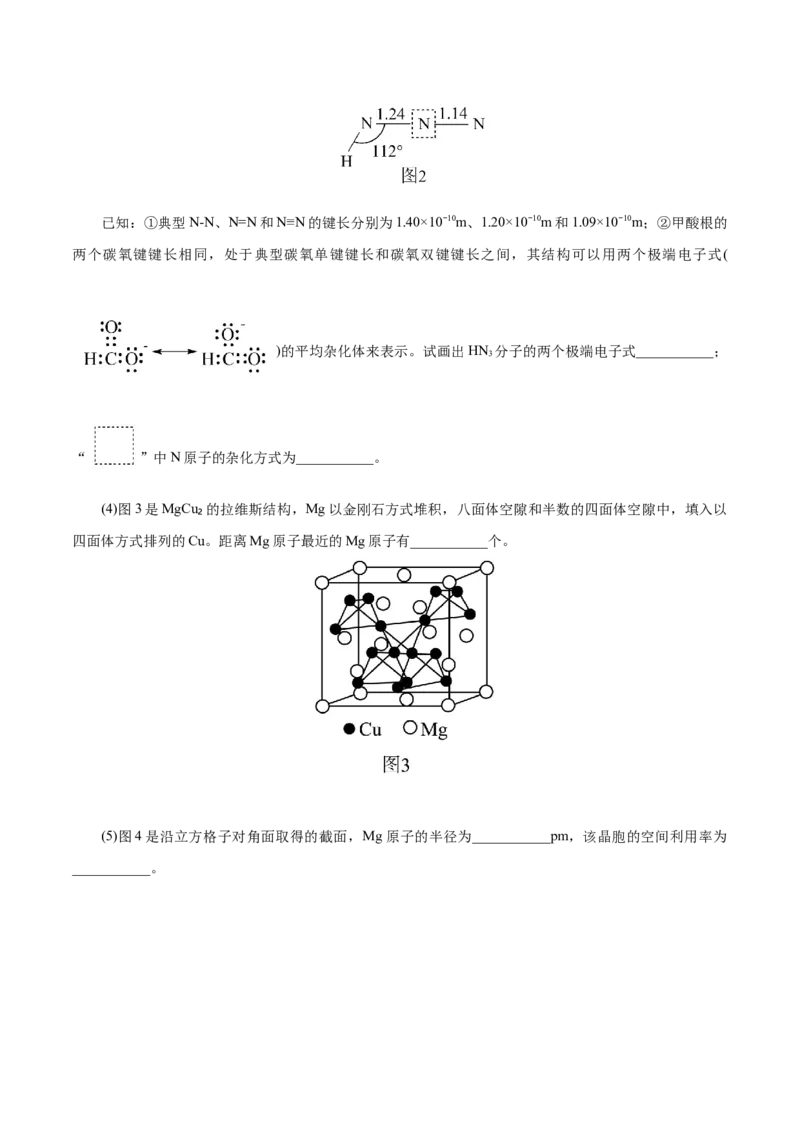
(2)N、O、F的第一电离能最小的是___________,SO₂F₂分子结构如图1所示,已知键角α为124°,β
为96°,则α>β的原因主要是___________。
(3)叠氮化物能与Fe³⁺、Cu²⁺及Co³⁺等形成配合物,如:[Co(N₃)(NH₃)₅]SO₄,该配合物中Co³⁺的配位数
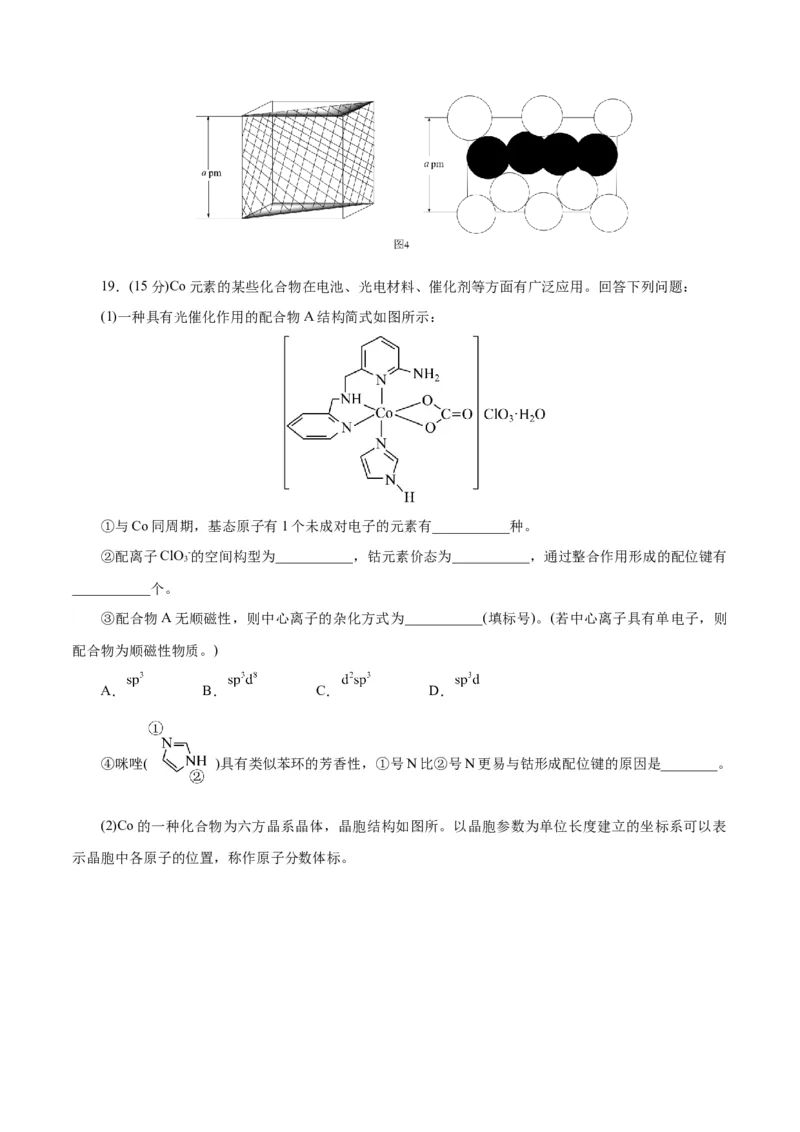
为___________。HN 分子的空间结构如图2所示(图中键长单位为10⁻10m)。
3已知:①典型N-N、N=N和N≡N的键长分别为1.40×10⁻10m、1.20×10⁻10m和1.09×10⁻10m;②甲酸根的
两个碳氧键键长相同,处于典型碳氧单键键长和碳氧双键键长之间,其结构可以用两个极端电子式(
)的平均杂化体来表示。试画出HN 分子的两个极端电子式___________;
3
“ ”中N原子的杂化方式为___________。
(4)图3是MgCu₂的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以
四面体方式排列的Cu。距离Mg原子最近的Mg原子有___________个。
(5)图4是沿立方格子对角面取得的截面,Mg原子的半径为___________pm,该晶胞的空间利用率为
___________。19.(15分)Co元素的某些化合物在电池、光电材料、催化剂等方面有广泛应用。回答下列问题:
(1)一种具有光催化作用的配合物A结构简式如图所示:
①与Co同周期,基态原子有1个未成对电子的元素有___________种。
②配离子ClO -的空间构型为___________,钴元素价态为___________,通过整合作用形成的配位键有
3
___________个。
③配合物A无顺磁性,则中心离子的杂化方式为___________(填标号)。(若中心离子具有单电子,则
配合物为顺磁性物质。)
A. B. C. D.
④咪唑( )具有类似苯环的芳香性,①号N比②号N更易与钴形成配位键的原因是________。
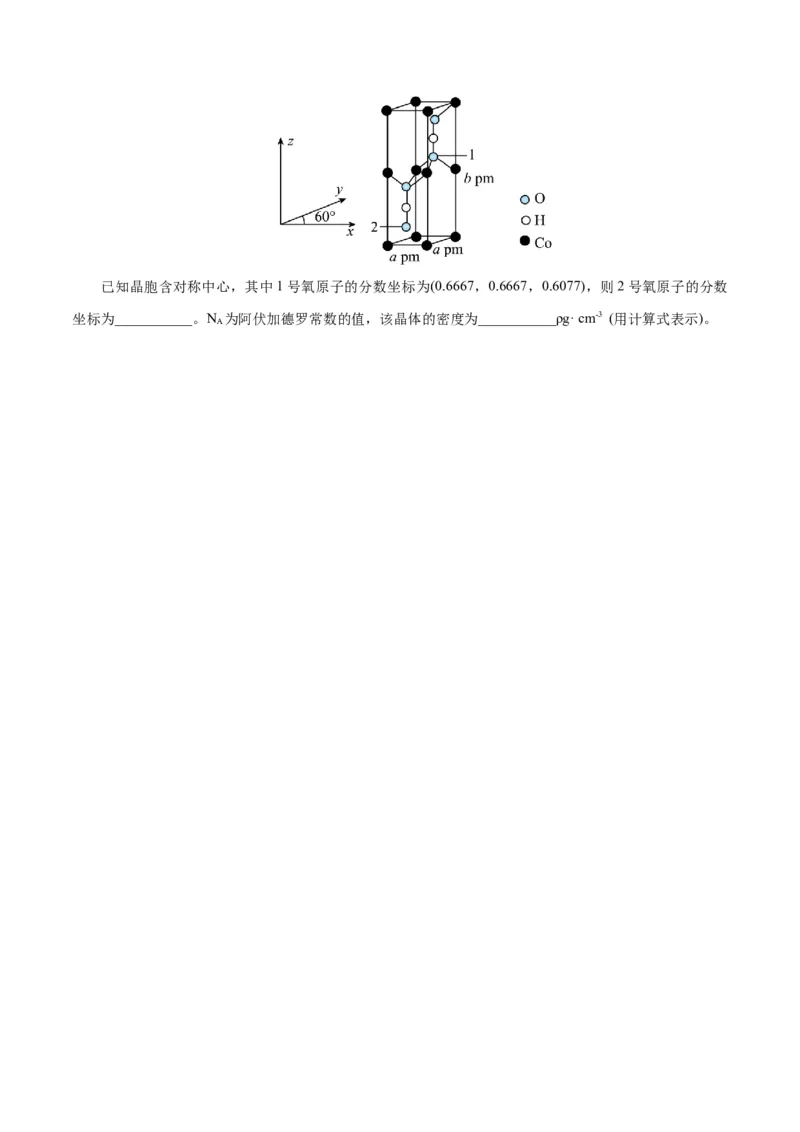
(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所。以晶胞参数为单位长度建立的坐标系可以表
示晶胞中各原子的位置,称作原子分数体标。已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数
坐标为___________。N 为阿伏加德罗常数的值,该晶体的密度为___________ρg· cm-3 (用计算式表示)。
A