文档内容
物质的分离与提纯
1.物质分离、提纯的方法
(1)依据物质的物理性质选择分离、提纯的方法
①“固+固”混合物的分离(或提纯)
②“液+液”混合物的分离(或提纯)
③“固+液”混合物的分离(或提纯)
(2)依据物质的化学性质选择分离、提纯的方法
方法 原理 杂质成分
沉淀
将杂质离子转化为沉淀
如Cl-、SO2-、CO2-及能形成沉淀的阳离子
4 3
法
气化
将杂质离子转化为气体
如CO2-、HCO- 、SO2-、HSO- 、S2-、NH+
3 3 3 3 4
法
杂转 将杂质转化为需要提纯的 如杂质中含不同价态的相同元素(用氧化剂或还原
纯法 物质 剂)、同一种酸的正盐与酸式盐(用酸、酸酐或碱)
氧化 用氧化剂(还原剂)除去具有如用 酸性 KMnO 溶液除去CO 中的SO 、用灼热
4 2 2
还原法 还原性(氧化性)的杂质 的铜网除去N 中的O
2 2
热分 加热使不稳定的物质分解
如除去NaCl中的NH Cl
4
解法 除去
酸碱 利用物质与酸或碱溶液混 如用过量的NaOH 溶液除去Fe O 中的Al O
2 3 2 3溶解法 合后的差异进行分离
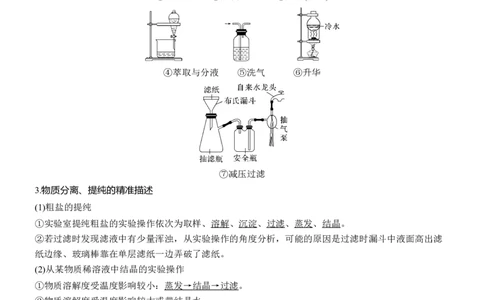
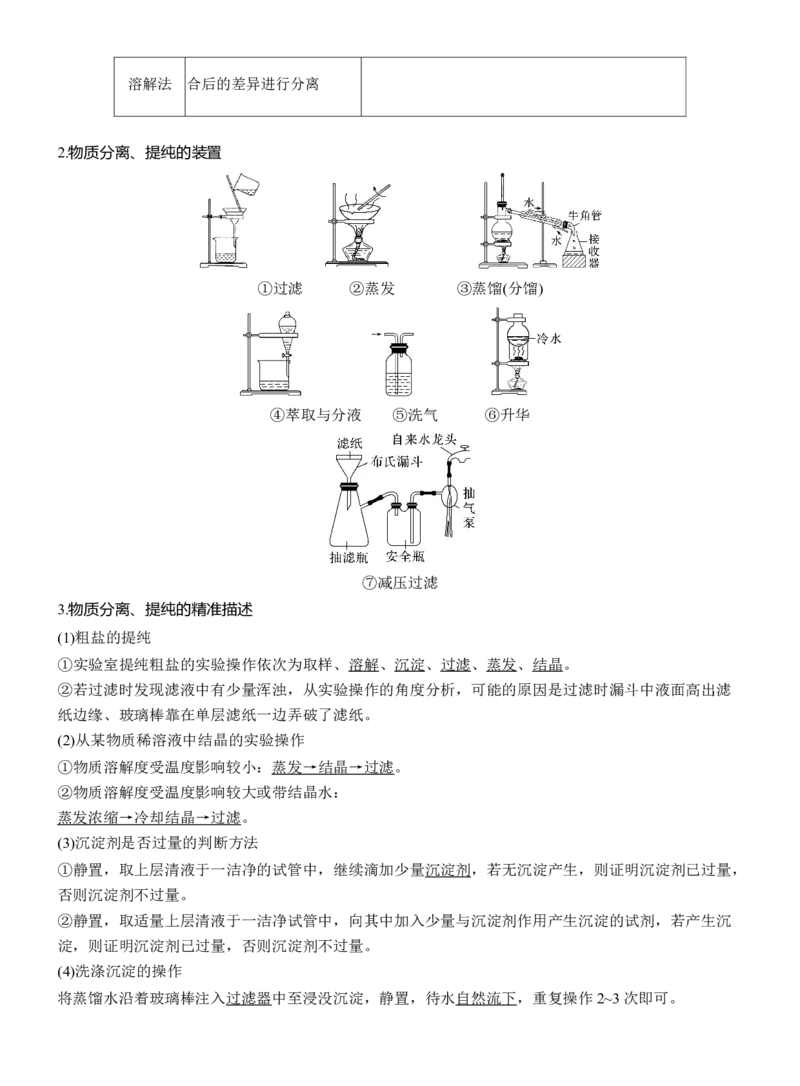
2.物质分离、提纯的装置
①过滤 ②蒸发 ③蒸馏(分馏)
④萃取与分液 ⑤洗气 ⑥升华
⑦减压过滤
3.物质分离、提纯的精准描述
(1)粗盐的提纯
①实验室提纯粗盐的实验操作依次为取样、溶解、沉淀、过滤、蒸发、结晶。
②若过滤时发现滤液中有少量浑浊,从实验操作的角度分析,可能的原因是过滤时漏斗中液面高出滤
纸边缘、玻璃棒靠在单层滤纸一边弄破了滤纸。
(2)从某物质稀溶液中结晶的实验操作
①物质溶解度受温度影响较小: 蒸发 → 结晶 → 过滤 。
②物质溶解度受温度影响较大或带结晶水:
蒸发浓缩 → 冷却结晶 → 过滤 。
(3)沉淀剂是否过量的判断方法
①静置,取上层清液于一洁净的试管中,继续滴加少量沉淀剂,若无沉淀产生,则证明沉淀剂已过量,
否则沉淀剂不过量。
②静置,取适量上层清液于一洁净试管中,向其中加入少量与沉淀剂作用产生沉淀的试剂,若产生沉
淀,则证明沉淀剂已过量,否则沉淀剂不过量。
(4)洗涤沉淀的操作
将蒸馏水沿着玻璃棒注入过滤器中至浸没沉淀,静置,待水自然流下,重复操作2~3次即可。(5)判断沉淀是否洗净的操作
取最后一次洗涤液,滴加……(试剂),若没有……现象,证明沉淀已经洗净。
应用示例
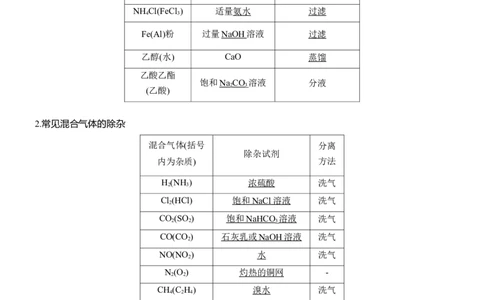
1.常见物质的除杂
物质(括号
除杂试剂 分离方法(或操作)
内为杂质)
FeCl (FeCl ) 氯水 加氧化剂转化法
3 2
Fe O (Al O ) 过量NaOH 溶液 过滤
2 3 2 3
NH Cl(FeCl ) 适量氨水 过滤
4 3
Fe(Al)粉 过量NaOH 溶液 过滤
乙醇(水) CaO 蒸馏
乙酸乙酯
饱和Na CO 溶液 分液
2 3
(乙酸)
2.常见混合气体的除杂
混合气体(括号 分离
除杂试剂
内为杂质) 方法
H (NH ) 浓硫酸 洗气
2 3
Cl (HCl) 饱和 NaC l 溶液 洗气
2
CO (SO ) 饱和 NaHCO 溶液 洗气
2 2 3
CO(CO ) 石灰乳或 NaOH 溶液 洗气
2
NO(NO ) 水 洗气
2
N (O ) 灼热的铜网 -
2 2
CH (C H ) 溴水 洗气
4 2 4
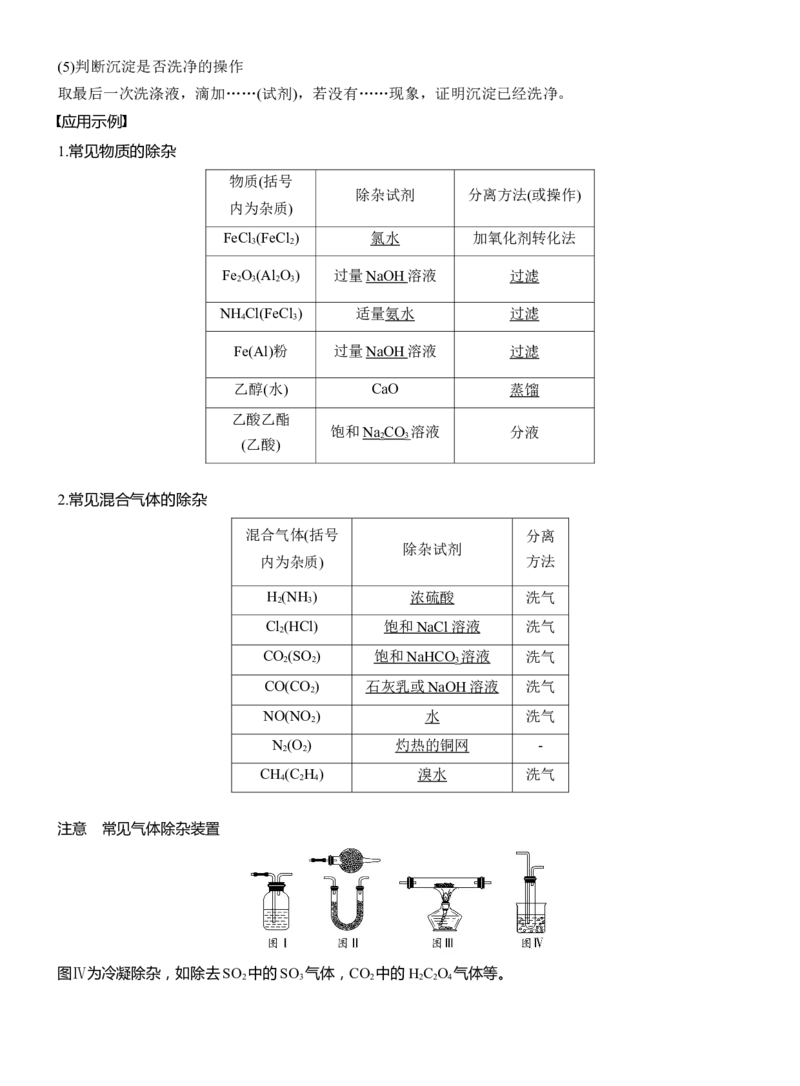
注意 常见气体除杂装置
图Ⅳ为冷凝除杂,如除去SO 中的SO 气体,CO 中的H C O 气体等。
2 3 2 2 2 41.(2024·湖北,3)关于物质的分离、提纯,下列说法错误的是( )
A.蒸馏法分离CH Cl 和CCl
2 2 4
B.过滤法分离苯酚和NaHCO 溶液
3
C.萃取和柱色谱法从青蒿中提取分离青蒿素
D.重结晶法提纯含有少量食盐和泥沙的苯甲酸
答案 B
解析 二氯甲烷和四氯化碳互溶,二者沸点不同,可用蒸馏法分离,A正确;将青蒿浸泡在有机溶剂中得
到提取液,寻找合适的萃取剂,利用萃取的方法将提取液中的青蒿素提取出来;也可以利用不同溶质在色
谱柱上的保留时间不同将青蒿素固定在色谱柱上,再利用极性溶剂将青蒿素洗脱下来,得到纯净的青蒿素,
C正确;苯甲酸在水中的溶解度随温度变化较大,可利用重结晶的方式将低温下溶解度较小的苯甲酸提纯
出来,D正确。
2.(2024·浙江1月选考,6)为回收利用含I 的CCl 废液,某化学兴趣小组设计方案如下所示,下列说法
2 4
不正确的是( )
A.步骤Ⅰ中,加入足量Na CO 溶液充分反应后,上下两层均为无色
2 3
B.步骤Ⅰ中,分液时从分液漏斗下口放出溶液A
C.试剂X可用硫酸
D.粗I 可用升华法进一步提纯
2
答案 B
解析 步骤Ⅰ中,加入足量碳酸钠溶液与碘反应得到含有碘化钠和碘酸钠的混合溶液,则充分反应后,上
下两层均为无色,上层为含有碘化钠和碘酸钠的混合溶液,下层为四氯化碳,分液时应从分液漏斗上口倒
出溶液A,故A正确、B错误;向溶液A中加入硫酸的目的是使碘化钠和碘酸钠在酸性条件下发生归中反
应生成碘,则试剂X可用硫酸,故C正确;碘受热会发生升华,所以实验制得的粗碘可用升华法进一步提
纯,故D正确。
3.(2020·全国卷Ⅰ,9)下列气体去除杂质的方法中,不能实现目的的是( )
选项 气体(杂质) 方法
A SO (H S) 通过酸性高锰酸钾溶液
2 2
B Cl (HCl) 通过饱和的食盐水
2
C N (O ) 通过灼热的铜丝网
2 2
D NO(NO ) 通过氢氧化钠溶液
2答案 A
解析 酸性高锰酸钾溶液不仅能与H S反应,也能与SO 反应,A项不能实现目的。
2 2
4.(2021·湖北,7)某兴趣小组为制备1⁃ 氯 ⁃2⁃ 甲基丙烷(沸点69 ℃),将2⁃ 甲基 ⁃1⁃ 丙醇和POCl
3
溶于CH
2
Cl
2
中,加热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl ,分液收集CH Cl 层,无
3 2 2
水MgSO 干燥、过滤、蒸馏后得到目标产物。上述过程中涉及的装置或操作错误的是(夹持及加热装置
4
略)( )
A B C D
答案 B
解析 依题意,制备产品需要“搅拌、加热回流”,A项正确;副产物氯化氢极易溶于氢氧化钠溶液,不
能直接将尾气通入氢氧化钠溶液中,这样易发生倒吸现象,B项错误;分液收集二氯甲烷层需用到分液漏
斗,振荡时需将分液漏斗倒转过来放气,避免分液漏斗内气压过大,发生危险,C项正确;蒸馏时需要用
温度计指示温度,冷凝水从下口进、上口出,提高冷凝效率,D项正确。
物质分离与提纯的思维模型
题型突破练 [分值:50 分]
(选择题1~6题,每小题3分,7~14题,每小题4分,共50分)
1.(2024·山东日照二模)《天工开物》有如下叙述:“凡硝刮扫取时(墙中亦或迸出),入缸内水浸一宿,秽
杂之物浮于面上,掠取去时,然后入釜,注水煎炼,硝化水干,倾于器内,经过一宿,即结成硝……欲去
杂还纯,再入水煎炼”。文中不涉及的操作方法是( )A.分液 B.溶解
C.蒸发结晶 D.重结晶
答案 A
解析 “秽杂之物浮于面上,掠取去时”,指过滤;“然后入釜,注水煎炼”,指溶解;“硝化水干”,
指蒸发结晶;“欲去杂还纯,再入水煎炼”,指重结晶。
2.(2024·济南高三一模)《本草纲目》富载中医药文化和科学知识。其中记载“冬月灶中所烧薪柴之灰。令
人以灰淋汁,取碱浣衣”。下列有关解释错误的是( )
A.“烧薪柴”主要是纤维素等有机物的燃烧
B.“薪柴之灰”可作农用肥,但不与铵态氮肥混用
C.“以灰淋汁”所涉及的分离操作有溶解、分液
D.“取碱浣衣”与酯的水解有关
答案 C
解析 “薪柴”的主要成分是纤维素等有机物,所以“烧薪柴”主要是纤维素等有机物的燃烧,A正确;
因碳酸根离子与铵根离子发生互相促进的水解反应可使肥效减弱,故“薪柴之灰”不与铵态氮肥混用,B
正确;“以灰淋汁”所涉及的操作有溶解、过滤,C错误;草木灰的主要成分是碳酸钾,碳酸钾水解显碱
性,可使衣服中的油脂水解,D正确。
3.(2024·江西赣州二模)中华传统文化源远流长。如图是传统酿酒工艺的装置。
下列仪器与装置X(虚线框内)作用相同的是( )
A.直形冷凝管 B.蒸馏烧瓶 C.分液漏斗 D.锥形瓶
答案 A
解析 图中装置X的作用是冷凝气体,与直形冷凝管作用相同。
4.(2024·安徽滁州二模)下列实验装置及操作正确的是( )A.除去乙酸中的乙醇
B.除去水中的苯酚
C.除去尾气中的SO
2
D.除去溶在CCl 中的Br
4 2
答案 D
解析 乙酸与乙醇互溶,应蒸馏分离,A错误;苯酚微溶于水,形成乳浊液,则过滤不能分离,B错误;
SO 不与饱和NaHSO 溶液反应,故无法除去尾气中的SO ,C错误;溴与氢氧化钠溶液反应,生成易溶于
2 3 2
水的溴化钠和次溴酸钠,与四氯化碳溶液不互溶,可分液将其除去,D正确。
5.下列除杂操作可行的是( )
A.加热升华除去铁粉中的I
2
B.加浓溴水用过滤法除去苯中的苯酚
C.蒸发结晶除去KNO 溶液中的NaCl
3
D.加MgO粉末用过滤法除去MgCl 溶液中的FeCl
2 3
答案 D
解析 铁粉中混有I 时,加热会促进二者发生反应生成FeI ,A不可行;苯中混有苯酚,加浓溴水时,苯
2 2
酚转化为2,4,6⁃三溴苯酚,但仍溶解在苯中,应加NaOH溶液将苯酚转化为苯酚钠,然后分液,B不可
行;KNO 溶液中混有NaCl,应采用蒸发浓缩、降温结晶的方法让KNO 结晶析出,C不可行;除去MgCl
3 3 2
溶液中的FeCl ,通常调节溶液的pH让FeCl 水解生成Fe(OH) 沉淀,再用过滤法除去Fe(OH) ,D可行。
3 3 3 3
6.(2024·河南信阳二模)除去下列物质中的杂质(括号中的物质为杂质),所选除杂试剂和分离方法均正确的
是( )
选项 被提纯的物质(杂质) 除杂试剂 分离方法
A KBr溶液(Br ) 四氯化碳 萃取、分液
2
B AlCl (小苏打) 蒸馏水 重结晶
3
C FeCl 溶液(FeCl ) 过量铜粉 过滤
2 3D 乙烷(乙烯) 酸性高锰酸钾溶液 洗气
答案 A
解析 Br 易溶于四氯化碳,KBr难溶于四氯化碳,加入四氯化碳萃取分液可除去KBr溶液中的Br ,故A
2 2
正确;AlCl 、碳酸氢钠溶于水后发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳,不能用蒸馏水除
3
AlCl 中的小苏打,故B错误;FeCl 和Cu反应生成FeCl 和CuCl ,若用铜粉除FeCl 溶液中的FeCl 会引
3 3 2 2 2 3
入新杂质CuCl ,故C错误;乙烯能被高锰酸钾氧化为二氧化碳,若用酸性高锰酸钾除乙烷中的乙烯会引
2
入新杂质二氧化碳,故D错误。
7.(2024·广东汕头一模)为除去物质中混有的杂质,所选试剂与方法均正确的是( )
选项 物质(杂质) 除杂试剂 方法
A CO (CO) O 点燃
2 2
B Na O (Na O) O 加热
2 2 2 2
C Al O (Fe O ) NaOH溶液 过滤
2 3 2 3
D 乙醇(H O) 无水CuSO 分液
2 4
答案 B
解析 无法控制O 的用量,易引入新杂质,且CO 中混有少量CO不易燃烧,A错误;Na O不稳定,与
2 2 2
O 在加热条件下反应生成Na O ,因此通入足量的O ,加热可以除杂,B正确;NaOH溶液能与Al O 发生
2 2 2 2 2 3
反应生成Na[Al(OH) ],将主要物质除去而不能除去杂质,C错误;除去乙醇中含有的水应该加入生石灰,
4
生石灰与水反应生成氢氧化钙,与乙醇不反应,氢氧化钙不挥发,蒸馏可以得到纯净的乙醇,若用无水
CuSO 吸水效果不理想,且CuSO 吸水后受热还会脱水,D错误。
4 4
8.(2024·吉林白山二模)历经千年传承积淀,形成精湛的东阿阿胶传统工艺,包括洗皮、泡皮、晾皮、刮毛、
铡皮、化皮、打沫、除渣、浓缩、挂旗、凝胶、切胶等工序。下列工序与化学实验中的原理不具有对应关
系的是( )
选项 A B C D
工序
化学
实验
答案 D解析 化皮指的是将皮煮化,与实验中的加热溶解原理相对应,A项不符合题意;除渣指的是用过滤的方
法将不溶性物质除掉,与实验中的过滤原理相对应,B项不符合题意;挂旗指的是熬制过程中达到挂旗的
状态,用勺子舀起来非常黏稠,与实验中的蒸发浓缩原理相对应,C项不符合题意;凝胶指的是阿胶冷却
凝固的过程,与实验中的渗析原理不具有对应关系,D项符合题意。
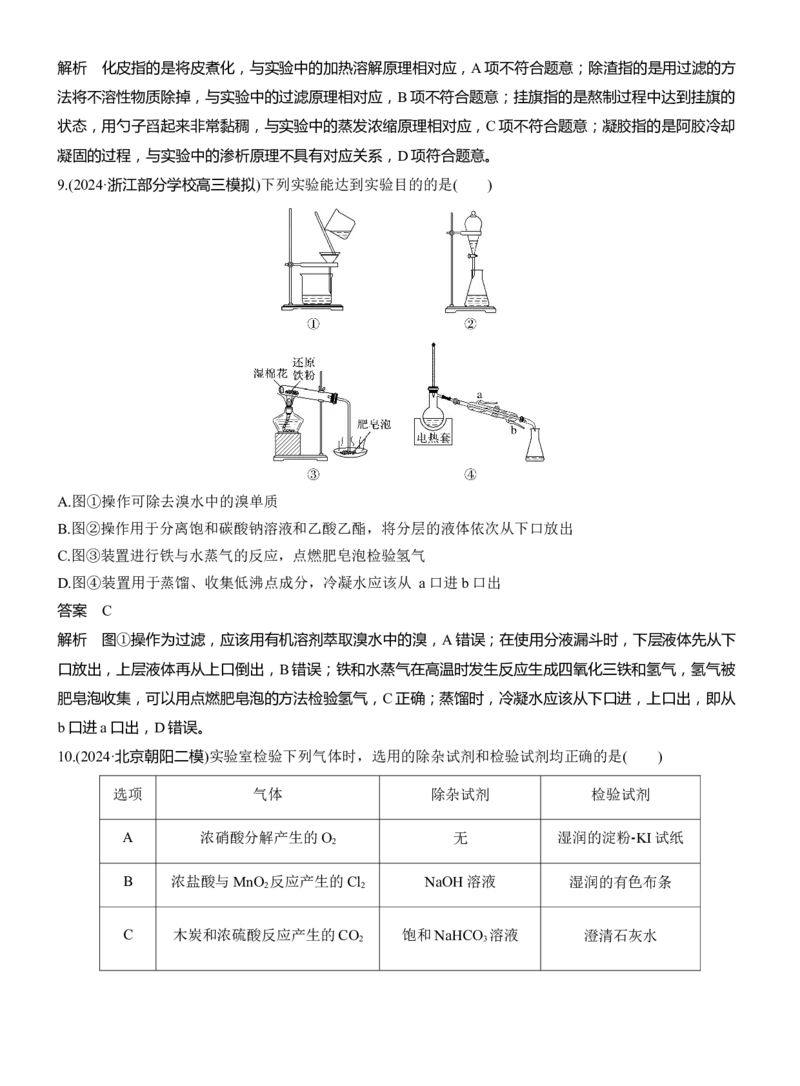
9.(2024·浙江部分学校高三模拟)下列实验能达到实验目的的是( )
A.图①操作可除去溴水中的溴单质
B.图②操作用于分离饱和碳酸钠溶液和乙酸乙酯,将分层的液体依次从下口放出
C.图③装置进行铁与水蒸气的反应,点燃肥皂泡检验氢气
D.图④装置用于蒸馏、收集低沸点成分,冷凝水应该从 a口进b口出
答案 C
解析 图①操作为过滤,应该用有机溶剂萃取溴水中的溴,A错误;在使用分液漏斗时,下层液体先从下
口放出,上层液体再从上口倒出,B错误;铁和水蒸气在高温时发生反应生成四氧化三铁和氢气,氢气被
肥皂泡收集,可以用点燃肥皂泡的方法检验氢气,C正确;蒸馏时,冷凝水应该从下口进,上口出,即从
b口进a口出,D错误。
10.(2024·北京朝阳二模)实验室检验下列气体时,选用的除杂试剂和检验试剂均正确的是( )
选项 气体 除杂试剂 检验试剂
A 浓硝酸分解产生的O
2
无 湿润的淀粉 ⁃KI试纸
B 浓盐酸与MnO 反应产生的Cl NaOH溶液 湿润的有色布条
2 2
C 木炭和浓硫酸反应产生的CO 饱和NaHCO 溶液 澄清石灰水
2 3D NH HCO 分解产生的NH CaO和NaOH混合物 湿润的红色石蕊试纸
4 3 3
答案 D
解析 挥发的硝酸或分解生成的二氧化氮氧化KI生成碘,淀粉遇碘单质变蓝,不能证明浓硝酸分解产生
O ,A错误;氯气与NaOH溶液反应,B错误;生成的二氧化硫与碳酸氢钠溶液反应生成二氧化碳,不能
2
证明木炭和浓硫酸反应产生CO ,C错误;碳酸氢铵分解生成氨气、水、二氧化碳, CaO和NaOH混合物
2
可除去水和二氧化碳,氨气可使湿润的红色石蕊试纸变蓝,可检验生成的氨气,D正确。
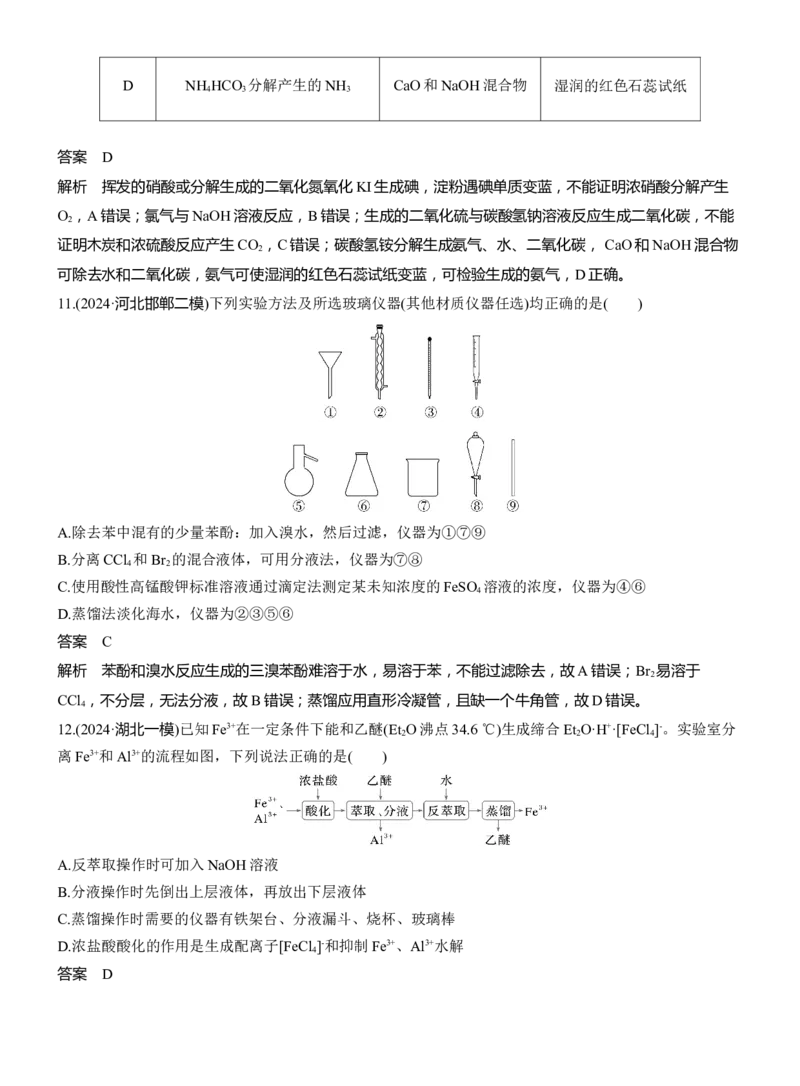
11.(2024·河北邯郸二模)下列实验方法及所选玻璃仪器(其他材质仪器任选)均正确的是( )
A.除去苯中混有的少量苯酚:加入溴水,然后过滤,仪器为①⑦⑨
B.分离CCl 和Br 的混合液体,可用分液法,仪器为⑦⑧
4 2
C.使用酸性高锰酸钾标准溶液通过滴定法测定某未知浓度的FeSO 溶液的浓度,仪器为④⑥
4
D.蒸馏法淡化海水,仪器为②③⑤⑥
答案 C
解析 苯酚和溴水反应生成的三溴苯酚难溶于水,易溶于苯,不能过滤除去,故A错误;Br 易溶于
2
CCl ,不分层,无法分液,故B错误;蒸馏应用直形冷凝管,且缺一个牛角管,故D错误。
4
12.(2024·湖北一模)已知Fe3+在一定条件下能和乙醚(Et O沸点34.6 ℃)生成缔合Et O·H+·[FeCl ]-。实验室分
2 2 4
离Fe3+和Al3+的流程如图,下列说法正确的是( )
A.反萃取操作时可加入NaOH溶液
B.分液操作时先倒出上层液体,再放出下层液体
C.蒸馏操作时需要的仪器有铁架台、分液漏斗、烧杯、玻璃棒
D.浓盐酸酸化的作用是生成配离子[FeCl ]-和抑制Fe3+、Al3+水解
4
答案 D解析 加水进行反萃取操作后,铁元素在溶液中主要以Fe3+形式存在,若加入NaOH溶液会导致Fe3+转化
为Fe(OH) 沉淀,故A错误;分液操作时应先放出下层液体,再倒出上层液体,故B错误;蒸馏操作时需
3
要的仪器有酒精灯、铁架台、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶等,故C错误;加入浓盐酸可
以提供H+和Cl-,前者抑制Fe3+、Al3+水解,后者与Fe3+络合生成[FeCl ]-,故D正确。
4
13.(2024·浙江丽水二模)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO2-
以及泥沙等杂质,某同学设计了一种制备
4
精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),下列有关说法正确的是( )
A.步骤①:根据粗盐的质量和溶解度来确定烧杯和量筒的规格
B.步骤②~④:BaCl 、NaOH和Na CO 的滴加“顺序”和“量”不可调整
2 2 3
C.步骤⑥:用玻璃棒搅拌滤液,直到没有气泡冒出,且pH试纸检验滤液呈碱性
D.步骤①~⑦:需要的实验仪器有分液漏斗、蒸发皿、玻璃棒、陶土网和胶头滴管
答案 A
解析 步骤②~④中:Na CO 必须要在加完BaCl 溶液之后再加入,作用是除去Ca2+和过量的Ba2+,NaOH
2 3 2
的滴加顺序没有要求,B错误;步骤⑥加适量HCl除去③加入的过量的OH-和④加入的过量的CO2-
,加入
3
的盐酸是过量的,溶液呈酸性,C错误;步骤①~⑦中没有分液,不需要用到分液漏斗,D错误。
14.(2024·浙江台州二模)某实验小组设计粗KNO 固体(只含有少量NaCl)的提纯方案如下:
3
下列说法不正确的是( )
A.操作Ⅰ中依据硝酸钾的溶解度估算加水量
B.操作Ⅱ缓慢冷却有利于硝酸钾析出大晶体
C.操作Ⅲ常用到的玻璃仪器为玻璃棒、烧杯和漏斗
D.操作Ⅳ用热水洗涤晶体
答案 D
解析 加水溶解时需保证硝酸钾完全溶解,则操作Ⅰ中依据硝酸钾的溶解度估算加水量,故A正确;操作
Ⅱ缓慢冷却,结晶的速度慢,有利于硝酸钾析出大晶体,故B正确;操作Ⅲ是过滤,常用到的玻璃仪器为
玻璃棒、烧杯和漏斗,故C正确;硝酸钾在冷水中溶解度小,则操作Ⅳ可用冷水洗涤晶体,减少溶解损失,
故D错误。