文档内容
2025新教材化学高考第一轮
专题八 化学键 分子和晶体的结构与性质
1.下列分子属于非极性分子的是( )
A.CH Cl B.CS C.NCl D.H S
2 2 2 3 2
2.反应SiO +4HF SiF ↑+2H O应用于玻璃雕刻。下列说法正确的是( )
2 4 2
A.SiO 属于共价化合物
2
B.HF的电子式为
C.SiF 是由极性键形成的极性分子
4
D.基态氧原子的价电子轨道表示式为
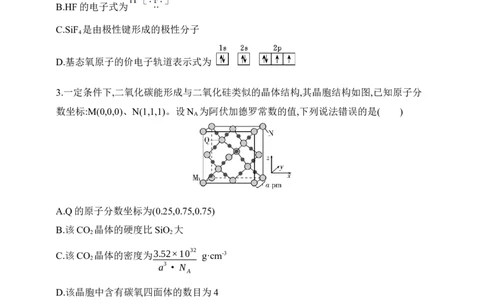
3.一定条件下,二氧化碳能形成与二氧化硅类似的晶体结构,其晶胞结构如图,已知原子分
数坐标:M(0,0,0)、N(1,1,1)。设N 为阿伏加德罗常数的值,下列说法错误的是( )
A
A.Q的原子分数坐标为(0.25,0.75,0.75)
B.该CO 晶体的硬度比SiO 大
2 2
C.该CO
晶体的密度为3.52×1032
g·cm-3
2
a3·N
A
D.该晶胞中含有碳氧四面体的数目为4
4.反应2NH +NaClO N H +NaCl+H O用于合成N H 。下列说法不正确的是( )
3 2 4 2 2 4
A.NH 的空间结构为正三角形
3
B.NaClO的电子式为
C.N H 含有极性键和非极性键
2 4
D.H O和N H 之间可以形成氢键
2 2 4
5.NCl 可发生水解反应NCl +3H O NH +3HClO,下列说法正确的是( )
3 3 2 3
A.NCl 中N原子的杂化类型为sp2杂化
3B.H O为非极性分子
2
C.NH 分子空间结构为平面三角形
3
D.HClO的电子式为
6.下列说法正确的是( )
A.SO 与CO 分子是含有极性键的极性分子
2 2
B.SO 与CO 中键角都为180°
2 2
C.1 mol (SO ) 分子中含有12 mol σ键(结构为 )
3 3
D.H SO 的酸性比H SO 的酸性强
2 3 2 4
7.下列有关说法正确的是( )
A.HCl与NaCl的晶体类型相同
B.Cl 和Cl 中的O—Cl—O夹角都为109°28'
O- O-
3 4
C.CuCl 中Cu2+基态时未成对电子数为5
2
D.Cl O与HClO都是由极性键构成的极性分子
2
8.含氰废水中氰化物的主要形态是HCN和CN-,CN-具有较强的配位能力,能与Cu+形成一
种无限长链离子,其片段为
CN-结合H+能力弱于C 。氰化物浓度较低时,可在碱性条件下用H O 或Cl 将其转化
O2− 2 2 2
3
为N ;浓度较高时,可加入HCN、Fe和K CO 溶液反应生成K [Fe(CN) ]溶液。下列说法
2 2 3 4 6
正确的是( )
A.基态Fe2+核外电子排布式为[Ar]3d54s1
B.Cu+与CN-形成的离子的化学式为[Cu(CN) ]2-
3
C.K [Fe(CN) ]中Fe2+的配位数为6
4 6
D.某铁晶体(晶胞如图所示)中与每个Fe紧邻的Fe数为6
9.下列化学用语或图示表达正确的是( )A.二氧化碳的电子式:
B.顺-2-丁烯的分子结构模型:
C.NH 的VSEPR模型:
3
D.基态Cr原子的价层电子轨道表示式:
10.下列有关说法错误的是( )
A.有手性异构体的分子叫做手性分子
B.臭氧是极性分子,可用于自来水的消毒
C.冠醚可利用其空穴大小适配相应碱金属离子,两者能通过弱相互作用形成超分子
D.乳酸加聚得到聚乳酸,聚乳酸因具有良好的生物相容性和可吸收性,可用于手术缝合
11.下列关于物质的结构或性质及解释均正确的是( )
选项 物质的结构或性质 解释
A 键角:H O>NH 水分子中O上孤电子对数比氨分子中N上的多
2 3
B 稳定性:HF>HCl HF分子间氢键强于HCl分子间作用力
C 熔点:碳化硅>金刚石 C—Si键的键能大于C—C键的键能
酸
C—F 键 的 极 性 大 于 C—Cl 键 的 极 性 , 导 致
D 性:CF COOH>CCl CO
3 3 CF COOH的羧基中的羟基极性更大,氢更易电离
OH 3
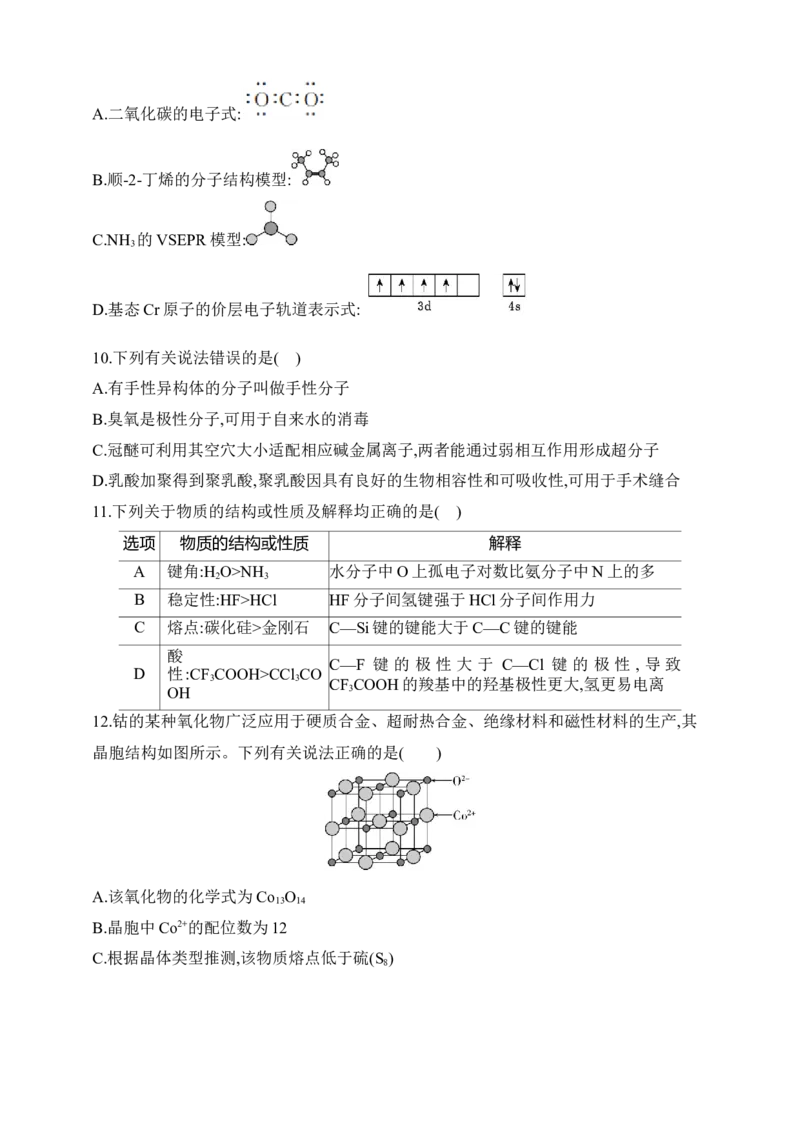
12.钴的某种氧化物广泛应用于硬质合金、超耐热合金、绝缘材料和磁性材料的生产,其
晶胞结构如图所示。下列有关说法正确的是( )
A.该氧化物的化学式为Co O
13 14
B.晶胞中Co2+的配位数为12
C.根据晶体类型推测,该物质熔点低于硫(S )
8D.若该氧化物的密度为ρ g·cm-3,阿伏加德罗常数为N mol-1,则晶胞中两个O2-间的最短
A
距离是√2×√ 300 cm
3
2 ρN
A
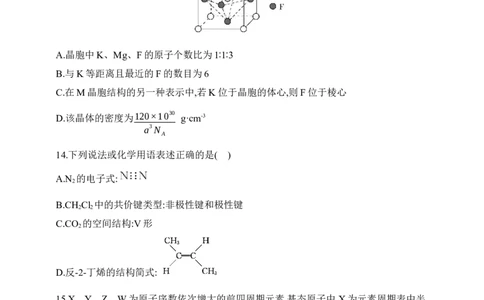
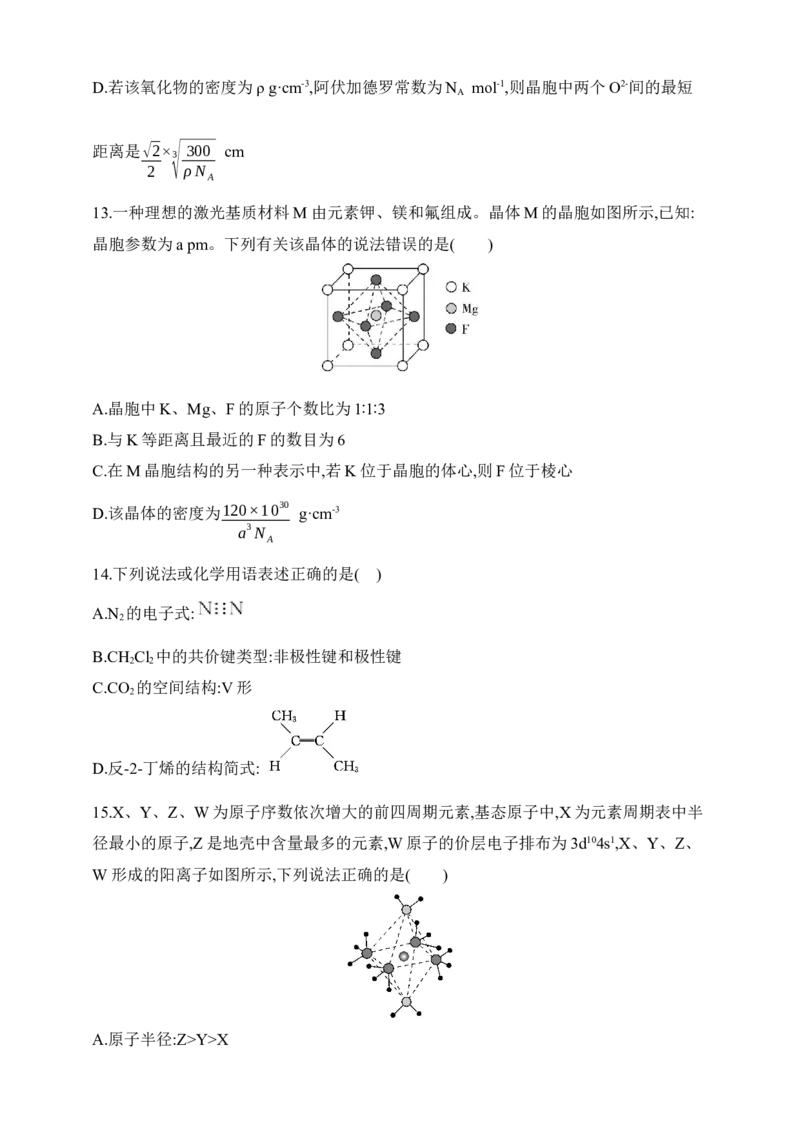
13.一种理想的激光基质材料M由元素钾、镁和氟组成。晶体M的晶胞如图所示,已知:
晶胞参数为a pm。下列有关该晶体的说法错误的是( )
A.晶胞中K、Mg、F的原子个数比为1∶1∶3
B.与K等距离且最近的F的数目为6
C.在M晶胞结构的另一种表示中,若K位于晶胞的体心,则F位于棱心
D.该晶体的密度为120×1030
g·cm-3
a3N
A
14.下列说法或化学用语表述正确的是( )
A.N 的电子式:
2
B.CH Cl 中的共价键类型:非极性键和极性键
2 2
C.CO 的空间结构:V形
2
D.反-2-丁烯的结构简式:
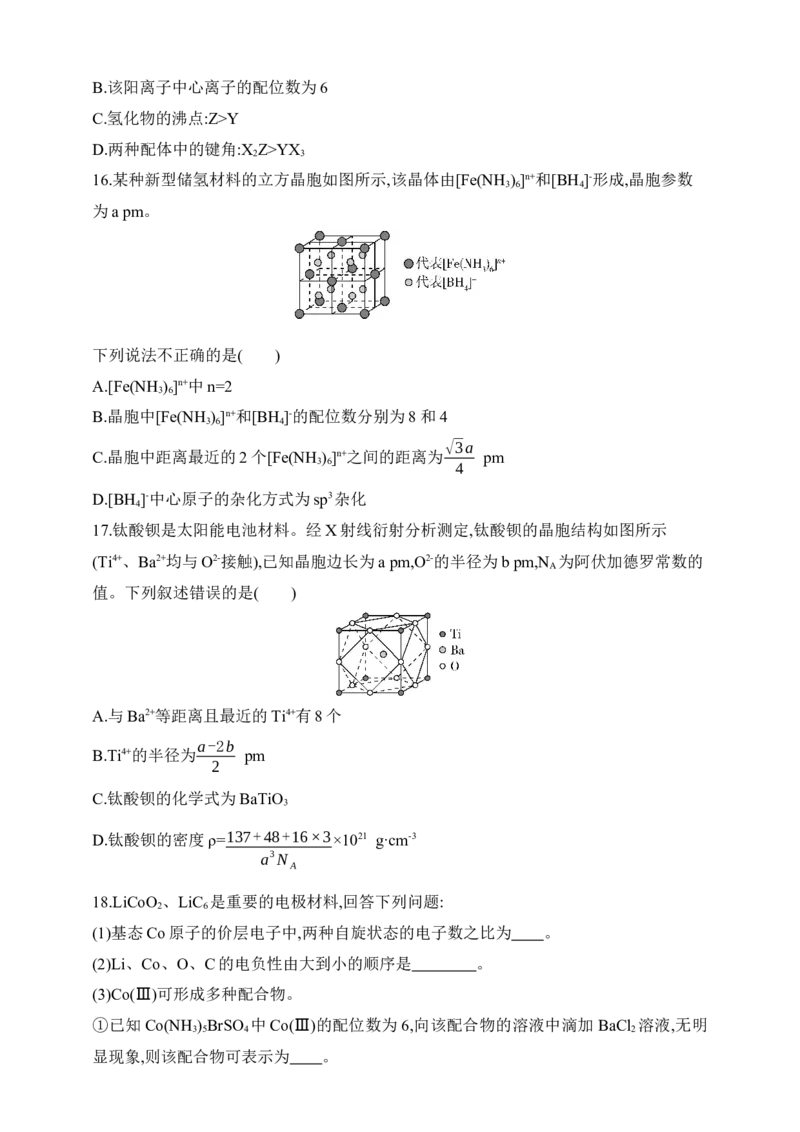
15.X、Y、Z、W为原子序数依次增大的前四周期元素,基态原子中,X为元素周期表中半
径最小的原子,Z是地壳中含量最多的元素,W原子的价层电子排布为3d104s1,X、Y、Z、
W形成的阳离子如图所示,下列说法正确的是( )
A.原子半径:Z>Y>XB.该阳离子中心离子的配位数为6
C.氢化物的沸点:Z>Y
D.两种配体中的键角:X Z>YX
2 3
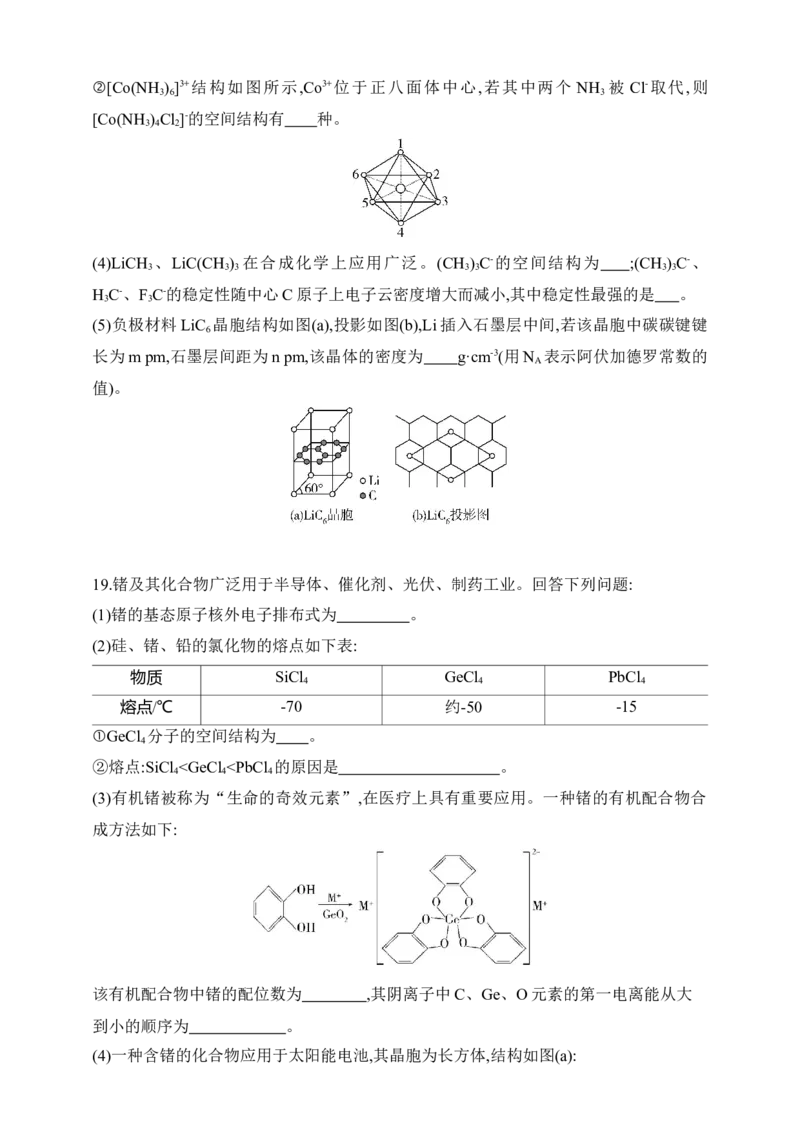
16.某种新型储氢材料的立方晶胞如图所示,该晶体由[Fe(NH ) ]n+和[BH ]-形成,晶胞参数
3 6 4
为a pm。
下列说法不正确的是( )
A.[Fe(NH ) ]n+中n=2
3 6
B.晶胞中[Fe(NH ) ]n+和[BH ]-的配位数分别为8和4
3 6 4
√3a
C.晶胞中距离最近的2个[Fe(NH ) ]n+之间的距离为 pm
3 6
4
D.[BH ]-中心原子的杂化方式为sp3杂化
4
17.钛酸钡是太阳能电池材料。经X射线衍射分析测定,钛酸钡的晶胞结构如图所示
(Ti4+、Ba2+均与O2-接触),已知晶胞边长为a pm,O2-的半径为b pm,N 为阿伏加德罗常数的
A
值。下列叙述错误的是( )
A.与Ba2+等距离且最近的Ti4+有8个
a-2b
B.Ti4+的半径为 pm
2
C.钛酸钡的化学式为BaTiO
3
D.钛酸钡的密度ρ=137+48+16×3×1021 g·cm-3
a3N
A
18.LiCoO 、LiC 是重要的电极材料,回答下列问题:
2 6
(1)基态Co原子的价层电子中,两种自旋状态的电子数之比为 。
(2)Li、Co、O、C的电负性由大到小的顺序是 。
(3)Co(Ⅲ)可形成多种配合物。
①已知Co(NH ) BrSO 中Co(Ⅲ)的配位数为6,向该配合物的溶液中滴加 BaCl 溶液,无明
3 5 4 2
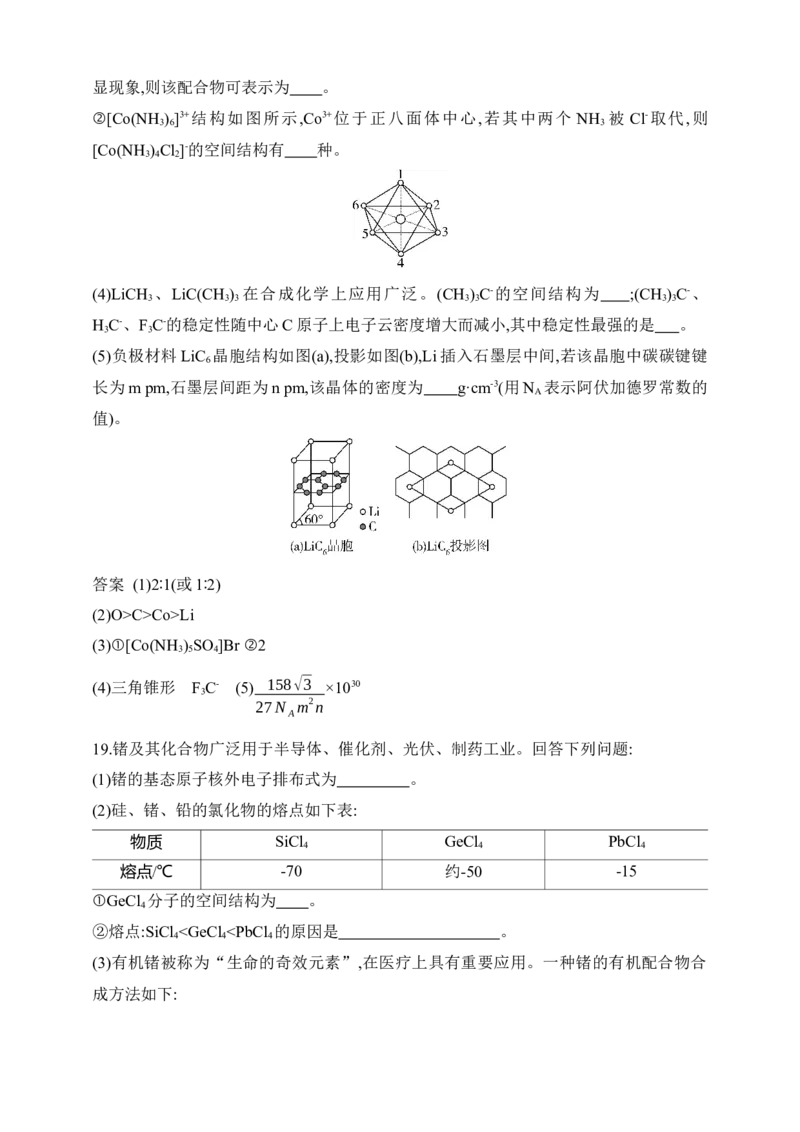
显现象,则该配合物可表示为 。②[Co(NH ) ]3+结构如图所示,Co3+位于正八面体中心,若其中两个 NH 被 Cl-取代,则
3 6 3
[Co(NH ) Cl ]-的空间结构有 种。
3 4 2
(4)LiCH 、LiC(CH ) 在合成化学上应用广泛。(CH ) C-的空间结构为 ;(CH ) C-、
3 3 3 3 3 3 3
H C-、F C-的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是 。
3 3
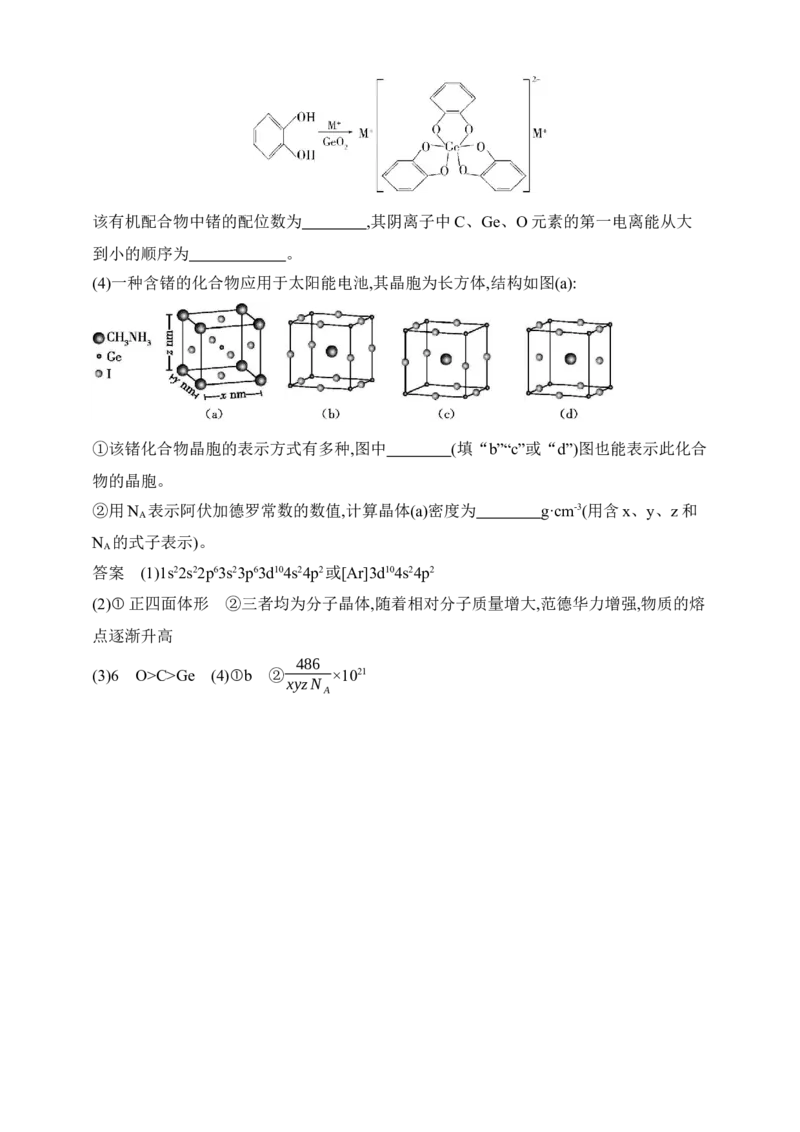
(5)负极材料LiC 晶胞结构如图(a),投影如图(b),Li插入石墨层中间,若该晶胞中碳碳键键
6
长为m pm,石墨层间距为n pm,该晶体的密度为 g·cm-3(用N 表示阿伏加德罗常数的
A
值)。
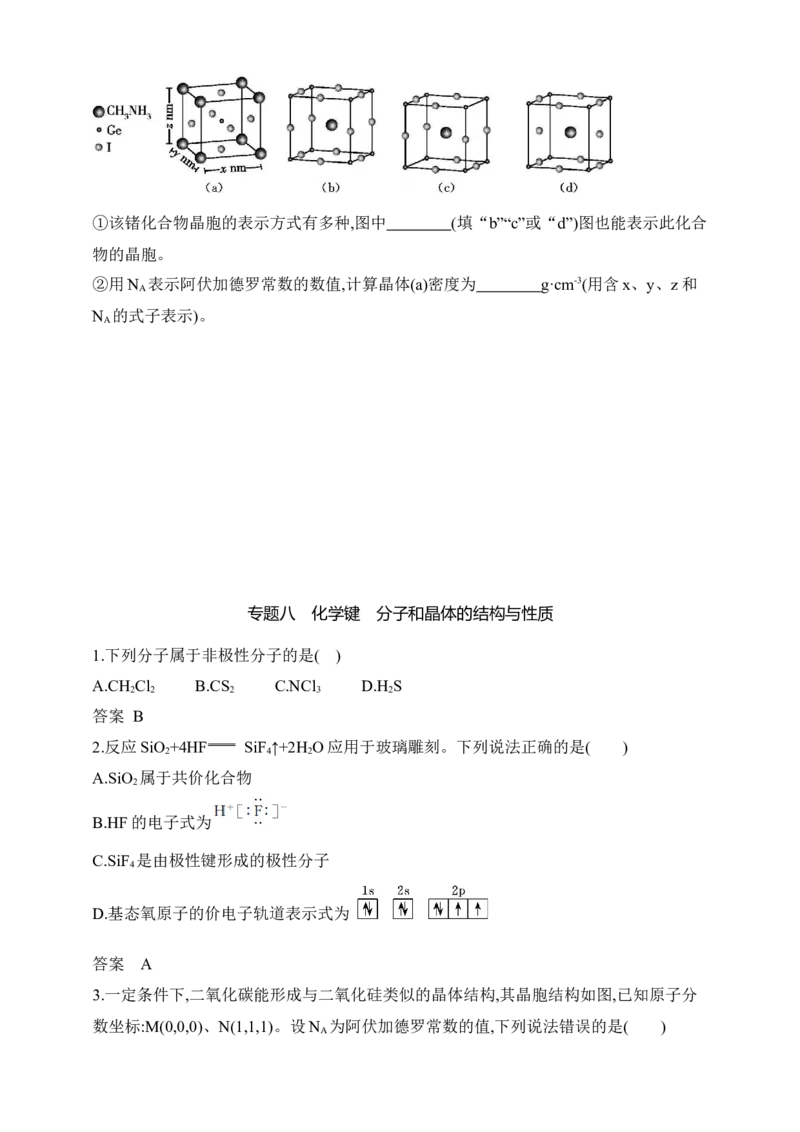
19.锗及其化合物广泛用于半导体、催化剂、光伏、制药工业。回答下列问题:
(1)锗的基态原子核外电子排布式为 。
(2)硅、锗、铅的氯化物的熔点如下表:
物质 SiCl GeCl PbCl
4 4 4
熔点/℃ -70 约-50 -15
①GeCl 分子的空间结构为 。
4
②熔点:SiCl NH 水分子中O上孤电子对数比氨分子中N上的多
2 3
B 稳定性:HF>HCl HF分子间氢键强于HCl分子间作用力
C 熔点:碳化硅>金刚石 C—Si键的键能大于C—C键的键能
酸
C—F 键 的 极 性 大 于 C—Cl 键 的 极 性 , 导 致
D 性:CF COOH>CCl CO
3 3 CF COOH的羧基中的羟基极性更大,氢更易电离
OH 3
答案 D
12.钴的某种氧化物广泛应用于硬质合金、超耐热合金、绝缘材料和磁性材料的生产,其
晶胞结构如图所示。下列有关说法正确的是( )
A.该氧化物的化学式为Co O
13 14
B.晶胞中Co2+的配位数为12
C.根据晶体类型推测,该物质熔点低于硫(S )
8
D.若该氧化物的密度为ρ g·cm-3,阿伏加德罗常数为N mol-1,则晶胞中两个O2-间的最短
A
距离是√2×√ 300 cm
3
2 ρN
A
答案 D13.一种理想的激光基质材料M由元素钾、镁和氟组成。晶体M的晶胞如图所示,已知:
晶胞参数为a pm。下列有关该晶体的说法错误的是( )
A.晶胞中K、Mg、F的原子个数比为1∶1∶3
B.与K等距离且最近的F的数目为6
C.在M晶胞结构的另一种表示中,若K位于晶胞的体心,则F位于棱心
D.该晶体的密度为120×1030
g·cm-3
a3N
A
答案 B
14.下列说法或化学用语表述正确的是( )
A.N 的电子式:
2
B.CH Cl 中的共价键类型:非极性键和极性键
2 2
C.CO 的空间结构:V形
2
D.反-2-丁烯的结构简式:
答案 D
15.X、Y、Z、W为原子序数依次增大的前四周期元素,基态原子中,X为元素周期表中半
径最小的原子,Z是地壳中含量最多的元素,W原子的价层电子排布为3d104s1,X、Y、Z、
W形成的阳离子如图所示,下列说法正确的是( )
A.原子半径:Z>Y>X
B.该阳离子中心离子的配位数为6
C.氢化物的沸点:Z>YD.两种配体中的键角:X Z>YX
2 3
答案 B
16.某种新型储氢材料的立方晶胞如图所示,该晶体由[Fe(NH ) ]n+和[BH ]-形成,晶胞参数
3 6 4
为a pm。
下列说法不正确的是( )
A.[Fe(NH ) ]n+中n=2
3 6
B.晶胞中[Fe(NH ) ]n+和[BH ]-的配位数分别为8和4
3 6 4
√3a
C.晶胞中距离最近的2个[Fe(NH ) ]n+之间的距离为 pm
3 6
4
D.[BH ]-中心原子的杂化方式为sp3杂化
4
答案 C
17.钛酸钡是太阳能电池材料。经X射线衍射分析测定,钛酸钡的晶胞结构如图所示
(Ti4+、Ba2+均与O2-接触),已知晶胞边长为a pm,O2-的半径为b pm,N 为阿伏加德罗常数的
A
值。下列叙述错误的是( )
A.与Ba2+等距离且最近的Ti4+有8个
a-2b
B.Ti4+的半径为 pm
2
C.钛酸钡的化学式为BaTiO
3
D.钛酸钡的密度ρ=137+48+16×3×1021 g·cm-3
a3N
A
答案 D
18.LiCoO 、LiC 是重要的电极材料,回答下列问题:
2 6
(1)基态Co原子的价层电子中,两种自旋状态的电子数之比为 。
(2)Li、Co、O、C的电负性由大到小的顺序是 。
(3)Co(Ⅲ)可形成多种配合物。
①已知Co(NH ) BrSO 中Co(Ⅲ)的配位数为6,向该配合物的溶液中滴加 BaCl 溶液,无明
3 5 4 2显现象,则该配合物可表示为 。
②[Co(NH ) ]3+结构如图所示,Co3+位于正八面体中心,若其中两个 NH 被 Cl-取代,则
3 6 3
[Co(NH ) Cl ]-的空间结构有 种。
3 4 2
(4)LiCH 、LiC(CH ) 在合成化学上应用广泛。(CH ) C-的空间结构为 ;(CH ) C-、
3 3 3 3 3 3 3
H C-、F C-的稳定性随中心C原子上电子云密度增大而减小,其中稳定性最强的是 。
3 3
(5)负极材料LiC 晶胞结构如图(a),投影如图(b),Li插入石墨层中间,若该晶胞中碳碳键键
6
长为m pm,石墨层间距为n pm,该晶体的密度为 g·cm-3(用N 表示阿伏加德罗常数的
A
值)。
答案 (1)2∶1(或1∶2)
(2)O>C>Co>Li
(3)①[Co(NH ) SO ]Br ②2
3 5 4
(4)三角锥形 F C- (5) 158√3 ×1030
3
27N m2n
A
19.锗及其化合物广泛用于半导体、催化剂、光伏、制药工业。回答下列问题:
(1)锗的基态原子核外电子排布式为 。
(2)硅、锗、铅的氯化物的熔点如下表:
物质 SiCl GeCl PbCl
4 4 4
熔点/℃ -70 约-50 -15
①GeCl 分子的空间结构为 。
4
②熔点:SiCl C>Ge (4)①b ② ×1021
xyzN
A