文档内容
第一章 原子结构与性质
单元测试卷
一、单选题(本题共15小题)
1.下列基态原子或离子的电子排布式或最外层电子的轨道表示式正确的是(
)
A.K+:1s22s22p63s23p6
B.AI3+:1s22s23p6
C.P原子最外层电子的轨道表示式:
D.Cr:1s22s22p63s23p63d44s2
2.下列对电子排布式或轨道表示式书写的评价错误的是( )
A.若Mn元素的基态原子核外电子排布式为1s22s22p63s23p63d7”,则违反了构造原
理
B.若基态硫原子的价层电子轨道表示式为 ,则违反了泡利原理
C.基态氮原子的核外电子轨道表示式为 ,符合洪特规则和泡
利原理
D.若基态O原子的轨道表示式为 ,则违反了洪特规则
3.下列描述正确的是( )
A.氮原子的价层电子轨道表示式
B.2p和3p轨道的形状均为哑铃形,能量也相等
C.价层电子排布式为4s24p3的元素位于第四周期第VA族,是p区元素
D.钠原子由1s22s22p63s1转化成1s22s22p63p1时,释放能量,由基态转化成激发态
4.某基态原子的M层上有4个p电子,下列有关该原子的叙述错误的是( )
A.N层上不含电子
B.L层上一定有8个电子
C.最外层电子数是4
D.核外电子占据的最高能级的电子云轮廓图为哑铃形5.工业上电解熔融Al O ,和冰晶石(Na A1F )的混合物可制得铝。下列说法正确
2 3 3 6
的是( )
A.半径:A13+③>②>①
B.电负性:①>②>④>③
C.第一电离能:①>④>②>③
D.最高正化合价:①>②>④>③
7. X、Y、Z为主族元素,X元素基态原子的最外层电子排布式为ns1;Y元素基
态原子的M电子层上有2个未成对电子;Z元素基态原子的最外层p轨道上只
有一对成对电子,且Z元素原子的核外比Y元素原子少8个电子,由这三种元
素组成的化合物的分子式不可能是( )
A.XYZ B.X YZ C.X YZ D.X Y Z
4 2 4 2 3 2 2 3
8.a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族。a的原子结构
示意图为 ,b、c形成的化合物的电子式为
下列说法正确的是( )
A.第一电离能:b>c>a>d
B.电负性:a>b>d>c
C.d位于周期表第三周期VA族
D.四种元素涉及周期表的两个区
9.短周期主族元素x、y、z、m、n的原子序数依次增大。x元素的某种核素可以
在考古时用来测定文物年代,常温时,测得0.1mol·L-1y、m、n的简单氢化物的水溶液的pH分别为11、4、1,且z、m还可以与Na形成如图所示电子式的化
合物。以下有关说法错误的是( )
A.原子半径:zy>x
D.x的最高价氧化物中各原子最外层均满足8电子稳定结构
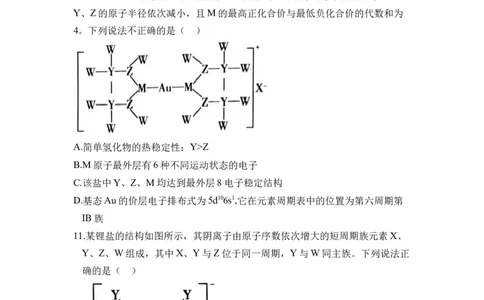
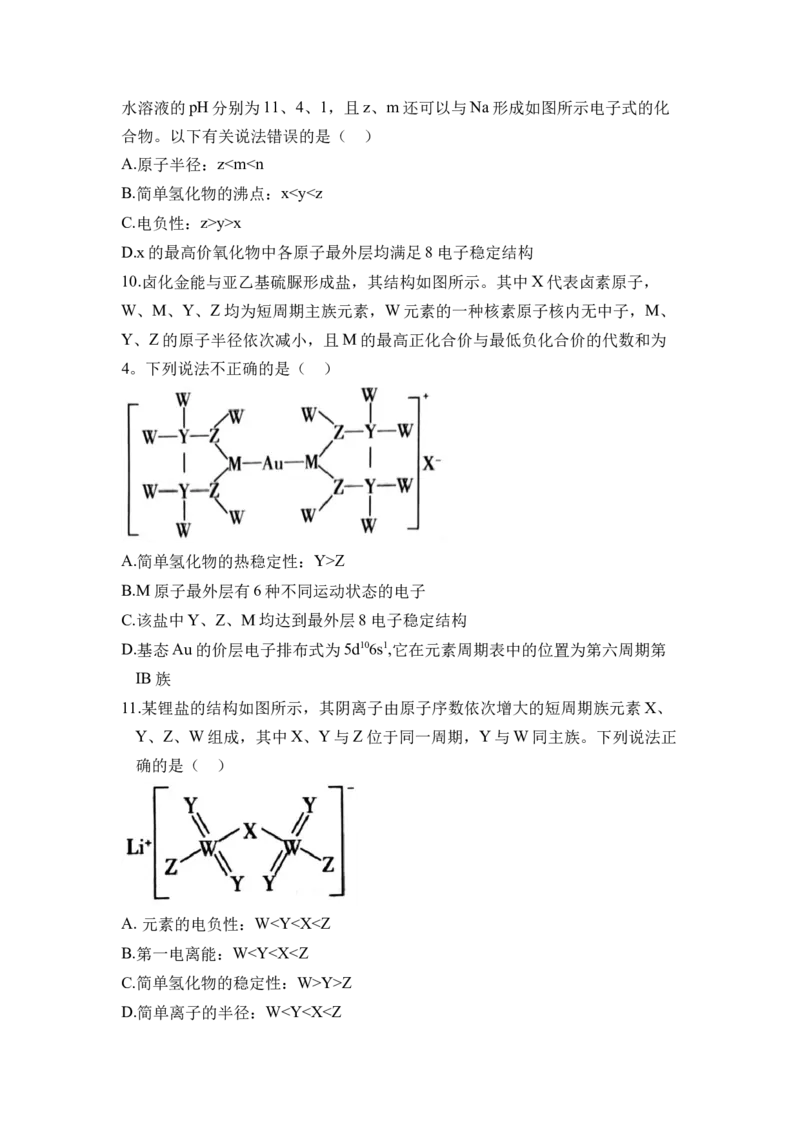
10.卤化金能与亚乙基硫脲形成盐,其结构如图所示。其中X代表卤素原子,
W、M、Y、Z均为短周期主族元素,W元素的一种核素原子核内无中子,M、
Y、Z的原子半径依次减小,且M的最高正化合价与最低负化合价的代数和为
4。下列说法不正确的是( )
A.简单氢化物的热稳定性:Y>Z
B.M原子最外层有6种不同运动状态的电子
C.该盐中Y、Z、M均达到最外层8电子稳定结构
D.基态Au的价层电子排布式为5d106s1,它在元素周期表中的位置为第六周期第
IB族
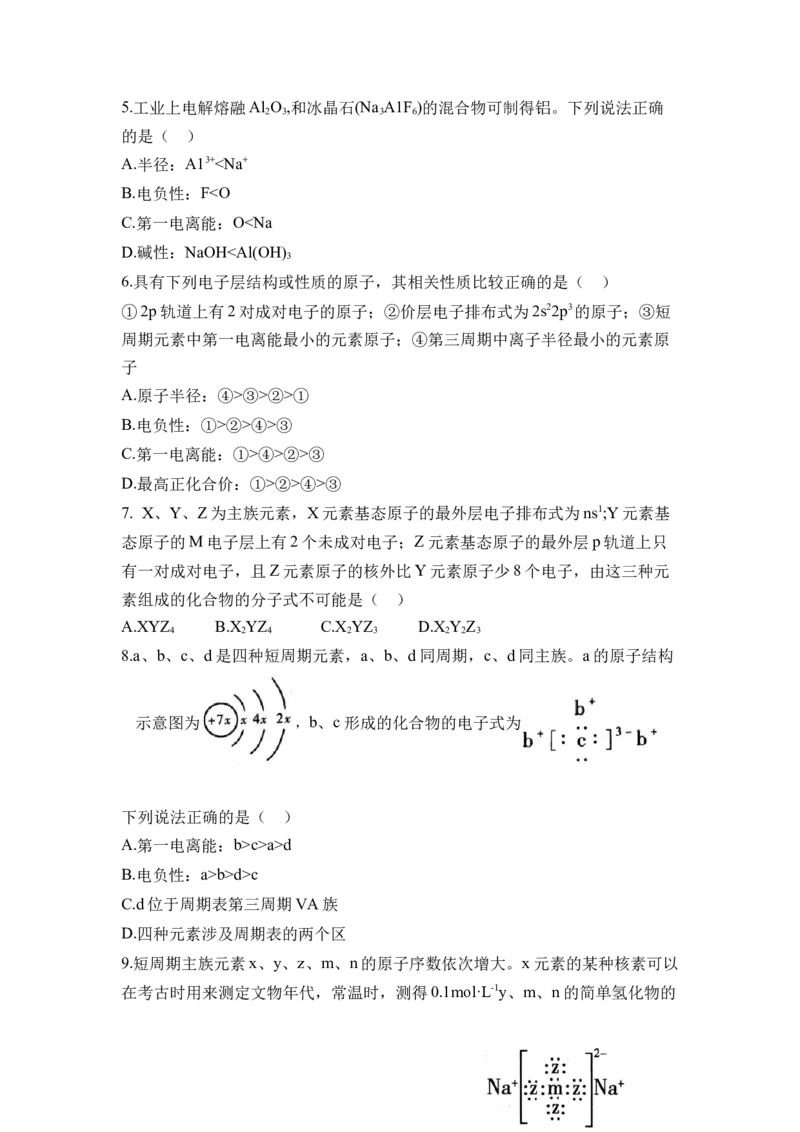
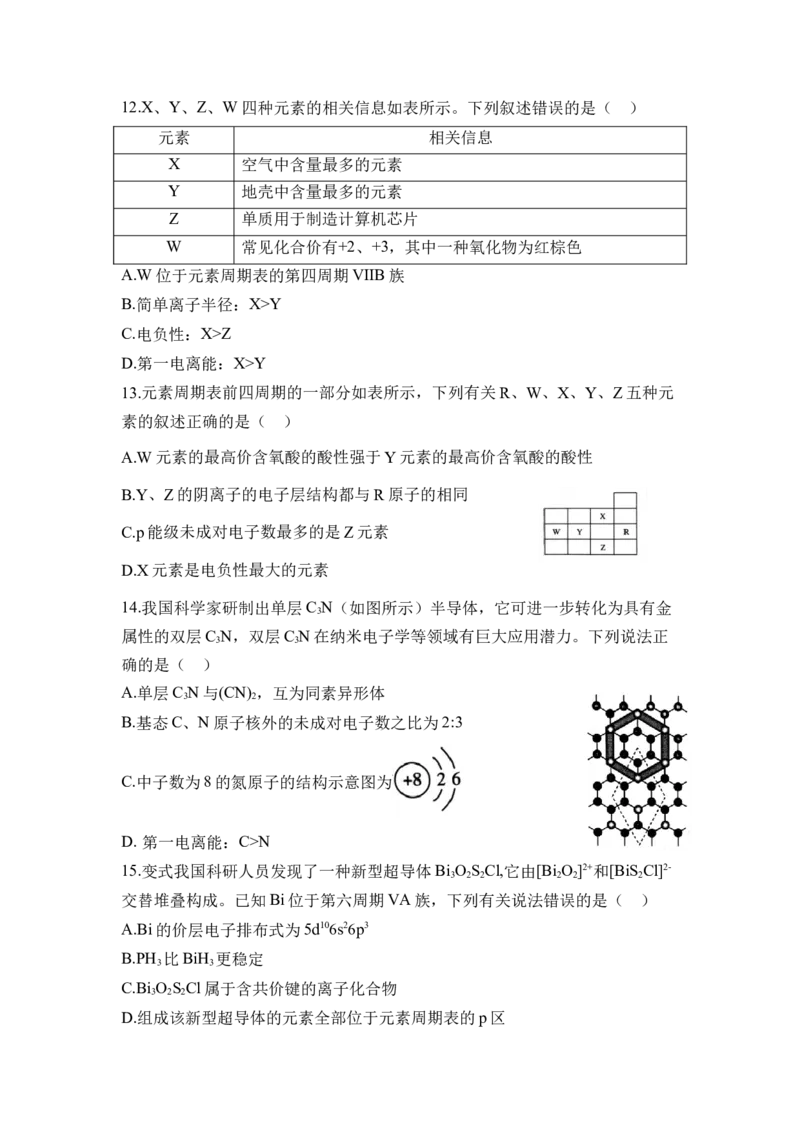
11.某锂盐的结构如图所示,其阴离子由原子序数依次增大的短周期族元素X、
Y、Z、W组成,其中X、Y与Z位于同一周期,Y与W同主族。下列说法正
确的是( )
A. 元素的电负性:WY>Z
D.简单离子的半径:WY
C.电负性:X>Z
D.第一电离能:X>Y
13.元素周期表前四周期的一部分如表所示,下列有关R、W、X、Y、Z五种元
素的叙述正确的是( )
A.W元素的最高价含氧酸的酸性强于Y元素的最高价含氧酸的酸性
B.Y、Z的阴离子的电子层结构都与R原子的相同
C.p能级未成对电子数最多的是Z元素
D.X元素是电负性最大的元素
14.我国科学家研制出单层C N(如图所示)半导体,它可进一步转化为具有金
3
属性的双层C N,双层C N在纳米电子学等领域有巨大应用潜力。下列说法正
3 3
确的是( )
A.单层C N与(CN) ,互为同素异形体
3 2
B.基态C、N原子核外的未成对电子数之比为2:3
C.中子数为8的氮原子的结构示意图为
D. 第一电离能:C>N
15.变式我国科研人员发现了一种新型超导体Bi O S Cl,它由[Bi O ]2+和[BiS Cl]2-
3 2 2 2 2 2
交替堆叠构成。已知Bi位于第六周期VA族,下列有关说法错误的是( )
A.Bi的价层电子排布式为5d106s26p3
B.PH 比BiH 更稳定
3 3
C.Bi O S Cl属于含共价键的离子化合物
3 2 2
D.组成该新型超导体的元素全部位于元素周期表的p区二、非选择题(本题共4小题)
16.根据原子结构、元素周期表和元素周期律的知识回答下列问题。
(1)A元素基态原子次外层电子数是最外层电子数的四分之一,其价层电子轨道
表示式是 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名
称是 ,在元素周期表中的位置是 。
(3)C元素基态原子的轨道表示式是下图中的 (填“①”或“②”),另一
轨道表示式不能作为基态原子的轨道表示式是因为它不符合
(填“A”“B”或“C”)。
A.能量最低原理 B.泡利原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正
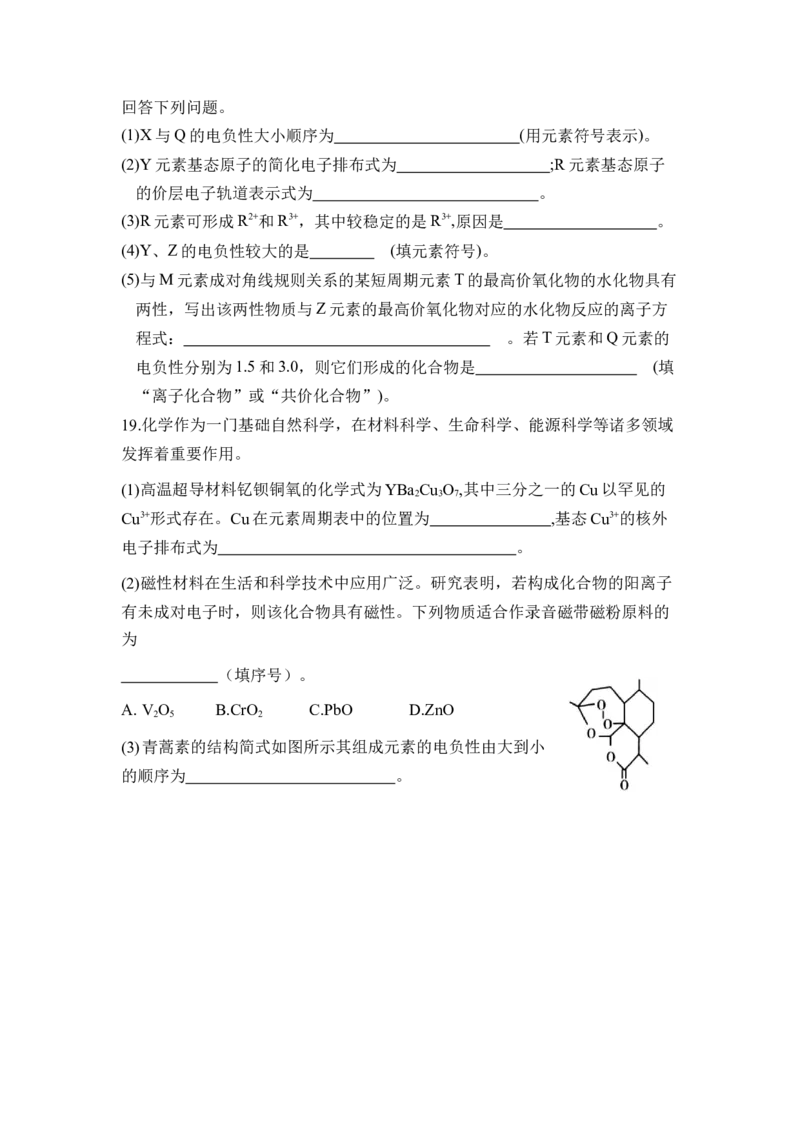
离子所需的最低能量叫第一电离能(设为E)。如图所示:
①同周期内,随若原子序数的增大,E值变化的总趋势是 ;
②根据图中提供的信息,可推断出E E (填“>”“<”或“=”,下同);
氧 氟
③根据第一电离能的含义和元素周期律,可推断出E E 。
镁 钙
17.氨硼烧(NH BH )具有含氢量高,热稳定性好的特点,是一种具有潜力的固体
3 3
储氢材料,回答下列问题。
(1)基态N原子核外电子占据的最高能级的电子云轮廓图为 形,基态N原子的轨道表示式为 。
(2)已知B的第一电离能I (B) =800kJ·mol-1,判断I (A1)
1 1
(填“>”或“<”)800kJ·mol-1,从核外电子排布的角度说明理由:
(3)NH BH 分子中,与N原子相连的H原子对键合电子的吸引力小于N原子,
3 3
与B原子相连的H原子对键合电子的吸引力大于B原子。则在H、B、N三种
元素中:
①电负性大小顺序是 (用元素符号表示,下同);
②原子半径大小顺序是 ;
③在元素周期表中的分区与其他两种元素不同的是 ;
(4) Fe、 Co、 Cu是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化
26 27 29
氨硼烷水解产氢的性能如图所示。
这四种催化剂中催化效果最好的金属的基态原子中的未成对电子数为 ,
催化效果最差的金属的基态原子的价层电子排布式为 。
18.X、Y、Z、M、Q、R是元素周期表中前四周期元素,且原子序数依次增大,
其相关信息如表所示。
元素 相关信息
X 原子核外有6种不同运动状态的电子
Y 基态原子中s电子总数与p电子总数相等
Z 原子半径在同周期主族元素中最大
逐级电离能(单位:kJ·mol-1)依次为 578、 1817、2745、
M
11575、14830、18376、23293
基态原子的核外电子占据5个能级,且最外层p轨道上有2个
Q
电子的自旋方向与其他电子的自旋方向相反
R 基态原子3d能级上有6个电子回答下列问题。
(1)X与Q的电负性大小顺序为 (用元素符号表示)。
(2)Y元素基态原子的简化电子排布式为 ;R元素基态原子
的价层电子轨道表示式为 。
(3)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是 。
(4)Y、Z的电负性较大的是 (填元素符号)。
(5)与M元素成对角线规则关系的某短周期元素T的最高价氧化物的水化物具有
两性,写出该两性物质与Z元素的最高价氧化物对应的水化物反应的离子方
程式: 。若T元素和Q元素的
电负性分别为1.5和3.0,则它们形成的化合物是 (填
“离子化合物”或“共价化合物”)。
19.化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域
发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBa Cu O ,其中三分之一的Cu以罕见的
2 3 7
Cu3+形式存在。Cu在元素周期表中的位置为 ,基态Cu3+的核外
电子排布式为 。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子
有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的
为
(填序号)。
A. V O B.CrO C.PbO D.ZnO
2 5 2
(3)青蒿素的结构简式如图所示其组成元素的电负性由大到小
的顺序为 。